Aplicação da espectroscopia de infravermelho na análise de clones
de azeitonas e azeites cv. “Cobrançosa” em dois estados de
maturação
Dissertação de Mestrado em Biotecnologia e Qualidade Alimentar
Manuela de Fátima Ferraz Machado
Orientador: Professora Doutora Ana Novo Barros
Coorientador: Professor Doutor José Manuel M. M. de Almeida
Aplicação da espectroscopia de infravermelho na análise de clones de
azeitonas e azeites cv. “Cobrançosa” em dois estados de maturação
Dissertação de Mestrado em Biotecnologia e Qualidade Alimentar
Manuela de Fátima Ferraz Machado
Orientador: Professora Doutora Ana Novo Barros
Coorientador: Professor Doutor José Manuel M. M. de Almeida
Composição do Júri:
Presidente: Doutor António Francisco Henrique Inês
Professor Auxiliar da Universidade de Trás-os-Montes e Alto Douro
Vogais: Doutora Paula Filomena Martins-Lopes
Professora Auxiliar da Universidade de Trás-os-Montes e Alto Douro
Doutor António Barros
Investigador Auxiliar da Universidade de Aveiro
i Agradecimentos
Com este trabalho concluído resta-me agradecer a todas as pessoas que para ele contribuíram direta ou indiretamente, especialmente:
À Professora Ana Novo Barros, excelente orientadora deste trabalho, por todo o apoio, por todos os conhecimentos transmitidos, por todo empenho, pela dedicação e amizade demonstrados ao longo deste trabalho, bem como ao longo da licenciatura e do mestrado.
Ao Professor José Manuel Almeida, pelos conhecimentos transmitidos, pelo empenho e dedicação que sempre demonstrou para como este trabalho.
Ao Gabriel, pelo apoio, pela ajuda no inglês e por tudo o que representa para mim.
A todos aqueles que me apoiaram, em especial à Sarinha pelos bons momentos passados durante o mestrado, pelos conselhos e pela amizade.
À Juliana, à Vera e à Filipa, pelos momentos de alegria passados durante o mestrado, pela partilha de dúvidas e conhecimentos.
À Olívia pelo apoio ao longo desta caminhada, por se ter mostrado uma grande amiga, sempre pronta a ajudar.
Aos meus pais, por possibilitarem a minha progressão nos estudos, mesmo nos tempos difíceis que se vivem.
ii Resumo
O azeite e a azeitona apresentam elevada importância socioeconómica na região de Trás-os-Montes. A qualidade destes produtos está inteiramente dependente da sua composição química. Esta é influenciada por vários fatores, como por exemplo as condições ambientais, as práticas agrícolas, a cultivar e o estado de maturação do fruto.
Neste trabalho estudaram-se as potencialidades da espetroscopia de infravermelho na distinção de dois estados de maturação (semiverde e maduro), em clones de azeitona e respetivos azeites da cultivar Cobrançosa. Aliando a espetroscopia de infravermelho à análise multivariada foi possível separar as amostras no estado semiverde, das amostras no estado maduro, bem como diferenciar os clones.
Recorrendo às regressões por componentes principais (PCR) e por mínimos quadrados parciais (PLS), conseguiu-se relacionar o espetro de infravermelho, com os parâmetros químicos: atividade antioxidante, fenóis totais, orto-difenóis e flavonoides. Verificou-se uma boa correlação entre os dados espetrais e os resultados obtidos por métodos clássicos.
No caso do azeite, na regressão PLS obtiveram-se correlações entre os 96% e os 97% com o valores de RMSECV (raiz quadrada do erro médio de validação) a variar entre 7,05% e 27,91%, já para a azeitona os valores das correlações variaram entre 94% e 98% e o erro associado ao modelo entre 18,84% e 19,49%. No que diz respeito a regressão PCR os valores do coeficiente de determinação (R2) variaram entre 90% e 95% no caso do azeite e entre 87% e 97% para a azeitona. Já os valores de RMSECV variaram entre 7,75% e 24,81% para o azeite e 17,81% e 20,55% para a azeitona. Em geral, a regressão PLS oferece melhores resultados que o PCR na análise quantitativa dos parâmetros químicos estudados.
iii Application of infrared spectroscopy in the analysis of olives and olive oil clones cv.
“Cobrançosa” in two ripening stages Abstract
The olive and olive oil have high socio-economic importance in the Trás-os-Montes region. The quality of these products depends entirely on its chemical composition being directly influenced by several factors such as environmental conditions, agricultural practices, cultivar and ripening stage.
In this study we used the potential of infrared spectroscopy to distinguish two ripening stages (semi-ripe and ripe) in olive and olive oil from Cobrançosa clones. After that, combining the infrared spectroscopy results with the multivariate analysis it was possible to distinguish the samples in the semi-ripe stage, from the samples in the ripe stage, as well as the discrimination of the clones.
Using the principal component regression (PCR) and partial least squares regression (PLS), we were able to relate the infrared spectrum with chemical parameters such as antioxidant activity, total phenols, ortho-diphenols and flavonoids. There was a good correlation between the spectral data and the results obtained by classical methods.
In the PLS regression, correlations between 96% and 97% were obtained in the case of olive oil, the RMSECV values ranged between 7.05% and 27.91%, yet to the olives correlations values ranged between 94% and 98% and the error varied between 18.84% and 19.49%. In terms of PCR, the regression coefficient of determination (R2) varied between 90% and 95% for olive oil and between 87% and 97% for the olives. The RMSECV values ranged between 7.75% and 24.81% for olive oil, yet to the olives values varied between 17.81% and 20.55%. In general, PLS offers better results than PCR for quantitative analysis of chemical parameters.
iv Índice Geral Agradecimentos ... i Resumo ... ii Abstract ... iii Índice Geral ... iv Índice de Figuras ... vi Índice de Tabelas ... ix Lista de abreviaturas ... x
Capítulo I – Revisão Bibliográfica 1. Introdução ... 1
1.1.Enquadramento temático ... 1
1.2. Oliveira (Olea europaea L.) ... 1
1.3. Olivicultura em Portugal e no Mundo ... 2
1.4. Cultivar Cobrançosa ... 3
1.5. Composição Química da Azeitona ... 3
1.6. Composição Química do Azeite ... 5
1.7. Importância da Azeitona e do Azeite na saúde ... 6
1.8. Evolução da composição química da azeitona ao longo da maturação ... 7
1.9. Espetroscopia de Infravermelho ... 8
1.9.1. Espetroscopia de Infravermelho com Transformada de Fourier ... 10
1.9.2. Aplicações da espetroscopia de infravermelho na análise de alimentos ... 12
1.10. Quimiometria ... 13
v Capítulo II – Material e Métodos
2. Material e Métodos ... 15
2.1. Amostragem ... 16
2.2. Preparação das amostras de azeitona ... 16
2.3. Aquisição dos espetros FTIR e pré-tratamento de dados ... 16
2.4. Análise multivariada ... 16
Capítulo III – Resultados e Discussão 3. Resultados ... 18
3.1. Espetro FTIR da azeitona e do azeite ... 18
3.2. Aplicação da análise de componentes principais (PCA) aos dados espetrais do azeite ... 20
3.3. Aplicação da análise discriminante (DA) aos dados espetrais do azeite ... 24
3.4. Regressão das componentes principais (PCR) para os dados do azeite ... 26
3.5. Regressão por mínimos quadrados parciais (PLS) para os dados do azeite ... 31
3.6. Comparação dos resultados obtidos por PCR e por PLS ... 34
3.7. Aplicação da análise de componentes principais (PCA) aos dados espetrais da azeitona ... 36
3.8. Aplicação da análise discriminante (DA) aos dados espetrais da azeitona ... 40
3.9. Regressão das componentes principais (PCR) para os dados da azeitona ... 42
3.10. Regressão por mínimos quadrados parciais (PLS) para os dados da azeitona ... 45
3.11. Comparação entre os resultados obtidos por PCR e PLS ... 48
Capítulo IV- Conclusão e perspetivas futuras ... 49
Capítulo V- Referencias Bibliográficas ... 50
vi Índice de Figuras
Figura 1- Fruto da cultivar Cobrançosa ... 3
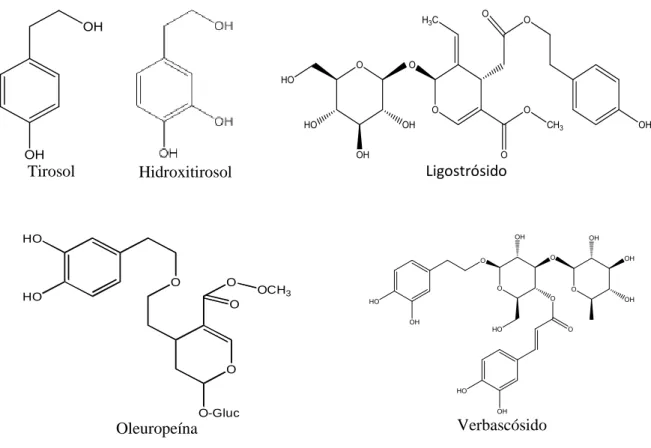
Figura 2- Estrutura química de alguns dos principais compostos fenólicos da azeitona; hidroxitirosol, tirosol, ligostrósido, oleuropeína, verbascósido ... 5
Figura 3- Esquema do interferómetro de Michelson, Skoog, 2008 ... 10
Figura 4 – Esquema de um dispositivo de ATR ... 12
Figura 5- Espetro FTIR-ATR de um dos clones nos dois estados de maturação ... 18
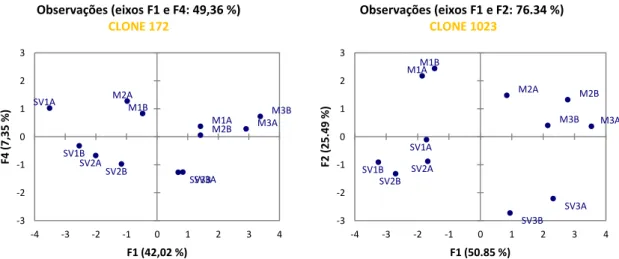
Figura 6- Gráfico das coordenadas fatoriais para os clones a) 172 no plano F1/F4 e b) 1023 no plano F1/F2 (SV - semiverde e M – maduro) ... 20
Figura 7- Números de onda que mais contribuem para a discriminação entre o estado semiverde e maduro ... 21
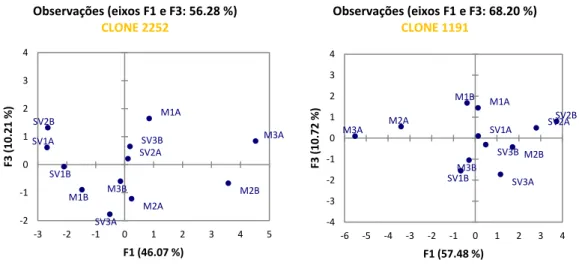
Figura 8- Gráfico das coordenadas fatoriais para os clones 2252 no plano F1/F3 e 1191 no plano F1/F3 ... 22
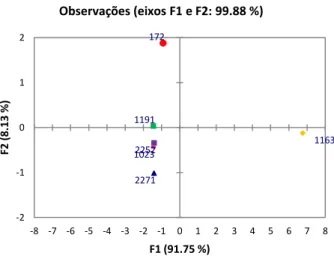
Figura 9- Coordenadas fatoriais de todos os clones independentemente do estado de maturação ... 22
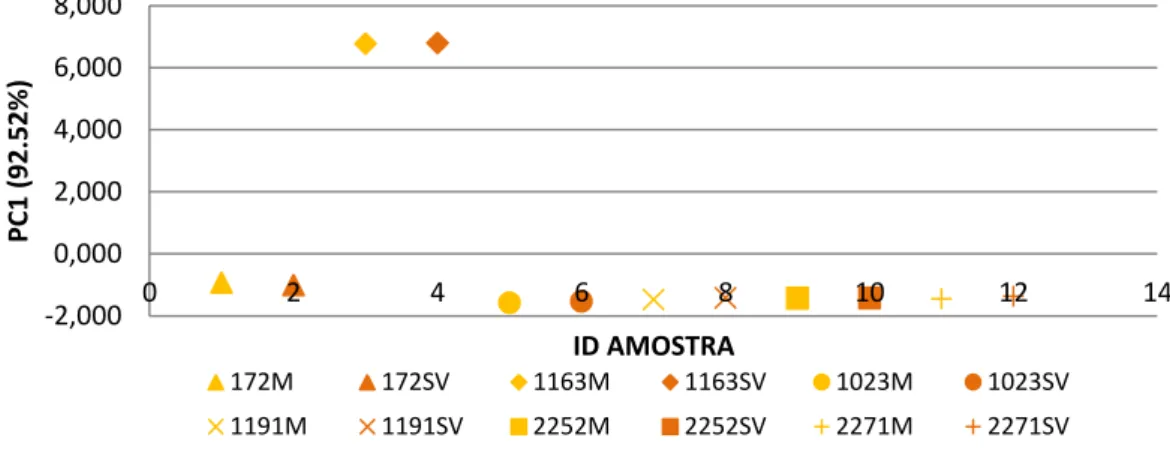
Figura 10- Coordenadas fatoriais da primeira componente principal para os dados FTIR ... 23
Figura 11- Coordenadas fatoriais de todos os clones apenas num estado de maturação (maduro) ... 24
Figura 12- Gráfico das coordenadas fatoriais para todos os clones nos dois estados de maturação ... 24
Figura 13 – Gráfico das coordenadas fatoriais da análise discriminante aplicada aos resultados das análises químicas do azeite ... 25
Figura 14- Análise discriminante em função da atividade antioxidante e rendimento de produção, coordenadas fatoriais nas dimensões DF1 e DF2 ... 26
Figura 15 – RMSEC e RMSECV em função do número de componentes principais para atividade antioxidante, fenóis totais, orto-difenóis e flavonoides ... 28
vii Figura 16- Ilustração da qualidade do modelo obtido por PCR. Relação entre os valores
estimados pelo método e os valores medidos para as grandezas químicas: a) Atividade antioxidante, b) Fenóis totais, c) orto-difenóis, d) Flavonoides ... 30
Figura 17- RMSEC e RMSECV em função do número de variáveis latentes para atividade
antioxidante, fenóis totais, orto-difenóis e flavonoides ... 32
Figura 18 – Ilustração da qualidade do modelo obtido por PLS. Relação entre os valores
estimados pelo método e os valores medidos para as grandezas químicas: a) Atividade antioxidante, b) Fenóis totais, c) orto-difenóis, d) Flavonoides ... 33
Figura 19- Gráfico das coordenadas fatoriais para os clones 1163; 1023; 2252; 2271 ... 36
Figura 20- Números de onda que mais contribuem para a discriminação entre o estado
semiverde e maduro ... 37
Figura 21-Gráfico das coordenadas fatoriais para todos os clones nos dois estados de maturação ... 38
Figura 22- Coordenadas fatoriais das observações na primeira componente principal para os
dados FTIR da azeitona ... 39
Figura 23- Gráfico das coordenadas fatoriais para todos os clones num só estado de maturação
(Maduro) ... 39
Figura 24- Gráfico das coordenadas fatoriais para a análise discriminante aplicada a todos os
clones nos dois estados de maturação ... 40
Figura 25- Gráfico das coordenadas fatoriais da análise discriminante aplicada aos resultados
das análises químicas da azeitona ... 40
Figura 26- Análise discriminante em função da atividade antioxidante e rendimento de
produção, coordenadas fatoriais nas dimensões DF1 e DF2 ... 41
Figura 27- RMSEC e RMSECV em função do número de variáveis latentes para atividade
viii Figura 28- Ilustração da qualidade do modelo obtido por RCP. Relação entre os valores
estimados pelo método e os valores medidos para as grandezas químicas: a) Atividade antioxidante, b) Fenóis totais, c) orto-difenóis, d) Flavonoides ... 44
Figura 29- RMSEC e RMSECV em função do número de variáveis latentes, para a atividade
antioxidante, fenóis totais, orto-difenóis e flavonoides ... 46
Figura 30 – Ilustração da qualidade do modelo obtido por PLS. Relação entre os valores
estimados pelo método e os valores medidos para as grandezas químicas: a) Atividade antioxidante, b) Fenóis totais, c) orto-difenóis, d) Flavonoides ... 47
ix Índice de Tabelas
Tabela 1- Gamas do infravermelho ... 8
Tabela 2-Valores de absorção dos diferentes grupos funcionais... 9
Tabela 3 – Amostragem ... 15
Tabela 4- Matriz de confusão para os dados, e resultados da validação cruzada com base na atividade antioxidante e rendimento de produção. Classificações observadas nas linhas, e classificações previstas nas colunas. ... 26
Tabela 5 – Calibração e validação da regressão PCR para o azeite ... 29
Tabela 6- Calibração e validação da regressão PLS para o azeite ... 31
Tabela 7- Coeficiente de determinação e RMSECV obtidos por PCR e PLS ... 34
Tabela 8- Matriz de confusão para os dados, e resultados da validação cruzada com base na atividade antioxidante e rendimento de produção. Classificações observadas nas linhas, e classificações previstas nas colunas. ... 41
Tabela 9 – Calibração e validação da regressão PCR para a azeitona ... 42
Tabela 4 – Calibração e Validação da regressão PLS para a azeitona ... 45
x Lista de Abreviaturas
AA- Atividade Antioxidante
ABTS – Ácido 2,2 – azino-bis-(3-etilbenzotiazolina-6-sulfónico)
AOAC- Association of Official Analytical Chemists
ATR- Reflexão Total Atenuada
DA- Análise Discriminante (do inglês “discriminant analysis”)
FTIR- Espetroscopia de Infravermelho com Transformada de Fourier
GAE- Equivalentes de ácido gálico (do inglês “gallic acid equivalents”)
M- Maduro
PC- Componente principal (do inglês “principal component”)
PCA- Análise em Componentes Principais (do inglês “principal component analysis”)
PCR- Regressão por Componentes Principais (do inglês “principal component regression”)
PLS- Regressão por Mínimos Quadrados Parciais (do inglês “partial least squares”ou
“Projection to latent structures)
RMSEC- raiz quadrada do erro médio de calibração (do inglês “root-mean-square error of
calibration”)
RMSECV- raiz quadrada do erro médio de validação (do inglês”root-mean-square error of
cross-validation”)
SNV- “Standard normal variate”
SV- Semiverde
Capítulo I
Revisão Bibliográfica
1 1. Introdução
1.1. Enquadramento temático
Em Portugal o olival apresenta uma importância relevante ao nível socioeconómico, especialmente nas regiões do Alentejo e de Trás-os-Montes. Os produtos desta cultura são amplamente valorizados pelo seu valor nutricional e pelos benefícios para a saúde que lhes são atribuídos (Cunha, 2007). Por esse fato, despertam muito interesse por parte dos investigadores e toda a comunidade científica. Assim, tornou-se necessário aprofundar conhecimentos, otimizar as práticas agrícolas e escolher adequadamente a data de colheitas dos frutos, de modo a garantir a qualidade quer da azeitona quer do respetivo azeite.
Nos últimos anos verifica-se um aumento do número de estudos científicos nesta área, destacando-se a caracterização de cultivares e estudos de melhoramento, bem como o desenvolvimento de metodologias científicas para a autenticação dos produtos (Frankel, 2010)
Deste ponto de vista, tornou-se importante desenvolver e aplicar metodologias de análise rápidas, como é o caso da espetroscopia de infravermelho com transformada de Fourier, para a distinção de cultivares, identificação rápida de adulterações e autenticação dos produtos (Lerma-Garcia et al., 2010; Dais & Halzakis, 2013).
1.2. Oliveira (Olea europaea L.)
A oliveira Olea europaea L. representa a única espécie da família oleácea com fruto comestível; é considerada a árvore mais antiga cultivada pelo homem.
Esta cultura é oriunda do Médio Oriente, estando a sua origem datada de 4000 anos a.C (Loukas & Krimbas 1983; Boskou 1998; Bacelar et al., 2009). Atualmente o cultivo da oliveira encontra-se amplamente difundido por todo o mundo, sendo em muitas regiões, a principal atividade económica (Pereira et al., 2007). A difusão desta cultura deve-se à sua grande capacidade de adaptação a condições ambientais adversas, apresentando uma elevada tolerância à seca e à salinidade.
2 Historicamente os produtos desta cultura eram utilizados na alimentação, e na medicina tradicional, tendo aplicação como emoliente, laxante, sedativo e tónico (Waterman et al., 2007)
Atualmente, a azeitona é valorizada comercialmente em duas vertentes, a produção de azeitona de mesa e a produção de azeite, sendo estes produtos amplamente valorizados, dado o seu importante valor nutricional.
1.3. Olivicultura em Portugal e no Mundo
Atualmente, cerca de 95% da produção oleícola mundial, está concentrada na bacia mediterrânica, sendo que os principais produtores da União Europeia (Espanha, Itália, França, Grécia e Portugal) são responsáveis por cerca de 74% da produção a nível mundial (Pereira et al., 2007; FAOStat, 2013).
Outros países com impacto na produção mundial são os países do norte de África, destacando-se a Tunísia, a Síria, Marrocos e a Argélia, com uma produção equivalente a 16% da total mundial (FAOStat, 2013).
Na União Europeia, a produção de azeite tem crescido significativamente nos últimos anos, continuando a Espanha a ocupar o primeiro lugar no ranking dos maiores produtores (Azeite, 2012).
Em Portugal, o olival é a segunda cultura agrícola mais importante em termos económicos, esta cultura encontrando-se difundida um pouco por todo o país, no entanto as maiores produções encontram-se nas regiões agrárias do Alentejo e de Trás-os-Montes.
No Alentejo situa-se a maior área de cultivo, sendo a produção destinada maioritariamente à produção de azeite, enquanto que em Trás-os-Montes, apesar de a área de cultivo ser menor, é onde se localiza uma maior produção de azeitona de mesa comparativamente ao Alentejo.
Esta cultura é de elevada importância para estas regiões, contribuindo de forma muito significativa para o seu desenvolvimento e economia. Nos últimos anos, tem-se assistido a uma recuperação da produtividade deste sector, estimando-se uma produção de 72 mil toneladas de azeite, na campanha 2011/2012 (Azeite, 2012).
3 Na região de Trás-os-Montes, as condições climáticas, a qualidade dos solos e as técnicas de produção tradicionais, conferem aos produtos uma elevada qualidade (Amaral et al., 2010). O azeite desta região está reconhecido com o selo de Denominação de Origem Protegida (Reg. 1107/96). Para este azeite de elevada qualidade contribuem cultivares com grande adaptação as condições da região, destacando-se neste ponto, as variedades Cordovil, Verdeal Transmontana, Madural e Cobrançosa (Amaral et al., 2010).
1.4. Cultivar Cobrançosa
A cultivar Cobrançosa é tipicamente portuguesa, encontrando-se em várias regiões agrárias. É no entanto na região de Trás-os-Montes que o seu cultivo tem maior expressão (Alves, 2007), sendo esta cultivar usada principalmente para a produção de azeite. Adapta-se facilmente às condições da região, apresenta menos sensibilidade às doenças e às pragas que frequentemente atingem a oliveira. Apresenta ainda grande tolerância ao frio e à clorose do ferro (Leitão et al.,1986; Alves, 2007). É uma cultivar à qual é apontada uma elevada produtividade, apresentando os seus frutos baixa resistência ao desprendimento, o que possibilita a utilização da apanha mecânica por vibração.
O fruto tem uma forma elíptica, assimétrica e encurvada no dorso, apresenta uma cor roxo vinhoso e pesa entre 3 e 4 gramas (Figura 1). O caroço é elíptico, assimétrico, terminando em bico encurvado, com a superfície rugosa e estrias mais regulares na base (Leitão et al., 1986).
Figura 1- Fruto da cultivar Cobrançosa
1.5. Composição química da Azeitona
A composição química e as propriedades físicas da azeitona são fatores fortemente influenciados pela cultivar, condições climáticas e estado de maturação (Amaral et al., 2010).
4 A polpa da azeitona é maioritariamente constituída por água, de 70 a 75%, e uma fração lipídica que varia entre 14 a 15% nas azeitonas verdes e cerca de 30% do peso da polpa, nas azeitonas pretas (Fernández et al., 1997; Conde et al., 2008; Sakouhi et al., 2008). Apresenta um baixo teor de açúcares (2-5%) e proteína (3%), fibra e cinzas (Conde et al., 2008). O teor de hidratos de carbono inclui polissacarídeos e substâncias pécticas, importantes para a textura da polpa.
A fração lipídica das azeitonas é constituída principalmente por ácidos gordos monoinsaturados, sendo o ácido oleico maioritário, e um pequeno teor de ácido gordos saturados que não ultrapassa os 15% do teor total de lípidos (Conde et al., 2008; Sakouhi et al., 2008). Os ácidos gordos encontram-se na forma de triglicéridos e a quantidade em ácidos gordos livres érelativamente baixa (Bianchi, 2003).
O principal açúcar livre presente na polpa é a glucose (1 a 3% do peso da polpa) seguida da frutose (0,1 a 1,1%) e pequenas concentrações de xilose, sacarose e manitol (Nout & Rombouts, 2000). Os açúcares solúveis diminuem ao longo do processo de maturação do fruto (Fernández et al., 1997; Nout & Rombouts, 2000).
Relativamente aos ácidos orgânicos, os ácidos oxálico, succínico, málico e cítrico existem numa percentagem entre 1,2 a 2,1% do peso da polpa em matéria seca, aumentando a sua concentração até à maturação completa do fruto (Bianchi, 2003).
As azeitonas contêm uma grande variedade de compostos fenólicos, com um papel fundamental nas propriedades químicas, organoléticas e nutricionais do azeite e das azeitonas. Os compostos fenólicos e os seus glucósidos representam cerca de 1 a 3% do peso da azeitona.
Os principais compostos fenólicos presentes na azeitona são os secoiridoides oleuropeína e ligostrósido (Figura 2), os flavonoides luteolina 7-O-glucósido, rutina e apigenina 7-O-glucósido, o verbascósido como principal ácido hidroxicinâmico (Figura 2) (Romero et al., 2002; Bianchi 2003; Vinha et al., 2005; Conde et al., 2008). Encontram-se também as antocianinas, cianidina 3-O-glucósido e cianidina 3-O-rutinósido, e os álcoois fenólicos tirosol e hidroxitirosol (Figura 2) (Bianchi, 2003; Vinha et al., 2005; Conde et al., 2008).
5
Tirosol Hidroxitirosol Ligostrósido
O O O O OCH3 O-Gluc HO HO Oleuropeína Verbascósido
Figura 2-Estrutura química de alguns dos principais compostos fenólicos da azeitona: hidroxitirosol, tirosol, ligostrósido, oleuropeína, verbascósido
1.6.Composição química do Azeite
O azeite é uma gordura líquida à temperatura ambiente, é obtido exclusivamente a partir de azeitonas sujeitas a processos mecânicos sob condições térmicas que não impliquem alterações na sua composição (Reg. 25687/91).
A sua composição química é influenciada pela cultivar utilizada, estado de maturação da azeitona, fatores climáticos, práticas agronómicas e tecnologia de produção utilizada (Kalua et al., 2005; Waterman et al., 2007; Amaral et al., 2010).
Do ponto de vista químico, o azeite pode ser dividido em duas frações, a fração saponificável e a fração insaponificável. A primeira fração constitui cerca de 97% do peso total do azeite, aqui encontram-se maioritariamente triglicéridos, uma pequena quantidade de mono e digliceróis e alguns ácidos gordos livres responsáveis pela acidez do azeite (Boskou et al., 2006; Cunha, 2007; Navarra et al., 2011). Segundo Boskou (1996), do conjunto de triglicéridos existentes, destacam-se a trioleína, a palmitoleína e a linoleodiolina.
6 Da fração insaponificável fazem parte um grande conjunto de compostos: ceras, álcoois alifáticos, hidrocarbonetos, pigmentos, fosfolípidos, fitoesteróis, tocoferóis e compostos fenólicos.
Os hidrocarbonetos presentes no azeite são de natureza terpénica, esterólica e policíclica aromática (Sánchez et al., 2001). O esqualeno e o β- caroteno são os hidrocarbonetos terpénicos mais importantes presentes no azeite, apontando-se ao esqualeno algumas propriedades quimiopreventivas (Boskou et al., 2006).
No azeite, os compostos fenólicos mais importantes e presentes em maior quantidade são os isómeros das agliconas da oleuropeína e ligostrósido, as lignanas e os álcoois fenólicos tirosol e hidroxitirosol (Servili et al., 2004).
Apesar da fração insaponificável ser minoritária no azeite, estes compostos assumem uma elevada importância a vários níveis, pois são responsáveis pela estabilidade oxidativa do azeite, pelas propriedades organoléticas e pelo seu valor nutricional. Por esse motivo, estes compostos são muitas vezes usados como critério de qualidade dos azeites (Boskou, 1998).
1.7. Importância da Azeitona e do Azeite na Saúde
Estudos epidemiológicos demonstram a importância do consumo de azeite e azeitona na saúde. Segundo vários autores (Tovar et al., 2002; Morelló et al., 2005; Rohman et al. 2010) os benefícios destes alimentos devem-se ao seu elevado teor de ácido oleico e à presença de compostos fenólicos, importantes antioxidantes naturais.
Aos compostos fenólicos são apontados diversos benefícios, de entre os quais se destacam a redução de risco de doenças cardiovasculares, principal causa de morte nos países industrializados (Owen et al., 2004; Waterman et al., 2007), redução do risco de doenças cancerígenas e degenerativas (Bendini 2007; Pereira et al., 2007; Waterman et al., 2007) e diminuição da incidência de arteriosclerose (Waterman et al., 2007).
Segundo Aouidi et al., (2012), a oleuropeína apresenta propriedades anti-inflamatórias, antimicrobianas e antivirais, apresentando ainda um efeito cardio e neuro-protetor. O hidroxitirosol é também apontado como potencial agente antimicrobiano (Turck et al., 2002).
Os compostos fenólicos são ainda responsáveis pela redução da hipertensão e do colesterol, problemas que afetam cada vez mais pessoas em todo o mundo (Rhoman et al., 2010). O consumo de azeite aumenta a atividade lipolítica no tecido adiposo, evitando a obesidade (Rhoman et al., 2010).
7 Os esteróis e terpenos apresentam, segundo alguns estudos, propriedades anti-inflamatórias; ao esqualeno é atribuído um importante papel na prevenção do cancro da pele (Waterman et al., 2007, Lukic et al., 2013).
1.8. Evolução da composição química da azeitona durante a maturação
Durante a maturação da azeitona ocorrem importantes modificações na sua composição química que influenciam significativamente a qualidade do azeite.
A maturação do fruto inicia-se com o aparecimento dos primeiros tons violeta no fruto, e termina quando é atingida a coloração característica de cada cultivar (Lopes et al., 2009); o período de maturação é variável, sendo afetado pelas condições climatéricas, colheitas na planta, quantidade de frutos presentes na árvore e pelas características de cada cultivar (Cobo et al., 1998).
Ao longo da maturação, verifica-se que o teor de gordura aumenta, atingindo o seu máximo nos frutos bem maduros (Salvador et al., 2001, Tovar et al., 2002, Machado et al., 2013). No entanto o teor de ácido oleico diminui nas últimas fases de maturação, o mesmo acontecendo como teor de ácido palmítico, e havendo no entanto um aumento do teor de ácido linoleico (Baccouri et al., 2008).
Estudos recentes mostram que o teor de esteróis e terpenos é um bom indicador do estado de maturação da azeitona (Lukic et al., 2013) uma vez que se verifica a diminuição do conteúdo destes compostos nas últimas fases de maturação, devido ao fim da sua biossíntese (Matos et al., 2007; Baccouri et al., 2008, Lukic et al., 2013).
No que diz respeito aos compostos fenólicos, o conteúdo total destes compostos aumenta nas primeiras fases de maturação do fruto, mas diminui nos últimos estados (Tovar et al., 2002, Bouaziz et al., 2004; Kalua et al., 2005; Machado et al., 2013). A diminuição do teor de compostos fenólicos ao longo da maturação é explicada pela diminuição da atividade da enzima fenilalanina amónia-liase, enzima responsável pela sua biossíntese (Tovar et al. 2002, Morelló et al., 2005, Machado et al., 2013). A redução do teor de compostos fenólicos compromete a estabilidade oxidativa dos azeites (Matos et al., 2007). Segundo Matos et al., (2007), o teor de oleuropeína sofre uma diminuição ao longo da maturação, originando posteriormente azeites menos picantes, mais apagados.
8 Uma colheita antecipada favorece assim a produção de azeites com melhores atributos sensoriais e maior estabilidade oxidativa. É também importante referir que uma colheita antecipada evita a perda de frutos provocada pelas pragas que os atingem, consequência das primeiras chuvas (Sousa, 2012).
1.9. Espetroscopia de Infravermelho
A espetroscopia de infravermelho tem sido adotada em muitas áreas científicas, superando por vezes os métodos tradicionais. As principais razões para a popularidade desta ferramenta analítica são a rapidez com que as amostras são caracterizadas, praticamente sem manipulação e a grande versatilidade do equipamento (De Luca et al., 2011; Aouidi et al., 2012; Lin et al., 2012). Obtém-se rapidamente informação relativa aos grupos funcionais presentes na amostra em estudo, e consegue-se também obter alguma informação sobre o tipo de ligações presentes na molécula.
A radiação de infravermelho divide-se em três gamas: infravermelho longínquo, infravermelho médio e infravermelho próximo (tabela 1), sendo os dois últimos os mais utilizados em química alimentar (Ismail et al., 2006).
Região Gama de comprimento de onda (µm) Números de onda (cm-1)
Próximo 0,78-2,5 12800-4000
Médio 2,5-50 4000-400
Longínquo 50-1000 400-10
Tabela 1- Gamas do infravermelho
De forma simples e resumida, pode dizer-se que quando a frequência de radiação infravermelha emitida é igual à frequência de um modo de vibração da molécula, ocorre absorção de energia por parte desta, resultando numa alteração da amplitude de vibração molecular (Costa, 2007).
Para as moléculas absorverem energia na região do infravermelho, tem de ocorrer alteração do momento dipolar como consequência dos seus movimentos vibracionais e rotacionais (Costa, 2007). Quanto maior for a simetria da molécula, menor será o número de bandas observado no seu espetro de infravermelho uma vez que algumas ligações absorvem à mesma frequência.
9 A intensidade das bandas depende da natureza e da polaridade das ligações. Uma ligação fortemente polar, como por exemplo, a ligação C=O, composta por átomos diferentes, absorve muito mais energia do que a ligação C=C, por exemplo (Costa, 2007; Karoui et al., 2010).
As moléculas com o mesmo grupo funcional apresentam espetros com bandas sensivelmente à mesma frequência, independentemente da cadeia principal onde estão inseridas. A estas absorções chamam-se frequências de grupo e são encontradas em números de onda superiores a 1300 cm-1.
Na região entre 1300 cm-1 e 400 cm-1 encontram-se bandas de difícil atribuição a grupos funcionais, devido à semelhança entre as massas e aforças de ligação de cada espécie absorvente. No entanto esta região contém bandas muito importantes para identificar a molécula, denominando-se por isso região fingerprint.
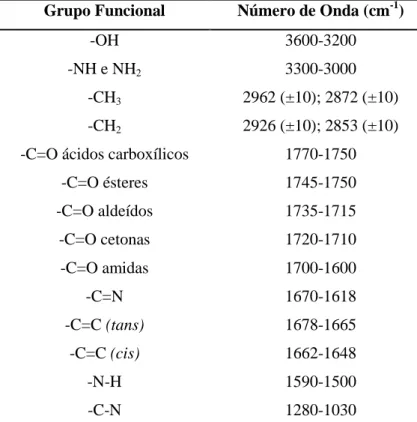
As bandas da região de frequências de grupo são facilmente identificáveis com recurso a tabelas, como a apresentada de seguida (tabela 2).
Grupo Funcional Número de Onda (cm-1)
-OH 3600-3200
-NH e NH2 3300-3000
-CH3 2962 (±10); 2872 (±10)
-CH2 2926 (±10); 2853 (±10)
-C=O ácidos carboxílicos 1770-1750
-C=O ésteres 1745-1750 -C=O aldeídos 1735-1715 -C=O cetonas 1720-1710 -C=O amidas 1700-1600 -C=N 1670-1618 -C=C (tans) 1678-1665 -C=C (cis) 1662-1648 -N-H 1590-1500 -C-N 1280-1030
10 Atualmente a espetroscopia de infravermelho é uma das técnicas analíticas mais promissoras, pois com ela consegue-se estudar praticamente qualquer tipo de amostra (Rohman & Man, 2012).
Os dados da espectroscopia de infravermelho são muito complexos, pelo que raramente são utilizados na sua forma original. Após a sua obtenção é necessário recorrer à quimiometria, por forma a extrair a maior quantidade de informação possível (Brereton, 2003). Essa informação pode ser interpretada recorrendo à análise multivariada, que relaciona os espetros obtidos com as propriedades em estudo (Brereton, 2003).
1.9.1. Espectroscopia de Infravermelho com Transformada de Fourier
Os espectrómetros de infravermelho começaram a ser usados na década de 40 do século XX e desde aí têm sido alvo de inúmeras modificações. Um dos mais importantes avanços nesta tecnologia foi a criação do espectrómetro de infravermelho com transformada de Fourier (FTIR). Este contém um interferómetro e explora um processo matemático denominado transformada de Fourier (Stuart, 2004; Skoog et al., 2008). Estes novos espectrómetros vieram melhorar de forma significativa a qualidade dos espetros obtidos e minimizaram o tempo de análise (Stuart, 2004).
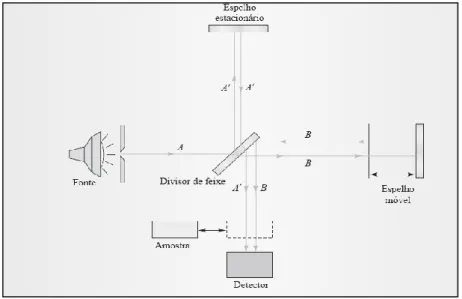
Os espectrómetros de infravermelho baseiam-se no interferómetro concebido por Michelson em finais do século XIX (Figura 3).
11 Neste aparelho, a radiação emitida interage com o divisor de feixe onde parte da radiação segue na mesma direção e outra parte é refletida para um espelho fixo. Os espelhos refletem a radiação de volta ao divisor de feixe onde se divide em duas partes. A parte da radiação que é refletida interage com a amostra. Os movimentos do espelho móvel determinam a intensidade com que a radiação interage com a amostra, em função do espaço que o espelho percorre. A isto chama-se interferograma, este é posteriormente convertido num espectro através dos algoritmos matemáticos da transformada de Fourier (Ismail et al., 2006; Skoog et al., 2008).
O recurso à transformada de Fourier permite uma melhor manipulação dos dados, uma vez que o sinal analógico e convertido num sinal digital, o ruído é minimizado e a resolução é melhorada (Ismail et al., 2006).
Na espectroscopia de FTIR, a transmissão e a reflexão total atenuada (ATR), são as técnicas mais usadas para a obtenção dos espectros. Na transmissão as amostras sólidas são misturadas com KBr, prensadas, formando uma pastilha que pode ser atravessada pela radiação. As amostras líquidas têm de ser colocadas numa célula-contentor específica, no entanto se, se tratar de amostras muito viscosas, estas podem ser colocadas entre duas janelas de KBr (Ismail et al., 2006).
Nesta técnica, a proporção de energia absorvida pelas moléculas é calculada a partir da medida da intensidade da radiação incidente e da radiação transmitida para a amostra. Esta técnica apresenta a desvantagem de ter de se controlar a espessura da amostra, uma vez que de acordo com a lei de Beer-Lambert, espessuras diferentes levam a absorções diferentes (Stuart, 2004).
A técnica de ATR utiliza a reflexão interna total. O feixe de radiação que penetra no cristal sofre reflexão interna total quando o ângulo de incidência na interface entre a amostra e o cristal for superior ao ângulo crítico, sendo este uma função dos índices de refração de duas superfícies. O feixe penetra uma fração de comprimento de onda para além da superfície refletora e, quando o material que absorve seletivamente a radiação está em contato com a superfície, o feixe perde energia no comprimento de onda em que o material absorve. É medida a radiação atenuada resultante, e usada pelo espetrofotómetro como uma função de comprimento de onda, dando assim as características espetrais de absorção da amostra (Stuart,
12 2004). Este método é utilizado na análise de amostras quer de sólidos quer de líquidos pouco ou muito viscosos.
Os modelos de cristais de ATR são vários, com especificidades diferentes; contudo, é o tamanho do cristal que vai determinar o número de interações que o feixe tem com a amostra. O modelo mais comum de um dispositivo de ATR encontra-se esquematizado na figura seguinte:
Figura 4 – Esquema de um dispositivo de ATR
1.9.2. Aplicações da espectroscopia de infravermelho na análise de alimentos
Nos últimos anos a espetroscopia de infravermelho tem-se afirmado com grande potencial na análise de amostras orgânicas e inorgânicas e, ainda, biológicas. Esta técnica tem especial utilidade na indústria farmacêutica, onde é utilizada no controlo da produção, e na indústria alimentar, permitindo garantir a autenticidade e características dos produtos (Aouidi et al., 2012).
A técnica FTIR-ATR possibilitou a evolução da espetroscopia de infravermelho, permitindo a análise de amostras sem qualquer preparação prévia. Viabiliza a automatização do controlo dos parâmetros mais importantes para a caraterização e diferenciação de vários produtos alimentares, como por exemplo óleos alimentares, vinagres, leite, bebidas alcoólicas, peixes, farinhas, mel e sumos de fruta (Duarte et al., 2002; Ruoff et al., 2006; Lachenmeier, 2007; Karoui et al., 2010; Santos et al., 2013).
13 1.10. Quimiometria
O termo quimiometria refere-se à aplicação de ferramentas matemáticas e estatísticas a problemas de origem química.
Em química alimentar recorre-se inúmeras vezes a métodos instrumentais como a espetroscopia e a cromatografia, para a caracterização de alimentos. No entanto, a informação obtida por estes meios apresenta uma grande complexidade, tornando-se difícil de interpretar (Pedrosa, 2010). A complexidade dos dados é agravada pela crescente sofisticação das técnicas instrumentais, aliada ao aparecimento de microprocessadores e microcomputadores.
Daqui decorre a necessidade de um tratamento de dados mais complexo, quer do ponto de vista matemático, quer estatístico, por forma a relacionar sinais obtidos por métodos instrumentais como, por exemplo, a concentração de um dado analito (Pedrosa, 2010).
A quimiometria utiliza métodos matemáticos, estatísticos e computacionais de forma a extrair o máximo de informação possível da análise química, podendo posteriormente ser retirada informação quantitativa e/ou qualitativa (Brereton, 2003).
A análise multivariada apresenta diferentes ferramentas de análise, sendo necessário escolher a mais adequada ao objetivo pretendido (Pedrosa, 2010). De entre todas as ferramentas destacam-se:
Análise de componentes principais (PCA) Regressão multivariada
Regressão linear múltipla (MLR) Regressão de Ridge (RR)
Regressão de componentes principais (PCR) Regressão por mínimos quadrados parciais (PLS) Análise fatorial de correspondência (AFC)
Análise discriminante (DA) Análise canónica de correlação Métodos de seleção de variáveis.
Os métodos de análise multivariada podem ser também divididos em dois tipos: métodos de análise supervisionada e métodos de análise não supervisionada. Os métodos supervisionados requerem um conhecimento prévio de informações acerca das amostras
14 utilizadas (Brereton, 2003; Lendl & Karlberg, 2005). Um exemplo de um método de análise supervisionada é a análise discriminante, em que se conhecem à priori os subgrupos nos dados observados (Brereton, 2003). Na análise não supervisionada, não é necessário ter qualquer informação sobre as amostras. O método de análise não supervisionada mais usado em quimiometria é a análise em componentes principais (Brereton, 2003; Lendl & Karlberg, 2005).
1.11. Objetivos do trabalho
A colheita da azeitona é normalmente iniciada pelos olivicultores durante os primeiros dias do mês de Novembro. Atualmente a tendência é antecipar a colheita em algumas cultivares como é o caso da Cobrançosa. No entanto, sabe-se que o estado de maturação influencia a composição química e a qualidade do azeite.
Os objetivos deste trabalho foram a aplicação da espectroscopia de infravermelho na distinção de clones de azeitona da cultivar Cobrançosa, bem como a distinção de dois estados de maturação muito próximos (semiverde e maduro) desses mesmos clones; este mesmo princípio foi aplicado aos respetivos azeites, com o mesmo objetivo. Em ambos os casos, recorreu-se à análise em componentes principais e análise discriminante.
Tendo em conta que num estudo prévio foi efetuada a caracterização química destas amostras de azeitonas e azeites, pretendeu-se ainda relacionar esses dados de composição química com os dados obtidos por espetroscopia de infravermelho, recorrendo para isso a técnicas de análise multivariada.
Capítulo II
Material e Métodos
15 2. Material e Métodos
2.1. Amostragem
Os seis clones estudados foram escolhidos, tendo em conta um estudo realizado durante dois anos consecutivos, no qual se utilizaram 24 clones provenientes de um campo clonal situado em Mirandela, Portugal.
As azeitonas foram colhidas em dois estados de maturação: semiverde e maduro. As amostras relativas ao estado semiverde foram colhidas em Outubro (14-10-2011), e as amostras maduras em Novembro (8-11-2011).
Os clones foram catalogados segundo o seu rendimento de produção e atividade antioxidante. Da amostragem escolhida para este trabalho, fazem parte os clones 1163 e 1191, catalogados como de alto rendimento de produção e com alta atividade antioxidante. Os clones 172 e 1023, com baixo rendimento de produção e alta atividade antioxidante; o clone 2271 que apresenta um alto rendimento de produção e uma baixa atividade antioxidante. Por fim o clone 2252 que tem um baixo rendimento de produção e uma baixa atividade antioxidante (Tabela 3).
Clone Rendimento de Produção Atividade Antioxidante
1163 Alto Alta 1191 Alto Alta 172 Baixo Alta 1023 Baixo Alta 2252 Baixo Baixa 2271 Alto Baixa Tabela 3 - Amostragem
As amostras de azeite foram preparadas na Unidade Nacional de Investigação Agrária (INIAV.I.P), Elvas, Portugal. Foram usados 3kg de azeitonas frescas, para a produção de azeite, usando um sistema Abencor.
16 2.2.Preparação das amostras de azeitona
As amostras de azeitona descaroçadas foram colocadas numa estufa a 60ºC, durante sete dias. Antes da leitura dos espetros, as amostras foram moídas, com recurso a azoto líquido, de modo a evitar problemas com a sobreposição das bandas relativas à água.
2.3. Aquisição dos espectros FTIR e pré-tratamento dos dados
A aquisição dos espetros de infravermelho do azeite foi efetuada num espectrómetro de infravermelho Unicam Research Series, equipado com um acessório de ATR de reflexão única (Golden Gate).
As amostras de azeite foram colocadas diretamente sobre o cristal, com auxílio de uma pipeta de Pasteur. No caso da azeitona colocou-se aproximadamente 0,1g de amostra sobre o cristal. A temperatura do cristal foi mantida a 40ºC. Os espetros foram medidos na região entre 4000cm-1 e 400cm-1, com uma resolução de 4cm-1 e 128 scans, com um tempo total de aquisição de cerca de 4 minutos. Mediram-se três réplicas de cada amostra de azeite e cinco para a azeitona, em cada réplica efetuaram-se duas repetições. Entre réplicas, o cristal foi cuidadosamente limpo com etanol a 95%, e efetuou-se um “background” (64 scans).
Após a aquisição dos espetros corrigiu-se automaticamente a linha de base no software winFirst versão 3.2. Os espetros foram divididos em duas regiões, uma primeira região entre 1800 cm-1 e 600 cm-1 e uma segunda região entre 3050 cm-1 e 2750 cm-1, as restantes regiões não foram utilizados pois não apresentam nenhum grupo funcional de interesse. Todos os dados foram normalizados, aplicando-se a normalização SNV (standard normal variate) e procedeu-se ao cálculo da 1ª derivada Savitzky–Golay. O cálculo da primeira derivada foi efetuado de modo a simplificar e sistematizar o tratamento dos dados.
2.4. Análise Multivariada
A análise multivariada foi realizada no programa XLSTAT versão 15.1. Para a distinção entre o estado semiverde e o estado maduro recorreu-se à análise em componentes principais (PCA). Esta análise foi também utilizada com o intuito de diferenciar cada clone.
17 Com o mesmo objetivo, aplicou-se a análise discriminante (DA) quer aos dados espetrais, quer aos dados relativos à composição química anteriormente efetuados (Sousa, 2012).
Por fim, tentou-se relacionar o espectro FTIR com esses parâmetros químicos, recorrendo a dois tipos de regressão: a regressão por componentes principais (PCR) e a regressão por mínimos quadrados parciais (PLS).
Capítulo III
Resultados e Discussão
18 3. Resultados e Discussão
3.1. Espetro FTIR típico da azeitona e do azeite
As técnicas espetroscópicas são extremamente úteis quando se pretende efetuar uma primeira análise não destrutiva às amostras. Estas técnicas permitem uma caracterização imediata dos constituintes da amostra em estudo. Quando as técnicas espectroscópicas são aliadas à análise multivariada permitem analisar uma grande variedade de amostras, identificando características particulares de cada uma delas. O desenvolvimento da técnica de ATR aumentou a importância e o uso do FTIR, em várias áreas científicas, muito devido à sua grande versatilidade, sendo facilmente aplicado quer em amostras orgânicas, quer inorgânicas (Rohman & Man, 2012).
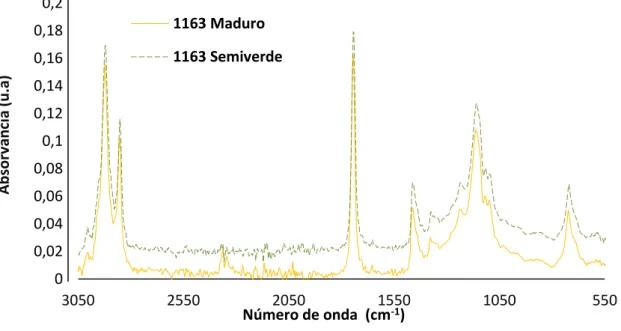
Apresenta-se na figura 5 um espetro típico de FTIR relativo ao estado semiverde e maduro de um dos clones analisados. Tal como se pode observar, não há alterações de perfil em termos de grupos funcionais entre os dois estados de maturação.
Figura 5- Espetro FTIR-ATR de um dos clones nos dois estados de maturação
Em ambos os casos encontra-se um pequeno pico a 3004cm-1 relativo à elongação da ligação =C-H em configuração cis. Os picos a 2923cm-1 e 2854cm-1 representam a elongação da ligação C-H dos grupos metileno das cadeias terminais dos ácidos gordos (Vlachos et al., 2006; Kuligwski et al., 2010; Lerma-Garcia et al., 2010).
0 0,02 0,04 0,06 0,08 0,1 0,12 0,14 0,16 0,18 0,2 550 1050 1550 2050 2550 3050 Abso rv ân ci a (u .a ) Número de onda (cm-1) 1163 Maduro 1163 Semiverde
19 O espetro contém ainda uma região, denominada região fingerprint (1900 cm-1 e 790 cm-1); esta é característica de cada substância, funcionando como uma impressão digital (Tapp et al., 2003). Segundo Lerma-Garcia et al., (2010), nesta região encontram-se os picos relacionados com a elongação do grupo –C-O- (1234 cm-1, 1160 cm-1, 1118 cm-1, 1099 cm-1). Este grupo pode pertencer quer aos ácidos gordos, quer a compostos fenólicos. Os picos a 1463 cm-1 e 1377 cm-1 correspondem à deformação da ligação C-H dos grupos metilo e metileno respetivamente. A 1745 cm-1 aparece um dos picos mais importante no espetro do azeite, que representa a elongação da ligação –C=O do grupo éster dos triglicéridos (Vlachos et al., 2006; Kuligwski et al., 2010; Lerma-Garcia et al., 2010).
A absorvância de cada um destes grupos funcionais varia consoante o estado de maturação. Verifica-se que de um modo geral, há uma diminuição da absorvância do estado semiverde para o estado maduro nos comprimentos de onda relativos à elongação do grupo -C-O, por outro lado ocorre um incremento na absorvância do grupo éster. O aumento do valor de absorvância do grupo éster no estado maduro pode ser explicado pelo aumento do teor de gordura que ocorre durante a maturação do fruto; o conteúdo de gordura é máximo nos frutos bem maduros (Salvador et al., 2001; Tovar et al., 2002; Baccouri et al., 2008; Campoeso et al., 2013). Por outro lado, a variação da absorvância na região de vibração do grupo –C-O- pode estar relacionada com a diminuição do teor de compostos fenólicos que ocorre nos frutos maduros (Tovar et al., 2002; Machado et al. 2013).
Durante a maturação do fruto ocorrem várias alterações na sua composição química principalmente no perfil fenólico, e no teor de gordura (Tovar et al. 2002; Kalua et al., 2005). Estas alterações vão condicionar de forma significativa a qualidade e características organolética dos azeites (Morelló et al., 2004). Vários estudos, demonstram que a diminuição do teor de compostos fenólicos ao longo da maturação do fruto vai originar azeites mais apagados e menos fragrantes, bem como azeites com menor resistência à oxidação (Salvador et al., 2001, Matos et al., 2007, Baccouri et al., 2008, Gómez-Rico et al., 2008; Nieto et al., 2010). Outra característica que é afetada é a acidez do azeite, que sofre um aumento ao longo da maturação (Salvador et al., 2001, Matos et al., 2007).
20 3.2. Aplicação da análise em componentes principais (PCA) aos dados espetrais do azeite
A análise em componentes principais é um dos métodos quimiométricos mais utilizado para a redução de dados e análise exploratória (Jolliffe, 1986; Brereton, 2003). O principal objetivo da PCA é a obtenção de um pequeno conjunto de componentes principais (também chamadas “variáveis latentes”) que contêm a maior parte da variabilidade. O novo subespaço definido por esses componentes principais conduz a um modelo que é mais fácil de interpretar que o conjunto de dados original (Jolliffe, 1986).
Para a análise em componentes principais, utilizaram-se os valores de absorvância dos picos da região entre 3050 cm-1 e 2750cm-1 e da região fingerprint. Aplicando a PCA a cada clone individualmente, obteve-se para a maioria dos clones uma boa separação entre os dois estados de maturação em estudo (Figura 6).
Figura 6- Gráfico das coordenadas fatoriais para os clones a) 172 no plano F1/F4 e b) 1023 no plano F1/F2
(SV - semiverde e M – maduro)
Na figura 7 estão representados os números de onda que contribuem para a distinção entre o estado maduro e o estado semiverde, sendo que os que mais contribuem para essa diferenciação são: 2923, 1745, 1463, 1234, 1160 e 1118cm-1. M1A M1B M2A M2B M3A M3B SV1A SV1B SV2A SV2B SV3A SV3B -3 -2 -1 0 1 2 3 -4 -3 -2 -1 0 1 2 3 4 F4 (7,35 %) F1 (42,02 %) Observações (eixos F1 e F4: 49,36 %) CLONE 172 M1A M1B M2A M2B M3A M3B SV1A SV1B SV2A SV2B SV3A SV3B -3 -2 -1 0 1 2 3 -4 -3 -2 -1 0 1 2 3 4 F2 ( 2 5 .4 9 % ) F1 (50.85 %) Observações (eixos F1 e F2: 76.34 %) CLONE 1023
21 Figura 7- Números de onda que mais contribuem para a discriminação entre o estado semiverde e maduro
O pico a 1745 cm-1, tal como já foi dito anteriormente, refere-se à elongação da ligação C=O do grupo éster dos triglicéridos. Tendo isto em consideração, pode dizer-se que a diferença do teor de gordura do estado semiverde para o estado maduro é determinante para a separação dos estados de maturação em estudo.
Os picos 1234 cm-1,1160 cm-1 e 1118 cm-1, estão relacionados com o grupo –C-O-, o que indica que a variação do teor de compostos de origem fenólica é também importante para se conseguirem separar claramente dois estados de maturação.
Verificou-se que quatro componentes principais englobavam cerca de 94% da variabilidade existente entre os dois estados de maturação. No entanto, na maior parte dos casos foram necessárias apenas duas componentes principais para separar os estados de maturação estudados. Verifica-se que, a componente principal responsável por essa separação não é sempre a mesma. Esta situação pode ser explicada por se tratar de diferentes clones, que apresentam algumas diferenças na sua composição química, uma vez que temos clones com alta atividade antioxidante e com baixa atividade antioxidante, o que estará diretamente relacionado com o teor de compostos fenólicos.
Nos clones 1191 e 2252 não se conseguiu obter uma distinção bem clara entre os estados de maturação (Figura 8).
-0,4 -0,2 0,0 0,2 0,4 0,6 0,8 1099 1119 1161 1234 1377 1464 1745 2854 2924 3004 Co n tr ib u iç ão Fato ri al Número de onda (cm-1) F1 F2
22 Figura 8- Gráfico das coordenadas fatoriais para os clones 2252 no plano F1/F3 e 1191 no plano F1/F3
Em estudos anteriores, Sousa, (2012) verificou que para o clone 2252 não existiam diferenças significativas entre o estado semiverde e o estado maduro, ao nível do perfil fenólico e atividade antioxidante. Segundo o mesmo estudo não se obtiveram diferenças significativas no teor de orto-difenóis e flavonoides no clone 1191.
Com vista à distinção dos clones, aplicou-se a PCA a todos os dados independentemente do estado de maturação, verificando-se a formação de três grupos (Figura 9).
Figura 9- Coordenadas fatoriais de todos os clones independentemente do estado de maturação
Há a clara formação de um grupo que se destaca dos restantes, onde se encontram as amostras relativas ao clone 1163; este clone apresenta um elevado rendimento de produção e uma elevada atividade antioxidante. Segundo Sousa (2012), este clone apresenta também
M1A M1B M2A M2B M3A M3B SV1A SV1B SV2A SV2B SV3A SV3B -2 -1 0 1 2 3 4 -3 -2 -1 0 1 2 3 4 5 F3 (10. 21 %) F1 (46.07 %) Observações (eixos F1 e F3: 56.28 %) CLONE 2252 M1A M1B M2A M2B M3A M3B SV1A SV1B SV2A SV2B SV3A SV3B -4 -3 -2 -1 0 1 2 3 4 -6 -5 -4 -3 -2 -1 0 1 2 3 4 F3 (10. 72 %) F1 (57.48 %) Observações (eixos F1 e F3: 68.20 %) CLONE 1191 172M 172SV 1163M 1163SV 1023M 1023SV 1191M 1191SV 2252SV 2252M 2271M 2271SV -3 -2 -1 0 1 2 3 4 -2 -1 0 1 2 3 4 5 6 7 F2 (7. 37 %) F1 (92.52 %) Observações (eixos F1 e F2: 99.88 %)
23 maior teor de compostos fenólicos comparativamente aos outros clones. Outro dos grupos formado corresponde ao clone 172 (clone com alta atividade antioxidante, mas baixo rendimento de produção). Por fim um grupo que engloba os clones 1191, 2252, 1023, 2271. Estes clones apresentam valores de absorvância muito semelhantes para os números de onda utilizados, tornando-se assim mais difíceis de separar. A componente principal 1 contém 92,5% da variabilidade total existente entre os clones. Utilizando as coordenadas fatoriais de cada amostra nesta componente principal, confirma-se que o clone 1163 se encontra destacado, de onde se pode deduzir que este tem características diferentes de todos os outros. Os restantes clones, tal como já foi referido, não se conseguem separar claramente, tendo um valor para PC1 muito semelhante (Figura 10).
Figura 10- Coordenadas fatoriais da primeira componente principal para os dados FTIR
Numa tentativa de obter uma melhor separação de cada clone utilizaram-se os dados de apenas um dos estados de maturação, conseguindo-se assim uma separação mais clara de cada clone (Figura 11). Os clones 172 e 1163 aparecem claramente distanciados de todos os outros levando a crer que sejam os clones mais diferentes. Já os clones 2252 e 1023 parecem muito próximos apesar de terem um comportamento diferente, visto que o clone 2252 apresenta baixa atividade antioxidante e baixo rendimento de produção. E por outro lado o clone 1023 apresenta baixo rendimento de produção mas elevada atividade antioxidante.
-2,000 0,000 2,000 4,000 6,000 8,000 0 2 4 6 8 10 12 14 PC1 (92.5 2% ) ID AMOSTRA 172M 172SV 1163M 1163SV 1023M 1023SV 1191M 1191SV 2252M 2252SV 2271M 2271SV
24 Figura 11- Coordenadas fatoriais de todos os clones apenas num estado de maturação (maduro)
3.3.Aplicação da Análise Discriminante (DA) aos dados espetrais do azeite
A análise discriminante (DA) é um método amplamente utilizado em aplicações que envolvam uma grande quantidade de dados (Pires e Branco, 2010). O recurso a componentes principais nem sempre é uma boa solução para efeitos de discriminação. Isto porque a direção da variabilidade principal pode não coincidir com as direções de melhor discriminação. A análise discriminante tem por objetivo separar subgrupos de amostras, que são previamente conhecidos nos dados observados (Hubert & Driessen, 2004).
De forma a tentar obter uma melhor diferenciação entre os clones, aplicou-se a análise discriminante aos mesmos dados utilizados na PCA (Figura 12).
Figura 12- Gráfico das coordenadas fatoriais para todos os clones nos dois estados de maturação
172 1163 1023 1191 2252 2271 -2 -1 0 1 2 -8 -7 -6 -5 -4 -3 -2 -1 0 1 2 3 4 5 6 7 8 F2 (8. 13 %) F1 (91.75 %) Observações (eixos F1 e F2: 99.88 %) 172M 172SV 1023M 1023SV 1163M 1163SV 1191M 1191SV 2252M 2252SV 2271M 2271SV -2000 -1500 -1000 -500 0 500 1000 1500 2000 -4000-3500-3000-2500-2000-1500-1000 -500 0 500 1000 1500 D F2 (0. 35 %) DF1 (99.65 %) Observações (eixos F1 e F2: 100.00 %) 172 1023 1163 1191 2252 2271
25 Verificou-se a formação de dois grupos, um com o clone 1163 muito distanciado dos restantes clones como de resto já acontecia na análise em componentes principais. Outro grupo com os clones 172, 1023, 1191, 2252, 2271, em que o clone 172 aparece ligeiramente distanciado dos restantes clones que compõem este grupo. Esta observação coincide também com os resultados obtidos por PCA, embora aqui o clone 172 não apareça tão destacado dos restantes.
Numa outra tentativa de distinguir clones, usaram-se apenas os resultados dos parâmetros químicos atividade antioxidante, fenóis totais, orto-difenóis e flavonoides analisados por Sousa (2012) (anexo C).
Neste caso, verifica-se uma distinção clara entre os clones e também entre os dois estados de maturação, semiverde e maduro (Figura 13).
Figura 13 – Gráfico das coordenadas fatoriais da análise discriminante aplicada aos resultados das análises
químicas do azeite
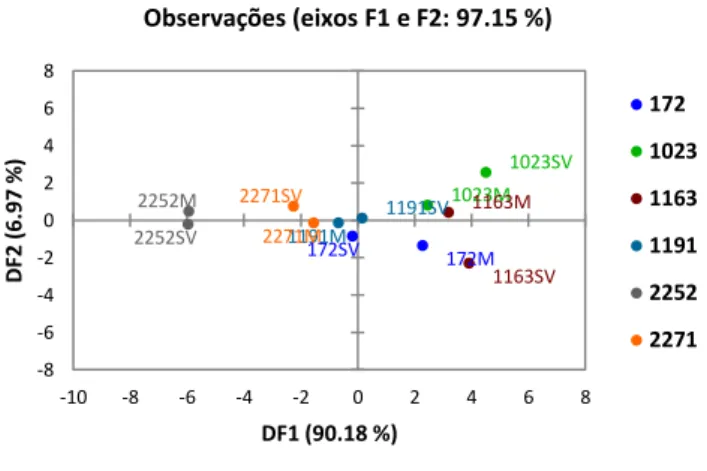
De forma a obter melhores resultados na distinção dos clones, utilizaram-se os dados obtidos através da 1ª derivada de Savitzky-Golay. Consideraram-se para esta análise os números de onda entre 740 e 700 cm-1, 1050 e 950 cm-1, 1250 e 1100 cm-1, 1500e 1350 cm-1, 1800 e 1700 cm-1 e 3050 e 2750 cm-1. Este novo conjunto de dados foi submetido à análise discriminante em função dos dados relativos ao rendimento de produção e atividade antioxidante. Na figura 14 é mostrado o diagrama das observações, definido pelos fatores discriminantes DF1 e DF2, que explicaram a variação total. Observa-se a formação de quatro grupos, um composto pelos clones de alto rendimento de produção e alta atividade antioxidante (AA), clones 1163 e 1191, outro grupo com os clones 172 e 1023 (BA), que apresentam baixo rendimento de produção, mas elevada atividade antioxidante. Um terceiro
172M 172SV 1023M 1023SV 1163M 1163SV 1191M 1191SV 2252M 2252SV 2271M 2271SV -8 -6 -4 -2 0 2 4 6 8 -10 -8 -6 -4 -2 0 2 4 6 8 D F2 (6. 97 %) DF1 (90.18 %) Observações (eixos F1 e F2: 97.15 %) 172 1023 1163 1191 2252 2271
26 grupo com o clone 2271, clone que apresenta alto rendimento de produção e baixa atividade antioxidante (BA) e por fim um grupo com o clone 2252, clone com baixo rendimento de produção e baixa atividade antioxidante (BB).
Figura 14- Análise discriminante em função da atividade antioxidante e rendimento de produção, coordenadas
fatoriais nas dimensões DF1 e DF2
Esta classificação resulta de um modelo de análise discriminante, com 85,4% de classificação correta aquando da sua validação (cross-validation) (Tabela 5).
Calibração Validação (Cross-validation)
HH LL LH HL % correta HH LL LH HL % correta HH 12 0 0 0 100 9 1 2 0 75,0 LL 0 6 0 0 100 1 5 0 0 83,3 LH 0 0 6 0 100 1 0 5 0 83,3 HL 0 0 0 12 100 0 0 0 12 100
Tabela 4- Matriz de confusão para os dados, e resultados da validação cruzada com base na atividade
antioxidante e rendimento de produção. Classificações observadas nas linhas, e classificações previstas nas colunas.
3.4. Regressão das componentes principais (PCR) para os dados do azeite
A regressão de componentes principais (PCR) tem por base a análise de componentes principais, sendo muito utilizada na calibração espetroscópica (Xie & Kalivas, 1997). A escolha do número de componentes principais a utilizar é a etapa chave para o sucesso da aplicação deste método de regressão. A regressão PCR e outros tipos de regressão como o PLS são normalmente aplicadas ao espetro completo, no entanto o espetro tem muitas vezes
-2,0 -1,5 -1,0 -0,5 0,0 0,5 1,0 1,5 2,0 -2,5 -2,0 -1,5 -1,0 -0,5 0,0 0,5 1,0 1,5 2,0 2,5 AA 1191 AA 1163 BB 2252 AB 2271 BA 172 BA 1023 DF1 (80.2%) DF2 (1 9 .8 %) Observações (eixos DF1 e DF2: 100,0%)
27 regiões pouco informativas, que influenciam a qualidade dos modelos obtidos (Malinowski, 1991; Faber et al., 1995a,b; Centner et al., 1996). A eliminação destas regiões leva a modelos menos complexos e mais robustos (Centner et al., 1996). A precisão do modelo é também melhorada quando se retiram regiões do espetro pouco informativas, sendo este efeito mais percetível quando se usam apenas uma ou poucas regiões do espetro.
A regressão das componentes principais foi utilizada para estabelecer a relação entre os dados espetrais e os parâmetros químicos estudados por Sousa, (2012): atividade antioxidante, teor de fenóis totais, orto-difenóis e flavonoides (anexo C).
A qualidade do modelo foi avaliada pela raiz quadrada do erro médio de calibração (RMSEC), coeficiente de determinação múltipla ou coeficiente de regressão (R2, onde R é o fator de correlação) e pela raiz quadrada do erro médio de validação cruzada (RMSECV).
Os valores de RMSEC e RMSECV são dados pelas seguintes equações:
√ √[ ]
Em que yi representa o valor de referência, e yi’ o valor estimado pelo modelo usando k variáveis latentes, e n representa o número de observações.
Os modelos PCR foram validados segundo o método de validação cruzada leave-one-out (LOO). O número ótimo de fatores é aquele que minimiza o valor RMSECV.
Na otimização das regiões espetrais a utilizar, foram selecionadas as regiões que contêm as informações mais significativas, De Luca (2009). As regiões de frequência utilizadas para a quantificação foram baseadas na capacidade de fornecer alta correlação entre as variáveis dependentes (respostas reais) e os espetros FTIR correspondentes. Com base nesta otimização, os pares de números de onda utilizados para a regressão foram 740 e 700 cm-1, 1050 e 950 cm-1, 1250 e 1100 cm-1, 1500e 1350 cm-1, 1800 e 1700 cm-1 e 3050 e 2750 cm-1. A figura 15 representa o comportamento de RMSEC e RMSECV em função do número de componentes principais, para a atividade antioxidante, fenóis totais, orto-difenóis e flavonoides.
28 0,000 0,200 0,400 0,600 0,800 1,000 1 2 3 4 5 6 7
Número de Componentes Principais
RMSEC orto-difenóis RMSECV orto-difenóis R M SE C / R M SE CV 0,0 0,2 0,4 0,6 0,8 1,0 1,2 1,4 1 2 3 4 5 6 7
Número de Componentes Principais
RMSEC Flavonoides RMSECV Flavonoides R M SE C / R M SE CV 0,0 2,0 4,0 6,0 8,0 1 2 3 4 5 6 7
Número de Componentes Principais
RMSEC Atividade Antioxidante RMSECV Atividade Antioxidante
R M SE C / R M SE CV 0,0 0,5 1,0 1,5 2,0 1 2 3 4 5 6 7
Número de Componentes Principais
RMSEC Fenóis Totais RMSECV Fenóis Totais
R M SE C / R M SE CV
29 Na tabela 6 encontram-se os dados da calibração e validação do método para todos os parâmetros químicos em estudo.
Parâmetro Químico Número de PC R 2 Calibração R 2 Validação RMSEC (%) RMSECV (%) Atividade Antioxidante 4 0,95 0,87 7,65 18,74 Fenóis Totais 4 0,93 0,89 16,47 14,08 orto-difenóis 4 0,92 0,81 9,30 24,81 Flavonoides 4 0,93 0,91 7,75 7,75
Tabela 5 – Calibração e validação da regressão PCR para o azeite
Na figura seguinte, encontra-se ilustrada a qualidade dos modelos PCR para os parâmetros químicos analisados por Sousa, 2012. Para a atividade antioxidante (AA) verificou-se uma correlação de 93,27% entre os dados preditivos do espetro de infravermelho e os dados medidos por Sousa (2012). Os teores de fenóis totais, orto-difenóis e flavonoides encontram-se também altamente correlacionados com os dados obtidos por FTIR, 94,33%; 90%; 95,39% respetivamente (Figura 16).