Les rétrotransposons LTR sont définis par la présence de longues répétitions terminales (LTR) aux extrémités 5' et 3', et l'archétype de ces éléments est la levure Ty1 (Cameron, Loh et al. 1979). Ce gène est responsable de l'assemblage des VLP (virus-like particules) dans la cellule et est nécessaire à la rétrotransposition dans les rétrotransposons de type IAP chez la souris (Dewannieux, Dupressoir et al. 2004).
R ETROVIRUS
Les rétrovirus, des rétroéléments
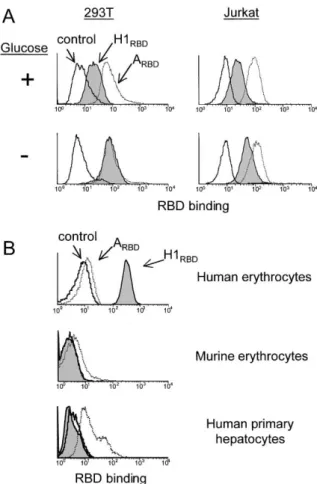
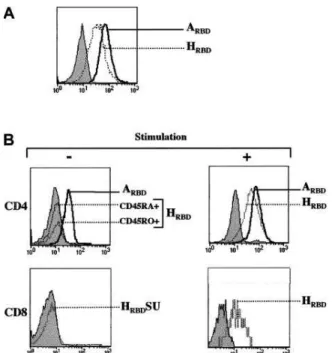
In contrast, amphotropic RBD (ARBD) binding was observed at all 3 temperatures (data not shown). Expression of the HTLV receptor on the glucose-starved CD147 cell ( Kirk et al., 2000 ) increases during T cell activation.
Biologie des rétrovirus
IN est responsable du clivage de 2 nucléotides 3' de chaque brin de la molécule d'ADN proviral (activité endonucléase) et de l'intégration de cet ADN proviral dans le génome cellulaire (activité de liaison à l'ADN). Le PPT est suivi de la région U3 (unique 3') qui est impliquée dans la rétrotranscription du génome viral et qui contient également les séquences promotrices de la transcription.
Ainsi, lors du bourgeonnement viral, la voie cellulaire par défaut semble être la dégradation du noyau viral dans la voie lysosomale (Basyuk, Galli et al. 2003). Zhang, Yang et coll. 2003) implique une activité cytidine désaminase pour le VIH et conduit à la dégradation du génome viral.
Emergence des rétrovirus par acquisition du gène env
Il pourrait donc être possible de proposer une vision alternative du cycle de réplication rétrovirale, où le métabolisme du virus à différentes étapes du cycle serait la voie « par défaut ». D'un point de vue évolutif, les mécanismes de réplication virale productive peuvent avoir été sélectionnés sur la base de l'évasion de ces voies de catabolisme des complexes ribonucléoprotéiques.
Initialement, le gène env du SERV (rétrovirus endogène simien) semble s'être recombiné avec le PcEV (virus endogène du papio cynocephalus) pour donner naissance au BaEV (virus endogène du babouin). Le virus ovin et caprin responsable de l'adénocarcinome pulmonaire ovin est un rétrovirus de type D dont le gène env est apparenté aux rétrovirus de type B selon l'ancienne nomenclature (York, Vigne et al. 1992).
Cependant, ce modèle est contredit par des données récentes indiquant que dans des conditions de non-surexpression, situations naturelles de rétrovirus réplicatifs, les protéines virales Gag en l'absence d'Env ne bourgeonnent pas à la surface cellulaire, mais sont ciblées vers des compartiments de dégradation (Basyuk, Galli et coll., 2003). En revanche, l'ajout d'Env redirige le corps viral vers un compartiment sécrétoire (surface cellulaire ou corps multivésiculaire) où le bourgeonnement est productif (Basyuk, Galli et al. 2003 ; Sandrin, Muriaux et al. 2004).
HTLV est-il un virus pathogène ?
L'ATL est une leucémie agressive qui, lorsqu'elle est présente, est mortelle en moins d'un an (Siegel, Gartenhaus et al. 2001). L'ATL est également caractérisée par une hypercalcémie ainsi que des lésions cutanées associées à une infiltration lymphocytaire (Blayney, Jaffe et al. 1983).
Une pandémie ou de nombreuses endémies ?
HTLV est un virus ancien
27 a été introduit beaucoup plus tard dans les populations humaines par des souches simiennes du SIV (Korber, Muldoon et al. 2000). Concernant ce dernier point, la réplication résultante du HTLV semble se produire principalement sous forme provirale, par division cellulaire (Wattel, Vartanian et al. 1995).
Tropisme
La recherche de séquences HTLV par hybridation in situ dans des cerveaux post-mortem de patients atteints de myélopathie a montré que les astrocytes peuvent également être infectés (Lehky, Fox et al. 1995). Une infection in vivo de cellules adhérentes sans culture a été occasionnellement décrite, en particulier dans l'épithélium des glandes salivaires (Setoyama, Kerdel et al. 1998; Setoyama, Mizoguchi et al. 1999; Tangy, Ossondo et al. 1999), dans les cellules endothéliales vasculaires (Setoyama, Kerdel et al. 1998) et les glandes mammaires (Loureiro, Southern et al. 2000).
La réponse immunitaire au HTLV
A fusion-active form of the ampho- MLV Env (A⌬R) and the vesicular stomatitis virus G glycoprotein also induced equivalent numbers of large syncytia in NIH 3T3(TK⫺) and NIH 3T3 cells (not shown). Notably, however, alignment of the HTLV-1 SU with that of the Friend murine leukemia virus (F-MLV) reveals highly conserved microdomains within the SU and underscores a similar general organization of the SU (Kim et al a) (Figure 2) .
Env
La région correspondant au premier exon de rex et la région pX sont donc requises. Il sera intéressant d'évaluer si d'éventuels sites d'épissage cryptiques dans env, démasqués en l'absence du premier exon de rex et de la région pX, pourraient expliquer cette observation.
32 L'ectodomaine du TM du HTLV pourrait être cristallisé et présente la forme d'un trimère d'hélices enroulées (coiled coil) à l'extrémité N-terminale, conservé dans les rétrovirus, suivi d'un domaine C-terminal replié de manière anti-parallèle dans le domaine de la bobine enroulée (Kobe, Center et al. 1999). Le HTLV TM, comme la plupart des MT rétrovirales (à l'exception du VIH, du MMTV et du HERV-K), possède également un motif homologue au domaine immunosuppresseur CKS17 du Moloney-MLV TM (Cianciolo, Copeland et al. 1985).
Amino acid residue numbering starts from the first signal peptide methionine of the HTLV-1 Env precursor. Notably, binding of HTLV SU to these cells occurred regardless of whether they formed syncytia or not in the presence of HTLV Env [29] and data not shown).
Une coopération positive entre les molécules réceptrices a été démontrée pour la liaison des RBD du MLV amphotrope (Battini, Rodrigues et al. 1996), mais un lien possible entre cette coopération de liaison et la mobilité des récepteurs n'est pas connu. Après l'entrée du virus, le devenir des complexes TM et SU/récepteur n'est pas connu, et une éventuelle colocalisation de ces complexes avec la capside entrante au niveau des vésicules endocytaires n'a pas été établie.
Attachement, liaison et récepteur cellulaire
Ainsi, les HSPG sont impliqués dans la fixation et l’entrée d’un grand nombre de virus humains et animaux enveloppés et non enveloppés, par ex. en amont d’une entrée virale appropriée, l’adhésion via les HSPG ou d’autres composants de la matrice extracellulaire module nécessairement la liaison spécifique aux récepteurs d’entrée.
Transmission cellule à cellule
Il est donc probable que les HSPG, comme d’autres enveloppes virales, soient impliquées dans la liaison non spécifique du HTLV Env et probablement aussi des virions eux-mêmes. Ce sont ces récepteurs d'entrée qui permettent (i) de lier spécifiquement le virus et (ii) d'induire, dans le confinement à la surface cellulaire, les changements conformationnels d'Env responsables de la fusion des membranes virales et cellulaires. .
L'infection par transmission de cellule à cellule, par exemple par co-culture de cellules cibles et de cellules infectées, n'a pas non plus été prouvée. Seules des cultures cellulaires infectées de manière chronique par HTLV (par exemple lignées MT-2, C91/PL) ont été établies.
Une seule étude a démontré une préférence formelle pour la transmission de cellule à cellule pour le HTLV (Landau, Page et al. 1991). Dans cette étude, les virions VIH pseudotypés par l'Env HTLV, mais aussi dans une moindre mesure d'autres Env rétroviraux, sont plus infectieux par coculture de cellules cibles avec des cellules productrices que par inoculation de cellules cibles avec un surnageant viral.
Cependant, la transmission de cellule à cellule du HTLV est plus efficace que la transmission par surnageant acellulaire dans des lignées cellulaires qui ne sont pas de type lymphoïde (Landau, Page et al. 1991). Il est donc important d'évaluer si les structures de contact impliquées dans ces lignées sont similaires à la synapse virologique telle que décrite (Igakura, Stinchcombe et al. 2003).
CARACTERISATION DE L'EXPRESSION DU RECEPTEUR HTLV A LA SURFACE DES
Résumé article 1
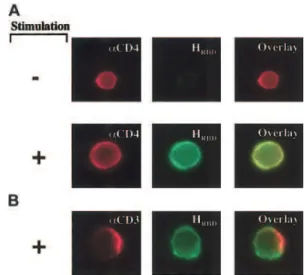
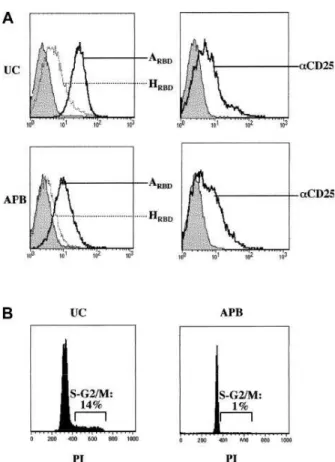
Dans ces cellules, nous avons pu démontrer que la prolifération est associée à l'expression du récepteur HTLV. Ainsi, l'apparition du récepteur HTLV à la surface des lymphocytes accompagne la prolifération, qu'il s'engage ou non avec le TCR.
Article original 1
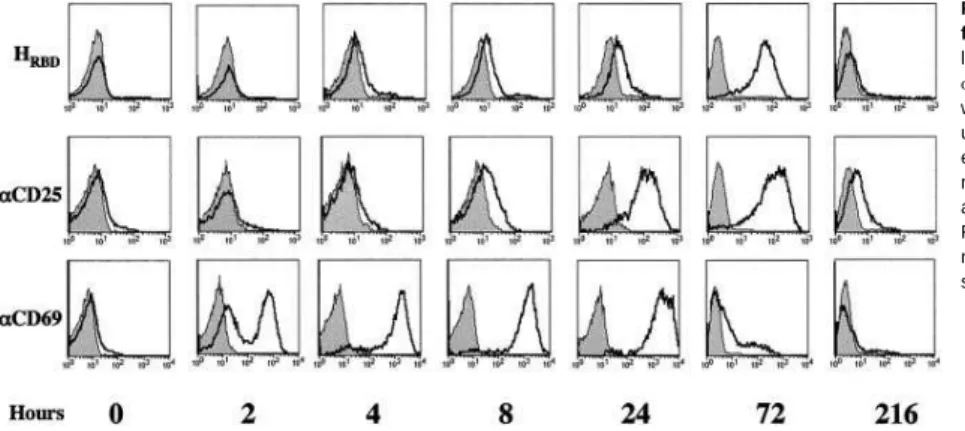
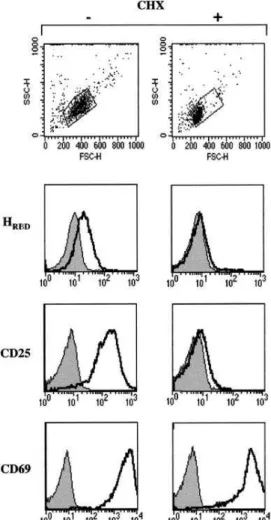
Cell surface expression of the HTLV receptor was compared with the expression of 2 markers of early activation, CD25 (IL-2R␣ chain) and CD69 (Figure 3). Upregulation of HTLV receptor as well as CD25 expression were completely abrogated by CHX treatment (Figure 4).
Conclusion article 1
Les cellules souches CD34+, qui sont à un stade de différenciation plus précoce, sont infectables ex vivo par HTLV (cependant cette observation n'a pas pu être confirmée chez les patients (Nagafuji, Harada et al. 1993)) et leur inoculation à des souris humanisées SCID conduit à l'apparition de thymocytes infectés (Feuer, Fraser et al. 1996). En effet, il a été démontré que la population de cellules infectées par HTLV dans le sang périphérique résulte d'un nombre limité, généralement d'une dizaine d'événements d'infection (Wattel, Vartanian et al. 1995 ; Cavrois, Gessain et al. 1996), qui résultent provenant de l'expansion oligoclonale à une charge provirale comprise entre 1 et 10 copies pour 100 PBMC (Wattel, Vartanian et al. 1995; Cavrois, Gessain et al. 1996).
IDENTIFICATION DU TRANSPORTEUR DE GLUCOSE GLUT1 COMME RECEPTEUR
Résume article 2
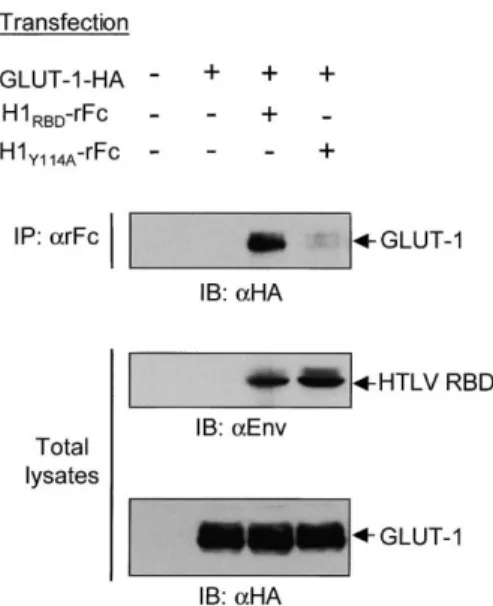
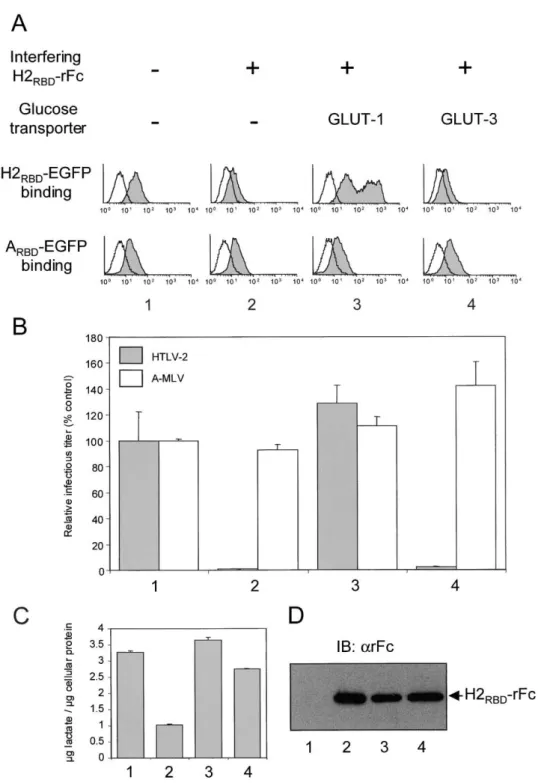
Le traitement des cellules avec un mélange d'ARN interférents entraîne une baisse de l'expression de GLUT1 d'environ 50 %, accompagnée d'une baisse du transport du glucose du même ordre. Toutes ces expériences prouvent donc que le transporteur de glucose GLUT1 est le récepteur du HTLV.
Article original 2
The positions of HTLV-1 Env precursors (Pr Env), mature TM, and mature SU envelope proteins are indicated. Organization and sequence homologies of SU MLV and HTLVenv (Kim et al., 2000, and submitted for publication).
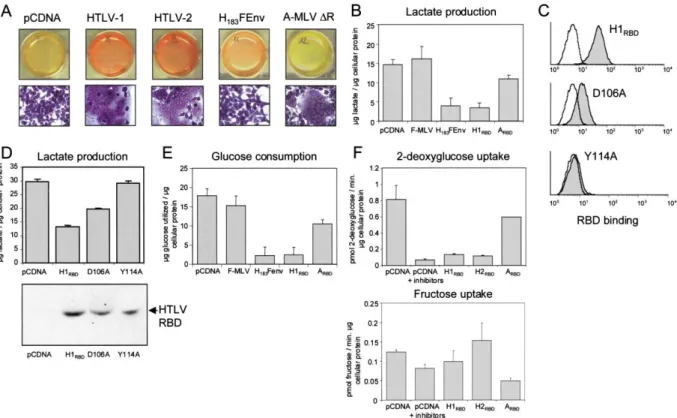
Conclusion article 2
PROPRIETES DISTINCTES DE LIAISON ET D'INFECTION SUR GLUT1
Résumé article 3
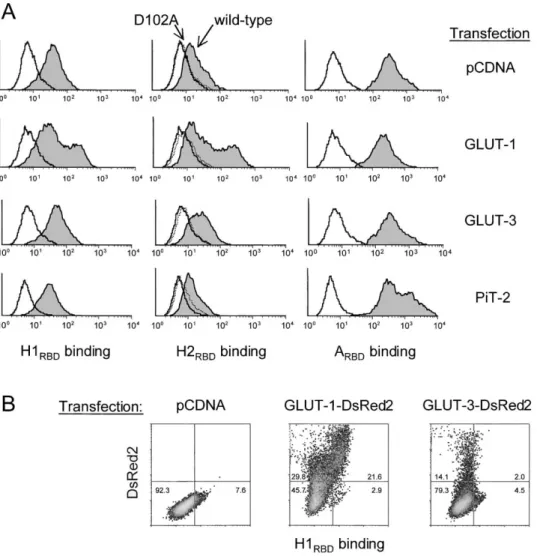
Nous avons montré que la simple présence des 7 acides aminés de la boucle numéro 6 de GLUT1 est suffisante pour conférer une activité de liaison à GLUT3 au RBD du HTLV Env. Cependant, cette activité n'est pas suffisante pour garantir l'infection des virions pseudotypés par le HTLV Env.
Article original 3
For example, insertion of the GLUT3 cytoplasmic tail into the GLUT1 background did not modify HTLV Env binding (data not shown). The Y-S-L-I tyrosine-based motif in the cytoplasmic domain of the T-cell leukemia virus type 1 envelope is essential for cell-to-cell transmission.
Conclusion article 3
BIOLOGIE DE L'ENV HTLV
Modulation de l'activité de l'Env HTLV
Il apparaît donc que les propriétés de fusion propres au HTLV Env sont altérées dans ces cellules. Récemment, il a été démontré que la protéine hDlg interagit avec le domaine intracellulaire du HTLV Env (Blot, Delamarre et al. 2004).
Env HTLV endogènes ?
Furthermore, introduction of the herpes simplex virus type 1tk gene into NIH 3T3(TK⫺) cells did not lead to HTLV Env syncytium sensitivity (not shown). In addition, GLUT1 is expressed in glial cells of the central nervous system (Kumagaiet al., 1994; Virgintino et al., 1997).
GLUT1 COMME RECEPTEUR HLTV
La famille des transporteurs de glucose
Dans les cellules épithéliales, GLUT1 et GLUT3 ont également une localisation différente (Inukai, Shewan et al. 2004). La protéine intracellulaire TUG interagit avec GLUT4 et est impliquée dans le trafic de GLUT4 (Bogan, Hendon et al. 2003).
GLUT1 et tropisme HTLV
De tous les GLUT, seul GLUT3 existe également en tant que pseudogène (il existe 3 pseudogènes GLUT3) (Zhang, Harrison et al. 2003). GLUT1 est une protéine hautement conservée chez les mammifères (identité à 86 % parmi GLUT1 provenant de l'homme, du chimpanzé, du lapin, de la souris, du rat, de la vache et de l'opossum), ce qui est en corrélation avec le large tropisme in vitro du HTLV Env.
GLUT1 et la famille des récepteurs rétroviraux
On pense que la paire de récepteurs Env a évolué principalement à partir d’un mécanisme cellulaire impliqué dans le transport vers la membrane plasmique. Les partenaires impliqués dans le transport des récepteurs vers la membrane plasmique ne sont pas connus.
Transporteurs de glucose, cycle cellulaire et trafic membranaire
HTLV Env serait recruté dans la synapse infectieuse lors d'un contact de cellule à cellule (Igakura, Stinchcombe et al. 2003). Il est possible que GLUT1 sur les cellules cibles soit recruté au voisinage de la synapse par HTLV Env exprimé à la surface des cellules infectées (observations non publiées mentionnées dans (Jolly et Sattentau 2004)) par un autre mécanisme impliquant, par exemple, l'adhésion immunologique des molécules synapses. (Derse et Heidecker 2003).
L'Env HTLV, un marqueur de marqueur
De plus, cette concentration locale d'Env se localise avec la protéine hDlg (Blot, Delamarre et al. 2004). GLUT1 est déjà utilisé comme marqueur pour de nombreuses tumeurs, et une expression élevée de GLUT1 est généralement de mauvais pronostic (Haber, Rathan et al. 1998).
Partenaires de GLUT1
Notamment, la détection des tumeurs cérébrales par PET-SCAN repose sur l'utilisation de fluorodésoxyglucose radioactif transporté dans les cellules exclusivement par GLUT1 (Brown et Wahl 1993 ; Higashi, Tamaki et al. 1997). La myosine VI est la seule myosine impliquée dans le transport rétrograde le long des filaments d'actine, et est impliquée dans la translocation des vésicules endocytaires depuis la périphérie après endocytose (Aschenbrenner, Lee et al.
Inhibition de l'activité de GLUT1 par l'Env HTLV
34;The complementary strand of the human T-cell leukemia virus type 1 RNA genome encodes a bZIP transcription factor that downregulates viral transcription." J Virol. SU peptide landmarks in the HTLV-1 SU homolog of the gammaretrovirus Friend murine leukemia virus (F-MLV) SU is indicated (Kimet al a, b).
GLUT1 ET LES MODELES DE PATHOGENESE
Article de revue 4
Discussion article 4
34; Definition of an amino-terminal domain of the human T-cell leukemia virus type 1 envelope surface unit that expands the fusogenic region of an ecotropic murine leukemia virus." J Biol Chem. Kim FJ, Seiliez I, Denesvre C, et al. .Definition of an amino-terminal domain of the human T-cell leukemia virus type 1 envelope surface unit that expands the fusogenic region of an ecotropic murine leukemia virus.