Ces travaux ont été réalisés au Laboratoire de Chimie Macromoléculaire (UMR-CNRS 5076) de l'Ecole Nationale Supérieure de Chimie de Montpellier, dirigé par le Professeur Bernard Boutevin. Le fluorure de vinylidène (1,1-difluoroéthylène, VDF ou VF2) est le monomère de base de tous nos (co)polymères.
Propriétés
Mais d'autres voies de synthèse du VDF ont également été réalisées : déshydrobromation du 1-bromo-1,1-difluoroéthane7, déshydrofluoration du 1,1,1-trifluoroéthane8 ou encore déchloration du 1,2-dichloro-1,1-difluoroéthane9. . Les principaux producteurs de VDF sont Arkéma (anciennement Atofina et anciennement ELF Atochem), (France), Daikin Kogyo Co., Ltd.
LE POLYFLUORURE DE VINYLIDENE
Synthèse
Les procédures décrites pour la polymérisation en suspension sont généralement très similaires à celles pour la polymérisation en émulsion. Des hydrocarbures fluorés ou chlorofluorés ont été utilisés comme solvants pour la polymérisation en solution.
Propriétés du PVDF
Le PVDF est un polymère difficile à réticuler, mais les copolymères à base de VDF (principalement poly(VDF-co-HFP)) peuvent être réticulés par les amines, les bisphénols et les rayonnements31,32. Le PVDF présente une bonne résistance à la traction, une bonne dureté, un faible fluage et une excellente résistance à l’usure28,29.
Applications
Le PVDF permet une manipulation sûre des aliments et des boissons comme les produits laitiers, les produits pharmaceutiques ou les produits médicaux comme le sang. Il est donc approuvé par l'USDA (Dpt of Agriculture) pour les produits alimentaires et laitiers, la viande et la volaille ; l'USP (pharmacopée) pour sa non-toxicité ; le NSF (Fonds National d'Assainissement) pour le contact avec l'eau potable ; la FDA (Food & Drug Administration) pour le contact alimentaire.
COPOLYMERES DU FLUORURE DE VINYLIDENE
Copolymères fluorés non fonctionnels
- VDF/CF 3 COCF 3
- VDF/H 2 C=C(CF 3 ) 2
- VDF/H 2 C=CHF
- VDF/HFC=CF-CF 3
- VDF/F 2 C=CH-CF 3
- VDF/F 2 C=CH-C 6 F 13
- VDF/F 2 C=CHF
- VDF/F 2 C=CFCF 3
- VDF/F 2 C=CF 2
La société Ausimont (aujourd'hui Solexis) commercialise un fluoroélastomère à base de poly(VDF-co-HPFP) sous la dénomination Tecnoflon SL (Tableau 2), mais la réactivité de l'HPFP vis-à-vis du VDF reste faible. Les copolymères Poly(VDF-co-HFP) possèdent de nombreuses propriétés qui dépendent de la proportion de HFP.
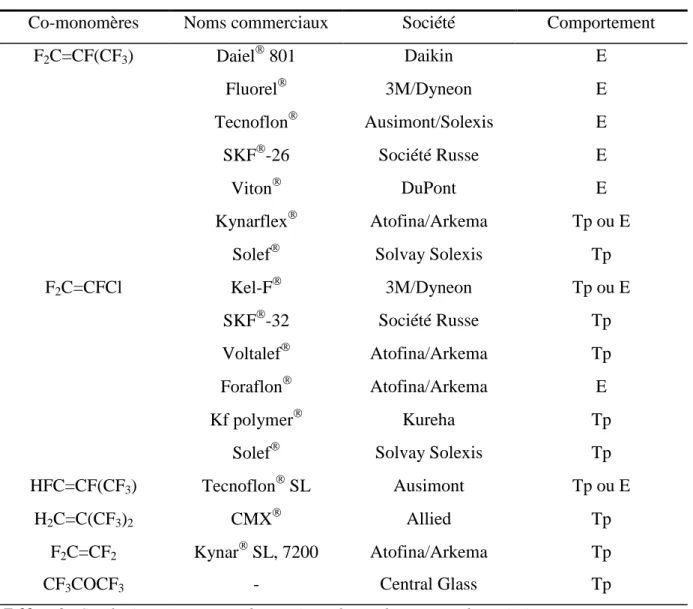
Copolymères fluorés fonctionnels
- VDF/H 2 C=CF-COOCH 3
- VDF/F 2 C=C(CF 3 )COF
- VDF/F 2 C=CF-COOCH 3
- VDF/H 2 C=C(CF 3 )-COOH
A partir des données de la littérature, on peut déterminer un degré de réactivité du macroradicalaire VDF envers différents monomères. Le tableau récapitulatif 4 permet ainsi de suggérer comme degré de réactivité du macroradical VDF : F2C=CHC6F13 < F2C=CHCF3 < HFP <.

CONCLUSION
INTRODUCTION
Il existe cinq grandes familles de batteries selon la nature de l'électrolyte utilisé (Tableau 1) : alcalines (AFC), acide polymère (PEMFC), acide phosphorique (PAFC), carbonate fondu (MCFC) et oxydes solides (SOFC)1, 2. Nous présentons ci-dessous brièvement un état de l'art sur la synthèse et l'application de monomères et copolymères clés pour obtenir des membranes entrant dans la composition de la pile à combustible (PEMFC).

MEMBRANES POLYMERES POUR PILE A COMBUSTIBLE
- Résines phénolformaldéhydes sulfonées et polystyrènes sulfonés
- Polyimides (PI) sulfonés
- Poly(aryl éther sulfones) sulfonés
- Poly(oxyde de phénylène) sulfoné
- Polymères sulfonés à base de silicate
- Poly(oxyde de phénylène) phosphoniques
- Polyphosphazènes sulfonés
- Les polymères fluorés
- Monomères fluorés aliphatiques porteurs de fonction fluorure de sulfonyle
Les performances de ces matériaux dans une pile à hydrogène à 70°C16 montrent que les membranes en polyimide sulfoné (sPI) se sont révélées trois fois plus perméables à l'hydrogène que le Nafion117. Les performances des piles à combustible de ces membranes réticulées se sont révélées médiocres car les membranes déshydratées étaient trop cassantes.
CFHSO 2 F
II SScchhéémmaa 1313 : : SSyynntthhèèssee dd’’éétthheerr vviinnyylliiqquuee flfluuoorruurree ddee ssuullffoonynyll alaliipphhaattiiqquueepperrofflluéeeee SSoollvvaayy SSoolleexxiiss7 I SScchhéémmaa 1144 :: SSyynntthhèèssee dd’’ééetthheerr vivinnyylliiqquuee ppeerrfflluuoorréé ppoorrtteeuurr ddee fflluuoorruurree ddeee supulluh rréré sseelloonn llee pprroocced AAssaahhii GGllaassss TTeecchhnnoollooggyy.
- 17 1 7 AS A SA AS SH HI I GL G LA AS SSS
- 18 1 8 AS A SA AS SH HI I CH C HE EM MI IC CA AL LSS
- I . 19 1 9 DO D OW W CH C HE EM MI IC CA ALL
- I . 20 2 0 SO S OL LV VA AY Y SO S OL LE EX XI ISS
- Monomères vinyl alkoxy perfluoré acide carboxylique
Dans la synthèse multi-étapes de ce monomère, la première étape conduit au méthyl-3-méthoxytétrafluoroéthylène avec un rendement de 74%, mais celui de la dernière est faible (de l'ordre de 8 à 15. Une synthèse alternative au vinyle obtenue) l'éther de lactone a été suggéré pour améliorer le rendement53,54.

L'ajout d'une mole de HFPO à la lactone est réalisé quantitativement et la pyrolyse du diacide fluorhydrique asymétrique conduit à l'éther vinylique perfluoré avec un rendement de 70.
- Monomères perfluorovinyléther acide phosphonique
- Membranes échangeuses de protons à base de VDF
- Membranes greffées par irradiation
- Membranes obtenues par modification chimique de poly[(VDF-alt-TFMAA)-co- HFP]
Gard et al.43 ont préparé le monomère hydrogéné avec une double liaison par éthylèneation de IC2F4OC2F4SO2F suivie d'une déshydroiodation comme suit. Schéma 27 : Membranes obtenues par greffage d'amine sulfo-aromatique sur des copolymères commerciaux poly(VDF-co-HFP).
MODELE DE COPOLYMERISATION RADICALAIRE DU PERFLUORO(4-METHYL-
3,6-DIOXAOCT-7-ENE) FLUORURE DE SULFONYLE AVEC DES ALCENES FLUORES
PLAN
INTRODUCTION
RESULTS AND DISCUSSION II.3 CONCLUSION
EXPERIMENTAL PART II.5 ACKNOLEDGEMENTS
MODELE DE COPOLYMERISATION RADICALAIRE DU PERFLUORO(4-METHYL-3,6-DIOXAOCT-7-ENE) FLUORURE DE
SULFONYLE AVEC DES ALCENES FLUORES
Le PFSVE ne s'homopolymérise pas par voie radicalaire, mais peut néanmoins être copolymérisé par voie radicalaire en solution avec le VDF, le HFP ou le CTFE. Alors que les copolymérisations avec HFP ou CTFE conduisent à des oligomères avec de faibles rendements, celles avec VDF conduisent à des copolymères poly(VDF-co-PFSVE) avec de bons rendements et pouvant contenir une large gamme d'incorporation dans le PFSVE. En revanche, les terpolymérisations radicalaires du PFSVE avec le VDF et le HFP, avec le VDF et le CTFE ou avec le VDF et le BrTFE ont conduit à des terpolymères fluorés originaux comportant des groupements fluorure de sulfonyle latéral (-SO2F).
INTRODUCTION
RESULTS AND DISCUSSION
1 Attempts to synthesize poly(HFP-co-PFSVE) copolymers
In addition, other signals are also good evidence of PFSVE units in the copolymers (Table 1). Influence of the molar percentages of PFSVE on the yield and physicochemical properties of the copolymers. However, the results showed that the presence of PFSVE in feed decreased the mass yields while the final mol.

2 Synthesis of poly(CTFE-co-PFSVE) copolymers
First of all, the good inclusion of CTFE with that of PFSVE is observed as expected due to the high prevalence of CTFE. Consequently, this poly(CTFE-co-PFSVE) copolymer is insoluble in common organic solvent (acetone, THF, acetonitrile, DMF, DMSO), as a result of the high amount and high crystallinity content of CTFE. However, regarding the yield of the reaction, this way of synthesizing the original sulfonic acid-containing polymers was not a suitable route.

3 Synthesis of poly(VDF-co-PFSVE) copolymers
As above, the radical copolymerizations of VDF with PFSVE were carried out under the same conditions as those of the synthesis of the resulting copolymers. Furthermore, the signal located at -110.4 ppm is assigned to the difluoromethylene groups of the VDF unit adjacent to a PFSVE unit. From the integrals of each characteristic signal (previously attributed) in the 19F NMR spectra, the determination of the.

This kinetics of copolymerization shows that PFSVE shows a good reactivity towards VDF and that the synthesis of PVDF bearing sulfonyl fluoride side groups in a high amount is therefore possible. In all cases, statistical terpolymers were obtained in which the different monomeric units were randomly distributed in the chain, and microblocks of oligo(VDF)s were observed in the terpolymers. In addition, all 1H NMR spectra display: i) the signals assigned to methylene groups of VDF units next to difluoromethylene groups in the 3.0-3.4 ppm range head-to-tail or.

1 Radical terpolymerization of PFSVE with VDF and HFP
2 Radical terpolymerization of PFSVE with VDF and BrTFE
Therefore, the molar percentages of each monomer unit in the terpolymers can be estimated from equation 7.

3 Radical terpolymerization of PFSVE with VDF and CTFE
Furthermore, the signals in the -127.8 to -138 ppm zone are attributed to the tertiary fluorine atom in the CTFE microblocks. Interestingly, the low intensity of the signal at ∼91 ppm indicated a negligible amount of oligo(VDF) microblock in the terpolymer.

4 Discussion
Nevertheless, a clear increase in the Tg values (close to -20 °C) is noted when using CTFE. The major difference between poly(VDF-ter-HFP-ter-PFSVE) and poly(VDF-ter-CTFE-ter-PFSVE) terpolymers is the role of the termonomer. Surprisingly, the consumption of VDF during the reaction was low (a drop of only 1 bar pressure was noted) in contrast to that obtained by the classical copolymerization of VDF with PFSVE.

CONCLUSION
The compositions of the co- and terpolymers (the molar contents of VDF, HFP, CTFE and PFSVE) were determined by 19F NMR spectroscopy. A vacuum of 2 mm Hg was then applied for 15 minutes and the initiator (usually 2,5-Bis(tert-butylperoxy)-2,5-dimethylhexane, DHBP, tech. 90%; or tert-butylperoxypivalate), PFSVE and 1,1 1,3,3-pentafluorobutane were introduced through a funnel closely connected to the introduction valve. After the reaction, the autoclave was cooled to room temperature and then placed in an ice bath.
L'autoclave a été laissé fermé pendant 20 min et purgé avec une pression d'azote de 30 bars pour éviter toute fuite, puis dégazé. L'introduction de HFP dans ces copolymères permet une augmentation du rendement de copolymérisation et l'incorporation de PFSVE au sein de ces matériaux. Ainsi, nous avons étudié la copolymérisation radicalaire du PFSVE avec le CTFE pour améliorer les propriétés mécaniques et l'insolubilité dans le méthanol.
UTILISATION DE LA POLYMERISATION RADICALAIRE CONTROLEE (PRC) POUR LA
HFP) A BLOCS
INTRODUCTION ET OBJECTIFS
LA POLYMERISATION RADICALAIRE CONTROLEE PAR TRANSFERT A L’IODE (ITP)
CONCLUSION
La polymérisation radicalaire contrôlée (CRP) est l'un des meilleurs outils actuels pour allier la flexibilité du procédé radicalaire et les avantages des systèmes dits « vivants ». Ainsi, plusieurs systèmes ont été conçus basés sur la cinétique de la polymérisation radicalaire conventionnelle. Comme le suggère Otsu1,2, l'un des pionniers du PRC, cet équilibre doit être largement en faveur des espèces dormantes pour aboutir à un système vivant.
Synthèse d’un copolymère poly(VDF-co-HFP) par polymérisation sans ATR
Bien entendu, ce calcul n’est qu’une estimation et dépend de la résolution du spectre RMN 1H et de l’intégration du signal. HFP * M HFP + Les déterminations de DPn(VDF) et Mn sont effectuées par RMN 1H dans le cas de l'utilisation de xanthate hydrogéné avec les ratios suivants. La figure 16 présente une superposition du spectre RMN 1H du copolymère poly(VDF-co-HFP) (Exp. 1) obtenu par MADIX avec celui du xanthate hydrogéné.
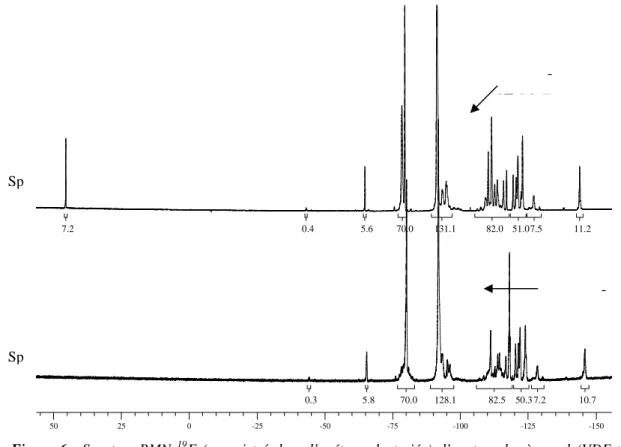
![Figure 14 : Spectre RMN du 19 F d’un copolymère poly(VDF-co-HFP) enregistré dans l’acétone d 6 ([TAPPI] 0 /([VDF] 0 +[HFP] 0 ) = 0,0025 ; composition initiale 70,0/30,0)](https://thumb-eu.123doks.com/thumbv2/1bibliocom/465477.70667/132.892.121.823.100.594/figure-spectre-copolymère-enregistré-acétone-tappi-composition-initiale.webp)
CONCLUSION
Perfluorinated membranes, In: Vielstich W, Hubert A, Gasteiger M, Lamm A, (eds); Handbook of Fuel Cells - Fundamentals, Technology and Applications; Fuel Cell Technology and Applications, New York, Wiley.
UTILISATION D’UN ‘CURE SITE MONOMER’ (CSM) PORTEUR D’UNE
SYNTHESE DE COPOLYMERES POUR MEMBRANE DE PAC
INTRODUCTION
MODELE DE COPOLYMERISATION DU BDFO AVEC LE VDF
CONCLUSION
UTILISATION D’UN COMONOMERE PORTEUR D’UNE FONCTION -CF 2 -BR RETICULABLE
- TERPOLYMERISATION DU BDFO AVEC LE VDF ET LE PERFLUORO(4-METHYL-3,6-DIOXAOCT-7-ENE) FLUORURE DE
- SYNTHESE ET CARACTERISATION DE TERPOLYMERES POLY(VDF-TER- PFSVE-TER-BDFO)
Des terpolymérisations radicalaires du VDF avec le PFSVE et le BDFO ont été réalisées en solution dans le 1,1,1,3,3-pentafluorobutane. Ce transfert, également observé lors de la copolymérisation du VDF et du BDFO24, était compris entre 3 et 8. Les résultats obtenus (Tableau 4) montrent tout d'abord que l'inclusion du BDFO dans la copolymérisation du VDF avec le PFSVE n'affecte pas la réactivité de ces deux comonomères. .
![Figure 4 : Spectre RMN du 19 F d’un terpolymère poly(VDF-ter-PFSVE-ter-BDFO) enregistré dans l’acétone d 6 (([DHBP] 0 /([VDF] 0 +[PFSVE] 0 +[BDFO] 0 ) = 0,01 ; composition initiale 76,8/18,1/5,1 ; composition finale 77,3/19,5/3,2)](https://thumb-eu.123doks.com/thumbv2/1bibliocom/465477.70667/158.892.147.856.101.505/figure-spectre-terpolymère-enregistré-acétone-composition-initiale-composition.webp)
CHCH2CF2
- Hydrolyse des terpolymères des fonctions -SO 2 F des poly(VDF-ter- PFSVE-ter-BDFO)
- RETICULATION DES TERPOLYMERES POLY(VDF-TER-PFSVE-TER-BDFO) HYDROLYSES
- Propriétés des membranes
- Synthesis of CH 2 =CH-C 6 F 12 -Br (BDFO) as a cure site monomer (C.S.M.)
- Radical terpolymerization of VDF, BDFO and hexafluoropropene (HFP)
Interestingly, at an initial mole ratio of BDFO in the feed higher than 10% (runs 4, 5 and 7), the yield and properties of the copolymers decrease dramatically, even in the presence of HFP. The thermal stability of the poly(VDF-ter-BDFO-ter-HFP) terpolymer is similar to that of the copolymer (for the same molecular weight), as decomposition occurred at approximately 335 °C (experiments 3 and 6). Crosslinking was monitored by the insolubility of the cured poly(VDF-co-BDFO) copolymer in acetone.