Doktori értekezés
Konz Viktória
Témavezet®k:
Dr. Kály-Kullai Kristóf, egyetemi adjunktus
Dr. Nosztizius Zoltán, professor emeritus
Budapesti M¶szaki és Gazdaságtudományi Egyetem
Fizika Tanszék
Kémiai Fizika Csoport
Köszönetnyilvánítás 4
Bevezetés 6
1. Irodalmi áttekintés 8
1.1. Sav-bázis diódák . . . 8
1.1.1. Nyitóirány . . . 8
1.1.2. Záróirány . . . 9
1.1.3. Fixált töltések hatása karakterisztikára . . . 10
1.2. Sószennyezés hatása adiódára . . . 11
1.2.1. Pozitívsóhatás . . . 11
1.2.2. Negatív sóhatás . . . 12
1.3. Konentráió- és poteniálproloka diódában . . . 13
1.3.1. Pozitívsóhatás . . . 13
1.3.2. Negatív sóhatás . . . 15
1.4. Összeköt®elem adiódában . . . 15
1.4.1. PVA gélhenger . . . 16
1.4.2. PVB membrán . . . 17
1.5. Gyengesav gyenge bázis diódák . . . 20
1.6. Sav-bázis tranzisztorok . . . 20
1.7. A diódamatematikaimodellje . . . 20
1.7.1. A diódát leíró pariális diereniálegyenlet-rendszer . . 20
1.7.2. Membránegyensúly . . . 23
1.8. Adaptív FEM . . . 24
1.9. Sav-bázis diódák modellezése történeti összefoglalás . . . 26
2. Adaptív hálógenerálási algoritmus 28 2.1. Modellépítés a COMSOL Multiphysis segítségével . . . 28
2.2. A rásfüggvény . . . 30
2.3. A diódareakiózónája . . . 32
2.4. Validáió. . . 36
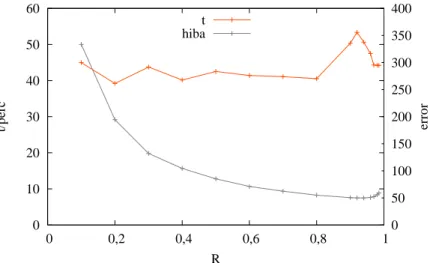
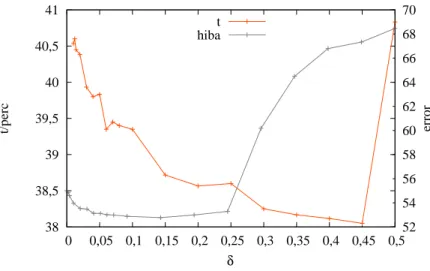
2.5. A rásfüggvény paraméterterének bejárása a közelítés hibája és afutási id®szempontjából. . . 40
2.5.1. Fix rás ésadaptív háló összehasonlítása . . . 41
2.5.2. A rásfüggvény paramétereinek ahatása . . . 42
2.5.3. A rásfüggvény paramétereinek folyamatosváltoztatása 44 2.6. Összegzés, kitekintés . . . 45
3.1. Id®függ® sóhatások . . . 48
3.1.1. Pozitívsóhatás . . . 48
3.1.2. Negatív sóhatás . . . 54
3.2. Impulzus-zavarás . . . 55
3.3. Feszültségmódosítása határon . . . 62
3.3.1. A polaritásváltáshatása a PVA hidrogélalapú diódára 63 3.3.2. Az átkapsolás idejének hatása a diódaválaszára . . . 63
3.3.3. H
+
ésOH−
diúziós állandójának sökkentése . . . 653.4. Összegzés, kitekintés . . . 67
4. Gyenge sav gyenge bázis diódák 71 4.1. Sóhatások a gyenge sav gyenge bázis diódákban - összeha- sonlítás azer®s sav er®s bázis diódákkal . . . 72
4.1.1. Pozitívsóhatás . . . 72
4.1.2. Negatív sóhatás . . . 77
4.2. Negatívsóhatás K
+
ionokkal . . . 784.3. A lúgoldalszennyezése Cl
−
ionokkal . . . 794.3.1. Hatás apozitív sóhatásra . . . 79
4.3.2. Hatás anegatív sóhatásra . . . 80
4.4. Összegzés, kitekintés . . . 84
5. Összefoglalás 86 5.1. Tézispontok . . . 87
5.2. A tézispontokhoz kapsolódópublikáiók . . . 89
Ábrák jegyzéke 90 Táblázatok jegyzéke 93 A. Modellezésben felhasznált állandók 94 B. Végeselem-módszer 95 C. Adaptív hálógenerálási algoritmus - kiegészítés 97 C.1. Szimuláióskörnyezet . . . 97
C.2. Az alkalmazottrásfüggvény . . . 97
C.3. A rásfüggvény - mesh s¶r¶ségfüggvény kapsolata . . . 103
C.4. Azegyeslépésekfutásiidejeazadaptívhálógenerálásialgorit- mus alkalmazásaesetén . . . 104
C.5. ACOMSOLnemlineáris algoritmusánakkonvergenia kritéri-
C.7. Az egyes diszkretizáiós sémák konvergenia rátája . . . 106
C.8. Mesh trajektóriák . . . 108
C.9. Munkám során az elkészült, és implementáltadaptív hálók a sav-bázis diódához . . . 110
D. Id®függ® modellezés - kiegészítés 115 D.1. Fixált töltés reakiótagjánakelhanyagolása . . . 115
D.2. Poteniálprol azátütés utáni er®s sav er®s bázis diódában . 124 E. Gyenge sav gyenge bázis diódák kiegészítés 125 E.1. Sószennyezés nélküli diódaprolja . . . 125
E.2. Feszültség hatása a pozitívsóhatásra . . . 126
E.3. Gyenge sav gyenge bázis diódamodellezése a COMSOL se- gítségével . . . 127
E.3.1. Megoldási módszer . . . 127
E.3.2. A COMSOL 3.5numerikus beállításai . . . 128
E.4. Prolok lúgoldaliKClszennyezésnél . . . 128
E.5. Konentráió-éspoteniálprolokadiódábannegatívsóhatás esetén lúgoldaliCl
−
iontartalmúsóval . . . 131F. A sav-bázis diódák témában végzett kutatásaim története 134
G. Forráskódok 136
Hivatkozások 137
"A tudós feladata a keresés,
szüntelen kutatás. Éshatalált
valamit, hafelért egy súsra,
akkor látja sak, milyennagy
terület nyúlik el®tte, amely még
teljesenismeretlen,feltárásra,
kutatásra vár. Szóval, haa
keresés sikerrel jár, akkor egyre
több és több keresnivalót talál.
Nem tudom,végére ér-e ennek
valaha azemberi tudomány, más
szóval, lesz-e valaha id®,amikor
mindent tudnifogunk, amit
tudniérdemes. (...) Mindinkább
az a meggy®z®désem, hogy az
ember sohasemjut majd a
tudomány végére, s®t
ellenkez®leg, minél többet
tudunk,annál kevesebbet
ismerünk ahhoz képest, amit
ismerni szeretnénk." Pheidiasz
Ezútonis szeretnék köszönetet mondani:
Témavezet®mnek, Dr. Kály-KullaiKristófnak, a jó hangulatért, a sok
nevetésért, melyetegész munkámsorán biztosított. KöszönömKristóf,
hogykell®enrugalmasan,ésmegért®en kezeltedakutatásraszántid®t.
Témavezet®mnek, Dr. Nosztizius Zoltánnak útmutató tanásaiért az
egész kutatómunkámsorán. Zolinak köszönöm még egyszer a magával
ragadó Elektrodinamikael®adásokat,melyekért mindigmegérte felkel-
ni.
Dr. Roszol Lainak, akinek a témavezetésével még TDK hallgatóként
elkezdtemsav-bázisdiódákkalfoglalkozni.Mégegyszer köszönömasok
tanítástéstürelmet,mellyelmegismertettélaszámítógépesmodellezés-
sel ésa FEM alapjaival.
Dr. Izsák Ferennek, az ELTE MatematikaiIntézet munkatársának, a
vezet®jének, akit®l megtanultam más szemmel is tekinteni a problé-
mákra, ésaki ráébresztettarra, hogymégnem tanultammeg bánni az
id®vel.
SomlayGergelynek,aGamaxKft.korábbimunkatársának,aCOMSOL
Supporttal való levelezésben, és hibabejelentésekben nyújtott segítsé-
gért.
KegyePéternek,akiméga"Tervezés" feladatátkészítette nálam2016-
ban akövetkez® ímmel:Sav-bázisdiódákimpulzuszavarásraadottvá-
laszának modellezése.
A KémiaiFizikaCsoportösszes munkatársánakmindenkoritámogatá-
sukért.
A MeVuKo Kft-neka szükség szerinti plusz számításikapaitás bizto-
sításáért.
Szüleimnek, hogy mindig lelket öntöttek belém, amikor már feladtam
volna, ésÖsémnek, Marinak,aki pedig mindig segítettszámítógépe-
ket szerelni.
"A tudomány izgalmas kaland.
Ajtókat nyitogatunk, keressük az
igazságot, s egyszerre ott van
el®ttünk, mintmesebelikins, a
maga kézzelfogható, tündökl®
valóságában." Kosztolányi
Dezs®
PhD dolgozatomban sav-bázis diódákkal,a nemlineáris kémiai dinamika
területéhez tartozó reakió-diúzió rendszerekkel foglalkozom. A sav-bázis
diódaa Budapesti M¶szaki ésGazdaságtudományiEgyetem Fizika Tanszék
Kémiai Fizika Csoportjának nagy hagyományokkal bíró kutatási területe,
melyetprof.NosztiziusZoltánötleteialapjánmégaz1970-esévekben kezd-
tek elvizsgálni.Ezen kutatásbamég BS-sTDK hallgatókéntkapsolódtam
be.Jelendolgozatbansakapublikáiókbanismegjelenteredményeketkívá-
nom összefoglalni, melyekbe természetesen korábbi eredményeim is be van-
nak építve. A teljes kutatómunkámról egy kronologikus összefoglaló az F.
függelékben található.
A sav-bázis diódaegy olyanreakió-diúziórendszer, melyben egy savas
és egylúgos oldatteret vékony gélvagy membrán köt össze, melymegakadá-
lyozza afolyadék áramlását,de megengedia különböz®oldatbelikomponen-
sek diúzióját és reakióját. A diódára feszültséget kapsolvaazt tapasztal-
juk, hogya diódán átfolyóáram nagysága, hasonlóana félvezet®diódákhoz,
függ a feszültségpolaritásától innen asav-bázis diódaelnevezés.
A záróirányba kapsolt diódán átfolyó áram az oldatterekbe juttatott
sószennyezésekre igen érzékenyen reagál, érdekes módon az áram nemsak
n®het, hanem sökkenhet is (pozitívésnegatív sóhatás).
Apozitívésnegatívsóhatás er®sennemlineárisjelenségét er®s sav er®s
bázis diódában staionárius állapotra korábban már sikerült számítógépes
szimuláiókkalrészletesen modellezni, valamintkísérletilegis alaposan meg-
vizsgálni. Ez alapján felmerült,hogy a sav-bázis diódából anegatív sóhatás
elvén m¶köd® iondetektort lehetne fejleszteni, mellyel savas közegben katio-
nokat lehetne kvantitatíve meghatározni [1℄. A kationok elválasztását a de-
tektálás el®tt pl. kapilláriselektroforézissel lehetne biztosítani.
Asav-bázis diódákkutatásánakbiológiaivonatkozása isvan.Azél®szer-
vezetben található membránokban gyakori,hogy pH gradiens és elektromos
er®tér együttesen hat a membránon átdiundálóionokra, így ezen biológiai
A dolgozatomban akövetkez®kr®l lesz szó:
El®szörasav-bázis diódákatmutatombe,melyetegyrövidösszefoglaló
követ azadaptív hálógenerálásialgoritmusokról.
Ezutána diódaid®függ®modellezéséhezkészültempirikusadaptív há-
lógenerálási algoritmusomatmutatom be, és egy példaszimuláión en-
nek teljesítményétvizsgálom.
Majd a diódasószennyezésével kapsolatosjelenségek id®belilefutását
tanulmányozom, valamintkülönböz® hipotetikus összeköt®elemekkela
diódafeszültségátkapsolásra adott válaszát.
Végül gyenge sav gyenge bázis diódák staionárius modellezésével
kapsolatoseredményeimet ismertetem.
"Ha egy új elmélet nem egy
gyermekek számára isjól
érthet®, konkrét képb®l indul ki,
akkor valószín¶leg semmitsem
ér." Albert Einstein
1.1. Sav-bázis diódák
Egy er®s sav er®s bázis dióda elvi elrendezése az1. ábrán látható: egysa-
vasésegylúgos oldatteret egygél(vagyegy membrán)kötössze, ill.választ
szét.Azösszeköt®elem(melylényegébenegyoldattérnektekinthet®,hidrogél
esetén vizes oldatnak) feladata, hogy megakadályozza a folyadék áramlását
és keveredését, de lehet®vé tegye a különböz® oldatbeli komponensek dif-
fúzióját és reakióját. Az oldatterekbe munkaelektródok merülnek, melyek
segítségével poteniálkülönbséget hozhatunk létre a két oldattér között. A
rendszeren mérhet® áramer®sség a feszültségt®l és az oldatterekben lév® io-
nok konentráiójától függ. A félvezet® diódákhoz hasonlóan, jelen esetben
is függ a mért áram nagysága attól, hogy a feszültséget milyen polaritással
kapsoljukrá arendszerre - innen azelektrolit diódaelnevezés [2,3℄. Ennek
mintájára megkülönböztethetünk nyitó- és záróirányt a sav-bázis diódában
(2.és3.ábra).A kés®bbiekben a diódajelenségeitbemutató szimulált ábrák
az1.7.fejezetbenbemutatottmodellelésaz5.táblázatbanszerepl®állandók-
kalkészültek, a pontos szimuláiós beállításokataz ábraaláírás tartalmazza,
ill.haegyfejezethez,alfejezethezugyanazok aparaméterektartoznak, akkor
az adott fejezet, alfejezet elején szerepelnek.
1.1.1. Nyitóirány
Ha a lúgoldalba (pl. KOH) merül® munkaelektródra pozitívabb (+), a sav-
ba (pl. HCl) merül®re pedig negatívabb (-) poteniált kapsolunk, akkor a
következ® folyamatok játszódnak le: a KOH disszoiáiója során keletkez®
K
+
ionoka a savoldal fele (-), az OH
−
ionoka bázisba merül®elektród (+)
felé vándorolnak. A savoldalon aHCldisszoiáiójábólképz®d®H
+
ionok 1
a
savoldali elektródfelé(-), aCl
−
ionokpedigalúgoldalfelé(+) vándorolnak.
1
H
+
ion (proton) az oldatban természetesen nins jelen. Az oldatban protonált víz
asszoiátumoktalálhatók,melyeketazegyszer¶bbkezelhet®ségérdekébenatovábbiakban
+
OH -
V
A - +
H + K +
Cl -
φ = 0 φ = φ = -U > 0
L
1.ábra. Er®ssaver®sbázisdiódasematikusrajza(HClKOH).Akétoldatteret
egy gél vagy egy membrán köti össze. Az oldatterekben az ionok konentráiója
állandó, mely az oldatok folyamatos seréjével érhet® el (ezt az ábrán a nyilak
jelölik).Haasavasoldattérneknagyobbapoteniálja(apoteniáltakés®bbiekben
ϕ
-vel jelölöm),minta lúgosnak, akkor adióda záróirányú.Ígyagélbenlényegébentiszta,jólvezet®KCloldatlesz,ezértazáramer®sség
lineáris függvénye arendszerre adott feszültségnek (2.ábra, ha
U > 0
).Nyitóirányban azáramer®sség a következ® összefüggéssel közelíthet® [2℄:
I = F (D
K+ + D
Cl− )c 0
F RT U A
L ,
(1)ahol
F
a Faraday állandó,R
az egyetemes gázállandó,T
a h®mérséklet,D
K+
a káliumionok,D
Cl−
a kloridionok diúziós állandója,c 0
a sav és alúg konentráiója a tartályokban,
U
a feszültség a tartályok között,A
azösszeköt®elem keresztmetszete,
L
pedig a hossza.1.1.2. Záróirány
Amikorabázisbamerül®elektródanegatívabb (-)ésasavbamerül®apozi-
tívabb (+) poteniálú, akkormindenfordítvatörténik. Azelektromoser®tér
hatásáraalúgoldalrólaOH
−
,asavoldalrólaH
+
ionokfognakagélirányába
vándorolni.Ekkorastaionáriusállapotbanlév®géltháromrészreoszthatjuk
fel [5℄: egy lúgoldali részre, egy középs® vizes zónára (záróréteg) és egy sav-
oldali részre. Ilyenkor a zárórétegben a H
+
és OH
−
ionok rekombinálódnak
vízzé. Természetesen nagyon kis mennyiségben, a víz ionszorzatábólszámít-
+ −
-1 -0.5 0 0.5 1 1.5 2
-20 -18 -16 -14 -12 -10 -8 -6 -4 -2 0 2
i/(mA/mm 2 )
U/V
PSfrag replaements
gyenge
er®s
2. ábra. Er®s (HCl KOH) és gyenge sav bázis dióda (CH
3
COOH NH4
Cl)szimulált feszültség-áramer®sség karakterisztikája, [KOH℄ = [HCl℄ = [NH
4
OH℄ =[CH
3
COOH℄ = 0,1 M. A nyitóirányt pozitív, a záróirányt negatív feszültségérté- keknéltüntettem fel.átfolyó áram abszolút értéke lényegesen kisebb, mint a nyitóirány esetében
(2. ábra, ha
U < 0
).A záróirányú áramer®sségre akövetkez® közelítésvezethet® le [2℄:
|I| = F (D
H+ + D
OH− )(2c 0 + p K
vF
RT |U |) A
L ,
(2)ahol
D
H+
a hidrogénionok,D
OH−
pedig a hidroxilionok diúziós állandója,K
v pedig avízionszorzat.Történeti okokból az értekezésben a továbbiakban a záróirányt pozitív,
míga nyitóirányt negatív feszültségértékeknél tüntetem fel.
1.1.3. Fixált töltések hatása karakterisztikára
Általában a polimergéleka polimerlánhoz rögzült ionos soportokat is tar-
talmaznak, melyek a közegt®l függ®en disszoiálhatnak, és x, nem mobilis
töltéseket eredményeznek. A gél azon zónáiban, ahol xált ionok vannak, a
mobil ellenionok konentráiója nem lehet kisebb, mint a xált ionoké. A
xálttöltések tehát(bár önmaguknem vezetnek)befolyásoljákagélvezet®-
képességét. Nyitóiránybanezeknekatöltéseknekakonentráiója lényegesen
3. ábra. Er®s (HCl KOH) és gyenge sav bázis dióda (CH
3
COOH NH4
OH)mért feszültség-áramer®sség karakterisztikája, [KOH℄ = [HCl℄ = [NH
4
OH℄ =[CH
3
COOH℄=0,1M. Forrás: [4℄.Azonban záróirányban anagy ellenállású zónában a xált töltések konent-
ráiója összemérhet® amobil ionokkonentráiójával,amimegnöveliazáró-
irányúkarakterisztikameredekségét[6℄. Ekkor azáróirányúkarakterisztikaa
következ® összefüggéssel közelíthet® [7℄:
|I| = F (2(D
H+ + D
OH− )c 0 + D
H+ · c
FA− · F
RT ·|U|) A
L ,
(3)ahol
c
FA−
a xált anionok konentráiója. Ez alapján a záróirányú karak- terisztika a gélben található xált töltések konentráiójának a számításá-ra is használható [8℄. A továbbiakban xált negatív töltéseket tételezek fel,
ugyanis akísérleteknagyrészébenalkalmazottpoli(vinil-alkohol)(PVA)gél-
ben a karboxil soportok disszoiáiójával xált anionok keletkeznek, ezért
a záróréteg gyengén savas. A xált töltések teljes konentráiója a gélben a
záróirányú karakterisztika alapján
c
x= 4 · 10 − 3
M.1.2. Sószennyezés hatása a diódára
1.2.1. Pozitív sóhatás
Sóhatásnak azt a jelenséget nevezzük, amikor a záróirányú sav-bázis dióda
sav- vagy lúgoldalához sószennyezést adagolunk (a sav- és lúgkonentráió
konstans
c 0
, általában0, 1
M töménység¶ oldatot használunk mindkét ol-dalon). Er®s sav er®s bázis diódát az eddigi vizsgálatok során KCl-dal
tegbeilyenkoraszennyez®sóanionjaill.kationjajut,azer®s saver®sbázis
diódánál ez például K
+
és Cl
−
ionokat jelent. Cl
−
ionokakkor kerülnek be,
ha a lúgoldalt szennyezzük, K
+
ionok pedig akkor, amikor a sószennyezés a
savoldalon történik.
Haaszennyez® sóta lúgoldalhozadagoljuk,akkorazárambaner®s nem-
lineárishatástgyelhetünkmeg[9,7,10℄.Kissószennyezéshatásáraazáram
aligváltozik (kisitperszen®), de egykritikus sókonentráió (ez akonent-
ráió-áramer®sséggörbeinexióspontja)közelébenazárammeredekenn®ni
kezd(4/a.ábra).Végüladiódaátüt(azárórétegelt¶nik),vagyisakárakkora
áram isátfolyhatadiódán,mintnyitóirányban.Az áramraa sómennyiségé-
nek ezután már nem ilyen jelent®s a hatása.
Asavoldalisószennyezésszinténnemlineárishatásteredményez:növelvea
szennyez® sókonentráiójátegykritikusértéknélazáramer®sségittisjelen-
t®sen megn®. Azonban az átütéshez nagyobb sókonentráióra van szükség,
mint lúgoldalon[11℄.
0 5 10 15 20 25 30
0 20 40 60 80 i/(mA/mm 2 )
[KCl] L /mM (a)
0 5 10 15 20 25 30
0 10 20 30
i/(mA/mm 2 )
[KCl] S /mM (b)
PSfrag replaements
Pozitívsóhatás Negatívsóhatás
4. ábra. Pozitív (a) és negatív (b) sóhatás az er®s sav er®s bázis diódában.
[KCl℄
L
a lúgoldali, míg [KCl℄
S
a savoldali szennyez® sókonentráióját jelöli. Ne-
gatív sóhatás esetén [KCl℄
L
= 60
mM, melyet a naranssárga pötty jelöl az (a) ábrán,∆ϕ = 10
V.A (b)ábrán [KCl℄S= 0
mM-nál az áramer®sségmegegyezika naranssárga pöttyeljelölttel az(a) ábrán.1.2.2. Negatív sóhatás
Aztazesetetsokáignemvizsgálták,hogymitörténikakkor,haadiódamind-
két oldatterét szennyezik, valószín¶leg úgy gondolták, hogy a még több jól
vezet® sóhatásárasakmég nagyobb áramokfolynak majd átadiódán. Ez-
zelszemben, ha alúgoldalisókonentráiótállandóértéken tartjuk,ésemel-
[KCl℄
AL
a lúgoldali, míg [KCl℄
AC
a savoldali szennyez® só konentráióját jelöli.
Negatív sóhatásesetén [KCl℄
AL
= 35
mM,∆ϕ = 10
V.Forrás:[12℄.tapasztaljuk, hogy az áramer®sség a savoldali sókonentráió függvényében
folyamatosansökken (adiódavisszazár).Ekkorismétmegjelenikagélbena
záróréteg (4/b.ábra).Eztajelenségetnegatívsóhatásnak nevezzük [12℄.To-
vább növelvea sókonentráióta diódán átfolyó áram meredeken n®ni kezd,
hasonlóan, mint saksavoldali sószennyezés esetén.
1.3. Konentráió- és poteniálprolok a diódában
1.3.1. Pozitív sóhatás
A 6/a. ábra mutatja a sószennyezés nélküli er®s sav er®s bázis diódában
lév®konentráió-és poteniálprolokat.(A gél"0mm"-néllév®széle alúg-
oldallal, "1 mm"-nél lév® széle a savoldallal érintkezik.) Az ábra alapján a
diódábanjólmegkülönböztethetünkháromrészt:egylúgos(bázikusoldattér
melletti) és egy savas zónát (a savas oldattér mellettit), valamint köztük a
záróréteget.A diódán átfolyóáram er®sségét alapvet®en azárórétegben lév®
ionokkonentráiójahatározzameg.Apoteniálprolonmeggyelhet®,hogy
adiódárakapsolt feszültségnagyrészeezen aközéps®zónánesik,tehát en-
nek a résznek az ellenállása a legnagyobb. Ez a középs® réteg enyhén savas
karakter¶, ezt bizonyítja a xált töltés (amely gyenge sav disszoiáiójából
keletkezik)konentráióproljais.Aközéps®zárórétegnekésalúgoszónának
a határát - mivel a diódára jellemz® sav-bázis reakió itt zajlik - reakiózó-
nának nevezzük.Akés®bbiekbenennek areakiózónának kiemelked®szerepe
lesz adióda id®függ®modellezésében.
0 25 50 75 100
0 0,2 0,4 0,6 0,8 1
[OH - ]/mM (a)
[H + ] [OH - ]
0 25 50 75 100
0 0,2 0,4 0,6 0,8 1
[K + ]/mM
[K + ] [Cl - ]
0 1 2 3 4
0 0,2 0,4 0,6 0,8 1
0 2,5 5 7,5 10
[FA - ]/mM
x/mm [FA - ]
ϕ
0 25 50 75 100
0 0,2 0,4 0,6 0,8 1
(b)
[H + ] [OH - ]
0 25 50 75 100 125 150
0 0,2 0,4 0,6 0,8 1
[K + ] [Cl - ]
0 1 2 3 4
0 0,2 0,4 0,6 0,8 1
0 2,5 5 7,5 10
x/mm [FA - ] ϕ
0 25 50 75 100
0 0,2 0,4 0,6 0,8 1
(c)
[H + ] [OH - ]
0 50 100 150
0 0,2 0,4 0,6 0,8 1
[K + ] [Cl - ]
0 1 2 3 4
0 0,2 0,4 0,6 0,8 1
0 2,5 5 7,5 10
x/mm [FA - ]
ϕ
0 25 50 75 100
0 0,2 0,4 0,6 0,8 1
[H + ]/mM (d)
[H + ] [OH - ]
0 50 100 150
0 0,2 0,4 0,6 0,8 1
[Cl - ]/mM [K + ]
[Cl - ]
0 1 2 3 4
0 0,2 0,4 0,6 0,8 1
0 2,5 5 7,5 10
ϕ /V
x/mm [FA - ]
ϕ
6.ábra. Staionáriuskonentráió-éspoteniálprolokazer®ssaver®sbázisdiódában,
∆ϕ = 10
V.(a)Sószennyezésnélkül.(b) Pozitív sóhatás.
[
KCl] = 50
mM. ()Pozitív sóhatásátütés után.[
KCl] = 60
mM. (d) Negatív sóhatás.[
KCl] = 60
14
kiterjedése sökken, továbbá a záróréteg helyzete is változik a gélben. (Kis
lúgoldali sószennyezés esetén a diódára jellemz® prolokat a 6/b. ábra mu-
tatja.) Alúgoldalisószennyezés hatásáraadiódasavoldalárólegyre többH
+
ion jut be a gélbe, melya gél elsavasodását okozza. A sószennyezést növelé-
sével a diódareakiózónája egyre közelebbkerül a lúgoldalhoz,a lúgos zóna
kiterjedése is egyre sökken.
Amennyiben még tovább növeljük a lúgoldali sókonentráiót, akkor a
záróréteg egy kritikus sókonentráiót elérve elt¶nik. A középs® zóna folya-
matos elt¶nése következtében sökken ennek arésznek az ellenállásais, ami
a diódán átfolyó áram növekedését eredményezi (a dióda átüt). Az átütés
utáni konentráióprolokat a6/. ábra mutatja,melyen jól látható,hogya
vezetésért a H
+
ionok megnövekedett konentráiója a felel®s. Az er®s sav
er®s bázis dióda annyira elsavasodik, hogy a lúgos zóna teljesen elvéko-
nyodik,továbbáasószennyezésb®lszármazó anionnak(Cl
−
ionnak)agélbeli
konentráiója is jelent®sen megn®.
1.3.2. Negatív sóhatás
Ha er®s sav er®s bázis diódában a savoldalt is sóval szennyezzük (állandó
lúgoldali sókonentráió mellett, általában a kritikus konentráió közelé-
ben), akkor a diódán átfolyó áram er®ssége sökkenni fog (negatív sóhatás),
mígnemadiódavisszazár.Er®s saver®s bázisdiódavisszazárásutánikon-
entráióproljáta6/d.ábramutatja.Avisszazárásutániprolokigazolják,
hogy kétoldalisószennyezés hatásáraa gélben ismét megjelenik a záróréteg,
emiatt a feszültség nagy része ismét ezen a középs® zónán esik. Az ellen-
oldalisószennyezés hatásáraasavoldalróltöbb,asóbólszármazó kation(K
+
ion) kerül be a zárórétegbe, mint sószennyezés nélkül. Er®s sav er®s bázis
dióda esetében valószín¶leg ez a többlet zárórétegbeli ionkonentráió okoz-
za, hogyellen-oldali sószennyezés hatásáraaz áram nem tud a sószennyezés
nélküli értékig visszasökkenni.
1.4. Összeköt®elem a diódában
A diódasav- éslúgoldalátösszeköt® elemr®l,vagyisazösszeköt®elemr®l, ed-
dig nem sok szót ejtettem, a modellszerint ennek egy polarizálható gélnek,
vagymembránnakkelllennie.Szerepeaz,hogyazadvekiótmegakadályozza.
A diódával kapsolatos kísérletek során eddig egy poli-vinil alkohol (PVA)
alapú gélhengert használtunk. Alapvet®en ennek a paramétereit (hossz, -
lyek mindegyikeezen PVA gélhengert jelenti.Ha nem, akkor azt külön jelö-
löm. Emellett készítettünk egy poli-vinilbutiral (PVB) alapú membránt is,
melyr®l a kísérletek azt mutatták, hogyez a membrána diódaösszeköt®ele-
meként használható [13℄. Az ideális összeköt®elem megtalálása továbbra is
él. Jelenlegúgy gondoljuk, hogyaz ideális összeköt®elemet a szilikonalapú
membránok között kell keresni.
Egy ún. ideálisösszeköt®elem tulajdonságaia következ®k:
igen jó ionvezet®nek kell lennie;
ugyanakkor az elektromos ellenállása elég nagy kell, hogy legyen az
oldatterekéhez képest, hogy a diódára kapsolt feszültség nagy része
ezen essen;
elég rövid kell, hogylegyen (
L
kisi), hogyaz id®állandó megfelel® le-gyen;
kémiailagellenálló asavvalés lúggal szemben;
tulajdonságaiid®benállandóak,feszültségrákapsolásánakhatásárais
megtartja azokat.
1.4.1. PVA gélhenger
Amérésekhez használthengeralakúgélpoli(vinil-alkohol)-ból(PVA)készül,
mely glutárdialdehiddel (GDA) van térhálósítva. A polimerlánok közötti
keresztkötések kialakítására a két vagy több funkiós soportot tartalma-
zó molekulák képesek, esetünkben aglutárdialdehid,amelyaetálkötést tud
kialakítani a PVA OH soportjával. A gél annál er®sebb, mehanikailag el-
lenállóbb,minélnagyobbbenneakeresztkötések száma.Adiódáhozhasznált
gélben aGDA mennyiségét úgyválasztjuk meg,hogyagélmeg tudjonkötni
és a mérési élnak megfelel®en er®s legyen, de ne legyen túl kemény, mert a
sok keresztkötés miatt azionokmozgékonysága sökkenne agélben.
A PVA gélnek azonban több hátránya is van. Egyik, hogy érzékenyen
reagál a savra. A sav a már kész gélben katalizálja a PVA és GDA között
az aetálkötés felhasítását. Ennek következtében minél többet használjuk a
PVA gélt(azer®s saver®s bázisdiódábaniser®s savbanázik 2
),annáltöbb
GDA oldódik ki bel®le, aminek következtében a géltulajdonságaiaz id®ben
változnak.
2
Erreaproblémáramegoldás,haadiódátgyengesavvalésbázissalüzemeltetjük.
(
L ≈ 1
mm) igen nagy a gélid®állandója.Erre jó megoldás lenne, ha ebb®l a PVA-GDA keverékb®l vékony membránt készítenénk. Ezt azonban nemlehetne megfelel®en használni, mert az így készült membránt nem tudnánk
polarizálni. A membrán túl jó vezet®, ezért a diódára kapsolt feszültség
nem a membránon, hanem az oldattereken esne. Mivel a membránon alig
esne feszültség, ezért az így összeállított diódában a nyitó- és záróirányú
karakterisztika számottev®en nem különbözne egymástól.
1.4.2. PVB membrán
Abban areményben kezdtünkelkülönböz®membránokkalkísérletezni, hogy
el®bb-utóbb sikerül találni olyat, mely átveheti a PVA gélhenger szerepét a
sav-bázis diódában. Pusztán egy jól vezet® vékony membrán nem alkalmas
erre a élra. Egy poli(vinil-butiral) (PVB) alapú membránt sikerült kifej-
leszteni ún. leheletmintázat tehnika segítségével,melyjól polarizálható,így
alkalmas lehet sav-bázis diódák összeköt®elemeként m¶ködni [13℄.
A PVB membránon hatszöges mikromintázatot fedeztünk fel, a száraz
körülmények között készítettPVB membránhoz képest amegnövekedett ve-
zet®képességet valószín¶leg jól vezet® foltok okozzák a hatszögek alján (7.,
8. és9.ábra).Itta membrán lényegesen vékonyabb lehet,továbbáakészítés
közben lesapódott vízseppek kis mértékben rendezhetik is a PVB poláris
hidroxilsoportjait,aminekkövetkeztébenvalószín¶legionvezet®"satornák"
jönnek létre.
A gyengesavgyenge bázisdióda[14, 4℄lényegében nemkülönbözikazer®s
saver®sbázisdiódától.Akülönbségsupánazoldattereketkitölt®oldatok-
ban van: er®s bázis (KOH) és er®s sav (HCl) helyett részlegesen disszoiáló
bázis (BOH
⇀ ↽
B+
+ OH−
) és sav (HA⇀ ↽
H+
+ A−
) oldata található adiódában(pl. NH
4
OH-CH3
COOH).Vagyisasavasoldattérben aH+
ésA
−
ionok mellett disszoiálatlan HA molekula, a lúgos oldattérben a B
+
és a
OH
−
ionokmellettBOH molekulais jelenvan.
Azer®s ésgyengesav-bázisdiódákfeszültségáramer®sségkarakteriszti-
káihasonlóak (2.ábra). A részleges disszoiáiómiatt az oldatterekben ésa
diódában azionokkonentráiója kisebb (mindkétesetben az oldatterekben
c 0 = 0, 1
M-oskonentráiójúsav- ill.lúgoldattalálható),aminyitó-észáró- iránybaniskisebbáramoteredményez (2.ábra).Nyitóiránybanészáróirány-banisazáramjóközelítéssellineárisfüggvényeadiódárakapsoltfeszültség-
nek. A xált töltések hatása miatt (a gélben mindkét esetben ugyanakkora
axálttöltések konentráiója) azáróirányúmeredekség megegyezikgyenge
és er®s sav-bázis diódában.
1.6. Sav-bázis tranzisztorok
Asóhatásazalapjaazelektrolittranzisztorokm¶ködésének.Afélvezet®tran-
zisztorok analógiájára két sav-bázis diódából is lehet tranzisztort készíteni
[15℄. A tranzisztort, hasonlóan a pnp ill. az npn összetétel¶ félvezet® tran-
zisztorokhoz lehet sav-lúg-sav, vagy lúg-sav-lúg elrendezésben üzemeltetni.
A sav-bázis-sav tranzisztoreredményeijóanalógjaiafélvezet®diódákbólké-
szíthet® tranzisztoroknak, azonban a bázis-sav-bázis tranzisztorok bizonyos
emitter-bázis feszültség felettnem stabilak, a kollektor áram értéke oszillál
[15, 11℄. A továbbiakbanelektrolit tranzisztorokkal nem foglalkozom.
1.7. A dióda matematikai modellje
1.7.1. A diódát leíró pariális diereniálegyenlet-rendszer
A gélben sav-bázis reakió, diúzió és az elektromos er®tér hatására be-
következ® ionmigráió egy id®ben zajlik [16, 17, 18℄, ezért a matematikai
modell egyenletei az egyes komponensekre felírható mérlegegyenletek és az
elektromos poteniálra felírható Poisson-egyenlet [19℄. A sav-bázis diódában
lejátszódó transzportfolyamatok lényegében egydimenziósaknak tekinthet®k
[6℄. A diódamatematikaimodelljejelenleg egypariális diereniálegyenlet-
rendszer. Akomponensmérlegazalábbiformábanírhatófeltetsz®legeskom-
∂c i
∂t = − ∂
∂x (J i ) + σ i ,
(4)ahol
J i
azi
-edikkomponensárams¶r¶sége,∂c i
∂t
akomponenskonentráiójá- nak id®szerinti deriváltja,σ i
pedig a forráss¶r¶sége, azaz azi
-edik kompo-nenst termel® ésfogyasztó reakiók sebességének a különbsége.
Az árams¶r¶ségre a Nernst-Plank egyenletet írjuk fel, amely szerint az
árams¶r¶ség egy diúziós ésegy migráióstagbóláll:
J i = J i
di+ J i
migr= −D i
∂c i
∂x − D i c i z i
∂ϕ
∂x F
RT ,
(5)ahol
J i
di az i-edikkomponens diúziós,J i
migr a migráiósárams¶r¶sége,D i
a diúziós állandója,
z i
a töltésszáma,ϕ
az elektromos poteniál,x
a hely-koordináta az összeköt®elem mentén,
F
a Faraday-állandó,R
az egyetemesgázállandó,
T
pedig azabszolút h®mérséklet.Avizsgált HClKOHdiódábana komponensek,melyekreazanyagmér-
legegyenletetfelkellírnistaionáriusállapoteseténakövetkez®k: H
+
,OH
−
,
K
+
és Cl
−
. Staionárius állapotban a xált töltések (FA
−
) konentráióját,
mivel nem tudnak mozogni, így árams¶r¶ségük nulla, a xált töltést adó
savassoport(karboxil soport) disszoiáiós egyensúlyábólszámíthatjuk:
K
x= c
H+ c
FA−
c
HFA= 10 − 4
M.
(6)Tranziensmodelleseténafentiegyszer¶sítésselnemélhetünk,konvergen-
iaproblémák miattugyanakkorkénytelenek voltunk (err®ltovábbirészletek
a D.1. függelékben találhatók). Tehát a tranziens modellben a xált töltés
protonálódási reakiójátisgyelembekellvenni.Így akomponensmérlegeta
xált töltésre(FA
−
) és ennek protonált formájára (HFA) is fel kell írni[20℄.
Ebben azesetben a reakiótagok akövetkez®k:
σ
H+ = k
v(K
v− c
H+ c
OH− ) + k
x(K
xc
HFA− c
H+ c
FA− )
(7)σ
OH− = k
v(K
v− c
H+ c
OH− )
(8)σ
K+ = σ
Cl− = 0
(9)σ
FA− = σ
HFA= k
x(K
xc
HFA− c
H+ c
FA− ).
(10)A vizsgált gyenge sav gyenge bázis diódában (NH
4
OH CH3
COOH)az egyes komponensek a következ®k: H
+
, OH
−
, B
+
, A
−
, BOH, HA, K
+
és
Cl
−
. Mivel a gyenge sav gyenge bázis diódát sak staionárius állapotra
vizsgáltam, ezért a xált töltések konentráióját az egyensúlyi állandóból
számítottam. A gyenge sav gyenge bázis diódában az egyes komponensek
reakiótagjai akövetkez®k:
σ
H+ = k
v(K
v− c
H+ c
OH− ) + k
HA(K
HAc
HA− c
H+ c
A− )
(11)σ
OH− = k
v(K
v− c
H+ c
OH− ) + k
BOH(K
BOHc
BOH− c
OH− c
B+ )
(12)σ
B+ = −σ
BOH= k
BOH(K
BOHc
BOH− c
OH− c
B+ )
(13)σ
A− = −σ
HA= k
HA(K
HAc
HA− c
H+ c
A− )
(14)σ
K+ = σ
Cl− = 0.
(15)A poteniáltmindkétesetben a Poisson-egyenlet alapjánszámolhatjuk:
∂
∂x (−ε ∂ϕ
∂x ) = F X
i
c i z i ,
(16)ahol
ε
a közeg permittivitása(dielektromos állandója).A dióda viselkedését leíró pariális diereniálegyenlet-rendszer megol-
dásából az egyes töltéssel rendelkez® komponensek árams¶r¶ségeit számítja
ki a programúgy, hogy a már kiszámított konentráiókat és az elektromos
poteniált visszahelyettesíti a Nernst-Plank-egyenletbe (5). Az egyes kom-
ponensek árams¶r¶ségeib®l a hely- és id®függ® elektromos árams¶r¶ség a
következ® módon számítható:
i = F X
i
z i J i .
(17)Staionáriusállapotban az így számítottárams¶r¶ség szinte végig állan-
dó a gélmentén, egyetlen kivétel adióda reakiózónája. A numerikus hibák
kiküszöbölése miatt staionárius állapotban a kapott árams¶r¶ség az elekt-
romosárams¶r¶séghelyszerintiintegráljaagélmentén. Azid®függ®esetben
viszont azárams¶r¶ség helyfügg®. Ennek ellenéreaz id®árams¶r¶ség gör-
béken ilyenkor is az árams¶r¶ség hely szerinti integrálját tüntetem fel. Az
így számított árams¶r¶ség, mind a staionárius, mind a tranziens esetben
arányos amért áramer®sséggel, és id®ben ugyanúgyváltozik a kísérletilegis
megvizsgáltesetekben. Annakmeghatározásához,hogya helyfügg® árams¶-
r¶ségpontosanhogyanviszonyulamértáramer®sséghezegyvalódidiódában,
további megfontolások és vizsgálatok szükségesek.
A gél két szélén Dirihlet-határfeltételt (x konentráiót) alkalmazok. Az
összeköt®elem (gél) két szélén az egyes ionok konentráióit az oldatterek
konentráióiból,amembránegyensúlyt,vagymásnéven Donnan-egyensúlyt
gyelembevéve számíthatjuk.Haahatárokonazoldatterekkonentráióival
számolnánk, és elhanyagolnánk aDonnan-egyensúlyt, akkora xálttöltések
miattkisugrástkapnánkagélvégeinakonentráióprolokban,amennyiben
ahatárokonnemtételezünk felxálttöltést.Ezleginkábbnumerikusproblé-
mákatokozna,ígyérdemesaDonnan-egyensúlybólapontoshatárfeltételeket
meghatározni.
A két különböz® zikai-kémiai közeg (oldattér, gél) érintkez® szélein az
elektrokémiai poteniálnak (
µ ˜
) kell megegyeznie, mely a következ®képpen fejezhet® ki[21℄:˜
µ = ln(c i ) + z i ϕ F
RT .
(18)Az elektrokémiai poteniálokállandóságábóla következ® összefüggés ve-
zethet® le:
([
Kat+ ]
gél) z + · ([
An− ]
gél) z − = ([
Kat+ ]
old) z + · ([
An− ]
old) z − ,
(19)ahol Kat és An egy kationt ill. aniont,
z +
ész −
pedig ezek töltésszámait jelöli. Ezaz összefüggés tetsz®leges ionpárraigaz.A gélhatárainmég jó közelítéssel igaz az elektroneutralitás is:
c
H+ +
n
X
i=1
c
Kat+ ,i = c
OH− +
m
X
j=1
c
An− ,i + c
FA− .
(20)Adiódábanmegtalálhatóanionok éskationokkonentráióját a(19)for-
mulasegítségévelkifejezhetjükvagya H
+
, vagyaz OH
−
iongélbelikonent-
ráiójának a függvényében, ahol az ionokoldatbelikonentráiói ismertek:
c
gélKat
+ ,i = c
oldKat
+ ,i · c
oldOH
−
c
gélOH
−
= c
oldKat
+ ,i · c
oldOH
−
K
v· c
gélH
+ ,
(21)soportok teljes konentráiója, a xált soport disszoiáiós állandója és a
H
+
, vagy azOH
−
ionkonentráiójának afüggvényében:
c
FA− = K
x· c
xc
H+ + K
x= K
x· c
xK
vc
OH
−
+ K
x,
(23)ahol
c
xaxálttöltésekteljeskonentráiójátjelöli(protonáltésdeprotonált formák összege).A savoldalon minden iont a H
+
ion konentráiójával, míg a lúgoldalon
minden iont azOH
−
ionkonentráiójával kifejezve, majd behelyettesítve a
(20) egyenletbe, egy
n
-ed fokú algebrai egyenletet kapunk.n
a max. töltés-számtól függ,a vizsgált esetekben
n = 2
,mely egyenletnek meg kellkeresni a pozitív valós gyökét. Ebb®l a gyökb®l pedig már minden konentráió ki-számolható a határon, valamint a Donnan-poteniál, az oldat és a gél fázis
között létrejöv® poteniálugrás is(18) segítségével.
1.8. Adaptív FEM
A sav-bázis dióda viselkedését leíró pariális diereniálegyenlet-rendszert
(PDE) végeselem-módszer (FEM) segítségével oldom meg. A FEM-r®l egy
rövid bevezetés azB függelékben található.
A PDE térbeli diszkretizáiója után egy közönséges diereniálegyenlet-
rendszert (ODE) kapunk, melynek megoldásával (id®beli "kiintegrálás") áll
el® a megoldás. Az alkalmazotttérbeli diszkretizáió (háló, rás vagy mesh)
kiemelt jelent®séggel bír az egyenlet megoldhatósága, a konvergeniasebes-
ség és a közelítés hibájának szempontjából.Általánosságban igaz, hogy mi-
nél több ráspontot alkalmazunk (s¶r¶bb a háló), annál pontosabb lesz a
megoldás. Ugyanakkor asok ráspont er®forrásigénye igen nagy lehet, meg-
n® a futási id®, és jóval több memóriára van szükség [22, 23℄. Amennyiben
a modellezett tartományon (domain-en) létezik egy (vagy több) zóna, ahol
igennagyok agradiensek, akonvergenia eléréséhezszükséges nagyfelbontá-
sú ekvidisztánsháló alkalmazásanemhatékony. A hálótilyenkorelég saka
problémásrészeken továbbnomítani,értelemszer¶enaszükségesmértékben.
Amennyiben egyid®függ®probléma eseténennek azónánakahelyeváltozik,
akkor ahálót is folyamatosan módosítani kell: ezt hívják adaptívmesh-nek,
ill. adaptív FEM-nek 3
.
AzadaptívFEM algoritmusokalapvet®enháromf® soportba oszthatók:
3
Természetesenaráspontokadaptívváltoztatásátnemsakvégeselem-módszeralkal-
pozíiójaváltozik;
h-renement vagylokáliss¶rítés:aráspontokszámanem x.Vanegy
x alap, mely pontok helyzete állandó, és a lokális követelményeknek
megfelel®en (általában valamilyen lokális hiba alapján) a problémás
részekre (hogy pontosan hova,az mindigváltozik) kerülnek még plusz
elemek;
p-renement:ebben azestben a háló x, a bázisfüggvények fokszámá-
nak növelésével javítható apontosság.
Természetesen ezen módszerek kombináiója is elképzelhet®, pl. a hp-
renement-nekkiterjedtirodalmaisvan[24℄.Amozgóhálók,atöbbiadaptív
hálógenerálásitehnikáhozképest kevésbé népszer¶ekésfejlettek,ennek oka,
hogyelég nehézahálómozgáshoz megfelel®vezérl®egyenletettalálni.Ugyan-
akkor ennek a módszernek számos el®nye is van: elég könny¶ bármilyen x
mesh szoftverhez illeszteni, ráadásul az elemszám változásból származó ne-
hézségek is elkerülhet®ek [25℄.
Általában a mozgó háló algoritmusok az ún. "equidistribution prinip-
le" -ön alapulnak [26℄, mely kb. azt jelenti, hogy a hálópontokat úgy kell
kiválasztani, hogy a közelítés hibája kiegyenlített legyen az elemek között.
Ehhezahibátfolyamatosan monitoroznikell,amiaváltozókels® ésmásodik
deriváltjasegítségével történik.
Azirodalombanszámospéldatalálható,hogyanleheta sav-bázisdiódáé-
hozhasonlópariálisdiereniálegyenlet-rendszertmegoldani[27℄.Alegtöbb
módszerhez nemsak a hálómozgástleíró részt, hanema teljesFEM algorit-
must, a térbeli- és id®beli diszkretizáióval együtt implementálni kell. Két
reakió-diúzió rendszerhez, nevezetesen a Gray-Sott és a Brusselator mo-
dellhez készült mozgó hálót mutatja be [28℄. Ebben a háló mozgáshoz egy
külön pariálisdiereniálegyenlet-rendszertírnakfel,melyninssatolvaaz
eredeti modell diereniálegyenleteihez. A mozgó mesh PDE-k (MMPDE)
az ún. mesh-energia funkionál minimalizálásából származnak. Ezen vari-
áiószámítási megközelítés elég általános a mozgó hálók módszerei között
[29℄, általában a hálóegyenleteket satolják az eredeti diereniálegyenlet-
rendszerhez [30℄. Néhány további példa r-renement-re[31, 32℄-ben találha-
tó.
Egyelektrokémiaiproblémavéges-diereniákkaltörtén®megoldásáraké-
szült h-renement módszert [33℄ mutat be. Kés®bb ezen módszert sikeresen
nita-ék algoritmusának [25℄ van a legnagyobb jelent®sége. k sószennye-
zés nélküli sav-bázis diódák id®függ® modellezéséhez készítettek empirikus
algoritmust, melyet a FEMLAB (a COMSOL el®dje) végeselem megoldó-
jához illesztettek. A monitorozó függvényük a H
+
, OH
−
logaritmusának a
deriváltjából és a poteniál els® és második térbeli deriváltjából áll össze.
Mivel ennek azid®lépésenkéntikiértékelése igen id®igényes, ezért azalgorit-
musatranszportid®kalapjánbesli, hogymikorlehetszükségamonitorozó
függvény kiértékelésére ésúj háló generálására.
1.9. Sav-bázis diódák modellezése történeti összefogla-
lás
A sav-bázis dióda konepiója prof. Nosztizius Zoltántól, még az 1970-es
évekb®lszármazik[2,3℄,intenzívkutatása ugyanakkoraz1990-esévekköze-
pén kezd®dött, melyhez a prágai soporta 2000-es évek elején satlakozott.
A diódamatematikaimodelljének,melya jelenközelítésben egynemlineáris
PDE rendszer (1.7. fejezet), numerikus módszerekkel történ® megoldása is
a 2000-es évekt®l vált lehet®vé [17℄. Korábban a diódát els®sorban kísérleti-
leg vizsgálták, a vizsgált jelenségekre leginkább analitikus közelítéseket, fél-
kvantitatívmagyarázatokatadtak (pl.nyitóirányú karakterisztikaegyenlete,
záróirányú karakterisztika egyenlete, összeköt®elemben három zóna találha-
tó, stb.).
Ezen analitikusközelítések ismár az 1.7. fejezetben bemutatott egyenle-
tekb®l indultak ki, és lényegében egydimenziósnak tekintették a gélben lév®
transzportfolyamatokat [16℄. A dióda viselkedését leíró pariális differeni-
álegyenlet-rendszer els® mindenféle elhanyagolás nélküli staionárius nume-
rikus megoldásai ezen analitikus közelítések létjogosultságát támasztották
alá [17℄. A kétpontos peremérték feladatot kezdeti érték feladattáfogalmaz-
ták át, melyre az ún. "belövéses" módszer (shooting method) nem konver-
gált. A numerikus megoldás egy ún. prediktor-korrektor módszer segítségé-
vel történt, melynek során a staionárius megoldás során az árams¶r¶séget
x értéken tartották, és az elektromostérer®sséget számították. (Azeredeti
diereniálegyenlet-rendszert még korábbilépésben dimenziómentesítették.)
A diódát leíró differeniálegyenlet-rendszer megoldása a végeselem-mód-
szerrelel®ször2002-bentörtént[18℄,enneksoránmáraFEMLAB-othasznál-
ták, melyaz általamis használt COMSOLel®djének tekinthet®. A pariális
differeniálegyenlet-rendszert nemlineárissá tev® reakiótagok fokozatos nö-
velésén alapuló relaxáiós algoritmus ötlete is ittkerült el®ször említésre. A
dióda numerikus modellezése során a végeselem-módszer és a FEMLAB /
gálata során [12℄. Ugyanígy a dióda tranziens modellezéséhez nita-ék so-
portjaadaptívFEMalgoritmustisfejlesztett,mellyel0V-rólindulvaadióda
feszültségmódosításraadott válaszátvizsgálták.
Az egész sav-bázis dióda matematikai modellje egy diereniálegyenlet-
rendszer, mely számos elhanyagolást tartalmaz. Ezek egyike a határfelületi
jelenségek (gél oldattérhatárfelület) gyelmen kívülhagyása. Ez jóközelí-
téssel megtehet®, ezt sikerült kísérletekkel igazolni[8℄. Ugyanakkor azt meg
kell jegyezni, hogy a sav-bázis diódák modellezése kapsán az elmúltkb. 20
évben amatematikaimodellnemváltozott,azújeredményeketazegyenletek
egyre változatosabbperemfeltételekkeltörtén® megoldása szolgáltatta.
"A tudomány végül is abból áll,
hogy van egy probléma, ésvan
egy megoldás. Ésközte ott a
nehéz út." Róna-Tas András
Értekezésem 2. fejezetében a dióda id®függ® modellezéséhez készült lo-
kális reakiósebességen alapuló adaptív hálógenerálási algoritmusomat mu-
tatom be,melyeta COMSOL végeselem-megoldóhoz illesztettem. El®ször a
COMSOL modellt és beállításokat, majd a hálógenerálás alapjául szolgáló
rásfüggvényt ismertetem. Ezután röviden bemutatom a reakiózónát, itt a
legnagyobbakakonentráiógradiensek,ígyezadiódánakanumerikusszem-
pontbóllegproblémásabb része.
Végülegyel®redeniáltbeállításokkalkészültszimuláiópéldáján(benh-
mark) vizsgálom az algoritmus teljesítményét a futási id® és a közelítés hi-
bájának a szempontjából. Példaszimuláiónak az id®függ® pozitív sóhatás
jelenségét választottamazer®s sav er®s bázisdiódában.Ennek soránasó-
szennyezés nélküli diódábólkiindulva
t = 0
s-ban adiódalúgoldalát[KCl℄L,t= 60mM sóvalszennyezem, ésakiindulási,valamintazátütöttstaionárius
állapot közötti tranzienst szimulálom,melynek id®tartama kb. 150 s, a dió-
dára kapsoltfeszültség általában
U = 10
V, amennyiben nem, azt külön azábraaláírás tartalmazza.
2.1. Modellépítés a COMSOL Multiphysis segítségével
A dióda id®függ® modellezését a COMSOL Multiphysis 4.3-as verziója se-
gítségével végzem 4
. A zikai modellt a következ® módon deniálom: a kom-
ponensmérleget a Nernst-Plank-egyenlettel a "Transport of Diluted Spei-
es" interfészb®l, a Poisson-egyenletet pedig a "Classial PDEs" interfészb®l
választom ki. Egy teljes modellszámítást két lépésre ("Study step") lehet
bontani.
Els®lépésakezdetifeltételekkiszámítása,melyahatárfeltételekkiszá-
mításautánegystaionáriusszimuláiónakfelelmeg.Ehheza[12℄-ben
bemutatott parametrikus megoldóthasználom.
4
Amodellépítésa4-esverziótólindult,melyneksoránaCOMSOLSupportfelészámos
hibát jelentettem.Azösszesjavítása4.3.0.233.verzióbakerültbe,ígyazittbemutatott
modellsakett®laverziótólhasználható.(2021-reaCOMSOLaz5.6-osverzióigjutott.)
A numerikus megoldókat, ill. az egyes lépéseket a "Study" menüpont
alatt lehet beállítani. A két lépés között a határfeltételeket át kell állítani
a tranziens számításnak megfelel® értékre. (A staionárius számításokat a
Compute to seleted,mígazid®függ®ketaCompute from seleted paransal
lehet indítani.)
A térbeli diszkretizáió után kapott id®függ® közönséges diereniále-
gyenlet-rendszer(ODE)numerikusintegrálásáhozaBDFmódszert,aSPOO-
LES ritkamátrix megoldóval,automatikus skálázássalalkalmaztam.A meg-
oldás során az id®lépést a solver automatikusan határozza meg. A numeri-
kus oszilláió elkerülése érdekében a "Crosswind diusion" nev¶ stabilizá-
iós tehnikát választottam. Itt meg kell jegyezni, hogy a diódához hasonló
reakió-diúziórendszerekmodellezésesorántapasztaltamolyat,hogyameg-
oldást egyik, a COMSOL-ban rendelkezésre álló stabilizáiós tehnika sem
volt képes stabilizálni, a megoldást sakis a háló extrém s¶rítésével, vagy
kézi skálázással sikerült stabilizálni. A térbeli diszkretizáláshoz másodfokú
Lagrange-féle alappolinomokathasználtam (els®fokúval nem is konvergált a
megoldó).
A FEM modellezéskulskérdése a hálózás,vagyis a rásgenerálás, mely-
nek igen nagy hatása van a konvergeniára. A sav-bázis dióda numerikus
szempontbólproblémás része a reakiózóna(ahol az egyes változók gradien-
sei a legnagyobbak), itt a legnagyobb a numerikus közelítés hibája. Ahhoz,
hogyasolver konvergáljon,ittextréms¶r¶háló szükséges, ezminimum500-
1000 elemetjelenta diódareakiózónájának0,01 mmsugarúkörnyezetében.
Id®függ®szimuláióeseténezenzónatérbelielhelyezkedésefolyamatosanvál-
tozik, így az er®forrásigény sökkentése érdekében valamilyen adaptív hálót
érdemes használni.
A COMSOL Multiphysis-ben az id®függ® modellekhez létezik adaptive
mesh renement kiterjesztés 5
, de ezzel nem sikerült konvergeniát elérni.
(Sajnosez atoolelég rosszul dokumentált, én úgy gondolom, hogy
h
-típusús¶rítésttakarhat.)A COMSOL-banlétezikegyún. "MovingMesh" interfész
(mellyela zikaimodellhezsatolvamozgóhálót lehetkészíteni), de ezt sem
sikerült m¶ködésre bírni. Ezért a hálómozgás biztosításához saját empiri-
kus hálógenerálásialgoritmustkészítettem, melyetaJava-banírtend-to-end
szimuláiós keretrendszerhez illesztettem 6
.
Egy adaptív hálógenerálási algoritmus általános m¶ködése az 10. ábrán
látható.Mindenegyesiteráióslépésutánelkelldönteni,hogykell-eújhálót
a két háló között a megoldást interpolálni kell. A COMSOL-ban a FEM
algoritmusok sok szempontból fekete doboznak tekinthet®k, tehát sakis a
COMSOL általbiztosított interfészeken keresztül érhet®k el.
NUMERIKUS
SOLVER MONITOR MESH
MEGFELEL -E?
ÚJ MESH GENERÁLÁS
Y
N
SOLVER ÚJRAINDÍTÁS
10.ábra. Adaptívhálógenerálási algoritmus általános m¶ködése.
A háló megfelel®ségének monitorozásához az ún. Domain Point Probe
segítségével egyStopondition-tdeniáltam.A COMSOL-bana point probe
expression a következ®: a modellezett tartomány egy el®re deniált pontján
a diereniálegyenlet változóiból tetsz®leges függvény deniálható, mely a
megoldás soránmindig kiértékelésre kerül.
AStopondition-hözareakiózónakétszélénkétpointprobeexpression-t
deniáltam, melynek értéke a sav-bázis rekombináió lokálisreakiósebessé-
gének abszolútértéke:
ppv = |σ
H+ | = |σ
OH− | =
k
v(K
v− c
H+ c
OH− )
.
(24)A Stop ondition a következ®: ha egy
ppv
értéke szignikánsan különbözik nullától (ppv > 1, 3 · 10 − 3
moldm
3
s
), akkor a solver-t meg kell állítani. Ezután
a reakiózóna tulajdonságai alapján új hálót kell generálni, majd a numeri-
kus megoldó újraindítása el®tt a két
ppv
számításának a helyét még át kell helyezni.2.2. A rásfüggvény
A hálót ún. rásfüggvény segítségével deniálom. A rásfüggvény egy olyan
x → f(x)
leképezés, mely egy ekvidisztáns rás koordinátáit a valódi háló((a) rész).Amennyibenavalódimeshegynagyrésztekvidisztánsmesh,mely
egy extrém nom felbontású zónát tartalmaz, akkor arásfüggvény egyenes
szakaszokból tev®dik össze ((b) rész). Végül az ábra () része az általam
használt rásfüggvényt ábrázolja.
f(x)
x
f(x)
x
f(x)
x
| | | | | | | | | ||||||||||||||||||||||||||||||||||| | | | | | | |
| | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | |||||||||||||||||||||||||||||| | | | | | | | | |
(a)
(b)
(c)
11.ábra. Néhányrásfüggvény ahozzátartozó hálósematikus rajzával. (a)Ekvi-
disztáns rás. (b) Ekvidisztáns rás egy extrém s¶r¶ zónával. () Az alkalmazott
rásfüggvény exponeniálissimítással.
Az általam használt () rásfüggvény a (b)-n ábrázolton alapul. A re-
akiózóna bizonyos kiterjedés¶ környezete extrém s¶r¶ hálóval van lefedve,
de hogyazegyesrészek deriváltjaiis folytonosansatlakozzanakegymáshoz,
a különböz® meredekség¶ egyenesek között két x szélesség¶ exponeniális
zónát deniálok. Ennek részleteia C.2. függelékben találhatók.
N
: a háló pontjainakszáma;
y
A, y
B: zikai koordináta-rendszerben (f(x)
) a nagy felbontású zónaszélei;
R
:annak aránya,hogyahálópontokmekkorarészekerüly
Aésy
Bközé;
δ
:a rásfüggvény exponeniálisrészének a szélessége;
d
:y
A vagyy
B és az annak megfelel® point probe expression közöttitávolság;
∆y
: annak a mértéke, amennyivel az el®z® rásfüggvény vezérl®pont- jai (y
A,y
B) a solver megállításaután a reakiózónahaladási irányába eltolódnak,ésazújhálógenerálása márezenrásfüggvény alapjántör-ténik.
Arásfüggvényen alapulóadaptív hálógenerálásialgoritmusel®nyeiakö-
vetkez®k:nagyonegyszer¶implementálni,könnyenésgyorsanlehetvelehálót
generálni.
2.3. A dióda reakiózónája
Asav-bázisrekombináiólokálisreakiósebessége(jelölje
σ
H2
O)a[
H] + ·[
OH] −
szorzatlineárisfüggvénye,amelyszorzategyensúlybanegyh®mérsékletfügg®
állandó. Staionárius állapotban a sószennyezés nélküli diódában a lokális
reakiósebesség a 12. ábrán látható.
σ
H2
O értéke egyedül a reakiózónában, ahol a sav-bázis reakió zajlik,különbözika zérustól.A dióda átütése során a lokális reakiósebesség néhány id®pillanatbana
13. ábrán látható. Nem sak staionárius állapotban, hanem az átütés so-
rán végig egyetlen régió létezik, ahol ez az érték különbözik a nullától, ez
a reakiózóna. Minél közelebb kerül a reakiózóna a lúgoldalhoz (bal oldal),
a sav-bázis reakió annál gyorsabb és gyorsabb lesz. Kb.
10
s után a reak-iózóna helyzete már lényegében nem változik, egyedül a reakiósebesség n®
tovább.
Az átütés során négy kiválasztott id®pontban a dióda reakiózónájában
alokálisreakiósebességet, továbbá azegyesváltozókels® ésmásodiktérbeli
deriváltjaita 14.ábra mutatja. Ahogyan asav-bázis reakió sebessége egyre
n®, a reakiózóna kiterjedése úgy sökken. Az új staionárius állapotban a
szélessége kb.azegyharmadaasószennyezés nélküli értéknek.Areakiózóna
kiterjedését a
σ
H2
O sús félértékszélességéb®l kalkuláltam.Akiindulási staionáriusállapotbanatérbelideriváltakszéls®értékei na-
-5 0 5 10 15 20 25 30 35
0 0,2 0,4 0,6 0,8 1
σ H 2 O /(M/s)
x/mm 0
5 10 15 20 25 30 35
0,197 0,1975 0,198
12. ábra. A sav-bázis rekombináióhoz tartozó lokális reakiósebesség (
σ
H2
O=
−k
v(K
v− c
H
+ c
OH
− )
) asószennyezés nélküli sav-bázis diódában.reakiósebessége nullától eltér. Az átütés során aderiváltakmaximumhelyei
együtt mozognak a kémiai reakióval. A konentráió deriváltak széls®érté-
ke (ennek abszolút értéke) a reakiósebességgel együtt folyamatosan n®nek,
ugyanakkor a poteniál derivált széls®értéke alig változik. A második deri-
váltakszéls®értékeimindakonentráiók,mindapoteniáleseténnagyrészt
ugyanígy viselkednek.
-100 0 100 200 300 400 500 600 700
0 0,05 0,1 0,15 0,2 0,25
σ H 2 O /(M/s)
x/mm
0 s 2 s 3 s 4 s 5 s 7,5 s
13. ábra. A sav-bázis rekombináió lokális reakiósebessége (
σ
H2
O= −k
v(K
v− c
H
+ c
OH
− )
)az id®függvényében a dióda átütésesorán.0,1965 0,197 0,1975 0,198 0,1985 0,199 0,1995 0,2 0,2005
t = 0 s
σ H + ,OH -
∂ [H + ]/∂x
∂ [OH - ]/∂x
∂ [K + ]/∂x
∂[Cl - ]/∂x
∂ϕ/∂x
0,148 0,1485 0,149 0,1495 0,15 0,1505 0,151 0,1515 0,152
t = 3 s
σ H + ,OH -
∂ [H + ]/∂x
∂ [OH - ]/∂x
∂ [K + ]/∂x
∂[Cl - ]/∂x
∂ϕ/∂x
0,048 0,0485 0,049 0,0495 0,05 0,0505 0,051 0,0515 0,052
t = 5 s
σ H + ,OH -
∂ [H + ]/∂x
∂ [OH - ]/∂x
∂ [K + ]/∂x
∂[Cl - ]/∂x
∂ϕ/∂x
0,008 0,0085 0,009 0,0095 0,01 0,0105 0,011 0,0115 0,012 x/mm
t = 20 s
σ H + ,OH -
∂ [H + ]/∂x
∂ [OH - ]/∂x
∂ [K + ]/∂x
∂[Cl - ]/∂x
∂ϕ / ∂ x
0,1965 0,197 0,1975 0,198 0,1985 0,199 0,1995 0,2 0,2005
t = 20 s
σ H + ,OH -
∂ 2 [H + ]/∂ x 2
∂ 2 [OH - ]/∂ x 2
∂ 2 [K + ]/∂ x 2
∂ 2 [Cl - ]/∂ x 2
∂ 2 ϕ/∂ x 2
0,148 0,1485 0,149 0,1495 0,15 0,1505 0,151 0,1515 0,152
t = 20 s
σ H + ,OH -
∂ 2 [H + ]/∂ x 2
∂ 2 [OH - ]/∂ x 2
∂ 2 [K + ]/∂ x 2
∂ 2 [Cl - ]/∂ x 2
∂ 2 ϕ/∂ x 2
0,048 0,0485 0,049 0,0495 0,05 0,0505 0,051 0,0515 0,052
t = 20 s
σ H + ,OH -
∂ 2 [H + ]/∂ x 2
∂ 2 [OH - ]/∂ x 2
∂ 2 [K + ]/∂ x 2
∂ 2 [Cl - ]/∂ x 2
∂ 2 ϕ/∂ x 2
0,008 0,0085 0,009 0,0095 0,01 0,0105 0,011 0,0115 0,012 x/mm
t = 20 s
σ H + ,OH -
∂ 2 [H + ]/∂ x 2
∂ 2 [OH - ]/∂ x 2
∂ 2 [K + ]/∂ x 2
∂ 2 [Cl - ]/∂ x 2
∂ 2 ϕ/∂ x 2
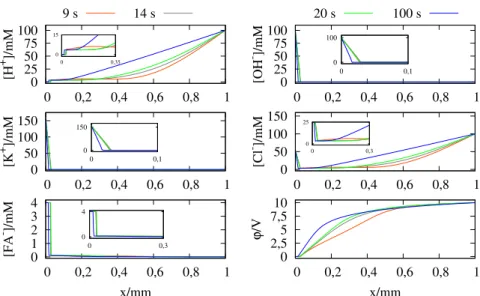
14.ábra. Areakiózónaadiódában:azegyeskomponensekkonentráióinak,vala-
mintapoteniálnakatérbelideriváltjai,valamintalokálisreakiósebességadióda
átütése sorána következ®id®pillanatokban:
t = 0
s,t = 3
s,t = 5
s ést = 20
s. Aderiváltakat ésareakiósebességet skáláztam.