FMA-UE – Fugl-Meyer Assessment-Upper Extremity, Skala do pomiaru wydolności fizycznej po udarze Fugl-Meyer w kończynie górnej. Porównanie jakości życia pacjentów po udarze mózgu ze spastycznością i jakości życia pacjentów po udarze mózgu bez spastyczności / 63.
PRZEGLĄD PIŚMIENNICTWA
Spastyczność i zespół górnego neuronu ruchowego – defınicje, patofızjologia i problem kliniczny
- Spastyczność – defınicje
- Spastyczność – wzorce ruchowe i patofızjologia
Spastyczność, która jest najbardziej charakterystycznym elementem zespołu uszkodzenia górnego neuronu ruchowego, nie oddaje w pełni obrazu klinicznego pacjentów z tym zespołem. Dlatego bardzo ważne jest, aby spastyczność pozostała jedyną składową zespołu górnego neuronu ruchowego, która podlega leczeniu farmakologicznemu i chirurgicznemu.
Spastyczność – wzorce ruchowe
W stwardnieniu rozsianym, po urazach rdzenia kręgowego lub w przypadku guzów rdzenia kręgowego często obserwowane wzorce spastyczności są związane z uszkodzeniem górnego neuronu ruchowego na poziomie rdzenia kręgowego i w zależności od stopnia uszkodzenia mogą przybrać postać zgięcia lub wyprostu spastycznego para- lub tetraparezy.
KOŃCZYNA GÓRNA
Spastyczność – patofızjologia
Reakcja statyczna są to skurcze mięśnia będącego w stanie rozciągnięcia związa- ne z aferentną (z wrzecion mięśniowych) impulsacją włóknami typu II zależną od długo-
Spastyczna dystonia jest to wzmożone napięcie mięśniowe, które nie jest zależ- ne od biernego lub czynnego rozciągania mięśnia (nie zależy od bodźców aferentnych
Reakcje stowarzyszone polegają na nasileniu wzmożonego napięcia mięśnio- wego przy wykonywaniu ruchów czynnych w oddalonych grupach mięśniowych (np
Spastyczność – metody klinicznej oceny spastyczności
1 + - Nieznaczny wzrost stanu napięcia mięśnia objawiający się oporem i rozluźnieniem, występujący w drugiej połowie zakresu ruchu w stawie. 2 - Bardziej wyraźny wzrost napięcia mięśniowego w większości zakresu ruchu w stawie, ale dotknięta chorobą część kończyny jest łatwo poruszana.
Spastyczność – metody leczenia
Jakie są ograniczenia i możliwe zagrożenia związane z każdą metodą leczenia. na przykład w zależności od wieku pacjenta lub innych stosowanych leków). Ponadto w większych dawkach często powodują ogólne skutki uboczne (np. senność, splątanie po baklofenie, niedociśnienie po tyzanidynie) lub prowadzą do uzależnienia (diazepam).
Udar mózgu i spastyczność poudarowa
- Udar mózgu jako problem kliniczny i społeczny. Epidemiologia udaru mózgu w Polsce i na świecie
- Następstwa udaru mózgu i metody ich klinicznej oceny
- Częstość i czynniki predykcyjne występowania spastyczności poudarowej
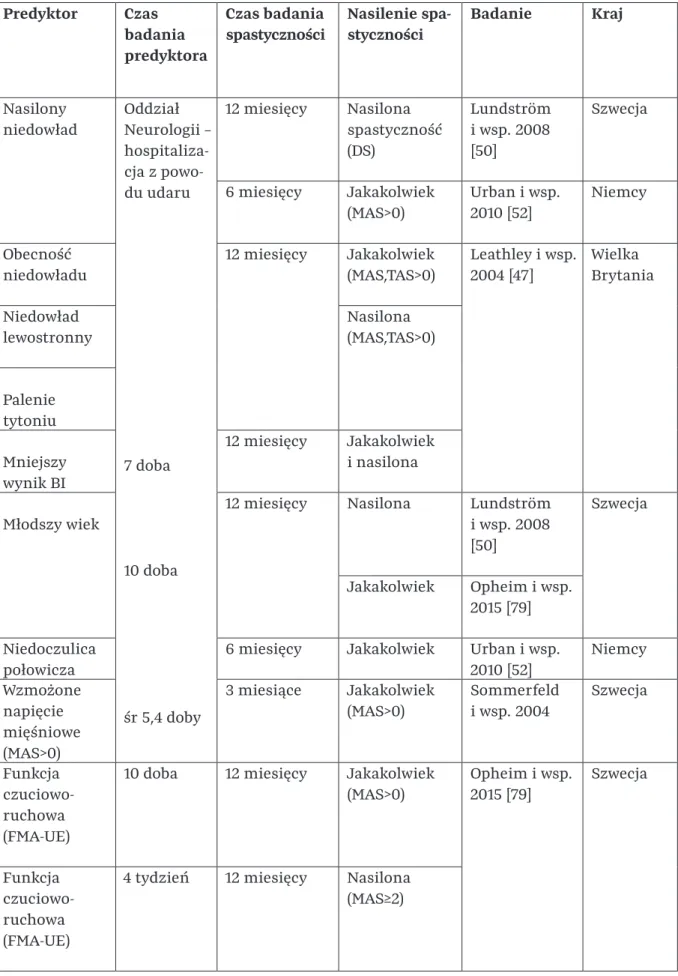
Niższy wynik BI w siódmej dobie udaru i większy stopień niedowładu w pierwszych 24 godzinach udaru predysponowały do wystąpienia jakiejkolwiek spastyczności w rocznej obserwacji. Z drugiej strony niższy wynik BI w siódmym dniu udaru, niedowład lewostronny i palenie były związane z cięższą spastycznością 12 miesięcy po udarze.
Predyktor Czas badania
Czas badania spastyczności
Nasilenie spa- styczności
- Wpływ spastyczności poudarowej na jakość życia i funkcjonowanie chorych
- CELE PRACY
- Określenie częstości występowania i stopnia nasilenia spastyczności kończyny górnej i dolnej u chorych po udarze mózgu. Wśród chorych poudarowych ze spa-
- Określenie różnic częstości, stopnia nasilenia i topografıi spastyczności zarów- no w kończynie górnej jak i dolnej w czasie (po 3, 6 i 12 miesiącach po udarze
- Porównanie niesprawności, funkcjonowania w życiu codziennym chorych ze spastycznością z chorymi bez spastyczności
- Ocena korelacji pomiędzy spastycznością a stopniem niedowładu, niesprawno- ścią, funkcjonowaniem w życiu codziennym u chorych po udarze
- Porównanie jakości życia chorych po udarze ze spastycznością z chorymi po udarze bez spastyczności
- Ocena korelacji pomiędzy spastycznością a domenami jakości życia chorych po udarze mózgu
- Określenie czynników ryzyka występowania spastyczności na podstawie danych klinicznych zbieranych od pacjentów hospitalizowanych w oddziale neurologii
- MATERIAŁ I METODY
- Dobór pacjentów uczestniczących w badaniu
Porównując grupę pacjentów ze spastycznością (n=13) do grupy pacjentów z niedowładem bez spastyczności (n=28) uzyskaliśmy istotnie gorsze wyniki kwestionariusza SF-36 w jednym obszarze: funkcjonowanie fizyczne (p<0,01). 52] jakość życia oceniano za pomocą kwestionariusza EuroQoL-5 Dimensions (EQ-5D), który opisuje stan zdrowia w 5 domenach: mobilność, samoopieka, codzienne czynności, ból/dyskomfort oraz lęk/depresja u pacjentów ze spastycznością ( n=75) i brak spastyczności (n=80) 6 miesięcy po udarze.

Metody oceny napięcia mięśniowego oraz stopnia niedowładu i niepełnosprawności
Pacjenci objęci badaniem byli badani podczas trzech wizyt z wykorzystaniem następujących narzędzi badawczych: 3, 6 i 12 miesięcy po udarze mózgu. Podczas kolejnych wizyt wykonano następujące badania: ocenę napięcia mięśniowego zmodyfikowaną skalą Ashwortha (MAS); ocena ciężkości niedowładu za pomocą skali Medical Research Council (MRC); ocena funkcjonowania pacjenta za pomocą skal klinicznych: Barthel Index i Rankine; ocena jakości życia związanej z chorobą za pomocą formularza SF-36.
Obecność umiarkowanej spastyczności została zdefiniowana jako MAS ≥2 w którymkolwiek z badanych stawów (przynajmniej w jednym) i brak MAS ≥3 w żadnym z badanych stawów. Obecność spastyczności wysokiego stopnia została zdefiniowana jako MAS ≥3 w którymkolwiek z badanych stawów (co najmniej w jednym).
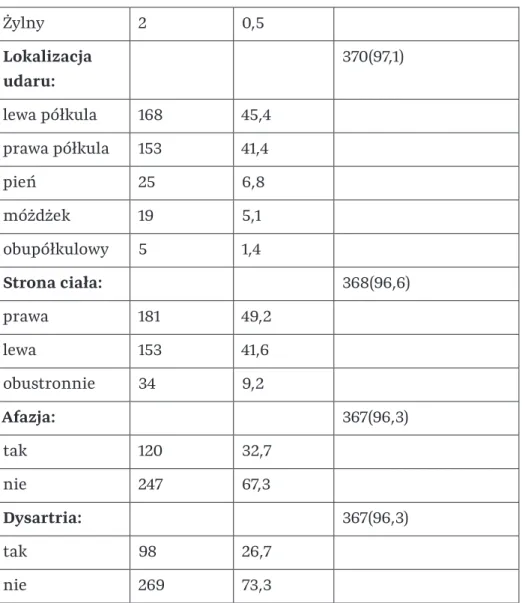
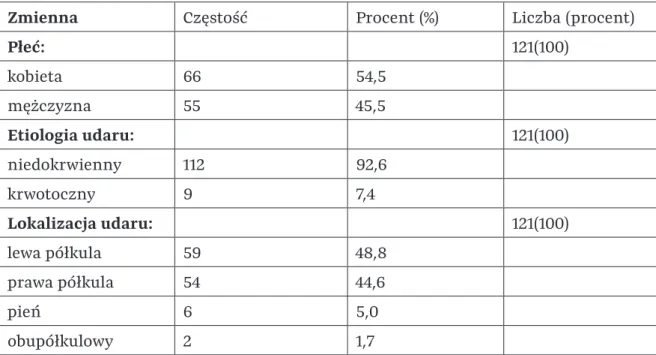
Etiologia udaru
0,5 Lokalizacja
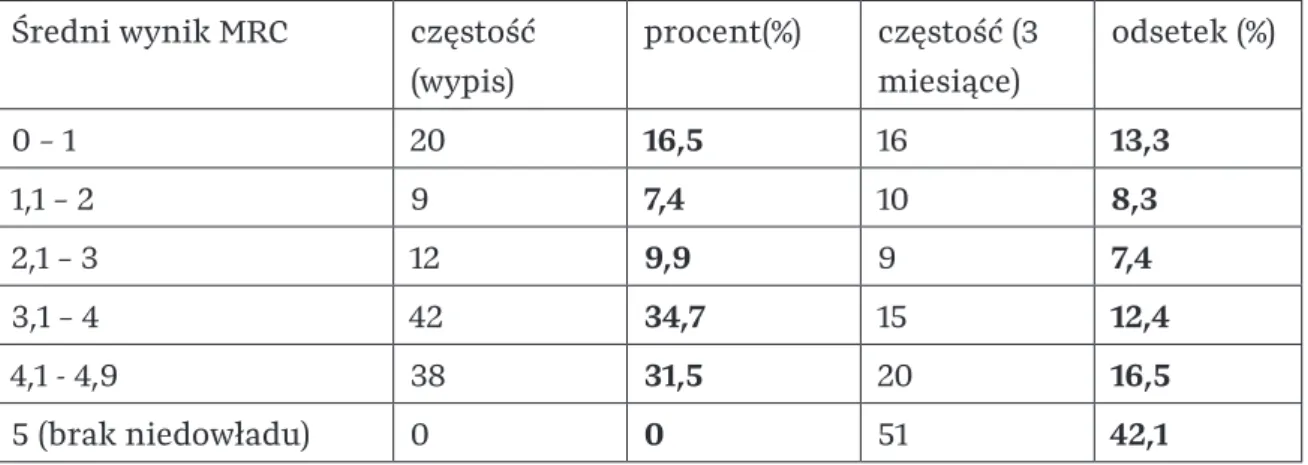
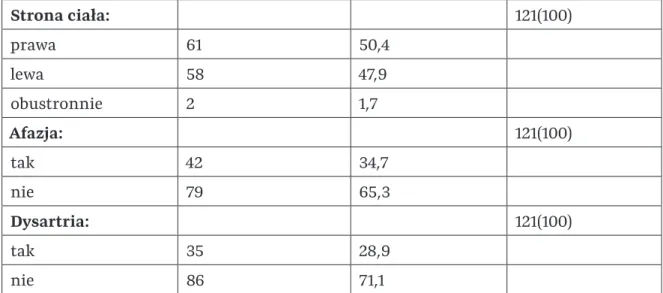
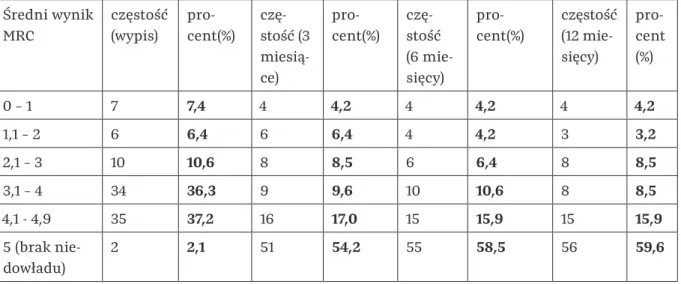
Dodatkowo w grupie wyjściowej przy wypisie z oddziału oceniano stopień niedowładu kończyn górnych i dolnych w stawach: barkowym, łokciowym, nadgarstkowym, palcowym, biodrowym, kolanowym i skokowym za pomocą skali MRC, którą również opisano szczegółowo w rozdziale „2.2 .2 Następstwa udaru mózgu i metody ich oceny klinicznej”. W tabeli 14 przedstawiono częstość i rozkład procentowy średnich wyników MRC dla kończyn górnych i dolnych w badanej grupie.
Średni wynik MRC przy wypisie
Opis grupy badanej po 3 miesiącach po udarze mózgu
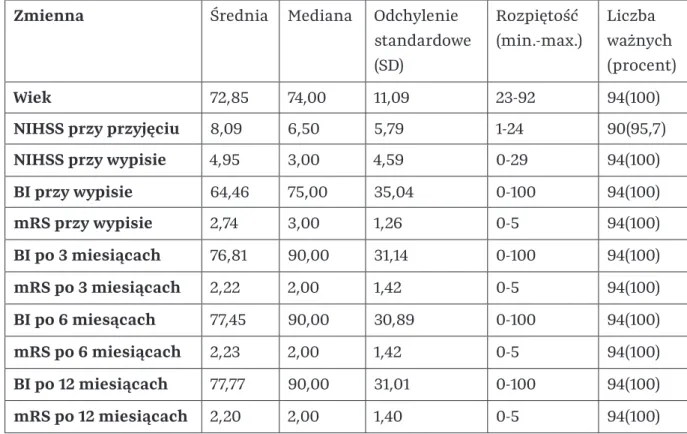
Wśród pacjentów kwalifikujących się do badania (n=121) ze średnią wieku 73,74 lat wyniki skal ciężkości udaru mózgu (NIHSS) oraz funkcjonowania pacjentów (BI i mRS) w poszczególnych przedziałach czasowych od wystąpienia udaru, tj. wyniki w skalach nasilenia udaru (NIHSS) i funkcjonowania pacjenta (BI i mRS) w oddzielnych odstępach czasu od początku udaru. W badaniu siły mięśniowej za pomocą skali MRC po 3 miesiącach większość pacjentów (71%) nie miała niedowładu lub tylko niedowład łagodny do umiarkowanego (MRC >3) (patrz tab. 20).
Średnie wyniki MRC dla obu kończyn (górnej i dolnej) na początku badania iw grupie badanej 3 miesiące po udarze. Średnie wyniki MRC oddzielnie dla kończyn górnych i dolnych w grupie badanej 3 miesiące po udarze mózgu.
- Opis grupy badanej po 6 miesiącach po udarze mózgu
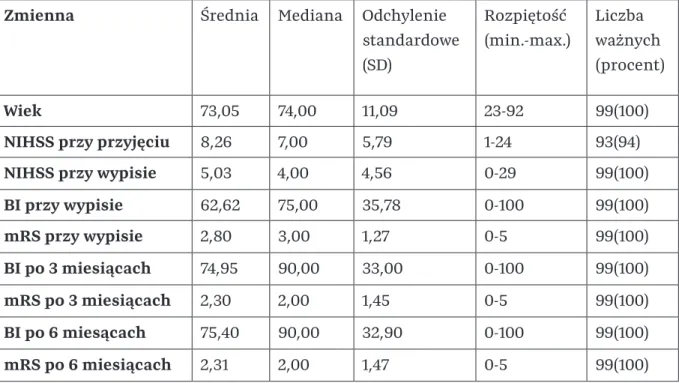
Wśród 99 chorych w średnim wieku 73,05 lat wyniki skali ciężkości udaru (NI- HSS) i funkcjonowania chorych (BI i mRS) w poszczególnych odstępach czasowych od
- Opis grupy badanej po 12 miesiącach po udarze mózgu
W obserwacji 3-miesięcznej niedowłady częściej iw większym stopniu występowały w kończynie górnej w porównaniu z dolną (tab. 24 i 25). Średnie wyniki MRC dla obu kończyn (górnej i dolnej) w grupie wyjściowej i badanej 3 i 6 miesięcy po udarze. Średnie wyniki MRC osobno dla kończyn górnych i dolnych w badanej grupie po 3 i 6 miesiącach od udaru.

- METODY STATYSTYCZNE
- WYNIKI
- Częstość występowania i stopień nasilenia spastyczności po udarze mózgu dla obu kończyn (górnej i dolnej)
- Częstości występowania i stopień nasilenia spastyczności po udarze mózgu dla kończyny górnej
- Częstości występowania i stopień nasilenia spastyczności po udarze mózgu w koń- czynie dolnej
- Topografıa częstości i stopnia nasilenia spastyczności w kończynie górnej i dolnej
- Częstość i stopień nasilenia spastyczności w zależności od czynników demografıcz- nych
- Ewolucja częstości spastyczności w czasie 12 miesięcy obserwacji
- Porównanie stopnia niesprawności i funkcjonowania w życiu codziennym chorych po udarze ze spastycznością ze stopniem niesprawności i funkcjonowaniem chorych
Częstość występowania spastyczności kończyn górnych i dolnych w zależności od stopnia nasilenia w różnych odstępach czasowych od wystąpienia udaru mózgu przedstawiono w tabeli 30. Częstość występowania spastyczności kończyn górnych i dolnych w zależności od stopnia nasilenia w różnych odstępach czasowych wystąpienia udaru mózgu. Częstość występowania spastyczności kończyny górnej w zależności od stopnia nasilenia w różnych odstępach czasu od wystąpienia udaru mózgu.
Średnie wyniki skali MAS dla wszystkich grup mięśni w badanych stawach kończyny górnej w zależności od czasu badania przedstawiono w tabeli 33. Częstość i ekspresja spastyczności w zależności od płci pacjentów w trzech obserwacjach: po 3, 6 i 12 miesięcy przedstawiono w tabeli nr. 39.
Porównanie wyników uzyskanych w skali mRS w dwóch grupach pacjentów: ze spastycznością i bez spastyczności wykazało istotną statystycznie różnicę (p<0,01) w stosunku do grupy ze spastycznością. Poniższa tabela przedstawia mediany i średnie wyniki mRS w dwóch badanych grupach oraz wartości p uzyskane w teście U Manna-Whitneya. Porównanie wyników mRS w grupach pacjentów ze spastycznością i bez spastyczności podczas trzech obserwacji: 3, 6 i 12 miesięcy po udarze mózgu.
- Porównanie funkcjonowania w życiu codziennym oceniane za pomocą skali BI chorych ze spastycznością i bez spastyczności
- Porównanie jakości życia chorych po udarze ze spastycznością z jakością życia chorych po udarze bez spastyczności
Porównanie jakości życia pacjentów po udarze mózgu ze spastycznością i jakości życia pacjentów po udarze mózgu bez spastyczności. Wśród pacjentów badanych 3 i 12 miesięcy po udarze mózgu przeprowadzono badanie kwestionariuszowe przy użyciu skali SF-36, oceniającej jakość życia związaną z chorobą. Na podstawie zebranych kwestionariuszy uzyskano wyniki oceny jakości życia w ośmiu obszarach: funkcjonowanie fizyczne, ograniczenia w pełnieniu ról społecznych z przyczyn fizycznych i psychicznych, odczuwanie bólu, ogólne poczucie zdrowia, witalność, funkcjonowanie społeczne i psychiczne. zdrowie. .
W poszczególnych domenach pacjent mógł uzyskać od 0 do 100 punktów, gdzie wyższy wynik oznacza lepszą jakość życia. W przypadku uzyskania wyniku potwierdzającego jednorodność wariancji wykorzystaliśmy test t-Studenta dla dwóch wartości średnich, aby sprawdzić, czy próby pochodzą z tej samej populacji.
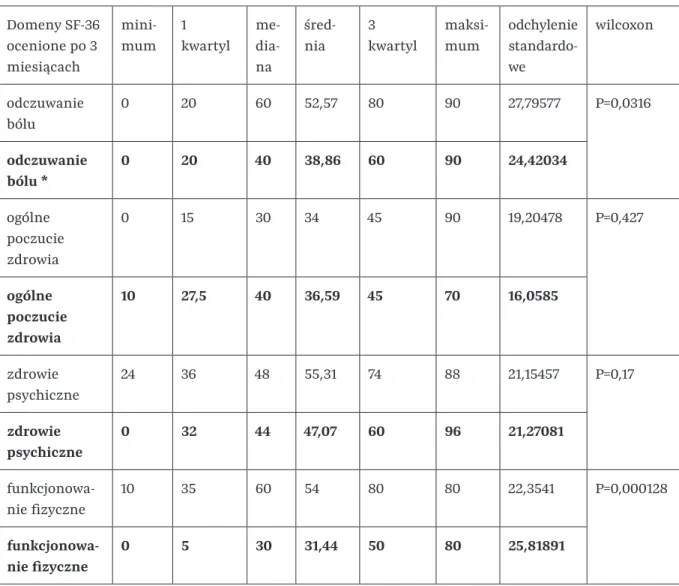
Pogrubieniem oznaczono wyniki grupy ze spastycznością
- miesiącach po 12 miesiącach
- miesiącach po 12 miesiącach
- miesiącach po 12 miesiącach
- miesiącach po 12 miesiącach
- miesiącach po 12 miesiącach
- Korelacje pomiędzy spastycznością a stopniem niedowładu, niesprawności, funk- cjonowaniem w życiu codziennym i jakością życia chorych po udarze
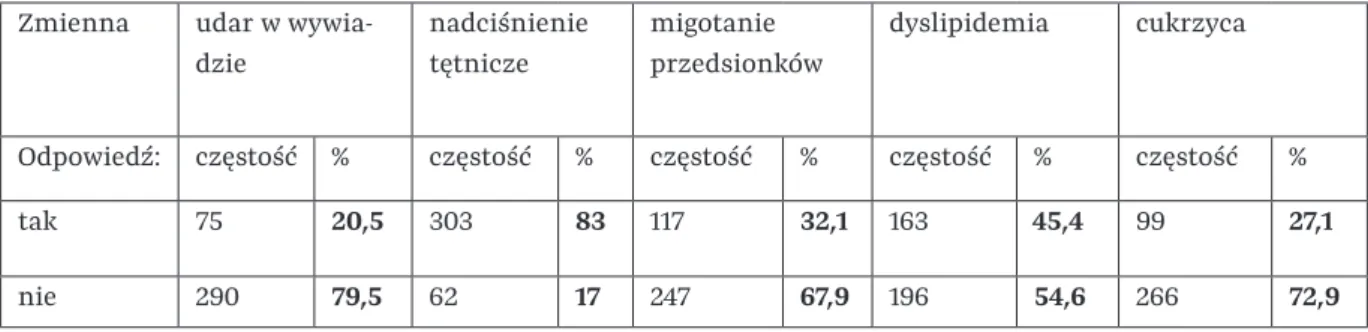
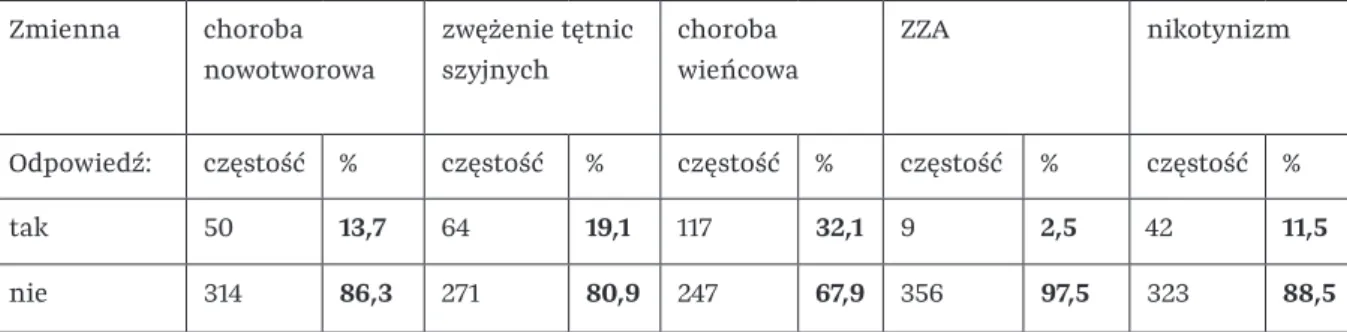
- Demografıczne i kliniczne czynniki ryzyka rozwoju spastyczności po udarze mózgu
Porównanie jakości życia SF-36 w zakresie funkcjonowania fizycznego pacjentów spastycznych i niespastycznych 3 i 12 miesięcy po udarze mózgu. Porównanie jakości życia SF-36 w domenie ograniczeń w rolach społecznych z przyczyn fizycznych u pacjentów ze spastycznością i bez spastyczności oraz artykulacji z przyczyn fizycznych u pacjentów ze spastycznością i bez spastyczności w 3 i 12 miesięcy po udarze mózgu. Porównanie jakości życia w domenie percepcji bólu SF-36 dla pacjentów spastycznych i niespastycznych 3 i 12 miesięcy po udarze.
Porównanie jakości życia witalności SF-36 dla pacjentów spastycznych i niespastycznych 3 i 12 miesięcy po udarze. Porównanie jakości życia zdrowia psychicznego SF-36 dla pacjentów spastycznych i niespastycznych 3 i 12 miesięcy po udarze.
Wyniki wieloczynnikowej regresji logistycznej w celu przewidywania potencjalnej spastyczności 3 miesiące po udarze (model A1) (n=114; AIC=123,03). Istotnymi czynnikami zmniejszającymi ryzyko ewentualnej spastyczności po 6 miesiącach od udaru mózgu są wyższy wynik MRC (OR=0,00034) oraz nikotynizm (OR=0,03). Z kolei istotnymi czynnikami zwiększającymi ryzyko ewentualnej spastyczności po 6 miesiącach od udaru mózgu są dyslipidemia (OR=37,26).
Wyniki wieloczynnikowej regresji logistycznej do przewidywania ewentualnej spastyczności 6 miesięcy po udarze (model A2) (n=93; AIC=55 036). Wyniki wieloczynnikowej regresji logistycznej do przewidywania ewentualnej spastyczności 12 miesięcy po udarze (model A3) (n=90; AIC=46 589).

AIC=113,42)
Wyniki wieloczynnikowej regresji logistycznej do przewidywania umiarkowanej spastyczności 3 miesiące po udarze (Model B1) (n=144; Istotnymi czynnikami zmniejszającymi ryzyko umiarkowanej spastyczności 6 miesięcy po udarze są wyższy wynik MRC (OR=0,009), palenie tytoniu (OR=0,02 ) ) Wyniki wieloczynnikowej regresji logistycznej przewidujące umiarkowaną spastyczność 6 miesięcy po udarze (Model B2) (n=93; AIC=56,70).
Istotnymi czynnikami zmniejszającymi ryzyko wystąpienia umiarkowanej spastyczności po 12 miesiącach od udaru mózgu są wynik w skali (OR=0,02) oraz nikotynizm (OR=0,08). Wyniki wieloczynnikowej regresji logistycznej do przewidywania umiarkowanej spastyczności 12 miesięcy po udarze (model B3) (n=90;

AIC=50,55)
Wyniki wieloczynnikowej regresji logistycznej w celu przewidywania spastyczności wysokiego stopnia 6 miesięcy po udarze (model C2) (n = 93; AIC = 37,24).
AIC=47,95)
PODSUMOWANIE WYNIKÓW
Częstość występowania spastyczności w obu kończynach (górnej i dolnej), w koń- czynie górnej oraz w kończynie dolnej u chorych po udarze mózgu
Występowanie spastyczności obu kończyn (górnej i dolnej), górnej i dolnej u pacjentów po udarze mózgu.
Ewolucja częstości spastyczności w czasie 12 miesięcy obserwacji
Korelacje spastyczności ze stopniem niedowładu, niesprawności, funkcjonowaniem w życiu codziennym i jakością życia chorych po udarze mózgu
W pozostałych domenach, tj. ogólne poczucie zdrowia, funkcjonowanie społeczne i zdrowie psychiczne, jakość życia SF-36 nie korelowała z rozpowszechnieniem i nasileniem spastyczności. Po roku rozpowszechnienie i nasilenie spastyczności było istotnie (rho -0,500, p<0,01) skorelowane z jakością życia SF-36 tylko w domenie funkcjonowania fizycznego. Większy stopień spastyczności wiązał się z gorszą jakością życia pacjentów po udarze w większości domen po 3 miesiącach od udaru, ale głównie w zakresie funkcjonowania fizycznego.
Porównanie pacjentów po udarze mózgu bez spastyczności i ze spastycznością pod względem niesprawności, funkcjonowania w życiu codziennym i jakości życia.
Porównanie chorych po udarze bez spastyczności i ze spastycznością pod względem niesprawności, funkcjonowania w życiu codziennym i jakości życia
Czynniki ryzyka występowania spastyczności po udarze mózgu
DYSKUSJA
- Częstość występowania spastyczności poudarowej
- Wpływ spastyczności na niesprawność i funkcjonowanie w życiu codziennym chorych po udarze mózgu
- Wpływ spastyczności poudarowej na jakość życia
- Predyktory występowania spastyczności po udarze mózgu
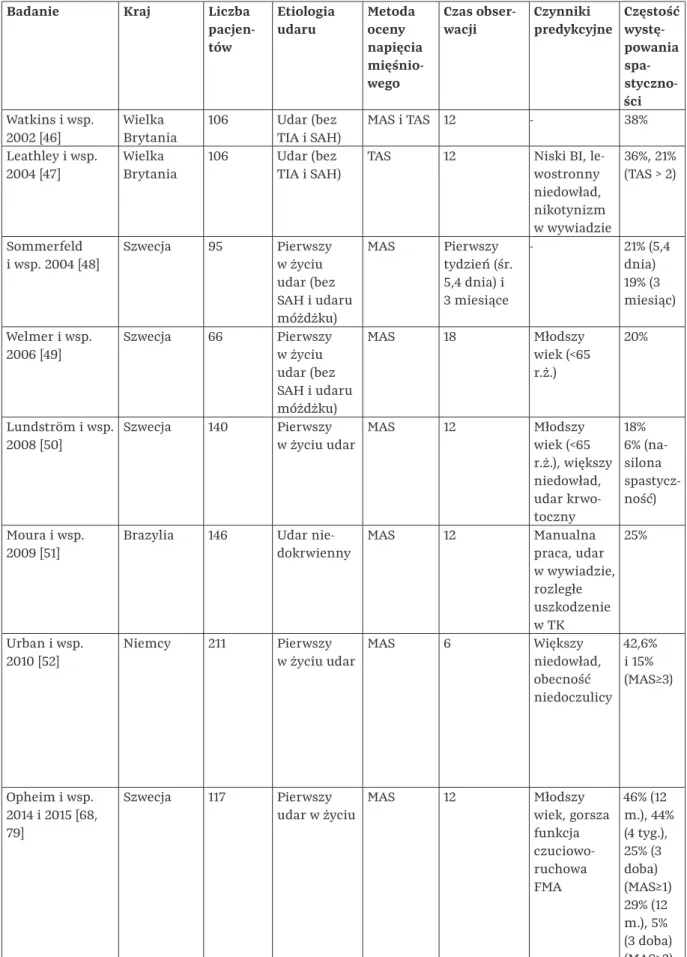
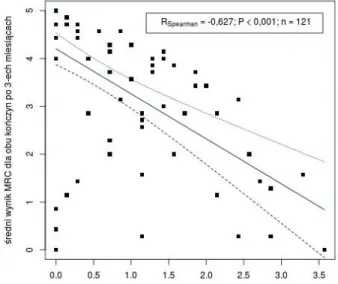
W brazylijskim badaniu [51] częstość występowania spastyczności wynosiła 25% rok po udarze, ale wśród pacjentów z niedowładem połowiczym na początku badania częstość występowania spastyczności była wyższa (36–38%). W naszym badaniu większy stopień spastyczności wiązał się z większym stopniem niedowładu zarówno kończyn górnych, jak i dolnych. W trakcie rocznej obserwacji obserwowano coraz istotniejsze korelacje między nasileniem niedowładu a występowaniem spastyczności (r=-0,62 po 3 miesiącach oraz r=-0,92 i -0,93 po 6 i 12 miesiącach od udaru).
Jest to jeden z powodów, dla których niedowład kończyn wysokiego stopnia (MRC = 0-1) opisywany podczas hospitalizacji na oddziale udarowym okazał się silnym predyktorem spastyczności. W dwóch prospektywnych badaniach na dużej grupie pacjentów ciężki niedowład był istotnym i bardzo silnym predyktorem wystąpienia jakiejkolwiek i ciężkiej spastyczności po 6 i 12 miesiącach od udaru mózgu [50,52].
WNIOSKI
Gdy porównano chorych po udarze mózgu ze spastycznością z chorymi po udarze bez spastyczności, ci pierwsi mieli istotnie większą niesprawność i gorsze funkcjono-
Spastyczność poudarowa istotnie korelowała z niesprawnością i funkcjonowaniem w życiu codziennym chorych po udarze mózgu ocenianych przy pomocy skal BI i mRS
Porównanie chorych po udarze mózgu ze spastycznością z chorymi po udarze bez spastyczności pod względem jakości życia ocenianej za pomocą skali SF-36 pokazało
Spastyczność poudarowa istotnie korelowała z jakością życia mierzoną za pomocą ska- li SF-36 w następujących domenach: funkcjonowania fızycznego, odczuwania bólu, ogra-
Wśród najistotniejszych predyktorów występowania spastyczności poudarowej w rocznej obserwacji znalazły się: stopień nasilenia niedowładu, młodszy wiek chorych,
PIŚMIENNICTWO
Lance J.W. Pathophysiology of spasticity and clinical experience with baclofen
Jóźwiak M. Kliniczna ocena spastyczności – metodyka badania ortopedycznego
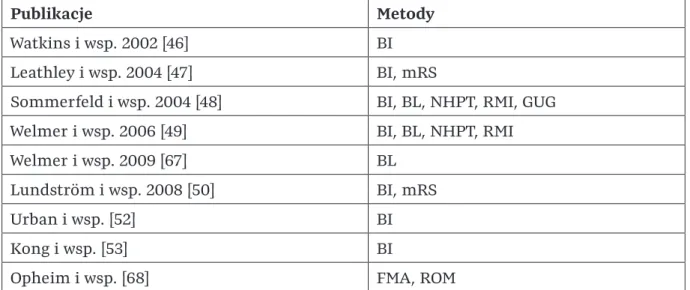
Spasticity and its association with functioning and health-related quality of life 18 months after stroke. The negative impact of spasticity on the health-related quality of life of stroke survivors. Location and severity of spasticity in the first 1–2 weeks and at 3 and 18 months after stroke.
Upper limb spasticity in the first year after stroke: a longitudinal study at the University of Gothenburg (SALGOT). Early prediction of long-term upper limb spasticity after stroke: part of the SALGOT study.
SPIS TABEL, WYKRESÓW I RYCIN
Średnie wyniki MRC osobno dla kończyn górnych i dolnych w grupie badanej 3 miesiące po udarze mózgu. Średnie wyniki MRC dla obu kończyn (górnej i dolnej) w grupie wyjściowej i badanej 3 i 6 miesięcy po udarze. Średnie wyniki MRC osobno dla kończyn górnych i dolnych w grupie badanej 3 i 6 miesięcy po udarze.
Średnie wyniki MRC dla obu kończyn (górnej i dolnej) w grupie wyjściowej i badanej po 3, 6 i 12 miesiącach od udaru. Średnie wyniki MRC osobno dla kończyn górnych i dolnych w badanej grupie po 3, 6 i 12 miesiącach od udaru.
Ryciny
ANEKS
1a. Stan przytomności 0 - przytomny
Ruchomość gałek ocznych (skojarzone spojrzenie) 0 – prawidłowa
Siła mięśni kończyny górnej
Siła mięśni kończyny dolnej
Ataksja kończyn 0 - nieobecna
Przemieszczanie się z wózka do łóżka i z powrotem
Chodzenie po schodach
Ubieranie się (w tym zapinanie guzików, wiązanie sznurowadeł itp.)
2 - Niewielka niepełnosprawność: Brak możliwości wykonywania wszystkich dotychczasowych czynności, ale zdolność do samodzielnej opieki.