Jörg Harloff für die wertvolle Hilfe und Ideen im Rahmen dieser Arbeit und für die Übernahme der Zweitmeinung. Außerdem möchte ich mich bei Markus Karsch, Thomas Jantz und Jonas Bresien für die gute Zusammenarbeit und das gute Arbeitsklima bedanken. Besonders danken möchte ich Markus für die Einarbeitung in dieses Thema und für seine tatkräftige Unterstützung im Laboralltag.
An dieser Stelle möchte ich mich auch bei allen anderen Mitgliedern der Arbeitsgruppe für den freundlichen Empfang und die vielen unterstützenden Helfer bedanken. Ein großes Dankeschön geht auch an die Analytik des Hauses und LIKAT für die gute und reibungslose Zusammenarbeit.
Zielsetzung
Grundlagen - Schwach koordinierende Anionen
- Allgemeines
- Borate
- Carborate
- Alkyloxy- und Aryloxymetallate
- Teflate
- Addukt-Anionen
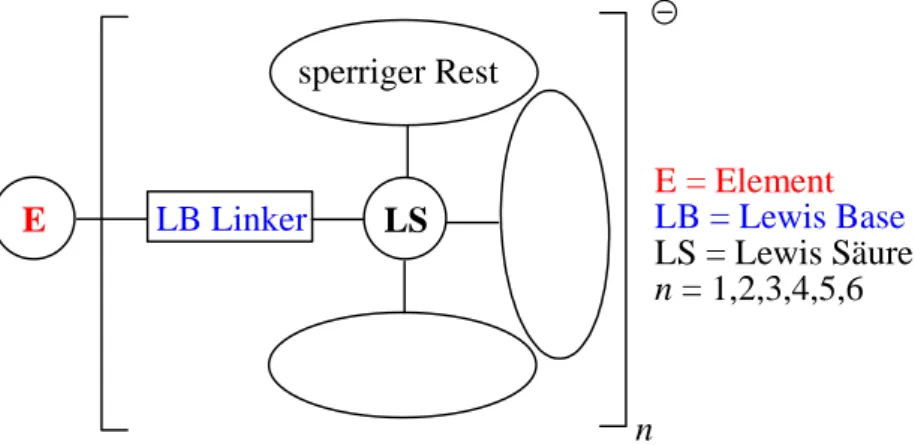
Eine weitere Synthesestrategie für schwach koordinierende Anionen besteht in der Reaktion eines Lewis-Base-Anions mit einer neutralen Lewis-Säure, um schwach koordinierende Lewis-Säure-Lewis-Base-Addukt-Anionen zu erhalten. stellten 1999 Anionen des Typs [(F5C6)3B(μ-X)B(C6F5)3]– (X = CN, NH2) her und veröffentlichten sie. [42,43] Darüber hinaus konnte das Boran-Addukt des Imidazolylanions erhalten wurden. [44], [45] Aufbauend auf dieser Arbeit konnte die Schulz-Gruppe im Jahr 2009 neue Lewis-Säure-Lewis-Base-Addukt-Anionen basierend auf dem folgenden Konzept entwickeln. Die Substitution der H-Atome durch Lewis-Baselinker führt zu den Grundstrukturen, die jedoch aufgrund ihrer hohen Nukleophilie noch nicht zu den WCAs gehören.
Als Kernelemente wurden Bor, Kohlenstoff und Stickstoff verwendet, und CN-Gruppen wurden als Lewis-Base-Linker gewählt. Zwischen dem Element und dem Lewis-Base-Linker wurde ein Substituent eingeführt, um noch sperrigere Adduktanionen zu erzeugen.
![Abbildung 1: Molekülstruktur des [B(C 6 F 5 ) 4 ] – als Vertreter der Borat-Anionen als Überlagerung einer ball-and-stick- und einer space-filling-Darstellung](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/14.892.272.618.254.582/abbildung-molekülstruktur-vertreter-borat-anionen-überlagerung-filling-darstellung.webp)
Ergebnisse und Diskussion
- Einleitung
- Darstellung und Charakterisierung von Li[B(C 6 H 4 -I) 4 ]
- Darstellung und Charakterisierung von K[B(C 6 H 4 -CN) 4 ] durch Pd-katalysierte
- Versuch der Darstellung von Li[B(C 6 H 4 -CN) 4 ] durch Umsetzung von Li[B(C 6 H 4 -
Die Ausbeute in diesem Experiment betrug etwa 46 %; die in der Literatur[50] genannte Ausbeute von 85 % wurde nicht erreicht. Es war weder aus konzentriertem THF noch aus gesättigter Dichlormethanlösung bei −40 °C möglich, Einkristalle für die Röntgenstrukturanalyse zu züchten, und in der Literatur wurden noch keine Ergebnisse einer Röntgenstrukturanalyse veröffentlicht. NMR: Das 1H-NMR-Spektrum zeigt ein Dublett aus zwei chemisch äquivalenten m-Protonen, die jeweils mit den o-Protonen bei 7,29 ppm paaren, und ein Septett aus chemisch äquivalenten o-Protonen, die mit beiden m-Protonen paaren und auch paaren mit dem 11B-Kern (I = 3/2) bei 6,88 ppm im Integralverhältnis 1:1.
Das 13C-NMR-Spektrum zeigt ein 1:1:1:1-Quartett der vier chemisch äquivalenten Kohlenstoffkerne, die bei 161,1 ppm direkt an das Bor gebunden sind, mit der Kopplungskonstante 1JC-B. Das Signal bei 134,3 ppm (C-2) spaltet sich in ein Quartett auf und ist das Ergebnis der 2JC-B-Kopplung mit einer Kopplungskonstante von 2,7 Hz. Das 11B-NMR-Spektrum zeigt nur ein scharfes Singulett bei -7,30 ppm, was im typischen Bereich für vierfach koordiniertes Bor liegt.
Die Werte stimmen sehr gut mit den Literaturwerten überein.[50] Außerdem wurde ein 19F-NMR-Spektrum erstellt, das zeigte, dass das Produkt kein LiF mehr enthielt. Das K[B(C6H4-CN)4] konnte dann durch Festkörperextraktion mit heißem Acetonitril gewonnen werden, wobei in der Kälte ein gräulicher Feststoff, höchstwahrscheinlich Rückstände des Katalysators, ausfiel. Selbst nachdem die Extraktion viermal wiederholt und jedes Mal der Feststoff abgetrennt wurde, fiel in der Kälte immer noch ein bräunlich-grauer Feststoff aus.
NMR: Das 1 H-NMR-Spektrum zeigt erneut das Dublett der m-Protonen bei 7,44 ppm (3JH-H = 7,9 Hz) und das Septett der o-Protonen bei 7,22 ppm, die im Vergleich zu Li[B(C6H4) leicht tieffeldverschoben sind -I)4] stehen im ganzzahligen Verhältnis von 1:1. Das Singulett im 11B-NMR-Spektrum liegt bei -6,37 ppm, etwas tiefer im Feld im Vergleich zum Signal von Li[B(C6H4-I)4], aber immer noch im Bereich vierfach koordinierter Borkerne. Rosenmund-von-Braun“-Synthese analog zu einer Veröffentlichung von Hoskins und Robson aus dem Jahr 1990, in der das isoelektronische Tetrakis(4-cyanophenyl)methan C(C6H4-CN)4 durch Reaktion von C(C6H4-Br)4 mit CuCN synthetisiert wird. vorgestellt.[52]
- Einleitung
- Darstellung und Charakterisierung von I-C 6 H 4 -CN
- Umsetzung von BF 3 ·OEt 2 mit I-C 6 H 4 -CN und n-BuLi
- Darstellung und Charakterisierung von Li[HO-B(C 6 H 4 -CN) 3 ]
NMR: Im 1H-NMR-Spektrum werden zwei Dubletts der Protonen o und m mit jeweils m und CN unter Verwendung eines Äquivalents n-BuLi, das das aromatische System durch einen Metall-Halogen-Austausch lithiiert, und BF3-Ethern (BF3 OEt2) hinzugefügt (5,5 Äq.). Diethylether ist hierfür ungeeignet, da die Löslichkeit von I-C6H4-CN bei -70 °C stark abnimmt und eine Suspension entsteht.
NMR: Im 11B-NMR-Spektrum des Acetonitril-Extrakts ist kein Bor-Signal zu erkennen, im 11B-NMR-Spektrum der verschiedenen Fraktionen sind drei dicht beieinander liegende Borsignale im Bereich vierfach koordinierter Borkerne zu erkennen. Dies sollte in Analogie zu einer Veröffentlichung von Liu und Tilley erfolgen, denen es gelang, durch Reaktion von Br-C6H4-CN mit n-BuLi und SiCl4 isovalensäurehaltiges Si(C6H4-CN)4 herzustellen.[56]Br -C6H4-CN ist im Handel günstiger erhältlich als das I-C6H4-CN. Für den Herstellungsversuch von Li[B(C6H4-CN)4] wurde 4-Iodbenzonitril I-C6H4-CN mit einem Äquivalent n-BuLi lithifiziert und im Molverhältnis 4:1 mit BCl3 (54,7 % Lösung in) behandelt n-Hexan) hinzugefügt.
NMR: Im 1H-NMR-Spektrum ist bei 1,28 ppm ein Singulett zu erkennen, das dem OH-Proton zugeordnet werden kann. Ein Vergleichswert aus der Literatur für das Salz [Et3NH][HO-B(C6F5)3] ergibt eine chemische Verschiebung von 2,47 ppm für das Proton der Hydroxylgruppe in CDCl3.[57] Allerdings hängt die Lage des Signals auch stark vom gewählten Lösungsmittel ab, da Wasserstoffbrücken zu einer schwächeren Abschirmung der Protonen und damit zu einer Feldverschiebung führen. Dies wird auch in vielen anderen Veröffentlichungen bestätigt.[58] Im 11B-NMR-Spektrum ist ein scharfes Signal bei -1,63 ppm zu erkennen, das auf einen vierfach koordinierten Borkern hinweist.
Um diesen mutmaßlichen Mechanismus zu verifizieren, wurde ein 11B-NMR-Spektrum der Reaktionslösung gemessen, der Li-C6H4-CN im Überschuss (5 Äquiv.) zugesetzt wurde. an das Borzentrum koordiniert, wie in der Literatur ebenfalls beschrieben.[42b] Die Position spricht auch für ein Addukt, ein Vergleichswert der chemischen Verschiebung von 3,3 ppm findet sich für THF·B(C6F5)3.[59 ] Die Das Signal liegt daher näher an diesem Wert als der Literaturwert für K[B(C6H4-CN)4] von -5,92 ppm.[50] Anschließend wurde versucht, die Reaktivität des Addukts zu erhöhen, indem man die Lösung, der noch kein Wasser zugesetzt worden war, mehrere Stunden lang unter Rückfluss erhitzte, es wurde jedoch keine Veränderung im 11B-NMR-Spektrum beobachtet. Es wurde auch versucht, die Reaktivität von Li-C6H4-CN durch Zugabe des Chelatliganden TMEDA zu erhöhen, der die Nukleophilie des aromatischen Kohlenstoffs durch Komplexierung von Lithium erhöhen sollte, um den nukleophilen Angriff auf Bor zu ermöglichen.
![Abbildung 11: ORTEP-Darstellung der Molekülstruktur von Li[HO-B(C 6 H 4 -CN) 3 ]](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/32.892.157.736.111.493/abbildung-ortep-darstellung-molekülstruktur-li-ho-b-cn.webp)
- Einleitung
- Darstellung und Charakterisierung von [NEt 4 ][H{HO-B(C 6 H 4 -CN) 3 } 2 ]
- Darstellung und Charakterisierung von [PPh 4 ][HO-B(C 6 H 4 -CN) 3 ]
- Darstellung und Charakterisierung von [BMIm][HO-B(C 6 H 4 -CN) 3 ]
- Darstellung und Charakterisierung von [EMIm][HO-B(C 6 H 4 -CN) 3 ]
- Versuch zur Darstellung des Ag[HO-B(C 6 H 4 -CN) 3 ]
NMR: Im 1H-NMR-Spektrum ist neben einem Singulett bei 1,36 ppm, das dem OH-Proton zugeordnet werden kann, im aromatischen Bereich ein „Quartett“ des AA'BB'-Systems zu beobachten. Darüber hinaus ist bei 3,20 ppm ein Quartett der CH2-Protonen in den Ethylgruppen zu sehen, das sich mit den drei Methylprotonen verbindet. Das den Methylprotonen zugeordnete 1,15-ppm-Signal spaltet sich aufgrund der Kopplung mit den CH2-Protonen einerseits und der Kopplung mit dem 14N-Kern (I = 1) andererseits in ein Triplett von Tripletts auf.
Darüber hinaus ist bei 2,18 ppm ein Singulett zu erkennen, das möglicherweise dem freien Proton H1a zugeordnet werden kann, das von zwei Hydroxylgruppen koordiniert wird. Das 11B-NMR-Spektrum zeigt eine scharfe Resonanz bei -1,58 ppm, was im gleichen Bereich wie der des Lithiumsalzes liegt. NMR: Im 1H-NMR-Spektrum ist neben einem Singulett bei 1,35 ppm, das dem OH-Proton zugeordnet werden kann, im aromatischen Bereich ein „Quartett“ des AA'BB'-Systems zu beobachten.
Weitere Multipletts bei 7,96 und 7,77 ppm können den aromatischen Protonen der Phenylringe am Phosphor zugeordnet werden. Das 11B-NMR-Spektrum zeigt eine scharfe Resonanz bei -1,70 ppm, die im gleichen Bereich wie die des Lithiumsalzes liegt und auf einen vierfach koordinierten 11B-Kern hinweist. Das BMIm-Kation zeigt zusätzliche Signale im 1H-Spektrum: Das Signal bei 9,23 ppm wird dem aromatischen Proton (H(C-7)) zugeordnet.
Im 11B-NMR-Spektrum ist ein scharfes Signal bei -1,74 ppm zu erkennen, das wie das Lithiumsalz im Bereich vierfach koordinierter 11B-Kerne liegt. Das EMIm-Kation zeigt zusätzliche Signale im 1 H-Spektrum: Das Signal bei 9,11 ppm wird dem aromatischen Proton (H(C-7)) zugeordnet. Im 11B-NMR-Spektrum ist ein scharfes Signal bei -1,65 ppm zu erkennen, das wie das Lithiumsalz im Bereich vierfach koordinierter 11B-Kerne liegt.
![Abbildung 16: ORTEP-Darstellung der Molekülstruktur von [[NEt 4 ][H{HO-B(C 6 H 4 -CN) 3 } 2 ]](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/40.892.168.725.123.597/abbildung-ortep-darstellung-molekülstruktur-net-h-ho-cn.webp)
Zusammenfassung und Ausblick
Arbeitstechnik
Analysemethoden
SADABS).[63] Alle Nichtwasserstoffatome wurden anisotrop verfeinert, Wasserstoffatome wurden in idealisierten Positionen berechnet, mit Ausnahme der der OH-Gruppe, die frei verfeinert wurde. Chemische Verschiebungen werden in ppm angegeben und tragen ein positives Vorzeichen, was einer Abwärtsverschiebung relativ zum Standard entspricht. Als externer Standard wurde für die 11B-Messung B(OH)3 und für die 31P-Messung jeweils 85 %iges wässriges H3PO4 mit δRef = 0 ppm verwendet.
Zur Aufnahme der Infrarotspektren wurde ein Nicolet 380 FT-IR-Spektrometer mit einer Smart Orbit ATR-Einheit verwendet. Kohlenstoff-, Wasserstoff- und Stickstoffanalysen der Proben wurden mit einem C/H/N/S-Analysator (Thermoquest Flash EA 1112) durchgeführt. Im Fall von Li[HO-B(C6H4-CN)3] wurde der Zersetzungspunkt optisch mit einem EZ-Melt von Stanford Research Systems bestimmt.
Darstellung und analytische Daten zu den Verbindungen
- Lithium-Tetrakis(4-iodophenyl)borat Li[B(C 6 H 4 -I) 4 ]
- Kalium-Tetrakis(4-cyanophenyl)borat K[B(C 6 H 4 -CN) 4 ]
- Lithium-Hydroxytris(4-cyanophenyl)borat Li[HO-B(C 6 H 4 -CN) 3 ]
- Tetraphenylphosphonium-Hydroxytris(4-cyanophenyl)borat
Li[B(C6H4-I)4] kann durch anschließende dreimalige Feststoffextraktion mit 20 mL Dichlormethan und Trocknen im Hochvakuum bei 200 °C als farbloser Feststoff gewonnen werden. Nach Abtrennung durch Filtration über eine G4-Fritte, Abdampfen des Lösungsmittels und Trocknen bei 80 °C im Hochvakuum erhält man einen bräunlich-grauen Feststoff. Das gewünschte Produkt kann dann durch Sublimation im Hochvakuum (0,005 mbar) und 70 °C als zunächst hellgelber Feststoff erhalten werden, der nach der zweiten Sublimation farblos ist.
Zu dieser Suspension wird unter Rühren portionsweise eine Lösung von 0,190 g (0,557 mmol, 1 Äquiv.) Li[HO-B(C6H4-CN)3] in 20 ml THF gegeben, wodurch sich die Suspension nahezu vollständig auflöst. Durch Einengen des Filtrats und Trocknen im Hochvakuum entsteht als Rohprodukt ein Feststoff, der dreimal mit je 20 ml entionisiertem Wasser gewaschen wird, um noch vorhandenes LiCl abzutrennen. Nach dem Trocknen bei 100°C im Hochvakuum erhält man das gewünschte Produkt als farblosen bis leicht gelblichen Feststoff.
Das Lösungsmittel wurde unter Hochvakuum verdampft und 10 ml THF wurden zu dem farblosen bis leicht gelblichen viskosen Material gegeben, was zu einer Suspension führte, die filtriert wurde, um ungelöstes LiCl zu entfernen. Nach Trocknen des Filtrats bei 100 °C im Hochvakuum erhält man einen farblosen Feststoff mit sehr geringer Dichte. Das Lösungsmittel wurde im Hochvakuum verdampft und 15 ml THF zugegeben, was zu einer Suspension führte, die filtriert wurde, um ungelöstes LiCl zu entfernen.
Nach dem Trocknen des Filtrats bei 100 °C im Hochvakuum erhält man eine farblose bis leicht gelbliche, sehr viskose Substanz. Durch Zugabe von 5 ml Diethylether als Treibmittel und anschließendes erneutes Trocknen bei 100°C im Hochvakuum erhält man einen farblosen, stellenweise leicht gelblichen Feststoff. Durch dreimaliges Extrahieren des Feststoffs mit je 20 ml Dichlormethan und anschließendes Trocknen zunächst bei 100 °C und anschließend bei 160 °C im Hochvakuum erhält man eine farblose, sehr viskose Substanz.
Anhang
- Daten zur Einkristallröntgenstrukturanalytik
- Abbildungsverzeichnis
- Gleichungsverzeichnis
- Schemataverzeichnis
- Tabellenverzeichnis
- Literaturverzeichnis
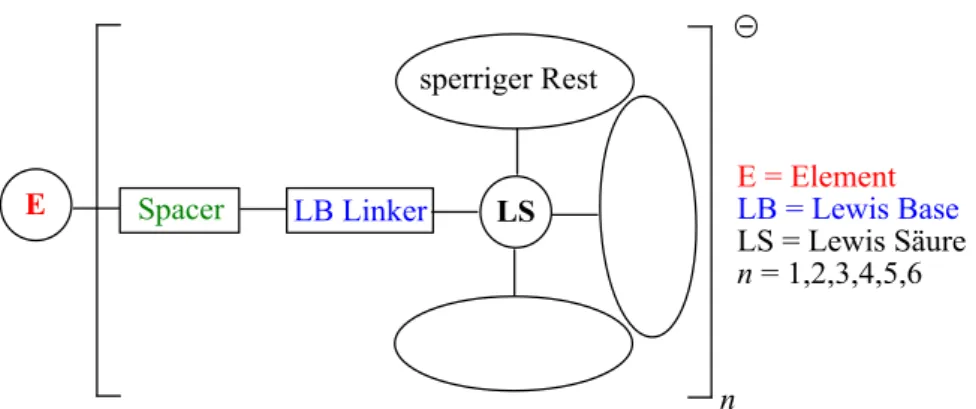
9 Abbildung 8: Konzept zur Darstellung schwach koordinierender, um einen Spacer verlängerter Lewis-Säure-Lewis-Base-Addukt-Anionen. 10 Abbildung 10: [B(C6H4-CN·B(C6F5)3)4]- als Zielanion für diese Arbeit, analog zur Darstellung des erweiterten Konzepts der schwachen Koordination von Lewis-Säure-Lewis-Base-Addukt-Anionen.
![Tabelle 2: Daten zur Einkristallröntgenstrukturanalytik der Verbindung [NEt 4 ][H{HO-B(C 6 H 4 - -CN) 3 } 2 ]](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/64.892.151.777.138.969/tabelle-daten-einkristallröntgenstrukturanalytik-verbindung-net-h-ho-cn.webp)
![Abbildung 2: Molekülstruktur des [CB 11 F 12 ] – als Vertreter der Carborat-Anionen als Überlagerung einer ball-and-stick- und einer space-filling-Darstellung](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/15.892.347.553.352.566/abbildung-molekülstruktur-vertreter-carborat-anionen-überlagerung-filling-darstellung.webp)
![Abbildung 3: Molekülstruktur des [Al(OC(CF 3 ) 3 ) 4 ] – als Vertreter der Alkyloxymetallate als Überlagerung einer ball-and-stick- und einer space-filling-Darstellung](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/16.892.289.603.412.772/abbildung-molekülstruktur-vertreter-alkyloxymetallate-überlagerung-stick-filling-darstellung.webp)
![Abbildung 4: Molekülstruktur des [Sb(OTeF 5 ) 6 ] – als Vertreter der Teflat-basierten Anionen als Überlagerung einer ball-and-stick- und einer space-filling-Darstellung](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/17.892.273.619.581.896/abbildung-molekülstruktur-vertreter-teflat-basierten-anionen-überlagerung-darstellung.webp)
![Abbildung 5: Molekülstruktur des [Sb 2 F 11 ] – als Vertreter der Addukt-Anionen als ball-and-stick- Darstellung](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/18.892.207.730.434.795/abbildung-molekülstruktur-vertreter-addukt-anionen-ball-stick-darstellung.webp)
![Abbildung 7: Molekülstruktur des dca_2b-Anions in K[dca_2b], des tcm_3b-Anions in [K(18-crown- [K(18-crown-6)][tcm_3b] und des tcb_4b-Anions in [K(Et 2 O)4][tcb_4b] als Überlagerung von ball-and-stick- und space-filling-Darstellungen](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/20.892.123.774.115.362/abbildung-molekülstruktur-anions-anions-anions-überlagerung-filling-darstellungen.webp)
![Abbildung 9: Schematische Darstellung der Fragmente Al(O-C 6 H 4 -CN·B(C 6 F 5 ) 3 ) 3 (links) und Na[(F 5 C 6 ) 3 B·O-C 6 H 4 -CN·B(C 6 F 5 ) 3 ] (rechts)](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/21.892.111.774.198.585/abbildung-schematische-darstellung-fragmente-al-cn-na-cn.webp)
![Abbildung 10: [B(C 6 H 4 -CN·B(C 6 F 5 ) 3 ) 4 ] – als Zielanion dieser Arbeit analog zur Darstellung des erweiterten Konzeptes für schwach koordinierende Lewis-Säure-Lewis-Base-Addukt-Anionen](https://thumb-eu.123doks.com/thumbv2/1library_info/19311194.0/22.892.227.660.500.727/abbildung-zielanion-arbeit-darstellung-erweiterten-konzeptes-koordinierende-anionen.webp)