ESTUDO COMPARATIVO DA AÇÃO DA TOXINA
BOTULÍNICA TIPO A E DA CROTOXINA SOBRE AS
CÉLULAS SATÉLITES DA MUSCULATURA EXTRÍNSECA
OCULAR EM MODELO ANIMAL
Belo Horizonte
Marta Halfeld Ferrari Alves Lacordia
ESTUDO COMPARATIVO DA AÇÃO DA TOXINA
BOTULÍNICA TIPO A E DA CROTOXINA SOBRE AS
CÉLULAS SATÉLITES DA MUSCULATURA EXTRÍNSECA
OCULAR EM MODELO ANIMAL
Tese apresentada ao Curso de Pós-Graduação em
Medicina, área de Oftalmologia, da Faculdade de Medicina
da Universidade Federal de Minas Gerais, como requisito
parcial à obtenção do grau de Doutor em Medicina.
Orientador: Prof. Dr. Henderson Celestino de Almeida
Co-orientador: Prof. Dr. Geraldo de Barros Ribeiro
Belo Horizonte
L143e Lacordia, Marta Halfeld Ferrari Alves
Estudo comparativo da ação da toxina botulínica tipo A e da croto- xina sobre as células satélites da musculatura extrínseca ocular em mo- delo animal. / Marta Halfeld Ferrari Alves Lacordia. – 2007.
140 f.
Orientador: Henderson Celestino de Almeida Co-orientador: Geraldo de Barros Ribeiro
Tese (doutorado) – Universidade Federal de Minas Gerais. Facul- dade de Medicina.
1. Músculos oculomotores. 2. Células satélites de músculo esquelé- tico. 3. Toxina botulínica Tipo A. 4. Crotoxina 5. Estudo comparativo 6. Animais. I. Almeida, Henderson Celestino de. II. Ribeiro, Geraldo de Barros. III. Universidade Federal de Minas Gerais. Faculdade de Me- dicina. IV. Título.
NLM: WW 400
UNIVERSIDADE FEDERAL DE MINAS GERAIS
Reitor
Prof. Ronaldo Tadêu Pena
Pró-Reitor de Pós-Graduação Prof. Jaime Arturo Ramirez
Pró-Reitor de Pesquisa
Prof. Carlos Alberto Pereira Tavares
Diretor da Faculdade de Medicina Prof. Francisco José Penna
Diretora do Hospital das Clínicas Profª. Tânia Mara Assis Lima
Coordenador do Centro de Pós-Graduação da Faculdade de Medicina Prof. Carlos Faria Santos Amaral
Coordenador do Curso de Pós-Graduação em Oftalmologia Prof. Joel Edmur Boteon
Chefe do Departamento de Oftalmologia e Otorrinolaringologia Profª. Ana Rosa Pimentel de Figueiredo
Membros do Colegiado do Curso de Pós-Graduação em Medicina, área de Oftalmologia Prof. Fernando Oréfice
Prof. Henderson Celestino de Almeida Prof. Homero Gusmão de Almeida Prof. Joel Edmur Boteon
Prof. Márcio Bittar Nehemy Prof. Marco Aurélio Lana Peixoto Prof. Sebastião Cronemberger Sobrinho
DEDICATÓRIA
Ao meu pai, Amaury, pelo amor incondicional e pelo exemplo de vida, de caráter
e de força.
À minha mãe, Dalva, também pelo amor, carinho e apoio constantes.
À minha irmã, Mírian, pela amizade e pela maneira de estar sempre presente na
minha vida, apesar da distância geográfica.
Ao meu irmão, Mauro, pelo modelo de dedicação aos estudos e à profissão.
Ao meu marido, Roberto, pelo amor, pelo companheirismo e por nunca ter me
deixado desistir.
E especialmente à minha filha, Raquel, que veio junto com este meu sonho,
trazendo mais alegria para a minha vida.
Eu te quero a todo instante Nem mil alto-falantes Vão poder falar por mim. Eu não existo longe de você E a solidão é meu pior castigo Eu conto as horas Pra poder te ver Mas o relógio tá de mal comigo
AGRADECIMENTOS
A Deus, por ter me poupado a vida e por ter me dado forças para continuar minha
missão.
Ao Professor Dr. Henderson Celestino de Almeida, pelo incentivo, pela dedicação,
pelo carinho e por ter contribuído tanto para meu aprimoramento científico e para a realização
deste grande sonho.
Ao Professor Dr. Geraldo de Barros Ribeiro, pela disponibilidade, pela competência,
pela simplicidade e por sua extraordinária orientação.
Ao Dr. Carlos Henrique Reis de Araújo Silva, médico veterinário e diretor da
Faculdade de Ciências da Saúde da Universidade Presidente Antônio Carlos (UNIPAC
Campus VI – Juiz de Fora), pelo grande auxílio prestado no desenvolvimento deste trabalho,
pela excelência e pelo profissionalismo.
Ao Dr. Raul Fernando Binato Lamim e à Dra. Maria do Carmo Jordão Coelho,
professores adjuntos do Departamento de Patologia da Faculdade de Medicina da
Universidade Federal de Juiz de Fora, pelo auxílio no estudo imunoistoquímico.
Ao Dr. Márcio José Martins Alves, professor adjunto do Departamento de Saúde
Coletiva da Faculdade de Medicina da Universidade Federal de Juiz de Fora, pela dedicação e
pela disponibilidade em ajudar na realização deste estudo.
À Dra. Maria de Lourdes Motta Moreira Villas Boas, por ter despertado em mim o
gosto pelo estudo do estrabismo e pelo privilégio de tê-la como amiga.
Ao Dr. Galton Carvalho Vasconcelos, pelos constantes incentivos.
Ao Professor Dr. Joel Edmur Boteon, coordenador do Curso de Pós-Graduação em
Oftalmologia da Faculdade de Medicina da UFMG, por ter acreditado em mim e por ter me
Ao Professor Dr. Márcio Bittar Nehemy, subcoordenador do Curso de Pós-Graduação
em Oftalmologia da Faculdade de Medicina da UFMG, pelos incentivos desde a minha
residência médica no Instituto Hilton Rocha e pelas gentilezas que lhe são peculiares.
A Rosemary Rodrigues Silva e a Maria do Rosário Pompéia de Aquino, secretárias do
Departamento de Oftalmologia e Otorrinolaringologia da Faculdade de Medicina da UFMG,
por terem sempre sido prestativas, acolhedoras, carinhosas e bem humoradas.
Ao Dr. Rafael Vidal Mérula, pelo apoio, pela amizade, pelos desabafos, pelos
estímulos e por ter entendido verdadeiramente o significado desta tese para mim.
À Dra. Juliana Lambert Oréfice, pelo coleguismo, pelo exemplo e pelo apoio.
Ao Laboratório de Anatomia Patológica da Santa Casa de Misericórdia de Juiz de Fora
e, em especial, a Débora Tavares Grizendi, pelo trabalho de preparação das lâminas.
À Universidade Federal de Juiz de Fora, por ter contribuído para a realização desta
etapa tão importante na minha vida profissional.
À UNIPAC (Faculdade de Medicina Veterinária), por ter cedido o espaço físico para a
realização do experimento com coelhos.
Ao Cleber Ornelas e à Beth Halfeld, por terem me hospedado com muito carinho
durante o curso do doutorado, incentivando-me a todo o momento. À Dona Cleonice, à Karla,
ao Pierre, à Renata, ao Nélson e a todos os familiares, pela torcida. Aos meus lindinhos
Alberto, Bernard, Henrique, Manuela, Pedro e Gustavo, por conseguirem, juntamente com
Aos amigos:
Se alguma coisa me consome e me envelhece é que a roda furiosa da vida não me permite ter sempre ao meu lado, morando comigo, andando comigo, falando comigo, vivendo comigo, todos os meus amigos, e, principalmente os que só desconfiam ou talvez nunca vão saber que são meus amigos!
Vinícius de Moraes
Cristine Sotto-Maior (pela generosidade), Ronaldo (merci beaucoup), Monica (companheira de estrada), Cristiana, Martinha e família (tão importantes para mim, desde
minha residência no Instituto Hilton Rocha), Christiane Marie (“meu anjo da guarda”), Eliane,
Carla, Angelina e Cleide (pela ajuda nos momentos mais críticos), Rubens, Ema, Dale (thank you), Regina Beluco, Lucianno e Hélio De Maria (amigos da pós-graduação), Dilourdes, Neide e Lúcia Gerhein (minha torcedora fiel e sempre presente) e todos aqueles que de
Dias inteiros de calmaria, noites de ardentia, dedos no leme e olhos no horizonte, descobri a alegria de transformar distâncias em tempo. Um tempo em que aprendi a entender as coisas do mar, a conversar com as grandes ondas e não discutir com o mau tempo. A transformar o medo em respeito, o respeito em confiança. Descobri como é bom chegar quando se tem paciência. E para chegar, onde quer que seja, aprendi que não é preciso dominar a força, mas a razão. É preciso, antes de mais nada, querer.
Amyr Klink
RESUMO
Lacordia MHFA. Estudo comparativo da ação da toxina botulínica tipo A e da crotoxina sobre
as células satélites da musculatura extrínseca ocular em modelo animal. Tese [Doutorado].
Belo Horizonte: Faculdade de Medicina da Universidade Federal de Minas Gerais; 2007.
Introdução: Quando ocorre uma lesão muscular, as células satélites tornam-se ativas,
dividem-se e reparam as fibras lesadas ou formam novas miofibras. Ao contrário da
musculatura esquelética, que é pós-mitótica, os músculos extrínsecos oculares apresentam-se
em contínua renovação celular, devido às células satélites. O tratamento cirúrgico do
estrabismo visa equilibrar as forças geradas pelos músculos oculares extrínsecos, porém
compromete a dinâmica muscular normal e, inevitavelmente, provoca cicatrizes,
incomitâncias e, ocasionalmente, estrabismos secundários. A necessidade de se descobrir um
tratamento farmacológico para o estrabismo que não cause enfraquecimento muscular
permanente, mas que tenha uma duração maior que a da toxina botulínica, estimula a
comunidade científica a pesquisar novas substâncias. Estudos recentes verificaram que a
crotoxina é capaz de induzir uma paralisia transitória em músculo reto superior de coelhos e
que sua ação e seu efeito foram semelhantes aos da toxina botulínica do tipo A.
Objetivo: Avaliar o efeito da toxina botulínica do tipo A e da crotoxina na ativação de células
satélites das fibras musculares de músculos retos superiores de coelhos.
Material e métodos: Os músculos retos superiores do olho direito de 29 coelhos machos
albinos neozelandeses foram inoculados com toxina botulínica do tipo A, ou com crotoxina,
em diferentes doses. Os músculos retos superiores contralaterais de cada coelho foram
inoculados com solução salina em volume igual ao das toxinas. Os animais foram sacrificados
retos superiores intactos. Cada músculo foi preparado para análise imunoistoquímica, com
marcadores de células satélites – Myo D e PCNA. Foi realizada contagem dos núcleos
corados pelos marcadores a cada cem miofibras.
Resultados: A aplicação de toxina botulínica e de crotoxina provocou um aumento no
número de células satélites ativadas e em proliferação nos músculos retos superiores dos
coelhos. A inoculação de solução salina nos músculos contralaterais não causou aumento
significativo. Uma maior ativação celular foi observada após a aplicação de crotoxina embora,
estatisticamente, a diferença do efeito de ativação entre os grupos botox e crotoxina não tenha
sido considerável. Nos grupos botox e crotoxina, não houve correlação estatisticamente
significativa entre a dose e o aumento na ativação das células. Da mesma forma, não foi
encontrada correlação entre o volume de substância aplicada e a ativação celular nos grupos
botox, crotoxina e controle. O tempo de vida após a aplicação contribuiu para o aumento de
células satélites ativadas em todos os grupos. No estudo histológico, o grupo crotoxina
revelou acentuado desarranjo na arquitetura das fibras musculares e mais evidências de
regeneração.
Conclusão: A observação de maior desorganização na estrutura muscular e de sinais de
regeneração mais evidentes no grupo crotoxina parece estar correlacionada ao aumento de
células satélites ativadas. Supõe-se que o processo de regeneração das fibras musculares após
a aplicação da crotoxina seja mais lento que após a aplicação da toxina botulínica, o que
explicaria a ação mais duradoura da crotoxina.
Palavras-chave: Células satélites. Toxina botulínica do tipo A. Crotoxina. Estrabismo.
ABSTRACT
Lacordia MHFA. A comparative study of the effects of type A botulinum toxin and crotoxin
on satellite cells of extraocular muscles in rabbits. Thesis (Doctorate) Belo Horizonte:
Faculdade de Medicina da Universidade Federal de Minas Gerais; 2007.
Introduction: When muscle lesions occur, the satellite cells spring into action, by dividing
and either repairing damaged fibers or forming new myofibers. Unlike skeletal muscle which
is postmitotic, the extraocular muscles are in a continuous process of cellular regeneration,
due to these satellite cells. Surgical treatment of strabismus attempts to balance the forces
generated by extraocular muscles. However, this procedure modifies the normal muscle
dynamics and unavoidably causes scarring, incomitant gaze and, occasionally, secondary
strabismus. The need to discover pharmacological treatment for strabismus, which does not
cause permanent muscle weakening, but has a longer lasting effect than botulinum toxin, has
stimulated the scientific community to seek alternative substances. Recent studies have
verified that crotoxin was successful in inducing temporary paralysis in the superior rectus
muscles of rabbits and that its action and effects were similar to those produced by botulinum
toxin A.
Purpose: To evaluate the effect of botulinum toxin A and crotoxin on satellite cell activation
in the muscle fibers of superior rectus muscles of rabbits.
Material and Methods: The superior rectus muscles in the right eyes of 29 male, albino,
New Zealand rabbits were inoculated with different doses of botulinum toxin A or crotoxin.
The contra-lateral superior rectus muscles in each rabbit were inoculated with the same
volume of saline solution only. The animals were sacrificed either 12, 18 or 25 days after the
Subsequently, each muscle was prepared for immunohistochemical analysis, using satellite
cell markers – Myo D and PCNA. The positive nuclei, revealed by the markers in each 100
myofibers, were counted.
Results: The application of the botulinum toxin A and crotoxin triggered a more significant
increase satellite cell activation and proliferation in right superior rectus muscles in rabbits
when compared with a saline solution inoculation in the contralateral muscles. Greater cell
activation was observed after crotoxin application, although, statistically, the difference in the
effects of this activation between the botox and crotoxin groups was not significant. There
was no statistically significant correlation between the dose applied and resulting cell
activation in the botox and crotoxin groups. Similarly, no correlation was found between the
volume of the applied substance and cell activation in the botox, crotoxin and control groups.
Post-application survival time contributed to the increase in activated satellite cells in all
groups. Histological examination revealed more accentuated disorganization in muscle fibre
architecture and more evidence of regeneration in the crotoxin group.
Conclusion: The observed increase in disorganization in the muscle structure together with
more obvious signs of regeneration in the crotoxin group suggests a correlation with the
increase in satellite cell activation. It may be concluded that the process of muscle-fibre
regeneration after the crotoxin application is slower than that which occurs after the
botulinum toxin A application, which may explain the longer lasting action of crotoxin.
Key words: Satellite cells. Botulinum toxin A. Crotoxin. Strabismus. Muscle-fibre
Lista de ilustrações
Figura 1- Desenho esquemático ilustrando a organização do músculo estriado
esquelético...9
Figura 2- Diagrama ilustrando a estrutura e a posição dos filamentos finos e grossos do
sarcômero...9
Figura 3- Estrutura dos tecidos conectivos orbitários e suas relações com as camadas de
fibras musculares...11
Figura 4- Desenho esquemático de uma célula satélite quiescente envolta pela lâmina basal e
pelo sarcolema da miofibra justaposta...14
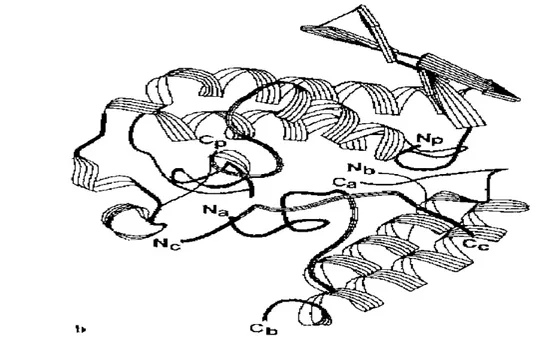
Figura 5- Modelo computacional da estrutura da crotoxina...34
Figura 6- Aplicação de toxina no músculo reto superior do olho direito de
coelho...44
Figura 7- Fase final da aplicação de toxina no músculo reto superior do olho
direito...44
Figura 8- Globo ocular de coelho enucleado...48
Figura 9- Lâmina preparada para análise imunoistoquímica ...52
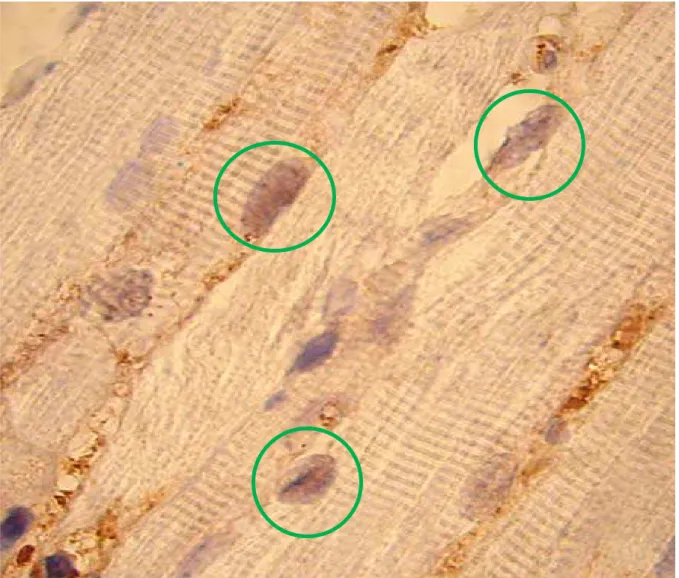
Figura 10- Corte longitudinal do músculo reto superior de um coelho, submetido à marcação
pelo anticorpo anti- Myo D...53
Figura 11- Corte longitudinal do músculo reto superior de um coelho, submetido à marcação
pelo anticorpo anti- PCNA...54
Figura 12- Ptose palpebral discreta em olho direito do coelho 12...60
Figura 13- Ptose palpebral moderada em olho direito do coelho 23...60
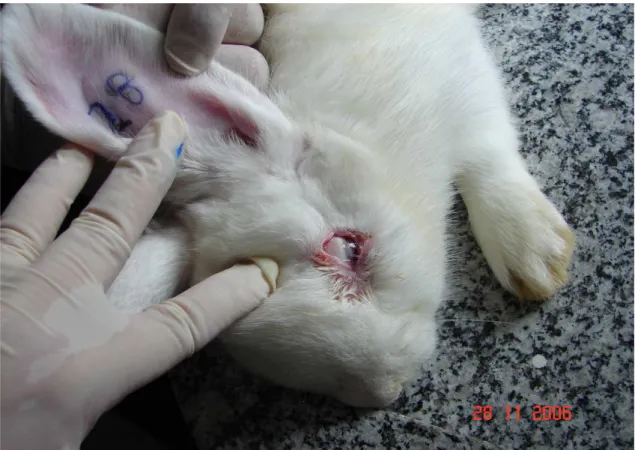
Figura 14- Coelho 28 com lesão na pálpebra inferior esquerda causada por provável
Figura 15- Corte histológico de área do músculo reto superior normal de coelho (aumento
de 100 vezes, corado pela hematoxilina-eosina)...101
Figura 16 - Corte histológico de área do músculo reto superior normal de coelho (corte
transversal, aumento de 100 vezes, corado pela hematoxilina-eosina)...101
Figura 17- Corte histológico do músculo reto superior do olho esquerdo do
coelho1...102
Figura 18 - Corte histológico de área do músculo reto superior do olho esquerdo do coelho
2...102
Figura 19 - Corte histológico de músculo reto superior do olho direito do coelho
6...103
Figura 20- Corte histológico de área do músculo reto superior do olho direito do coelho
6...103
Figura 21- Corte histológico do músculo reto superior do olho direito do coelho
7...104
Figura 22 - Corte histológico do músculo reto superior do olho direito do coelho
7...104
Figura 23 - Corte histológico do músculo reto superior do olho direito do coelho
7...105
Figura 24 - Corte histológico do músculo reto superior do olho direito do coelho
7...105
Figura 25 - Corte histológico do músculo reto superior do olho direito do coelho
7...106
Figura 26- Corte histológico de músculo do reto superior do olho direito do coelho
Figura 27- Corte histológico do músculo reto superior do olho direito do coelho
9...107
Figura 28- Corte histológico de área do músculo reto superior do olho direito do coelho
15...107
Figura 29- Corte histológico de área do músculo reto superior do olho direito do coelho
15...108
Figura 30- Corte histológico de área do músculo reto superior do olho direito do coelho
15...108
Figura 31- Corte histológico de músculo reto superior do olho direito coelho
16...109
Figura 32 - Corte histológico do músculo reto superior do olho direito do coelho
19...109
Figura 33 - Corte histológico de área do músculo reto superior do olho direito do coelho
20...110
Figura 34 - Corte histológico de área do músculo reto superior do olho direito do coelho
20...110
Figura 35 - Corte histológico do músculo reto superior do olho direito do coelho
21...111
Figura 36 - Corte histológico do músculo reto superior do olho direito do coelho
23...111
Figura 37 - Corte histológico do músculo reto superior do olho direito do coelho
23...112
Figura 38 - Corte histológico de área do músculo reto superior do olho direito do coelho
Figura 39 - Corte histológico de área do músculo reto superior do olho direito do coelho
25...113
Figura 40 - Corte histológico de área do músculo reto superior do olho direito do coelho
25...113
Figura 41 - Corte histológico de área do músculo reto superior do olho direito do coelho
25...114
Figura 42 - Corte histológico de área do músculo reto superior do olho direito do coelho
25...114
Figura 43 - Corte histológico de área do músculo reto superior do olho direito do coelho
25...115
Figura 44 - Corte histológico do músculo reto superior do olho esquerdo do coelho
25...115
Figura 45- Esquema dos estágios de regeneração da reparação
muscular...86
Lista de tabelas
Tabela 1- Núcleos corados e total de núcleos em cada grupo (botox e controle)...100
Tabela 2- Núcleos corados e total de núcleos em cada grupo (crotoxina e controle)...100
Tabela 3-Percentuais de núcleos corados pelo Myo D e PCNA nos grupos controle, botox e crotoxina...63
Tabela 4- Percentuais de núcleos corados pelo Myo D e PCNA nos grupos botox e
crotoxina...66
Tabela 5- Percentuais de núcleos corados pelo Myo D e pelo PCNA nos grupos de acordo com as doses...67
Tabela 6- Percentuais de núcleos corados pelo Myo D e pelo PCNA nos grupos de acordo com os volumes...71
Lista de quadros
Quadro 1- Ações dos músculos oculomotores a partir da posição primária do olhar...7
Quadro 2- Distribuição dos coelhos em grupos...43
Quadro 3- Toxina botulínica aplicada no músculo reto superior do olho direito dos coelhos 1 a 14...45
Quadro 4- Crotoxina aplicada no músculo reto superior do olho direito dos coelhos 15 a 29...46
Quadro 5- Relação dos dias em que foram realizadas as eutanásias dos coelhos, coelhos sacrificados e número de olhos enucleados...47
Quadro 6- Ocorrência de ptose palpebral no olho direito dos coelhos após a aplicação de toxina botulínica e de crotoxina...59
Quadro 7- Alterações histológicas de cada músculo reto superior em que foram aplicados Botox® 10 U e solução salina em igual volume...80
Quadro 8- Alterações histológicas de cada músculo reto superior em que foram aplicados Botox® 5 U e solução salina em igual volume...80
Quadro 9- Alterações histológicas de cada músculo reto superior em que foram aplicados Botox® 2,5 U e solução salina em igual volume...81
Quadro 11- Alterações histológicas de cada músculo reto superior em que foram aplicadas crotoxina 5 U e solução salina em igual volume...82
Diagrama
Diagrama 1-Representação gráfica das variáveis do presente estudo...56
Lista de gráficos
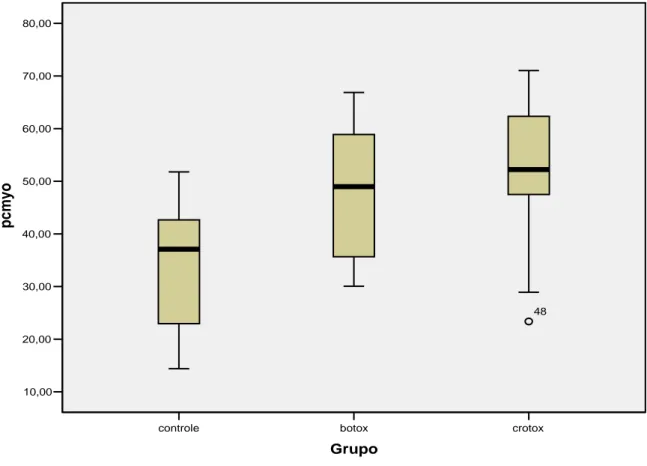
Gráfico 1- Representação em box-plot dos percentuais de núcleos de CS ativados e marcados pelo Myo D...64
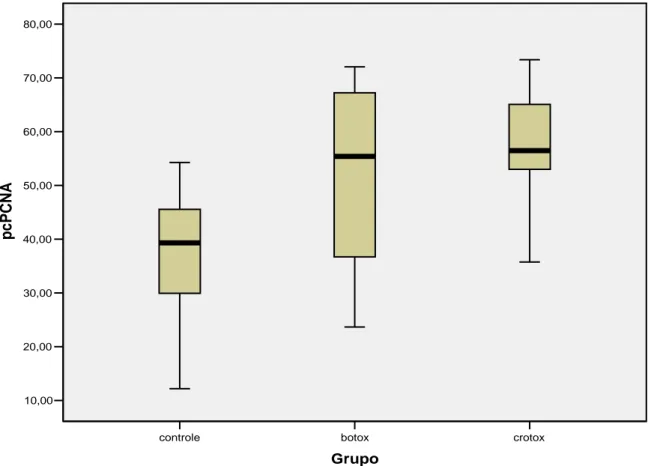
Gráfico 2- Representação em box-plot dos percentuais de núcleos de CS ativados e marcados pelo PCNA...65
Gráfico 3-Diagrama de dispersão representando a correlação entre a dose (U) e o percentual de núcleos ativados marcados pelo Myo D...68
Gráfico 4- Diagrama de dispersão representando a correlação entre a dose (U) e o percentual de núcleos ativados marcados pelo PCNA...69
Gráfico 5- Diagrama de dispersão representando a correlação entre o volume (ml) e o
percentual de núcleos ativados marcados pelo Myo D...72
Gráfico 6-Diagrama de dispersão representando a correlação entre o volume (ml) e o
percentual de núcleos ativados marcados pelo PCNA...73
Gráfico 7- Diagrama de dispersão representando a correlação entre os dias de vida após a aplicação e o percentual de núcleos ativados marcados pelo Myo
D...76
Gráfico 8- Diagrama de dispersão representando a correlação entre os dias de vida após a aplicação e o percentual de núcleos ativados marcados pelo
PCNA...77
Lista de abreviaturas, siglas e símbolos
ANOVA- análise de variância
Brd U- bromodeoxiuridina
°C- grau Celsius
CETEA- Comitê de Ética em Experimentação Animal
CICS- crotoxin inhibitor from Crotalus serum
COBEA- Colégio Brasileiro de Experimentação Animal
Crtx- crotoxina
CS- células satélites
DAB- diaminobenzidina
DFP- di-isopropil-fluor-fosfato
DL-50- dose letal em 50% dos animais inoculados
EUA- Estados Unidos da América
FDA- Food and Drug Administration
FGF- fibroblast growth factor
FUNED- Fundação Ezequiel Dias
g- grama
GB- grupo botox
GC- grupo controle
GCrtx- grupo crotoxina
H0- hipótese de nulidade
HGF- hepatocyte growth factor
IGF - I- insulin-like growth factor I
IL-6- interleucina 6
kDa- quilodalton
kg- quilograma
LIF- leukemia inhibitory factor
M- mol
mg- miligrama
MG- Minas Gerais
MIFs- multiply innervated muscle fibers (fibras de contração lenta) ml- mililitro
MOE- músculos oculares extrínsecos
Myo D- myogenic determination gene D
μg- microgramas
nº- número
N-CAM- neural cell adhesion molecule
OD- olho direito
OE- olho esquerdo
p- nível de significância
PBS- phosphate-buffered saline
PCNA- proliferating cell nuclear antigen
pH- potencial de hidrogênio iônico
PR- Paraná
r- coeficiente de correlação
SIFs- singly innervated muscle fibers (fibras de contração rápida) SP- São Paulo
TGF- - transforming growth factors
U- unidade
UFMG- Universidade Federal de Minas Gerais
UNIPAC- Universidade Presidente Antônio Carlos
%- percentual
®- marca registrada
™- marca comercial
SUMÁRIO
1 INTRODUÇÃO...1 2 REVISÃO DA LITERATURA...5 2.1 Musculatura ocular externa e células satélites...6 2.1.1 Anatomia dos músculos oculares extrínsecos...6 2.1.1.1 Aspectos macroscópicos...6 2.1.1.2 Organização celular...8 2.1.1.3 Tipos de fibras da musculatura extrínseca ocular...10 2.1.2 Células Satélites...13 2.1.2.1 Identificação das células satélites musculares...15
2.1.2.2 Marcadores para células satélites...15 2.1.2.3 Distribuição e quantificação das células satélites...17
2.1.2.4 Fatores de crescimento como reguladores das células satélites..18 2.1.2.5 Respostas funcionais das células satélites a estímulos
fisiológicos...21 2.1.2.5.1 Estímulo hipertrófico...21 2.1.2.5.2 Estímulo atrófico...22 2.1.2.5.3 Envelhecimento...23 2.1.2.6 Respostas funcionais e estados de doença...23
2.1.2.7 Modelos de regeneração muscular...24 2.1.3 Particularidades da musculatura ocular extrínseca...24
2.3.2 Estrutura...34
2.3.3 Mecanismo de ação...34 2.3.4 Imunologia da crotoxina...36 2.3.5 Utilização da crotoxina...36
3 OBJETIVOS...38 4 MATERIAIS E MÉTODOS...40 4.1 Estudos anatomopatológico e imunoistoquímico...47 4.2 Metodologia estatística...55 5 RESULTADOS...58 5.1 Análise estatística dos dados...62 5.1.1 Comparação das médias entre os grupos independentemente dos
co-fatores...62 5.1.1.1 Comparação com o grupo controle...62 5.1.1.2 Comparação sem o grupo controle...66 5.1.2 Avaliação da influência dos co-fatores nos grupos...67 5.1.2.1 Comparação entre a dose e a resposta...67 5.1.2.2 Comparação entre o volume e a resposta...70 5.1.2.3 Comparação entre os dias de vida após a aplicação e a resposta.74
1 Introdução
O estrabismo é um desalinhamento dos olhos, freqüentemente associado à hiper ou à
hipofunção de músculos oculares extrínsecos. Quando surge na infância, pode causar
ambliopia e incapacidade visual permanente; quando surge na fase adulta, pode acarretar
diplopia.
O objetivo do tratamento cirúrgico do estrabismo é equilibrar as forças musculares, de
maneira que, na presença de impulsos motores eferentes anormais, o alinhamento binocular
normal possa ser alcançado ou mantido. Normalmente, um ou mais músculos oculares
extrínsecos são fortalecidos ou enfraquecidos, o que altera o comprimento do músculo
(ressecção) ou a inserção do músculo no globo ocular (retrocesso). (1, 2)
Embora eficaz na mudança da posição rotacional do globo ocular, a cirurgia
compromete a dinâmica muscular normal. O arco de contato com o globo ocular, a
elasticidade intrínseca dos músculos envolvidos na cirurgia, a tensão latente no
agonista/antagonista e a contração muscular mudam após a cirurgia. Além disso, tal
procedimento inevitavelmente provoca cicatrizes que podem alterar a função do músculo
ocular extrínseco. Ressecções e retrocessos amplos podem resultar em incomitâncias e,
ocasionalmente, em estrabismos secundários. (1)
Em 1977, Scott começou a utilizar a toxina botulínica do tipo A para a correção do
estrabismo em seres humanos. A toxina foi aprovada para uso clínico na década de 1980 e
tem sido utilizada eficazmente para o enfraquecimento de músculos hiperfuncionantes no
estrabismo de crianças e adultos, o que mostra que a idéia de um tratamento medicamentoso
para o estrabismo é possível. A toxina botulínica gera um enfraquecimento do músculo em
que é aplicada, sem alterar sua inserção e sem causar as cicatrizes e/ou fibroses que um
Outras toxinas e outras substâncias começam a ser estudadas com o objetivo de se
aprimorar o tratamento do estrabismo.
A crotoxina, principal neurotoxina do veneno da cobra cascavel sul-americana
Crotalus durissus terrificus, atua como bloqueador neuromuscular. Ribeiro (2001) avaliou, em coelhos, a ação e a aplicabilidade da crotoxina na indução da paralisia da musculatura
extrínseca ocular, comparando seus efeitos com os da toxina botulínica do tipo A. (5)
As fibras musculares esqueléticas dos mamíferos adultos não são substituídas nem
remodeladas sem que haja algum processo de crescimento ou trauma. Entretanto, tais
músculos possuem uma população quiescente de células progenitoras, conhecidas como
células satélites. Após um trauma, essas células tornam-se ativas e dividem-se, promovendo,
assim a regeneração do músculo lesado. (6)
As células satélites foram identificadas e descritas pela primeira vez por Mauro, em
1961, como células intimamente associadas à periferia de fibras musculares de rãs. Tal
denominação se deve a sua localização anatômica. (7)
Em 2002, McLoon et al. utilizando marcadores específicos, demonstraram a existência de células satélites ativadas na musculatura extrínseca ocular de mamíferos, incluindo
coelhos, macacos e humanos. (8, 9) McLoon e Wirtschafter (2003) identificaram, em macacos
e humanos adultos, células satélites ativadas em miofibras de músculos extrínsecos oculares
que não haviam sofrido qualquer trauma. (9) Ugalde et al. (2005) estudaram o efeito da paralisia induzida pela toxina botulínica nas fibras musculares remodeladas de músculos
extrínsecos oculares de coelhos. (10) O aumento de células satélites nos músculos retos de
coelhos submetidos à ressecção foi verificado por Christiansen e McLoon, em 2006. (11)
comparados com os músculos oblíquos inferiores de pacientes sem história de estrabismo.
(12)
A compreensão do efeito dos procedimentos cirúrgicos, assim como da utilização de
toxinas na ativação de células satélites musculares, é útil para o aperfeiçoamento do
tratamento do estrabismo.
Este estudo tem o propósito de verificar comparativamente o efeito da aplicação da
toxina botulínica do tipo A e da crotoxina sobre as células satélites de músculos retos
superiores de coelhos, o que poderá ajudar na investigação da ação dessas toxinas e na
2 Revisão da literatura
2.1 Musculatura ocular externa e células satélites
2.1.1 Anatomia dos músculos oculares extrínsecos
2.1.1.1 Aspectos macroscópicos
Os músculos oculares extrínsecos (MOE) exercem uma função importante para a
visão, promovendo não só um ajuste estático para o alinhamento binocular, necessário para se
obter a fusão e a estereopsia, como também movimentos dinâmicos precisos, importantes para
adquirir e manter a visão foveal, independentemente da movimentação da cabeça e do corpo.
(2)
Os MOE e suas ações a partir da posição primária do olhar estão resumidos no
QUADRO 1. (2)
Os quatro músculos retos originam-se de um anel tendinoso, o anel de Zinn, que
envolve o forame óptico e uma porção da fissura orbital superior, circundando o nervo óptico.
(2, 13) Eles inserem-se na esclera, perto do limbo, a distâncias crescentes em relação a este,
partindo do reto medial (RM) em direção horária e formando uma espiral imaginária chamada
espiral de Tillaux.
O músculo oblíquo superior também se origina do anel de Zinn, no ápice da órbita.
Entretanto, sua origem funcional é a tróclea, situada na porção súpero-medial, próxima à
borda orbitária. Nos humanos, o músculo é tendinoso após passar por esse anel
temporal súpero-posterior do globo ocular. O músculo oblíquo inferior origina-se da parede
medial da órbita e insere-se no quadrante temporal ínfero-posterior do globo ocular. (2, 13)
QUADRO 1
Ações dos músculos oculomotores a partir da posição primária do olhar
O III nervo craniano (nervo oculomotor) inerva os músculos reto medial, reto
superior, reto inferior e oblíquo inferior. O IV nervo craniano (nervo troclear) inerva o
oblíquo superior. O VI nervo craniano (nervo abducente), inerva o reto lateral. (2, 13)
As artérias musculares provêm dos ramos musculares medial e lateral da artéria
oftálmica e dirigem-se anteriormente, pelos corpos dos músculos retos. A partir das inserções
dos músculos retos, percorrem um curto trajeto pela episclera e, denominando artérias ciliares
anteriores, perfuram a esclera e passam a constituir importantes vias de irrigação para o
segmento anterior do olho. Cada músculo reto possui duas artérias musculares, exceto o reto
lateral, que possui apenas uma. (2)
Músculo Ação primária Ação secundária
Reto medial Adução ---
Reto lateral Abdução ---
Reto superior Elevação Adução, inciclodução
Reto inferior Depressão Adução, exciclodução
Oblíquo superior Inciclodução Depressão, abdução
2.1.1.2 Organização celular
Embora a musculatura ocular extrínseca difira em vários aspectos da musculatura
esquelética típica, algumas características são comuns. (13)
O músculo é envolvido por uma membrana de tecido conjuntivo chamada
epimísio. Do epimísio, partem septos muito finos de tecido conjuntivo, que se dirigem para o
interior do músculo, dividindo-o em fascículos. Esses septos são denominados perimísios.
Cada fibra muscular, por sua vez, é envolvida por uma camada muito fina de fibras
reticulares, formando o endomísio. (13)
A fibra muscular é delimitada por uma membrana, o sarcolema. O seu citoplasma
(sarcoplasma) é preenchido principalmente por fibrilas paralelas, as miofibrilas, que
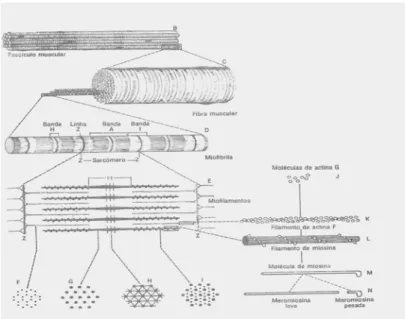
correspondem ao tecido contrátil. (FIGURA 1) (13, 14)
As miofibrilas possuem estriações que alternam zonas claras (bandas I) e escuras
(bandas A). No centro de cada banda I, aparece uma linha transversal escura – a linha Z. A
banda A apresenta uma zona mais clara no centro – a banda H, que possui uma linha escura
central, chamada banda M. (13, 14)
A unidade contrátil da miofibrila chama-se sarcômero e localiza-se entre duas
linhas Z sucessivas. Quando estimulado, o sarcômero contrai-se pela aproximação das bandas
FIGURA 1: Desenho esquemático ilustrando a organização do músculo estriado esquelético. À direita, esboço de um músculo do qual foi retirado um segmento, representado na figura maior, à esquerda.
Fonte: Junqueira LC, Carneiro J. Histologia básica. 5ª edição. Rio de Janeiro: Guanabara Koogan; 1982.
FIGURA 2: Diagrama ilustrando a estrutura e a posição dos filamentos finos e grossos do sarcômero.
As miofibrilas do músculo estriado contêm pelo menos quatro proteínas principais:
miosina, actina, tropomiosina e troponina. Os filamentos grossos são formados de miosina, e
as outras três proteínas são encontradas nos filamentos finos. (14)
A miosina e a actina, juntas, representam 55% do total de proteínas do músculo
estriado. (14)
A força contrátil de um músculo é gerada pela interação da miosina e da actina. As
bandas I (regiões claras) são compostas de filamentos finos (actina); as bandas A (escuras)
são compostas de filamentos espessos (miosina) e de filamentos finos (actina) interpostos. A
banda H apresenta apenas filamentos espessos. (13, 14)
A contração muscular é estimulada por impulsos nervosos que levam à liberação
de cálcio do retículo sarcoplasmático, gerando mudanças nas interações entre as pontes de
ligação formadas entre a porção globular da molécula de miosina e a molécula de actina. Isso
resulta no deslizamento dos filamentos finos sobre os espessos. A banda A permanece com o
mesmo tamanho, e as bandas I e Z diminuem de tamanho quando ocorre contração. (14)
2.1.1.3 Tipos de fibra da musculatura extrínseca ocular
As miofibras da musculatura ocular externa são derivadas do mesoderma,
enquanto o tecido conectivo adjacente e a musculatura lisa da órbita são derivados da crista
neural. (2, 15, 16)
A miogênese dos músculos estriados oculares ocorre em duas fases: primária e
secundária. (2, 15)
Cedo, na primeira etapa da miogênese, na 11ª semana de gestação, os tecidos
associações com as condensações de mioblastos que irão formar os MOE. Os tecidos
conectivos perioculares desenvolvem-se posteriormente, por volta da segunda etapa da
miogênese. O desenvolvimento dos MOE induz a inervação pelos nervos cranianos
correspondentes. (2)
A musculatura ocular externa é classicamente dividida em duas camadas distintas.
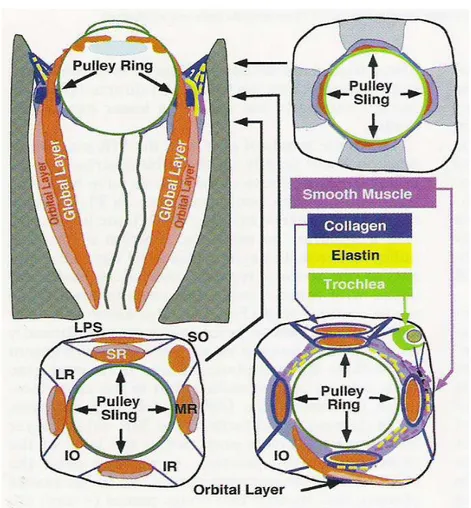
(FIGURA 3) A camada orbital periférica estende-se ao longo da superfície muscular,
faceando a parede da órbita. Essa camada circunda outra, a camada global, próxima ao globo
ocular. (13, 16, 17, 18, 19) Uma zona intermediária entre as camadas orbital e global tem sido
descrita. (2)
FIGURA 3: Estrutura dos tecidos conectivos orbitários e suas relações com as camadas de fibras musculares. IO: oblíquo inferior; IR: reto inferior; LPS: elevador da pálpebra superior; LR: reto lateral; MR: reto medial; SO: oblíquo superior; SR: reto superior.
A camada orbital contém fibras de diâmetro menor, com numerosas mitocôndrias
e abundantes vasos. A camada global contém fibras de diâmetro maior, com variável
conteúdo mitocondrial e poucos vasos. (16)
A camada global existe por toda a extensão de cada músculo reto, desde a origem,
no ápice da órbita, até a continuidade com o tendão, que se insere no globo. (2) A porção
média do músculo (correspondente à região entre a terminação anterior das miofibras no
tendão e sua origem posterior no ápice da órbita) contém de 8 280 a 16 374 fibras, com
variação discreta entre os quatro músculos retos. (17)
Na porção média da camada orbital, o número de fibras varia amplamente de
acordo com o músculo reto considerado, sendo maior no músculo reto medial (de 7 845 a 14
991 fibras) e menor no músculo reto superior (de 5 119 a 9 367 fibras). (2, 17)
As fibras da camada orbital não são contíguas com as inserções esclerais, pois se
inserem nas polias dos respectivos músculos. (19)
Estudos anatômicos recentes confirmaram que cada músculo reto passa através de
uma polia, que consiste em um anel (ou uma bainha) de colágeno, localizado próximo ao
equador do globo ocular, na fáscia de Tenon. (18)
No mínimo seis tipos diferentes de fibras musculares foram identificados nos
músculos oculares. Esses tipos podem ser divididos em duas categorias principais: fibras
musculares de contração lenta e fibras musculares de contração rápida. (20) Pela classificação
de Siebeck e Krüger (1955), as fibras de contração lenta são aquelas com inervação múltipla
(multiply innervated muscle fibers - MIFs) e são chamadas de “Felderstruktur”; as fibras de contração rápida são inervadas por terminações nervosas simples (singly innervated muscle fibers - SIFs) e denominadas de “Fibrillenstruktur”. (13, 20, 21)
As fibras de contração rápida (SIFs) são o tipo de fibra muscular que constitui
apresentam contração total, que se propaga ao longo de toda fibra. São inervadas por nervos
relativamente grandes (de 7 a 11 μm), que terminam como uma grande placa motora no terço
central do músculo. (20)
As fibras de contração lenta (MIFs) são incomuns em mamíferos, ocorrendo
apenas em músculos oculares, na laringe e em músculos do ouvido médio. Entretanto, são
comuns em músculos de anfíbios. Elas são resistentes à fadiga e respondem ao estímulo
elétrico com uma contração tônica lenta que se propaga ao longo da fibra muscular. São
inervadas por fibra nervosa mielinizada, usualmente de calibre fino (de 3 a 5 μm). As placas
motoras são tipicamente pequenas e estão distribuídas ao longo de toda a fibra, mas têm uma
concentração maior na metade distal do músculo. (13, 20)
A camada orbital dos MOE contém dois tipos de fibras musculares.
Aproximadamente 80% das fibras são de contração rápida e 20% são de contração lenta. (2,
13)
A camada global possui um tipo de fibra de contração lenta e três tipos de fibra de
contração rápida. (2)
2.1.2 Células satélites
Em 1961, Mauro identificou e descreveu pela primeira vez células intimamente
relacionadas com a fibra muscular esquelética de rãs. Denominou-as de células satélites (CS)
devido à localização anatômica – periferia da fibra muscular. (FIGURA 4)(7)
Os músculos esqueléticos de mamíferos adultos apresentam uma notável
capacidade de adaptação a exigências como crescimento, remodelação e trauma. Os
processos pelos quais essas adaptações ocorrem são largamente atribuídos à pequena
CS quiescentes distinguem-se fisicamente das fibras musculares adultas por
localizarem-se nas identações entre o sarcolema e a lâmina basal. Fibras musculares
esqueléticas são terminalmente diferenciadas, de modo que o crescimento muscular e a
regeneração são realizados pelas CS. (6, 22)
FIGURA 4: Desenho esquemático de uma célula satélite quiescente
envolta pelalâmina basal e pelo sarcolema da miofibra justaposta.
Fonte: adaptado de Vierk J, O’Reilly B, Hossner K, Antonio J, Byrne K, Bucci L, et al. Satellite cell regulation following myotrauma caused by resistance exercise. Cell Biol Int 2000; 24: 263-72.
Enquanto o tecido muscular esquelético encontra-se livre de agressões, as CS
permanecem em um estado não proliferativo, quiescente. Entretanto, em resposta a
estímulos como trauma, as CS tornam-se ativas, proliferam-se e expressam marcadores
miogênicos, sendo então denominadas mioblastos. Essas células fundem-se a fibras
musculares pré-existentes ou a CS vizinhas para formar novas fibras musculares. (6, 22,
2.1.2.1 Identificação das células satélites musculares
Tais células constituem uma população de células miogênicas mononucleadas
e indiferenciadas. São encontradas nos músculos esqueléticos de mamíferos, aves, répteis
e anfíbios. (24)
Uma característica importante das CS é que a lâmina basal que as circunda e a
fibra muscular associada são contínuas. Outras características das CS são: alta relação
núcleo/citoplasma com poucas organelas; núcleo menor em comparação com os núcleos
adjacentes da fibra muscular; e aumento na quantidade de heterocromatina nuclear,
comparada à do mionúcleo. (6, 22, 23, 24)
Essas características morfológicas são compatíveis com a idéia de que, em
condições normais, as CS são relativamente quiescentes e menos ativas, mas desaparecem
após a ativação ou a proliferação das CS em resposta ao crescimento, à remodelação ou ao
trauma muscular. (6, 22, 23, 24)
Após a ativação, as CS são mais facilmente identificadas, pois aparecem como
um edema na fibra muscular devido ao aumento na relação citoplasma/núcleo. Em
associação com o aumento da atividade mitótica, existe uma redução na heterocromatina e
um aumento no número de organelas intranucleares. (6, 23, 24)
2.1.2.2 Marcadores para células satélites
O método mais fidedigno para identificar as CS é a microscopia eletrônica.
Porém esse método não é muito acessível. (25)Conseqüentemente, grande interesse foi
dado a bons anticorpos para a identificação de proteínas específicas nas CS quiescentes e
O perfil de expressão gênica das CS quiescentes ou ativadas ainda é pouco
conhecido. (6, 27)
Através da identificação de marcadores de CS, pesquisadores estarão aptos a
lidar com a origem das CS, com o controle do ciclo celular e com a regulação molecular
dessa população única de células durante o crescimento e a regeneração. (6)
Diversos marcadores de CS foram identificados, mas são restritos para os
estados quiescente, ativado ou proliferativo. (6, 23, 24, 27)
Alguns marcadores já bem estabelecidos são:
a) Myo D (Myogenic determination gene D)
É um fator de transcrição descoberto em 1987, pertencente à família de
proteínas basic helix-loop-helix, à qual também pertencem outras proteínas, como o Myf 5, a miogenina e o MRF 4. Tais proteínas controlam a diferenciação de células da
linhagem miogênica. (23)
CS Myo D negativas apresentam capacidade de diferenciação reduzida e
retardada. (28)
O Myo D é um excelente marcador para CS ativadas. (28) É encontrado em
elevados níveis no músculo em regeneração e em recém-nascidos. Sua função na
musculatura esquelética após o nascimento de mamíferos ainda não é clara. Doze horas
após o trauma muscular, pode-se detectar a presença de Myo D e de outras proteínas
relacionadas à diferenciação de células da linhagem miogênica, como desmina e
miogenina. Em relação às fases do ciclo celular, o Myo D apresenta-se em altos níveis
baixos na transição G1/S e aumenta novamente no transcorrer da fase S para a mitose
propriamente dita. (23, 27, 29)
b) PCNA (Proliferating cell nuclear antigen)
É uma proteína cuja síntese ocorre no início das fases G1 e S do ciclo celular.
Mesmo sendo inespecífica, é um excelente marcador para CS em proliferação. (23)
2.1.2.3 Distribuição e quantificação das células satélites
A quantificação da população de CS na musculatura esquelética de adultos
tornou-se possível graças à utilização de técnicas ultraestruturais. Recentemente, técnicas
imunoistoquímicas foram utilizadas para identificação de CS. (6)
A expressão de Myo D ocorre precocemente durante a ativação de CS
(aproximadamente seis horas após o trauma muscular). (6)
Vários marcadores não seletivos para proliferação celular têm sido utilizados
também para caracterizar a proliferação de CS. Esses marcadores incluem antígeno
nuclear de células proliferativas, bromodeoxiuridina (Bdr U) e [³H] timidina. (6)
O número de CS depende da espécie animal, da idade e do tipo de fibra
muscular. (6, 23, 24, 31, 32, 33, 34, 35)
Em ratos, as CS constituem aproximadamente 30% dos núcleos no músculo de
neonatos. Decrescem para cerca de 4% nos adultos e para 2% nos idosos. (6, 23, 24, 31,
32, 35)
A diminuição da porcentagem de CS com a idade é resultado de um aumento
A distribuição de CS entre os grupos de músculos é resultado da
heterogeneidade no conteúdo de CS nos diferentes tipos de fibras musculares. Há um
aumento no número de CS nas proximidades de capilares, nos mionúcleos e nas junções
mioneurais. (6, 23, 33)
2.1.2.4 Fatores de crescimento como reguladores das células satélites
O processo de regeneração muscular requer a influência de fatores de
crescimento e uma seqüência de eventos celulares que resulta na regulação da população
de CS. (6, 24)
Muitos dos estudos que analisaram o efeito dos fatores de crescimento na
biologia das CS têm utilizado cultura de CS. Esses estudos têm definido o efeito de
fatores de crescimento isolados ou combinados e têm proporcionado um discernimento
preciso sobre a regulação de CS. (6)
Os estudos in vitro são limitados devido à carência de fatores permissivos ou repressivos que estão presentes in vivo e que podem influenciar a atividade celular. (6, 23)
A maioria das culturas de CS é feita na musculatura esquelética neonatal
devido à abundância delas nesses tecidos em comparação com indivíduos mais idosos. (6)
Fatores de crescimento que são importantes na regulação da proliferação,
a) Fatores de crescimento semelhantes à insulina
Músculos esqueléticos secretam fatores de crescimento semelhantes à insulina
(IGF – insulin-like growth factor) I e II (IGF-I e IGF-II). Tais fatores são importantes na regulação do metabolismo da insulina. Também são importantes na regulação da
regeneração da musculatura esquelética. Tanto o IGF-I quanto o IGF-II aumentam a
proliferação e a diferenciação de CS in vitro. (6)
b) Fator de crescimento do hepatócito
O fator de crescimento do hepatócito (HGF – hepatocyte growth factor) é uma citoquina multifuncional, inicialmente descrita como um mitógeno para hepatócitos
maduros. (6)
Atualmente, o HGF é considerado um dos fatores de crescimento mais
importantes no que diz respeito à regeneração orgânica devido às suas propriedades
mitogênica e motogênica. (24)
O HGF é a chave reguladora da atividade das CS durante a regeneração
muscular. (24)
O HGF e seu receptor c-Met têm sido localizados nas CS e miofibras
adjacentes, mas estão ausentes nos fibroblastos adjacentes. (6)
A expressão do HGF é proporcional ao grau de lesão muscular. (2) O
estiramento mecânico induz a ativação das CS em cultura, com liberação de HGF. Assim,
c) Fatores de crescimento de fibroblastos
O fator de crescimento de fibroblastos (FGF – fibroblast growth factor) tem nove isoformas diferentes (FGF-1 a FGF-9). A isoforma FGF-6 é restrita para músculos
esqueléticos. (37)
Os FGFs estimulam a síntese de tecido conjuntivo, induzem a proliferação de
CS e suprimem a diferenciação miogênica. (23)
Os níveis dos FGFs são proporcionais ao grau de expressão dos seus
receptores. Quando ocorre um aumento na expressão dos receptores para o FGF, há
aumento na proliferação e redução na diferenciação de CS. (23)
d) Fatores de crescimento de transformação
Fatores de crescimento de transformação (TGF-β - transforming growth factors) são importantes citoquinas que regulam o crescimento celular. (6, 24)
Geralmente, a função dos membros da família dos TGF-β é a inibição da
proliferação e da diferenciação musculares através da inibição da transcrição de genes da
família Myo D. (6)
e) Citoquinas interleucina-6
O fator inibidor de leucemia (LIF – leukemia inhibitory factor) e a interleucina-6 (IL-6) são membros da família de citoquinas IL-6 produzidas por diferentes
A regeneração de músculo esquelético é atenuada após lesão no LIF de
camundongo mutante. A administração exógena de LIF aumenta o processo de
regeneração e produz aumento de miofibras. (6, 24, 38)
A IL-6 promove a degradação de tecido necrótico, sincroniza o ciclo de CS e
induz a apoptose de macrófagos após trauma muscular. (6, 30)
Diferente do LIF, a expressão de IL-6 em músculo lesado não aumenta a
proliferação de CS. Coletivamente, essa família de fatores de crescimento parece ter a
função integral na regeneração da musculatura esquelética. (6)
Muitos outros fatores podem estar envolvidos na regulação de CS de músculo
esquelético adulto, como, por exemplo, óxido nítrico e testosterona. (6)
2.1.2.5 Respostas funcionais das células satélites a estímulos fisiológicos
2.1.2.5.1 Estímulo hipertrófico
Exercícios de resistência e de carga induzem à hipertrofia muscular, tanto em
humanos como em modelos animais. (6) A hipertrofia muscular ocorre através de um
processo de ativação, proliferação e quimiotaxia de CS, além da fusão dessas células a
miofibras já existentes, para contribuir com o crescimento muscular. (39)
A capacidade migratória (quimiotaxia) das CS depende da integridade da lâmina
basal. Após a ruptura ou interrupção na lâmina basal ocasionada por miotrauma, CS podem
migrar para as miofibras adjacentes, utilizando pontes de tecidos. (40) Em resposta a
miotrauma em que não ocorra ruptura da lâmina basal, CS migram da porção proximal intacta
da miofibra, por baixo da lâmina basal, para o local do trauma, com a finalidade de participar
Miotrauma induzido por exercícios provoca uma resposta imunológica, resultando
no fluxo de macrófagos para a região lesada. Após a fase aguda, a infiltração de macrófagos
chega ao máximo em quarenta e oito horas. Inicialmente, acreditava-se que a função desses
macrófagos era limitada à fagocitose e à digestão de fibras musculares necrosadas. Entretanto,
novas funções dos macrófagos, durante o estágio inicial do reparo muscular, foram descritas.
Os macrófagos são essenciais na orquestração do processo de reparo muscular, pois secretam
uma coleção de fatores citoquímicos que regulam o número de CS. (41, 42, 43)
Não há regeneração muscular na ausência de uma resposta dos macrófagos, mas,
na presença dessa resposta, ocorre aumento na proliferação e na diferenciação de CS. (44)
Na resposta a exercícios de resistência, o miotrauma resulta na liberação de fatores
de crescimento que irão, em parte, regular a população de CS durante a regeneração. (42)
Embora ainda existam dúvidas sobre a função das CS na remodelação muscular, a
conseqüência fisiológica primária da resposta hipertrófica é produzir um músculo com
capacidade para gerar força máxima. (6)
2.1.2.5.2 Estímulo atrófico
A atrofia de um músculo esquelético resulta na redução do número de núcleos da
miofibra e pode ser induzida por diversos fatores, como denervação, imobilização e nutrição
deficiente. (45)
Em experiências com ratos pré-púberes, a imobilização de um músculo levou à
diminuição do número e da capacidade proliferativa de CS, o que alterou irreversivelmente a
remodelação muscular. Isso não ocorreu em animais adultos, nos quais as CS proliferaram e
Após a denervação, há um aumento de CS na fase aguda; posteriormente, na fase
crônica, ocorre um decréscimo dessas células. (47)
2.1.2.5.3 Envelhecimento
O aumento da idade está associado à diminuição da capacidade de proliferação e
de diferenciação das CS. (6, 23, 48)
2.1.2.6 Respostas funcionais a estados de doença
A maioria das miopatias apresenta uma mutação molecular que afeta as proteínas
musculares, acarretando alterações estruturais no músculo esquelético. (6, 23)
A distrofia muscular de Duchenne é a mais comum e a mais devastadora das
distrofias musculares. (6, 23, 49) A progressão da doença e a morte ocorrem porque as CS
falham em manter a regeneração muscular. (6) É uma doença recessiva ligada ao cromossoma
X, que resulta em mutação em um gene relacionado a uma proteína do citoesqueleto da fibra
muscular. A ausência dessa proteína no citoesqueleto torna a fibra muscular extremamente
frágil. O estresse mecânico associado a contrações repetidas leva a uma degeneração difusa.
As CS respondem a essa lesão repovoando o músculo esquelético com miofibras defeituosas,
com falta de distrofina. Tal processo resulta em ciclos contínuos de degeneração-regeneração,
culminando com a exaustão das CS. (6, 23, 50, 51)
Renault et al. demonstraram que a sobrevida das CS provenientes de um paciente de nove anos com distrofia muscular de Duchenne era de aproximadamente um terço da
2.1.2.7 Modelos de regeneração muscular
Uma estratégia para o estudo da ativação, da proliferação e da regeneração de CS
é produzir experimentalmente uma lesão muscular controlada. Estratégias incluindo
compressão, congelamento e lesão química induzida foram utilizadas com sucesso para o
estudo biológico das CS. (6, 38)
Um dos modelos mais estudados consiste na injeção da cardiotoxina (purificada
do veneno da cobra Naja nigricollis) no músculo gastrocnêmico, levando a uma degeneração de cerca de 80% a 90% das fibras musculares. Seis horas após a lesão, as CS tornam-se ativas
e proliferam durante dois a três dias. A arquitetura do músculo lesado regenera-se após dez
dias. (6, 23)
2.1.3
Particularidades da musculatura ocular extrínseca
A presença de um grande número de isoformas da cadeia pesada da miosina (uma
das proteínas responsáveis pela contração muscular) representa uma das características que
tornam a musculatura ocular extrínseca distinta dos outros músculos esqueléticos. As
isoformas rápida e lenta, a específica para a musculatura cardíaca e as isoformas encontradas
no período de desenvolvimento e no período neonatal estão presentes na musculatura ocular
extrínseca. Existe também uma co-expressão de mais de um tipo de isoforma em uma mesma
fibra. (52, 53, 54)
Outra característica das fibras musculares da musculatura ocular extrínseca é a
em fibras musculares em desenvolvimento ou em regeneração; ela é ausente em fibras
musculares esqueléticas adultas. (55, 56)
Fibras musculares esqueléticas normais de mamíferos adultos não são substituídas
nem remodeladas, a menos que sofram algum trauma. Após o trauma, as CS tornam-se ativas
e dividem-se, resultando na regeneração do músculo lesado. Os músculos em regeneração
expressam um número de fatores de crescimento miogênico e isoformas de cadeia pesada de
miosina imatura que permanecem metabolicamente ativas na musculatura ocular extrínseca
adulta lesada. (9,57)
McLoon e Wirtschafter demonstraram, em 2002, que existe uma adição contínua
de mionúcleos a miofibras normais, não lesadas, na musculatura ocular extrínseca de coelhos
e ratos adultos. (8, 57) Em 2003, os mesmos autores descreveram a presença de CS ativadas
nos MOE de macacos e humanos adultos normais. (9)
Novos estudos sobre o papel das CS na musculatura ocular extrínseca são
necessários para aumentar os conhecimentos e a capacidade de tratar desordens musculares
2.2 Revisão da toxina botulínica do tipo A
2.2.1 Introdução
O fisiologista Claude Bernard, em 1875, escreveu que “venenos podem ser
empregados com o objetivo de destruir a vida ou como agentes terapêuticos na doença”.
Diversas substâncias tóxicas de origem animal e vegetal foram usadas na prática médica
durante sua época. Atualmente, uma grande variedade de substâncias venenosas de plantas,
animais e microrganismos é utilizada em estudos de fisiologia animal, e algumas já são
aplicadas medicinalmente em humanos. (59, 60)
A primeira descrição dos sintomas do botulismo foi publicada entre os anos de
1817 e 1822, pelo médico e poeta alemão Justinus Kerner (1786-1862). Kerner descreveu
clinicamente o botulismo: os sintomas, a duração dos sintomas e os achados clínicos (o
desaparecimento da secreção lacrimal, as pupilas dilatadas, a paralisia dos músculos oculares
extrínsecos, a supressão da secreção salivar, o ressecamento da pele, a paralisia dos músculos
esqueléticos e a preservação da cognição). Finalmente, Kerner sugeriu o uso terapêutico da
toxina causadora do botulismo para bloquear movimentos anormais, como na coréia, e o uso
em desordens como hipersecreção. (61, 62, 63)
Em 1895, a bactéria Bacilinum (posteriormente denominada Clostridium botulinum) foi identificada por E. P. van Ermengem, professor de bacteriologia da Universidade de Gante, na Bélgica. Na década de 1920, a toxina botulínica do tipo A foi
isolada na forma purificada pelo Dr. H. Sommer, da Universidade da Califórnia, São
Francisco. Em 1946, a toxina foi isolada na forma cristalina por Edward J. Schantz, ph.D. da
Universidade de Wisconsin-Madison. Na década de 1950, o Dr. Vernon Brooks provou que a
provocando um relaxamento dos músculos. Na década de 1960-1970, o processo de
purificação da toxina botulínica do tipo A foi aprimorado. (64)
A idéia de injetar um agente farmacológico nos músculos extrínsecos oculares
para produzir uma paralisia temporária foi de Conrad Behrens. Ele injetou álcool, método que
se demonstrou ineficaz. Em 1973, Alan Scott e colaboradores experimentaram várias drogas
como o di-isopropil-fluor-fosfato (DFP), a neurotoxina bungaro (toxina do veneno da cobra
Bungarus multicinactus), o álcool e a toxina botulínica tipo A – na tentativa de paralisar os músculos extrínsecos oculares de macacos Rhesus. (3, 4, 65, 66)
A intoxicação alimentar, ou seja, o botulismo, provoca sintomas oculares como
visão embaçada e diplopia, pois paralisa os músculos oculares intrínsecos e extrínsecos. Daí a
idéia de se utilizar a toxina botulínica para provocar o enfraquecimento transitório de
músculos oculares e mudanças permanentes no alinhamento ocular, sem efeitos colaterais
severos. (3)
Scott iniciou a utilização da toxina botulínica do tipo A em seres humanos em
1977. Seus relatos preliminares haviam demonstrado que a toxina poderia ser utilizada como
alternativa à cirurgia tradicional de estrabismo. (3, 66)
Posteriormente, a toxina botulínica foi considerada eficaz para o tratamento de
outras patologias, como blefaroespasmo, espasmo hemifacial, mioquimias, entrópio da
pálpebra inferior, oftalmopatia de Graves, nistagmo, úlcera corneana e regeneração aberrante
do sétimo nervo. (65)
Em 1982, a toxina passou a ser utilizada, ainda experimentalmente, por vários
pesquisadores nos Estados Unidos e em outros países, sob a orientação de Scott. Foram
tratados 5 725 pacientes com estrabismo, 9 983 pacientes com blefaroespasmo e 3 571
Em 29 de dezembro de 1989, o FDA (Food and Drug Administration) liberou a toxina botulínica para o tratamento do estrabismo, do espasmo hemifacial e do
blefaroespasmo, em pacientes acima de 12 anos de idade. (60, 65)
2.2.2 Farmacologia
As toxinas do Clostridium botulinum (bactéria anaeróbica, Gram positivo) são potentes neurotoxinas. São classificadas em oito sorotipos (A, B, C1, C2, D, E, F e G),
baseados nas propriedades imunológicas. Os tipos A, B e E são comumente associados à
intoxicação humana. O tipo A foi o primeiro a ser obtido na forma cristalizada, altamente
purificada e estável. (3, 60, 65, 66, 67)
A forma cristalizada do tipo A é uma proteína de alto peso molecular (cerca de 900
kDa [quilodaltons]) e consiste em duas subunidades que se dissociam em solução. Cada
subunidade (450 kDa) consiste de três cadeias peptídicas de peso molecular semelhante (150
kDa). Uma das cadeias é tóxica, enquanto as outras duas não têm toxidade. A cadeia peptídica
tóxica consiste de uma unidade pesada (100 kDa) e de uma leve (50 kDa). (65, 66, 67)
2.2.3 Mecanismo de ação
A ação da toxina botulínica do tipo A ocorre na terminação nervosa e é processada
em três etapas: acoplamento, internalização e paralisia. A toxina, quando injetada, é rápida e
firmemente acoplada aos receptores das fibras colinérgicas. O acoplamento ocorre através da
porção pesada da cadeia peptídica tóxica. A penetração da toxina através da membrana até o
causada pela inibição da liberação da acetilcolina. A toxina ocupa os sítios que seriam
ocupados pelo cálcio e, desse modo, previne a exocitose da acetilcolina, que é
cálcio-dependente. (65, 68, 69)
O efeito parético da toxina botulínica é dose-dependente, e o efeito máximo ocorre
de cinco a sete dias após a injeção. (70)
Histopatologicamente, o músculo denervado mostra atrofia muscular e um grau
leve de mudanças desmielinizantes na terminação nervosa, com subseqüente regeneração. O
tempo é de seis a nove meses para que se recupere totalmente dos efeitos da toxina. (3, 70, 71)
Os experimentos de Scott com macacos Reshus indicaram que:
1- a toxina botulínica produziu um enfraquecimento transitório dos músculos
oculares extrínsecos e mudanças permanentes no alinhamento ocular, sem efeitos colaterais
severos;
2- o início e a duração da denervação foram dose-dependentes;
3- o efeito da toxina foi reduzido pela injeção de antitoxina no músculo tratado (se
a injeção fosse aplicada de 0 minuto a 30 minutos após a primeira injeção);
4- injeções repetidas de toxina não foram reconhecidas pelo sistema imune;
5- os efeitos tóxicos locais foram evitados por imunização prévia com toxóide. (3,
70)
2.2.4 Preparações comerciais
A toxina botulínica do tipo A é comercializada com o nome de Botox® 100 U
(Allergan Herbert, Irvine, Califórnia), Dysport® 500 U (Speywood Group Beautour-Ipsen) e