RELAÇÕES SOCIAIS DE Callithrix jacchus MACHOS:
COMPETIÇÃO OU COOPERAÇÃO?
RELAÇÕES SOCIAIS DE Callithrix jacchus MACHOS: COMPETIÇÃO OU COOPERAÇÃO?
Dissertação apresentada à Universidade Federal do Rio Grande do Norte para a obtenção do título de mestre em Psicobiologia.
Orientador: Prof. Arrilton Araújo
Catalogação da Publicação na Fonte. UFRN / Biblioteca Setorial do Centro de Biociências
Santiago, Alessandra Maressa Lessa.
Relações sociais de Callithrix jacchus machos: competição ou cooperação? / Alessandra Maressa Lessa Santiago. – Natal, RN, 2012.
48 f.: il.
Orientador: Prof. Arrilton Araújo.
Dissertação (Mestrado) - Universidade Federal do Rio Grande do Norte. Centro de Biociências. Programa de Pós-Graduação em Psicobiologia.
1. Callithrix jacchus. – Dissertação. 2. Acasalamento. – Dissertação. 3. Relações sociais. – Dissertação. I. Araújo, Arrilton. II. Universidade Federal do Rio Grande do Norte. III. Título.
Autor: ALESSANDRA MARESSA LESSA SANTIAGO
Data da defesa: 27 de abril de 2012
BANCA EXAMINADORA
____________________________________ Profa. Maria Adélia Borstelmann de Oliveira Universidade Federal Rural de Pernambuco
____________________________________ Profa. Maria Emília Yamamoto
Universidade Federal do Rio Grande do Norte
____________________________________ Prof. Arrilton Araújo - Orientador Universidade Federal do Rio Grande do Norte
• Gostaria de agradecer a meu querido orientador Arrilton, por ter acreditado em mim e apostado no meu sucesso quando ninguém mais havia;
• À Bárbara, por me auxiliar nas observações e por acordar um ano inteiro de madrugada, nos feriados e finais de semana, independente das condições climáticas;
• À minha família, pelo apoio, pela paciência e principalmente pelo incentivo à minha carreira acadêmica;
• À minha querida irmã Talita, por ter se sacrificado tanto por mim e por sua preciosa ajuda com os gráficos;
• Aos funcionários do LEAP: Edinólia, Flávio, Francisco, Geniberto, Antônio Barbosa e José Luiz, pelo auxílio com o manejo dos saguis;
• À minha companheira de turma Priscilla Kelly, pela amizade e pelas longas conversas de desabafo;
• À Felipe, sem o qual não teria conseguido entender estatística até hoje;
• À Patrícia, Eliane, Edilma e Hélderes por todo apoio e ajuda na análise hormonal;
• Aos meus colegas do LBC, pelas boas risadas e muito companheirismo;
• À Fívia por ter me ouvido quando precisei e ter sido uma das primeiras pessoas a me ensinar sobre o comportamento de saguis;
• Aos professores do programa de Psicobiologia, que me fizeram amar tanto a área do comportamento animal;
• À CAPES pelo auxílio financeiro na forma de bolsa;
machos.
The group Callithrichidae is characterized by the flexibility in its mating system. This fact generates questions about the mechanisms that Callithrix jacchus males reach the breeding position in a group and how they prevent the subordinates’ reproduction, since the competition apparently happens with less intensity when compared to the females. Studies have shown the importance of social interactions and kinship among individuals in the distribution of mating opportunities in a group. This work aimed to evaluate if dyads of Callithrix jacchus males acted socially different due to kinship. We observed the agonistic and affiliative behaviours made by the males when associated in dyads (Phase 1) and when these dyads received a female (Phase 2), which was introduced in the pair`s cage for 45 minutes. In the phase 2, we also accounted for the sexual interactions between
males and female in each trio. We used 16 males, 8 related (brothers-R) and 8
non-related (NR), as well as 8 females. Each phase lasted 4 weeks, with 3
observations/week, during 15 min/male in phase 1 and 2. In the first phase, two
pairs of R males had a contested dominance and the other two, just like in the NR
males, had an uncontested dominance. The NR dominant males were more
aggressive than the subordinates. With the female`s entrance in the cage, all male
pairs began to have an uncontested dominance. The NR males’ aggression
frequency rose along with the subordinates` submission. In the R males, the
frequency of grooming and physical contact was higher than in the NR males. So,
we conclude that the low levels of agonism presented by the R males, along with the
higher tolerance shown amongst them, lead us to believe that kinship attenuate the
1 INTRODUÇÃO...8
2 OBJETIVO GERAL...13
3 OBJETIVOS ESPECÍFICOS………...13
4 HIPÓTESES E PREDIÇÕES...13
5 METODOLOGIA...15
5.1 SUJEITOS...15
5.2 PROCEDIMENTO EXPERIMENTAL...15
5.3 CATEGORIAS COMPORTAMENTAIS REGISTRADAS...16
5.4 ANÁLISE HORMONAL...17
5.5 CLASSIFICAÇÃO HIERÁRQUICA DOS MACHOS...18
5.6 ANÁLISE DE DADOS………...18
6 RESULTADOS...………..19
7 DISCUSSÃO...………28
8 CONCLUSÕES....………...39
1 INTRODUÇÃO
Os calitriquídeos são animais arbóreos, vivendo em grupos familiares pequenos de 3 a
17 indivíduos (ARAÚJO, 1996; FRENCH, 1997; TARDIF, 1997). Sua reprodução é
monopolizada por um ou por um número pequeno de indivíduos dominantes de cada sexo
(FRENCH, 1997; TARDIF, 1997). Em condições naturais, normalmente o grupo consiste no
casal reprodutor e sua prole (EPPLE, 1975; DIGBY E BARRETO, 1993). Os membros que
não se reproduzem auxiliam no cuidado dos infantes (YAMAMOTO E BOX, 1997).
A posição social pode ter um papel importante na determinação das oportunidades
reprodutivas e no sucesso reprodutivo de machos e de fêmeas de calitriquídeos (SOUZA ET
AL., 2005; YAMAMOTO ET AL., 2009). As fêmeas reprodutoras são tipicamente aquelas
socialmente dominantes sobre as outras do grupo, inibindo a ovulação das subordinadas
(ABBOTT, BARRETT E GEORGE, 1993; ABBOTT ET AL., 1998; BARRETT, ABBOTT
E GEORGE, 1993; ROTHE, 1975). Essas fêmeas dominantes geralmente são as únicas
fêmeas em seus grupos sociais que exibem níveis hormonais, circulante ou excretado,
indicativo de ciclos ovarianos (ABBOTT ET AL., 1981), apesar de ser comum outra fêmea
também ovular no grupo (ARRUDA ET AL., 2005; SOUSA ET AL., 2005; YAMAMOTO
ET AL., 2009). Como outros Platyrrhini, os calitriquídeos não menstruam e não exibem
sinais externos conspícuos de ovulação. O comportamento sexual ocorre ao longo do ciclo
ovariano e da gravidez, sendo mais comum durante o período peri-ovulatório (DIXSON,
1998; ROTHE, 1975) e logo após o parto (DIXSON, 1998).
Machos e fêmeas não reprodutores de calitriquídeos quase não apresentam
comportamento de cópula quando estão em grupos familiares monogâmicos, evitando desta
forma o incesto (BAKER, ABBOTT E SALTZMAN, 1999). Em estudo do perfil social de
machos de C. penicillata realizado por Decanine & Macedo (2008a), não se observou padrão
de dominância entre os machos, havendo ligação social entre apenas um do grupo com a
fêmea dominante, sugerindo-se ser esse o macho reprodutor sem aparente competição por tal
posição.
Embora a monogamia seja o sistema de acasalamento prevalente, com reprodução
tipicamente restrita a uma fêmea e a um macho reprodutores específicos, a presença de duas
fêmeas reprodutoras em alguns grupos demonstra que a supressão reprodutiva não é absoluta
(ARRUDA ET AL., 2005; YAMAMOTO ET AL., 2009). Portanto, o sistema de
acasalamento é variável dentre as espécies de Callithrichidae, já havendo sido reportados
FERRARI, 2009; FERRARI E DIGBY, 1996; SCHAFFNER E FRENCH, 2004;
YAMAMOTO ET AL., 2009). As espécies desta família geralmente concebem gêmeos e o
papel dos ajudantes não reprodutivos do grupo é de auxiliar no cuidado da prole da fêmea
reprodutora. Este auxílio consiste no compartilhamento do carregar os gêmeos infantes por
seu habitat arbóreo, como também a cooperação através da provisão de alimento (TARDIF,
HARRISON E SIMEK, 1993). Espécies nas quais os adultos que não os pais regularmente
auxiliam no cuidado da prole tipicamente defendem território contra a investida de grupos
vizinhos e intrusos (GASTON, 1978). Sistemas de acasalamento com cooperação se
caracterizam pelo monopólio da reprodução por um ou mais animais dominantes de cada
sexo (TARDIF, 1997), o que pode afetar o envolvimento dos animais reprodutores e dos
ajudantes em interações entre os grupos (LAZARO-PEREA, 2001).
Estudo em uma população de Saguinus mostrou que o sistema social variava entre monogâmico e poliândrico de acordo com o número de ajudantes disponíveis para auxiliar no
cuidado da prole. Assim, se houvesse ajudantes não reprodutivos disponíveis, esses animais
reproduziam-se monogamicamente e se os mesmos não estivessem presentes,
reproduzir-se-iam poliandricamente, dividindo os custos do cuidado dos infantes (GOLDIZEN, 1987).
De acordo com Goldizen (1988), a poliandria cooperativa é um dos padrões variados
de sistema de acasalamento que ocorrem em Callithrichidae e o grau de parentesco entre
machos é um fator importante na disputa pela reprodução (BAKER, ABBOTT E
SALTZMAN, 1999; SCHAFFNER E FRENCH, 2004). Deduz-se que esta ocorrência é
devido a alta incidência de gêmeos, juntamente com o relativo alto peso dos infantes, o que
torna o cuidado dos mesmos bastante difícil. Assim, os ajudantes não reprodutivos,
geralmente compostos pelos filhotes mais velhos, e os machos poliândricos podem servir
como fontes de ajuda extra no cuidados dos filhotes. Existe também a evidência de que
machos irmãos, como também pai e filho, sendo membros permanentes do grupo, se unem
para receber uma nova fêmea reprodutora em casos nos quais o par reprodutor ou a antiga
fêmea reprodutora morrem ou desaparecem (CASTRO E ARAÚJO, 2004;
LAZARO-PEREA ET AL., 2000).
Yamamoto & Araújo (1991) também sugeriram a flexibilidade do sistema de
acasalamento dos calitriquídeos, onde, ao compilar dados de campo e de cativeiro,
observaram que a tolerância e o grau de parentesco entre os machos estaria influenciando no
tipo de sistema social. Esta flexibilidade também pode ser explicada como um ajuste
número de cuidadores do grupo (GOLDIZEN, 1990) e/ou da influência das pressões
ambientais (DIGBY E FERRARI, 1994; RYLANDS, 1996).
A maneira mais frequentemente utilizada para se aferir tolerância é através da reação
a indivíduos da mesma espécie. Em cativeiro, a reação de C. jacchus a intrusos é afetada pelo
sexo do residente e do intruso (ARAÚJO E YAMAMOTO, 1993; BAKER, ABBOTT E
SALTZMAN, 1999; HARRISON E TARDIF, 1988), presença do parceiro
(ANZENBERGER, 1985; ARAÚJO E YAMAMOTO, 1993; HARRISON E TARDIF, 1988)
e status social no grupo (ANZENBERGER, 1985).
Araújo & Yamamoto (1993) reportaram que fêmeas acasaladas ou não são mais
agressivas com fêmeas intrusas que os machos acasalados com machos intrusos. Porém,
machos não acasalados são tão agressivos quanto às fêmeas com intrusos do mesmo sexo,
sugerindo que esses machos solitários são tão agressivos quanto as fêmeas quando uma
relação de dominância ainda não foi estabelecida. Os autores sugerem que a maior tolerância
dos machos acasalados com os machos intrusos pode trazer vantagem aos primeiros, como a
assistência de ajudantes e o aumento de seu sucesso reprodutivo. O parentesco também pode
atenuar a competição entre os machos (YAMAMOTO E ARAÚJO, 1991), sendo observados
maiores níveis de comportamentos afiliativos entres estes que naqueles sem parentesco
(GALVÃO-COELHO ET AL., 2008; YAMAMOTO E ARAÚJO, 1991). Tais
comportamentos afiliativos, como também o contato físico, aparentemente são usados por
machos com parentesco como um mecanismo para contrabalançar os efeitos causados por
condições estressantes (GALVÃO-COELHO ET AL., 2008).
De acordo com o modelo teórico de Troisi (2001), machos e fêmeas de uma espécie
desenvolvem mecanismos diferentes para suportar o estresse social. Baseados neste modelo,
Silva, Leão e Sousa (2008) investigaram a resposta hormonal e comportamental de pares de
gêmeos isossexuais de machos e fêmeas de C. jacchus. Ao separar esses pares de seus grupos
natal, os pares de gêmeos machos mostraram maiores níveis de aumento de cortisol fecal que
as fêmeas. Estes dados mostram uma maior tendência a filopatria dos machos e a maior
frequência na qual fêmeas selvagens migram de seus grupos em relação aos machos
selvagens. Assim, para as fêmeas, a estratégia de migrar significa oportunidade de
acasalamento. Para os machos, a estratégia de permanecer no grupo pode representar também
uma oportunidade de acasalamento, envolvendo o estabelecimento de ligação social com
outros machos, o que fortalece o grupo através da cooperação entre estes, dando suporte ao
cuidado e proteção da prole do par reprodutor (LAZARO-PEREA, 2001; SOUSA ET AL.,
interações afiliativas (catação social e comportamento de se amontoarem) depois que
separados do grupo natal que as fêmeas. Tais resultados indicam que mudanças no ambiente
social e fisiológico aumentam a competição entre as fêmeas aparentadas, enquanto que nos
machos aparentados há um aumento dos comportamentos afiliativos, sugerindo-se uma
estratégia de cooperação entre os mesmos.
Os trabalhos acima citados, juntamente com dados experimentais de Werdenich e
Huber (2002), que mostraram que díades de machos cooperavam com sucesso em uma dada
tarefa instrumental, independente da quantidade de alimento disponível, reforçam a evidência
que os machos são mais propensos a cooperar uns com os outros.
De modo a mostrar a importância do tipo de interação social de animais de um grupo e
sua consanguinidade na distribuição de oportunidades reprodutivas e na organização social
dos grupos, Yamamoto e Araújo (1991) observaram os comportamentos afiliativos e sexuais
de dois pares de machos de C. jacchus na presença de uma fêmea. Um dos pares era formado
por gêmeos e o outro por animais não aparentados. Os autores observaram que havia uma
dominância clara de um dos indivíduos sobre o outro, porém esta era menos consistente nos
gêmeos que no par não aparentado. Harrison e Tardif (1988), ao testarem a hipótese da
atenuação de agressão baseada em parentesco, relataram uma diminuição significativa de
comportamentos agressivos entre aos machos aparentados em relação aos desconhecidos,
permitindo a formação de grupos poliândricos fraternos. Estudo sobre poliandria cooperativa
em Saguinus (GOLDIZEN, 1989) também mostrou a baixa incidência de agressão entre os machos poliândricos, os quais raramente atrapalhavam a cópula um do outro, dividiam o
alimento e catavam um ao outro ocasionalmente, mostrando um teor mais afiliativo que
agressivo de sua relação.
De maneira a se analisar a resposta fisiológica (níveis de cortisol) e comportamental
diante de agentes estressores físicos e sociais, Galvão-Coelho (2009) reuniu díades de
machos gêmeos e não aparentados e com base em seus níveis basais de testosterona os
classificou em dominante, subordinado e com hierarquia de dominância indefinida (HDI).
Foram observadas diferenças nos níveis de cortisol de acordo com o posto social.
Considerando todos os dias do estudo em conjunto, os machos dominantes apresentaram uma
maior tensão do que os demais machos, pois mostraram maiores níveis de cortisol que os
machos dos outros grupos. Esta maior tensão foi descrita como uma frequência mais elevada
de comportamentos de piloereção, indicativo de competitividade, e uma maior frequência de
afastamento do outro macho, ocasionando a diminuição da frequência de contato físico que é
Schaffner e French (2004) perceberam que ao colocar dois machos relacionados
juntamente com uma fêmea, numa situação de poliandria artificial, os mesmos apresentavam
baixos níveis de agonismo notório e pouca diferença em seus comportamentos. Além disso,
não havia mudança em seus níveis urinários de testosterona e cortisol quando eram colocados
sozinhos com a fêmea numa situação de monogamia, sugerindo o baixo nível de competição
entre estes machos. Outros estudos com Callithrix também mostraram poucas interações agonistícas entre os machos aparentados (ARAÚJO E YAMAMOTO, 1993; BAKER ET
AL., 1999; DECANINE E MACEDO, 2008A; LAZARO-PEREA ET AL., 2001).
Estudo com grupos familiares em cativeiro mostrou que não houve diferença
significativa nos níveis plasmáticos de testosterona entre pais (dominantes) e filhos
(subordinados) (BAKER, ABBOTT E SALTZMAN, 1999). Abbott (1984) também não
encontrou diferença nos níveis de testosterona entre machos dominantes e subordinados não
aparentados. Porém, Castro & Sousa (2005) encontraram diferença significativa nos níveis
fecais de andrógenos entre pais e filhos. Diferenças encontradas no volume dos testículos
entre machos reprodutores e não reprodutores nos levam a crer que os níveis de andrógenos
variam entre os machos de acordo com a sua posição reprodutiva no grupo (ARAÚJO E
SOUSA, 2008).
Esta flexibilidade no sistema de acasalamento de Callitrichidae tem suscitado
questões sobre os mecanismos pelos quais os machos de C. jacchus atingem a posição de reprodutor no grupo e como impedem a reprodução dos outros machos subordinados, já que
aparentemente a competição, quando ela existe, ocorre com menos intensidade por essa
posição, diferentemente do que acontece com as fêmeas. De maneira a tentar elucidar este
problema, Araújo e Sousa (2008) correlacionaram o volume testicular e massa corpórea de
machos selvagens. Estes autores descobriram que o volume testicular varia com o status
reprodutivo dos machos em seu grupo social, possuindo os machos reprodutores testículos
maiores. Assim, sugere-se que a estratégia reprodutiva destes machos seja uma combinação
de mecanismos fisiológicos e comportamentais, com pouca competição explícita (ABOTT,
1985; ARAÚJO E SOUSA, 2008).
Em resumo, Yamamoto et al. (2010) caracterizam a organização social das fêmeas de
C. jacchus como competitiva, reforçando a monopolização reprodutiva da mesmas e evitando os pesados custos da criação de filhotes de mais de uma fêmea simultaneamente. Entre os
machos, os autores descrevem a organização como cooperativa. Esta cooperação é
organização social se complementam, sendo o sucesso deste sistema social altamente
dependente de um balanço entre os dois.
A influência do parentesco nas relações sociais entre os machos pode ajudar no
esclarecimento sobre a questão da flexibilidade do sistema de acasalamento desta espécie.
Este trabalho visa testar a influência do parentesco nas interações sociais entre machos
adultos de Callithrix jacchus.
2 OBJETIVO GERAL:
Avaliar se as díades de machos de Callithrix jacchus apresentam padrões de comportamento socialmente diferentes em função do parentesco.
3 OBJETIVOS ESPECÍFICOS:
• Comparar o nível de tolerância entre os pares de machos com parentesco e sem parentesco antes e depois da introdução de uma fêmea em suas gaiolas.
• Avaliar o nível de competição sexual pela posse da fêmea entre os machos de acordo com sua hierarquia (dominante ou subordinado) e grupo (com parentesco e sem
parentesco).
• Comparar os níveis de cortisol dos machos quando solitários, quando pareados com
outro macho e quando na presença da fêmea.
• Avaliar os níveis de progesterona das fêmeas antes e depois de serem introduzidas na gaiola dos machos.
4 HIPÓTESES E PREDIÇÕES:
Hipótese 1:
Predição 1:
O parentesco reduz a competição social entre os machos. Assim, a tolerância será
maior naqueles animais que possuem relação de parentesco.
Hipótese 2:
Os comportamentos agonistas e afiliativos entre os machos de C. jacchus mudarão com a presença da fêmea.
Predição 1:
A competição pela fêmea ocorrerá de maneira menos agressiva entre machos com
parentesco, podendo, inclusive, haver compartilhamento da posse da mesma por estes
machos.
Predição 2:
A disputa pela fêmea será mais intensa entre os machos sem relação de parentesco,
pois os mesmos precisarão assegurar seu sucesso reprodutivo.
Hipótese 3:
As interações sexuais entre as díades de machos de C. jacchus e a fêmea ocorrerão de
acordo com o parentesco apresentado entre eles.
Predição 1:
Os pares de machos com parentesco interagirão sexualmente com a fêmea em
frequência similar, havendo pouca ou nenhuma competição pela posse da fêmea.
Predição 2:
Os pares de machos não aparentados competirão pela posse da fêmea e uma relação
de dominância será estabelecida entre eles. O animal dominante possuirá maior frequência de
interações sexuais com a fêmea que o subordinado.
Hipótese 4:
Os níveis fecais de cortisol variarão de acordo com o posto social e grau de
Predição 1:
Pares de machos que não apresentam uma posição hierárquica clara possuem níveis
basais de cortisol semelhantes.
Predição 2:
Em pares de machos onde existe uma hierarquia definida, os machos dominantes
apresentarão níveis basais de cortisol mais elevados que os subordinados.
5 METODOLOGIA
O estudo foi realizado no Laboratório de Estudos Avançados em Primatas (LEAP) da
Universidade Federal do Rio Grande do Norte e foi aprovado pela comissão de ética no uso
de animais (CEUA) protocolo 042/2010.
5.1 Sujeitos:
Foram utilizados 24 animais da espécie Callithrix jacchus, todos adultos, dentre os quais foram 8 fêmeas, 8 machos com parentesco (dois pares de gêmeos e dois pares de
irmãos separados apenas por 1 geração) e 8 machos sem parentesco. Os machos foram
agrupados em pares, totalizando 4 pares de machos com parentesco e 4 pares de machos sem
parentesco. Cada par de machos foi colocado em uma gaiola (2,0 X 1,0 X 2,0 m), estando
expostos às condições naturais de temperatura, umidade e iluminação. A alimentação ocorreu
duas vezes ao dia e consistiu numa papa proteica pela manhã e frutas tropicais à tarde.
5.2 Procedimento Experimental:
O experimento foi dividido em 2 fases com duração de quatro semanas cada. Antes de
se iniciar o experimento, cada animal foi acompanhado durante 4 semanas, não havendo
observação comportamental, somente coleta de fezes três vezes por semana. As fezes foram
coletadas para servir como fase basal para as outras fases do experimento.
Fase I:
Os machos foram agrupados em duplas, de maneira a formarem 4 pares de machos
com parentesco e 4 pares de machos sem parentesco. A junção dos pares ocorreu de forma
gradativa, sempre com a presença de um observador a fim de separar os animais caso a
foi acompanhado pelo veterinário da colônia. Padronizou-se que as observações de
determinada dupla iniciavam-se na manhã seguinte a primeira noite que os animais
dormissem na mesma gaiola. Foram feitos os registros de seus comportamentos (descritos no
item 5.3 ) e a coleta de suas fezes. Durante esta fase, as fêmeas permaneceram isoladas em
suas gaiolas.
Fase II:
Nesta fase, uma fêmea adulta foi introduzida na gaiola de cada par de machos
previamente formados durante 45 minutos. Durante este período foram realizados os registros
das interações sócio-sexuais dos trios. A mesma fêmea foi utilizada para cada par ao longo do
experimento. Nenhuma das fêmeas possuía relação de parentesco com os machos da gaiola
onde foram introduzidas. Os comportamentos foram observados na presença de dois
observadores.
As observações na fase 1 do experimento foram realizadas através da técnica
amostragem de tempo focal ("focal time sampling") com duração de 15 min para cada
indivíduo e registro instantâneo a cada minuto. Foi realizado um focal/dia/indivíduo, três
vezes por semana. O animal focal foi escolhido de forma randômica entre os indivíduos do
par a ser observado. Na fase 2, as observações foram realizadas através da técnica “scan
sample”, onde os trios foram observados durante 45 minutos, com registro instantâneo a cada
minuto. As observações iniciaram-se em Julho/2010 e estenderam-se até Junho/2011.
5.3 Categorias Comportamentais Registradas :
Os comportamentos abaixo descritos, baseados nas descrições de Alencar et al.
(2006), Decanine e Macedo (2008a,b) e Stevenson e Poole (1976) e foram registrados quanto
as suas frequências para cada sujeito:
1. Interações Agonísticas:
• Vocalização agonística: Execução de vocalização do tipo ehr ehr.
• Vocalização de submissão: Execução de vocalização do tipo nga-nga.
• Agressão: Agarrar, morder, bater, empurrar outro indivíduo.
• Perseguição: Seguir e perseguir outro na gaiola.
• Postura de submissão: se apoiar nas pernas traseiras, com os tufos murchos. O
inferiormente em relação aos outros animais na gaiola.
• Exposição de genitália: Levantar a cauda e expor a genitália para outro indivíduo.
• Piloereção: A pelagem corporal do animal encontra-se completamente ereta,
acompanhada de ereção cônica da pelagem da cauda.
• Marcação de cheiro: Esfregar a área anogenital no substrato.
• Frown: O animal encara com os olhos abertos e sobrancelhas caídas. Ocorre em contexto agressivo, podendo ser acompanhado de vocalização erh-erh e de
“tufts flick stare”, no qual os tufos do animal se movem para trás e depois para
frente. Aqui foram registradas todas as ocorrências deste comportamento
durante o tempo de observação.
2. Interações Afiliativas:
• Contato físico: Contato de qualquer parte do corpo de um indivíduo com outro, com exceção da cauda.
• Catação:
Recebida: a pelagem do animal focal é catada por outro animal;
Realizada: o animal focal cata a pelagem de outro indivíduo.
3. Interações Sexuais:
Estas só foram registradas na segunda fase do experimento, com a introdução da
fêmea. Os registros ocorreram através da técnica de amostragem comportamental durante os
45 minutos de observação dos trios.
• Tentativa de cópula: Animal focal monta sobre a fêmea, mas esta recusa.
• Cópula: Macho monta sobre a fêmea, acompanhada de movimentos pélvicos. Como não foi possível se observar se houve cópula efetiva, reunimos os
comportamentos de cópula e tentativa de cópula em uma categoria única: comportamentos
sexuais.
5.4 Análise Hormonal:
As fezes de cada macho e fêmea foram coletadas antes do início das observações nas
duas fases do experimento e na etapa anterior as mesmas, para se verificar os níveis de
intervalo entre 06h30min e 09h30min da manhã, para evitar a influência circadiana sobre as
variáveis em estudo (SOUSA E ZIEGLER, 1998). Após a coleta, as amostras foram
armazenadas em freezer, aproximadamente a 5oC. Posteriormente, estas amostras foram
processadas para extração e dosagem hormonal através da técnica de ELISA de acordo com o
protocolo de Raminelli et al. (2001). O coeficiente de variação interensaio para o cortisol foi
de 5,22% e o coeficiente de variação intraensaio foi de 1,89%. Para a progesterona, o
coeficiente de variação interensaio foi de 9,93% e o coeficiente de variação intraensaio foi de
2,67%. A análise dos níveis de progesterona das fêmeas do presente estudo mostrou que as
mesmas apresentaram ciclos hormonais normais durante o período do experimento.
5.5 Classificação hierárquica dos machos:
Afim de saber se houve diferença hierárquica entre os machos observados, calculamos
o índice de DeVries (DEVRIES E APPLEBY, 2000; WHITEHEAD, 2008). Para isto,
somamos, para cada par de machos, os comportamentos agonísticos feitos para o outro
macho e os de submissão recebidos pelos mesmos.
5.6 Análise de dados:
As frequências dos comportamentos acima citados foram totalizados para cada sessão
de observação para os pares de saguis com parentesco e sem parentesco em todas as fases do
experimento e foi realizada uma comparação intra grupo e entre os grupos. Para testar se
houve normalidade, utilizamos o teste de Kolmogorof-Smirnoff. Devido a natureza dos
dados, optamos por utilizar análises não paramétricas. Para as comparações nas quais foram
contrastados dois grupos independentes, utilizamos o teste Mann-Whitney, para o contraste
de mais de dois grupos com medidas independentes utilizamos o teste Kruskal-Wallis. Nas
comparações de dois grupos com medidas relacionadas foi utilizado o teste de Wilcoxon e
para comparações com mais de duas medidas o teste de Friedman. Nestes testes o índice de
significância adotado foi 5% (bicaudal). Nas análises post hoc dos testes Kruskal-Wallis e
Friedman foram aplicadas comparações par a par utilizando o teste Mann-Whitney e
Wilcoxon, respectivamente. Nestas comparações foi aplicada a correção de Bonferroni a fim
de evitar o erro do tipo I. Os valores das concentrações fecais de cortisol de todas as fases do
estudo foram normalizados por meio de transformação logarítmica. Os dados foram
analisados através de modelos lineares generalizados (GLM) e o teste de Bonferroni nas
Para iniciar nossos experimentos, não conseguimos agrupar alguns pares de machos
na primeira tentativa de junção, pois os níveis de agressão eram bastante altos. O
estabelecimento dos pares foi acompanhado de perto, havendo separação dos pares se os
níveis de agressão se intensificassem, reagrupando-os no dia seguinte, até que os animais
dormissem juntos na gaiola. Esta situação ocorreu em dois pares de macho sem parentesco
como também em três pares com parentesco, dois dos quais possuíam dominância clara. Um
dos pares com parentesco com dominância contestada foi agrupado sem dificuldades na
primeira tentativa, mesmo estando separados um do outro por 4 anos. No outro par com
parentesco e dominância contestada, os machos brigaram bastante nas duas primeiras
tentativas de junção e um dos machos exibia comportamentos de agonismo e o outro de
submissão. Na terceira tentativa, ambos os machos começaram fugir um do outro e nenhum
dos dois exibiu comportamentos agressivos, somente de submissão. Também houve dois
casos nos quais machos sem parentesco, ao serem agrupados, não apresentaram nenhum
comportamento de agressão explícito, e minutos após a junção, os animais estavam em
contato físico e/ou em comportamento de catação.
6 RESULTADOS:
Fase I:
Após juntarmos os pares de machos em uma gaiola neutra, todos os animais exibiram
comportamentos de agonismo e/ou submissão. Calculamos o índice de DeVries através da
seguinte fórmula:
DAB= (IAB + 0.5)/(IAB + IBA + 1)
Onde: IAB= índice de interação do indivíduo A com o B;
IBA= índice de interação do indivíduo B com a A.
Estes índice foi calculado para cada par e observamos que em todos os pares de
machos sem parentesco, um dos machos assumia o posto de dominante e o outro de
subordinado (Tabela 01). Entre os machos com parentesco, dois dos pares apresentaram um
perfil de dominância clara entre eles. Já os outros dois pares não, embora um dos machos
apresentasse comportamentos agressivos mais frequentemente que o outro (Tabela 01). Desse
modo realizamos todas as análises comportamentais e hormonais nesta fase, considerando
três grupos: sem parentesco, com parentesco com dominância clara e com parentesco com
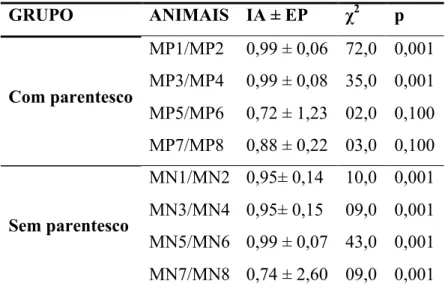
Tabela 01. Índice de DeVries na Fase 1 para os machos com parentesco e sem parentesco.
Os valores indicados são o índice de assimetria (IA), o valor do qui-quadrado (χ2) e o nível de
significância correspondente (p).
GRUPO ANIMAIS IA ± EP χ2 p
Com parentesco
MP1/MP2 0,99 ± 0,06 72,0 0,001
MP3/MP4 0,99 ± 0,08 35,0 0,001
MP5/MP6 0,72 ± 1,23 02,0 0,100
MP7/MP8 0,88 ± 0,22 03,0 0,100
Sem parentesco
MN1/MN2 0,95± 0,14 10,0 0,001
MN3/MN4 0,95± 0,15 09,0 0,001
MN5/MN6 0,99 ± 0,07 43,0 0,001
MN7/MN8 0,74 ± 2,60 09,0 0,001
Fonte: Autoria própria.
Os machos dominantes sem parentesco apresentaram maior frequência de
comportamentos agressivos que os subordinados, como esperado (U=1,00 p=0,03). No
entanto, os machos dominantes do grupo com parentesco com dominância clara apresentaram
os mesmos níveis agressivos que os subordinados deste grupo(U=0 p=0,10), ocorrendo o
mesmo com os machos de dominância contestada (U=0 p=0,12) (Fig. 1).
Todos os machos dominantes apresentaram níveis semelhantes de comportamentos de
agressão (χ2(2)=5,19 p=0,07). A mesma comparação foi feita entre os machos subordinados
dos diferentes grupos e nenhuma diferença na frequência deste comportamento foi
Figura 01. Frequência dos comportamentos agressivos ocorridos durante os 15 minutos de
observação entre os machos de C. jacchus dos grupos sem parentesco, com parentesco com dominância clara e com dominância contestada na primeira fase do experimento.
Fonte: Autoria própria.
Quanto aos comportamentos de submissão, os machos dominantes e subordinados dos
três grupos analisados se comportaram de maneira similar nesta fase do experimento (com
parentesco com dominância clara: U=0 p=0,10; com parentesco com dominância contestada:
U=2,0 p=1 e sem parentesco: U=6,0 p=0,31). Comparando os machos dominantes dos três
grupos percebemos que eles apresentaram frequência semelhante de submissão (χ2(2)=0 p=1),
Quanto às interações afiliativas, os machos com parentesco e os sem parentesco se
cataram (U=30,0 p=0,83) e estiveram em contato físico (U=24,50 p=0,43) com similar
frequência. Não encontramos diferença na frequência que o macho dominante catou o
subordinado e vice-versa nem no grupo dos machos com parentesco com dominância clara
(U=1,50 p=0,68), nem com dominância contestada (U=1,0 p=0,44) nem nos sem parentesco
(U=7,0 p=0,77). Na comparação entre os grupos, observamos que machos com parentesco
com dominância clara e contestada e os sem parentesco, dominantes (χ2(2)=1,0 p=0,61) e
subordinados (χ2(2)=1,10 p=0,57) apresentaram similar frequência deste comportamento.
Fase II:
Com a presença da fêmea na gaiola dos machos, o índice de DeVries foi mais uma
vez calculado para todos os pares (Tabela 02). Percebemos que as relações previamente
estabelecidas entre os machos na fase 1 foram reafirmadas nos casos nos quais houve uma
relação hierárquica clara. No caso dos dois pares de machos com parentesco com dominância
contestada, a presença da fêmea faz surgir a dominância clara, tornando-se dominante o
macho que apresentava maior frequência de comportamentos agonistas tanto nesta como na
fase anterior. Dessa forma apresentamos os resultados do grupo de animais com parentesco
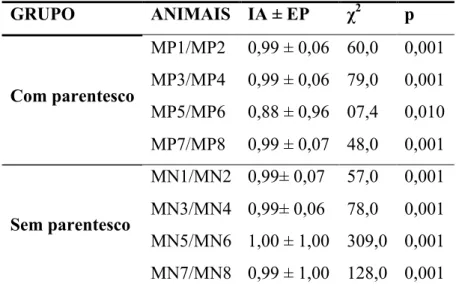
Tabela 02. Índice de DeVries na Fase 2 para os machos com parentesco e sem parentesco.
Os valores indicados são o índice de assimetria (IA), o valor do qui-quadrado (χ2) e o nível de
significância correspondente (p).
GRUPO ANIMAIS IA ± EP χ2 p
Com parentesco
MP1/MP2 0,99 ± 0,06 60,0 0,001
MP3/MP4 0,99 ± 0,06 79,0 0,001
MP5/MP6 0,88 ± 0,96 07,4 0,010
MP7/MP8 0,99 ± 0,07 48,0 0,001
Sem parentesco
MN1/MN2 0,99± 0,07 57,0 0,001
MN3/MN4 0,99± 0,06 78,0 0,001
MN5/MN6 1,00 ± 1,00 309,0 0,001
MN7/MN8 0,99 ± 1,00 128,0 0,001
Fonte: Autoria própria.
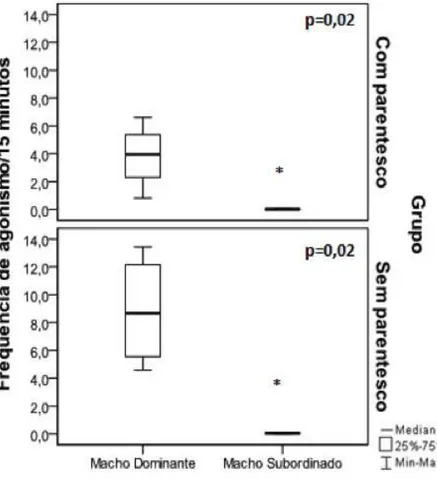
Com relação às interações agonísticas, os machos dominantes do grupo com
parentesco (U= 0 p=0,02) e dos sem parentesco (U=0 p=0,02) apresentaram maior frequência
de agressão que os subordinados de seus respectivos grupos (fig. 2). Não houve diferença na
frequência de agressão dos machos dominantes dos pares com parentesco e sem parentesco
(U=2,0 p=0,08). Da mesma forma para os machos subordinados, que se comportaram de
maneira similar nos dois grupos (U=5,0 p=0,37).
No grupo dos animais com parentesco, os machos dominantes e subordinados
apresentaram frequência de submissão semelhante (U=4,0 p=0,13). Já no grupo sem
parentesco, os machos subordinados apresentaram maior frequência deste comportamento
que os dominantes (U=2,0 p=0,04) (Fig. 3).
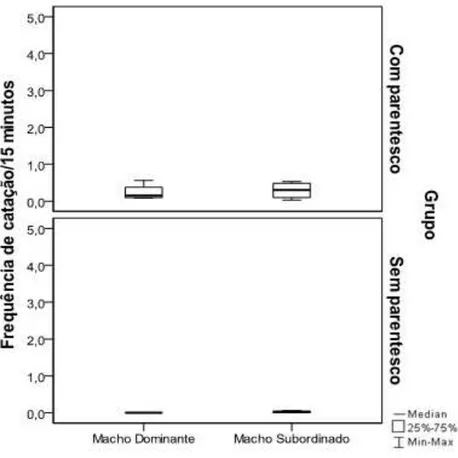
Com a entrada da fêmea, os machos do grupo com parentesco se cataram mais que os
do sem parentesco (U=1,50 p=0,001). Os machos dominantes (U=0, p=0,01) e os
subordinados (U=1,50 p=0,058) do grupo dos animais com parentesco cataram mais um ao
outro que os do grupo sem parentesco (Fig. 04). Nessa fase, machos pertencentes a ambos os
Figura 02. Frequência dos comportamentos de agonismo ocorridos durante os 15 minutos de
observação entre os machos de C. jacchus do grupo com parentesco e sem parentesco, na segunda fase do experimento.
Figura 03. Frequência dos comportamentos de submissão ocorridos durante os 15 minutos de
observação entre os machos de C. jacchus do grupo com parentesco e sem parentesco, na segunda fase do experimento.
Figura 04. Frequência dos comportamentos de catação ocorridos durante os 15 minutos de
observação entre os machos de C. jacchus do grupo com parentesco e sem parentesco, na segunda fase do experimento.
Fonte: Autoria própria.
Os machos dominantes, tanto no grupo com parentesco (U=1,0 p=0,04) quanto no sem
parentesco (U=0 p=0,02), exibiram comportamentos sexuais mais frequentemente que os
subordinados. A comparação dos machos dominantes (U=8,0 p=1) e dos subordinados
(U=5,50 p=0,46) mostrou frequência similar de comportamentos sexuais nas duas categorias,
Figura 05. Frequência de comportamentos sexuais dos machos de C. jacchus ocorridos durante os 15 minutos de observação por hierarquia (dominantes e subordinados) e por grupo
(com parentesco e sem parentesco) com a fêmea.
Fonte: Autoria própria.
Comparação entra as fases:
Os machos dominantes com parentesco mantiveram os mesmos níveis agonísticos de
uma fase à outra (Z= -1,80 p=0,07), enquanto os dominantes sem parentesco aumentaram as
agressões direcionadas ao macho subordinado (Z= -2,50 p=0,01). Os machos subordinados
do grupo com parentesco (Z= -0,40 p=0,65) e sem parentesco (Z= 0 p=1) mantiveram a
mesma frequência baixa de agressão da fase 1.
Os machos subordinados do grupo com parentesco (Z= -1,10 p=0,28) e sem
submissão da fase 1, ocorrendo o mesmo para os machos dominantes de ambos os grupos
(Z=0 p=1 para ambos os grupos).
Com a entrada da fêmea, a frequência de catação entre os machos diminuiu em
relação a fase 1 do experimento, tanto entre machos com parentesco (Z= -2,10 p=0,04)
quanto entre os sem parentesco (Z= -2,50 p=0,01). Já o contato físico não sofreu alterações
em sua frequência entre as fases [machos com parentesco (U= -1,50 p=0,14), sem parentesco
(U= -1,80 p=0,07)] .
Resultado Hormonal:
Não encontramos diferença na medida do cortisol entre as fases basal, 1 e 2 para
nenhum dos machos dos três grupos do estudo [grupo com parentesco com dominância clara
(F(2,8)=0,85 p=0,46), com parentesco com dominância contestada (F(2,8)=0,85 p=0,46) e
sem parentesco dominantes (F(2,6)=0,65 p=0,55) e subordinados (F(2,6)=0,77 p=0,51)].
Também não encontramos diferença significativa ao compararmos os machos dominantes e
subordinados dos três grupos estudados em nenhuma das fases.
7 DISCUSSÃO:
As relações de dominância se estabeleceram rapidamente na maioria dos pares de
machos, sob a modulação da relação de parentesco. Essas relações de dominância foram
reforçadas com a exibição mais frequente dos comportamentos de agressão.
Estes resultados mostram que o parentesco influenciou nas interações sociais apenas
em alguns pares de machos do experimento, corroborando em parte nossa predição inicial, a
qual estabelece que a relação de parentesco seria responsável por maior tolerância entre
machos com parentesco e maior competição entre os sem parentesco. Nem sempre foi isso
que ocorreu neste trabalho, já que o agonismo ocorreu em diferentes duplas de machos,
independente do parentesco apresentado entre eles e os comportamentos afiliativos ocorreram
em frequência similar entre todos os machos, independente do grupo.
De acordo com o índice de DeVries calculado para cada par de machos na primeira
fase do experimento, o grupo dos saguis sem parentesco apresentou uma relação de
dominância clara entre os machos. Os machos dominantes deste grupo apresentaram maior
frequência de agressão que os subordinados. Os machos subordinados não responderam a
esta maior frequência de agressão com comportamentos de submissão, já que a frequência
Nos machos com parentesco, duas duplas de machos apresentaram uma relação de
dominância clara, assim como aconteceu entre os machos sem parentesco. Nestas duplas, o
macho dominante também apresentou mais comportamentos de agressão que o subordinado.
Porém, em nossa análise estatística não encontramos diferença quantitativa para estes
comportamentos entre machos. Isto pode ter ocorrido provavelmente pelo pequeno número
de animais nesta categoria para análise estatística, apenas duas duplas. Nos outros dois pares
com parentesco, não houve uma relação hierárquica clara. Os níveis de agonismo e
submissão entre os machos foi bastante similar, não sendo possível diferenciar
estatisticamente o macho dominante do subordinado. Assim, denominamos estas duplas
como possuindo dominância contestada. Nestas duas duplas não houve agressão física entre
os machos e o agonismo, quando presente, foi um comportamento mais ritualizado (p.e.,
“tuf-flick stare”, piloereção), sendo sempre executado pelo macho que na segunda fase se
consolidou como o macho dominante da dupla.
Alencar et al. (2006) reportam situação similar de diferentes padrões de dominância
entre fêmeas aparentadas de C. jacchus. Nos pares em que havia dominância clara, a fêmea dominante exibia agonismo mais frequentemente que a subordinada, não havendo exibição
de comportamentos de submissão entre as mesmas. As fêmeas do grupo com dominância
contestada apresentaram frequência similar de comportamentos de agressão e submissão, mas
a dominante sempre exibia uma frequência um pouco maior de comportamentos agressivos.
Altos níveis de agressividade direcionado à animais intrusos têm sido relatado em
experimentos utilizando o paradigma do intruso. Este tipo de experimento é realizado em
cativeiro e imita encontros sociais de animais em campo, introduzindo indivíduos do mesmo
sexo ou do sexo oposto na gaiola de animais isolados, famílias ou casais de animais
(HARRISON E TARDIF , 1988). As espécies do grupo dos calitriquídeos têm sido relatadas
como bastante intolerantes à intrusos (FRENCH E SNOWDON, 1981; SUTCLIFF E
POOLE, 1978). Sutcliff e Poole (1984) relatam que quando intrusos do mesmo sexo de C. jacchus eram colocados nas gaiolas dos animais residentes, ambos residente e intruso eram bastante hostis um com o outro, menos quando eram parentes ou se já fossem familiarizados
um com o outro. A alta agressividade à intrusos ocorreria pois estes seriam seus potenciais
competidores.
Abbott (1984) percebeu que na formação de novos grupos por animais desconhecidos
entre si, os índices de agressão entre estes animais é alto até o estabelecimento das relações
de dominância. Estes altos níveis de agressividade a animais estranhos está relacionado a
(ANZENBERGER, 1985).
French e Inglett (1989, 1991) em estudo com Leontopitecus rosalia, também em cativeiro, mostraram que as fêmeas desta espécie eram bastante agressivas com outras fêmeas
intrusas. Já os machos apresentavam agonismo moderado direcionado a outros machos
intrusos. Os autores sugerem que a alta intolerância apresentada pelas fêmeas pode ser um
importante regulador das relações sócios-sexuais entre o casal reprodutor. A intolerância
direcionada à conspecíficos não familiares promoveria a exclusividade reprodutiva e
associação preferencial entre o par reprodutor. Em S. oedipus, French e Inglett (1991) encontraram que os machos eram altamente agressivos a outros machos intrusos, para
expulsar os potenciais competidores. As fêmeas possuíam baixos níveis de agressão às
intrusas, já que nesta espécie as mesmas inibem diretamente a capacidade reprodutiva de
outras fêmeas no grupo, não havendo competição por seu cargo de reprodutora.
Anzenberger (1985) e Araújo e Yamamoto (1993), em experimentos utilizando o
paradigma do intruso em C. jacchus, observaram que existia uma maior tolerância à intrusos
machos quando os residentes eram machos e já estavam previamente acasalados. Machos não
acasalados eram altamente agressivos com outros intrusos machos, assim como as fêmeas
acasaladas e não acasaladas eram com as fêmeas intrusas, sugerindo que os níveis de
agressão são mais altos quando as relações de dominância ainda não foram estabelecidas. No
campo, alta agressividade direcionada a animais intrusos do mesmo sexo foi encontrada em
trabalhos de Dawson (1978) em S. oedipus e Hubrecht (1985) em C. jacchus. Castro e Araújo
(2004) em trabalho em campo com C. jacchus, observaram o nível de agressividade durante
encontros entre grupos e a reação dos grupos aos intrusos. Os animais reprodutores
aumentaram os níveis de agonismo na presença de intrusos do mesmo sexo, o que sugere um
comportamento de defesa do parceiro sexual.
Após a junção dos machos de nosso experimento na primeira fase, as relações de
dominância começaram a se estabelecer, de maneira que em todos os oito pares de machos
estudados, o macho que iniciou os comportamentos de agressão foi aquele que se tornou o
macho dominante da dupla. As agressões cessaram, mas o agonismo ritualizado continuou a
ser exibido em baixa frequência, mantendo-se como reforço às novas relações hierárquicas
estabelecidas. Além disso, os machos de todos os grupos passaram boa parte do tempo de
observação em contato físico e se catando. Nos três grupos, machos dominantes e
subordinados se cataram com igual frequência, permanecendo mais próximos um do outro,
Diferentemente do que encontramos em nosso trabalho, Heymann (1996), Heymann e
Valdez (1988) e Lazaro-Perea, Arruda e Snowdon (2004) mostraram que existe uma
assimetria na frequência em que machos ou fêmeas catam outros membros do grupo do
mesmo sexo nos calitriquídeos, sendo os animais subordinados mais catados pelos
dominantes que o contrário. Harrison (1965) ao estudar aves e Rasa (1987) e Sparks (1967)
mamíferos sugerem que esse direcionamento na catação, dos machos dominantes para os
subordinados, funcionaria como um redutor de tensão entre estes animais, substituindo ou
redirecionando os comportamentos de agressão. No entanto, Lazaro-Perea, Arruda e
Snowdon (2004) não encontraram esta relação em fêmeas de C. jacchus. Os autores sugerem
que em grupos com reprodução cooperativa, os animais subordinados auxiliam aos
dominantes e o fato dos dominantes catarem mais os subordinados poderia ser visto como um
incentivo à sua permanência no grupo ou, como sugerem Zahavi e Zahavi (1997), como um
sinal de interesse em manter um vínculo social com estes animais.
Com a entrada da fêmea, as relações hierárquicas entre os machos foram reafirmadas
quando estas já eram claras, e estabelecidas nos casos dos pares aparentados com dominância
contestada. Nestas duplas, os machos que realizaram maior frequência de comportamentos de
agonismo ainda na primeira fase se tornaram os dominantes. Notamos que a frequência de
comportamentos de agonismo, principalmente a agressão e a perseguição, eram mais intensas
na primeira semana de observação, justamente onde as relações de dominância estavam se
reafirmando. Após estes primeiros contatos dos machos com a fêmea, notamos pouca ou
nenhuma agressão evidente entre os machos e um aumento dos comportamentos afiliativos
entre eles.
A competição pela fêmea levou os machos dominantes, tanto do grupo dos saguis
com parentesco, quanto dos sem parentesco, a realizarem maior frequência de
comportamentos de agressão que os subordinados de seus respectivos grupos, como também
a realizarem maior frequência de interações sexuais com a fêmea. Observamos que qualquer
tentativa de interação sexual pelo macho subordinado era impedida através do
comportamento de “tufs flick stare” ou, mais raramente, de agressões para afastá-lo da fêmea.
Por consequência, o macho dominante interagiu quase que com exclusividade com a fêmea.
A agressão clara aconteceu com pouca frequência. Apesar deste resultado, observamos que
em dois dos trios aparentados, um que possuía dominância clara e outro contestada na
primeira fase do experimento, ambos os machos interagiram sexualmente com a fêmea,
havendo pouco ou nenhum impedimento ou qualquer tipo de comportamento agressivo por
Schaffner e French (2004) agruparam pares de machos de C. kuhlii com e sem parentesco, os quais conviveram por um período de pelo menos 6 semanas. Os machos
apresentavam relações sociais estáveis, não havendo incidência de agressão entre eles e
havendo catação mútua e frequente contato físico. Os autores formaram grupos poliândricos
compostos por machos irmãos e observaram que não houve monopólio da fêmea por nenhum
dos dois machos nem competição evidente entre eles. Porém, não conseguiram formar grupos
poliândricos de animais sem parentesco, pois com a entrada da fêmea, a relação bem
estabelecida previamente entre estes machos foi abalada e comportamentos agonistas foram
intensificados, havendo vocalização agonística e de submissão, perseguição, agressão e a
presença do macho subordinado no canto inferior da gaiola, em postura de submissão. Estes
comportamentos foram similares aos que ocorreram em algumas duplas com e sem
parentesco no nosso trabalho na junção dos machos na primeira fase do experimento. Na
segunda fase, a entrada da fêmea não gerou tal reação comportamental em nenhum dos
grupos.
Ao compararmos o agonismo apresentado entre os machos de ambos os grupos antes
e depois da entrada da fêmea, pudemos perceber que entre os animais com parentesco, o nível
de agonismo se manteve o mesmo em ambas as fases, tanto para os machos dominantes,
como para os subordinados. Já entre os sem parentesco, os machos dominantes aumentaram a
frequência deste comportamento como consequência da entrada da fêmea. Como resposta a
este aumento no agonismo, os machos subordinados deste grupo aumentaram a frequência de
comportamentos de submissão. Este resultados corroboram as nossas predições que
estabeleciam uma disputa mais intensa pela posse da fêmea pelos machos sem parentesco.
Diferentemente do nosso experimento, as diferenças nos padrões de dominância se
mantiveram após a entrada de um macho não relacionado às fêmeas do experimento de
Alencar et al. (2006). Os autores observaram que fêmeas de C. jacchus com parentesco e dominância contestada apresentavam frequência similar de comportamentos de agonismo e
submissão. Mesmo com a entrada do macho continuou a competição pelo posto de
dominância nestes pares. Já nas fêmeas que apresentavam dominância clara, as dominantes
apresentavam maior frequência de comportamentos de agonismo que as subordinadas e estas
apresentaram maior frequência de comportamentos de submissão que as dominantes de seu
grupo, como também que as dominantes e subordinadas do grupo com dominância
contestada. Nestes pares, a dominante reforçou sua posição com alta frequência de
comportamentos de agonismo, e a subordinada respondeu à este agonismo através de
macho sem parentesco, que também possuíam uma relação de dominância clara. Estas
diferenças apresentadas entre machos e fêmeas de C. jacchus serão discutidas mais a frente.
Quanto aos comportamentos afiliativos, os machos de ambos os grupos diminuíram a
frequência de catação entre eles ao compararmos a primeira com a segunda fase. Isso
provavelmente ocorreu pela maior frequência de catação destinada à fêmea. Mesmo com esta
diminuição da frequência de catação nos dois grupos, os machos com parentesco se cataram
mais que os sem parentesco. Apesar do contato físico entre os machos dos dois grupos haver
sido estatisticamente semelhante, os machos com parentesco tenderam a apresentar maior
frequência deste comportamento, já que a mediana do grupo dos machos sem parentesco
estava mais próxima dos 25% interquartílicos. Isto pode indicar maior tolerância entre os
machos com parentesco que nos sem parentesco.
Yamamoto e Araújo (1991) em estudo semelhante ao nosso, agruparam pares de
machos gêmeos ou sem parentesco e encontraram uma alta frequência de agressão entre os
machos sem parentesco. Os gêmeos possuíam uma relação mais afiliativa, indicativa de
maior tolerância entre estes. O parentesco diminuiria a competição social entre os machos, já
que estes animais compartilham de genes comuns. Assim, os machos com parentesco são
menos agressivos e apresentam maior frequência de comportamentos afiliativos um com o
outro que aqueles machos sem relação de parentesco, pois a competição entre eles é menor já
que a reprodução de um parente também garantiria a passagem de seus genes adiante
(HAMILTON, 1964).
Harrison e Tardif (1988) em trabalho realizado com C. jacchus e S. oedipus em cativeiro observaram que em ambas as espécies, quando o macho intruso era parente do
macho residente, os níveis de agressão eram consideravelmente mais baixos em relação
àqueles apresentados entre animais sem parentesco, mesmo estes machos estando sem se ver
há pelo menos 4 meses. A preferência por parentes ocorreu em ambas as espécies, na
presença ou não de uma fêmea. Os autores sugerem que no campo, machos calitriquídeos
estariam mais aptos a admitir irmãos em um grupo já estabelecido que outros machos sem
parentesco, mesmo após longa separação. Em campo, Goldizen (1988) observou baixa
agressividade presente entre os machos poliândricos de S. fuscicollis, ausência de hierarquia
entre eles, raras interrupções de cópula um do outro com a fêmea, catação recíproca,
comportamento de carregar os filhotes do grupo realizado por ambos e até mesmo divisão
ocasional de alimento. A relação entre eles era mais afiliativa que agonista. O autor relata não
machos não eram parentes. Esta afirmativa sugere que a poliandria traria vantagens além do
aumento da aptidão direta ou indireta destes machos.
Este padrão de baixa agressividade entre os machos com parentesco de grupos
poliândricos encontrado em nosso trabalho corrobora dados de outros trabalhos realizados
com espécies de calitriquídeos (BAKER ET AL., 1993; GARBER ET AL., 1993;
GOLDIZEN, 1987; GOLDIZEN, 1989, HEYMANN, 1996; LAZARO-PEREA ET AL.,
1999; SOINI, 1987). Porém, nestes trabalhos, não houve clara definição de hierarquia entre
os machos, e ambos interagiam sexualmente com a fêmea sem haver agressão ou
interferência na atividade sexual realizada por algum dos machos.
Os trabalhos realizados em campo por Dawson (1979) e Neyman (1978) sugerem que
os padrões em cativeiro são similares ao que ocorre em campo. Estes trabalhos mostraram
que agressões e ameaças são bastante raras entre os machos, mesmo na presença de um
intruso macho desconhecido por eles. Os autores sugerem que baixos níveis de agressão
direcionados à animais intrusos poderiam ser um mecanismo no qual grupos menores
recrutariam ajudantes adicionais. Grupos maiores, mais estáveis e já contando com a ajuda de
sua prole mais velha, não precisariam de mais ajudantes e agiriam com grande agressividade
aos intrusos, por serem estes potenciais competidores reprodutivos.
Goldizen et al. (1996) estabelecem ser quase impossível para os casais reprodutores
de S. fuscicollis em campo criarem com sucesso sua prole sem a assistência de ajudantes. Nos
grupos de calitriquídeos, este auxílio provém de ajudantes não reprodutores, que auxiliam no
cuidado dos infantes e geralmente são a prole mais velha do casal reprodutor (TARDIF,
HARRISON E SIMEK, 1993). Mesmo não se reproduzindo diretamente, estes animais
recebem benefícios indiretos, aumentando sua aptidão indireta auxiliando no cuidado de seus
parentes para que os mesmos sobrevivam e também venham a se reproduzir, como também
estão ganhando experiência em cuidado parental (TARDIF, 1997). Claramente, a relação de
parentesco nestas situações explica porque os machos com parentesco seriam mais tolerantes
um com o outro. Faulkes, Arruda e Cruz (2003) realizaram análise genética de indivíduos de
diferentes grupos em campo, os quais já haviam sido previamente estudados quanto a sua
estrutura e relações sociais por outros autores. Observações prévias mostraram a imigração de
um macho de um grupo para outro. Neste novo grupo, este macho era um grande ajudante. A
análise genética mostrou que o macho imigrante era parente dos machos residentes do grupo
ao qual se juntou, justificando a sua grande frequência de ajuda destinada à este grupo, sendo
tal comportamento explicado pelo altruísmo por seleção de parentesco.
com parentesco do que aqueles sem parentesco, principalmente em pares ainda sem filhotes,
pois os mesmos representariam um auxílio extra na divisão dos custos do cuidado de seus
futuros filhotes. Este prerrogativa seria especialmente importante para espécies que possuem
sistema de reprodução cooperativo, como é o caso da espécie C. jacchus. Em cativeiro, os custos de criar a prole são menores, podendo os níveis de agonismo serem mais altos já que
os machos não se beneficiam com a poliandria neste caso. Sendo os machos parentes, os
níveis de agressão seriam baixos pois mesmo assim a aptidão indireta destes animais seria
mais alta (GOLDIZEN, 1988).
Ross, French e Orti (2007) encontraram uma correlação entre o cuidado parental nos
machos de Callithrix kuhlii e a presença de quimerismo epitelial. O quimerismo genético consiste na mistura de duas ou mais linhagens genômicas em um único indivíduo
(MCLAREN, 1976). Os machos de C. kuhlli carregavam infantes quiméricos com mais frequência que os não quiméricos. O quimerismo genético raramente ocorre em mamíferos,
mas em espécies de calitriquídeos é muito comum que os gêmeos fraternos troquem células
através do fuso coriônico nos primeiros estágios de seu desenvolvimento (BENIRSHKE,
ANDERSON E BROWNHILL, 1962), o que deve provavelmente influenciar nos
comportamentos de cooperação e conflitos apresentados por este grupo. Esta troca de
material genético mais comumente ocorre em tecidos epiteliais, porém foi encontrado
quimerismo genético em células do tecido germinativo de calitriquídeos, os quais
frequentemente transmitem alelos fraternos adquiridos no útero para sua própria prole,
evidenciando que nem sempre o animal que forneceu os gametas à uma prole é
necessariamente o pai genético da mesma (ROSS, FRENCH E ORTI, 2007).
Faulkes, Arruda e Cruz (2003, 2009) em estudo genético com famílias de C. jacchus
já previamente estudadas por outros pesquisadores, descobriram que os grupos familiares são
mais heterogêneos do que se pensava. Cinco dos nove grupos analisados possuíam animais
sem parentesco. Em um destes grupos, mais da metade dos componentes era formado por
animais que não possuíam relação de parentesco com o restante do grupo. Tais resultados
sugerem que outras questões, além do altruísmo por seleção de parentesco, devem estar por
trás da evolução do sistema de reprodução cooperativo de maneira que traga vantagens
evolutivas aos animais não reprodutores sem parentesco com o grupo.
Digby, Ferrari e Saltzman (2007) e Yamamoto et al. (2010) discutem o papel da
cooperação e da competição em calitriquídeos. Apesar deste grupo ser caracterizado por
relações sociais com cooperação e grande tolerância entre seus membros, a competição entre
mais intensa nas fêmeas, as quais se utilizam de supressão reprodutiva e comportamental para
reforçar seu monopólio reprodutivo e evitar os altos custos do cuidado da prole em um
sistema poligínico. Entre os machos existe a competição por tal posição, porém a relação
entre os mesmos no grupo parece ser mais afiliativa, havendo baixos níveis de agressão e
maior frequência de comportamentos afiliativos como catação e contato físico. Nas espécies
que apresentam sistema de reprodução mais cooperativo, a divisão de trabalho no grupo entre
os sexos parece diferir para os diferentes tipos de cuidado parental. As fêmeas são
responsáveis por todo custo energético da gestação e da lactação. Os machos adultos
carregam até duas vezes mais a prole que as fêmeas e este comportamento é bastante custoso,
só não mais que a lactação (GOLDIZEN, 1987; YAMAMOTO ET AL., 2008), justificando
uma maior tolerância apresentada entre os machos dos grupos que possuem reprodução
cooperativa devido à importância que os ajudantes têm nestes grupos.
As fêmeas de todos os grupos de nosso experimento engravidaram após o término das
observações. Os trios foram separados em média uma semana após o término das
observações por motivo de briga entre os animais ou devido à utilização de algum deles em
outros experimentos. As brigas ocorreram devido a mudança de gaiola, o que desestabilizou
as relações entre os animais dos trios, principalmente os machos. A chegada dos animais em
um novo território fez com que a competição pela posição de dominância entre os machos
naquele novo ambiente recomeçasse. Araújo e Yamamoto (1994) perceberam que colocar um
intruso do mesmo sexo na gaiola de machos ou fêmeas de C. jacchus gerava uma competição
entre estes saguis, marcada por altos níveis de agressão do macho residente para com o
intruso, indicando defesa do território pelo primeiro.
Somente um dos trios, formado por machos irmãos separados por uma geração,
permaneceu junto durante oito meses. Este par possuía dominância contestada na primeira
fase e foi observado compartilhando a posse da fêmea. Ambos os machos foram vistos
carreando os filhotes e não houve nenhum relato de briga entre os machos. O macho
subordinado só foi removido da família por motivo de doença que o levou a eventual óbito.
Os outros machos subordinados que foram separados dos trios foram acasalados e geraram
filhotes, mostrando que todos os machos do experimento eram funcionais e que a supressão
reprodutiva que estava ocorrendo no experimento poderia ser comportamental. Baker, Dietz e
Kleiman (1993) encontraram que quando fêmeas intrusas não familiares eram colocadas nas
gaiolas, só o macho dominante copulava com ela. Quando o macho subordinado ficava