AVALIAÇÃOIN VITRO DAS ALTERAÇÕES DO ESMALTE HUMANO, EFETIVIDADE CLÍNICA E SENSIBILIDADE PÓS-CLAREAMENTO
DENTÁRIO
Tese apresentada à Faculdade de Odontologia de São José dos Campos, Universidade Estadual Paulista, como parte dos requisitos para a obtenção do título de DOUTOR, pelo Programa de Pós-Graduação em ODONTOLOGIA RESTAURADORA, Especialidade em Endodontia.
Orientadora: Profa. Adj. Marcia Carneiro Valera
DEDICATÓRIA
Dedico este trabalho a essas pessoas que são as mais importantes na minha vida:
Aos meus pais, Mario e Mercedes, por todo o amor, carinho e dedicação que me foram dados durante toda a minha vida, sempre acreditando e
incentivando a mim e meus irmãos, nunca deixando que nos faltasse nada. A vocês, meus amados pais, minha eterna admiração e gratidão.
A Sandra, minha alma gêmea, pelo incansável apoio e compreensão, permitindo que meus objetivos se tornem mais claros. A você, pelo
sentimento de amor que nos une.
A Júlia, minha querida filha, pelas mudanças provocadas em minha vida e por despertar este sentimento maravilhoso em mim e em sua mãe.
AGRADECIMENTOS
A DEUS, por ter me abençoado, colocando pessoas tão boas em meu
caminho
À Profa. Adj. Márcia Carneiro Valera, por sua orientação segura e
sempre presente. Agradeço a confiança depositada desde a
graduação, passando pela especialização e também na
pós-graduação. Sua dedicação ao ensino, conduzida com muita
honestidade e dignidade, é uma grande lição para mim.
À Faculdade de Odontologia de São José dos Campos, pela oportunidade de realizar o curso de Pós-Graduação.
Ao Programa de Pós-Graduação em Odontologia Restauradora, coordenado pelo Prof. Adj. Clóvis Pagani.
Ao Departamento de Odontologia Restauradora, docentes e funcionários, pelo auxílio e amizade.
Aos professores da Disciplina de Endodontia – Márcia, Ana Paula, Alberto, Carlos Henrique, Cláudio e Simone, por terem-me recepcionado com muita amizade e companheirismo.
Ao Departamento de Materiais Odontológicos e Prótese, docentes, estagiários e funcionários, pelo apoio e agradável convivência.
Aos Profs. Lafayette Nogueira Junior, Eduardo Shigueyuki Uemura, Marcos Yasunóri Maekawa e Carlos Augusto Pavanelli, pelo apoio, orientação e principalmente pela amizade.
Aos grandes amigos: Luzia, Kazu e Luciana, por estarem sempre presentes, pelo apoio nos momentos de dificuldade, companheirismo e pela amizade intensa e verdadeira.
Aos colegas de curso: Ângela, Gustavo e André, pelo companheirismo durante nosso curso.
Aos amigos Wagner e Alexandre, pelos momentos agradáveis que passamos juntos.
Ao Prof. José Eduardo Junho de Araújo e à Profª. Maria Amélia Máximo de Araujo, pelo incentivo e orientação durante toda a minha formação acadêmica.
Aos professores Marcelo, Silvio, Rebeca, Karen e Alessandra, pelos agradáveis momentos.
Às funcionárias da Seção de Pós-Graduação, pela disposição em ajudar e atenção dispensada durante todo o curso.
Às funcionárias da Biblioteca, pela prestatividade e disposição.
Aos meus irmãos Cristina, Mônica, Sueli, Marcos, Márcia e Noêmia, por tudo que vivemos juntos desde a nossa infância.
A meus cunhados, cunhada, sobrinhos e sobrinhas, pelos momentos de alegria e descontração que me proporcionam
À família Akamine e ao amigo Alessio, por terem-me acolhido tão bem desde o início, pela convivência e apoio em todos os momentos.
Aos pacientes que participaram da fase experimental desta pesquisa.
Ao Prof. Ivan Balducci, pela realização da análise estatística, possibilitando a compreensão desta parte indispensável do trabalho.
Ao INPE, na pessoa da sra. Maria Lucia, pela prestatividade e colaboração para a execução da microscopia eletrônica de varredura.
SUMÁRIO
LISTA DE FIGURAS... 9
LISTA DE ABREVIATURAS E SIGLAS... 11
RESUMO... 12
1 INTRODUÇÃO... 14
2 REVISÃO DA LITERATURA... 19
2.1 Histórico do clareamento... 19
2.2 Efeito nos tecidos dentários: esmalte, dentina e ... 25
2.3 Efeito no tecido pulpar... 44
3 PROPOSIÇÃO... 62
4 MATERIAL E MÉTODO... 63
4.1 Avaliação dos efeitos clínicos após clareamento dentário... 63
4.1.1 Procedimentos pré-operatórios e operatórios:... 63
4.1.2 Análise estatística... 73
4.2 Avaliação das alterações no esmalte após clareamento... 74
4.2.1 Análise morfológica da superfície do esmalte e ... 78
4.2.2 Análise Estatística... 79
5 RESULTADOS... 80
5.1 Avaliação da cor dos dentes... 80
5.2 Avaliação da sensibilidade... 84
5.3 Espectrometria de energia dispersiva (EDS)... 86
5.4 Avaliação morfológica superficial do esmalte... 89
6 DISCUSSÃO... 95
6.1 Da metodologia... 95
6.1.1 Avaliação clínica... 95
6.1.2 Microscopia eletrônica de varredura (MEV) e ... 100
6.2 Dos resultados... 102
6.2.1.1 Avaliação colorimétrica... 102
6.2.1.2 Sensibilidade pós-clareamento... 105
6.3 Efeitos no emalte... 106
7 CONCLUSÕES... 112
8 REFERÊNCIAS... 113
ANEXO... 123
LISTA DE FIGURAS
FIGURA 1 Procedimentos pré-operatórios: a)Isolamento ... 64
FIGURA 2 Exemplo do sistema de rodízio... 66
FIGURA 3 Peróxido de hidrogênio utilizado e aplicação: ... 67
FIGURA 4 Fotoativação do peróxido de hidrogênio:... 68
FIGURA 5 Passos operatórios do clareamento nos grupos... 69
FIGURA 6 Peróxido de carbamida: a) Peróxido de carbamida... 70
FIGURA 7 Gel de flúor fosfato neutro incolor... 71
FIGURA 8 Escala Visual Análoga... 72
FIGURA 9 Delineamento experimental... 76
FIGURA 10 Passos operatórios do clareamento nos grupos ... 77
FIGURA 11 Diagrama de pontos (Dot Plot) dos escores de ... 81
FIGURA 12 Resultado do teste de comparação múltipla de ... 83
FIGURA 13 Diagrama de pontos (Dot Plot) dos escores de ... 84
FIGURA 14 Resultado do teste de comparação múltipla de ... 86
FIGURA 15 Diagrama de pontos (Dot Plot) das concentrações... 88
FIGURA 16 Fotomicrografia eletrônica de varredura de espécime.. 90
FIGURA 17 Fotomicrografia eletrônica de varredura de espécime.. 90
FIGURA 18 Fotomicrografia eletrônica de varredura de espécime.. 91
FIGURA 20 Fotomicrografia eletrônica de varredura de espécime.. 92
FIGURA 21 Fotomicrografia eletrônica de varredura de espécime.. 92
FIGURA 22 Fotomicrografia eletrônica de varredura de espécime.. 93
FIGURA 23 Fotomicrografia eletrônica de varredura de espécime.. 93
LISTA DE ABREVIATURAS E SIGLAS
ǖ Ângstrons
ANOVA Análise de variância
CO2 Dióxido de carbono
EDS Espectrometria por energia dispersiva
F- Flúor
h Horas LED Diodos emissores de luz
MEV Microscopia eletrônica de varredura mg miligramas
min Minutos ml Mililitros mm Milímetros
mW/cm2 Miliwatt por centímetro quadrado nm Nanômetro
PC Peróxido de carbamida PH Peróxido de hidrogênio
pH Potencial hidrogeniônico
s Segundos V Volts
Pg Micrograma
Pm Micrômetro
ºC Grau Celsius
Murakami JT. Avaliação in vitro das alterações do esmalte, efetividade clínica e sensibilidade pós-clareamento dentário [tese]. São José dos Campos: Faculdade de Odontologia de São José dos Campos, Universidade Estadual Paulista; 2007.
RESUMO
O objetivo deste trabalho foi avaliar: a) em humanos, a efetividade clínica e a sensibilidade pós-clareamento dentário; b) in vitro, as
1 INTRODUÇÃO
O clareamento dental tem-se tornado um dos tratamentos estéticos mais populares e intensamente procurados pelos pacientes, que buscam um sorriso mais harmonioso, simétrico e com dentes mais brancos, por ser um tratamento menos agressivo aos tecidos dentais e de fácil execução pelo profissional90.
Antes de se instituir o tratamento de clareamento, é importante diagnosticar as causas do escurecimento, que podem ser endógenas ou exógenas75 pois, de acordo com a etiologia, as alterações de cor podem ser tratadas de maneiras diferentes. Além disto, o clareamento pode ser realizado em dentes com vitalidade pulpar ou em dentes tratados endodonticamente. O clareamento de dentes com vitalidade pulpar pode ser realizado pelo método caseiro, em consultório ou a técnica associada (caseiro + consultório). Para o restabelecimento da cor dos dentes tratados endodonticamente pode-se utilizar a técnica mediata (também chamada walking bleaching), a técnica imediata (termocatalítica) ou ainda a associação de técnicas para dentes com vitalidade pulpar e para dentes tratados endodonticamente.
O clareamento de uso caseiro ou doméstico normalmente utiliza o peróxido de carbamida 10%, 16% e 22%, ou o peróxido de hidrogênio 3 a 9%55, 95, enquanto que os agentes clareadores utilizados no consultório incluem o peróxido de hidrogênio 30-38%, o peróxido de carbamida 35-37%, o perborato de sódio e o ácido clorídrico 18% ou 36%63,68,70,82,95.
imediatamente43,67,71,72; entretanto, a desvantagem desta técnica é que despende maior tempo clínico e maior custo para o paciente5,46.
O mecanismo de ação do peróxido de hidrogênio ou carbamida é semelhante, uma vez que o peróxido de carbamida dissocia-se em peróxido de hidrogênio e uréia. O peróxido de hidrogênio em contato com os dentes, por ser altamente instável, se decompõe em dois subprodutos: água e oxigênio nascente23. O oxigênio oriundo dessa reação é o responsável pelo clareamento propriamente dito. Devido ao seu baixo peso molecular, ele apresenta um alto poder de penetrar nas porosidades do esmalte dental e dentina, transformando substâncias pigmentadas em substâncias intermediárias que possuem coloração mais clara, resultando na conversão dos materiais orgânicos em dióxido de carbono e água45,68.
Os pigmentos são cadeias moleculares longas de alto peso molecular (macromoléculas) e portanto difíceis de serem eliminados da estrutura dental. O oxigênio promove a quebra das macromoléculas dos pigmentos por meio de reações de oxirredução. Durante o processo de clareamento, compostos de anéis de carbono altamente pigmentados são abertos e convertidos em cadeias que são mais claras na cor; compostos de carbono com ligação dupla, usualmente pigmentados de amarelo, são convertidos em grupos hidroxilas (tipo álcool) que são geralmente incolores. Além disso, ao final do processo as moléculas, agora menores, são total ou parcialmente eliminadas da estrutura dental por um processo de difusão5,99.
Embora as técnicas de clareamento produzam resultados estéticos favoráveis, existe a toxicidade das substâncias empregadas para essa finalidade e seus efeitos biológicos sobre os tecidos dentários.
Na técnica do clareamento no consultório, a irritação da gengiva ocorre quando a proteção do tecido gengival não é bem executada por meio do isolamento absoluto. Pelo fato de se utilizar peróxido de hidrogênio em elevadas concentrações e tratando-se de uma substância cáustica aos tecidos moles, todos os cuidados são necessários no momento do isolamento absoluto, a fim de evitar o escoamento do produto sobre a gengiva e tecidos adjacentes. O contato do agente clareador com os tecidos moles pode produzir ardência e inflamação, fatores que dificultam a higienização da região pelo paciente. Entretanto, esse tipo de irritação normalmente desaparece após algumas horas.
A irritação tecidual provocada no tecido pulpar pelos peróxidos também tem sido estudada, embora alguns autores acreditem que estes efeitos sejam reversíveis, desde que a utilização dos agentes clareadores seja adequada29,30,84. Clinicamente, o principal e mais comum efeito colateral do clareamento em dentes com vitalidade pulpar é a sensibilidade dentária6,32.
Para maior compreensão dos efeitos dos peróxidos sobre a polpa, diversos estudos de penetração do peróxido ao interior da cavidade pulpar16 e de citotoxicidade têm sido realizados a fim de verificar o grau de agressão ao tecido pulpar frente a agentes e técnicas de clareamento42. Oberva-se nestes estudos que o tecido pulpar apresenta a capacidade de neutralizar o peróxido de hidrogênio através da produção de enzimas. Porém, Bowles & Burns13 verificaram que o peróxido inativa a ação destas enzimas apresentando, portanto, potencial tóxico.
confirmaram e quantificaram a penetração de peróxidos de hidrogênio para o interior da câmara pulpar através de diferentes metodologias, sendo a penetração tanto maior quanto maior a concentração e tempo de exposição do agente clareador10,37,42,74,91.
Quanto aos efeitos provocados no esmalte, dentina e cemento, estudos demonstram alterações na textura superficial dos dentes clareados, sendo observadas erosões, porosidades e depressões; além da diminuição da microdureza. Alterações na composição química da estrutura dental, como proporção cálcio/fósforo também foram observadas, principalmente quando se utilizaram peróxidos de hidrogênio em altas concentrações80. Outro estudo demonstrou aumento da permeabilidade do esmalte à penetração de corantes, quando exposto a materiais clareadores17.
A potencialização dos agentes químicos clareadores por alguma fonte de calor pode ser realizada por raios infravermelhos, espátula aquecida e luzes que geram calor. Porém, esse aumento da temperatura pode causar injúrias ao tecido pulpar. Neste aspecto, o uso do LED como ativador trouxe melhorias para a técnica de clareamento em consultório, já que resulta em menor aquecimento, quando comparado a outras fontes de luz88.
2 REVISÃO DA LITERATURA
Este capítulo apresenta uma revisão de literatura sobre o histórico do clareamento, efeito nos tecidos dentários: esmalte, dentina e periodonto e efeito no tecido pulpar.
2.1 Histórico do clareamento
Goldstein et al.38 (1989) ressaltam que há mais de um século o clareamento é eficaz no tratamento de manchamentos dentários. Os autores consideram o clareamento como tratamento de escolha, embora também possa ser realizado em associações a restaurações adesivas, facetas laminadas de porcelana ou tratamentos protéticos para a obtenção do clareamento de um sorriso inteiro. O peróxido de hidrogênio, utilizado para o clareamento, apresenta baixo peso molecular e habilidade de desnaturar proteínas, o que aumenta a movimentação de íons através da estrutura dentária. Embora exista preocupação quanto à permeabilidade das estruturas dentárias ao peróxido de hidrogênio, especialmente seu potencial de penetração para o interior do esmalte e dentina, este peróxido é o agente clareador de escolha.
ao éter ou ácido clorídrico, aplicados principalmente com uso associado de calor. As sessões variavam de 20 a 30 minutos, e ao final da década de 80, o condicionamento ácido prévio da superfície do esmalte passou a ser empregado para facilitar a ação do peróxido de hidrogênio sobre a estrutura dental.
Em 1989, Haywood e Heymann47 descreveram uma técnica inovadora para o clareamento de dentes com vitalidade pulpar, que consiste na aplicação do agente clareador, peróxido de carbamida, em uma moldeira plástica individual, recobrindo as superfícies dentárias com mínima sobreposição aos tecidos gengivais, utilizada pelo paciente durante a noite. Após a adaptação da moldeira, cada espaço correspondente ao dente a ser clareado era preenchido com duas a três gotas de peróxido de carbamida 10%. O material era removido pela manhã durante a escovação dos dentes. Os resultados da exposição de sete a oito horas, durante cinco semanas de tratamento, mostraram que os dentes clarearam o equivalente a dois tons da escala Vita. O clareamento caseiro noturno tornou-se uma alternativa eficaz ao método de clareamento convencional e passou a ser indicado pelos autores como primeira opção de tratamento.
necessidade de novos estudos com o intuito de esclarecer os possíveis efeitos deste tratamento sobre os tecidos.
Machado e Frasca61 (1994) relembram que o prognóstico do tratamento clareador está relacionado ao fator etiológico do manchamento. O manchamento dental pode ser resultado de fluorose, ingestão de tetraciclina, trauma ou escurecimento pelo envelhecimento. Para as manchas castanhas de fluorose, manchamento discreto por tetraciclina ou escurecimento devido ao envelhecimento o prognóstico é mais favorável. Segundo os autores, as técnicas mais usadas para o clareamento de dentes com vitalidade pulpar são o clareamento caseiro e de consultório, que empregam tanto o peróxido de hidrogênio como o peróxido de carbamida, substâncias de baixo peso molecular e capazes de penetrar através do esmalte e para o interior dos túbulos dentinários, agindo também na dentina mais profunda.
o uso insistente de produtos clareadores resulte apenas em maiores perdas minerais e agressões periodontais.
Barghi7 (1998) avaliou a aplicação prática do clareamento de dentes vitais, bem como as vantagens e desvantagens de diferentes técnicas. O autor relata que existe uma maior procura pelos pacientes pela técnica realizada em consultório, devido ao maior conforto e rapidez dos resultados e tendo como vantagem a supervisão e controle pelo profissional. Por outro lado, 62% dos profissionais preferem ainda o clareamento caseiro, devido à maior simplicidade da técnica. A escolha da técnica a ser utilizada deverá seguir alguns fatores clínicos, como: sensibilidade dos dentes, manchamento por tetraciclina, necessidade de clareamento de todos os dentes (anteriores e posteriores), necessidade de clarear apenas um dente vital, hábitos parafuncionais ou disfunções temporomandibulares, manchamentos interproximais. Além disso, o autor destaca a colaboração do paciente, tempo de tratamento e custo como fatores a serem analisados para escolha da técnica de clareamento.
teste térmico. Observaram que o peróxido de hidrogênio promoveu alteração de cor e sensibilidade estatisticamente maiores quando comparado com o peróxido de carbamida.
Rotstein81 (2000) relatou que a descoloração dos dentes pode muitas vezes ser tratada com sucesso através do clareamento. Os procedimentos para o clareamento são mais conservadores do que os métodos restauradores, além de serem relativamente simples de serem executados e apresentarem custos menores. Podem ser realizados intracoronariamente nos dentes não vitais e extracoronariamente nos dentes vitais. Soluções de várias concentrações de peróxido de hidrogênio, perborato de sódio e peróxido de carbamida são comumente utilizados. Os peróxidos de hidrogênio e de carbamida estão principalmente indicados para o clareamento extracoronário, ao passo que o perborato de sódio é indicado para o clareamento intracoronário. Os agentes clareadores, principalmente os oxidantes, agem na estrutura orgânica dos tecidos duros dentais, degradando-os lentamente em subprodutos químicos, como o dióxido de carbono, que apresentam coloração mais clara. Muitos procedimentos de clareamento utilizam o peróxido de hidrogênio porque ele é instável e se decompõe em oxigênio e água. O peróxido de carbamida, por sua vez, libera baixas concentrações de peróxido de hidrogênio e, por isso, requer um maior tempo de exposição ou uma maior concentração.
Christensen20 (2003) apresenta a evolução e mudanças nos materiais e técnicas de clareamento, bem como as vantagens e desvantagens de cada técnica. O autor relata que todos os métodos e materiais possuem sua indicação, não existindo uma total superioridade em uma das técnicas. O autor relata não haver trabalhos na literatura comprovando a efetividade e efeitos adversos do uso da fonte de luz e calor nos métodos que utilizam peróxidos em altas concentrações nas técnicas de clareamento em consultório.
Araújo et al.3 (2005) relatam que os agentes clareadores empregados na técnica de clareamento de consultório são peróxido de hidrogênio de 35-38% (Superoxol® ou Peridrol, Opalescence XtraBoost®) e peróxido de carbamida a 35-37%. A técnica de clareamento de consultório possui como vantagens: controle do processo de clareamento, maior rapidez de resultado em relação à técnica de clareamento caseiro e possibilidade de clarear apenas alguns dentes. Entretanto, apresenta algumas desvantagens, como maior tempo operatório e clínico, alto custo e sensibilidade devido à utilização de agentes clareadores com alta concentração.
2.2 Efeito nos tecidos dentários: esmalte, dentina e periodonto
da resposta celular após a difusão do agente clareador através da dentina. No primeiro experimento pode-se verificar que a citotoxidade do peróxido de hidrogênio sobre cultura de células aumentou proporcionalmente a sua concentração e pelo período de tempo, sendo que no período de 6 horas houve maior citotoxicidade. No segundo experimento observou-se que quantidades significantes de peróxido de hidrogênio penetraram através da dentina em um período de tempo menor que 15 minutos. O terceiro experimento sugere que no período de 15 minutos os agentes clareadores usados na pesquisa são capazes de causar danos ao tecido pulpar levando a uma possível resposta inflamatória. Os autores concluem que, antes da aplicação do agente clareador sobre dentes com vitalidade pulpar, é importante verificar alguns fatores como espessura da dentina e se existem áreas de dentina exposta.
resultados mostraram que, in vitro, o agente clareador é tóxico aos fibroblastos gengivais, inibindo várias funções celulares. Os autores afirmam que enzimas presentes no meio bucal, como a catalase, glutatione peroxidase e a lactoperoxidase, são capazes de neutralizar o agente clareador, protegendo os tecidos e seus componentes celulares de possíveis efeitos adversos.
Em geral, as taxas de cálcio e fósforo diminuíram mais no cemento e na dentina do que no esmalte, provavelmente devido a diferenças nos componentes orgânicos e inorgânicos destes tecidos. O peróxido de hidrogênio 30% foi o único agente que diminuiu significativamente a taxa de cálcio e fósforo dos tecidos dentários. Os autores concluíram que os agentes clareadores podem causar danos aos tecidos dentários, e portanto devem ser usados com cautela.
Bitter11 (1998) realizou um estudo in vivo com o propósito de avaliar os efeitos dos agentes clareadores sobre a superfície do esmalte após o clareamento. Foram selecionados três pacientes que possuíam dentes condenados à extração por cárie ou problemas periodontais, sendo escolhidos catorze dentes. Os pacientes foram moldados e foi confeccionada uma moldeira de acetato para a realização do tratamento clareador que consistiu na utilização desta toda noite por um período de trinta minutos. Após um período de 14 dias, dois dentes de cada paciente foram extraídos e preparados para avaliação em microscópio eletrônico de varredura. Novas extrações foram realizadas em 21, trinta e noventa dias após o término do tratamento clareador. O grupo controle, onde não foi aplicado o agente clareador, demonstrou uniformidade na camada superficial aprismática e indicação de desgaste fisiológico devido à exposição bucal. Depois de 14 dias da exposição ao agente clareador pode-se observar uma remoção parcial da camada aprismática e início da exposição de prismas de esmalte. Em 21 dias, a exposição e desmineralização dos prismas de esmalte são evidentes. Depois de trinta dias de exposição ao agente clareador, permaneceu a perda da camada aprismática e ocorreu severa exposição dos prismas do esmalte, mostrando severidade aumentada após noventa dias do término do clareamento. Esse estudo concluiu que o efeito do clareamento no esmalte pode levar ao longo do tempo a aumento de desgaste do esmalte ou fratura de cúspides, principalmente em dentes restaurados. Os autores reforçam a necessidade de informar aos pacientes as alterações no esmalte e efeitos prejudiciais sobre a estrutura dental como conseqüência do uso prolongado dos agentes clareadores.
se inicia quando o pH encontra-se em torno de 6,0. Os autores relembram que o local preferencial de penetração dos agentes clareadores é a região cervical, no limite amelo-cementário. Portanto, se estas áreas estiverem expostas, recomendam o uso de agentes dessensibilizantes, para promover o selamento dos túbulos e reduzir a permeabilidade dentinária desta região. Citaram ainda uma possível alteração na matriz orgânica do esmalte promovida pela utilização de peróxido de carbamida, já que trabalhos mostram redução na resistência à abrasão e dureza. Os autores consideraram que, embora existam diversas investigações sobre os efeitos biológicos dos produtos clareadores sobre os tecidos dentários, muitas vezes as metodologias descritas permanecem confusas e contraditórias. Ressaltam que mais pesquisas devem ser realizadas e que o clareamento por períodos prolongados deve ser evitado.
término do tratamento. Os autores concluíram que o Opalescence é um agente de clareamento dental seguro e efetivo.
molecular do peróxido de hidrogênio que pode penetrar no esmalte afetando a fase orgânica do mesmo.
Jones et al.51 (1999) avaliaram a eficácia de técnicas de clareamento pela observação da mudança de cor de dentes extraídos e submetidos a três técnicas de clareamento: peróxido de hidrogênio 35% ativado com laser de argônio (5 aplicações de 3 minutos com ativação de 30 segundos); peróxido de carbamida 10% e 20% (14 aplicações de 2 horas). Um quarto grupo (controle) não recebeu nenhum tratamento clareador. As cores dos dentes foram avaliadas antes do tratamento clareador e após 7 e 14 dias. O grupo controle não apresentou diferenças de cor durante os períodos analisados. O grupo do laser não apresentou diferenças estatisticamente significantes em relação ao grupo controle; entretanto houve diferenças entre os grupos dos peróxidos de carbamida 10 e 20% e o grupo controle. Os autores concluem que a exposição ao peróxido de carbamida 20% apresentou o maior efeito de clareamento e que o clareamento em sessão única com peróxidos em altas concentrações parece não ser eficiente e pode necessitar de técnicas adicionais ou maior tempo de aplicação.
aspectos semelhantes aos que foram submetidos ao tratamento durante três semanas. Os cortes correspondentes ao período de tratamento de seis semanas exibiram aspectos atípicos na morfologia e coloração. Os autores concluíram que nas condições experimentais do trabalho o esmalte dentário, sob ação do peróxido de carbamida 10% após seis semanas de tratamento, exibiu aspectos morfológicos atípicos e sugestivos de alterações estruturais.
Gultz et al.41 (1999) analisaram, por MEV, os efeitos de agentes clareadores na morfologia superficial do esmalte dental. Utilizaram dentes humanos extraídos que foram divididos em quatro grupos: grupo I - controle (nenhum tratamento); grupo II – dentes tratados com Opalescence Quick (peróxido de carbamida 35%); grupo III – dentes tratados com Opalescence Xtra (peróxido de carbamida 35%); grupo IV – dentes condicionados com ácido fosfórico 35% por 15 a 20 segundos. O peróxido de carbamida foi aplicado por 2 horas na face vestibular do dente e foi previamente aquecido em água por 3 minutos para acelerar a atividade do material; o peróxido de hidrogênio foi aplicado por 8 a 10 minutos com fotoativação por 4 minutos com aparelho fotopolimerizador. Todos os espécimes foram preparados para avaliação em MEV, que indicou que apenas o grupo IV (ácido fosfórico) exibiu um padrão de condicionamento do esmalte. Não foram encontradas diferenças na morfofologia superficial do esmalte entre o grupo controle e os espécimes submetidos às duas técnicas de clareamento.
Os dentes foram cortados longitudinalmente e montados em stubs com a parte interna voltada para cima. Após impregnação com carbono, avaliaram-se, através de Espectrometria por Dispersão de Energia (EDS), as concentrações de oxigênio, cálcio e fósforo em diferentes profundidades (1, 5 e 10Pm) e localização na superfície vestibular (1/3 médio, cervical e incisal). Após análise estatística, verificaram diferença para o fósforo, que apresentou redução nos seus valores sob ação do agente clareador. Já para o cálcio e oxigênio não houve diferença estatisticamente significante entre o grupo não clareado e o grupo clareado. Também não verificaram diferenças quanto à profundidade (1, 5 ou 10Pm) ou quanto à localização (1/3 cervical, médio ou incisal).
com 12h em saliva). A avaliação por microscopia eletrônica de varredura revelou que houve variação na morfologia da superfície do dente de acordo com os diferentes protocolos utilizados. Os espécimes do grupo controle mostraram que o padrão da superfície do esmalte é diferente em dentes erupcionados e não-erupcionados. O peróxido de hidrogênio 35% promoveu aumento na rugosidade de superfície nos espécimes tratados de acordo com o protocolo 1. A morfologia padrão dos espécimes tratados com o protocolo 2 foi marcada pela presença de partículas e glóbulos esféricos incorporados na estrutura mineralizada do esmalte. Uma superfície lisa e brilhante foi observada nos espécimes tratados pelo protocolo 3. Apesar das mudanças observadas na superfície do esmalte após o clareamento e considerando as características morfológicas da superfície dentária, o clareamento, como foi descrito no estudo, pode ser considerado um procedimento seguro ao esmalte.
fosfórico 37% ou com ácido fosfórico + agente clareador demonstraram morfologias diferentes na superfície do esmalte. Os autores concluíram que a exposição do esmalte ao peróxido de hidrogênio 35% não foi capaz de danificar a superfície deste tecido dentário. Entretanto, mais estudos devem ser realizados com intuito de garantir uma aplicação segura do agente clareador sobre a superfície do esmalte por tempos mais longos.
Deliperi et al.24 (2004) avaliaram clinicamente a combinação do clareamento em consultório com a técnica caseira. Utilizaram 10 pacientes que tiveram metade dos dentes superiores clareados com peróxido de hidrogênio 35 % e metade com 38%, ambos por 30 minutos, complementada com peróxido de carbamida 10% por 60 minutos. Este procedimento foi repetido por 3 dias consecutivos. Avaliaram-se as alterações de cor antes e após o clareamento com o auxílio de uma escala de cores Vita. Além disso, avaliou-se a sensibilidade pós-clareamento: 1-nenhuma; 2-discreta; 3-moderada; 4-considerável; 5-severa. Nenhum paciente relatou sensibilidade pós-operatória e os resultados mostraram um clareamento significante nos grupos dos peróxidos 35% (8,5) e 38% (9,0), porém sem diferenças estatísticas entre si. Os autores concluem que esta técnica associada produz resultados satisfatórios, com média de 5 escalas de cor em um tempo bastante reduzido.
aplicação por um tempo maior foi prejudicial ao componente orgânico da dentina e permitiu a dissolução de quantidades significantes de cálcio.
Park et al.73 (2004) avaliaram esmalte bovino submetido ao agente clareador peróxido de hidrogênio 30% por longos períodos. Utilizaram duas avaliações: teste de microdureza e avaliação em espectrofotômetro Raman. Avaliaram inicialmente as alterações morfológicas com o uso de microscópio de força atômica, seccionando cinco incisivos bovinos longitudinalmente ao meio, sendo metade armazenada em água destilada e que serviram como controle; a outra metade foi clareada com peróxido de hidrogênio 30% (Sigma Chemical Co., USA) por 120 horas ininterruptamente. A morfologia superficial foi então avaliada nas duas metades antes e após o experimento. Para a avaliação do espectro Raman, dentes bovinos foram cortados e adaptados em um porta-amostra. O espectro inicial foi anotado e serviu como controle. As amostras foram então imersas na mesma solução clareadora por 120 horas. Em seguida, foram lavadas, secas e avaliadas novamente no espectrofotômetro. Outros sete incisivos bovinos seguiram o mesmo protocolo de clareamento e foram avaliados quanto a microdureza superficial. Os autores não encontraram diferenças para o espectro FT-Raman para os espécimes clareados e não clareados. Quanto a microdureza, os autores encontraram uma diminuição significativa após o clareamento. Entretanto, os valores de microdureza do esmalte submetido ao clareamento e o armazenado em água destilada não mostraram diferenças estatísticas. Os autores concluem que apesar de o peróxido de hidrogênio dissolver componentes orgânicos e minerais do esmalte dental e de tornar esta superfície mole e menos compacta, este clareador parece ser seguro e necessita de mais estudos.
realizada a aplicação do produto clareador e os testes de dureza Knoop utilizando um aparelho microdurômetro. Os primeiros valores foram obtidos antes do clareamento e serviram como controle. Os grupos experimentais foram divididos em: OX – peróxido de hidrogênio 35% Opalescence Xtra (Ultradent, South Jordan, Utah), após 5, 15 e 35 minutos de clareamento e fotoativação com aparelho halógeno Optilux 400 (Demetron); OQ – peróxido de carbamida 35% Opalescence Quick, após 5, 15 e 35 minutos de clareamento; OF – peróxido de carbamida 15% Opalescence F verificado de hora em hora por 14 horas; O – peróxido de carbamida 10% Opalescence verificado de hora em hora por 14 horas. Os testes de microdureza foram realizados após o clareamento e após a imersão dos espécimes em solução de fluoreto de estanho 0,05% por 5 minutos. Os valores de microdureza foram transformados em porcentagem, sendo os valores do grupo controle adotados como 100%, sendo calculada a porcentagem de redução após as condições experimentais. Após o teste de ANOVA, verificaram uma diminuição na microdureza diretamente proporcional ao tempo em todos os grupos experimentais. Comparando OX e OQ, verificaram um efeito mais acentuado no primeiro grupo em dentina e em esmalte, que apresentou a maior redução de microdureza (25%) após 35 minutos de aplicação. Comparando OF e O, verificaram um efeito mais acentuado no primeiro grupo em dentina e em esmalte. A imersão em fluoreto por 5 minutos restaurou a dureza da dentina e esmalte em todos os grupos em valores similares ao grupo controle (inicial).
peróxido de carbamida 10% (8 horas), peróxido de carbamida 20% com flúor (8 horas) e peróxido de hidrogênio 35% (30 minutos). Após o clareamento, os espécimes foram desmineralizados em um modelo de cárie microbiano in vitro e então analisados utilizando um scanner microscópico a laser. Os resultados demonstraram que não houve diferenças estatísticas entre os espécimes clareados e não clareados nos grupos de peróxido de carbamida 10% e peróxido de hidrogênio 35%. Entretanto os espécimes tratados com peróxido de carbamida 20% com flúor foram menos susceptíveis a cáries que o grupo controle. O autor concluiu que os agentes clareadores não aumentaram a susceptibilidade à cárie em esmalte humano.
Candido et al.17 (2005) avaliaram a permeabilidade do esmalte bovino exposto ao peróxido de hidrogênio e peróxido de carbamida em diferentes concentrações, sendo empregados de forma contínua ou intercalados por saliva artificial. Utilizaram 121 incisivos bovinos distribuídos de acordo com o agente clareador e o armazenamento em saliva artificial. Após impermeabilização e colocação em corante de azul de metileno, os dentes foram seccionados para avaliação da penetração do corante. Os autores verificaram que a infiltração foi diretamente proporcional ao tempo de aplicação e à concentração do agente clareador. Verificaram ainda que a infiltração foi menor nos grupos onde foi intercalada a saliva artificial. Desta forma, concluíram que a exposição à saliva apresentou um importante papel na redução da permeabilidade do esmalte dentário durante o tratamento clareador, e que o emprego de agentes clareadores por tempos excessivos pode aumentar significativamente esta permeabilidade.
Schiavoni et al.83 (2006) avaliaram a permeabilidade do esmalte após a utilização de clareadores. Utilizaram 75 caninos humanos, que tiveram as raízes cortadas e desprezadas. A porção radicular da coroa foi selada com resina composta. Em seguida, uma área circular de 7,1mm2 na face vestibular foi delimitada, sendo o restante impermeabilizado com três camadas de esmalte para unhas. Os dentes foram então divididos nos grupos experimentais: peróxido de carbamida (CP) 10% e 16% - 4 horas diárias por 21 dias; PC 37% - 3 aplicações consecutivas de 20 minutos com intervalo semanal por 21 dias; peróxido de hidrogênio (PH) 35% - duas aplicações consecutivas de 15 minutos com intervalo semanal por 21 dias. O grupo controle foi armazenado em saliva artificial durante todo o experimento. A avaliação da permeabilidade do esmalte foi realizada por método histoquímico através da penetração de sulfato de cobre. A infiltração deste marcador foi obtida após a secção dos espécimes no sentido vestíbulo-lingual e leitura e digitalização em um microscópio com aumento de 50X. O PC 10% e o PH tornaram o esmalte mais permeável, quando comparado ao grupo controle. Não houve diferenças estatisticamente significantes entre os grupos experimentais.
consultório são menos eficazes para remoção de depósitos de pigmentos em dentina.
Turssi et al.94 (2006) avaliaram o aumento da permeabilidade do esmalte após clareamento com fotoativação. Utilizaram caninos humanos, que foram clareados com peróxido de hidrogênio 35% por 3 sessões de 10 minutos. Os dentes clareados foram ativados ou não com LED/laser ou lâmpada halógena por 30 segundos. Os grupos controles não foram clareados e foram armazenados em saliva artificial. Espécimes foram analisados por método histoquímico colorimétrico com penetração de sulfato de cobre analisado em microscópio óptico. A permeabilidade foi analisada em imagens digitalizadas da penetração dos íons de cobre na espessura do esmalte. Os resultados não mostraram diferenças nos grupos clareados fotoativados ou não, bem como entre as diferentes fontes de fotoativação. Entretanto, todos os grupos clareados mostraram altos valores de permeabilidade quando comparados com os grupos não-clareados.
2.3 Efeito no tecido pulpar
suas raízes seccionadas e o tecido pulpar eliminado. A face vestibular da coroa permaneceu exposta enquanto as demais partes foram isoladas com cera pegajosa. O interior da câmara foi preenchido com solução salina fisiológica, permanecendo a face vestibular exposta aos agentes de tratamento durante cinco minutos. A penetração das substâncias testadas através do esmalte e dentina para o interior da câmara pulpar foi determinada através do marcador radioativo fosfato, incorporado às soluções testadas. A solução foi removida do interior da câmara pulpar e adicionada a uma mistura de cintilação, que permitiu quantificar o fosfato que penetrou para o interior da câmara pulpar. Após a quantificação do agente radioativo presente no interior da câmara, os dentes foram submetidos a um segundo teste, para determinar se os tratamentos executados alteraram a permeabilidade dentária. Para isso, os dentes foram lavados durante vinte minutos para eliminar qualquer resíduo de fosfato, sendo em seguida imersos em solução salina contendo iodo durante um período de 24 horas. Os resultados encontrados mostraram não haver diferença estatisticamente significante entre os grupos quanto à penetração de fosfato. Os autores concluíram que nenhuma das soluções testadas foi capaz de atravessar o esmalte e a dentina e que, tanto o ácido clorídrico como a solução de McInnes desmineralizaram a superfície do esmalte, mas não o suficiente para provocar aumento na permeabilidade dentária.
dentes foram imediatamente imersos em solução de formalina por 48 horas, lavados e descalcificados em solução de ácido fórmico, Os dentes foram seccionados no sentido longitudinal e corados pela técnica de hematoxilina e eosina para exame histopatológico. A camada odontoblástica dos dentes clareados estava intacta, exceto próximo a junção amelo-cementária em 36% dos dentes. Nestes casos, foi observada aspiração do núcleo do odontoblasto para dentro dos túbulos dentinários. Entretanto, o autor conclui que, nestas condições, o clareamento com calor e peróxido de hidrogênio 35% pode ser considerado inofensivo para o tecido pulpar.
ou não ao calor não causou resposta inflamatória significante comparada ao grupo controle.
A resposta pulpar foi avaliada ainda por Baumgartner et al.8 (1983) utilizando a técnica modificada de McInnes que consiste na associação do clareamento, desgaste e remoção química da mancha. Pré-molares de nove pacientes foram tratados pela técnica modificada de McInnes ou da mesma maneira que os dentes do grupo experimental, entretanto substituindo o agente clareador por solução salina fisiológica (controle). A mistura clareadora era composta por 1ml de ácido clorídrico 36%, 1ml de peróxido de hidrogênio 30% e 0,2ml de éter etílico. Essa mistura foi aplicada por 3 vezes de 5 minutos seguida do desgaste superficial do esmalte por 15s, totalizando 15 minutos de aplicação do agente clareador e 45s de desgaste. Para a neutralização do agente clareador os dentes foram lavados com solução de hipoclorito de sódio 5,25% e extraídos após intervalos de 1, 3, 5, 7, 9, 11, 13, 17 ou 19 dias do tratamento clareador. Na análise macroscópica observou-se que a técnica modificada de McInnes promoveu maior perda de esmalte quando comparado ao grupo controle. A avaliação histológica microscópica da polpa revelou pequena ou nenhuma resposta pulpar depois do tratamento clareador. Verificou-se uma reação inflamatória leve em algumas amostras dos grupos experimentais e controle que pode ser atribuída ao desgaste do esmalte ou aos procedimentos de extração dentária. Ainda que a aplicação do mistura clareadora não cause significante reação pulpar, ela é capaz de remover quantidades substanciais de esmalte o que poderia afetar, a longo prazo, o prognóstico da polpa. Portanto, é importante que o clínico seja cuidadoso na remoção de esmalte durante o tratamento clareador pela técnica modificada de McInnes.
um método de clareamento que causasse o mínimo de danos ao tecido pulpar. O estudo foi realizado in vivo em seis cães que receberam inicialmente administração de tetraciclina. Após a erupção dos dentes permanentes, com manchamento amarelado induzido pela tetraciclina, os dentes caninos de cada animal foram submetidos à aplicação do peróxido de hidrogênio 35% associado ao calor (62oC) durante 15, 30 ou 45 minutos. Foram realizadas quatro sessões em intervalos de quinze dias em cada grupo, sendo que o grupo controle permaneceu sem qualquer tratamento. Os cães foram sacrificados em períodos de 13, 62 e 92 dias após a última sessão do tratamento clareador e os dentes foram preparados para análise microscópica. Verificou-se que, quanto mais longo o período de aplicação do peróxido de hidrogênio e calor, mais severas foram as respostas pulpares, evidenciando a formação de dentina reparadora, achatamento dos odontoblastos, hemorragia pulpar e presença de infiltrado inflamatório crônico. Os autores concluíram que os danos causados à polpa são reversíveis, mas contra-indicam tratamentos clareadores por períodos prolongados já que quanto maior o tempo de contato do produto com o esmalte, maior é a sua penetração em quantidade e profundidade.
final variando de 1,25 a 1,5%; c) o extrato pulpar foi exposto ao peróxido de hidrogênio em concentrações de 2,5, 7,5 e 15% e em seguida imerso em banho quente por 7,5, 15 e 30 minutos, respectivamente; d) controle – o extrato pulpar foi diluído em solução de tampão fosfato. Após os tratamentos, as amostras sofreram diálise e a estas foram adicionadas duas gotas de catalase para remover o peróxido de hidrogênio remanescente que pudesse interferir na análise enzimática. A atividade enzimática foi determinada pela análise em espectrofotômetro. Observou-se que quando o extrato pulpar sofreu tratamento com calor, somente algumas enzimas mostraram variações consideráveis em sua atividade. A sensibilidade enzimática decresceu significativamente quando em contato com o peróxido de hidrogênio isoladamente. No entanto, as enzimas pulpares foram inibidas quando houve a associação do peróxido de hidrogênio com aplicação do calor. Os resultados do estudo sugerem que o dano das células pulpares decorrentes do clareamento pode resultar em inativação das enzimas e conseqüente interrupção das atividades celulares normais.
leucocristal. Os valores de densidade óptica das soluções foram mensurados em espectrofotômetro, sob um comprimento de onda de 596nm, e posteriormente comparados a uma curva padrão de peróxido de hidrogênio, levantada a partir de concentrações conhecidas de peróxido correspondentes a valores específicos de absorbância. Os maiores valores de penetração puderam ser observados em amostras tratadas com peróxido de hidrogênio 30% (25,4+8,5µg), seguidos do peróxido de hidrogênio 10% (5,8+2,6µg) e peróxido de hidrogênio 1% (1,8+1,7µg). Nas amostras tratadas com peróxido de hidrogênio 10% e calor (25,5+9,3µg), a quantidade de peróxido encontrada no interior da câmara foi equivalente àquela observada nas amostras tratadas com peróxido de hidrogênio 30%. Os autores concluíram que a penetração de peróxido de hidrogênio para o interior da câmara pulpar é estatisticamente significante, estando principalmente relacionada à concentração da solução aplicada e à temperatura de aplicação.
pulpar é muito pequena e sugerem que há necessidade de cautela no uso de agentes clareadores em dentes com vitalidade pulpar.
Cooper et al.22 (1992) avaliaram a quantidade de peróxido de carbamida que penetra para o interior da câmara pulpar quando comparado ao peróxido de hidrogênio. Uma vez que o peróxido de carbamida se decompõe em peróxido de hidrogênio, foi possível quantificar o peróxido de hidrogênio liberado a partir do peróxido de carbamida. Neste estudo, foram utilizados dentes anteriores humanos que tiveram suas raízes seccionadas e o tecido pulpar coronário extirpado. A câmara pulpar foi preenchida com tampão acetato e o dente foi submetido ao clareamento com gel de peróxido de carbamida (10% ou 15%) ou gel de peróxido de hidrogênio (5% ou 30%). Toda a coroa permaneceu exposta ao agente clareador a 37oC durante 15 minutos. A solução tampão foi removida do interior da câmara para reagir em um tubo de ensaio com peroxidase e corante violeta leucocristal, sendo as densidades ópticas das soluções registradas em espectrofotômetro calibrado a 596nm. Posteriormente, estes dados foram convertidos em microgramas de peróxido de hidrogênio a partir de uma curva padrão estabelecida previamente, a partir de quantidades conhecidas de peróxido de hidrogênio. Os resultados obtidos foram estatisticamente significantes sendo, respectivamente: peróxido de carbamida 10% - 3,3+0,38µg; peróxido de carbamida 15% - 4,8+0,27µg; peróxido de hidrogênio 5% - 10,4+0,24µg; peróxido de hidrogênio 30% - 40,4+3,51µg. Os autores concluíram que ocorre menor penetração para o interior da câmara pulpar a partir do peróxido de carbamida quando comparado ao peróxido de hidrogênio livre.
ácidas e básicas, além do efeito do calor e da presença de íons metálicos na sua decomposição. As seguintes soluções foram testadas: peróxido de hidrogênio 30%; peróxido de hidrogênio associado ao ácido clorídrico 36% e éter (semelhante a solução de McInnes); peróxido de hidrogênio 30% e cloreto férrico; peróxido de hidrogênio 30% e hidróxido de cálcio. A liberação de gás oxigênio foi mensurada à temperatura ambiente (20oC) e após aquecimento a 45oC. Verificou-se que a maior liberação de oxigênio ocorreu na solução de peróxido de hidrogênio 30% e hidróxido de cálcio em temperatura ambiente. Ainda observou-se que a decomposição do peróxido de hidrogênio 30% isolado foi acelerada pelo calor. Assim, os autores recomendam a utilização do peróxido de hidrogênio à temperatura ambiente para minimizar possíveis danos ao tecido pulpar.
Haywood44 (1997) relatou trabalhos mostrando que uma pequena quantidade de peróxido de carbamida 10% alcançou o interior da câmara pulpar em 15 minutos de exposição ao produto, Segundo ele, os produtos resultantes da decomposição do peróxido de carbamida (peróxido de hidrogênio e uréia) atravessam facilmente o esmalte e dentina devido à permeabilidade destes substratos. Dessa forma, o clareamento dental é capaz de, além de eliminar manchas intrínsecas ou extrínsecas, promover o clareamento das próprias estruturas dentais, esmalte e dentina. O autor ressalta que o peróxido de hidrogênio 35% chega à polpa muito mais rapidamente, sendo que em 15 minutos de exposição há penetração doze vezes superior à quantia de peróxido obtida a partir do peróxido de carbamida 10%. Mesmo registrando tamanha agressão, o autor considera que não há dano pulpar irreversível.
grupos: 17 dentes foram clareados com peróxido de carbamida 10% durante 4 horas e 14 dentes não receberam clareamento. Os dentes foram extraídos, fixados, desmineralizados, congelados, seccionados e marcados histoquimicamente com anticorpo anti-heme-oxigenase-1. O controle negativo foi feito em dois cortes de cada grupo, que não receberam marcação. O controle positivo foi feito com cortes de baço de rato, por se tratar de tecido com maior quantidade da enzima dentre todos os tecidos estudados. Os autores observaram ausência de reação inflamatória e marcação mais intensa das células da camada odontoblástica, que são as primeiras células a responder às agressões externas. Estes achados indicam que a polpa responde ao estresse oxidativo em nível molecular, o que pode explicar a reversibilidade dos danos causados durante o clareamento.
California) e Rembrandt Lighten (Den-Mat, Santa Maria, California). A análise de variância mostrou uma diferença estatisticamente significativa nos níveis de peróxido de hidrogênio entre os três grupos (p<0,05). Os autores concluíram que a penetração do peróxido de carbamida varia conforme a marca comercial, podendo resultar em diferentes níveis de sensibilidade dentinária e diferença na eficácia do clareamento.
Supõe-se que a profundidade, o tamanho da restauração e o tempo de exposição ao agente clareador possam afetar a taxa de penetração do agente clareador para o interior da câmara pulpar.
concentração do agente clareador do que do tempo em que o agente fica em contato com as estruturas dentais.
Lozada et al.59 (2000) confirmaram que a sensibilidade dentária pós-tratamento clareador está relacionada com a passagem das substâncias clareadoras através do esmalte e dentina, produzindo uma ligeira irritação pulpar. Normalmente a sensibilidade pós-operatória é relatada após uma semana de clareamento, sendo significativamente maior quando se utilizam soluções de peróxido de carbamida em concentrações superiores a 15%. Os autores ressaltam ainda que a sensibilidade dentária está mais relacionada ao baixo peso molecular do agente clareador do que ao eventual baixo pH dos produtos clareadores.
Esposito et al.28 (2003) examinaram a capacidade protetora da polpa dentária humana em relação ao peróxido de hidrogênio em condições de saúde pulpar ou pulpites reversíveis e irreversíveis através da determinação da atividade da catalase. No estudo foram avaliadas clinicamente e radiograficamente as condições dos tecidos pulpares de 35 pacientes, verificando que 11 tecidos pulpares estavam sadios, 12 apresentavam pulpite reversível e 12 apresentavam pulpite irreversível. Em seguida, as polpas foram extirpadas, pesadas e homogeinizadas obtendo-se um extrato pulpar que foi adicionado a uma solução tampão de fosfato. A degradação do peróxido de hidrogênio em contato com o extrato pulpar foi analisada pela atividade da enzima catalase. A atividade da catalase foi de 1,61 +/- 0,23Umg(-1) em polpas sadias, de 2,99 +/- 0,45Umg(-1) em pulpites reversíveis e de 2,44 +/- 467Umg(-1) em pulpites irreversíveis. Verificou-se que houve uma maior atividade da catalase em tecidos pulpares inflamados comparados com a polpa sadia, pois ocorre um mecanismo defensivo contra o peróxido de hidrogênio que é liberado durante tais processos inflamatórios. A atividade enzimática mostrou-se maior na pulpite reversível comparada com a irreversível, devido a capacidade de reparação do tecido neste tipo de inflamação pulpar. Além disso, a baixa atividade enzimática na pulpite irreversível pode ser atribuída a progressão do processo inflamatório que levaria a depleção ou diminuição da catalase. Esses resultados apontam que a enzima catalase possui um importante papel durante a inflamação do tecido pulpar em humanos e, portanto demonstra o inerente sistema defensivo biológico da polpa dentária contra os agentes oxidantes.
de carbamida 35%. A câmara pulpar foi preenchida com solução de tampão de acetato, sendo em seguida a coroa exposta aos agentes clareadores durante 60 minutos. Os resultados mostraram que o procedimento restaurador aumentou a penetração dos agentes clareadores para o interior da câmara pulpar, sendo esta penetração concentração-dependente. Concluíram que embora ainda sejam necessárias mais investigações sobre a penetração de agentes clareadores para o interior da câmara pulpar in vivo, os resultados deste estudo sugerem que os agentes clareadores em baixas concentrações podem ser usados com segurança em dentes restaurados.
Joiner e Thakker52 (2004) realizaram um estudo in vitro para determinar a quantidade de peróxido de hidrogênio encontrada no interior da câmara pulpar de dentes tratados com Xtra White (peróxido de hidrogênio 6%). Foram utilizados caninos e incisivos humanos hígidos que tiveram as câmaras pulpares preenchidas com solução tampão de acetato, sendo em seguida, a coroa exposta ao agente clareador ou à água durante 20 minutos. Os resultados mostraram que baixos níveis (0,37µg) de peróxido de hidrogênio foram encontrados no interior da câmara pulpar de dentes tratados com Xtra White (peróxido de hidrogênio 6%) depois de 20 minutos de tratamento. Deste modo, a quantidade de peróxido encontrada no interior da câmara pulpar de dentes expostos ao Xtra White é infinitamente menor que o necessário para causar inativação de enzimas pulpares. Além disso, a penetração do peróxido para dentro da câmara pulpar in vitro não acontece como na cavidade bucal, onde há degradação do peróxido por peroxidases. Os autores concluem que o agente clareador testado no estudo pode ser usado com segurança em dentes hígidos, pois não é prejudicial ao tecido pulpar.
Pretti et al.76 (2004) estudaram, in vitro, a penetração do peróxido de hidrogênio 35% (Whiteness HP) e peróxido de hidrogênio 38% (Opalescence Xtra Boost) para o interior da câmara pulpar de dentes bovinos submetidos ao clareamento externo. Concluíram que no clareamento externo com peróxido de hidrogênio em concentrações iguais ou superiores a 35%, ocorre penetração do peróxido para o interior da câmara pulpar.
(2004) avaliaram in vitro a possível penetração de dois agentes clareadores (peróxido de hidrogênio 6,5% e 14%), contidos nestas tiras, para o interior da câmara pulpar. Vinte e quatro incisivos centrais superiores humanos foram divididos em três grupos. Todos os dentes foram seccionados 3mm apical à junção amelo-cementária, o tecido pulpar foi removido e a câmara pulpar foi preenchida com uma solução tampão de acetato. Nas superfícies vestibulares das coroas foi acoplada a tira contendo o agente clareador por 30 minutos; os dentes do grupo controle foram expostos apenas à água destilada. Os resultados indicaram que o agente clareador contendo 14% de peróxido de hidrogênio penetrou mais que o peróxido de hidrogênio 6,5%. Os autores concluíram que concentrações mais altas de peróxido de hidrogênio são capazes de penetrar mais para o interior da câmara pulpar que concentrações mais baixas deste agente. Entretanto, mais estudos são necessários para avaliar o comportamento clínico e outras propriedades das tiras de clareamento.
Para avaliar o aumento da temperatura intrapulpar resultante de diferentes fontes fotoativadoras para clareamento, Eldeniz et al.27 (2005), compararam quatro fontes de luz: fotopolimerizador convencional, fotopolimerizador de alta potência, LED e laser diodo. A temperatura foi medida no interior da câmara pulpar. Todos os métodos de fotoativação apresentaram aumento significativo (entre 6oC e 11,7oC). Os autores alertam para os efeitos deletérios e capacidade de causar danos ao tecido pulpar, quando se utilizam essas fontes fotoativadoras.
Os autores verificaram penetração para a câmara pulpar em todos os grupos e diretamente proporcional à concentração do clareador. Entretanto, os autores não contra-indicam o uso clínico destes novos materiais e indicam a necessidade de novos trabalhos clínicos e outras propriedades destes novos materiais.
3 PROPOSIÇÃO
Este trabalho propõe avaliar:
a) em humanos, a efetividade clínica e a sensibilidade pós-clareamento dentário;
b) in vitro, as alterações morfológicas e na composição química do esmalte após clareamento.
4 MATERIAL E MÉTODO
4.1 Avaliação dos efeitos clínicos após clareamento dentário
Este projeto foi submetido ao comitê de ética em pesquisa da Faculdade de Odontologia de São José dos Campos – UNESP (protocolo no 064/2005–PH/CEP) (Anexo A) e todos os pacientes leram o texto de esclarecimento e assinaram o consentimento da pesquisa.
Para a execução deste trabalho foram utilizados 60 dentes pré-molares humanos, com indicação para exodontia por motivos ortodônticos, em pacientes com idade entre 16 e 25 anos.
4.1.1 Procedimentos pré-operatórios e operatórios
Foi realizada a verificação da cor de todos os dentes a serem submetidos ao tratamento clareador. Para isto utilizou-se uma escala de cores Vita® (Vita, Zahnfabrik, Alemanha) sob luminosidade natural. Para o clareamento, os dentes foram isolados com dique de borracha (Figura 1a) e em seguida receberam profilaxia dental com escovas de Robson, em baixa rotação, com pedra-pomes e água (Figura 1b).
FIGURA 1 – Procedimentos pré-operatórios: a)Isolamento absoluto; b) Profilaxia com pedra-pomes e água.
Os dentes foram divididos em grupos de acordo com a técnica de clareamento e agente clareador utilizados (Quadro 1):
x Grupo 1 (n=10): dentes clareados com peróxido de hidrogênio 35%; aplicação por 40 minutos, com fotoativação pela luz emitida pelos LED (diodos emissores de luz);
x Grupo 2 (n=10): dentes clareados com peróxido de carbamida 35%; aplicação por 40 minutos, com fotoativação com LED;
x Grupo 3 (n=10): dentes clareados com peróxido de hidrogênio 35%; aplicação por 40 minutos sem fotoativação;
x Grupo 4 (n=10): dentes clareados com peróxido de carbamida 35%; aplicação por 40 minutos sem fotoativação;
b
x Grupo 5 (n=10): dentes clareados com peróxido de hidrogênio 35%; aplicação por 40 minutos, com fotoativação com LED e aplicação tópica de flúor;
x Grupo 6 (n=10): dentes clareados com peróxido de carbamida 35%; aplicação por 40 minutos, com fotoativação com LED e aplicação tópica de flúor;
QUADRO 1 – Divisão dos grupos de acordo com as técnicas de clareamento e agente clareador.
Grupos Agente
clareador Fotoativação Procedimento imediato após o clareamento
G1 Peróxido de
hidrogênio 35%
LED ________
G2 Peróxido de
carbamida 35%
LED ________
G3 Peróxido de
hidrogênio 35%
____ ________
G4 Peróxido de
carbamida 35% ____ ________
G5 Peróxido de
hidrogênio 35% LED Aplicação tópica de flúor
G6 Peróxido de
carbamida 35%
LED Aplicação tópica de flúor
Grupo 1 Grupo 2
Grupo 3 Grupo 4
Paciente 1
Grupo 5 Grupo 6
Grupo 1 Grupo 2
Paciente 2
Grupo 3 Grupo 4
Grupo 5 Grupo 6
Paciente 3
Grupo 1 Grupo 2
Grupo 3 Grupo 4
Paciente 4
FIGURA 2 – Exemplo do sistema de rodízio.
Para o clareamento, o peróxido de hidrogênio 35% (Whiteness HP - FGM Produtos Odontológicos Ltda. – Joinville - Brasil) utilizado nos grupos 1, 3 e 5 foi aplicado seguindo as instruções do fabricante. Para isto, foi obtido um gel pela mistura da fase Peróxido – FASE 1 (peróxido de hidrogênio 45-50%) com a fase Espessante – FASE 2 (Figuras 3a e 3b). O gel obtido, de coloração vermelha, foi aplicado na superfície vestibular dos dentes com auxílio de um pincel, formando uma camada de aproximadamente 2mm de espessura (Figura 3c).
FIGURA 3 – Peróxido de hidrogênio utilizado e aplicação: a) Agente clareador utilizado – Fase 1 e Fase 2; b) Gel de peróxido de hidrogênio 35% após a mistura; c) Aplicação do gel de peróxido de hidrogênio com pincel.
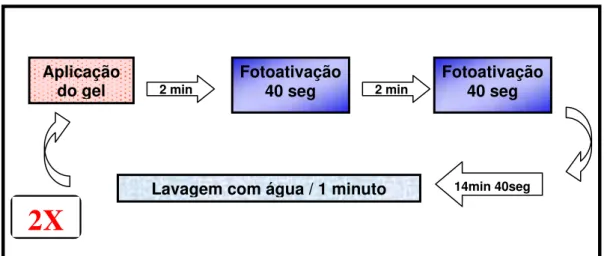
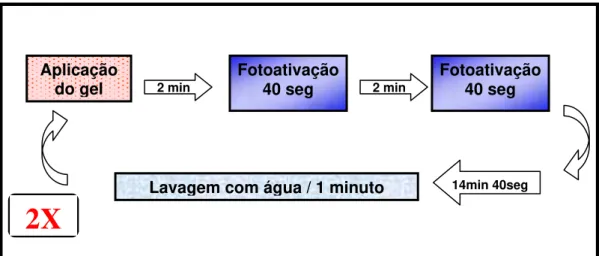
Nos grupos 1 e 5, após aplicação do gel de peróxido de hidrogênio na superfície vestibular, aguardou-se dois minutos e em seguida foi realizada fotoativação inicial com diodos emissores de luz (LED). Foram realizadas duas fotoativações utilizando o aparelho Three Light (Clean Line – São José dos Campos) (Figura 4a) em alta intensidade, de 40 segundos cada (Figura 4b), com intervalo de 2 minutos entre as fotoativações e aguardando 14 minutos e 40 segundos até totalizar 20 minutos de aplicação.
b
c
FIGURA 4 – Fotoativação do peróxido de hidrogênio: a) Aparelho utilizado para fotoativação; b) Peróxido de hidrogênio sendo fotoativado com LED.
Após 20 minutos, o dente foi lavado com água durante 1 minuto, e feita uma nova aplicação do gel clareador, seguindo os mesmos procedimentos anteriormente citados, totalizando 40 minutos (2 aplicações de 20 minutos cada) (Figura 5).
FIGURA 5 – Passos operatórios do clareamento nos grupos com fotoativação.
No grupo 3, o gel de peróxido de hidrogênio foi aplicado e mantido por 40 minutos na superfície vestibular dos dentes, com uma renovação após 20 minutos, sem fotoativação e com a luz do refletor apagada.
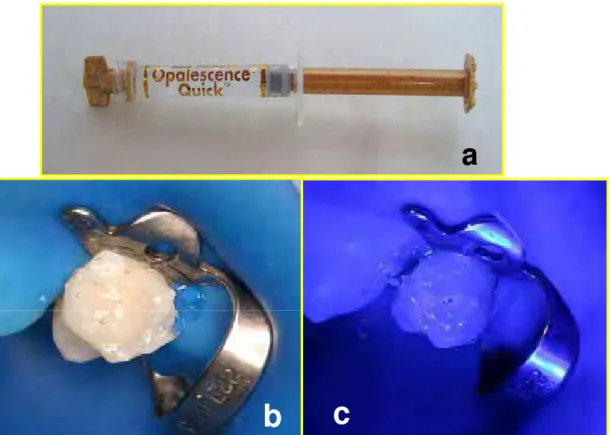
O peróxido de carbamida 35% (Opalescence Quick - Ultradent – South Jordan – Utah – USA) utilizado nos grupos 2, 4 e 6 (Figura 6a ) foi aplicado com o auxílio de uma seringa na superfície vestibular dos dentes, formando uma camada de aproximadamente 2mm de espessura.
Nos grupos 2 e 6, o gel de peróxido de carbamida foi aplicado na superfície vestibular do dente de modo a formar uma camada com aproximadamente 2 mm de espessura (Figura 6b), sendo que após a aplicação foram aguardados 2 minutos e em seguida foi realizada a fotoativação (Figura 6c), seguindo os mesmos procedimentos realizados para os grupos 1 e 5 (Figura 5).
Lavagem com água / 1 minuto Aplicação
do gel 2 min Fotoativação40 seg
Fotoativação 40 seg
14min 40seg 2 min
FIGURA 6 – Peróxido de carbamida: a) Peróxido de carbamida utilizado; b) Gel de peróxido de carbamida sobre o dente; c) Peróxido de carbamida sendo fotoativado com LED.
No grupo 4, o gel de peróxido de carbamida foi aplicado e mantido por 40 minutos na superfície vestibular dos dentes, com renovação após 20 minutos, sem fotoativação e com a luz do refletor apagada.
Ao término do clareamento, os dentes foram novamente lavados com água durante 1 minuto.
Nos grupos 5 e 6, após o clareamento foi aplicado o gel de flúor fosfato neutro incolor (Flúor tópico gel – DFL) (Figura 7) sobre a superfície dos dentes, permanecendo por 4 minutos. Em seguida, foi realizada lavagem com água corrente por 2 minutos.
a
FIGURA 7 – Gel de flúor fosfato neutro incolor.
Após o procedimento de clareamento, os pacientes foram prevenidos quanto ao aparecimento de sensibilidade pós-operatória e orientados para classificarem a intensidade da dor utilizando uma escala analógica visual (Figura 8).
QUADRO 2 – Ordem numérica de valores da escala Vita clássica.
cor valor cor valor
B1 1 A3 9
A1 2 D3 10
B2 3 B3 11
D2 4 A3,5 12
A2 5 B4 13
C1 6 C3 14
C2 7 A4 15
D4 8 C4 16
FIGURA 8 - Escala Visual Análoga
10 DOR INTOLERÁVEL 9
8 7
DOR FORTE TOLERÁVEL
6 5 4
DOR MODERADA
3 2 1
DOR LEVE
4.1.2 Análise estatística
Os dados referentes a sintomatologia pós-clareamento dentário e análise da escala de cor antes e após o clareamento foram avaliados estatisticamente pelo teste não paramétrico de Kruskal-Wallis e teste de Dunn.
Para avaliar se existem diferenças significantes na coloração antes e após o clareamento foram comparados os valores numéricos ordenados da escala Vita (escores). Inicialmente, realizou-se o teste de Sinais de Postos de Wilcoxon (5%) para verificar se existiam diferenças entre os dados iniciais e após o clareamento em cada grupo separadamente. Para avaliar a existência de diferenças entre os grupos, aplicou-se o teste de Kruskall-Wallis, nível de significância 5%. No caso de haver diferenças entre os grupos, aplicou-se o teste de comparação múltipla de Dunn, nível de significância de 10%, para avaliar entre quais grupos estas diferenças ocorreram. Na seqüência, para confirmar o teste de Dunn, realizou-se a correção de Bonferroni (5%).
4.2 Avaliação das alterações no esmalte após clareamento
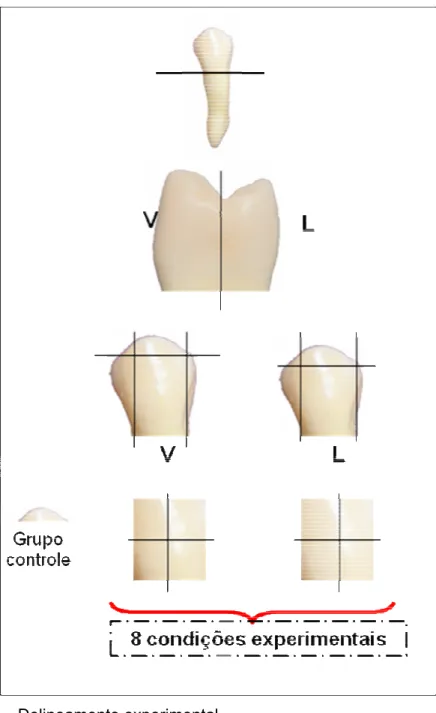
Para esta parte do experimento foram utilizados 10 pré-molares humanos extraídos e armazenados em solução salina fisiológica, que tiveram suas raízes cortadas na junção esmalte/cemento. As coroas foram seccionadas longitudinalmente no sentido mésio-distal em duas metades: vestibular e lingual, e posteriormente cada metade foi seccionada em quatro partes (Figura 9). Em seguida os espécimes foram colocados em cuba ultrassônica durante 15 minutos para limpeza e, após, foram divididos em nove grupos (Quadro 3):
- Grupo 1 (n=10): aplicação de gel de peróxido de hidrogênio
35%, seguida de fotoativações com aparelho de LED. Em seguida foi realizada aplicação tópica de gel de flúor fosfato;
- Grupo 2 (n=10): aplicação de gel de peróxido de hidrogênio
35%, seguida de fotoativações com aparelho de LED;
- Grupo 3 (n=10): aplicação de gel de peróxido de hidrogênio
35%. Em seguida foi realizada aplicação de gel de flúor fosfato;
- Grupo 4 (n=10): aplicação de gel de peróxido de hidrogênio
35%;
- Grupo 5 (n=10): aplicação de peróxido de carbamida 35%,
seguida de fotoativações com aparelho de LED. Em seguida foi realizada aplicação de gel de flúor fosfato;
- Grupo 6 (n=10): aplicação de gel de peróxido de carbamida
35%, seguida de fotoativações com aparelho de LED;
- Grupo 7 (n=10): aplicação de gel de peróxido de carbamida
35%. Em seguida foi realizada aplicação de gel de flúor fosfato;
- Grupo 8 (n=10): aplicação de gel de peróxido de carbamida
35%.
QUADRO 3 – Divisão dos grupos experimentais para posterior avaliação das alterações do esmalte.
Grupos Agente clareador Fotoativação Procedimento imediato após o clareamento
G1 Peróxido de
hidrogênio 35% LED flúor (4 min)Aplicação tópica de ĺsaliva artificial
G2 Peróxido de
hidrogênio 35% LED Saliva artificial
G3 Peróxido de
hidrogênio 35% ____ flúor (4 min)Aplicação tópica de ĺsaliva artificial
G4 Peróxido de
hidrogênio 35%
____ Saliva artificial
G5 Peróxido de
carbamida 35% LED flúor (4 min)Aplicação tópica de ĺsaliva artificial
G6 Peróxido de
carbamida 35% LED Saliva artificial
G7 Peróxido de
carbamida 35% ____ flúor (4 min)Aplicação tópica de ĺsaliva artificial
G8 Peróxido de
carbamida 35% ____ Saliva artificial G9
FIGURA 9 – Delineamento experimental.