TESE DE DOUTORADO
Estudo da remoção de Ba
2+, Ni
2+, Cd
2+, Cu
2+, Cr
3+, Sr
2+,
Zn
2+por eletrocoagulação em água associada à produção
de petróleo
Katia Regina Souza
Orientadora:
Prof.ª Dr.ª Ana Lúcia de Medeiros Lula da Mata
Coorientador:
Prof. Dr. Wilson da Mata
Centro de Tecnologia
Departamento de Engenharia Química
Estudo da remoção de Ba
2+, Ni
2+, Cd
2+, Cu
2+, Cr
3+, Sr
2+, Zn
2+por eletrocoagulação em água associada à produção de
petróleo
Tese de Doutorado apresentada ao Programa de Pós-Graduação em Engenharia Química - PPGEQ, da Universidade Federal do Rio Grande do Norte - UFRN, como parte dos requisitos necessários para obtenção do título de Doutor em Engenharia Química, sob a orientação da Profa. Dra. Ana Lúcia de Medeiros Lula da Mata e do Prof. Dr. Wilson da Mata.
Catalogação da Publicação na Fonte. UFRN / CT / PPGEQ
Biblioteca Setorial “Professor Horácio Nicolas Solimo”.
Souza, Katia Regina. Estudo da remoção de Ba2+, Ni2+, Cd2+, Cu3+, Cr3+, Sr2+, Zn2+ por
eletrocoagulação em água associada à produção de petróleo / Katia Regina Souza. - Natal, 2012.
128 f.: il.
Orientadores: Ana Lúcia de Medeiros Lula da Mata. Wilson da Mata.
Tese (Doutorado) - Universidade Federal do Rio Grande do Norte. Centro de Tecnologia. Departamento de Engenharia Química. Programa de Pós-Graduação em Engenharia Química.
SOUZA, Katia Regina - Estudo da remoção de Ba2+, Ni2+, Cd2+, Cu2+, Cr3+, Sr2+ e Zn2+ por eletrocoagulação em água associada à produção de petróleo. Tese de Doutorado, UFRN, Programa de Pós-graduação em Engenharia Química. Área de Concentração: Engenharia Química.
Orientadora: Profa. Dra. Ana Lúcia de Medeiros Lula da Mata
Coorientador: Prof. Dr. Wilson da Mata.
RESUMO. Dentre os resíduos gerados na indústria petroquímica a água associada à produção de petróleo é a mais importante. Ela é considerada um dos grandes desafios devido à presença de substâncias químicas consideradas tóxicas presente na sua composição. A presença dessas substâncias dificulta a reutilização da água associada nos processos de recuperação avançada, fazendo com que antes da sua reutilização ou descarte, seja necessário seu tratamento. Este trabalho teve como objetivo o estudo da eficiência de remoção das espécies químicas: Ba2+, Ni2+, Cd2+, Cu2+, Cr3+, Sr2+e Zn2+, presentes na composição da água associada à produção de petróleo por eletrocoagulação. A avaliação de remoção dessas espécies químicas foi realizada por testes em laboratório utilizando reatores eletroquímicos de batelada e de fluxo contínuo. Os testes iniciais da eletrocoagulação foram realizados com efluente sintético em reator batelada utilizando eletrodo de ferro. Os resultados de remoção de Zn2+ e de Ni2+ foram de 78% e 59%, respectivamente. Enquanto que o percentual removido de Ba2+ foi de 19%, em 30 minutos de tratamento, aplicando corrente de 1,10A. Os testes com efluente foram realizados em reator batelada aplicando a técnica eletroquímica com eletrodos de inox 304, o objetivo foi remover parte do óleo disperso e também, de compostos orgânicos presentes no efluente. De acordo com as condições experimentais usadas, o resultado máximo obtido de TOG foi de 60% e de TOC foi aproximadamente de 50%, em relação à concentração inicial. Para os experimentos realizados em reator contínuo, com efluente semi-sintético, foram usados eletrodos de ferro e de alumínio e os resultados obtidos foram de 100% de remoção de Cd2+, Cu2+, Cr3+ e Zn2+ e 77% de Sr2+. Esses percentuais só foram possíveis de alcançar mediante o uso do eletrodo de ferro. Entretanto quando esse eletrodo foi substituído pelo de alumínio, ocorreu um decréscimo no percentual de remoção para 65%, utilizando-se a mesma vazão e corrente. Portanto segundo os resultados obtidos, a utilização do eletrodo de ferro mostrou-se mais eficaz na remoção desses metais e as condições de menor vazão e menor corrente foram satisfatórias, conforme observado no planejamento fatorial adotado.
ABSTRACT
Among the waste generated in the petrochemical industry water associated with oil production is the most important. It is considered one of the great challenges due to the presence of considered toxic chemicals present in this composition. The presence of these substances difficult to reuse the water associated with the enhanced recovery processes, so that prior to their reuse or disposal, treatment is necessary. This paper aimed to study the removal efficiency of chemical species: Ba2+, Ni2+, Cd2+, Cu2+, Cr3+, Sr2+ and Zn2+, present in the composition of the water associated with oil production by electrocoagulation. The evaluation of removal of these chemical species was performed by laboratory tests using electrochemical batch reactors and continuous flow. Initial tests were performed with electrocoagulation of synthetic wastewater in batch reactor using iron electrode. Results of removal of Zn2+ and Ni2+ were 78 % and 59 % respectively. While the percentage of removed Ba2+ was 19 % by 30 minutes of treatment and by applying current of 1.10 A. The tests were performed on effluent batch reactor applying the electrochemical technique with stainless steel electrodes 304, the objective was to remove part of the dispersed oil and also of organic compounds in the effluent. Under the experimental conditions used, the maximum result was obtained TOG was 60 % and TOC was approximately 50 % compared to the initial concentration. In the experiments carried out in continuous reactor, with effluent semi-synthetic, have been used electrodes of iron and aluminum and the results were 100 % removal of Cd2+, Cu2+, Cr3+ and Zn2+ and 77 % of Sr2+. These percentages were only attainable through the use of the iron electrode. However, when the electrode was replaced by aluminum, there was a reduction in the percentage of removal to 65 %, using the same flow rate and current. Therefore according to the results obtained using the iron electrode was more effective in removing these metals and the conditions of lower current and lower flow rate was satisfactory, as observed in the experimental design adopted.
Dedicatória
Aos meus pais e irmãos Maria Ozete F. de Souza Erasmo Alves de Souza Sara Jane Souza
Agradecimentos
A Deus, pela oportunidade de vida, pelos ensinamentos de amor, luz e evolução. Aos Meus Pais, Erasmo Alves e Maria Ozete; aos meus irmãos, Sara e Junior; pelo incentivo e compreensão dedicados ao longo de minha vida, que Deus sempre os ilumine.
À Professora Dra. Ana Lúcia de Medeiros Lula da Mata, pela amizade, orientações e oportunidade.
Ao Professor Dr. Wilson da Mata, pela amizade e orientações.
Ao Professor Dr. Djalma Ribeiro, pela orientação, apoio e suporte necessário à realização dos experimentos.
Ao Professor Dr. Carlos Alberto Martínez-Huitle pela orientação, que sempre com muita presteza, esteve disposto a orientar, e tirar dúvidas.
Ao Professor Dr. Almir Mirapalheta, que sempre com muita paciência e presteza, esteve disposto a orientar, tirar dúvidas, e discutir sobre o trabalho.
À empresa PETROBRÁS, pela doação das amostras.
Aos funcionários do PPGEQ: Mazinha e Medeiros, pela atenção e préstimos sempre dedicados.
Ao CNPq pelo auxílio financeiro, da bolsa e da taxa de bancada, que proporcionou a realização desse trabalho.
À direção e aos colegas do IFRN – Campus Pau dos Ferros – pelo apoio e companheirismo.
À Aécia, Emily, Rina, Tarcila e Rayana as técnicas e amigas que conquistei e que muito colaboraram nas análises realizadas.
À grande amiga Jennys, que sempre me apoiou, sempre esteve disposta a ajudar. Aos amigos do LEAP, Rafel, Elton, Marcos, Janusa, Robson e Keyla.
Às minhas amigas maravilhosas: Adriana, Bia, Juliana, Daniela, Débora e Rayanna. À André, Igor e Filipe, pela colaboração na realização dos experimentos.
Em especial, a Andreza, Ineuda, Fredinho, Olívia, Carlos Henrique, Chiquinho e Márcio, amigos do IFRN, que dividiram comigo moradia e translado Natal – Pau dos Ferros/RN.
Sumário
1. Introdução Geral ...2
2 – Objetivos ...6
2.1 Geral ...6
2.2 Específicos ...6
3. Revisão Bibliográfica ...8
3.1 O Petróleo ...8
3.2 Efluente da indústria de petróleo ... 10
3.2.1 Água associada à produção de petróleo ... 10
3.2.2 Composição da água de produção ... 13
3.2.3 Espécies químicas e seus efeitos tóxicos ... 15
3.2.4 Impactos ambientais causados pela água de produção ... 16
3.2.5 Custo de tratamento da água associada à produção de petróleo ... 18
3.2.6 Tipos de métodos utilizados para o tratamento da água associada à produção de petróleo .. 19
3.2.7 Reuso da água associada à produção de petróleo ... 20
3.3 Princípio da eletroquímica ... 21
3.3.1 Definição e funcionamento de uma célula eletroquímica ... 21
3.3.2 Lei de Faraday ... 23
3.3.5 Reatores eletroquímicos ... 26
3.3.6 Objetivos da técnica eletroquímica ... 27
3.3.7 Vantagens e desvantagens dos processos eletroquímicos ... 27
3.3.8 Estudos e aplicações da eletroquímica na indústria de petróleo ... 29
3.4 Eletrocoagulação ... 38
3.4.1 Fatores que afetam a eletrocoagulação ... 41
4. Metodologia ... 47
4.1 Montagem experimental ... 48
4.1.1 Reator eletroquímico de batelada ... 48
4.1.2 Reator eletroquímico contínuo ... 51
4.1.3 Fonte de corrente contínua ... 55
4.1.4 Sistema: tanque de mistura, eletro bomba e rotâmetro... 55
4.1.5 Eletrodos de trabalho ... 56
4.2 Água associada à produção de petróleo ... 56
4.4 Análise da viabilidade técnica do sistema de tratamento contínuo ... 62
4.4.1 Taxa da velocidade de remoção de metais em função do tempo ... 62
4.4.2 Análise dos custos de energia por consumo de material dos eletrodos ... 63
4.5 Procedimento experimental ... 65
4.5.1 Procedimentos de lavagem e tipo de recipientes, técnica de coleta e preservação de amostras para os tratamentos Batelada e Contínuo. ... 65
4.5.2 Pré-montagem do sistema de tratamento ... 65
4.5.3 Preparo do efluente sintético ... 66
4.5.4 Inicio do tratamento – Batelada ... 66
4.5.5 Pré-montagem do sistema de tratamento ... 67
4.5.6 Preparo do efluente semi-sintético ... 68
4.5.7 Inicio do tratamento – Contínuo ... 69
4.5.8 Limpeza dos reatores ... 69
4.5.9 Limpeza, pesagem e conservação dos eletrodos ... 70
4.6 Análises ... 71
5. Resultados e discussões ... 75
5.1 Resultados iniciais - reator batelada ... 76
5.1.1 Testes de eletrocoagulação para remoção de Zn2+, Ni2+ e Ba2+ em efluente sintético ... 76
5.1.2 Testes de eletrofloculação para remoção de TOG e degradação de TOC em efluente de água associada à produção de petróleo ... 77
5.2 Resultados dos testes realizados com o reator contínuo ... 79
5.2.1 Planejamento fatorial 23 - Tratamento eletrocoagulação (EC) para remoção de Cd2+, Cu2+, Cr3+, Sr2+ e Zn2+ em efluente semi-sintético ... 79
5.3 Análise da viabilidade técnica da eletrocoagulação na remoção de Cd2+, Cu2+, Cr3+, Sr2+ e Zn2+ presente em efluente semi-sintético ... 101
5.3.1 Efeito do pH e do material do eletrodo na eficiência de remoção ... 101
5.3.2 Resultados da taxa de remoção de contaminantes em função do tempo de tratamento ... 102
5.3.3 Quantidade de resíduos de ferro e alumínio presente no efluente após os testes de eletrocoagulação ... 103
5.3.4 Análise dos custos de energia por consumo de material dos eletrodos ... 104
5.3.5 Análise dos resultados obtidos com outras referências bibliográficas ... 106
6. Conclusão ... 108
Referências Bibliográficas ... 112
Capítulo 3
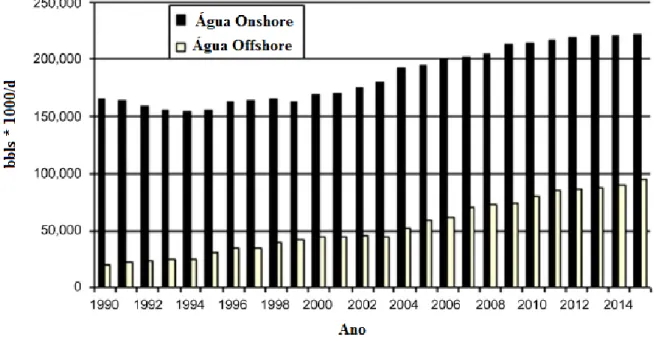
Figura 3.1 Gráfico da estimativa de produção Onshore e Offshore de água produzida. 09
Figura 3.2 Ilustração de um aquífero natural ativo. 10
Figura 3.3 Ilustração da água de injeção sendo colocada dentro do poço. 11
Figura 3.4 Esquema da recuperação terciária por injeção de vapor. 12
Figura 3.5 Direção do fluxo de elétrons do anodo para o catodo em uma célula eletroquímica.
22
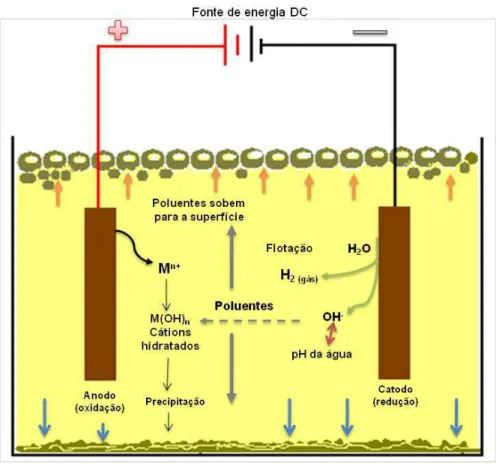
Figura 3.6 Esquema do processo de floculação dos poluentes de uma célula eletroquímica. 40
Figura 3.7 Arranjo dos eletrodos de acordo com a conexão. 43
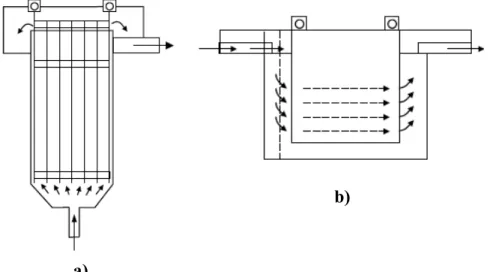
Figura 3.8 Esquema da direção de fluxo de acordo com a posição dos eletrodos dentro do reator de eletrocoagulação.
44
Figura 3.9 Direção do fluxo de fluido conforme a quantidade de canais. 44
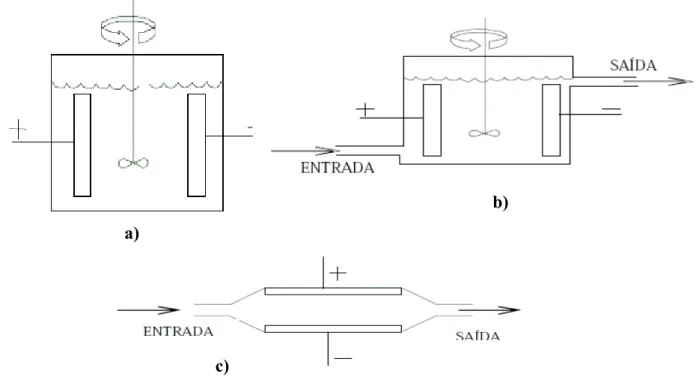
Figura 3.10 Geometria dos reatores de operações simples: a) batelada, b) contínuo com agitação e c) contínuo.
45
Capítulo 4
Figura 4.1 Vista frontal do reator de batelada pós-montagem. 49
Figura 4.2 Vista da parte interna e do tarugo de nylon na base inferior do reator. 50
Figura 4.3 Disposição dos 4 pares de eletrodos dentro do reator eletroquímico. 50
Figura 4.4 Visão completa do sistema em batelada. 51
Figura 4.5 Imagem da formação de bolhas na parte superior devido ao desprendimento de gás 4.5a e a precipitação de partículas 4.5b.
52
Figura 4.6 Vista do posicionamento das calhas dentro do reator e suas respectivas dimensões.
53
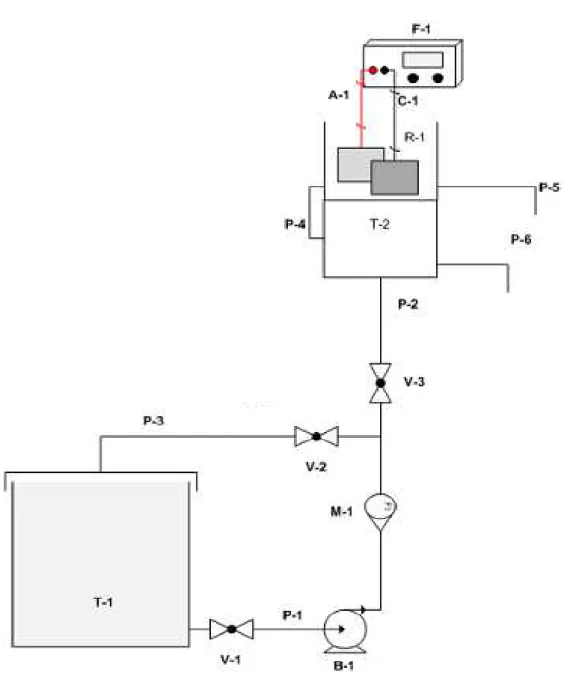
Figura 4.7 Esquema de montagem do sistema de tratamento contínuo. 54
Figura 4.8 Fonte de alimentação de corrente contínua. 55
Figura 4.9 Componentes do sistema contínuo. 55
Figura 4.10 Fotos dos eletrodos de alumínio, inox e ferro. 56
Figura 4.11 Representação espacial, cubo 3D dos oitos experimentos no planejamento fatorial 23.
59
Figura 4.12 Quadro dos valores utilizados para as variáveis de controle e de resposta, utilizando a eletrofloculação em reator batelada.
60
Figura 4.13 Parte superior do reator de bancada contínuo. 68
Figura 4.14 Espectrofotômetro de emissão óptica com plasma indutivamente acoplado (ICP-OES) – marca Thermo Analítica.
72
Figura 4.15 Analisador de óleos e graxas (TOG/TPH), InfraCal da Wilks Enterprise. 72
Figura 4.16 Analisador TOC da Analytik Jena Multi NC® 3100. 73
Figura 5.1 a) Aspecto da camada de espuma composta por óleo e b) Aspecto da camada formada pela mistura de óleo e material dissolvido do eletrodo.
77
Figura 5.2 Gráficos dos percentuais de óleo e graxas (TOG) removidos e recuperados em 30 minutos de tratamento eletroquímico por diferentes correntes.
78
Figura 5.3 Concentração de TOC removida da amostra de efluente real de água associada à produção de petróleo pela técnica eletroquímica.
79
Figura 5.4 Superfícies tridimensional para a remoção de Cd2+ em função do eletrodo de (a) alumínio e do eletrodo de (b) ferro.
81
Figura 5.5 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para o % de remoção de Cd2+ em função ao eletrodo de Alumínio.
82
Figura 5.6 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para o % de remoção de Cd2+ em função ao eletrodo de ferro.
82
Figura 5.7 Diagrama de dispersão para os limites de confiança de ± 95% para o Cd2+ com eletrodo de alumínio.
84
Figura 5.8 Diagrama de dispersão para os limites de confiança de ± 95% para o Cd2+ com eletrodo de ferro.
84
Figura 5.9 Superfície tridimensional para a remoção de Cu2+ em função do eletrodo Alumínio (a) e do eletrodo de ferro (b).
85
Figura 5.10 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para a remoção de Cu2+ em função do eletrodo de alumínio.
86
Figura 5.11 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para a remoção de Cu2+ em função do eletrodo de ferro.
86
Figura 5.12 Diagrama de dispersão para os limites de confiança de ± 95% para o Cu2+ com eletrodo de alumínio.
88
Figura 5.13 Diagrama de dispersão para os limites de confiança de ± 95% para o Cu2+ com eletrodo de ferro.
88
Figura 5.14 Superfície tridimensional para a remoção de Cr3+ em função do eletrodo Alumínio (a) e do eletrodo de ferro (b).
89
Figura 5.15 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para a remoção de Cr3+ em função ao eletrodo de alumínio.
90
Figura 5.16 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para a remoção de Cr3+ em função ao eletrodo de ferro.
90
Figura 5.17 Diagrama de dispersão dos valores calculados em função dos valores observados para os limites de confiança de ± 95% para o Cr3+ com eletrodo de alumínio.
92
Figura 5.19 Superfície tridimensional para a remoção de Sr2+ em função do eletrodo Alumínio (a) e do eletrodo de ferro (b).
93
Figura 5.20 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para a remoção de Sr2+ em função ao eletrodo de alumínio.
Figura 5.21 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para a remoção de Sr2+ em função ao eletrodo de ferro.
94
Figura 5.22 Diagrama de dispersão dos valores calculados em função dos valores observados para os limites de confiança de ± 95% para o Sr2+ para o eletrodo de alumínio.
96
Figura 5.23 Diagrama de dispersão dos valores calculados em função dos valores observados para os limites de confiança de ± 95% para o Sr2+ para o eletrodo de ferro.
96
Figura 5.24 Superfície tridimensional para a remoção de Zn2+ em função do eletrodo Alumínio (a) e do eletrodo de ferro (b).
97
Figura 5.25 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para remoção de Zn2+ em função do eletrodo de alumínio.
98
Figura 5.26 Gráfico de Pareto dos parâmetros lineares das variáveis x2 (corrente) e x3 (vazão)
para remoção de Zn2+ em função do eletrodo de ferro.
98
Figura 5.27 Diagrama de dispersão dos valores calculados em função dos valores observados para os limites de confiança de ± 95% para o Zn2+ para o eletrodo de alumínio.
100
Figura 5.28 Diagrama de dispersão dos valores calculados em função dos valores observados para os limites de confiança de ± 95% para o Zn2+ para o eletrodo de ferro.
100
Figura 5.29 Gráficos a) comportamento do pH de acordo com o material do eletrodo e b) remoção dos contaminantes devido a mudança de pH para o eletrodo de ferro.
101
Figura 5.30 Curvas da taxa de remoção de Cd2+, Cu2+, Cr3+,Sr2+ e Zn2+ em 96 min. de tratamento da água associada à produção de petróleo semi-sintética por eletrocoagulação.
LISTA DE TABELAS
Capítulo 3
Tabela 3.1 Fenóis e compostos aromáticos voláteis em água associada à produção petróleo. 14
Tabela 3.2 Hidrocarbonetos policíclicos aromáticos polinucleados (HPAs). 14
Tabela 3.3 Metais presentes na composição química de uma água associada à produção de petróleo
15
Tabela 3.4 Efeitos causados pelas substâncias presentes na água associada à produção de petróleo
18
Capítulo 4
Tabela 4.1 Condições experimentais usadas para os tratamentos no reator batelada no 1º e 2º teste.
61
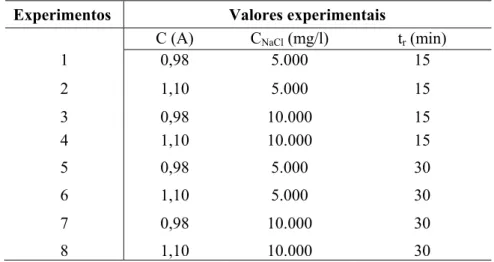
Tabela 4.2 Valores experimentais das variáveis: eletrodo, corrente e vazão. 62
Tabela 4.4 Tipos de análises e equipamentos usados 71
Capítulo 5
Tabela 5.1 Resultados de % de remoção de Zn2+, Ni2+ e Ba2+ 76
Tabela 5.2 Resultados do % de remoção de Cd2+, Cu2+, Cr3+, Sr2+ e Zn2+ referente ao planejamento fatorial 23 utilizando reator contínuo
80
Tabela 5.3 Análise de variância (tabela ANOVA) para o Cd2+ eletrodo de alumínio 83
Tabela 5.4 Análise de variância (tabela ANOVA) para o Cd2+ eletrodo de ferro 83
Tabela 5.5 Análise de variância (tabela ANOVA) para o Cu2+ eletrodo de Alumínio 87
Tabela 5.6 Análise de variância (tabela ANOVA) para o Cu2+ eletrodo de Ferro 87
Tabela 5.7 Análise de variância (tabela ANOVA) para o Cr3+ eletrodo de Alumínio 91 Tabela 5.8 Análise de variância (tabela ANOVA) para o Cr3+ eletrodo de Ferro 91 Tabela 5.9 Análise de variância (tabela ANOVA) para o Sr2+ eletrodo de Alumínio 95
Tabela 5.10 Análise de variância (tabela ANOVA) para o Sr2+ eletrodo de Ferro 95
Tabela 5.11 Análise de variância (tabela ANOVA) para o Zn2+ eletrodo de Alumínio 99
Tabela 5.12 Análise de variância (tabela ANOVA) para o Zn2+ eletrodo de Ferro 99 Tabela 5. 13 Valores da taxa de remoção de Cd, Cu, Cr, Sr e Zn no tempo de 96min. de
tratamento por eletrocoagulação
102
Tabela 5.14 Resíduo de ferro e alumínio gerado depois da coagulação 103
Tabela 5.15 Valores dos custos operacional elétrico (COE) e os custos do material (CM) 105
LISTA DE ABREVIATURAS E SIGLAS
ADE – Anodo Dimensionalmente Estável
CONAMA – Conselho Nacional do Meio Ambiente
COE – custo operacional elétrico R$m-3
CM – Custo do material R$m-3
DC – direct current (Corrente contínua) DQO – Demanda Química de Oxigênio EC – Eletrocoagulação
ER – Efluente real ES – Efluente sintético ESS – Efluente semi-sintético
ETE – Estação de tratamento de efluente
EUA – United States of America (Estados Unidos da América) HPA – Hidrocarbonetos Policíclicos Aromáticos
ICP-OES - Espectrometria de emissão ótica por plasma acoplado indutivamente IOR – Improved Oil Recovery (Recuperação Avançada de Óleo)
Máx. – máximo Mín. – mínimo
NEPGN – Núcleo de Estudos em Petróleo e gás natural
NORM – Naturally Occurring Radioactive Material (Material Radioativo Ocorrido Naturalmente)
NUP-ER – Núcleo de Pesquisa de Petróleo e Energias Renováveis NUPRAR – Núcleo de Pesquisas de Reuso da Água
OGP – International Association of Oil & Gas Producers
OSPAR – Commission Protecting and Conserving the North-East Atlantic and its Resources (Comissão de Proteção e Conservação do Atlântico Norte e seus Recursos)
PA – Para análise
POA – Processos Oxidativos Avançados PEE – Preço da energia elétrica
TOG – Teor de Óleos e Graxas
TPH – Total Petroleum Hydrocarbon (Hidrocarboneto de Petróleo Total) UFRN – Universidade Federal do Rio Grande do Norte
UN-RN/CE – Unidade de Negócio e Exploração do Rio Grande do Norte e Ceará da bacia Potiguar
LISTA DE SIMBOLOS
A – Ampere
AgFe – área geométrica do ferro 128 cm²
AgAl – área geométrica do alumínio 89,63 cm²
Ci – concentração inicial mg L-1
Cf – concentração final mg L-1
d – densidade de corrente mA cm-2
E – potêncial V
Fcal – F calculado
Ftab – F tabelado
F – constante de Faraday 96.500 C mol-1
I – corrente A
MFe – massa molar do ferro 55,84 g mol-1
MAl – massa molar do alumínio 26,98 g mol-1
min. – minuto
nFe – nº de elétrons de ferro 2e
-nAl – nº de elétrons de alumínio 3e
-PEE – preço da energia elétrica R$ kWh-1
PMEFe – preço do material do eletrodo de ferro 3,86 x 10-03 R$ g-1
PMEAl – preço do material do eletrodo de alumínio 0,017 R$ g-1
Q – vazão mLmin.-1
Tr – tempo de residência dentro do reator min.
Vb – volume do reator de batelada L
Vc – volume do reator contínuo L
Veff – volume do efluente sem tratamento m3
∫– Integral
Introdução Geral
Capítulo
1. Introdução Geral
Ao longo dos anos o setor industrial, conforme o ramo de atividade e tipo de processo, ela vem desenvolvendo técnicas para aumentar sua produtividade no que resulta, muitas vezes, no aumento da geração de resíduos. Esses resíduos, antes de serem descartados, devem ser caracterizados a fim de avaliar qual a sua classificação, a presença e a concentração de possíveis contaminantes na sua composição química.
No Brasil a Resolução do CONAMA n° 357, de 17 de março de 2005, ‘dispõe sobre classificação dos corpos de água e diretrizes ambientais para o seu enquadramento, bem como estabelece as condições e padrões de lançamento de efluentes’, destacando que os artigos de 24 a 37 são específicos para efluentes industriais. Essas condições e os padrões de lançamento de efluentes foram impostos pelos órgãos ambientais às indústrias a fim de que realizassem o tratamento de seus resíduos de acordo com o tipo de atividade, carga poluidora e quantidade gerada, e com isso se evitaria danos ao meio ambiente
Dentre as atividades industriais, pode-se destacar a exploração de petróleo como uma das atividades de maior geração de resíduos e de carga poluidora, devido ao alto grau de toxicidade.
Esse índice de toxicidade está associado aos constituintes presentes naturalmente na composição do petróleo (hidrocarbonetos saturados e insaturados, hidrocarbonetos aromáticos, compostos sulfurados, nitrogenados, oxigenados, asfaltenos, espécies químicas), que se apresentam como sais dissolvidos na água emulsionada ao petróleo e também na forma de compostos organometálicos complexos e além de outros aditivos químicos adicionados durante a exploração, (THOMAS, 2001).
Além da Resolução do CONAMA nº357, existe especificamente a Resolução CONAMA de n° 393, de 08 de Agosto de 2007, que ‘dispõe sobre descarte contínuo de água de produção em plataformas marítimas de petróleo e gás natural’. Essa resolução ressalta que deve ser feito o monitoramento semestral das espécies químicas pelas empresas operadoras de plataformas, destacando: arsênio, bário, cádmio, cromo, cobre, ferro, mercúrio, manganês, níquel, chumbo, vanádio e zinco.
elementos ocorrem no ambiente aquático sob diversas formas: i) em solução na forma iônica ou na forma de complexos solúveis orgânicos ou inorgânicos, ii) formando ou ficando retidos às partículas coloidais minerais ou orgânicas e iii) ficando também retidos no sedimento ou incorporados à biota (FEEMA, 1992; MEYNBURG et al., 1995).
Algumas espécies químicas são substâncias altamente tóxicas e não são compatíveis com alguns dos tratamentos convencionais, por exemplo, os biológicos. As espécies químicas quando presentes nos efluentes industriais reduzem a capacidade autodepurativa das águas, devido à ação tóxica que elas exercem sobre os microorganismos. Estes microorganismos são os responsáveis pela recuperação das águas, através da decomposição dos materiais orgânicos presente nos efluentes (FELLENBERG, 1980 apud AGUIAR et al., 2002).
Dessa forma, a escolha da técnica de tratamento para esse tipo de efluente deve já ser bastante eficaz e considerar também determinados fatores, tais como, a carga poluidora do efluente (composição e concentração), a localização do processo industrial (área física de instalação da unidade e impactos ambientais), os custos operacionais (equipamentos, manutenção, mão-de-obra e recursos energéticos), a segurança operacional (riscos ligados a planta de tratamento), a destinação final, (reuso no processo ou lançamento em corpos d’água) e o mais importante desses, a limitação a determinados contaminantes (eficiência de remoção ou degradação de compostos tóxicos), os quais devem apresentar valores, depois do tratamento, de acordo com os estabelecidos pela legislação.
A eletroquímica vem se destacando como uma técnica bastante promissora em tratamentos de efluentes industriais, em pesquisa científica e no desenvolvimento de equipamentos, como no caso dos reatores eletroquímicos, utilizados como unidades de tratamento que auxiliam na transformação dos contaminantes tóxicos em substâncias mais facilmente degradáveis.
Com base nos princípios da técnica de tratamento, no tipo de efluente a ser tratado (água associada à produção de petróleo) e no volume gerado, este trabalho se propôs a estudar o percentual de remoção das espécies químicas, tais como: Cd2+ (cádmio), Cr2+ (cromo), Cu2+ (cobre), Zn2+ (zinco), Ni2+ (níquel), Ba2+ (bário) e Sr2+ (estrôncio), utilizando os princípios da técnica da eletrocoagulação.
Esta tese é composta de 6 capítulos, referências bibliográficas e os anexos.
O Capítulo III – Revisão Bibliográfica – neste capítulo é apresentado os aspectos mais relevantes em relação à água associada à produção de petróleo, as etapas de produção onde é gerado esse efluente, suas características e composição química, danos causados ao meio ambiente devido a sua toxicidade, tipos de tratamentos e os custos com o descarte da água de produção. Além disso, foi realizado um levantamento em ordem cronológica dos principais trabalhos que aplicaram a eletroquímica no tratamento da água de produção. Com respeito à eletroquímica são enfocados os princípios e as reações de oxidação e redução, definição da eletrocoagulação e como são formados os coagulantes naturais responsáveis pelo tratamento, objetivos e os fatores que influenciam no processo da eletrocoagulação.
No Capítulo IV – Metodologia – apresenta os materiais e equipamentos utilizados nos experimentos (reatores eletroquímicos), a metodologia usada e as variáveis de controle escolhidas para o planejamento fatorial. Apresenta as equações usadas para calcular os percentuais de remoção dos contaminantes e os custos relacionados ao consumo de energia e à dissolução do material do eletrodo.
No Capítulo V – Resultados e discussões – esta parte da tese apresenta os resultados obtidos com os experimentos mediante o planejamento fatorial, evidenciando os mesmos e comparando com dados da literatura. Além disso, mostra os valores dos percentuais de remoção dos contaminantes e em que condições foram a que melhor influenciou o processo de remoção. Destaca a influência dos parâmetros mais importantes e como eles atuam sobre a eletrocoagulação. Apresenta os resultados relacionados aos tipos de materiais dos eletrodos e qual foi mais eficiente no processo de remoção dos contaminantes e quantifica o resíduo gerado após o tratamento. Apresenta os custos mediante o consumo de energia e de material dissolvidos dos eletrodos durante o processo de eletrocoagulação.
As conclusões obtidas neste trabalho e sugestões para trabalhos futuros estão apresentadas no Capítulo VI.
Referências bibliográficas – são listadas segundo as normas da ABNT as referências citadas no texto.
Objetivos
Capítulo
2 – Objetivos
2.1 Geral
Estudar a remoção de Ba2+, Ni2+, Cd2+, Cu2+, Cr3+, Sr2+, Zn2+ por eletrocoagulação em água associada à produção de petróleo.
2.2 Específicos
Montar em escala de laboratório um reator eletroquímico em sistema de batelada e contínuo;
Realizar testes iniciais em batelada para avaliar a eficiência do processo de eletrocoagulação na remoção de Zn2+ (zinco), Ni2+ (níquel) e Ba2+ (bário) em efluente sintético;
Avaliar os resultados de remoção dos testes iniciais e a influência dos parâmetros das variáveis de processo: concentração de NaCl (g/ml), corrente (A), tempo de residência (minutos);
Realizar experimentos com a finalidade de remover outros contaminantes, tais como, Cd2+, Cr3+, Cu2+, Sr2+, Ni2+ presentes em solução sintética de água associada a produção de petróleo;
Realizar testes da eletrocoagulação com efluente de água associada à produção de petróleo e avaliar a eficiência de remoção do teor de óleos e graxas (TOG) e também, de carbono orgânico total (TOC);
Revisão Bibliográfica
Capítulo
3. Revisão Bibliográfica
Neste capítulo são apresentados os aspectos mais relevantes referentes ao petróleo, à água associada à produção de petróleo, as técnicas de tratamento eletroquímico (eletrofloculação, oxidação eletroquímica, eletroflotação e a eletrocoagulação), princípio e fatores que afetam o tratamento e variáveis envolvidas, vantagens e desvantagens da eletrocoagulação, principais reações envolvidas e os tipos de material dos eletrodos.
3.1 O Petróleo
O petróleo, do latim petra (pedra) e oleum (óleo), é constituído basicamente por uma mistura de compostos orgânicos (hidrocarbonetos), podendo conter também quantidades pequenas de nitrogênio, oxigênio, enxofre e metais. No estado líquido é uma substância oleosa, inflamável, menos densa que a água, com cheiro característico e cor variando entre o negro e o castanho-claro (THOMAS, 2001).
O petróleo é uma fonte energética de grande importância para a economia mundial. Porém, seu valor comercial depende do tipo de óleo e esse, pode ser dividido em leve e pesado, naftênicos ou parafínicos. Dependendo do tipo de óleo é que se define o processo a ser usado nas etapas de exploração e explotação e associado a essas, estão os resíduos gerados (SOUZA et al., 2010).
Naturalmente além dos hidrocarbonetos, ocorre a produção de água. Sua quantidade vai depender das condições em que ela se encontra no meio poroso (THOMAS, 2001).
De acordo com Thomas, (2001), a água é um dos resíduos gerados intrínseco ao processo de produção de óleo e gás, e por se encontrar adjacente às formações portadoras de hidrocarbonetos, contém gotas de óleo que podem está dispersas ou dissolvidas.
Essas águas residuais do campo de petróleo ou água associada à produção de petróleo são resíduos que contêm vários componentes orgânicos e inorgânicos, cuja disposição inapropriada desse rejeito pode poluir superfícies, corpos d’ água e o solo (FAKHRU´L-RAZI et al., 2009).
aumentando continuamente através da exploração de campos maduros, porém as melhores técnicas de manejo e a exploração de campos novos tendem a diminuir essa produção.
Figura 3.1 – Gráfico da estimativa de produção Onshore e Offshore de água produzida. Fonte: DAL FERRO E SMITH (2007)
Reynolds e Kiker, (2003) apud Fakhru´l-Razi et al., (2009), avaliaram diversos fatores que podem afetar a quantidade de água de produção em relação à vida de um poço. Dentre eles podem ser destacados, o método de perfuração de poços, a localização do óleo dentro de reservatórios homogêneos ou heterogêneos, diferentes tipos de completação, única ou múltiplas zonas de perfuração, tipos de tecnologias para separação de água, a injeção de água em processo de recuperação avançadas de óleo, presença de furos causados pela corrosão ou desgaste e comunicações subterrâneas.
De acordo com Neto et al., (2005), no Rio Grande do Norte foi estimado uma produção de petróleo aproximadamente 86.000 m3 por dia apenas de água originada da extração e do refino do petróleo. Após tratamento esta água era injetada em poços ou era descartada via emissário diretamente no mar ou em efluentes.
3.2 Efluente da indústria de petróleo
3.2.1 Água associada à produção de petróleo
A produção de petróleo e gás está associada à produção de água. Essa água pode receber as seguintes denominações: água de formação, água de produção, água associada ao petróleo ou ao efluente salino (FREIRE, 1999).
Além da água de formação, existem outras formas de geração de água associada à produção de petróleo. Sendo a recuperação avançada de óleo IOR (Improved Oil Recovery) uma delas. Em uma dessas técnicas, o petróleo é produzido mediante a suplementação da energia natural do reservatório, denominado de recuperação secundária. Ela pode ser feita por meio da injeção da mistura da água de formação e da água subterrânea dentro do poço para manter as condições de pressão na rocha reservatório. Essa condição é fundamental para que haja migração do petróleo para os poços produtores (SILVA, 2000). A Figura 3.3, mostra o mecanismo de produção de óleo mediante a injeção de água.
Figura 3.3 - Ilustração da água de injeção sendo colocada dentro do poço (Fonte: CORREIA, 2009). ÁGUA
ÓLEO
ÁGUA
ROCHA IMPERMEÁVEL
Gás Natural
Poço de injeção de água
Poço de injeção de água Unidade de Produção
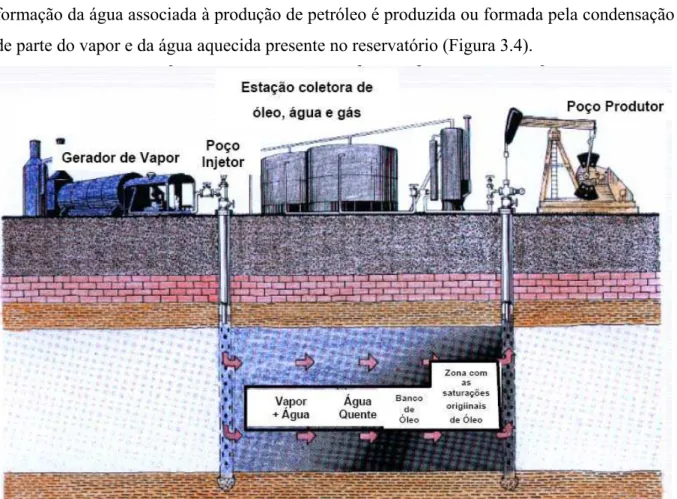
Outra forma de IOR é a recuperação terciária. Nesse mecanismo o petróleo é produzido de forma assistida por outras fontes de energia e/ou efeitos físicos, químicos e biológicos. A injeção de vapor é um dos métodos térmicos utilizados. Nessa técnica, a formação da água associada à produção de petróleo é produzida ou formada pela condensação de parte do vapor e da água aquecida presente no reservatório (Figura 3.4).
Figura 3.4 - Esquema da recuperação terciária por injeção de vapor. (Fonte: ALMEIDA, 2004)
A água é praticamente intrínseca ao processo de extração de petróleo, sendo produzida tanto em operações em terra (onshore), quanto no mar (offshore). Ela é considerada o rejeito de maior volume em todo o processo de exploração e produção de petróleo (FREIRE, 1999).
Os riscos associados à água de produção podem variar em função da sua composição, das características do local de origem e da disposição final, representando um perigo potencial para o meio ambiente (SILVA, 2000).
Sabe-se que, durante a vida útil de um reservatório, o volume de água de produção pode chegar a exceder o volume de produção de óleo (VIEIRA, et al., 2003 apud HENDERSON et al., 1999). Um campo de petróleo novo quando no início de produção, pode produzir água, em torno de 5 a 15 %, e na medida em que sua vida econômica vai se esgotando, o volume de água pode aumentar chegando atingir uma faixa de 75 a 90 % (ALI et al., 1998 apud VIEIRA, et al., 2003; THOMAS, 2001), o que além de representar um volume de água bastante expressivo é um dos grandes gargalos na produção de Óleo e Gás.
Segundo o relatório emitido pela OGP (Associação Internacional de Produtores de Óleo e Gás), o volume de água associada à produção de petróleo nos reservatórios produtores de gás tende a produzir menor volume de água, porém essa água presente nesses reservatórios possui altas concentrações de contaminantes orgânicos. Nos reservatórios produtores de óleo, o volume de água associada à produção de petróleo é muito maior comparado com os reservatórios de gás.
3.2.2 Composição da água de produção
De acordo com Stephenson (1991), o óleo pode está disponível na água de produção tanto na forma de material insolúvel, como dissolvida. A quantidade desse material disperso depende da influência de alguns fatores, tais como: densidade do óleo, forma e tamanho das gotas de óleo e tensão interfacial entre a água e o óleo. Segundo Palmer et al., (1979) apud Freire (1999), esses fatores influenciam na eficiência dos processos gravimétricos de separação e/ou de flotação.
A fração insolúvel em água é constituída principalmente de hidrocarbonetos alifáticos, cíclicos e aromáticos de alto peso molecular. A presença desses hidrocarbonetos na composição das águas de produção de campos petrolíferos no Novo México, é em média, de 60 mg/L de n-alcanos na faixa de C10 a C30 (TELLEZ et al.,1995 apud FREIRE, 1999).
A composição e as concentrações mínima, média e máxima dos compostos presentes na composição da água associada à produção de petróleo estão apresentados nas Tabelas 3.1 e 3.2.
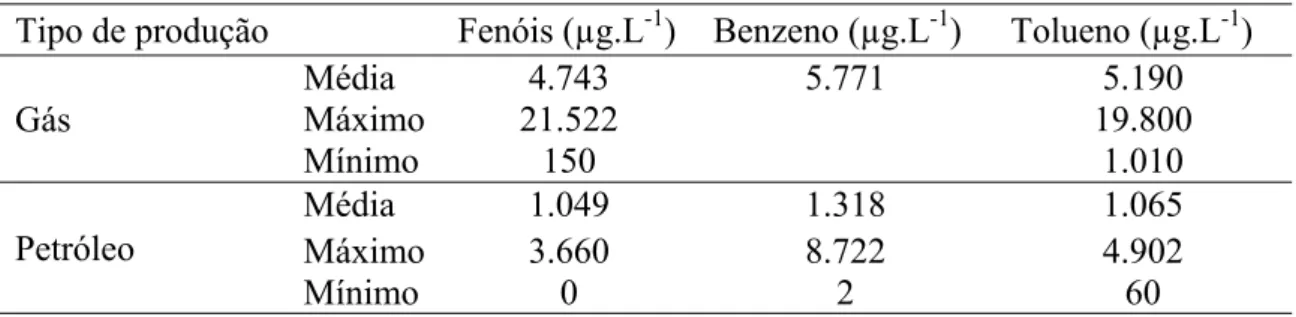
Tabela 3.1 - Fenóis e compostos aromáticos voláteis em água associada a produção petróleo.
Tipo de produção Fenóis (µg.L-1) Benzeno (µg.L-1) Tolueno (µg.L-1) Gás
Média 4.743 5.771 5.190
Máximo 21.522 19.800
Mínimo 150 1.010
Petróleo
Média 1.049 1.318 1.065
Máximo 3.660 8.722 4.902
Mínimo 0 2 60
Fonte: STEPHENSON, 1991
Tabela 3.2 - Hidrocarbonetos Policíclicos Aromáticos polinucleados (HPAs)
Fonte: STEPHENSON, 1991
As águas produzidas são efluentes complexos, com altas salinidades e composição química que pode variar amplamente, dependendo do tipo de campo, idade, origem e qualidade do óleo. Os compostos que normalmente compõem esta água são: óleo disperso e dissolvido, sais minerais dissolvidos, sólidos oriundos da corrosão, graxas e asfaltenos, produtos químicos adicionados para prevenir e/ou tratar problemas operacionais, tais como biocidas, inibidores de incrustação, quebradores de espumas, coagulantes, quebradores de emulsão, surfactantes e inibidores de corrosão, e gases dissolvidos, incluindo CO2 e H2S
(STEPHENSON, 1991).
As águas produzidas apresentam em sua constituição diferentes concentrações de cátions (Na+, K+, Ca2+, Mg2+, Ba2+, Sr2+, Fe2+) e ânions (Cl -, SO42-, CO32-, HCO3-), sendo
esses íons os responsáveis pelo potencial de incrustação destas águas. Além dos íons, outros compostos estão presentes na água de produção, por exemplo, as espécies químicas (WANG e MA, 2006). A Tabela 3.3 mostra a concentração de metais presentes em água de produção.
Naftaleno (µg.L-1) Outros HPAs (µg.L-1)
Tabela 3.3 – Metais presentes na composição química de uma água associada à produção de petróleo.
Fonte: (STEPHENSON, 1991)
3.2.3 Espécies químicas e seus efeitos tóxicos
Os metais são classificados segundo Salgado (1996), em:
• elementos essenciais: sódio, potássio, cálcio, ferro, zinco, cobre, níquel e magnésio;
• micro-contaminantes ambientais: arsênico, chumbo, cádmio, mercúrio, alumínio, titânio, estanho e tungstênio;
• elementos essenciais e micro-contaminantes simultaneamente, cromo, zinco, ferro, cobalto, manganês e níquel.
Os efeitos tóxicos dos metais são considerados como eventos de curto prazo, agudos e evidentes. Atualmente, ocorrências a médio e longo prazo são observadas, e as relações causa-efeito são pouco evidentes e quase sempre subclínicas. Geralmente os efeitos são difíceis de serem distinguidos e perdem em especificidade, pois podem ser provocados por outras substâncias tóxicas ou por interações entre esses agentes químicos (SALGADO, 1996). Na produção de óleo os rejeitos de perfuração são cascalhos da formação e os fluidos de perfuração, que podem ser à base de água ou de óleo. O primeiro pode conter em sua formulação agentes controladores de viscosidades, por exemplo, argila, agentes controladores de densidade (sulfato de bário ou barita), defloculantes (lignosulfato de cromo ou lignita), hidróxido de sódio, inibidores de corrosão, biocidas, lubrificantes, materiais de perda de circulação e outros agentes compatibilizantes com a formação. Os fluidos a base de óleo também contêm hidrocarbonetos como fase contínua e outros produtos químicos para manter a emulsão da água em óleo. O hidrocarboneto mais utilizado nesses fluidos é o diesel, seguido pelos óleos minerais e sintéticos, que são menos tóxicos (REIS, 1996).
Os fluidos de perfuração caracteristicamente contêm espécies químicas como o bário, cromo, cádmio, mercúrio e chumbo. Esses elementos podem entrar no sistema a partir dos produtos adicionados ao fluido ou a partir dos minerais de ocorrência natural nas formações
Cd (µg.L-1)
Cr (µg.L-1)
Cu (µg.L-1)
Pb (µg.L-1)
Ni (µg.L-1)
Ag (µg.L-1)
Zn (µg.L-1) Média 27 186 104 315 192 63 170 Máximo 98 390 1.455 5.700 1.674 152 1.600
Mínimo 0 0 0 2 0 12 17
que estão sendo perfurados. Esses metais, entretanto, não são tipicamente biodisponíveis (REIS, 1996).
A toxicidade das espécies químicas encontrados no segmento upstream da indústria do petróleo varia amplamente. Essa toxicidade das espécies químicas está relacionada à sua interferência nas atividades enzimáticas, que pode limitar ou interromper os processos bioquímicos nas células. Seus efeitos são gerais e incluem danos ao fígado, rins, ou sistema reprodutivo, nervoso e sanguíneo. No caso de alguns metais, além desses efeitos podem ser incluídas as mutações ou tumores. A concentração de espécies químicas permitida para a água potável varia para cada metal, mas se encontra geralmente abaixo de 0,01 mg/L. As espécies químicas presentes nos fluidos de perfuração que são descartados em alto mar (offshore) normalmente se combinam rapidamente com os sulfatos encontrados em abundância na água do mar, que formam sais insolúveis precipitando e sendo depositado no fundo do mar (REIS, 1996).
3.2.4 Impactos ambientais causados pela água de produção
O descarte inadequado de águas produzidas pode poluir o solo, águas subterrâneas, bem como, águas superficiais, que pode implicar em efeitos nocivos e irreversíveis ao meio ambiente, na repercussão negativa indesejada, bem como a aplicação de penalidades, diversas ações corretivas e mitigadoras, que em geral são de alto custo.
Pensando nisso, as agências reguladoras ambientais estabelecem nos parâmetros presentes nas águas produzidas os limites máximos permitidos para o descarte de água associada à produção de petróleo.
de concentração média aritmética simples mensal do TOG de até 29 mg/L, e o valor máximo diário de 42 mg/L.
Por outro lado, países que apresentam grande volume de água associada à produção de petróleo, estão cada vez mais focando esforços para encontrar métodos de tratamento para remoção de poluentes que sejam mais eficientes e de menor custo-benefício, assim poderão complementar seus limitados recursos de água doce.
A reutilização e a reciclagem de água associada à produção de petróleo incluem a injeção subterrânea para aumentar a produção de óleo, após tratamento, podendo também ser usada em produção de pasto, ornamentação, e também, em aplicações industriais, tais como, controle de diminuição de poeira, lavagem de veículos, pátios de jardinagem, controle do fogo e em caldeiras (VEIL, et al., 2004).
Wathern (1988) apud Sánchez (2006) definiu impacto ambiental como sendo: “a mudança em um parâmetro ambiental, num determinado período e numa determinada área, que resulta de uma dada atividade, comparada com a situação que ocorreria se essa atividade não tivesse sido iniciada.”
Os impactos ao meio ambiente causado pela água associada à produção de petróleo são devido a vários elementos que a compõem. A combinação de um ou mais elementos a torna potencialmente perigosa, podendo poluir rios, mares, lagos, aquíferos, solos, e causar danos a fauna e a flora (SILVA, 2000).
O impacto ambiental causado pelo descarte de águas contendo óleo disperso em um corpo receptor (onde será lançado o efluente) dependerá da localização do ponto de descarga, da profundidade e de suas características. Além dessas, outras considerações devem ser levadas em conta, por exemplo, as características de escoamento, taxas de diluição dos constituintes presentes na composição da água de produção no ambiente, os quais estão relacionados com a velocidade de corrente, da altura da coluna d’água, do volume total e das taxas de circulação de água (RIBEIRO, 1995 apud FREIRE, 1999).
Segundo Silva (2000), as principais causas potenciais de perigo atribuídas à água associada à produção de petróleo, é a presença da salinidade, de sólidos suspensos, metais pesados, orgânicos insolúveis e solúveis, produtos químicos e radioativos.
Tabela 3.4 – Efeitos causados pelas substâncias presentes na água associada à produção de petróleo.
Causas Efeitos
Alta salinidade Uso na irrigação, a salinidade torna o solo improdutivo para a agricultura, devido ao sódio
Sólidos suspensos
Grande quantidade de sólidos pode interferir na autopurificação de rios e ocasiona depósitos de lama, danifica pontos de pesca e pode impactar esteticamente os mananciais.
Metais pesados Capacidade de bioacumulação na cadeia alimentar. Orgânicos insolúveis São tóxicos para peixes, reduzem a geração, causam gosto
desagradável e aparência inaceitável á água. Orgânicos solúveis Responsáveis por efeitos tóxicos agudos. Produtos químicos
Biocidas - podem ser tóxicos a muitos organismos.
Biodegradáveis e surfactantes podem ser potencialmente perigosos em concentrações elevadas
Radioatividade Ra-226, Ra-228 e Es-90 os quais tendem a bioacumular, como os metais pesados, em peixes e crustáceos
Fonte: ELIAS-SAMLALSINGH e AGARD, (2003); HAMILTON e MEINHOLD, (1992) apud
AHMADUN et al., (2009).
A medida básica do impacto ambiental dos resíduos do petróleo é a sua toxicidade aos organismos expostos. A toxicidade de uma substância é mais comumente empregada como sendo a sua concentração em água que resulta na morte da metade dos organismos expostos em um determinado intervalo de tempo (REIS, 1996).
3.2.5 Custo de tratamento da água associada à produção de petróleo
Quando um barril de água é produzido, os operadores têm duas opções: a água pode ser eliminada das instalações de superfície ou reinjetada ao fundo de poço para controle de pressão. Ambas as opções implicam em custos adicionais.
Uma tendência recente da indústria petrolífera nos EUA é completar operações que são iniciadas por IOR (recuperação avançada) de imediato, e não a longo prazo de produção, como normalmente acontece. Muitas vezes, as propriedades são vendidas logo no início de vida do reservatório, juntamente com todos os problemas associados, incluindo a produção de água.
Registros precisos de geração de água de produção são difíceis de obter, mesmo assim são necessários porque afeta a vida econômica dos poços produtores. Mais dinheiro é gasto em água de processamento do que em todos os outros serviços do campo petrolífero. O custo do tratamento da água associada à produção de petróleo varia muito, mas, na maioria dos casos, uma abordagem mais pró-ativa no início da vida de um poço levará a uma melhor economia para a indústria. Essa abordagem pró-ativa para o problema da água na produção de petróleo e gás poderia reduzir significativamente os custos operacionais e aumentar a vida útil econômica do bem (RICHARD, 2004).
No Rio Grande do Norte, em 2008, o custo para o tratamento e descarte da água associada à produção de petróleo encontrava-se estimado no valor de US$ 1,00/bbl (GALVÃO, 2008). Se o volume gerado de água produzida, por exemplo, fosse de 120.000 m3/d e considerando, que a capacidade de um (1) barril seja de 0,159 m3, tomando como base o custo de tratamento segundo Galvão (2008) de US$ 1,00/bbl, logo, os custos do tratamento desse volume de água produzida seriam de US$ 760.000,00 por dia.
Do ponto de vista econômico e devido à alta valorização do petróleo no mercado, o tratamento da água associada à produção de petróleo pode ser considerado viável, apesar do grande volume gerado e os custos envolvidos.
3.2.6 Tipos de métodos utilizados para o tratamento da água associada à produção de petróleo O tratamento da água é uma opção eficaz desde que ao ser aplicado possa remover as substâncias nocivas aos organismos que compõe as cadeias alimentares, deixando-a um resíduo inofensivo, valioso e disponível para diversas atividades.
Em geral os objetivos do tratamento da água associada, segundo FAKHRU’L-RAZI (2009), são:
• Remover óleo disperso e graxa (TOG);
• Remover orgânicos solúveis;
• Realizar a desinfecção;
• Remover gás dissolvido: remover gases de hidrocarbonetos leves, dióxido de carbono e sulfeto de hidrogênio;
• Dessalinizar: remover os sais dissolvidos;
• Abrandar: diminuir a dureza da água;
• Outros: remover Material Radioativo Ocorrido Naturalmente (NORM).
Os métodos comumente utilizados para realizar o tratamento são os físicos, os químicos e os biológicos. De acordo com FAKHRU’L-RAZI (2009), esses processos podem ser aplicados separadamente e/ou combinados.
Os tratamentos físicos são: adsorção de compostos orgânicos dissolvidos em carvão ativado, argila organofílica, copolímeros, zeólito e resinas, filtros de areia, ciclones, evaporação, precipitação de ar dissolvido, membrana filtrante e C-TOUR, uma tecnologia patenteada, que é uma substância líquida condensada usada como líquido de extração para os componentes dissolvidos na água produzida (FAKHRU’L-RAZI, 2009).
Os tratamentos químicos utilizados são: precipitação química, oxidação química, processo eletroquímico, fotocatalítico, Fenton, uso de ozônio e desemulsificante.
O tratamento biológico é realizado com microrganismos aeróbios e anaeróbios.
3.2.7 Reuso da água associada à produção de petróleo
3.3 Princípio da eletroquímica
3.3.1 Definição e funcionamento de uma célula eletroquímica
Segundo Bard et al. (1980), a eletroquímica é definida como sendo o estudo das interfaces carregadas eletricamente e dos fenômenos que ocorrem nestas interfaces, as quais são consideradas superfícies de separação entre um condutor eletrônico e um condutor iônico. O condutor eletrônico pode ser um metal ou semicondutor e o condutor iônico, uma solução eletrolítica, podendo ser soluções líquidas ou um sal fundido, por exemplo, NaCl (cloreto de sódio) ou sólido, tal como, o sódio β-alumina, que tem íons móveis de sódio. Esse sistema formado, quando posto em contato, é denominado de eletrodo (BARD et al., 1980).
De maneira geral pode-se dizer que a eletroquímica é o estudo de fenômenos químicos associados a fenômenos elétricos. Segundo Ticianelli, et al. (2006), essa passagem de corrente elétrica através de uma célula eletroquímica provoca um desequilíbrio no sistema e ela está associado aos seguintes fenômenos:
• Transferência de carga, necessariamente ocorre um par de reações nos eletrodos;
• Condução iônica, a movimentação de espécies na solução eletrolítica;
• Polarização eletródica, deslocamento dos potenciais dos eletrodos.
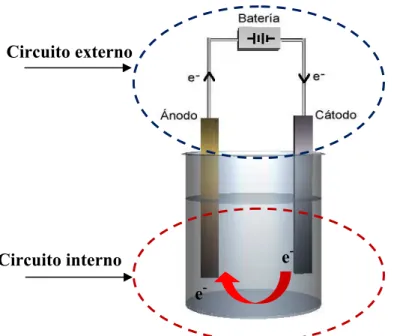
A passagem de corrente gera um circuito elétrico na célula eletroquímica e pode ser dividido em duas partes (SCHULTZ, 2003):
• A primeira refere-se ao circuito elétrico externo, onde a corrente (I) flui em direção do anodo para o catodo ocorrendo um fluxo de elétrons;
• A segunda ocorre dentro da célula, na qual a corrente (I) flui eletricamente dentro da estrutura dos eletrodos, os quais por estarem imersos em uma solução eletrolítica, promove a passagem de fluxo da corrente (I) por migração de íons, onde os ânions migram em direção ao anodo (pólo positivo) e os cátions em direção ao catodo (pólo negativo).
Figura 3.5 – Direção do fluxo de elétrons do anodo para o catodo em uma célula eletroquímica.
Os fenômenos químicos envolvidos na eletroquímica são reações diversificadas que ocorrem nas células eletroquímicas, com variações de simples reações monofásicas do tipo redox, que envolve desde a fase de transição (deposição de metal, evolução de gás, precipitação e outras) a reações de múltiplos-estágios, combinando processos químicos e eletroquímicos.
Essas reações simples de redox, por exemplo, com um metal (M), são favorecidas quando é aplicado um potencial sobre os eletrodos através de uma fonte de corrente contínua. O material anodo sofre a oxidação, enquanto no catodo, ocorre a redução do metal (M). As reações 3.1, 3.2, 3.3 e 3.4 mostram como essas reações ocorrem em cada eletrodo (MOLLAH, etal., 2004).
No anodo (ocorre a reação de oxidação):
(3.1)
(3.2)
e
-e -Circuito externo
No catodo (ocorre a reação de redução):
(3.3)
(3.4)
Onde n corresponde ao nº do nox (número de oxidação) do elemento químico, ou nº de elétrons envolvidos na estequiometria das reações 3.1 e 3.3. Segundo Walsh (1993), essa estequiometria, refere-se ao balaço de carga envolvida no processo de redução (no catodo), que deve ser o mesmo para o processo de oxidação (no anodo). A Figura 3.4 mostra o fluxo de elétrons distribuídos na célula eletroquímica.
3.3.2 Lei de Faraday
Segundo Scott (1995), a taxa de transferência de carga em uma célula eletroquímica é dada pela taxa total das reações no eletrodo, que é medida pela corrente (I). A relação entre a passagem de carga e a quantidade de reação é encontrada através da Lei de Faraday. Além disso, a quantidade de carga passada (q) em um determinado intervalo de tempo (t), como mostrado na Equação 3.5, indica a quantidade total da reação que ocorreu em uma célula eletroquímica. Esse fenômeno denominado de eletrólise foi resumido por Faraday.
(3.5)
Faraday descobriu que íons de metal são depositados no estado de metal sólido quando uma corrente elétrica flui através de uma solução iônica de um sal do metal, por exemplo, a semi-reação Mn+ + ne-→ M, representa a deposição desse metal (SALVADOR e USBERCO, 1997).
A massa eletrolisada (m) é diretamente proporcional à carga que atravessa a solução, que é dada pela Equação 3.6 (SCHULTZ, 2003).
(3.6) Onde β é uma constante e q a carga.
(3.7) Onde:
K : constante de proporcionalidade, Mi: massa molar da espécie química i (g.mol-1) e
ni: número de elétrons envolvidos na reação eletroquímica.
Após as substituições de parâmetros, a Equação 3.6 passa a ser representada pela Equação 3.8:
(3.8) O inverso do valor de K, ou seja, F = 1/K é denominado como sendo a constante de
Faraday (F), que é calculada pelo produto da carga de um elétron por 1 mol de elétrons. A Equação 3.9 mostra o produto corresponde à quantidade de carga transportada pela passagem de 1 mol de elétrons (SALVADOR e USBERCO, 1997).
(3.9)
Assim, substituindo as Equações 3.9 e 3.5 na Equação 3.8, resulta na quantidade de massa que pode ser eletroprocessada a uma dada corrente que passa através da solução eletrolítica num intervalo de tempo (PONTE, 1998).
(3.10)
3.3.3 Eficiência de corrente (EC)
De acordo com Chen, (2004), a eficiência de corrente indica a especificidade de um processo, o desempenho da eletrocatalise das reações envolvidas na superfície do eletrodo, bem como, a transferência de massa.
(3.11) A eficiência de corrente (EC) é o rendimento de um processo baseado na passagem de carga e pode ser definida, como:
(3.12)
A eficiência de corrente é obtida a partir da medida da quantidade de produto formado, ou reagente consumido, mi e a quantidade teórica, m, é mostrado pela Equação 3.13.
(3.13)
Substituindo o valor de m dado pela equação 3.10 tem-se, a Equação 3.14
(3.14)
3.3.4 Potencial do eletrodo e densidade de corrente
Quando a corrente flui, o eletrodo é dito polarizado e o potencial de equilíbrio da célula é composto a partir dos dois componentes: o potencial de equilíbrio do anodo e o potencial de equilíbrio do catodo, cada um desse representando uma meia-célula, como mostra a Equação 3.15 (SCOTT, 1995).
(3.15)
Onde:
(Ee)c : Potencial de equilíbrio do catodo (V);
(Ee)a: Potencial de equilíbrio do anodo (V).
(3.16) 3.3.5 Reatores eletroquímicos
O reator eletroquímico é uma versão industrial da célula eletroquímica. Sua aplicação depende largamente do seu projeto (design) industrial e da implementação de uma ou mais unidades efetivas do reator (SCOTT, 1995).
Fatores que são importantes no projeto de um reator eletroquímico: Produtividade - capacidade de tratamento;
Consumo energético e voltagem da célula (a aplicação de altas voltagens faz aumentar o consumo de energia);
Controle de temperatura (alta voltagem possibilita dissipação de energia em forma de calor, aumentando a temperatura do efluente durante o processo de tratamento);
Hidrodinâmica (vazão e fluxo de entrada e saída do efluente) e transporte de massa (perda de massa do anodo de sacrifício);
Fatores operacionais do reator (densidade de corrente, tempo de residência, concentração da solução eletrolítica, concentração dos contaminantes);
Material do eletrodo (ferro, alumínio, aço inox, ADE). 3.3.5.1 Capacidade de produção e rendimento
A capacidade de produção de um reator eletroquímico está relacionada diretamente à aplicação da densidade de corrente que pode ser expressa pela Equação 3.17.
(3.17)
Enquanto que, o rendimento (YST) de um determinado reator é especificado pela
3.3.5.2 Consumo energético (CE)
O consumo energético é dado pela quantidade de energia consumida para depositar uma unidade de massa do metal, como mostra a Equação 3.19 (ÖNDER, et al., 2006).
(3.19)
Onde:
i: corrente aplicada (A); V: valor do potencial (Volt); t: tempo (h);
C0: concentração inicial do contaminante (mg L-1);
C: concentração no tempo ‘t’ (mg L-1); Q: taxa de vazão da solução (L min-1). 3.3.6 Objetivos da técnica eletroquímica
Atualmente esses processos eletroquímicos têm sido desenvolvidos de acordo com a tecnologia existente exigida ao tratamento e também o nível de toxicidade dos efluentes industriais. Esses processos visam minimizar os efeitos nocivos dos contaminantes presentes nesses dejetos, sendo parte integrante das unidades de tratamentos. Segundo pesquisadores, os processos eletroquímicos seriam incluídos como uma das etapas subseqüente de forma combinada com outros processos físicos, químicos e/ou biológicos em uma estação de tratamento de efluentes (CHEN, 2004).
3.3.7 Vantagens e desvantagens dos processos eletroquímicos
A tecnologia eletroquímica tem alcançado um nível que pode ser comparada com outras técnicas de tratamento de efluentes, segundo algumas vantagens e desvantagens (SILVA, 2005a e RAJESHWAR e IBAÑEZ, 1997).
Vantagens:
Os equipamentos são simples e de fácil operação;
A unidade eletroquímica pode ser acoplada como uma das seqüências das etapas de processo em uma planta de tratamento de efluentes;
Pode ser utilizado como etapa de processo reduzindo ou degradando os compostos químicos que podem influenciar na eficiência do tratamento biológico;
Não usa produtos químicos nocivos e prejudiciais ao meio ambiente; Processo de tratamento a frio (tratamento a temperatura ambiente); Plantas relativamente compacta;
A eletrocoagulação inclui alta eficiência na remoção de partículas em suspensão (exemplo: óleos e graxas);
Atendimento à legislação ambiental (redução do teor de óleos e graxas); Segurança (facilidade operação);
Seletividade (possibilidade de escolha do eletrodo específico para um determinado contaminante);
Efetividade de custo (uso de células fotovoltaicas na conversão em energia elétrica para redução de custo no consumo de energia utilizada no tratamento);
Flexibilidade na automação (substituição de energias renováveis, solar no lugar de energia elétrica convencional, uso de eletrodos de variados tipos de metais).
Desvantagens:
Baixa atuação em compostos que não são eletroquimicamente degradados, por exemplo: o Fenol;
Uso de alto potencial sobre contaminantes que requer potencial de redução elevado, necessitando de maior consumo de energia. O Bário tem alto potencial de redução, para sua redução é necessário aplicar um potencial (V) elevado o que leva ao aumento do consumo de energia;
Os eletrodos são consumidos e necessitam de substituição regularmente. Esse desgaste dependerá do tipo do material do eletrodo. No caso de eletrodos de ferro e alumínio que possuem baixo custo, não é considerado como desvantagem;
3.3.8 Estudos e aplicações da eletroquímica na indústria de petróleo
A eletricidade como método utilizado em técnica de tratamento tem sido usada desde o século XIX. A primeira aplicação ocorreu em 1889, no Reino Unido, em tratamento de água. Outra utilização se deu em 1904, quando Elmore fez uso da eletrólise para beneficiar o mineral (Chen, 2004).
Atualmente, o processo eletroquímico tem sido usado numa ampla faixa de aplicação, como por exemplo, na recuperação e remoção de metais pesados, separação e recuperação de óleo e graxas, na oxidação de substâncias orgânicas e também, em técnicas para tratamento de água e de efluentes industriais.
Vários estudos contribuíram para a aplicação da eletroquímica na indústria de petróleo, tais como: Comninellis et al. 1997; Zanta et al. 2005; Santos et al. 2007; Nahui et al. 2008; 2010; Wei et al. 2010; Moussavi et al. 2011, conforme estudo destes pesquisadores, os processos eletroquímicos podem ser incluídos como uma das etapas de tratamento em uma estação de tratamento de efluentes combinado com outros processos físicos, químicos e/ou biológicos. Sua aplicação tem sido desenvolvida de acordo com a tecnologia exigida ao tratamento e pelos contaminantes presentes nos efluentes industriais.
A eletroquímica é uma tecnologia bastante versátil, pois permite a utilização de eletrodos com diferentes tipos de materiais conforme o tipo de contaminante que se deseja eliminar. Além do mais, pode ser considerada como uma tecnologia “limpa” por não necessitar de reagentes químicos para realizar o tratamento.
As técnicas de eletrodeposição, eletrocoagulação (EC), eletroflotação (EF) e oxidação eletroquímica, foi revisada por Chen (2004), nesta pesquisa foram observados que os estudos combinando as técnicas da eletrocoagulação com a eletroflotação apresentavam maior eficiência na remoção de poluentes utilizando eletrodos de alumínio, ferro ou híbridos (Al/Fe). Também foram observados vários tipos de células eletroquímicas com fluxo de alimentação pela vertical e horizontal, várias unidades ou reatores eletroquímicos com geometria cúbica e cilindrica, onde a melhor eficiência no tratamento dependia das características dos efluentes e da carga de poluentes presentes.
3.3.8.1 Oxidação eletroquímica
Brasileiro et al. (2005) estudaram o efeito da oxidação eletroquímica do fenol presente em águas de produção de campos de petróleo. O tratamento foi realizado em reator de fluxo ascendente utilizando efluente sintético com as mesmas características e composição da água de produção do Pólo Petroquímico de Guamaré-RN. O reator eletroquímico possuía uma geometria cilíndrica com eletrodos de inox (o catodo) e ADE® (anodo). Para seus experimentos foi realizado planejamento experimental do tipo fatorial 22 e com as variáveis de controle, potencial elétrico e vazão. Os autores concluíram na sua pesquisa que o coeficiente de correlação (R2) obtido para as variáveis respostas, o percentual de remoção de sulfeto e consumo energético foram de 90 e 97 %, comprovando o ajuste dos seus dados experimentais ao modelo quadrático utilizado na análise estatística. Através da relação, FCalculado/FTabelado, aplicado para as taxas de remoção do N-NH4+ e fenol, observou-se que as