PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA
TESE DE DOUTORADO
OTIMIZAÇÃO DA SÍNTESE DO AlSBA-15 PARA
PRODUÇÃO DE BIODIESEL POR
TRANSESTERIFICAÇÃO DO ÓLEO DE COCO
Gicélia Rodrigues
Orientador: Prof. Dr. Marcus Antônio de Freitas Melo (DEQ/UFRN)
Coorientador: Prof. Dr. Marcelo José Barros de Souza (DEQ/UFS)
OTIMIZAÇÃO DA SÍNTESE DO AlSBA-15 PARA
PRODUÇÃO DE BIODIESEL POR
TRANSESTERIFICAÇÃO DO ÓLEO DE COCO
Tese apresentada ao Corpo Docente do Programa de Pós-graduação em Engenharia Química – PPGEQ, da Universidade Federal do Rio Grande do Norte – UFRN, como parte dos requisitos necessários à conclusão do curso de Doutorado, sob a orientação do Prof. Dr. Marcus Antônio de Freitas Melo (DEQ/UFRN) e do Prof. Dr. Marcelo José Barros de Souza (DEQ/UFS).
Catalogação da Publicação na Fonte. UFRN / CT / DEQ
Biblioteca Setorial Professor Horácio Nícolás “ólimo .
Rodrigues, Gicélia.
Otimização da síntese do AlSBA-15 para produção de biodiesel por transesteri-ficação do óleo de coco / Gicélia Rodrigues. - Natal, 2014.
130 f.: il.
Orientador: Marcus Antônio de Freitas Melo. Coorientador: Marcelo José Barros de Souza.
Tese (Doutorado) - Universidade Federal do Rio Grande do Norte. Centro de Tecnologia. Departamento de Engenharia Química. Programa de Pós-graduação em Engenharia Química.
1. Biodiesel - Tese. 2. Óleo de coco - Tese. 3. Biocombustíveis - Tese. 4. Die-sel - Tese. I. Melo, Marcus Antônio de Freitas. II. Souza, Marcelo José Barros de. III. Universidade Federal do Rio Grande do Norte. IV. Título.
Engenharia Química. Área de Concentração: Engenharia Química, Natal/RN, Brasil. Orientador: Prof. Dr. Marcus Antônio de Freitas Melo (DEQ/UFRN)
Coorientador: Prof. Dr. Marcelo José Barros de Souza (DEQ/UFS)
RESUMO: O estímulo à produção e ao consumo do biodiesel favorece a política de preservação ao meio ambiente contribuindo na redução de gases, causadores do aquecimento globo, assim reduzindo as alterações climáticas. A tendência atual das pesquisas nesse campo foca no aprimoramento desses processos com o uso de catalisadores heterogêneos, visto que eles apresentam vantagens significativas, tais como: menor contaminação dos produtos, facilidade de separação do catalisador do meio reacional, possibilidade de reaproveitamento do catalisador, diminuição dos problemas de corrosão. O objetivo deste trabalho foi a otimização da síntese de AlSBA-15 para a produção de biodiesel através do processo de transesterificação via rota etílica, utilizando planejamento fatorial 23 com onze ensaios de síntese hidrotérmica. Para a otimização da síntese hidrotérmica do catalisador tipo AlSBA-15 foi montada uma matriz experimental fatorial 23 com onze ensaios. As quantidades estequiométricas dos materiais precursores foram variadas de acordo com diferentes razões de Si/Al que é um dos fatores do planejamento experimental, além o tempo e temperatura de envelhecimento do gel de síntese. O material que apresentou os melhores resultados de caracterização ( SBET = 591,7(m2/g); Vp = 0,83(cm3 /g ); Dp = 5,59 (nm); w = 6,48(nm)) foi
sintetizado a 100°C, por 24 horas, com razão de Si/Al = 10. Este material foi aplicado como catalisador heterogêneo na reação de transesterificação etílica como matéria-prima o óleo de coco in natura. O óleo de coco apresentou-se com uma matéria-prima apropriada para obtenção do biodiesel via rota etílica. Os aspectos visuais e as características físico-químicas, dos produtos da reação, mostram que o catalisador AlSBA-15 favoreceu a reação. De acordo com as análises físico-químicas a ordem de estabilidade oxidativa do produto da reação de transesterificação foi: reação catalítica a 150°C > reação não catalítica a 100°C > Reação catalítica a 100°C > Reação catalítica a 200°C. Os resultados de estabilidade oxidativa e viscosidade cinemática mostram que o biodiesel produzido na areação catalítica realizada a 150°C foi a que se manteve dentro das normas ABNT NBR 7148, ABNT NBR 10441 e EN 14112.
Engineering, Area of Concentration: Chemical Engineering, Natal/RN, Brazil.
Supervisor: Prof.Dr. Marcus Antônio de Freitas Melo (DEQ/UFRN
Co-supervisor: Prof.Dr. Marcelo José Barros de Souza (DEQ/UFS).
ABSTRACT
Stimulus encouraging the production and consumption of biodiesel favors the policy of pre-serving the environment, contributing to the reduction of greenhouse gas reducing climate change. The current trend of research in this field focuses on improving these processes with the use of heterogeneous catalysts, seeing has significant advantages such as: low contamination of products, ease of separation of the catalyst from the reaction medium, possibili-ty of reuse of the catalyst, decreased corrosion problems. The objective of this research was to optimize the synthesis of AlSBA-15 for the production of biodiesel through transesterification process via ethyl route. For the optimization of hydrothermal synthesis of type AlSBA-15 catalyst has assembled a 23 factorial experimental matrix with eleven trials. The stoichiometric amounts of starting materials were varied according to different ratios Si / Al which is a factor in the experimental design, in addition to the time and temperature of aging of the synthesis gel. The material showed the best results of characterization (SBET = 591.7 (m2 / g), Vp = 0.83 (cm3 / g), Dp = 5.59 (nm), w = 6.48 (nm) was synthesized at 100 ° C for 24 hours, with a ratio Si / Al = 10.This material was applied as a heterogeneous catalyst in the reaction of ethyl transesterification as raw coconut oil in natura. Coconut oil presented suitable for obtaining biodiesel via ethyl route.The visual aspects and physical-chemical characteristics of the reaction products show that AlSBA-15 catalyst favored the reaction. According to physical-chemical analysis the order of oxidative stability of the product of the transesterification reaction was: catalytic reaction at 1500 ° C> non-catalytic reaction at 100 ° C> 100 ° C catalytic> catalytic reaction at 200 ° C Reaction. The results of oxidative stability and kinematic viscosity shows that the biodiesel produced in the catalytic sandblasting held at 150 ° C which was maintained within the ABNT NBR 7148, ABNT NBR 10441 and EN 14112.
Aos meus pais, que me ensinaram o verdadeiro amor da vida, dando-me disciplina e incentivo em tudo que eu faço. A minha avó (Valdice) que, por muitas vazes sentiu a minha ausência nas reuniões familiares, minha razão de viver. Agradeço a vocês por quem sou!
Agradeço primeiramente ao Espírito Santo, que ilumina o meu caminho a cada dia. Aos meus pais, que são as pessoas mais importantes da minha vida, pois o amor que a me dedicaram é o meu maior legado,
Aos meus irmãos, que são meus grandes e verdadeiros amigos.
Aos meus sobrinhos e sobrinhas, afilhados e afilhadas, cujos sorrisos revelam a espe-rança no futuro e me fortalecem a cada dia.
Aos meus amigos do grupo de Catalise do LabCat (UFS), e ao Grupo do LabTam (UFRN) pelas importantes contribuições em todos os momentos. E a todos os meus amigos em especial agradeço a Cléa, Lídia Gabriela, Larissa, Rodolfo Luiz, Rodrigo Melo, Sheyla Almeida, Maria de Socorro, Maria Susana e pela grande ajuda no momento final deste traba-lho.
A Professora Luciene e ao Professor Eledir pelo grande carinho que tenho recebido com bastante alegria a todo instante.
Aos professores doutores Marcus Antonio Freitas de Melo, Marcelo José Barros de Souza,Dulce Maria de Araújo Melo, Anne MIchelle G.P de Souza pela excelente orientação, disposição e paciência, sem os quais este trabalho não teria se realizado. Muito obrigada, por me aceitarem com orientanda!
Aos professores doutores Joana Maria Farias Barros, Renata Martins Braga, Carlos Henrique Catunda Pinto e João Marci de Andrade, meus sinceros agradecimentos pela parti-cipação nesta banca de tese, o que certamente contribuirá para melhoria na minha vida aca-dêmica.
Aos professores do Departamento de Engenharia Química (UFS), pela contribuição em meu processo de formação. A Mazinha, secretária da Pós Graduação de Engenharia Quí-mica(UFRN), pelo seu carinho e gentileza no atendimento aos alunos.
Ao Laboratório de Combustíveis e Materiais (LaCom-UFPE), pela realização das aná-lises do biodiesel.
1. INTRODUÇÃO ... 2
2. REVISÃO BIBLIOGRÁFICA ... 5
2.1-COMBUSTÍVEIS QUE MAIS CONTRIBUEM NA EMISSÃO DE GASES DO EFEITO ESTUFA ... 5
2.2-DEFINIÇÕES DE BIOCOMBUSTÍVEIS... 9
2.3-HISTÓRICOS DOS BICOMBUSTÍVEIS ... 9
2.4-MATÉRIAS PRIMAS PARA PRODUÇÃO DE BIODIESEL ... 13
2.4.1 - Extração do óleo de coco ... 16
2.4.2 - Óleos e Gorduras ... 17
2.4.3 - Álcool ... 21
2.5-MÉTODOS PARA PRODUÇÃO DE BIOCOMBUSTÍVEIS ... 22
2.5.1 - Transesterificação ... 23
2.5.2 - Esterificação ... 26
2.5.3 - Pirólise ... 27
2.5.4 - Obtenção dos parâmetros cinéticos dos ensaios da pirólise ... 28
2.6-PRINCIPAIS PROPRIEDADES FÍSICO-QUÍMICA DO BIODIESEL ... 34
2.6.1 - Densidade ... 34
2.6.2 - Viscosidade Cinemática a 40 °C ... 34
2.6.3 - Número de Cetanos ... 35
2.6.4 - Comportamento à baixa temperatura... 35
2.6.5 - Estabilidade à Oxidação a 110 °C ... 36
2.6.6 - Água e sedimentos... 37
2.6.7 - Índice de Acidez ... 38
2.7-CATALISADORES NOS PROCESSOS DE PRODUÇÃO DE BICOMBUSTÍVEIS ... 38
2.7.1 - Catálise Homogênea para Produção de Biodiesel ... 38
2.7.2 - Catálise Heterogênea para Produção de Biodiesel ... 39
2.8-PLANEJAMENTO EXPERIMENTAL ... 49
2.8.1 - Planejamento fatorial ... 49
2.8.2 - Execução do planejamento fatorial 2k ... 50
2.8.3 - Metodologia de Análise de Variância ... 54
2.8.4 - Superfície de resposta ... 56
3. METODOLOGIA ... 58
3.1-PLANEJAMENTO EXPERIMENTAL PARA SÍNTESE DO ALSBA-15 ... 58
3.2-SÍNTESE DE CATALISADORES HETEROGÊNEOS TIPO ALSBA-15 ... 59
3.2.1 - Síntese Hidrotérmica do AlSBA-15 ... 59
3.3-CARACTERIZAÇÕES FÍSICO-QUÍMICAS DOS CATALISADORES ... 62
3.3.1 Análise Térmica Via TG/DTG ... 62
3.3.2 - Estudo cinético da remoção do surfactante P123 dos poros do AlSBA-15 ... 62
3.3.3 - Difração de Raios X ... 63
3.3.4 - Espectroscopia na Região do Infravermelho ... 63
3.3.5 - Adsorção de Nitrogênio ... 63
3.3.6 - Microscopia Eletrônica de varredura (MEV) ... 64
3.3.7 - A Microscopia Eletrônica de Transmissão (MET) ... 64
3.3.8 - Metodologia de Análise de Variância ... 64
3.3.9 - Metodologia de superfícies de resposta ... 65
3.4-AVALIAÇÃO CATALÍTICA DO ALSBA-15 COMO CATALISADOR NA REAÇÃO DE TRANSESTERIFICAÇÃO ... 65
4. RESULTADOS E DISCUSSÕES ... 73
4.1-CARACTERIZAÇÃO DO ALSBA-15 ... 73
4.1.1 - Análise térmica via TG/DTG ... 73
4.1.2 - Estudo cinético da remoção do surfactante P123 dos poros do ... 74
AlSBA-15 ... 74
4.1.3 - Espectroscopia na região do infravermelho (FT-IR) - espectros de absorção das amostras de AlSBA-15. ... 75
4.1.4 - Difração de Raios X (DRX) ... 77
4.1.5 - Adsorção de Nitrogênio ... 80
4.1.6 - Microscopia eletrônica de varredura ... 88
4.1.7 - Microscopia eletrônica de transmissão (MET) ... 91
4.2-RESULTADOS DO PLANEJAMENTO EXPERIMENTAL FATORIAL 23 OBTIDOS DOS ENSAIOS DA SÍNTESE DO ALSBA-15 ... 94
4.2.1 - Metodologia de análise de variância ... 94
4.3-TESTES CATALÍTICOS ... 102
4.3.1 - Determinação do índice de acidez ... 102
4.3.2 - Reação de transesterificação do óleo de coco br... 104
4.4-PERFIL TERMOGRAVIMÉTRICO DAS AMOSTRAS DO ÓLEO DE COCO IN NATURA ... 108
4.5-PERFIL DAS CURVAS DE CALORIMETRIA EXPLORATÓRIA DIFERENCIA (DSC) DAS AMOSTRAS DO ÓLEO DE COCO BRUTO E DO PRODUTO DA REAÇÃO DE TRANSESTERIFICAÇÃO. ... 109
5. CONCLUSÕES E SUGESTÕES FUTURAS ... 118
5.1-SUGESTÃO PARA TRABALHOS FUTUROS ... 119
Figura 2. 1 - Emissão de CO2 por tipo de combustível. ... 6
Figura 2. 2 - Emissão de NOx por tipo de combustível. ... 6
Figura 2. 3 - Emissão de CO por tipo de combustível. ... 7
Figura 2. 4 - Emissões de N2O por tipo de combustível. ... 7
Figura 2. 5 - Emissões de CH4 por tipo de combustível. ... 8
Figura 2. 6 - Evolução dos biocombustíveis no Brasil. ... 12
Figura 2. 7 - Cenário das matérias-primas para produção de biocombustíveis. ... 13
Figura 2. 8 - Albúmen do coco. ... 15
Figura 2. 9 - Estrutura química de um triglicerídeo. ... 19
Figura 2. 10 - Composição em ácido graxo presente no óleo de coco in natura. ... 20
Figura 2. 11 - Fluxograma - Rotas de Produção de Bicombustíveis... 22
Figura 2. 12 - Estrutura química do copolímero tribloco Plurônic. ... 41
Figura 2. 13 - Estrutura dos poros da família do SBA. ... 42
Figura 2. 14 - Representação esquemática do SBA-15 antes e após da calcinação. ... 43
Figura 2. 15 - Fluxograma do tratamento pós síntese realizado por Morales at al., 2011. ... 46
Figura 2. 16 - fluxograma da Síntese do SBA-15 descrita por Sang & Bhatia, (2007). ... 48
Figura 2. 17 - Fluxograma da Síntese do AlSBA-15 descrita por Sang & Bhatia, (2007). ... 48
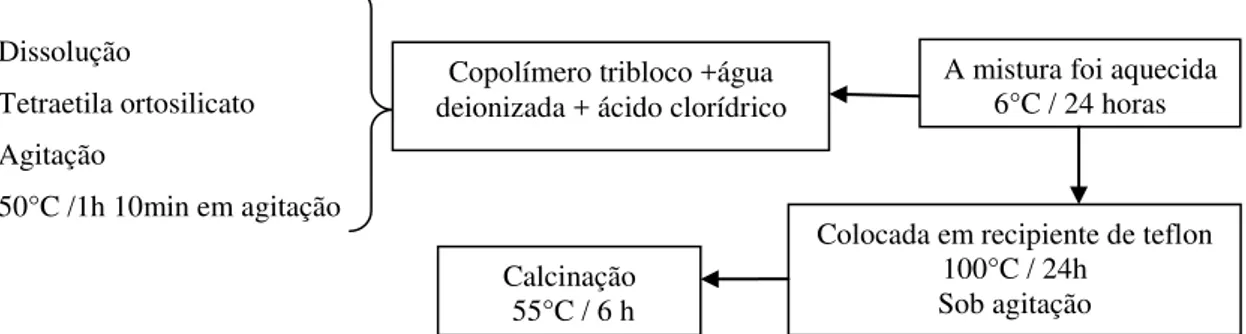
Figura 3. 1 - Fluxograma da metodologia experimental da síntese de AlSBA-15. ... 61
Figura 3. 2 - Reator Parr. ... 69
Figura 3. 3 - (a) catalisador antes da lavagem, (b) catalisador após a lavagem. ... 70
Figura 3. 4 - Decantação dos produtos de reação: (a) reação a 100°C sem catalisador; (b) reação a 100°C com catalisador, (c) reação a 150°C com catalisador; (d) reação a 200°C com catalisador. ... 70
Figura 4. 1 - Curvas de TG e DTG das amostras de AlSBA-15 (INC) não calcinadas em diferentes taxas de aquecimento. 74 Figura 4. 2 - Curva de Energias de ativação aparentes em função do grau de remoção do surfactante P123 dos poros do AlSBA-15. ... 75
Figura 4. 3 - Espectro de infravermelho das amostras do AlSBA-15(IC) calcinado e não calcinado (INC). ... 76
Figura 4. 4 - Difratogramas de raios-X das amostras dos ensaios I, II, III e IV do AlSBA-15 calcinados. ... 78
Figura 4. 5 - Difratogramas de raios-X das amostras dos ensaios V, VI, VII e VIII do AlSBA-15 calcinados. ... 79
Figura 4. 9 - Isotermas de adsorção de N2 e distribuição de diâmetro de poros do AlSBA-15(V). ... 82
Figura 4. 10 - Isotermas de adsorção de N2 e distribuição de diâmetro de poros do AlSBA-15(VI). ... 83
Figura 4. 11 - Isotermas de adsorção de N2 e distribuição de diâmetro de poros do AlSBA-15(VII). ... 84
Figura 4. 12 - Isotermas de adsorção de N2 e distribuição de diâmetro de poros do AlSBA-15(IX). ... 84
Figura 4. 13 -Esquema representativo da estrutura hexagonal de materiais mesoporosos. ... 85
Figura 4. 14 - Variação dos diâmetros médios de poros (Dp), parâmetros mesoporos (a0) e espessura de parede (wt) das diferentes condições de síntese do AlSBA-15. ... 86
Figura 4. 15 - Microscopia Eletrônica de varredura do AlSBA-15 (I). ... 89
Figura 4. 16 - Microscopia Eletrônica de varredura do AlSBA-15 (III). ... 89
Figura 4. 17 - Microscopia Eletrônica de varredura do AlSBA-15 (V). ... 90
Figura 4. 18 - Microscopia Eletrônica de varredura do AlSBA-15 (IX). ... 90
Figura 4. 19 - Imagens de microscopia eletrônica de transmissão do AlSBA-15 (I). ... 92
Figura 4. 20 - Imagens de microscopia eletrônica de transmissão do AlSBA-15 (V). ... 92
Figura 4. 21 - Imagens de microscopia eletrônica de transmissão do AlSBA-15 (IX). ... 93
Figura 4. 22 - Diagrama de Pareto. ... 96
Figura 4. 23 - Gráfico do ajuste do modelo linear. ... 97
Figura 4. 24 - Superfície de resposta relacionando as variáveis tempo e temperatura com a área específica. ... 98
Figura 4. 25 - Superfície de resposta relacionando as variáveis razão de Si/Al e temperatura com a área específica. ... 99
Figura 4. 26 - Superfície de resposta relacionando as variáveis tempo e razão de Si/Al com a área específica. . 100
Figura 4. 27 - Curva de conversão de óleo de coco in natura em função do tempo, nas temperaturas de 40, 60, 80 e 100°C, utilizando catalisador AlSBA-15. ... 103
Figura 4. 28 - (A) Óleo de coco após a prensagem, (B) óleo de coco mantido a temperatura ambiente, (C) produto da reação sem catalisador a 100°C, (D) produto da reação a 100°C com AlSBA-15, (E) ) produto da reação a 150°C com AlSBA-15, (F) produto da reação a 200°C. ... 105
Figura 4. 29 - Espectros de infravermelho (IR): (a) o óleo de coco bruto, (b) produto da transesterificação a 100°C, (c) produto da transesterificação catalíticas a 100°C (d) produto da transesterificação catalítica a 150 e 200°C. ... 106
Figura 4. 30 - TG do óleo de coco bruto... 108
Figura 4. 31 - Curvas de DSC do óleo de coco bruto a diferentes taxas de aquecimento. ... 109
Figura 4. 34 - Gráfico dos valores da tabela da Tabela 4.7. (c) entalpia versus taxa de aquecimento, (d) calor versus taxa de aquecimento. ... 114
Figura 4. 35 - Gráfico dos valores de calor e entalpia obtidos na análise de DSC das amostras do produto de transesterificação. ... 115
Tabela 2. 1 - Percentual das matérias-primas utilizadas para produção de biodiesel por região em abril de 2014.
... 14
Tabela 2. 2 - Fatores e seus níveis para um planejamento fracionado 23... 52
Tabela 2. 3 - Matriz dos experimentos para síntese com ponto central. ... 52
Tabela 3. 1 - Variáveis e seus níveis para um planejamento fracionado 23 da síntese do AlSBA-15... 58
Tabela 3. 2 - Matriz de planejamento experimental para síntese de AlSBA-15. ... 59
Tabela 3. 3 - Reagentes utilizados na síntese do AlSBA-15... 59
Tabela 3. 4 - Identificações dos componentes presentes no óleo de coco utilizado para a realização dos cálculos da massa molar do óleo. ... 67
Tabela 3. 5 - Parâmetros reacionais da transesterificação do óleo de coco. ... 69
Tabela 3. 6 - Parâmetros de Qualidade e Métodos Analíticos do biodiesel. ... 71
Tabela 4. 1 Dados referentes às frequências vibracionais observadas e suas respectivas atribuições feitas para os espectros de infravermelho das amostras de AlSBA-15 não calcinada e calcinada. ... 77
Tabela 4. 2 - Propriedades texturais das amostras de AlSBA-15 C( calcinadas). ... 86
Tabela 4. 3 - A análise de regressão para a área específica do AlSBA-15. ... 95
Tabela 4. 4 - Análise da variância (ANOVA) para o ajuste do modelo matemático para o parâmetro área específica. ... 95
Tabela 4. 5 - Níveis propostos para síntese do AlSBA-15. ... 101
Tabela 4. 6 - principais características físico-químicas do óleo de coco bruto e dos produtos da transesterificação. ... 107
Reação 2. 1 - Reação Química de Transesterificação. ... 23
Reação 2. 2 - Mecanismo de Transesterificação de Óleos Vegetais. ... 24
Reação 2. 3 - Mecanismo de reação de transesterificação alcalina. ... 25
Reação 2. 4 - Reação Química da Esterificação. ... 27
ABNT Associação Brasileira de Normas Técnicas
ANP Agência Nacional do Petróleo, Gás Natural e Biocombustíveis ASTM American Society for Testing and Materials
BASF Badische Anilin und Soda-Fabrik CEN Comité Européen de Normalisation CFPP Cold-Filter Plugging Point
CNPE Conselho Nacional de Política Energética CSTR Continuous Stirred-Tank Reactor
DOU Diário Oficial da União EO Polioxietileno
ICI Imperial Chemical Industries
ISO International Organization for Standardization MDA Ministério do Desenvolvimento Agrário MMA Ministério do Meio Ambiente
MME Ministério de Minas e Energia PEO poli(óxido de etileno
PF Ponto de Fuidez PN ponto de Névoa
PNPB Programa Nacional de Produção e Uso do Biodiesel PPO poli(óxido de propileno)
RANP Resolução ANP
CAPÍTULO 1
Gicélia Rodrigues, Agosto/2014 2
1. Introdução
A extração de petróleo está se tornando cada vez mais difícil e com preços elevados. Este fato se deve a uma demanda crescente de combustíveis pelo mercado consumidor, ao processo natural de esgotamento dos reservatórios, que contém petróleos cada vez mais pesa-dos e com alto teor de impurezas, o que encarece os processos de refino físico e químico e também as ações preventivas a nível ambiental.
Atualmente, o Brasil conta com grande potencial e boas perspectivas futuras para a manutenção e ampliação de sua matriz energética. São exemplos de alternativas para o futuro, os petróleos oriundos do pré-sal, energia eólica, hidrelétricas, nuclear, além dos biocombustí-veis. O estímulo à produção e ao consumo de bicombustível favorece mundialmente a política de preservação ao meio ambiente, contribuindo na redução dos gases poluentes, causadores do aquecimento global e redução das alterações climáticas. O nordeste apresenta uma grande diversificação em termos de matérias-primas para produção de biocombustíveis. Entre as al-ternativas tem-se o óleo de coco para produção de biodiesel. O coqueiro Cocos nucifera L é uma das árvores mais importante do mundo e seu fruto contêm um elevado teor de óleo no albúmem sólido. Analisando o cenário, o cultivo esta árvore gera emprego e renda para toda a região com viabilidade técnico-ambiental. O incentivo a implementação das culturas olea-ginosas pela agricultura familiar, visando a produção de biodiesel e, também a sustentabilida-de financeira dos produtores, assegura preços mínimos competitivos para a produção( (MDA, 2010).
Os biocombustíveis têm atraído atenção considerável principalmente por causa dos al-tos preços do petróleo, preocupações com a segurança nacional, e consequências da mudança climática. Além da produção comercial de biodiesel e etanol, pesquisas estão cada vez mais focadas no desenvolvimento de processos de produção de outros combustíveis líquidos a par-tir da biomassa. O biodiesel é um combustível biodegradável derivado de fontes renováveis que pode ser obtido por diferentes processos tais como a pirólise, a esterificação ou a transes-terificação, este biocombustível pode ser usado em substituição ao óleo diesel sem qualquer modificação nos motores. Atualmente, estão sendo desenvolvidas pesquisas que contribuam na melhoria das suas rotas de produção. A presença de catalisadores heterogêneos nesses pro-cessos desempenha um importante papel na melhoria da rotas de produção, tais como taxa de reação e rendimento.
Gicélia Rodrigues, Julho/2014 3
um planejamento fatorial 23 visto que, é de fundamental importância conhecer as interações que essas variáveis exercem na síntese do material, contribuindo para minimização dos erros experimentais e otimização das condições de síntese. Sem o uso do planejamento estatístico as importantes interações entres os parâmetros não são muito bem detectadas e a otimização da síntese do AlSBA-15 pode levar mais tempo para alcançar uma área específica desejada. Este estudo é importante quando o objetivo é a síntese do AlSBA-15 de área específicas seletiva para determinados reagentes em uma reação química, como por exemplo a reação de transesterificação para produção de biodiesel. Através do planejamento experimental é possível estimar as condições ótimas para obtenção deste material com um determinada área podendo representar uma economia significativa de tempo e custo de síntese.
CAPÍTULO 2
Gicélia Rodrigues, Julho/2014 5
2. Revisão Bibliográfica
2.1 - Combustíveis que mais contribuem na emissão de gases do efeito
estufa
O efeito estufa é um fenômeno natural e necessário para manter a vida no planeta, po-rém a emissão de grandes quantidades de gases que causam o aquecimento global e conse-quentemente, alterações climáticas tornou-se uma preocupação mundial. O Protocolo de Quioto é resultado direto de três décadas de conscientização ambiental e de uma agenda de negociações internacionais que resultaram em um compromisso formal dos países signatários em reduzir suas emissões dos chamados gases de efeito estufa.
Em 2011 foi lançado o 1° Inventário Nacional de Emissões Atmosféricas por Veículos Automotores Rodoviários, que estimou as emissões nacionais de poluentes atmosféricos e de gases de efeito estufa nesse segmento do transporte de cargas e passageiros. Este inventário traz dados oficiais sobre as emissões de 1980 a 2012, dos poluentes regulamentados pelo PROCONVE (Programa de Controle de Poluição do ar por Veículos Automotores), tais co-mo: monóxido de carbono (CO), óxidos de nitrogênio (NOx), hidrocarbonetos não-metano (NMHC), aldeídos (RCHO), material particulado (MP),além dos gases de efeito estufa, como: dióxido de carbono (CO2), metano (CH4) e óxido nitroso (N2O). Os resultados mostram que o
diesel emitiu maior teor de CO2 e NOx, enquanto que a gasolina emitiu maior teor de CO e
CH4. As Figuras 2.1 a 2.5 mostram, respectivamente, as quantidades emitidas dos CO2, NOx,
Gicélia Rodrigues, Julho/2014 6
Figura 2. 1 - Emissão de CO2 por tipo de combustível.
Fonte: (MMA, 2013)
Figura 2. 2 - Emissão de NOx por tipo de combustível.
Gicélia Rodrigues, Julho/2014 7
Figura 2. 3 - Emissão de CO por tipo de combustível.
Fonte: (MMA, 2013).
Figura 2. 4 - Emissões de N2O por tipo de combustível.
Gicélia Rodrigues, Julho/2014 8
Figura 2. 5 - Emissões de CH4 por tipo de combustível.
Fonte: (MMA, 2013).
Gicélia Rodrigues, Julho/2014 9
2.2 - Definições de biocombustíveis
Biocombustíveis são derivados de biomassa renovável que podem substituir, parcial ou totalmente, combustíveis derivados de petróleo e gás natural em motores a combustão ou em outro tipo de geração de energia. Os dois principais biocombustíveis líquidos usados no Brasil são o etanol, extraído de cana-de-açúcar e, em escala crescente, o biodiesel, que é pro-duzido a partir de óleos vegetais ou de gorduras animais sendo adicionado ao diesel de petró-leo em proporções variáveis (ANP, Decreto nº 5.448, 2005).
Biodiesel é o nome dado aos ésteres alquílicos de ácidos graxos, desde que atendam aos parâmetros de qualidade, derivado de fontes renováveis. É um combustível biodegradável que possui um desempenho muito próximo ao diesel do petróleo, podendo ser utilizado na substituição do diesel sem qualquer modificação nos motores (ANP, Decreto nº 5.448, 2005). O biodiesel pode ser obtido por meio de diferentes processos, tais como: a pirólise, a esterifi-cação ou a transesterifiesterifi-cação de biomassa. Este último, mais utilizado, consiste numa reação química de óleos vegetais ou de gorduras animais com um álcool de cadeia pequena (etanol ou metanol), utilizando um catalisador. Desse processo também se obtém a glicerina, empre-gada na fabricação de sabonetes, além de outros cosméticos e fármacos.
2.3 - Históricos dos Bicombustíveis
Cerca de 45% da energia e 18% dos combustíveis consumidos no Brasil são renová-veis. Em outros países, 86% da energia vêm de fontes energéticas não-renovárenová-veis. Pioneiro mundial no uso de biocombustíveis, o Brasil alcançou uma posição almejada por muitos paí-ses que buscam fontes renováveis de energia como alternativas estratégicas a substituição do petróleo ( ANP, 2012).
Visando atender as exigências ambientais, investimentos em pesquisas atuam no sen-tido de reduzir as emissões de gases poluentes. A introdução de um combustível mais limpo dentro da matriz energética vem sendo pesquisada e já é conhecida desde o início do século passado, principalmente na Europa. Segundo registros históricos, Rudolf Diesel desenvolveu o motor diesel, em 1895, tendo levado sua invenção à mostra mundial em Paris, em 1900,
usando óleo de amendoim como combustível. Em 1911, teria afirmado que “o motor diesel
Gicélia Rodrigues, Julho/2014 10
Nessa época, os óleos vegetais apresentavam dificuldades quanto à sua combustão, problema atribuído à sua elevada viscosidade, que impedia uma adequada injeção nos moto-res. O combustível de origem vegetal deixava depósitos de carbono nos cilindros e nos injeto-res, requerendo uma manutenção intensiva. Os trabalhos desenvolvidos para resolver esses problemas conduziram à descoberta da transesterificação, que é a quebra da molécula do óleo, com a separação da glicerina e a recombinação dos ácidos graxos com álcool. Este tratamento permitiu superar as dificuldades com a combustão. Charles G. Chavanne patenteou o processo de produção de biodiesel por transesterificação em 1937 (Dabdoub & Bronzel, 2001).
Na década de 1930, o governo francês incentivava as experiências com o óleo de amendoim, visando conquistar a independência energética. Durante a II Guerra Mundial, o combustível de origem vegetal foi utilizado extensamente em vários países, incluindo a Chi-na, a Índia e a Bélgica. Em 1941 e 1942, havia uma linha de ônibus entre Bruxelas e Louvain, que utilizava combustível obtido a partir do óleo de palma (Knothe, 2001).
Nesse período, foram cortadas partes das linhas de abastecimento de combustíveis, o que causou uma grande escassez no mercado. Estimulando a busca de fontes alternativas de combustíveis baseadas em fontes vegetais, surgindo, na Bélgica, a ideia de transesterificar óleos vegetais com etanol para produzir um biocombustível conhecido hoje como biodiesel (Suarez & Meneghetti, 2007). Com o mesmo propósito, países como a França e os Estados Unidos desenvolveram pesquisas para a produção de bicombustíveis. Outro processo estudado foi o craqueamento ou pirólise convencional para a produção de um biocombustível conheci-do como bio-óleo que é uma mistura de compostos de diferentes classes químicas, similares aos encontrados no petróleo, sendo na sua maioria compostos oxigenados. Diferentemente da transesterificação, que possui relatos apenas de estudos em bancada e testes-piloto em moto-res, o craqueamento chegou a ser usado em larga escala, utilizando o óleo de tungue na China no período de guerra para a obtenção de combustível para substituir a gasolina e o diesel (Chang & Wan, 1947).
Gicélia Rodrigues, Julho/2014 11
ser o etanol hidratado, usado puro em motores adaptados para o combustível. Entre 1983 e 1988, mais de 90% dos automóveis vendidos no país eram movidos a etanol. Quando os pre-ços do petróleo começaram a cair, no fim da década de 80, a produção do etanol hidratado declinou. Ao fim da década de 90, apenas cerca de 1% dos carros vendidos tinham motores a etanol (ANP, 2012). No mesmo ano, o governo criou, mas não implementou, o Pro-óleo (Pla-no de Produção de Óleos Vegetais para Fins Energéticos ) transformando-o em programa (Pla-no ano de 1983, quando dá início ao Programa Nacional de Óleos Vegetais para Produção de Energia, também chamado de Pro-óleo (Suarez & Meneghetti, 2007).
Em 2003, tiveram início os primeiros estudos concretos para a criação de uma política do biodiesel no Brasil e, em dezembro de 2004, o governo lançou o Programa Nacional de Produção e Uso do Biodiesel (PNPB). O objetivo, na etapa inicial, foi introduzir o biodiesel na matriz energética brasileira, com enfoque na inclusão social e no desenvolvimento regio-nal. O principal resultado dessa primeira fase foi a definição de um arcabouço legal e regula-tório, com a edição de duas leis e diversos atos normativos (MME, 2012).
No Brasil, a Lei 11.097/05 instituiu a obrigatoriedade da adição de 2% de biodiesel ao diesel (mistura B2) a partir de janeiro de 2008 e tornam obrigatórias as misturas de 3% até 2013.
A partir de 1º de janeiro de 2010, o óleo diesel comercializado em todo o Brasil con-tém 5% de biodiesel. Esta regra foi estabelecida pela Resolução nº 6/2009 do Conselho Naci-onal de Política Energética (CNPE), publicada no Diário Oficial da União (DOU) em 26 de outubro de 2009, que aumentou de 4% para 5% o percentual obrigatório de mistura de biodi-esel ao óleo dibiodi-esel. A contínua elevação do percentual de adição de biodibiodi-esel ao dibiodi-esel de-monstra o sucesso do Programa Nacional de Produção e Uso do Biodiesel, lançado em 2004, e da experiência acumulada pelo Brasil na produção e no uso em larga escala de biocombustí-veis.
O Brasil está entre os maiores produtores e consumidores de biodiesel do mundo, com uma produção anual, em 2010, de 2,4 bilhões de litros e uma capacidade instalada, no mesmo ano, para cerca de 5,8 bilhões de litros.
Gicélia Rodrigues, Julho/2014 12
ser misturado com o diesel mineral, são estabelecidas pela Agência Nacional do Petróleo, Gás Natural e Biocombustíveis (ANP), através da Resolução nº 07 de 2008 (RANP 07/08) que substituiu a Resolução nº 42 de 2004, tornando os critérios de avaliação da qualidade do bio-diesel brasileiros mais restritivos. As determinações das características do biobio-diesel são feitas mediante o emprego das normas da Associação Brasileira de Normas Técnicas (ABNT), das normas internacionais "American Society for Testing and Materials" (ASTM), da "Internatio-nal Organization for Standardization" (ISO) e do "Comité Européen de Normalisation" (CEN). A Figura 2.6 mostra a evolução dos biocombustíveis no Brasil.
A evolução dos biocombustíveis no Brasil
Figura 2. 6 - Evolução dos biocombustíveis no Brasil.
Gicélia Rodrigues, Julho/2014 13 Matéria- prima para
Biocombustíveis
Biomassa
Lignocelulósicas Oleaginosas
Óleo derivado de algas Óleo não
comestíveis
Resíduos agrícolas
Biomassa aquática Culturas
energéticas
Resíduos florestais Bio óleo
2.4 - Matérias Primas para Produção de Biodiesel
A produção de combustível a partir dessa matéria-prima, com baixo valor de mercado e com sustentabilidade, apresenta-se como uma alternativa atraente e viável. Elas podem ser divididas em quatro categorias, dependendo da fonte da biomassa. As matérias - primas da biomassa oleaginosas que são obtidas a partir de: óleos comestíveis e não – comestíveis; óleos derivados de algas e óleo residual. Matérias - primas da biomassa lignocelulósica, tais como: resíduos (agrícolas e agroindustriais), biomassa aquática (algas, erva daninha), culturas ener-géticas (culturas de amido, oriundo do milho, trigo e cevada, culturas de açúcar) e resíduos florestais (madeira, resíduos de madeireiras). A Figura 2.7 mostra o cenário das matérias-primas para produção de biocombustíveis.
Figura 2. 7 - Cenário das matérias-primas para produção de biocombustíveis.
Gicélia Rodrigues, Julho/2014 14
O estudo da viabilidade da matéria prima é de fundamental importância para a implan-tação de projetos de ampliação de escala piloto, incluindo a realização de testes de longa du-ração em motores de ciclo diesel. E a condução de estudos agronômicos mais aprofundados que venham a garantir sua disponibilidade nos períodos de maior demanda. A Tabela 2 1 mostra o percentual das matérias-primas utilizadas para produção de biodiesel por região em abril de 2014.
Tabela 2. 1 - Percentual das matérias-primas utilizadas para produção de biodiesel por região em abril de 2014. Região
Matéria-Prima Norte Nordeste Centro-Oeste Sudeste Sul
Óleo de Soja 49,06% 57,40% 89,62% 37,16% 77,48%
Gordura Bovina 10,35% 25,56% 8,73% 61,42% 19,26%
Óleo de Algodão 10,70% 0,30% 0,55% NC
Outros Materiais Graxos 40,59% 6,16% 0,46% 0,65% 0,26%
Óleo de Fritura usado NC NC 0,90% 0,23% 0,38%
Gordura de Porco NC NC NC NC 2,03%
Gordura de Frango NC NC NC NC 0,59%
Óleo de Palma / Dendê NC 0,17% NC NC NC
*NC – Não contabilizado.
Fonte: Boletim mensal do biodiesel, ANP, maio 2014.
Segundo o Ministério do Desenvolvimento Agrário (MDA), a diversificação das maté-rias- primas para produção de biodiesel é de interesse do governo federal. A diversificação das matérias-primas é importante porque reduzirá o custo final do biodiesel, que é bastante influenciado pelo mercado internacional da soja. A Tabela 2.1 mostra que o uso do óleo de soja como matéria-prima para a produção de biodiesel ainda é predominante, no nordeste, centro-oeste e sul. Esse panorama pode mudar, com o incentivo do uso de outras matérias-primas bastante promissoras, como óleo de coco que é a matéria-prima de estudo neste traba-lho. O coqueiro Cocos nucifera L é uma das árvores mais importante do mundo, pois sua
Gicélia Rodrigues, Julho/2014 15
consumidos in natura ou industrializados na forma de mais de 100 produtos e subprodutos de interesse econômico (ARAGÃO et al., 1993).
O Brasil é o único país produtor onde o coco é tratado como uma fruta e não como uma oleaginosa. Durante a década de 70, no Brasil, houve um forte incentivo governamental para a implantação de unidades industriais para processamento de sua polpa (coco ralado, leite e óleo). Essas empresas foram implantadas com sucesso e passaram a gerar emprego e renda para as áreas onde eram instaladas e postas em funcionamento. Nessa fase todas as em-presas foram implantadas na Região Nordeste, onde a cultura do coqueiro já estava bem di-fundida (Abreu, 2003).
O Brasil, apesar de figurar entre os 10 maiores produtores mundiais de coco, não apa-rece na lista dos maiores produtores de óleo. Isto se deve ao fato de destinar a quase totalidade da sua produção para o consumo in natura do fruto, para as agroindústrias de água de coco e de albúmen sólido (polpa) (Agrianual, 2010). O fruto do coqueiro Cocos nucifera L, apresenta
um elevado teor de óleo no albúmen sólido do fruto, é uma característica bastante explorada pelos principais países produtores de coco. A Figura 2.8 mostra o albúmen do coco.
Figura 2. 8 - Albúmen do coco.
Gicélia Rodrigues, Julho/2014 16
2.4.1 - Extração do óleo de coco
A extração do óleo de coco pode ser realizada por métodos tradicionais ou utilizando diferentes forças como pressão, calor e movimento, para separar o óleo da polpa branca (al-búmen sólido) da fruta ( Peterson, 2014). Dependendo do método de extração utilizado, o óleo extraído pode ser completamente puro ou precisar de um processo de refinamento adicional.
Métodos de extração do óleo de coco
Processamento aquoso - Este método consiste na utilização de água para extrair óleo de coco. Primeiramente separa-se a polpa da casca da fruta, em seguida a polpa é fervida em água e durante o cozimento e amolecimento da mesma, o óleo sai da polpa e fica separado da água, por fim o óleo é removido da super-fície e armazenado.
Prensa hidráulica – Neste método a polpa é pressionada por uma prensa hidráu-lica. A prensagem é feita utilizando um pistão pesado e um tubo de metal. O tubo de metal é capaz de filtrar o óleo, uma vez que a polpa da fruta é introdu-zida no tubo metálico, um macaco hidráulico é utilizado para forçar a prensa contra a polpa e fazer com que o óleo seja comprimido pelo tubo e coletado. Esse processo ajuda a preservar o estado natural do óleo de coco e não exige outros métodos de refinamento.
Gicélia Rodrigues, Julho/2014 17
Extração Ghani – É um método tradicional que utiliza um pilão gigante e um sistema de morteiro para esmagar a polpa da fruta. Atualmente, sistemas me-canizados de extração Ghani estão disponíveis, embora as prensas tradicionais de tração animal ainda sejam utilizadas. Ainda que o resultado desse processo seja o óleo de coco completamente puro, ele requer trabalho intenso e produz menos óleo que os outros métodos.
Método de expulsão - Esse método utiliza um tonel cilíndrico mecanizado para criar uma versão pulverizada da polpa do coco, conhecida como "bolo de co-co". A fruta aquecida é colocada dentro do tonel, onde é esmagada através da rotação de uma haste metálica. Esse processo ajuda a quebrar os componentes da polpa e prepará-la para a extração do óleo. O último passo consiste-se na utilização de um solvente químico, hexano, para separar o bolo de coco do óleo. A refinação é, geralmente, necessária para separar o extrato do óleo.
2.4.2 - Óleos e Gorduras
Os óleos e gorduras são substâncias insolúveis em água, obtidas de vegetais, animais e fontes marinhas. Seus principais componentes são os ácidos graxos esterificados com gliceri-nas, denominados de triglicerídeos. A diferença entre uma gordura e um óleo é arbitrária, as-sim são considerados gorduras os triglicerídeos sólidos à temperatura ambiente e óleos aque-les que são líquidos. Os óleos vegetais e gorduras animais que podem ser utilizados na produ-ção de biodiesel são classificados nos seguintes grupos:
a) Óleos vegetais convencionais: Girassol e colza (canola) largamente usados na Europa, Soja nos EUA, coco nas Filipinas e óleo de palma (dendê) na Indoné sia, Malásia, Colômbia.
b) Óleos vegetais alternativos: São espécies adaptadas às condições dos países, as quais são melhores posicionadas no domínio de energia, tais como o óleo de Camelia Sativa, Crambe abyssinica, Jatropba curcas.
Gicélia Rodrigues, Julho/2014 18
d) Óleos usados: Sebo de vaca, de porco e de frituras.
e) Óleos de outras fontes: Lipídios com composição semelhante as dos óleos vegetais, provenientes de algas e microalgas, bactérias e fungos.
Gicélia Rodrigues, Julho/2014 19
H
2C
H
2C
H
2C
O
O
O
O
O
O
H
2C
H
2C
H
2C
O
O
O
O
O
O
H
2C
H
2C
H
2C
O
O
O
O
O
O
Glicerol + 3 ácido graxosTriglicerídeo Saturado
Triglicerídeo monoinsaturado
Triglicerídeo Poli-insaturado
Figura 2. 9 - Estrutura química de um triglicerídeo.
Gicélia Rodrigues, Julho/2014 20
Ácido Caprílico (C8:0) Ácido Cáprico (C10:0) Ácido Láurico (C12:0) Ácido Mirístico (C14:0) Ácido Palmítico(C16:0) Ácido Esteárico (C18:0) Ácido Oléico (C18:1) Ácido Linoléico (C18:2)
3,44% 9,44% 2,23% 11,62% 19,94%
42,51%
4,68%6,13%
Composição em ácidos graxos presentes no óleo de coco in natura.
Atualmente, a maior parte dos óleos utilizados na produção de biodiesel possui ácidos graxos predominantemente insaturados o que torna esse combustível susceptível à oxidação, principalmente quando estocado por longos períodos. As substâncias geradas pela degradação oxidativa do biodiesel comprometem tanto a qualidade do combustível quanto o funciona-mento dos motores que o utilizam (Ferrari & Souza, 2009). A composição em ácidos graxos, em esteróis e em triacilglicerídeos são as principais análises utilizadas na determinação da identidade dos óleos. Para os óleos e gorduras refinados, as análises mais usuais são os índices de peróxido e de acidez, na avaliação da qualidade dos óleos.
As plantas como matéria-prima à base de óleo vegetal, como o óleo de coco, são maté-rias-primas comuns para produzir biocombustíveis, devido à presença de triglicérides.Os tri-glicerídeos são fáceis de converter em combustíveis líquidos para transporte em relação à bi-omassa, uma vez que, são líquidos de alta energia e contêm menos oxigênio.
Na composição do óleo de coco predominam os ácidos graxos saturados, cujos teores superam 90% do peso total dos ácidos graxos constituintes deste óleo (Tangsathitkulchai et al., 2004). Essa característica, pouco comum entre os óleos de origem vegetal, confere ao óleo
de coco elevada resistência à oxidação, o que torna o armazenamento do biodiesel menos complexo e representa um importante fator para adição desse óleo como matéria-prima para a produção de biodiesel. A Figura 2.10 mostra a composição em ácido graxo presente no óleo de coco.
Figura 2. 10 - Composição em ácido graxo presente no óleo de coco in natura.
Gicélia Rodrigues, Julho/2014 21
2.4.3 - Álcool
Gicélia Rodrigues, Julho/2014 22 ROTAS DE PRODUÇÃO DE
BIOCOMBUSTÍVEL
Craqueamento Catalítico
Pirólise da Biomassa
Fermentação Transesterificação Esterificação
Gasolina, Querosene, Diesel, Aromáticos Olefinas.
Bio-óleo Bio- álcool Biodiesel
2.5 - Métodos para produção de biocombustíveis
As rotas de produção de biodiesel podem ser por transesterificação, que é uma rota convencional, esterificação e pirólise. A Figura 2.11 mostra o fluxograma dos possíveis bi-combustíveis produzidos a partir de uma dada rota escolhida.
Figura 2. 11 - Fluxograma - Rotas de Produção de Bicombustíveis
Gicélia Rodrigues, Julho/2014 23 O O R3 O C R1 O C C O C R2 C O C Catalisador 3 R4 OH
O
O R4
R1
C
O
O R4
R2
C
O
O R4
R3 C + OH C H2 C C OH OH H
Triglicerídeo Ésteres de Ácidos Graxos Glicerol H2
H H2
H2
2.5.1 - Transesterificação
A transesterificação, também chamada alcoólise, pode ser descrita de maneira geral como sendo uma reação reversível em que um éster reage com um álcool, na presença de um catalisador, e através da troca da alcoxila, origina-se um novo éster e um novo álcool. É um processo similar ao da hidrólise, exceto o fato de que se trata de um álcool no lugar da água. Os alcoóis que podem ser utilizados são: o metanol, etanol, propanol, butanol, sendo que os mais utilizados são o metanol e etanol. Nos estudos publicados, o metanol tem sido o mais empregado devido ao seu custo reduzido e grande disponibilidade no mercado. O etanol pode também ser utilizado, visto que, no Brasil, existe grande disponibilidade deste produto a baixo custo (Geris et.al., 2007).
No processo de produção convencional, a transesterificação de óleo vegetal, um trigli-cerídeo reage com um álcool que pode ser o metanol ou etanol, na presença de um catalisador, produzindo uma mistura de ésteres de ácidos graxos e glicerol. Assim, ésteres etílicos ou me-tílicos de ácidos graxos (conhecidos por biodiesel) obtidos por alcoólise de óleos vegetais podem ser usados como combustíveis alternativos para os motores a diesel (Candeia, 2008). O processo de transesterificação é afetado por vários fatores, dependendo das condições de rea-ção utilizadas. Alguns dos fatores são: a fonte de óleo que determina a umidade de ácido gra-xo livre, o tipo de catalisador e de carga utilizados, razão molar de álcool e óleo, tipo de álco-ol, tempo e temperatura de reação, intensidade e efeitos de misturas de solventes. A Reação 2.1 mostra a reação Química de Transesterificação.
Reação 2. 1 - Reação Química de Transesterificação.
Gicélia Rodrigues, Julho/2014 24
Principais métodos catalíticos do processo de transesterificação:
a) Método de transesterificação catalítica ácida: Este método consiste na utilização de um catalisador ácido de Brønsted, industrialmente os ácidos mais usados são sulfônicos e sul-fúricos. O uso destes catalisadores produzem elevados rendimentos em alquil-ésteres, porém as reações são lentas. O processo de catálise ácida pode ser considerado como um pré -tratamento, no qual os ácidos graxos livres são convertidos em monoésteres. A razão malar e a quantidade de catalisador a ser utilizada na reação são calculadas de acordo com a quantida-de inicial quantida-de ácidos graxos livres presentes na matéria-prima. A principal quantida-desvantagem do processo de pré-tratamento é a formação de água. Quando os ácidos graxos livres reagem com o álcool, a água também é formada juntamente com os monoésteres, inibindo a conversão de ácidos graxos livres em ésteres. De uma forma geral as reações de transesterificação catalisa-das por ácidos são realizacatalisa-das com elevacatalisa-das razões molares de álcool/óleo, temperaturas e pressões de baixas a moderadas e com altas concentrações de catalisador (Lora & Venturini, 2012).
A Reação 2.2 mostra o mecanismo da reação de transesterificação de óleos vegetais. Cada etapa do processo é reversível, mas a presença de um excesso de álcool pode deslocar o ponto de equilíbrio para a complementação do processo. O passo inicial da etapa do processo de transesterificação dos óleos vegetais e a protonação do ácido para originar um íon oxônio (1). Esse íon passa por uma reação de troca com o álcool para gerar uma espécie intermediá-ria (3), que pode ser dissociado através de um estado de transição (4) produzindo o éster (5).
Reação 2. 2 - Mecanismo de Transesterificação de Óleos Vegetais.
Gicélia Rodrigues, Julho/2014 25
OH- + ROH RO- + H
2O
Etapa 1 :
R1 C O OR2
+ RO- R1 C
OR2 O
-OR
Etapa 2 :
OR2 R1 C
O
-OR + ROH R1 C
O
-OR R2OH+
+ RO
-R1 C O
-OR R2OH+
Etapa 3 :
R1 COOR + R2OH Pré-início
b) Método de transesterificação catalítica alcalina: Este processo consiste na utilização de um catalisador alcalino que podem ser metais alcalinos, alcóxidos e hidróxidos, bem como carbonatos de sódio e de potássio. Este processo apresenta um elevado rendimento na obten-ção de ésteres derivados de óleos vegetais com alta qualidade de combustíveis. No entanto, a reação de transesterificação alcalina apresenta uma desvantagem significativa, pois os ácidos graxos livres reagem com o catalisador alcalino produzindo sabão, dificultando a separação do biodiesel, da glicerina e da água de lavagem (água + álcool) (Lora & Venturini, 2012).
A Reação 2.3 mostra o mecanismo da reação de transesterificação alcalina. Assim como na reação catalítica ácida , a reação de transesterificação catalítica básica é reversível, mas a presença de um excesso de álcool pode deslocar o ponto de equilíbrio para a comple-mentação do processo. A primeira etapa, (1), ocorre o ataque do íon alcóxido do carbono da molécula do triglicerídeo, resultando na formação de um intermediário tetraédrico. A reação do intermediário com um álcool produz o íon alcóxido, etapa (2). Na última etapa(3) ocorre o rearranjo da espécie intermediária tetraédrica produzindo um diglicerídeo.
Reação 2. 3 - Mecanismo de reação de transesterificação alcalina.
Fonte: Elaboração própria.
Gicélia Rodrigues, Julho/2014 26
R2= CH2
CH OCO R
1
CH 2 OCO R1
R1 = Cadeia de carbono do ácido graxo
R = Grupo alquil do álcool
b) Método de transesterificação catalítica enzimática: Neste processo as enzimas mais utilizadas são lípases provenientes de bactérias e fungos. Os parâmetros ótimos para o uso destas enzimas específicas dependem da origem e da formação da lípase. Na catálise enzimá-tica o glicerol pode ser facilmente recuperado, sem a necessidade de um processo complexo, os ácidos graxos livres contidos no óleo podem ser completamente convertidos em ésteres e o tratamento da água residual não é necessário. No entanto, a principal desvantagem do proces-so catalisado por enzima é o alto custo das lípases usadas como catalisador.
2.5.2 - Esterificação
A reação de esterificação difere da transesterificação por partir de ácidos graxos livres, ao invés de triglicerídeos, o que a torna mais vantajosa devido à possibilidade do uso de resí-duos (borra ácida) e a não formação de glicerol. Apenas catalisadores ácidos podem ser utili-zados para a reação de esterificação, uma vez que o uso de catalisadores básicos levaria à neu-tralização dos mesmos pela acidez da matéria-prima, ocorrendo a saponificação (Gonzalez et al., 2008). Destaca-se ainda, que a catálise ácida heterogênea é preferencial, pois, além da
Gicélia Rodrigues, Julho/2014 27
O
OH
R
1C
+ HO R
2O
O
R
1C
R
2+
H
2O
Ácido carboxílico
+
Álcool
Éster
+ Água
Reação 2. 4 - Reação Química da Esterificação.Fonte: Elaboração própria.
Os produtos obtidos pela reação de esterificação, apesar de apresentarem propriedades muito próximas às do diesel convencional, não devem ser utilizados diretamente nos motores diesel, devido à sua elevada viscosidade. Para que não sejam necessárias adaptações nos mo-tores, têm sido utilizadas misturas do biodiesel com o diesel convencional, conhecidas como blendas (biodiesel/diesel fóssil) (Candeia, 2008).
2.5.3 - Pirólise
O processo de pirólise pode ser: convencional ou catalítico. O craqueamento catalítico tem a vantagem de obter produto de alta qualidade a partir de qualquer óleo cru. Este processo é favorável em comparação com a pirólise convencional, uma vez que, ele pode ocorrer em temperaturas muito mais baixas e a baixa pressão, tornando o processo economicamente viá-vel. No entanto, o coque gerado durante a reação é depositados nos sítios ativos dos catalisa-dores, levando-o à desativação (Ciola et al., 1981). Portanto, para recuperar a atividade do catalisador desativado é necessário que o mesmo passe por um processo de regeneração, a qual é realizada continuamente através de uma reação exotérmica, ou seja, pela queima do coque depositado nos sítios ativos do catalisador.
Gicélia Rodrigues, Julho/2014 28
Pesquisas estão sendo realizadas através doprocesso da pirólise de triglicerídeos que consiste na quebra das moléculas do óleo vegetais e da gordura animal, levando à formação de uma mistura de compostos químicos com propriedades muito semelhantes às do diesel de petróleo (Suarez, 2005). Essa reação é realizada a uma temperatura acima de 350°C, na pre-sença ou ausência de catalisadores obtendo uma mistura de hidrocarbonetos, compostos oxi-genados e água. É importante destacar que a quantidade de carbono contido na matéria-prima é um fator importante para a determinação do tamanho e do grau de insaturação dos produtos orgânicos obtidos.
A pirólise de óleos vegetais foi usada para o fornecimento de combustíveis durante a Segunda Guerra Mundial. Desde então, numerosos estudos vêm sendo desenvolvidos sobre os principais parâmetros que determinam a qualidade e o rendimento do produto pirolisado (Morcelin & Assis, 2007). A definição de parâmetros como: tempo de residência, taxa de aquecimento, pressão, temperatura e o produto desejado são essenciais na determinação do tipo de processo de pirólise a ser realizado.
As reações de pirólise referem-se à ruptura da ligação carbono-carbono dos hidrocar-bonetos, que são termodinamicamente favorecidas a altas temperaturas por serem um proces-so endotérmico. As reações de pirólise catalítica de óleos vegetais são feitas com catalisadores ácidos e, portanto, podem ser definidas como uma reação de baixa especificidade, o que signi-fica que existe uma série enorme de reações secundária, tais como a isomerização, transferên-cia de hidrogênio, alquilação de aromáticos, ciclização etc. Os produtos que se obtêm são hi-drocarbonetos de menor massa molar do que os de partida; daí o emprego industrial na trans-formação de óleo pesado em gasolina. Por outro lado, a trans-formação de compostos de alta massa molar, chamados geralmente de coque, ocorre em pequenas quantidades que permanecem sobre a superfície do catalisador, desativando-o(Ciola, 1981).
2.5.4 - Obtenção dos parâmetros cinéticos dos ensaios da pirólise
Gicélia Rodrigues, Julho/2014 29
qualquer uma desses fatores tornaria os cálculos dos parâmetros cinéticos e previsão dos me-canismos de reação inválidos (Lu et al., 2009). Dentre os parâmetros cinéticos, a energia de
ativação (Ea) é um parâmetro importante para se avaliar o comportamento térmico de um
bi-combustível e a influência do catalisador na decomposição térmica.
Antes de determinar os parâmetros cinéticos é necessário compreender a cinética das
rea-ções catalíticas heterogêneas a qual está descrita da seguinte forma: para que um reagente ga-soso possa ser convertido cataliticamente em produtos, torna-se necessário que o mesmo seja
transferido da fase gasosa para a superfície do catalisador, onde é adsorvido e reage formando um produto. Este, por sua vez, deve ser desorvido e transferido para a fase gasosa. A partir desse contexto, considerando um catalisador poroso, o processo catalítico ocorre basicamente da seguinte forma: Primeiramente, o reagente difunde tanto na superfície como no interior dos poros do catalisador, após a difusão os reagentes são adsorvidos nos centros ativos e a reação ocorrerá na superfície entre a espécie adsorvida. Os produtos formados sofrerão o processo de desorção e, em seguida, são transferidos por difusão tanto para o exterior da partícula como para a fase gasosa (Figueiredo & Ribeiro, 1989). O entendimento das etapas do processo ciné-ticos das reações catalíticas heterogêneas é de fundamental importância para a aplicação do modelo cinético.
De acordo com as equações não-isotérmicas, os modelos matemáticos utilizados para a obtenção dos parâmetros termodinâmicos são usualmente baseados na Equação (2.1) Partin-do-se desta equação e aplicando as condições necessárias, obteve-se a equação dinâmica não-isotérmica apropriada para estudar os parâmetros cinéticos.
(2.1)
Onde é a grau de conversão (%), K é a constante de velocidade (sP -1
P); e f(α) a expressão da
equação da taxa de reação expressa em termos da conversão α.
(2.2)
A Equação (2.2) é a Equação de Arrhenius, onde K0 é o fator pré-exponencial (s-1), Ea
Gicélia Rodrigues, Julho/2014 30
1
( )
α
=
0
−
�
Considerando a cinética não-isotérmica dα/dT deve ser medido em diferentes temper a-turas, contudo, a maior parte das reações acontecem com absorção ou liberação de calor;o que afeta a temperatura do sistema. Esta é uma das razões pelas quais se mostra mais conveniente trabalhar em condições não- isotérmicas controladas. Sabe-se que a razão da taxa de
aqueci-mento β (°C s-1) é dada através da Equação (2.3 ).
(2.3)
Dividindo-se a Equação (2.1 ) pela taxa de aquecimento Equação (2.3), obtém a Equa-ção (2.4).
(2.4)
A Equação (2.4) representa o comportamento cinético do sistema não-isotérmico. Substituindo-se a Equação (2.2) na Equação (2.4) e rearranjando-se, acha-se uma nova Equação (2.5).
(2.5)
Integrando-se a Equação (2.5) temos a Equação (2.6)para β constante.
(2.6)
Gicélia Rodrigues, Julho/2014 31
(2.7)
Substituindo-se os valores da temperatura, e aplicando-se o logaritmo, obtém-se a Equação (2.8).
(2.8)
A Equação (2.8 ) é denominada de equação dinâmicae pode ser usada para estudar a influência da temperatura e do tempo na degradação térmica de óleos vegetais. Uma das grandes vantagem desse modelo é que, para cada conversão de óleo (α), ln(β/Tα2 ) é
representado graficamente contra 1/ Tα, dando uma reta cuja inclinação corresponde (– Ea/R).
Assim, pode-se calcular a energia de ativação pelo coeficiente angular, isolando a função g(α)
Gicélia Rodrigues, Julho/2014 32
A Reação 2.5 mostra a pirólise de triglicerídeos, levando a formação de ácidos carbo-xílicos, cetenos, acroleína e hidrocarbonetos com ou sem insaturações terminais.
Reação 2. 5 - Pirólise de triglicerídeos (1), levando a formação de ácidos carboxílicos (2), cetenos (3), acroleína (4) e hidrocarbonetos com (5) ou sem insaturações terminais (6).
Fonte: (Suarez et al., 2007).
As reações de pirólise são reações complexas, então métodos cinéticos tradicionais como por exemplos, reações de primeira e segunda ordem não são normalmente aplicáveis. Portanto, uma variedade de modelos matemáticos foi desenvolvida para caracterizar o com-portamento cinético das reações complexas (Leiva et al., 2006).
O bio-óleo produzido na reação de pirólise tem um rendimento energético em torno de 70%. No entanto, as propriedades indesejáveis do bio-óleo são resultantes da sua composição química, que consiste principalmente de diferentes classes de compostos oxigenados. A eli-minação de oxigênio é, portanto necessário para transformar o bio-óleo em um combustível que seja economicamente atraente (French & Czernik, 2010).
Gicélia Rodrigues, Julho/2014 33
espectrometria de massa, eles observaram que os espectros de pirólise catalítica são muito diferentes dos não catalíticos demonstrando que a presença de um catalisador específico me-lhora o rendimento do produto da reação.
Lu et al., (2009) utilizaram em seu trabalho três métodos cinéticos, o modelo de
Co-ats-Redfern, o modelo de Friedman, e a regressão não-linear. O modelo de Coats-Redfern foi utilizado para analisar o comportamento cinético da pirólise catalítica da biomassa compro-vando que a reação de pirólise envolve varias etapas, ao invés de uma reação simples de pri-meira ordem. Através do modelo de Friedman, foi possível observar, segundo Lu e colabora-dores (2009), que quando os índices estão abaixo da conversão de 50%, ou seja, a temperatura a baixo de 350ºC, a energia de ativação mantém-se relativamente estável, porém quando a taxa de conversão e superior a 50% ocorre um aumento de erros de cálculos, originando valo-res irrelevantes de energias de ativação. Assim, o uso geral dos cálculos de Friedman descreve os tipos de reação de partida e dos correspondentes parâmetros cinéticos iniciais necessários para permitir a iteração dos cálculos adicionais para todo o processo. As análises de regressão não-linear mostram que a pirólise de biomassa pode ser descrita cineticamente por três rea-ções sucessivas.
Gicélia Rodrigues, Julho/2014 34
2.6 - Principais propriedades físico-química do biodiesel
As propriedades do biodiesel dependem do processo de produção, e da natureza da matéria-prima, a qual confere ao biodiesel, características especiais como combustíveis.
2.6.1 - Densidade
A densidade do biodiesel situa-se na faixa de 826 a 860 kg/m3 e está relacionada com a estrutura molecular das suas moléculas. Quanto maior o comprimento da cadeia carbônica do alquiléster, maior será a densidade, no entanto, este valor decrescerá quanto maior o núme-ro de insaturações presentes na molécula (Lôbo et al., 2009). O aumento da densidade,
contri-bui para uma maior diâmetro da gota do combustível e uma maior inércia, ocasionando uma penetração bastante elevada dessas gotas na câmara de combustão. Quando um combustível com menor densidade e viscosidade é injetado, a atomização é melhorada e pode ser alcança-da uma melhor formação alcança-da mistura (Lora & Venturini, 2012). A presença de impurezas tam-bém poderá influenciar na densidade do biodiesel como, por exemplo, o álcool ou substâncias adulterantes. Comparado com o diesel mineral, o biodiesel apresenta maior densidade. Dentre os padrões de qualidade apresentados, a norma ASTM (American Society for Testing and Materials) não considera relevante a densidade do biodiesel como parâmetro de qualidade. Tanto para a resolução brasileira, como para a norma européia, os métodos de análise da den-sidade do biodiesel são os mesmos comumente aplicados aos derivados de petróleo. A resolu-ção brasileira estabelece ainda que o biodiesel produzido tenha um prazo máximo de um mês, a contar da data de certificação, para ser comercializado. Passado este prazo, deve ser realiza-da uma nova análise realiza-da massa específica a 20 ºC, caso haja diferença inferior a 3,0 kg/m3 em relação ao valor do certificado, é necessário fazer uma nova análise das seguintes proprieda-des físico-química: teor de água, índice de acidez e a estabilidade à oxidação a 110 ºC (Lôbo
et al., 2009).
2.6.2 - Viscosidade Cinemática a 40 °C
Gicélia Rodrigues, Julho/2014 35
Os óleos vegetais puros não podem substituir o diesel, uma vez que, esses óleos apre-sentam alta viscosidade (Lora & Venturini, 2012). A viscosidade do biodiesel aumenta com o comprimento da cadeia carbônica e com o grau de saturação e tem influência no processo de queima na câmara de combustão do motor. É importante ressaltar que o número de insatura-ções não tem apenas efeito nos valores de densidade e de viscosidade dos biodieseis, mas também é de grande importância na sua estabilidade oxidativa. Alta viscosidade ocasiona he-terogeneidade na combustão do biodiesel, devido à diminuição da eficiência de atomização na câmara de combustão, ocasionando a deposição de resíduos nas partes internas do motor. Os sabões residuais, bem como os glicerídeos não reagidos (mono-, di- e triglicerídeos) e os pro-dutos da degradação oxidativa do biodiesel, aumentam a viscosidade do biodiesel. Estes con-taminantes podem, portanto, ser monitorados indiretamente através da determinação da visco-sidade cinemática a 40 ºC ( Lôbo et al., 2009).
2.6.3 - Número de Cetanos
A facilidade de um combustível entrar em ignição por compressão é expressa pelo número de cetano. Um número de cetano elevado facilita a inflamação do combustível quan-do injetaquan-do no motor (Lora & Venturini, 2012). Assim como a octanagem, o número de ceta-nos é indicativo do tempo de atraso na ignição de combustíveis para motores do ciclo diesel. Quanto maior o número de cetanos mais curto será o tempo de ignição. O número de cetanos aumenta com o comprimento da cadeia carbônica não ramificada, desta forma, o hexadecano (cetano) é estabelecido como padrão de valor de 100 na escala de cetano, enquanto que para o 2, 2, 4, 4, 6, 8,8-heptametilnonano são atribuídos o valor 15. O teste de cetano é realizado em um motor de bancada de quatro tempos, com um único cilindro e ignição por compressão, projetado para testes de amostras de combustíveis para motor diesel. Comparado com o diesel fóssil, o biodiesel apresenta maiores valores de número de cetanos ( Lôbo et al., 2009).
2.6.4 - Comportamento à baixa temperatura