REVISTA
BRASILEIRA
DE
ANESTESIOLOGIA
PublicaciónOficialdelaSociedadeBrasileiradeAnestesiologiawww.sba.com.br
ARTÍCULO
CIENTÍFICO
Efecto
hiperalgésico
de
la
fentolamina
por
vía
subaracnoidea
en
ratones
夽
Desiré
Carlos
Callegari
a,
João
Antônio
Correa
a,
Oscar
César
Pires
b,∗,
Renan
Batista
Corrêa
Braga
c,
Ana
Flávia
Marques
Gimbo
d,
Adriana
Aparecida
de
Souza
e,
Marta
Helena
Rovani
Pires
f,
Elton
Constantino
be
Irimar
de
Paula
Posso
baFacultaddeMedicinadelABC(FMABC),SantoAndré,SP,Brasil
bUniversidaddeTaubaté(Unitau),Taubaté,SP,Brasil
cCursodeMedicina,UniversidaddeTaubaté(Unitau),Taubaté,SP,Brasil
dCursodeEnfermería,UniversidaddeTaubaté(Unitau),Taubaté,SP,Brasil
eCursodeBiología,UniversidaddeTaubaté(Unitau),Taubaté,SP,Brasil
fCursodeMedicina,FacultaddeMedicinadePetrópolis,Petrópolis,RJ,Brasil
Recibidoel12deagostode2013;aceptadoel12deseptiembrede2013 DisponibleenInternetel13deenerode2015
PALABRASCLAVE
Ratones; Fentolamina; Dolor;
Testdelaformalina; VonFrey
Resumen
Justificaciónyobjetivos: Elfenómenodoloroso es unade lasmás importantes ycomplejas experiencias.Lafentolaminaesunantagonistaalfaadrenérgiconoselectivo.Elobjetivofue compararlosefectosdedosiscrecientesdefentolaminaporvíasubaracnoideaenlamodulación delfenómenodolorosoenratones.
Método: Fueronusados84ratonesWistarmachos,divididosenlosgruposformalinaeincisión plantar,subdivididosen6subgrupos(n=7).Enelsubgrupocontrol(GC)solamenteseadministró soluciónsalina(10L);enlossubgruposactivos,10gdefentolamina(GF10),20g(GF20),
30g(GF30),40g(GF40)y50g(GF50).Enelgrupoformalina,eldolorfueinducidoconuna
inyecciónde50Ldeformalinaal2%enlaregióndorsaldelapataposteriorderecha.Enel
grupoincisiónplantar,eldolorseindujoporincisiónplantaryevaluaciónporlosfilamentosde VonFrey.Lainducciónyelmantenimientoanestésicosellevóacaboconhalotanoal3%para laintroduccióndecatéterenelespaciosubaracnoideoylarealizacióndelaincisiónplantar.El análisisestadísticodelosresultadossehizomedianteelprogramaJMP®delSASconunnivel designificacióndel5%.
Resultados: Lafentolaminaenlasdosisde20y30gprodujounaumentodelarespuestade
dolorenlafaseintermediadeltestdelaformalina.Eneltestdelaincisiónplantar,generó unefectohiperalgésicoenelprimero,tercero,quintoyséptimodíascondosisde10g;enel
primero,terceroyquintodíascondosisde20g;yenelquintodíacondosisde30g.
夽 TrabajodesarrolladoenlaFacultaddeMedicinadelABC,SantoAndré,SP,Brasil.
∗Autorparacorrespondencia.
Correoelectrónico:[email protected](O.C.Pires). http://dx.doi.org/10.1016/j.bjanes.2014.12.002
Conclusión:Lafentolaminaporvíasubaracnoideageneróunefectohiperalgésicoposiblemente porlaparticipacióndediferentessubclasesdereceptoresalfaadrenérgicosenlasvías modula-dorasdeldolor.
©2014SociedadeBrasileiradeAnestesiologia.PublicadoporElsevierEditoraLtda.Todoslos derechosreservados.
KEYWORDS
Mice;
Phentolamine; Pain;
Formalintest; VonFrey
Hyperalgesiceffectofsubarachnoidadministrationofphentolamineinmice
Abstract
Backgroundandobjectives: Painfulphenomenon isone ofthemost importantandcomplex experiences.Phentolamineis anon-selectivealpha-adrenergic antagonist. Theobjectiveof thisstudywastocomparetheeffectofincreasingdosesofphentolamineintosubarachnoid spaceinratsinthemodulationofpainfulphenomenon.
Methods:EightyfourmaleWistarratsweredividedintoformalinandplantarincisiongroups, subdividedintosixsubgroups (n=7).Controlgroup (CG)receivedonlysaline(10L);active
subgroupsreceivedphentolamine10g(GF10),20g(GF20),30g(GF30),40g(GF40),and
50g(GF50).Informalingroup,painwasinducedbyinjectionof50Lof2%formalinindorsal
regionofrightposteriorpaw.Inplantarincisiongroup,painwasinducedbyplantarincision andevaluatedusingVonFreyfilaments.Inductionandmaintenanceofanesthesiawere perfor-medwith3%halothaneforcatheterplacementintosubarachnoidspaceandplantarincision. StatisticalanalysiswasperformedusingtheJMP®programfromSASwith5%significancelevel.
Results:Phentolamineatdosesof20and30gincreasedthealgesicresponseinthe
interme-diatephaseoftheformalintest.Inplantarincisiontest,ithadhyperalgiceffectonfirst,third, fifth,andseventhdaysatadoseof10gandonfirst,third,andfifthdaysatadoseof20g
andonfifthdayatadoseof30g.
Conclusion:Subarachnoidadministrationofphentolamineshowedhyperalgesiceffect,possibly duetotheinvolvementofdifferentsubclassesofalpha-adrenergicreceptorsinmodulatingpain pathways.
©2014SociedadeBrasileiradeAnestesiologia.PublishedbyElsevier EditoraLtda.Allrights reserved.
Introducción
Elpasodeinformacionesnociceptivasporelcuerno poste-riordelamédulaespinalendirecciónanivelesrostralesdel sistemanerviosocentralsufreprofundasinfluencias excita-toriase inhibitorias.Laelucidacióndela farmacologíade esos sistemas moduladores ha orientado la apreciación delahabilidaddereceptoresespecíficos1.
Losneurotransmisores,aminoácidosyneuropéptidosson liberadosporlosterminales delosaferentes primariosen el cuerno posterior de la médula espinal, donde actúan enlamodulacióndelatransmisiónnociceptiva.Entreotros sedestacanlosaminoácidosexcitatoriosglutamatoy aspar-tato,losneurotransmisoresyneuropéptidos,incluyendolas taquicininassustanciaP,neurocininaA,neurocininaB, pép-tido gen relacionado con la calcitonina, colecistocinina, somatostatina, óxido nítrico, prostaglandinas, galanina, encefalinasyendorfinas2.
La fentolamina, antagonista alfaadrenérgico competi-tivo que pertenece al grupo imidazolina, no selectivo, con eficacia similar sobre los receptores alfa1 y alfa 2, puede también bloquear receptores 5-HT y canales de potasio y causar la liberación de histamina por los mastocitos3.
Estainvestigaciónevaluólosefectosdedosiscrecientes defentolamina,administradasporvíasubaracnoidea,sobre eldolorinducidoenratonesusandoeltestdelaformalina modificado ydeltest dela incisiónplantar, paraverificar si la involucración de las vías adrenérgicas en el sistema inhibitoriodescendientedeldoloresdosis dependientede lafentolamina.
Método
Los procedimientos experimentalesrespetaron las normas éticasdelaInternationalAssociationfortheStudyofPain (IASP), que regula los experimentos hechos en animales (CommiteeforResearchandEthicalIssuesoftheIASP,1983) yelproyectofueaprobadoporelComitédeÉticaenelUso deAnimalesCeua/Unitau,coneln.o019/11.Fueronusados 84ratonesWistarmachos,conpesoentre220y300g,que fueroncolocadosindividualmenteenunacámaradevidrio transparentede15×25×15cm,conunorificioenlaparte
seleretirabayseleponíaendecúbitodorsalhorizontalcon elabdomensobreuncilindroplástico,conelhocicoenuna mascarilla,pordondecontinuabarecibiendoelhalotanoen lamismaconcentración.
Acontinuaciónseintroducíauncatéterdepolietileno(PE 10),enelespaciosubaracnoideoensentidocaudal,por pun-ciónconaguja22GdeTuohyenlalíneamediadelespacio intervertebralporencimadelapenúltimavértebralumbar, hastaelespaciosubaracnoideo,queeraidentificadoporel movimientoreflejodelacolao deunadelaspatas trase-ras.Elcatétersefijabaeneltejidosubcutáneoylapielse suturabaconunhilodenilón4-0yalfinaldelexperimento, después delsacrificio del animal con tiopental sódico, se seccionabalacolumnalumbarparaconfirmarlapresencia delcatéterenelespaciosubaracnoideo4.
Losanimalesfuerondistribuidosaleatoriamenteen2 gru-pos: formalinae incisiónplantar.Los del grupo formalina fuerondivididosen6subgruposconsieteratonescadauno. Los del grupo control (GC) recibieron por vía subaracnoi-deainmediatamentedespués delacolocacióndelcatéter 10l desoluciónsalina;y losdelosgrupos activosGF10, GF20,GF30,GF40yGF50recibieronporlamismavía10lde soluciónconfentolaminaenlasdosisrespectivasde10g, 20g,30g,40gy50g,quecorrespondieron respectiva-mente a31,5nmol,63nmol,94nmol,126nmoly157nmol defentolaminaensoluciónsalinaestéril.
La induccióndeldolorporla formalina(test dela for-malinamodificado),sehizoatravésdelaadministraciónde 50ldesolucióndeformalinaal2%,enlaregióndorsaldela pataposteriorderecha,25mindespuésdelaadministración delasoluciónsalinaodelafentolamina5.
Fueron consideradas todas las elevaciones de la pata no relacionadas con el caminar, independientemente del tiempo enquepermanecíalevantada.El recuentosehizo continuamentedurante60min.Seanotóelnúmeroparcial deelevacionescada5min.Eltestfuedivididoen3fases:i,
intermediayii.Lafaseicomprendióelnúmerode
elevacio-nesdelapatadurantelosprimeros5min,lafaseintermedia delminuto6alminuto20,ylafaseiidelminuto21al60.
Los animalesdelgrupoincisiónplantarfuerondivididos en6subgruposcon7ratonescadauno.Losdelgrupocontrol (GC)recibieronporvíasubaracnoideainmediatamente des-puésdelacolocacióndelcatéter,10ldesoluciónsalina;y losdelosgruposactivosGIP10,GIP20,GIP30,GIP40yGIP50 recibieronporlamismavía 10l desolucióncon fentola-minaenlasdosisrespectivasde10g,20g,30g,40g y50g,loquecorrespondiórespectivamentea31,5nmol, 63nmol, 94nmol, 126nmol y157nmol defentolamina en soluciónsalinaestéril.
Conelanimalanestesiado,sehizounaincisiónquirúrgica longitudinal,de1cmdeextensión,enlapataposterior dere-chaconunbisturídelnúmero11.Fueronincisionadaslapiel ylafasciadelaregiónplantardelapata,coninicioa0,5cm desdeelbordedelcalcáneoyextensiónendirecciónalos dedosdelapata.Elmúsculoplantarseelevóysehizouna incisiónlongitudinal,permaneciendoestaintacta.Después delahemostasiaconunaligerapresiónsobreelsitio quirúr-gico,todoslosplanosfueron aproximadosysuturadoscon 2puntosseparadosconunhiloenunaagujademononilón 4-0.Laevaluación delahiperalgesiasehizoporla aplica-cióndefilamentosdevonFrey,enlasegundahorayenel primero,tercero,quinto,séptimo,decimocuartoyvigésimo
GC GF10 GF20 GF30 GF40 GF50
7,00
6,00
5,00
4,00
3,00
2,00
1,00
0,00
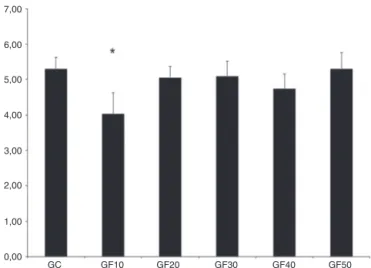
Figura1 Promediosdelnúmerodeelevacionesdelapatade losanimalesdurantelafase intermediadeltest dela forma-lina,en losgrupos estudiados. *Diferencia estadísticamente significativa(p<0,05).
primerdíadespuésdelaadministracióndelasoluciónsalina odelafentolamina6.
Elvolumen delasolución inyectadaenel espacio sub-aracnoideo de 10l, se definió a partir de los estudios previos4,7,8.
Parael análisisestadísticodelosresultados obtenidos, usamoselsoftwareJMP®delStatisticalAnalysisSystem Ins-tituteyseaplicóelanálisisdevarianciaseguidodeltestde Dunnett,con la adopcióndel nivelde significaciónmenor del5%(p<0,05).
Resultados
Intensidaddeldolorevaluadoporeltestdela fentolaminamodificado
Lafentolamina,administradaporvíasubaracnoidea,enlas dosisde20gy30g,produjounaumentoenlarespuesta álgicaenlafaseintermediadeltestdelaformalina modifi-cado,porqueelpromediodelnúmerodeelevacionesdela patadelosanimalesdurantelafaseintermediadeltestde laformalinavarióentre16,28enelgrupoGF10y27,95enel grupoGF30.Losmayoresvaloresfueronencontradosenlos gruposGF20yGF30,quepresentarondiferencias estadísti-camentesignificativascuandofueroncomparadosconelGC (figs.1y2).
Elpromediodelnúmerodeelevacionesdelapatadelos animalesdurantelafaseiylafaseiideltestdela
forma-linanopresentódiferenciasestadísticamentesignificativas entrelosgruposestudiados.
Intensidaddeldolorevaluadoporlosfilamentosde vonFreyeneltestdelaincisiónquirúrgicaplantar
GC GF10 GF20 GF30 GF40 GF50 0,00
5,00 10,00 15,00 20,00 25,00 30,00 35,00 40,00 45,00 50,00
Figura2 Promedios del número de elevaciones de la pata
delosanimalesdurantetodaslasfasesdeltestdela forma-lina,en losgrupos estudiados. * Diferencia estadísticamente significativa(p<0,05).
inducidoporlaincisiónplantaryenladosisde30ggeneró unefectohiperalgésicoenelquintodíaeneldolorinducido porlaincisiónplantar.
Enlasegundahorayenelprimero,terceroyquintodías despuésdela aplicación dela fentolaminasubaracnoidea hubounamenorsensibilidadalosfilamentosdevonFreyen losgrupos GF10yGF20,quepresentaron diferencias esta-dísticamentesignificativas cuandofueron comparados con elGC(figs.3---6).
Al séptimo día de la evaluación se observóuna mayor sensibilidadalosfilamentosdevonFreyenelgrupoGF10, quepresentóunadiferenciaestadísticamente significativa cuandofuecomparadoconelGC(fig.7).
Laevaluaciónhechaeldecimocuartoyelvigésimoprimer día no mostró diferencias estadísticamente significativas entrelos grupos sobre la sensibilidad a los filamentosde vonFrey.
I INT II
Tiempo (minutos)
CN
10
20
30
50
0 10 20 30 40 50 60 70 80 90 100
Número de elevaciones de la pata
Figura3 RespuestaalosfilamentosdevonFreyenlasegunda horadespuésdelaadministracióndelafentolamina subarac-noidea.Diferenciaestadísticamentesignificativa(p<0,05).
GC GF10 GF20 GF30 GF40 GF50
3,00
2,50
2,00
1,50
1,00
0,50
0,00
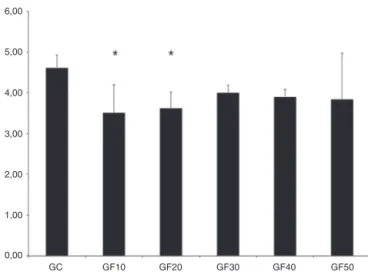
Figura4 RespuestaalosfilamentosdevonFreyenelprimer díadespuésdelaadministracióndelafentolamina subaracnoi-dea.*Diferenciaestadísticamentesignificativa(p<0,05).
GC GF10 GF20 GF30 GF40 GF50
6,00
5,00
4,00
3,00
2,00
1,00
0,00
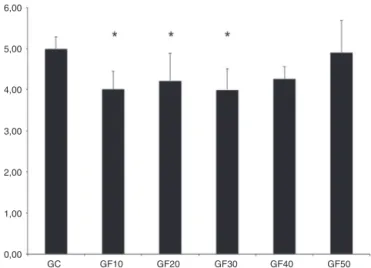
Figura5 RespuestaalosfilamentosdevonFreyeneltercer díadespuésdelaadministracióndelafentolamina subaracnoi-dea.*Diferenciaestadísticamentesignificativa(p<0,05).
GC GF10 GF20 GF30 GF40 GF50
6,00
5,00
4,00
3,00
2,00
1,00
0,00
GC GF10 GF20 GF30 GF40 GF50 6,00
5,00
4,00
3,00
2,00
1,00
0,00
Figura7 RespuestaalosfilamentosdevonFreyenelséptimo díadespuésdelaadministracióndelafentolamina subaracnoi-dea.*Diferenciaestadísticamentesignificativa(p<0,05).
Discusión
El sistema inhibitorio descendente del dolor se compone principalmente de 4 partes del sistema nervioso central interconectadas: a) sistemas corticales y diencefálico; b) sustancias grisesperiacueductal y periventricularricas en encefalinas y en receptoresopioides; c)partes del bulbo rostroventral, especialmente el núcleo magno delrafe, y núcleosadyacentesquerecibenlosimpulsosexcitatoriosde lasustanciasgrisesperiacueductalyque,asuvez,envían fibrasserotoninérgicasynoradrenérgicas,atravésdel funí-culodorsolateral, queseproyectanhaciaelcuernodorsal de la médula y bulbo. Las fibras del sistema inhibitorio descendiente terminan principalmente en las láminas i, II
y v, donde inhiben las neuronas nociceptivas, incluyendo
las interneuronas y tractos ascendientes que se proyec-tan rostralmente, entre ellos los tractos espinotalámico, espinorrecticular y espinomesencefálico. Otro importante grupo de fibras que ha sido incluido en la formación del sistemaendógenodecontroldeldolorsonlasneuronas nora-drenérgicas originariasen el locus coeruleus y el sistema colinérgicocentral2,9---11.
Paraestudiarlosefectosdelafentolaminasobrelasvías deldolorseadministrandiversasdosisporvíasubaracnoidea enratones.Enesteestudiofueronusadasdosiscrecientes, a partir dedosis ya descritasyhabitualmente usadas por otros autores,que demostraronresultados contradictorios ymostraronlanecesidaddeestudioscondosisvariadas,lo quemotivóesteestudiocondosiscrescientes4,8,12.
Eltestdeformalinamodificado,porproducirrespuestas próximasalasqueocurrenensereshumanos,esmuyusado comomodelodenocicepciónenanimales.Elnúmerode ele-vacionesdelapatacomodispositivoparalacuantificación delcomportamientodolorosoinducidoporlaformalina pre-sentaunacorrelaciónimportanteconeltestdelaformalina clásicoyconlasalteracionescardiovascularesenrespuesta al dolorcausado por la formalinaenla pata, llevándonos aunacorrelaciónestrechaconelcomportamientodoloroso enanimalesconscientes13---16.
Durantelasfasesiyiideltestdelaformalinamodificado
noobservamos diferenciasentrelosgrupos estudiados,lo
quemuestraquenohayinterferenciadelsistema noradre-nérgico.Sinembargo,durantelafaseintermedia,propuesta comorelacionadaconlainhibicióncentraldeldolor,vimos unsignificativoaumentodel númerodeelevaciones dela pataencomparaciónconelgrupocontrol,cuandoseusaron lasdosisde20y30gporvíasubaracnoidea,sinobservar diferenciasestadísticamentesignificativasencomparación conlosdemásgrupos.
Estudiosquedemuestranlaaparicióndeunefecto anal-gésicoenpresenciadeunestímulodelosreceptoresalfa-2 medulares, muestran que 10g fueron insuficientes para ejercerunefectoagonistasobreesosreceptoresyquelas dosissuperioresa30gtalvezejerzanunefectoagonista tambiénsobrelosreceptoresalfa-1,efectoesteque anta-gonizalosefectosdelestímulodelosreceptoresalfa-217.
El modelo de dolor a partir de la incisión plantar en ratones, propuesto por Brennan et al.6 es muy útil para comprenderlosmecanismosfisiopatológicosdeldolor.Enla prácticaclínica,seasemejamuchoaldolorquelos pacien-tessientenenelperíodopostoperatorio,involuntarioyde menorintensidadenreposo.
La fentolamina administrada por vía subaracnoideaen ratones,enlasdosisde10y20g,presentócaracterísticas analgésicasen la segundahora después de la administra-ción.Estopuedeserexplicadoporunpredominiodelefecto moduladorcentralsobrebajasdosisdelfármaco.Ellasson incapacesde antagonizarel efecto de la liberación nora-drenérgica descendiente, visto que con el aumentode la dosiseseantagonismosemantuvosinqueseobservase nin-gunareduccióndelasensibilidad(analgesia).Sinembargo, ladosisde10gadministradaporvíasubaracnoideatuvoun efectohiperalgésicoenel primero, tercero,quintoy sép-timodía, como tambiénla dosis de 20g enel primero, tercero y quinto día. La dosis de 30g solo presentó un efectohiperalgésicoenelquintodíadespuésdela adminis-tración,loqueevidenciaqueeneseperíodo,sinlaacción moduladora,elbloqueodelosreceptoresadrenérgicoscon mayorselectividad,posiblementesobrelosreceptores alfa-2,generóunamayorsensibilidadehiperalgesia.
Otros estudios mostraron el surgimiento de un efecto analgésicoenpresenciadeestímulodelosreceptoresalfa-2 ubicados en la médula espinal, por inhibición de la des-carga neuronal17,18. Eso podría explicar los resultados de este experimento, visto que dosis mayores del antago-nista adrenérgico fentolamina podrían estimular también losreceptoresalfa-1,producirunefectoantagonistaa los efectosdelestímulodelosreceptoresalfa-2ypotenciarel efectoadrenérgicosobrelosreceptoresalfa-1.
Lahipótesisdequedosismayoresdelantagonista fento-laminapodríanestimularlosreceptoresalfa-1adrenérgicos yproducirunefectoantagonistaalosefectosdelestímulo delosreceptoresalfa-2adrenérgicosyporende,potenciar elefectoadrenérgico sobrelosreceptoresalfa-1 adrenér-gicos,debeserelucidadaennuevosestudiosquecomparen bloqueantesconunamayorselectividadporlosreceptores alfa-1adrenérgicosconaltasdosisdefentolamina.
Conclusión
posiblementeporlaparticipacióndedistintassubclasesde receptores alfaadrenérgicos en las vías moduladoras del dolor.
Conflicto
de
intereses
Losautoresdeclarannotenerningúnconflictodeintereses.
Bibliografía
1.BudaiD.Neurotransmittersandreceptorsinthedorsalhornof thespinalcord.ActaBiolSzegediensis.2000;44:21---38. 2.TermanGW,BonicaJJ.Spinalmechanismsand their
modula-tion.En: Bonica’smanagementofpain.3thed.Philadelphia: LippincottWillians&Wilkins;2001.p.73---152.
3.McPhersonGA.Currentetrendsinthestudyofpotassium chan-nelopeners.GenPharmacol.1993;24:275---81.
4.PiresOC,AshmawiH,ConstantinoE,etal.Antagonistas sero-toninérgicoenoradrenérgicoporviasubaracnóideaaumentam a resposta álgica em ratos. Rev Bras Anestesiol. 2011;61: 202---10.
5.D’ArmourFE,SmithD.Amethodfordetermininglossofpain sensation.JPharmacolExpTher.1941;72:74---9.
6.BrennanTJ,VandermeulenEP,GebhartGF.Characterizationof aratmodelofincisionalpain.Pain.1996;64:493---501. 7.CalejesanAA, Chang HC, ZhuoM.Spinal serotonergic
recep-torsmediateofanociceptivereflexbysubcutaneousformalin injectionintohindpawinrats.BrainRes.1998;798:46---54.
8.LiuRJ,ZhangRX,QiaoJT,etal.Interrelationsofopioideswith monoaminasindescendinginhibitionofnociceptive transmis-sionatthespinallevel:animmunocytochemicalstudy.Brain Res.1999;830:183---90.
9.VanegasH,SchaibleHG.Descendingcontrolofpersistentpain: inhibitoryorfacilitatory?BrainResRev.2004;46:295---309. 10.MasonP.Deconstructingendogenouspainmodulation.J
Neu-rophysiol.2005;94:1659---63.
11.D’MelloR,DickensonAH.Spinalcordmechanismsofpain.BrJ Anaesth.2008;101:8---16.
12.ObataH,SaitoS,SasakiM.Antiallodyniceffectofinthathecally administered5-HT2agonistsinratswithnerveligation.Pain.
2000;90:173---9.
13.Wheeler-AcetoH, PorrecaF,Cowan A.The ratpawformalin test:comparisonofnoxiousagents.Pain.1990;40:229---38. 14.Doak GJ, SawynokJ. Formalin-induced nociceptivebehavior
and edema: involvement of multiple peripheral 5-hydroxy-tryptaminereceptorsubtypes.Neuroscience.1997;3:939---49. 15.Parada CA, Tambelli CH, Cunha FQ, et al. The major role
of peripheral release of histamine and 5-hydroxytryptamine in formalina-induced nociception. Neuroscience. 2001;102: 937---44.
16.AshmawiHA,ChambergoFS,PalmeiraCCA,etal.Theeffects ofpirilamineandcimetidineandnociceptiveflinchingbehavior inrats.AnesthAnalg.2003;97:541---6.
17.AfonsoJ,ReisF.Dexmedetomidina:papelatualemanestesiae cuidadosintensivos.RevBrasAnestesiol.2012;62:118---33. 18.NocitiJR,SerzedoPSM,ZuccolottoEB,etal.Dexmedetomidina