Mestrado em
Engenharia Ambiental
Programa de Pós-Graduação em Engenharia Ambiental
DISSERTAÇÃO
CARACTERIZAÇÃO BIOQUÍMICA
E MOLECULAR DE BACTÉRIAS
REDUTORAS DE SULFATO
ISOLADAS NA RPPN DO CARAÇA,
MG
AUTOR: IVAN CEZARINI PATRÍCIO
OURO PRETO, MG
Universidade Federal de Ouro Preto
Programa de Pós-Graduação Engenharia Ambiental
Mestrado em Engenharia Ambiental
Ivan Cezarini Patrício
“
CARACTERIZAÇÃO BIOQUÍMICA E MOLECULAR DE
BACTÉRIAS REDUTORAS DE SULFATO ISOLADAS NA
RPPN DO CARAÇA, MG
”
Dissertação apresentada ao Programa de Pós-Graduação em Engenharia Ambiental, Universidade Federal de Ouro Preto, como parte dos requisitos necessários para a obtenção do título: “Mestre em Engenharia Ambiental – Área de Concentração: Saneamento Ambiental”
Orientadora: Profa. Dra.. Maria Célia da Silva Lanna
Co-Orientadora: Profa. Dra.. Silvana de Queiroz Silva
Ouro Preto, MG
Catalogação: sisbin@sisbin.ufop.br
P314c Patrício, Ivan Cezarini.
Caracterização bioquímica e molecular de bactérias redutoras de sulfato isoladas na RPPN do Caraça, MG [manuscrito] / Ivan Cezarini Patrício. - 2009. xi, 89f. : il., graf., tabs.
Orientadora: Profa. Dra. Maria Célia da Silva Lanna. Co-orientadora: Profa. Dra. Silvana de Queiroz Silva.
Dissertação (Mestrado) - Universidade Federal de Ouro Preto.
Instituto de Ciências Exatas e Biológicas. Mestrado em Engenharia Ambiental.
Área de concentração: Saneamento Ambiental.
1. Sulfatos - Teses. 2. Biorremediação - Teses. 3. Bioquímica molecular - Teses. I. Universidade Federal de Ouro Preto. II. Título.
AGRADECIMENTOS
A realização deste trabalho contou com a ajuda de várias pessoas, tanto de maneira
direta quanto indiretamente, aos quais agradeço:
- Em primeiro lugar meus pais e familiares, que sempre me apoiaram para a continuidade
de meus estudos desde o meu ingresso na universidade;
- Ao Programa de Pós-graduação em Engenharia Ambiental – ProAgua – e seus
coordenadores, professores e funcionários pela oportunidade de realizar o presente
trabalho;
- Ao programa de bolsas da CAPES e ao PRODOC-CAPES que forneceram recursos
sem os quais a minha estadia na instituição e realização do trabalho não seriam
possíveis;
- À Profa. Dra. Maria Célia da Silva Lanna, que me concedeu a possibilidade de
confeccionar este projeto no Laboratório de Microbiologia do ICEB-UFOP além com
os meios necessários à realização do mesmo;
- À Profa. Dra.Silvana de Queiroz Silva, que como minha co-orientadora deu importantes
contribuições para a realização do trabalho;
- Ao Profo. Dr. Hubert Mathias Peter Roeser e seus alunos e pesquisadores do DEGEO,
que realizaram a coleta das amostras utilizadas neste trabalho, além de fornecer ajuda
necessária á sua confecção;
- A Universidade Federal de Ouro Preto – UFOP – e seus professores e técnicos que
forneceram apoio á confecção do trabalho;
- Aos professores, técnicos, estagiários, bolsistas e mestrandos que atualmente fazem
parte, ou mesmo já fizeram, do Laboratório de Microbiologia do ICEB cuja ajuda na
confecção dos experimentos e apoio foram imprescindíveis para o término do trabalho;
- Aos estudantes do Laboratório de Microscopia e Microanálise (Microlab) do
Departamento de Geologia da UFOP (DEGEO), pela disponibilidade para realização
das análises;
- Aos meus grandes amigos da República DNA, da qual fui morador, que sempre me
SUMÁRIO
1 INTRODUÇÃO ... 12
1.1 Objetivo Geral ... 14
1.2 Objetivos Específicos ... 14
2 REVISÃO BIBLIOGRÁFICA ... 15
2.1 Classificação Taxonômica e Caracterização dos Grupos de BRS ... 15
2.2 Distribuição e Ecologia dos Grupos de BRS ... 18
2.3 Bioquímica e Fisiologia das Bactérias Redutoras de Sulfato ... 20
2.4 Utilização das BRS para Imobilização de Metais e Biorremediação ... 23
2.5 Estudo de BRS em Biorreatores ... 27
2.6 BRS Associadas à Biocorrosão ... 30
3 MATERIAIS E MÉTODOS ... 33
3.1 Área de Estudo e de Amostragem ... 33
3.2 Cultivo Inicial das Amostras ... 34
3.3 Isolamento das Culturas Puras de Bactérias Redutoras de Sulfato ... 35
3.4 Caracterização dos Isolados Obtidos ... 36
3.4.1 Caracterização Morfológica ... 36
3.4.2 Caracterização Bioquímica Visando a Identificação Taxonômica ... 37
3.4.3 Caracterização Bioquímica Visando a Identificação de Processos ... 38
3.4.4 Caracterização Taxonômica Presuntiva dos Isolados ... 39
3.4.5 Caracterização Molecular dos Isolados ... 39
3.5 Métodos para Escolha de Linhagens para Testes Fisiológicos ... 40
3.5.1 Determinação do Tempo de Redução de Sulfato em Relação ao pH ... 41
3.5.2 Determinação do Número de Células dos Isolados após Redução de Sulfato em Diferentes Valores de pH ... 41
3.6 Determinação das Curvas de Crescimento e Tempo de Geração dos Isolados 42 3.7 Quantificação do Consumo de Sulfato pelos Isolados ... 44
3.8 Quantificação da Produção de Sulfeto pelos Isolados ... 45
4.1 Amostras Positivas para Redução de Sulfato ... 46
4.2 Linhagens Isoladas ... 47
4.3 Caracterização Morfológica dos Isolados ... 48
4.3.1 Morfologia das Colônias ... 48
4.3.2 Morfologia das Células Observadas ao Microscópio Ótico (M.O.) ... 48
4.3.3 Morfologia das Células ao Microscópio Eletrônico de Varredura (MEV) ... 49
4.4 Caracterização Bioquímica dos Isolados ... 51
4.5 Identificação Taxonômica Presuntiva dos Isolados ... 57
4.6 Caracterização Molecular dos Isolados ... 58
4.7 Escolha de Linhagens para Testes Fisiológicos ... 62
4.8 Curva de Crescimento e Tempo de Geração dos Isolados ... 65
4.9 Quantificação do Consumo de Sulfato e Produção de Sulfeto pelos Isolados .. 66
5 DISCUSSÃO ... 69
6 CONCLUSÕES ... 75
7 PERSPECTIVAS ... 77
8 REFERÊNCIAS BIBLIOGRÁFICAS ... 78
LISTA DE FIGURAS
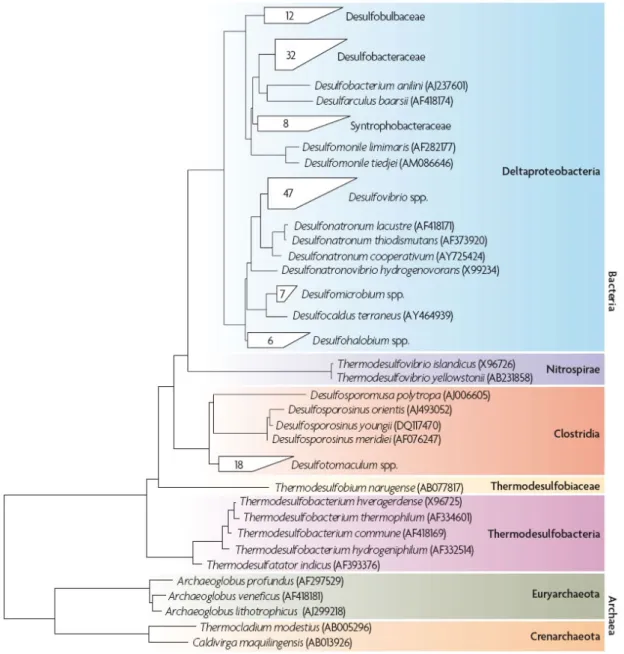
FIGURA 2-1: Árvore filogenética baseada em seqüências de DNA ribossomal descritas em bactérias redutoras de sulfato. Números dentro dos quadros indicam o número de espécies diferentes presentes em um determinado grupo e entre parênteses a identificação no banco de dados. Modificado de Muyzer e Stams (2008). ... 17
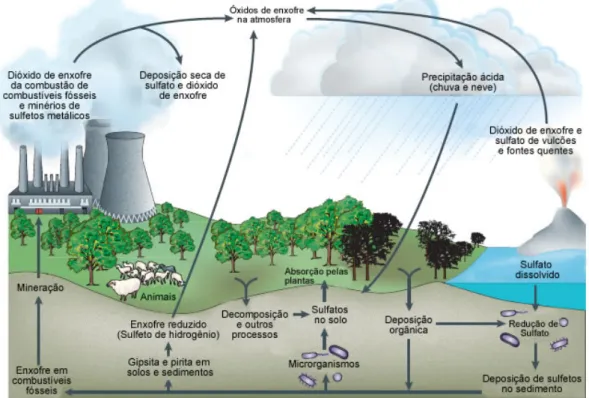
FIGURA 2-2: Ciclo biogeoquímico do enxofre segundo Muyzer e Stams (2008). ... 18 FIGURA 2-3: Redução assimilativa e dissimilativa do sulfato. Adaptado de Madigan et al. (2009). ... 21
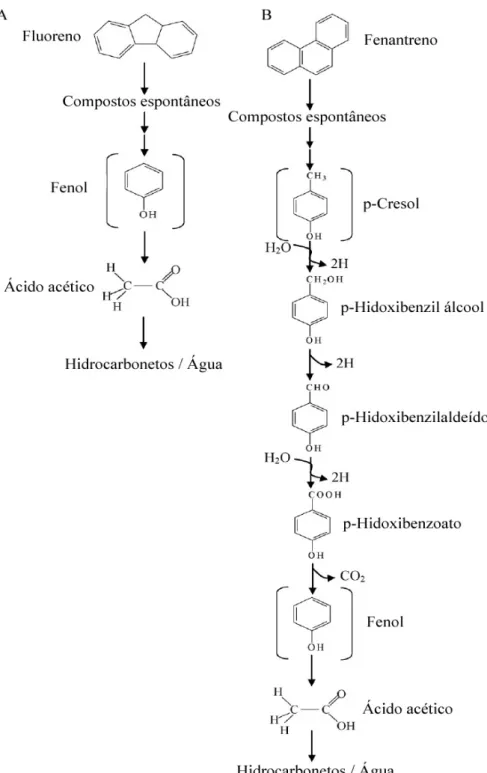
FIGURA 2-4: Modelo de Ress revisado segundo Brunner e Bernasconi (2005). ... 22 FIGURA 2-5: Rota de biodegradação proposta para (A) Fluoreno e (B) Fenantreno por
BRS segundo TSAI et al. (2008). ... 25
FIGURA 2-6: Modelo da corrosão do aço por BRS segundo Barton e Fauque (2009). .... 30 FIGURA 3-1: Região do Rio Conceição, MG. Locais de coleta e principais atividades
humanas próximas. ... 33
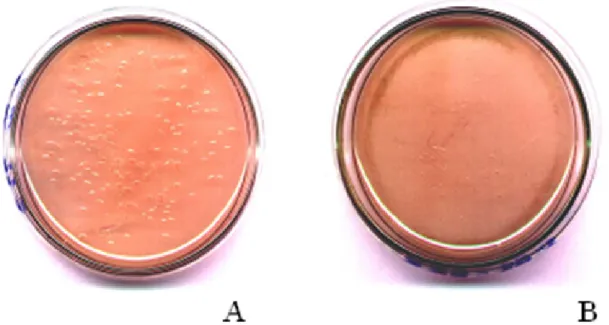
FIGURA 4-1: Crescimento dos organismos em meio sólido de Postgate C após enriquecimento e espalhamento das amostras. Incubação em anaerobiose por 24 horas. ... 46
FIGURA 4-2: Isolados de BRS das amostras apresentando diferenças na redução de sulfato (visualmente) em meio Postgate C após uma semana de incubação à 32 ºC em anaerobiose, o primeiro tubo (da esquerda para a direita) demonstra um controle negativo. ... 47
FIGURA 4-3: Isolados bacterianos ao microscópio eletrônico. A: R104A, B: R105A, C: R107A, D: R111A, E: R301A, F: R305A, G: R307A e H: R310A. ... 50
FIGURA 4-4: Teste de desnitrificação de dois dos isolados. O primeiro e o segundo tubos (da esquerda para a direita) representam, respectivamente, um controle negativo e um positivo utilizando E. coli. ... 53
FIGURA 4-5: Dendrograma indicando a diferenciação bioquímica entre os isolados da amostra R1A. Os números de 1 à 12 representam, respectivamente, os isolados de R101A à R112A. ... 56
FIGURA 4-7: Gel de agarose mostrando a amplificação do DNA dos isolados. ... 59 FIGURA 4-8: Gel de agarose mostrando a amplificação do DNA dos isolados. ... 59 FIGURA 4-9: Gel de agarose mostrando a quantificação do DNA dos isolados. ... 60 FIGURA 4-10: Árvore filogenética contendo sequências do gene DNAr 16S (1.137 pb)
construída pelo método Neighbor-Joining e modelo Maximum Composite Likelihood no programa Mega 4.1. Análise de Bootstrap com 1000 réplicas. Números de referência no GenBank se encontram entre parênteses.. ... 61
FIGURA 4-11: Curvas de crescimento dos isolados e equação de sua fase exponencial. . 65 FIGURA 4-12: Valores das concentrações de sulfato e sulfeto acumulado dos isolados em
crescimento controlado. ... 67
LISTA DE QUADROS
QUADRO 4-1: Características das colônias das linhagens isoladas observadas em meio Postgate C sólido. ... 48
QUADRO 4-2: Características morfológicas ao M.O. das linhagens isoladas após técnica de coloração de Gram. ... 49
QUADRO 4-3: Características metabólicas gerais dos isolados da Amostra R1A incubados em anaerobiose à 32ºC por 48 horas. ... 51
QUADRO 4-4: Características metabólicas gerais dos isolados da Amostra R3A incubados em anaerobiose à 32 ºC por 48 horas. ... 52
QUADRO 4-5: Diferenciação dos isolados quanto à atividade de catalase e desnitrificação. Teste de desnitrificação realizado após incubação à 32 ºC em anaerobiose por uma semana em meio de cultura peptonado (CLESCERI et al., 1999). ... 52
QUADRO 4-6: Características dos isolados quanto à utilização de diferentes substratos como fonte de carbono. Incubação à 32 ºC em anaerobiose por uma semana. Amostras R1A. ... 54
QUADRO 4-7: Características dos isolados quanto à utilização de diferentes substratos como fonte de carbono. Incubação a 32 ºC em anaerobiose por uma semana. Amostras R3A. ... 55
QUADRO 4-8: Similaridade bioquímica entre os isolados da amostra R1A. ... 57 QUADRO 4-9: Similaridade bioquímica entre os isolados da amostra R3A. ... 57 QUADRO 4-10: Proximidade taxonômica entre os isolados seqüenciados e os
LISTA DE TABELAS
TABELA 2-1: Equações estequiométricas dos principais doadores de elétrons utilizados pelas BRS. Baseada no trabalho de Liamleam e Annachhatre (2007). ... 29
TABELA 4-1: Número médio de UFC´s entre as amostras positivas para redução de sulfato. ... 46
TABELA 4-2: Concentração de DNA das amostras purificadas segundo leitura do Ladder Massa. ... 60
TABELA 4-3: Determinação do tempo de início de redução do sulfato pelos isolados em diferentes valores de pH. ... 62
TABELA 4-4: Determinação do tempo de redução completa de sulfato pelos isolados em diferentes valores de pH. ... 63
TABELA 4-5: Determinação do número de células em cada isolado após redução total do sulfato nos diferentes valores de pH testados. ... 64
TABELA 4-6: Equação da fase exponensial, R2, µmax e Tg dos isolados calculados com
base em suas curvas de crescimento. ... 66
TABELA 4-7: Relação entre o consumo de sulfato e a produção de sulfeto pelos isolados. ... 68
TABELA 9-1: Solução Tampão A para dosagem de sulfato, segundo Clesceri et al. (1999). ... 86
LISTA DE ABREVIATURAS E SIGLAS
AFS: Adenosina Fosfosulfato.
BRN: Bactérias Redutoras de Nitrato. BRS: Bactérias Redutoras de Sulfato.
BTEX: benzeno, tolueno, etilbenzeno e xileno. DAM: Drenagem àcidas de minas.
DEGEO: Departamento de Geologia. FAFS: Fosfoadenosina fosfosulfato.
ICEB: Instituto de Ciências Exatas e Biológicas. MEV : Microscópio Eletrônico de Varredura.
MICROLAB: Laboratório de Microscopia e Microanálise do Departamento de Geologia. M.O.: Microscópio ótico.
PAH’s: Polycyclic Aromatic Hydrocarbons = Hidrocarbonetos Aromáticos Policíclicos. RPPN: Reserva Particular do Patrimônio Ambiental
Tg: Tempo de geração.
RESUMO
O estudo sobre as bactérias redutoras de sulfato (BRS) tem sido direcionado, entre
vários aspectos, a sua identificação, considerando a importância das mesmas para os
processos de remediação de ambientes contaminados pelas mais diversas substâncias, visto
a atual demanda ambiental nos países industrializados. O uso de microrganismos na
remediação requer um conhecimento detalhado sobre a sua fisiologia e bioquímica, o qual
tem sido subsidiado por diversas pesquisas visando o aprimoramento de técnicas de
isolamento e identificação das diferentes características que tornam este grupo de bactérias
de grande utilidade nestes processos. No presente trabalho, a partir de amostras de
sedimento do Rio Conceição localizado na RPPN do Caraça em Minas Gerais, Brasil,
foram isoladas linhagens bacterianas de bastonetes Gram negativos e Gram positivos
capazes de reduzir sulfato a sulfeto de hidrogênio. Esses isolados bacterianos foram
submetidos a testes para a sua caracterização bioquímica e mostraram-se capazes de
utilizar variados substratos como fonte de carbono e elétrons para a redução de sulfato.
Testes adicionais demonstraram a capacidade destas linhagens em realizar metabolismos
diferenciados como a redução de nitrato. Em relação à investigação da sua fisiologia foram
determinadas as taxas de crescimento dos isolados R102A, R106A, R112A, R304A,
R307A e R313A em cultivo controlado, assim como a eficiência destas diferentes
linhagens para a produção de sulfeto como produto da redução do sulfato consumido,
embora não tenham sido observadas diferenças significativas entre algumas linhagens. A
identificação filogenética dos isolados citados, baseada nas sequências do DNAr 16S,
indicou que os mesmos pertencem à família Enterobacteriaceae, com similaridade em
torno de 99% com espécies de Enterobacter sp. e Pantoea sp. Com base nos resultados
fisiológicos e filogenéticos pode-se definir tais isolados como possivelmente pertencentes à
família Enterobacteriaceae. A utilização alternativa do sulfato como aceptor final de
elétrons demonstrada pelas linhagens isoladas, apesar desta característica metabólica ser
pouco comum entre os representantes da família Enterobacteriaceae é condizente com a
versatilidade desse grupo taxonômico. Destaca-se ainda que, a flexibilidade metabólica
para os isolados indica a possibilidade da sua utilização em processos de biorremediação e
ABSTRACT
The study of sulphate-reducing bacteria (SRB) has been conducted, among several
aspects, for their identification, considering the importance of this bacteria for remediation
of contaminated environments by many substances, in observation at the current
environmental demands in industrialized countries. The application of microorganisms in
remediation requires a detailed knowledge about their physiology and biochemistry, which
has been subsidized by many approaches seeking the improvement of isolation and
identification techniques of different characteristics that make this bacterial group very
helpful in these processes. In this work, from sediment samples of Rio Conceição located
in the Caraça’s RPPN in Minas Gerais, Brazil, were isolated bacterial strains of Gram
negative and Gram positive rods able to reduce sulphate to hydrogen sulfide. These
bacterial strains were tested for their biochemical characterization and proved capable of
using several substrates as carbon and electrons sources to reduce sulphate. Additional
tests demonstrated the ability of these strains to perform distinguished metabolic features
as nitrate reduction. In relation to the physiological properties were determined the growth
rates of R102A, R106A, R112A, R304A, R307A e R313A strains in controlled cultivate,
as well as the efficiency of the various lineages for the production of sulfide as
sulphate-reduction product, although no significant differences have been observed among some
strains. Phylogenetic identification of these strains based on 16s rDNA sequences,
indicated that many of the isolates belong to the family Enterobacteriaceae, with similarity
around 99% with species of Enterobacter sp. and sp Pantoea. Based on the physiology and
phylogenetic results it can be conclude that the isolates as belong to the family
Enterobacteriaceae. The capability of using sulphate as electron’s acceptor demonstrated
by strains, despite being unusual among the family Enterobacteriaceae members is
consistent with the versatility of this taxonomic group. The metabolic flexibility
demonstrated by the isolates indicates the possibility of their use in bioremediation and
1
INTRODUÇÃO
Bactérias redutoras de sulfato (BRS) é uma designação usual para alguns grupos
bacterianos de vida livre, no meio ambiente. Estes são organismos que utilizam formas
oxidativas de enxofre, ao invés do oxigênio, como aceptor final de elétrons, tendo como
produto dessa reação o gás sulfídrico (H2S), processo esse denominado de “respiração do
sulfato” ou também de redução dissimilativa do enxofre (MADIGAN et al., 2009).
Atualmente, dezenas de gêneros de bactérias redutoras de sulfato são conhecidos,
podendo os mesmos ser distribuídos em vários grupos, tanto de bactérias Gram negativas
quanto de Gram positivas. As BRS apresentam um bom desenvolvimento em uma faixa
ampla de pH, podendo ser mesófilas, ou seja, a temperatura ideal de crescimento é de 20ºC
a 40ºC, ou termófilas crescendo e temperatura de até 70ºC (BARTON e FAUQUE, 2009).
A literatura registra vários trabalhos subseqüentes à descoberta das BRS, entretanto
não se identifica continuidade nos trabalhos iniciais, ou seja, inicialmente os trabalhos
eram baseados somente em questões de identificação e caracterização das BRS, sendo que
o seu uso biotecnológico só foi abrangido mais tardiamente, principalmente com o
surgimento de questões ambientais. Provavelmente este fato possa ser atribuído à
dificuldade de isolamento e manutenção das culturas puras, pois essas são bactérias
anaeróbias e o contato com o oxigênio pode levar á inativação ou inibição de muitas
enzimas ou proteínas utilizadas no processo de redução. Entretanto, mais recentemente,
têm sido detectados alguns desses microrganismos com certa habilidade na utilização de
oxigênio (LEMOS et al., 2001). Já foi comprovada a presença da enzima catalase nesses
organismos, fato que justifica o possível crescimento na presença de oxigênio
(WIERINGA et al., 2000).
Este grupo de bactéria é bastante difundido na natureza podendo ser encontrado
tanto no ambiente aquático quanto no ambiente terrestre, mas ocorre principalmente em
sedimentos, onde as condições redutoras são mais favoráveis. Por serem
quimioheterotróficos utilizam compostos orgânicos de baixo peso molecular, tais como:
lactose, acetato e propionato, além do hidrogênio molecular (H2), como doadores de
elétrons e fonte de energia para o seu crescimento. Os compostos de enxofre mais
utilizados como aceptores finais de elétrons pelas BRS, são sulfitos (SO32-), tiossulfatos
enxofre, é a mais difundida devido à abundância do mesmo no ambiente (RABUS et al.,
2006).
Outro aspecto relevante com relação à redução dissimilativa do sulfato é a
importância geológica e processos, visto que o gás sulfídrico produzido pode reagir com
metais presentes no ambiente levando a formação de sulfetos metálicos. Evidências dessa
atuação podem ser remetidas à participação das BRS na formação, por exemplo, de
depósitos de Pirita (FeS2) (CARVALHO, 2004). O conhecimento desse processo permitiu
investigar o uso dessas bactérias em processos de remediação de metais pesados no
ambiente (WEEB et al., 1998).
Com a crescente preocupação com relação às questões ambientais, a investigação
de vários aspectos das BRS tornou-se relevante, uma vez que as BRS são importantes no
ciclo do carbono e do enxofre, em condições anaeróbicas (MUYZER e STAMS, 2008).
Com isso, muitos estudos sobre a sua dinâmica biogeoquímica, problemas chaves de
filogenia e relação evolutiva, fisiologia celular, ecologia microbiana e aplicabilidade
1.1
Objetivo Geral
Isolar e caracterizar bactérias com capacidade de redução do íon sulfato de
sedimentos do rio Conceição, buscando elucidar aspectos bioquímicos e fisiológicos úteis
das mesmas para bioprocessos.
1.2
Objetivos Específicos
O presente trabalho engloba os seguintes objetivos:
1. Isolar bactérias redutoras de sulfato de amostras de corpos d’água e sedimentos;
2. Caracterizar e identificar os isolados e seus gêneros taxonômicos levando em
consideração seus aspectos morfológicos e metabólicos;
3. Investigar possíveis adaptações fisiológicas ao ambiente, como o crescimento em
diferentes pHs, respiração do nitrato e a utilização de diferentes fontes de carbono
como doadores de elétrons;
4. Determinar as curvas de crescimento dos isolados e seu tempo de geração, podendo
inferir sobre sua velocidade de crescimento;
5. Determinar a capacidade dos isolados em consumir sulfato com concomitante produção
de sulfeto;
6. Caracterizar o perfil filogenético dos fragmentos amplificados de 16s DNA dos
2
REVISÃO BIBLIOGRÁFICA
2.1
Classificação Taxonômica e Caracterização dos Grupos de BRS
No mundo dos procariotos existem diversos organismos que são capazes de realizar
vários tipos diferentes de metabolismos, sendo que entre eles existem os que possuem a
capacidade única de viverem em ambientes totalmente isentos de oxigênio; realizando
assim reações bioquímicas que produzem energia por meio da redução dos mais diferentes
tipos de compostos que agem como aceptores finais de elétrons, entre os quais se podem
citar o nitrato, manganês, ferro, enxofre (em diferentes formas), dióxido de carbono, bem
como formas oxidadas de compostos naturalmente menos abundantes como o arsenato,
cromato, selenato e urânio (RABUS et al., 2006).
Entre estes organismos existe um grupo microbiano de grande interesse, as BRS,
que se apresentam na forma de células esféricas, ovóides, bastonetes ou vibrióides, com
diâmetro em torno de 0,3 a 0,4 μm, ocorrendo sozinhas, em pares ou, algumas vezes, em
agregados. Algumas apresentam flagelos polares ou peritríquios; vivendo principalmente
em ambientes anóxicos aquáticos e sedimentos (HOLT, 1994), e perfazem o único grupo
de organismos procariotos com a habilidade comum de produzir energia por meio da
redução dissimilativa de sulfato para gás sulfídrico (LLOYD et al., 2001).
Por redução dissimilativa de sulfato entende-se a utilização conjunta da oxi-redução
de compostos orgânicos ou hidrogênio molecular com a redução de sulfato como um
aceptor externo de elétrons sob condições anaeróbicas (TEBO e OBRAZTSOVA, 1998);
este processo se diferencia em muito da redução assimilativa de sulfato, onde o mesmo é
convertido a enxofre molecular na forma de aminoácidos e segue por diferentes vias
bioquímicas (MADIGAN et al., 2009).
Embora haja diversos estudos recentes sobre as BRS, as mesmas são conhecidas há
muito tempo, sendo que os pesquisadores Ferdinand Cohn em 1867 e Lothar Meyer em
1964 foram os primeiros a identificar a redução biológica do sulfato como a responsável
por crescentes concentrações de gás sulfídrico em habitats aquáticos (RABUS et al., 2006).
No entanto, apenas em 1895 o professor holandês Martinus W. Beijerinck (1851 – 1931)
conceito e metodologia, por ele mesmo formulados, de “cultura de enriquecimento”
(MADIGAN et al., 2009).
Desde esta época muitos avanços têm ocorrido quanto à identificação das BRS,
uma vez que muitos trabalhos têm proposto várias características tanto bioquímicas quanto
morfológicas visando à construção de uma chave para os grupos. Em seu trabalho, HOLT
et al. (1994), propuseram uma divisão em quatro subgrupos levando se em consideração
características morfológicas e bioquímicas, sendo estas últimas ligadas à oxidação
completa dos substratos orgânicos até CO2 (QUADRO 2-1). Nas demais chaves presentes
no livro são propostas diversas outras características para identificação de gêneros e
espécies para cada grupo.
QUADRO 2-1: Diferenciação de subgrupos de 1 a 4 de bactérias dissimilativas de sulfato ou enxofre segundo HOLT (1994).
Características
1. BRS formadoras de
esporos
2. BRS não formadoras de
esporos; oxidação incompleta de
substratos
3. BRS não formadoras de esporos; oxidação completa de substratos 4. Bactérias redutoras de enxofre Sulfato reduzido a
sulfito
+
+
+
-
Enxofre reduzido a
sulfito
-
+ ou -
-
+
Substratos orgânicos completamente
reduzidos à CO2
+ ou -
-
+
+
Muitos outros autores também citam a oxidação completa de compostos orgânicos
como uma característica muito importante para a caracterização destas bactérias
(MADIGAN et al., 2009 e CASTRO et al., 2000), sendo que a oxidação do acetato é muito
conhecida e considerada relevante. Embora a energética de sua reação ainda não tenha sido
totalmente elucidada, o seu mecanismo é muito bem conhecido (MADIGAN et al., 2009).
Além desta, dentre as principais características citadas para identificação estão a
motilidade, forma da célula e tipo de reação ao procedimento de coloração de Gram
Embora estas características bioquímicas e morfológicas sejam até hoje muito
utilizadas para a identificação das BRS, deve-se salientar que vários trabalhos têm se
utilizado de ferramentas moleculares (DIAS et al., 2008; BAHR et al., 2005; MENERT et
al., 2004; CASTRO et al., 2000 e STACKEBRANDT et al., 1997), a fim de buscar
métodos para catalogar as diversas espécies que, atualmente, passam de 220 estando
divididas em cerca de 60 gêneros (BARTON e FAUQUE, 2009).
Em relação a este tópico pode-se citar um trabalho bastante abrangente realizado
por Muyzer e Stams (2008), que agruparam grande parte das espécies conhecidas de BRS
em uma árvore filogenética confeccionada segundo seqüências de DNA ribossomal
presentes em banco de dados ARB-SILVA (FIGURA 2-1).
Assim, as BRS fazem parte de cinco subdivisões pertencentes ao domínio Bacteria
(Deltaproteobacteria, Nitrospirae, Clostridia, Thermodesulfobiaceae e
Thermodesulfobacteria), além de 2 subdivisões pertencentes ao domínio Archaea
(Euryarchaeota e Crenarchaeota). Deve-se ressaltar que, segundo Barton e Fauque (2009),
as BRS presentes à subdivisão Clostridia são todas pertencentes à família Firmicutes e
perfazem os únicos gêneros de BRS Gram positivas formadoras de esporos.
Tais características mostram como as BRS são um grupo diverso, sendo
adicionadas cada vez mais espécies e gêneros a este grupo em função dos estudos cada vez
mais freqüentes.
2.2
Distribuição e Ecologia dos Grupos de BRS
Segundo observado em relação ao grupo das BRS, as mesmas são importantes não
apenas pelo seu óbvio papel no ciclo biogeoquímico do enxofre (FIGURA 2-2), como
também pela produção do gás sulfídrico que não só é conhecido pela sua toxicidade e
cheiro característico, como também pela sua alta reatividade que causa um grande impacto
de alterações nos constituintes do ambiente (RABUS et al., 2006).
Com relação à sua distribuição ambiental, as BRS são consideradas amplamente
presentes em grandes profundidades. A grande maioria de suas espécies foram
encontradas, principalmente, em ambientes considerados anóxicos como minas profundas
de ouro da África do Sul e aqüíferos basálticos profundos em Washington, EUA (BAKER
et al., 2003), ou mesmo poços petrolíferos do Golfo do México (MIRANDA-TELLO et
al., 2004).
Porém, muitos pesquisadores, a exemplo de Wieringa et al. (2000), evidenciam as
descobertas de BRS com capacidade de sobreviver em ambientes onde existe a presença de
oxigênio, sendo relatada a presença de enzimas de proteção contra os danos celulares
recorrentes do metabolismo de redução de oxigênio como, por exemplo, a catalase e a
superóxido dismutase. Além disso, Lemos et al. (2001) demonstraram a presença de
metabolismo oxidativo em um exemplar de BRS identificado como Desulfovibrio gigas
cujo gênero, a exemplo do gênero Desulfomicrobium, é amplamente relatado como capaz
de sobreviver ao oxigênio tendo não apenas espécies identificadas em condições
oligotróficas, como também relatadas a presença de enzimas redutoras de oxigênio em
alguns de seus exemplares (SANTANA, 2008; BADE et al., 2000 e SASS et al., 1997).
Assim, vários estudos recentes mostram que este grupo de microrganismos pode ser
identificado em diversos ambientes como, por exemplo, na rizosfera de algumas plantas
(CIFUENTES et al., 2003); em solos diversos (MILETTO et al., 2007), bem como em
solos úmidos usados para o cultivo de arroz (LIU et al., 2009) onde os seus representantes
Gram positivos já foram identificados como de grande importância nos processos
biogeoquímicos destes locais (STUBNER e MEUSER, 2000), em sedimentos marinhos
(ISHII et al., 2004), de estuários (DEVEREUX et al., 1996), e de lagos de água doce e
salgada (PEDUZZI et al., 2003 e LI et al., 1999), no trato gastrointestinal de humanos e
animais (DETHLEFSEN et al., 2006 e LIN et al., 1997), e até mesmo associadas à doenças
periodontais e colites ulcerativas em humanos (LANGENDIJK et al., 2000 e PITCHER et
al., 2000). Dentre todos estes locais, as BRS marinhas são consideradas como as mais
abundantes já que este ambiente apresenta maior quantidade de sulfato dissolvido em
relação aos outros citados (MUYZER e STAMS, 2008).
Por fim, as BRS foram provavelmente as maiores responsáveis pela formação de
depósitos de sulfetos metálicos em ambientes pré-históricos anaeróbios, sendo tais jazidas
Assim, as BRS se mostram amplamente difundidas no ambiente, o que, ligado à sua
diversidade metabólica, as torna de grande valia no equilíbrio dos processos biológicos dos
ecossistemas.
2.3
Bioquímica e Fisiologia das Bactérias Redutoras de Sulfato
Segundo Rabus et al. (2006) existem cinco importantes atributos referentes ao
metabolismo das BRS que são explorados na maioria dos estudos realizados atualmente:
1. O metabolismo de sulfato a sulfeto que é bioquimicamente mais complexo do que a
redução do oxigênio pelas bactérias aeróbicas;
2. A ampla variedade de compostos orgânicos que podem ser utilizados pelas BRS como
fontes de carbono e energia;
3. O fluxo que ocorre entre doadores e aceptores de elétrons associado à cadeia
respiratória e que envolve uma grande quantidade de carreadores;
4. A capacidade de alguns grupos de síntese celular utilizando CO₂ durante seu
crescimento na presença de H₂ e sulfato;
5. A regulação do metabolismo, que o aspecto menos explorado entre os grupos de BRS.
Quanto ao metabolismo as BRS são um grupo formado essencialmente por
bactérias quimiorganotróficas heterotróficas, embora representantes de alguns gêneros
como Desulfosarcina, Desulfonema, Desulfococcus, Desulfobacterium, Desulfotomaculum
e algumas espécies de Desulfovibrio apresentem a capacidade de crescer com metabolismo
quimiolitotrófico autotrófico, utilizando H₂ como doador de elétrons e CO₂ como fonte de
carbono (MADIGAN et al., 2009). Porém, embora ocorram tipos diferentes de
metabolismo em algumas espécies, todas as BRS possuem a capacidade de utilizar o
sulfato como seu aceptor final de elétrons, sendo a rota bioquímica muito bem conhecida,
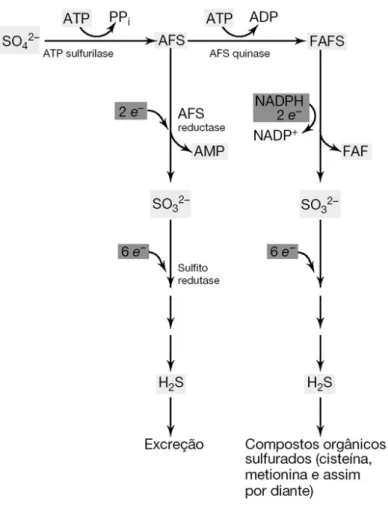
FIGURA 2-3: Redução assimilativa e dissimilativa do sulfato. Adaptado de Madigan et al. (2009).
AFS: Adenosina Fosfosulfato.
FAFS: Fosfoadenosina fosfosulfato.
As taxas de crescimento das BRS sugerem que para cada sulfato reduzido há a
formação de uma molécula de ATP (MADIGAN et al., 2009). Além disso, diferente de
algumas espécies de bactérias redutoras de nitrato, as BRS usualmente não excretam
intermediários de seu metabolismo respiratório, liberando assim apenas o produto final do
mesmo, o ácido sulfídrico (RABUS et al., 2006).
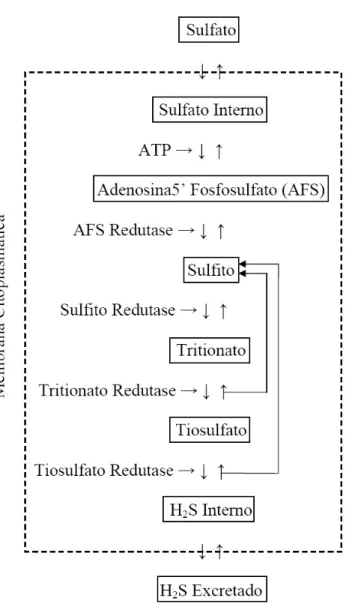
A rota demonstrada na FIGURA 2-3 é baseada no modelo proposto por Ress
publicado em 1973, sendo que, recentemente Brunner e Bernasconi (2005) propuseram, em
um trabalho de revisão, adições ao mesmo levando em conta observações de muitos outros
trabalhos posteriores. Assim, segundo a revisão do modelo de Ress proposta por ambos
(FIGURA 2-4), a redução do sulfito para a formação do gás sulfídrico possui diversos
passos com a formação de vários compostos intermediários como, por exemplo, o
tiosulfato e o tritionato, além disso, pode ser observado um fluxo inverso para algumas
FIGURA 2-4: Modelo de Ress revisado segundo Brunner e Bernasconi (2005).
O metabolismo de redução de sulfato apresenta uma enorme variedade de possíveis
compostos que podem ser utilizados pelas BRS como aceptores finais de elétrons, sendo
que, Madigan et al. (2009) e Rabus et al. (2006), citaram, além do sulfato, o enxofre
orgânico, sulfeto, enxofre elementar, tiossulfato, sulfito, sulfonatos, dimetilsulfoxido,
nitrato (desnitrificação), nitrito, arsenato, oxigênio, fumarato, acrilato, urânio entre outros.
Além disso, os autores ressaltam que compostos como o gás hidrogênio, lactato, etanol,
acetaldeido, acetona, açucares, glicolato, malato, fumarato, succinato, aminoácidos,
compostos aromáticos polares, hidrocarbonetos aromáticos, hidrocarbonetos saturados,
metano, acetato, propionato, formiato, butirato e ácidos graxos diversos entre outros já
foram identificados como doadores de elétrons, assim como a fermentação de alguns
compostos orgânicos como o piruvato formando acetato, H₂ e CO₂ também já foi relatada.
metabolismo de vários dos compostos citados, pela ação das BRS, serão discutidos
posteriormente com mais detalhes.
Outra interessante via que podemos citar é a capacidade de redução de alguns
metais pesados utilizados como aceptores finais de elétrons. Embora não se tenha
detectado crescimento significativo das culturas nas condições propensas à tais reações
(LLOYD et al., 2001 e TEBO e OBRAZTSOVA, 1998), Cheung e Gu (2003), realizaram
estudos com BRS em relação à redução de cromo hexavalente (Cr6-). O cromo oxidado é
considerado altamente tóxico e cancerígeno, sendo este oriundo de vários tipos de
indústrias, demonstrando como pode ser de grande valia o uso destas bactérias na
biotecnologia industrial. Assim, a gama de possíveis compostos que estas bactérias podem
utilizar em diferentes etapas de seu metabolismo, mostram como as mesmas podem
participar dos diferentes processos bioquímicos presentes nos mais diversos ambientes.
Em relação ao seu crescimento, as BRS mostram em vários estudos uma grande
diversidade de dados, tendo sido relatados tempos de geração (Tg) de 1,5 dias (d) com
velocidade máxima de crescimento (µmax) de 0,5 dias-1 (d-1) para espécies de
Desulfoharbdus amnigenus (OUDE ELFERINK et al., 1995); 5,3 horas (h) e 0,13 horas-1
(h-1); 8,6 h e 0,08 h-1, e 6,9 h e 0,10 h-1, respectivamente para Desulfobacter postgatei,
Desulfobulbus propionicus e Desulfovibrio bacuolatus (LAAMBROEK et al., 1984); 7 d e
0,004 h-1 para uma cultura degradadora de naftaleno (HaphS1) (GALUSHKO et al., 1999);
e, por fim; 5,33 d e 0,13 d-1, e 2,47 d e 0,28 d-1 para uma cultura de Desulfovibrio sp. em
cultivo controlado com lactato sem agitação e com agitação, respectivamente (SILVA,
1999).
2.4
Utilização das BRS para Imobilização de Metais e Biorremediação
Devido à produção do H2S em seu metabolismo final as BRS têm a capacidade de
complexar metais em ambientes aquáticos, já que o mesmo reage rapidamente com os íons
metálicos formando sulfetos insolúveis, sendo muito utilizadas para remediar drenagens
ácidas de minas (DAM) em barragens de resíduos (WEEB et al., 1998). Tais
características, e também a enorme capacidade metabólica destas bactérias as tornam hoje
Huisman et al. (2006) evidenciaram muito bem a utilidade destas bactérias para as
indústrias de mineração e metalurgia, pois, a excreção de H2S pelas BRS, permite a
recuperação de metais de importância econômica, na forma de sulfetos, liberados nas
DAM destas atividades. Prática que é mais vantajosa do que a precipitação em forma de
hidróxidos. Além disso, relata que o uso destas bactérias tem maior vantagem econômica,
uma vez que o uso de reagentes para esse fim, como o NaHS ou H2S industrializados, têm
custo muito elevado. Um bom exemplo é fornecido por Lengke e Southam (2006) que
demonstraram o uso das BRS na recuperação de ouro por bioacumulação.
Em relação ao uso das BRS em biorremediação, as mesmas já foram identificadas
atuando como reguladoras de uma variedade de processos que ocorrem em solos inundados
incluindo a reciclagem de matéria orgânica, biodegradação de diversos poluentes
aromáticos clorados em anaerobiose e a metilação do mercúrio (CASTRO et al., 2000).
A este respeito, Teclu et al. (2008) evidenciaram que as BRS podem ser utilizadas
como ferramentas úteis para inativar um rejeito muito comum em algumas atividades de
mineração, os arsênicos tri e pentavalentes, que podem ser precipitados em formas menos
tóxicas e praticamente insolúveis como por exemplo o trisulfeto de arsênico (As2S3).
Além disso, Kleikemper et al. (2004) reforçaram, em seu estudo, como as BRS têm
sido altamente utilizadas em áreas contaminadas por hidrocarbonetos de petróleo, sendo a
degradação de sulfato considerada um importante processo nestes locais, Robertson et al.
(2000), também citam esta capacidade das BRS, tendo relacionado em seu trabalho a
degradação de certos hidrocarbonetos como naftaleno, 1,3,5-trimetilbenzeno (TMB),
tolueno, p-xileno e etilbenzeno à degradação de sulfato por associações bacterianas, uma
vez que nesta investigação culturas puras não foram capazes de degradar todos os
compostos sozinhas como, por exemplo, o benzeno. Resultado parecido foi observado por
Dou et al. (2008) que, por meio de um consórcio formado por BRS e por bactérias
redutoras de nitrato coletado e enriquecido de um ambiente contaminado por combustíveis,
foi capaz de realizar a degradação biológica do BTEX (benzeno, tolueno, etilbenzeno e
xileno), um conjunto de poluentes comuns de vários tipos combustíveis e cuja presença no
ambiente é muito preocupante devido aos seus potenciais tóxico e cancerígeno.
Tsai et al. (2008) também evidenciaram a capacidade de associações de BRS em
utilizar PAH’s (Polycyclic Aromatic Hydrocarbons = Hidrocarbonetos Aromáticos
Policíclicos) para suas biossínteses, o que segundo os mesmos, é de grande valia para o
ambiente já que tais compostos são potencialmente cancerígenos e muito estáveis à
qual um consórcio de BRS degradou dois tipos diferentes PAH’s, o fluoreno e o fenantreno
(FIGURA 2-5), que são comumente encontrados em diversos locais contaminados e, assim
como todos PAH’s compostos de 2 ou 3 anéis aromáticos, perfazem um grande perigo para
os humanos devido à sua solubilidade em água e, logo, fácil dispersão no ambiente.
Consórcios de BRS (inclusive associados a outros grupos de bactérias) também já
foram identificados como responsáveis pela degradação de compostos nitroaromáticos
presentes no ambiente como, por exemplo, os encontrados em solos e sedimentos de
corpos d’água próximos a fábricas de explosivos, pesticidas, herbicidas e produtos
farmacêuticos (KULKARNI e CHAUDHARI, 2007). Como tais rejeitos são considerados
altamente prejudiciais, visto sua grande estabilidade ambiental e capacidade cancerígena
comprovada, a sua degradação visando a remediação do ambiente é altamente prioritária
em diversos países, visto o uso desenfreado dos mesmos ao longo dos anos (LEWIS et al.,
2004).
Embora grande parte dos estudos cite a biodegradação de compostos aromáticos de
carbono como realizadas principalmente por consórcios microbianos, visto a complexidade
da estrutura dos mesmos, Wilkes et al. (2000) evidenciaram em seu trabalho como muitos
estudos têm identificado culturas puras de bactérias anaeróbias capazes de utilizar tais
compostos como, por exemplo, duas culturas de BRS isoladas em seu trabalho capazes de
degradar alquil-benzenos na presença de petróleo. Outro exemplo pode ser observado no
trabalho de Galushko et al. (1999), que identificaram uma cultura pura de BRS isolada de
sedimento marinho com a capacidade de degradar naftaleno.
Ao se considerar contaminantes presentes no ambiente, as BRS também apresentam
grande atuação. Azabou et al. (2005) em um estudo sobre a degradação por BRS do
“Phosphogypsum” (CaSO4), um subproduto potencialmente tóxico advindo da produção
industrial do ácido fosfórico ou por meio da reação entre o fosfato de cálcio [Ca3(PO4)2]
das rochas e o ácido sulfúrico (H2SO4) das chuvas ácidas, identificaram a possibilidade de
uso das mesmas para a degradação deste composto e seu tratamento industrial antes do
despejo. Em trabalho semelhante Schröder-Wolthoorn et al. (2008) demonstraram que
BRS podem ser utilizadas para conversão de anglesita (PbSO4) para galena (PbS), que é
um composto bem menos solúvel e de fácil remoção por processos eletroquímicos,
evidenciando que tal processo não pode ser apenas utilizado em solos ricos em anglesita e,
por conseguinte, contaminados por chumbo, mas também para tratamento de despejos
2.5
Estudo de BRS em Biorreatores
Como tratado anteriormente as BRS possuem muitos possíveis usos industriais em
relação à biorremediação e imobilização de metais, sendo que não apenas as indústrias de
mineração podem ser beneficiadas pelo seu estudo, como também várias outras cujos
despejos sejam ricos em sulfatos e metais a exemplo de processos galvânicos, baterias,
tintas e várias outras manufaturas químicas (BASKARAN e NEMATI, 2006), além de
indústrias com despejos ricos em diferentes formas de compostos de enxofre como, por
exemplo, curtumes, fábricas de papel, óleos comestíveis, fermentações e produtos de
amido (HIRASAWA et al., 2008). Assim, visando esta capacidade das BRS, muitos
trabalhos têm atualmente se dedicado ao estudo da utilização das mesmas em condições
controladas como os biorreatores, o que pode ser muito útil para atingir o seu melhor
potencial em processos industriais, já que se podem definir as melhores formas para seu
cultivo.
Embora as BRS já tenham sido utilizadas em biorreatores com resultados positivos
para o aumento da capacidade de degradação de sulfato para diversos tipos de rejeitos
(GROUDEV et al., 2008; MOHAN et al., 2005; ELLIOTT et al., 1998), sabe-se que as
condições de tais despejos muitas vezes não são favoráveis para as mesmas.
Xin et al. (2008), por exemplo, mostraram que vários estudos não atingiram bons
resultados para tratamento de DAM utilizando BRS, e demonstra que para garantir um
bom rendimento em relação à redução de sulfato, biorreatores que utilizam BRS podem ser
enriquecidos com ferro metálico, já que o mesmo aumenta o pH do meio além de fornecer
hidrogênio ao sistema pela Equação 2-1. Isso é importante porque a grande maioria das
BRS não suportam valores muito baixos de pH (WILLOW e COHEN, 2003) e algumas
espécies podem utilizar o hidrogênio gasoso para a redução do sulfato. Assim, os baixos
valores de pH presentes em alguns sistemas, como as DAM, podem ser o motivo pelo qual
o uso de BRS para remediar estes locais não tenha tido sucesso efetivo em alguns
trabalhos.
Equação 2-1 Feº + 2H₂O = Fe²⁺ + 2OH⁻ + H₂
Além da limitação do pH, Martins et al. (2009) citam como outro grande empecilho
biorremediação, já que compostos de metais pesados podem bloquear muitas enzimas do
metabolismo celular; o que evidencia a necessidade de selecionar cepas resistentes para
tais situações, uma vez que BRS crescendo em condições teoricamente adversas como
baixos valores de pH e temperatura já foram identificadas (TSUKAMOTO et al., 2004).
Outra possibilidade para o uso das BRS em biorreatores, visando a imobilização de
metais, foi proposta no trabalho de Luptakova e Kusmierova (2005) que compararam um
sistema comum utilizando apenas um biorreator com um sistema de biorreatores duplos
para redução de sulfato pelas BRS e concomitante precipitação de cobre. No sistema
comum as bactérias se encontravam junto ao rejeito e no sistema duplo a redução de
sulfato acontecia no primeiro reator e o gás sulfídrico era lançado dentro do segundo
reator. O sistema duplo mostrou uma precipitação mais rápida do cobre presente na
amostra além de uma maior facilidade de recuperá-lo do meio. Assim, como as bactérias
não precisariam entrar em contato com o rejeito, este sistema poderia ser uma alternativa
para a utilização das BRS em rejeitos onde as mesmas não apresentam um bom
crescimento devido a condições adversas do ambiente.
Outra questão que deve ser considerada em se tratando do uso de BRS em
biorreatores é a necessidade de se complementar os despejos com uma fonte de carbono
para as mesmas, já que muitos rejeitos industriais, embora ricos em sulfato, são deficientes
em possíveis doadores de elétrons que as BRS possam utilizar para suas biossínteses
(LIAMLEAM e ANNACHHATRE, 2007).
Segundo van Houten et al. apud Liamleam e Annachhatre (2007 - pag. 461), a
seleção de um doador de elétrons deve ser baseada em duas considerações:
1. A eficiência do tratamento ou habilidade do doador de elétrons para completamente
reduzir e remover sulfato enquanto minimiza a ocorrência de outros poluentes no
efluente e;
2. O custo do doador de elétrons por unidade de sulfato convertida.
Como evidenciado anteriormente são muitos os doadores de elétrons que podem ser
utilizados pelas BRS, o que providencia uma enorme gama de possíveis compostos que
podem ser utilizados para biorremediação, devendo apenas ser observados os critérios
citados.
Assim, levando-se em consideração a importância em se determinar as fontes de
TABELA 2-1 que apresenta além das reações estequiométricas de utilização de alguns dos
principais doadores de elétrons já identificados como de uso comum pelas BRS, como
também a relação entre a quantidade de cada substrato necessária para a utilização de certa
quantidade de sulfato. Tal tabela foi baseada em dados compilados por Liamleam e
Annachhatre (2007) em seu excelente trabalho de revisão.
TABELA 2-1: Equações estequiométricas dos principais doadores de elétrons utilizados pelas BRS. Baseada no trabalho de Liamleam e Annachhatre (2007).
Substrato Equação Estequiométrica
Relação Substrato/Sulfato
Reduzido (Mol) Formiato SO42- + 4HCOO- + H+→ HS- + 4HCO3- 4/1
Metanol 4CH3OH + 3SO42-→ 4HCO3- + 3HS- + 4H2O + H+ 4/3
Etanol 2C2H5OH + 5SO4
+ 8H2 + 1H+→ 4HCO3- +
5HS- + 10H2O
2/5
Lactato 2CH3CHOHCOOH + H2SO4→ 2CH3COOH + 2CO2 + H2S + 2H2O
2/1
Acetato CH3COO- + SO42-→ HS- + 2HCO3- 1/1
Propionato CH3CH2COO
+ 2SO42- + H2→ 2HS- + 3HCO3- +
H2O
1/2
Butirato CH3CH2CH2COO
+ 3SO42- + 2H2→ 3HS- +
4HCO3- + 2H2O
1/3
Além da possibilidade de se utilizar qualquer um dos compostos citados é válido
ressaltar que muitos trabalhos têm obtido bons resultados empregando soluções mistas de
doadores de elétrons em estudos de redução de sulfato, o que não só pode ser usado como
forma de diminuir custos como abrange uma maior diversidade bacteriana já que diferentes
espécies de BRS podem não ser capazes de utilizar o mesmo tipo de substrato
(WAYBRANT et al., 1998 e CHRISTENSEN et al., 1996).
Assim, ao se observar estas questões, um trabalho indicando características de
interesse para o uso de BRS em biorreatores pode ser altamente vantajoso para tratamentos
2.6
BRS Associadas à Biocorrosão
A capacidade das BRS de ampliar a corrosão de vários tipos de ligas metálicas tem
levado a muitos estudos visando o melhor entendimento deste processo e possíveis ações
para o seu controle, uma vez que a corrosão causa grandes danos à estruturas metálicas em
ambientes marinhos a exemplo de pontes, cais, plataformas e tubulações (DUAN et al.,
2008).
Devido à produção do gás sulfídrico, a maioria dos metais é susceptível à ação das
BRS (FIGURA 2-6). Javaherdashti et al. (2006) demonstraram em seu trabalho como as
BRS participam da transformação de metais em ambientes aquáticos, relatando a grande
perda de ductibilidade e quebra de amostras de aço muito mais elevadas em condições
bióticas quando comparado as abióticas, resultado também relatado por Liu et al. (2008),
que evidenciaram como as BRS aumentaram visivelmente a corrosão de ligas de magnésio,
sendo observada a formação ativa de biofilmes sobre as mesmas, o que é um aspecto muito
interessante visto que biofilmes já foram relatados como causadores de cavidades em ligas
metálicas devido à biocorrosão (DUAN et al., 2008).
FIGURA 2-6: Modelo da corrosão do aço por BRS segundo Barton e Fauque (2009).
È importante ressaltar que, além de sua grande afinidade por metais, o gás
sulfídrico já foi identificado causando corrosões em outros tipos de materiais como, por
exemplo, o concreto (ABDELMSEEH et al., 2008), sendo reportado por Postgate (1979)
que estátuas de pedra do Camboja tem sido sujeitas à corrosão envolvendo atividades de
A indústria petrolífera é uma das mais preocupadas com esta questão já que BRS
termofílicas já foram reconhecidas como uma importante fonte de gás sulfídrico em
reservatórios de petróleo (LEU et al. 1998), sendo encontradas participando da corrosão de
equipamentos nas próprias indústrias como, por exemplo, os tanques para separação de
óleo (MIRANDA et al., 2006) além da corrosão de diferentes tipos de peças metálicas em
ambientes marinhos (PINEAU et al., 2008).
Em observação à corrosão de metais por BRS em ambientes aquáticos, Dinh et al.
(2004), propuseram dois mecanismos que podem vir a ocorrer em relação ao ferro (Fe),
sendo um indireto pelo ataque químico do sulfito de hidrogênio (H2S) produzido pelas
BRS e representado pela Equação 2-2, e outro direto por meio da formação de um “filme
de hidrogênio” sobre o ferro exposto à água representado pela Equação 2-3. A formação
deste filme despolariza o ferro e estimula a sua corrosão. Além disso, cita a capacidade de
algumas BRS em corroer o ferro por utilizá-lo como suplemento energético através de uma
rota bioquímica envolvendo um citocromo associado à membrana celular e um sistema de
transferência de elétrons mediado por uma hidrogenase intracelular (Esquema 2-1).
Equação 2-2 2[CH2O] + 11/3Fe + 11/3SO42- + 2/3H+ → 2HCO3- + 11/3FeS + 11/3H2O
Equação 2-3 4Fe + SO42- + 4H2O → FeS + 3Fe2+ + 8HO
-Esquema 2-1 Fe → Citocromo → Hidrogenase (1) → H2→ Hidrogenase (2) →
→ Sistema de transporte de elétrons → Enzimas de redução de sulfato
Além de mostrar possíveis caminhos para a corrosão de um metal amplamente
utilizado, estes mecanismos nos fornecem dados que podem ser utilizados na elucidação de
certas vias bioquímicas pelas quais estes organismos utilizam seu substrato, uma vez que,
como discutido anteriormente, as capacidades metabólicas destas bactérias se mostram
altamente variáveis.
Em relação às alternativas para o controle da ação das BRS, Haveman et al. (2005)
demonstraram em seu trabalho que o nitrito produzido por bactérias redutoras de nitrato
(BRN) age como um inibidor para as enzimas que atuam na redução do sulfato, sendo que
Barton e Fauque (2009) propuseram que a simples adição de nitrato à reservatórios de
petróleo pode controlar a ação das BRS já que o mesmo seria posteriormente convertido a
(2006) mostra em seu trabalho que uma melhor atividade inibitória do nitrito em relação à
redução de sulfato pode ser obtida se o mesmo for combinado com diversos tipos de
3
MATERIAIS E MÉTODOS
3.1
Área de Estudo e de Amostragem
As amostras foram coletadas no mês de Abril do ano de 2004 em trabalho
associativo com pesquisadores do Departamento de Geologia/DEGEO/UFOP em pontos
escolhidos aleatoriamente na extensão do Rio Conceição situado na região do Reserva
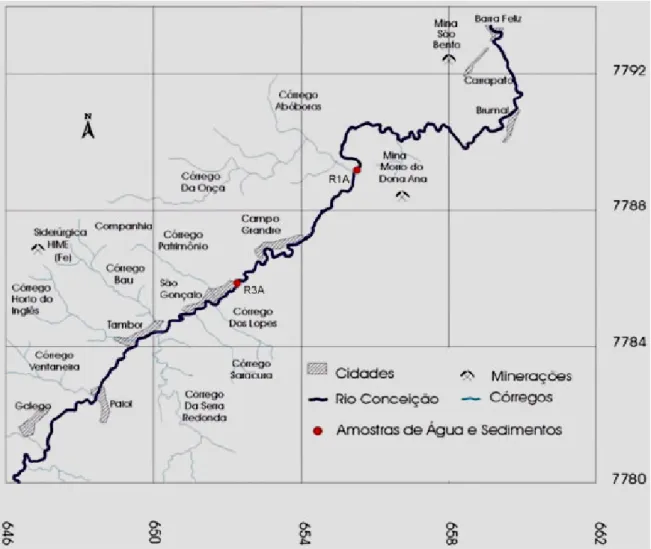
Particular de Patrimônio Natural (RPPN) Santuário do Caraça, MG (FIGURA 3-1).
FIGURA 3-1: Região do Rio Conceição, MG. Locais de coleta e principais atividades humanas próximas.
A coleta foi feita por meio de metodologia padrão (CLESCERI et al., 1999), na
qual frascos de vidro estéreis foram levados até o local onde as amostras foram recolhidas.
Após este procedimento o material levado ao Laboratório de Microbiologia do Instituto de
identificados como: R1A e R3A (FIGURA 3-1). De cada um deles foi retirada uma
amostra de sedimento.
3.2
Cultivo Inicial das Amostras
As amostras foram enriquecidas com o objetivo de aumentar o número de bactérias,
além de selecionar o tipo de bactéria de interesse (BRS) aumentando assim a efetividade
dos passos posteriores do experimento. Para este fim foi escolhido um meio de cultura
específico: Meio de cultura modificado de Postgate C segundo Cheung e Gu (2003) que se
mostrou muito eficiente em trabalhos anteriores realizados no Laboratório de
Microbiologia do DECBI-ICEB/UFOP (RAMPINELLI, 2004).
O enriquecimento das amostras, utilizando-se do meio de cultura citado, foi feito da
seguinte forma: uma alíquota de 10g de cada amostra de sedimento foi transferida para um
Erlenmeyer diferente contendo o meio de cultura citado em uma proporção de 1:25
(amostra: meio). Os frascos foram incubados a 32ºC, durante uma semana, após a qual foi
verificada a redução do sulfato por meio da formação de sulfeto de ferro (FeS), resultando
em um precipitado negro característico. Como estas bactérias são anaeróbias, um ambiente
próprio foi necessário para seu enriquecimento, assim as mesmas foram incubadas em
cubas de anaerobiose que eram na verdade confeccionadas a partir de dessecadores de
vidro hermeticamente fechados. Segundo o procedimento adotado, o oxigênio presente no
interior do dessecador era esgotado utilizando-se uma chama de vela e, após a mesma se
apagar, era retirada uma parte da atmosfera do dessecador com a ajuda de uma bomba de
vácuo previamente acoplada á sua tampa. O vácuo formado ajudava a selar o ambiente
interno do dessecador garantindo a anaerobiose, sendo adicionada também sílica para
remover a umidade, por fim, o dessecador era fechado e incubado em estufa segundo as
necessidades do experimento.
Após o período citado, objetivando um maior enriquecimento e seleção do referido
grupo, uma alíquota de 10mL cada cultura enriquecida que apresentou formação de
precipitado negro foi transferida para um novo Erlenmeyer contendo o mesmo meio de
cultura, seguido do mesmo tratamento descrito acima, resultando assim o segundo
maneira similar. As amostras que não apresentaram precipitação foram submetidas a novo
enriquecimento com nova alíquota buscando uma melhor varredura das BRS.
3.3
Isolamento das Culturas Puras de Bactérias Redutoras de Sulfato
Após as etapas descritas de enriquecimento, realizou-se o isolamento das bactérias
pelo método espalhamento em placa, que consiste na diluição seriada (10-1 a 10-5) do
material enriquecido das amostras de água e sedimento. De cada diluição foram colhidos
0,1mL e aplicados sobre placa de Petri contendo o meio sólido modificado de Postgate C
(CHEUNG e GU, 2003), totalizando cinco placas por amostra (uma para cada diluição). A
solução foi espalhada com o uso de uma alça de vidro estéril (alça de Drigalski) para
contagem das colônias isoladas. As placas foram então incubadas a uma temperatura de
32ºC, durante 24 horas, em ambiente anaeróbio segundo metodologia utilizada por
Rampinelli (2004). A metodologia de espalhamento foi aplicada visando uma maior
facilidade em se coletar as colônias isoladas, visto que as mesmas crescem em sua
totalidade na superfície do meio o que não ocorre no método de pour plate onde colônias
crescem no interior do meio sólido, dificultando assim a sua obtenção.
Destes procedimentos resultaram colônias isoladas em algumas diluições. As placas
que apresentavam colônias mais diversas e bem definidas foram separadas para que as
mesmas fossem obtidas com agulha bacteriológica e inoculadas, separadamente em frascos
de 2mL contendo o mesmo meio de cultura em sua forma líquida. Como estas bactérias são
anaeróbias, o uso dos tubos foi de grande ajuda já que são herméticos e propiciam bem esta
condição.
Para a confirmação de BRS, as culturas puras inoculadas foram incubadas a
temperatura de 32ºC, durante uma semana. Os inóculos que apresentaram a formação de
precipitado negro de sulfeto de ferro foram separados e identificados com números
começando por 01.
De cada isolado que apresentou teste positivo para BRS foi feita uma cultura de
estoque em frascos herméticos, tipo penicilina, contendo o meio sólido descrito
anteriormente picado com agulha de repicagem, incubado nas condições descritas para
crescimento e, após verificação de redução de sulfato, conservado em geladeira no
3.4
Caracterização dos Isolados Obtidos
Após obtenção das culturas puras de BRS, prosseguiram-se os trabalhos com os
testes para a identificação do gênero e/ou espécies das mesmas. A identificação foi
realizada observando-se as características morfológicas tanto das células (forma, arranjo,
entre outras) quanto das colônias (tamanho, cor, entre outras); além das bioquímicas,
relacionadas com a capacidade das bactérias de sintetizar enzimas, assimilarem diferentes
substratos e gerar produtos metabólicos específicos.
Por fim, procurando resultados mais seguros para a identificação dos isolados e
assim inferir mais características sobre os mesmos, foi realizada a sua caracterização
molecular.
3.4.1
Caracterização Morfológica
As características de cada colônia foram descritas observando-se
macroscopicamente as mesmas após o crescimento dos isolados em meio sólido. Em
seguida utilizou-se o Método de Coloração de Gram para a identificação da forma, arranjo
celular bacteriano como também sua definição de Gram positivo ou Gram negativo como
parâmetros usuais para etapa inicial de classificação taxonômica (RABUS et al., 2006). As
observações de morfologia foram reforçadas com a sua visualização por meio de exame à
fresco utilizando microscopia de contraste de fase. Todos os testes citados foram realizados
com a utilização de Microscópio ótico marca Olympus (Modelo BX41).
Para melhor avaliação morfológica das referidas células dos isolados utilizou-se o
Microscópio Eletrônico de Varredura, Marca Jeol, Modelo JSM-5510 (MEV),
equipamento do Laboratório de Microscopia e Microanálise (Microlab) do Departamento
de Geologia (DEGEO)-UFOP. Para esta análise seguiu-se o protocolo padronizado do
3.4.2
Caracterização Bioquímica Visando a Identificação Taxonômica
Para esta caracterização metabólica realizou-se uma série de testes bioquímicos a
fim de avaliar a fermentação de glicose e de lactose pela produção de ácido e/ou gás.
Também foi utilizado citrato como única fonte de carbono e uréia como única fonte de
nitrogênio além da produção de indol e ácido sulfídrico a partir de triptofano e
aminoácidos sulfurados, respectivamente. A motilidade foi também avaliada pela
visualização do padrão de crescimento em meio semi-sólido, sendo posteriormente
confirmada por meio do método da gota pendente em lâmina escavada (MILOSTAN,
2006).
Após a incubação dos tubos a 32ºC, durante 48 horas em condições anóxicas, foi
feita a leitura das reações bioquímicas dos testes supracitados. Para certificação foram
feitos controles positivos e negativos para os meios.
A verificação da capacidade das culturas puras para a utilização de diversos
compostos orgânicos como fontes de carbono e energia foi também realizada utilizando o
meio de cultura modificado de Postgate C contendo cada um dos compostos, citados à
seguir, como única fonte de carbono, estando todos à uma concentração de 5g/L no meio
de cultivo. Como dito anteriormente, este parâmetro é muito importante para uma melhor
identificação dos isolados, além de fornecer importantes informações sobre as capacidades
metabólicas dos mesmos. Assim, verificou-se o grau de oxidação dos seguintes compostos:
acetato, lactose, glicose, lactato, etanol, acetona, benzeno, propionato e butirato,
observando-se a formação de precipitado negro de FeS e produção de gás em tubo de
Durhan, esta última evidencia uma oxidação completa do composto à CO2. Para realização
deste teste foram utilizados tubos de ensaio herméticos com rosca, contendo o meio dotado
de apenas um dos compostos citados como fonte de carbono disponível, para cada
composto testado foi feita uma bateria de tubos em duplicatas para maior certeza dos
testes. Foram utilizados controles negativos, ou seja, um tubo contendo o meio sem as
bactérias e com a fonte de carbono, e outro contendo as bactérias, mas sem a fonte de
carbono.
O último teste realizado visando à identificação taxonômica dos isolados, o teste
que indica a presença da enzima desulfoviridina, é muito importante uma vez que esta
enzima (um tipo de sulfato redutase) está presente em apenas alguns grupos de BRS
Este teste seguiu uma metodologia citada por Silva (1999) pela qual o isolado, após
seu crescimento em meio de cultura apropriado, é colocado em uma lâmina e tem sua
células lisadas com a utilização de algumas gotas de NaOH 2N, em seguida a lâmina é
observada ao microscópio óptico sob luz fluorescente de comprimento de onda de 365nm
onde se nota a formação de manchas avermelhadas caso haja a presença da enzima em
questão, uma vez que, o cromóforo sirohidroclorina presente na mesma reage desta
maneira à este tipo de luz (POSTGATE, 1979). Este teste teve o seu resultado confirmado
posteriormente pela metodologia citada por Postgate (1979) onde os isolados tem suas
células lisadas ao se adicionar o NaOH 2N em tubos de ensaios fechados hermeticamente
contendo os mesmos após incubação, neste caso a formação das manchas avermelhadas é
confirmada ao se observar os tubos junto a uma lâmpada teste com luz de comprimento de
onda de 365nm. Para as duas metodologias utilizaram-se controles negativos.
3.4.3
Caracterização Bioquímica Visando a Identificação de Processos
Por fim, foram realizados outros 2 testes: a presença da enzima catalase e a
capacidade dos isolados em realizar a desnitrificação.
Os testes de catalase e desnitrificação foram feitos por meio de metodologias
padrão (CLESCERI et al., 1999) utilizando-se, respectivamente, a reação das células com
água oxigenada 30V (trinta volumes) e reação dos isolados com soluções de naftiamina e
ácido sulfanílico após o seu crescimento em meio de cultura peptonado. Nos testes, foram
utilizados controles positivo e negativo, de bactérias de referência pertencentes ao
laboratório.
De posse dos resultados destes testes os mesmos foram utilizados, juntamente com
os testes bioquímicos de caracterização taxonômica, para a construção de um dendrograma
indicando a variabilidade bioquímica entre as bactérias. Este teste permite determinar com
maior nível de confiabilidade quais bactérias possuem maior semelhança bioquímica o que
facilita a escolha das cepas que devem ser usadas para os experimentos de fisiologia. Os
dendrogramas foram confeccionados por meio do programa Minitab 15.1.30.0., da Minitab