Universidade de Trás-os-Montes e Alto Douro
Cardiomiopatia Hipertrófica do gato: Casos Clínicos
Dissertação de Mestrado em Medicina Veterinária
Iolanda Inês Múrias Parreira
Orientadora:
Professora Doutora Maria João Miranda Pires, UTAD
Universidade de Trás-os-Montes e Alto Douro
Cardiomiopatia Hipertrófica do gato: Casos Clínicos
Dissertação de Mestrado em Medicina Veterinária
Iolanda Inês Múrias Parreira
Orientadora:
Professora Doutora Maria João Miranda Pires, UTAD
Composição do Júri:
Prof.ª Dr.ª Maria da Conceição Medeiros Castro Fontes, UTAD
Prof.ª Dr.ª Felisbina Luísa Pereira Guedes Queiroga, UTAD
Prof.ª Dr.ª Maria João Miranda Pires, UTAD
Agradecimentos
i
Agradecimentos
Agradeço à minha orientadora, a Professora Maria João, por ter aceitado orientar este trabalho, pelo seu apoio, e pela sua disponibilidade e ajuda na realização da minha dissertação.
Agradeço a toda a equipa do Hospital Veterinário do Baixo Vouga, à Dr.ª Sónia, ao Dr. Pedro, ao Dr. Olivério, ao Dr. Tiago, à Dr.ª Mariana, ao Dr. Hugo, ao Dr. Hélder, à Dr.ª Carla, ao Dr. Artur, ao Dr. Rafael, à Dr.ª Raquel; aos enfermeiros e enfermeiras Daniela Ribau, Luciana, Pedro, Joana, Lima, Daniela Almeida, Eduarda; à Dona Graça, à Kátia, à Lili, à Anastasiya, à “Luba”, à Sandra e à Natasha, pelos excelentes meses de estágio, por todos os conhecimentos transmitidos e por me ajudarem a crescer como profissional. Obrigada pela dedicação que tiveram comigo!
Obrigada ao Dr. Hélio pela paciência e por ter tornado a ecocardiografia num exame de fácil compreensão. Sem o seu incentivo este trabalho não seria o mesmo!
Agradeço a toda a equipa da Clínica Veterinária Terra Quente, à Dr.ª Ana, à Dr.ª Cláudia, à Bernardete e à Tânia, que me acolheram desde o primeiro dia, mesmo quando ainda só sonhava em entrar na universidade. Obrigada por me apoiarem do inicio ao fim desta jornada e me ensinarem tanto!
Agradeço aos meus colegas de estágio, Laura, Sofia, Marta, João, Rita e Lara, por todos os bons momentos passados durante o estágio. Obrigada pelo ânimo que me davam todos os dias.
Agradeço à Cathy, Sónia, Daniela, Diana, Helena e Catarina, por me aturarem sem pedir nada em troca, por tornarem o meu percurso durante o curso muito mais alegre e me apoiarem incondicionalmente.
Agradeço à Daniela, à Ana, à Ana Luísa, à Ana Isabel e à Telma, pelos momentos que passamos juntas e por acreditaram em mim.
Aos meus colegas de curso, obrigada por fazerem destes 5 anos especiais. À minha madrinha Christina e à minha afilhada Daniela, agradeço, por serem a melhor família de curso que poderia ter tido!
Agradeço á minha família, avós, tios e primos por todo o incentivo e carinho incondicional.
Agradeço à minha Fly, Kitty e Rex por me lembrarem, sempre, de que estava no caminho correto.
Agradeço à minha tia Antónia e à minha irmã por todo o amor, paciência, e por estarem sempre presentes.
Agradecimentos
ii E finalmente, agradeço aos meus pais por estarem sempre ao meu lado, me apoiarem sempre nos momentos mais importantes, e por me terem permitido alcançar os meus objetivos.
Resumo
iii
Resumo
A cardiomiopatia hipertrófica é uma doença caracterizada pela hipertrofia concêntrica do ventrículo esquerdo. Esta cardiomiopatia tem prevalência elevada em gatos, sendo a doença cardíaca adquirida mais frequente nesta espécie e a maior causa de mortalidade relacionada com morte súbita, insuficiência cardíaca congestiva e tromboembolismo arterial. Ela está associada a um grande número de apresentações clínicas e a ecocardiografia é o
gold standard para o seu diagnóstico. No entanto, o tratamento continua a ser um assunto
de grande controversa entre os Médicos Veterinários. Sendo assim, este trabalho pretende, contribuir para o conhecimento da cardiomiopatia hipertrófica em gatos, fazendo o paralelismo entre o descrito na literatura e a prática clínica, utilizando para isso vários casos clínicos com diferentes apresentações clínicas.
Esta dissertação começa com a revisão bibliográfica do tema seguindo-se da parte prática, que expõe os resultados obtidos da observação de 14 gatos com cardiomiopatia hipertrófica, recebidos no Hospital Veterinário do Baixo Vouga. Foram registadas as alterações obtidas na anamnese, no exame físico, nos exames complementares realizados (análises laboratoriais, ecocardiografias, radiografias torácicas, eletrocardiogramas, medição da pressão arterial), a abordagem terapêutica instituída para cada caso, e em alguns animais a monitorização/controlo e evolução da doença.
Dos casos clínicos observados, 9 gatos eram fêmeas e 5 eram machos, a média de idades dos animais foi de 6,7 anos (havendo animais com idades entre 1 e os 14 anos) e estavam representados gatos Persa (n=7), Europeu Comum (n=6), e Azul da Rússia (n=1). Havia animais assintomáticos (n=5) e sintomáticos (n=9), sendo que 2 foram internados com tromboembolismo e 7 tinham insuficiência cárdica congestiva. Na avaliação do exame físico verificaram-se alterações à auscultação cardíaca (como presença de sopro em 11 animais) e respiratória (como dispneia presente em 5 gatos), ausência de pulso (n=2) e paresia do membro pélvico (n=2). Em relação aos exames complementares como a radiografia torácica verificou-se a presença de derrame pleural (n=1), cardiomegalia (n=1) e um padrão intersticial/alveolar compatível com edema pulmonar (n=7). À ecocardiografia todos os animais tinham hipertrofia ventricular esquerda (>6mm), 11 tinham disfunção diastólica, 10 tinham dilatação atrial esquerda, 6 tinham presença de smoke ou trombo intracardíaco, e 5 apresentavam obstrução do trato de saída do ventrículo esquerdo e movimento sistólico anterior da válvula mitral. Quanto ao diagnóstico clínico, 5 gatos tinham cardiomiopatia hipertrófica obstrutiva, enquanto que os restantes 9 apresentavam cardiomiopatia hipertrófica não obstrutiva. No que diz respeito aos fármacos utilizados 4 animais não receberam qualquer tratamento e aos restantes 10 foi-lhe administrado um ou mais
Resumo
iv fármacos, como antitrombóticos (n=9 gatos), diuréticos (n=8), benazepril (n=7) e atenolol (n=5).
Deste trabalho conclui-se: que qualquer gato pode ser afetado pela doença independentemente da idade ou género; que o sopro e a dispneia são as alterações principais nestes animais; que a radiografia e a ecocardiografia são os exames complementares mais utilizados; e que o tratamento e prognóstico variam com os sinais clínicos e ecocardiográficos apresentados pelo animal, sendo diferente para cada caso.
Abstract
v
Abstract
Hypertrophic cardiomyopathy main characteristic is the concentric hypertrophy of the left ventricle, is a high prevalence disease in cats, being the most common acquired heart disease in this species is the greatest cause of mortality related with sudden death, heart failure and arterial thromboembolism. It is related to innumerous clinical presentations and echocardiography is the gold standard for the disease’s diagnostic. However treatment is still a subject of controversy among the veterinary doctors. So the objective of this work is to contribute to the knowledge of hypertrophic cardiomyopathy in cats, comparing the ideas from the theory to what is seen in clinical practice, using different clinical cases.
This dissertation starts with a bibliographic review of the subject followed by the results obtained through the observation of 14 cats with hypertrophic cardiomyopathy, assisted in Hospital Veterinário do Baixo Vouga. The changes in anamnesis, physical exam and complementary exams (like laboratory tests, echocardiography, radiography, electrocardiogram, blood pressure measurements) were recorded, besides the treatment, and, in some animals, the disease evolution.
In the clinical cases observed there was 9 females and 5 males, 6,7 years was the average age of the animals (but there were animals between 1 to 14 years of age) , and the represented breeds were Persians (n=7), European Shorthair cats (n=6) and Russian blues (n=1). There was 5 asymptomatic animals and 9 symptomatic cats, being that 2 were hospitalized with thromboembolism and 7 with heart failure. The changes noticed on the physical examination were abnormal cardiac and respiratory auscultation, like heart murmurs (n=11) and dyspnea (n=5), pulse deficit (n=2) and pelvic limb paresis (n=2). Regarding to radiography the observed changes were the presence of pleural effusion (n=1), cardiomegaly (n=1) and an interstitial/alveolar pattern compatible with pulmonary edema (n=7). In echocardiography all animals had hypertrophy of the left ventricle (>6mm), 11 had diastolic dysfunction, 10 had left atrial enlargement, 6 had smoke/intracardiac thrombus, and 5 had left ventricular outflow tract obstruction and systolic anterior motion of the mitral valve. 5 of the cats were diagnosed with obstructive hypertrophic cardiomyopathy and the remaining 9 had non-obstructive hypertrophic cardiomyopathy. About the therapy applied, 4 animals didn’t receive any medication, while, the other 10 cats were given one or more medicaments, like antithrombotics (n=9 cats), diuretics (n=8), benazepril (n=7) and atenolol (n=5).
From this work it’s concluded that any cat can be affected by the disease independently of age or gender, that heart murmur and dyspnea are the main alterations in this animals, that echocardiography and radiography are the most common exams made,
Abstract
vi and that treatment and prognostic change with the physical and echocardiographyc signs presented by the animal, being different for each case.
Índice geral
viiÍndice geral
Agradecimentos ... i Resumo ... iii Abstract ... vÍndice geral ... vii
Índice de quadros ... x
Índice de figuras ... xi
Índice de tabelas ... xiii
Lista de abreviaturas, siglas, símbolos e acrónimos ... xiv
Capitulo I – Introdução ... 1
Capitulo II – Cardiomiopatia Hipertrófica do gato ... 2
1. Definição... 2 2. Epidemiologia ... 2 3. Fenótipos ... 3 4. Etiologia ... 4 4.1. Causas genéticas ... 5 5. Fisiopatologia ... 6 5.1. Diástole ... 7 5.1.1. Disfunção diastólica ... 7 5.1.2. Taquiarritmias ... 8 5.1.3. Isquemia do miocárdio ... 8 5.2. Sístole ... 9
5.2.1. Obstrução dinâmica do trato de saída do ventrículo esquerdo ... 9
5.2.2. Regurgitação da válvula mitral ...10
5.2.3. Disfunção sistólica regional do ventrículo esquerdo ...10
5.3. Cardiomiopatia hipertrófica em fase-terminal ...10
5.4. Tromboembolismo arterial ...10
5.5. Morte súbita ...11
6. Diagnóstico ...11
6.1. Apresentação clínica ...11
Índice geral
viii
6.1.2. Exame físico ...12
6.2. Exames complementares de diagnóstico ...13
6.2.1. Análises sanguíneas e medição da pressão arterial ...13
6.2.2. Eletrocardiograma ...14
6.2.3. Radiografia torácica ...14
6.2.4. Ecocardiografia ...15
6.2.4.1. Hipertrofia ventricular esquerda ...16
6.2.4.2. Dilatação atrial esquerda ...17
6.2.4.3. Movimento sistólico anterior da válvula mitral ...19
6.2.4.4. Disfunção diastólica ...20 6.2.5. Ressonância magnética ...23 6.2.6. Biomarcadores ...23 6.2.6.1. Péptidos natriuréticos...24 6.2.6.2. Troponina I cardíaca ...24 6.2.7. Testes genéticos ...24 7. Tratamento ...25
7.1. Fármacos mais utilizados no tratamento da cardiomiopatia hipertrófica ...25
7.1.1. Bloqueadores-beta ...25
7.1.2. Bloqueadores dos canais de cálcio ...26
7.1.3. Antagonistas do sistema renina-angiotensina-aldosterona ...26
7.1.4. Furosemida ...27
7.2. Animais assintomáticos com cardiomiopatia hipertrófica ...28
7.3. Animais sintomáticos com cardiomiopatia hipertrófica ...30
7.3.1. Gatos com tromboembolismo arterial ...31
7.3.2. Gatos com insuficiência cardíaca congestiva refratária ...32
8. Monitorização ...33
9. Prognóstico ...34
Capitulo III – Casos Clínicos ...35
1. Objetivos...35
2. Metodologia ...36
3. Resultados ...38
3.1 Identificação dos animais ...38
3.2 Anamnese ...38
3.3 Exame físico ...40
Índice geral
ix
3.4.1 Análises laboratoriais ...40
3.4.2 Medição da hormona T4 e da pressão arterial ...41
3.4.3 Eletrocardiografia ...41 3.4.4 Radiografia Torácica ...41 3.4.5 Ecocardiografia ...42 3.5 Diagnóstico ...44 3.6 Tratamento ...45 3.7 Evolução ...46 4. Discussão ...48 Capitulo IV - Conclusão ...54
Índice de quadros
x
Índice de quadros
Quadro 1 – Classificação da gravidade da cardiomiopatia hipertrófica em gatos segundo a espessura da parede do ventrículo esquerdo, medida através de ecocardiografia (adaptado de Côté et al., 2011). ...16 Quadro 2 – Classificação do grau de dilatação do átrio esquerdo, segundo o rácio LA:Ao e o diâmetro absoluto do átrio esquerdo (adaptado de Côté et al., 2011)...18 Quadro 3 - Classificação do grau de obstrução do trato de saída do ventrículo esquerdo (adaptado de Côté et al., 2011) ...20 Quadro 4 – Comparação dos parâmetros ecocardiográficos de função diastólica, de gatos normais e de gatos com cardiomiopatia hipertrófica (adaptado de Bright et al., 1999) ...21 Quadro 5 – Classificações atribuídas segundo a hipertrofia do ventrículo esquerdo, a dilatação atrial, o grau de obstrução do trato de saída do ventrículo esquerdo e função diastólica ...37
Índice de figuras
xi
Índice de figuras
Figura 1 – Representação dos diferentes fenótipos cardíacos existentes na cardiomiopatia hipertrófica do gato (adaptado de Fox, 2003a). ... 4 Figura 2 – Esquema das proteínas que compõem os sarcómeros dos miócitos cardíacos. (adaptado de Côté et al., 2011). ... 5 Figura 3 – Esquema do mecanismo fisiopatológico da cardiomiopatia hipertrófica, desde a mutação na proteína do sarcómero até à disfunção cardíaca (adaptado de Côté et al., 2011). ... 6 Figura 4 – Esquema da fisiopatologia da cardiomiopatia hipertrófica e das suas consequências (adaptado de Chetboul, 2017). ... 7 Figura 5 – Esquema da obstrução do trato de saída do ventrículo esquerdo num gato com cardiomiopatia hipertrófica (adaptado de Chetboul, 2017). ... 9 Figura 6 – Coração de “São Valentim” em gato com cardiomiopatia hipertrófica (adaptado de Côté et al., 2011). ...15 Figura 7 – Radiografia de um gato com insuficiência cardíaca congestiva.s) (imagem gentilmente cedida por HVBV). ...15 Figura 8 – Hipertrofia ventricular num gato com cardiomiopatia hipertrófica. (imagem gentilmente cedida por HVBV). ...17 Figura 9 – Dilatação atrial num gato com cardiomiopatia hipertrófica (imagem gentilmente cedida por HVBV). ...18 Figura 10 – Ecocardiografias de gato com cardiomiopatia hipertrófica obstrutiva, com movimento sistólico anterior da válvula mitral (adaptado de Côté et al., 2011). ...19 Figura 11 – Doppler contínuo do coração de um gato com cardiomiopatia hipertrófica obstrutiva (adaptado de Côté et al., 2011). ...20 Figura 12 – Esquema dos diferentes padrões de função diastólica (adaptado de Ware, 2007). ...21 Figura 13 – Doppler púlsatil de um gato com cardiomiopatia hipertrófica (adaptado de Chetboul, 2017). ...21
Índice de figuras
xii Figura 14 – Radiografia torácica, da projeção lateral do animal 5, onde se observa cardiomegalia (VHS=10), e presença de padrão intersticial compatível com edema pulmonar (imagem gentilmente cedida por HVBV). ...41 Figura 15 – Radiografia torácica, da projeção lateral do animal 4, onde se observa a presença de derrame pleural e de um padrão intersticial compatível com edema pulmonar (imagem gentilmente cedida por HVBV). ...41 Figura 16 – Ecografia em modo B do plano paraesternal direito de eixo curto ao nível dos músculos papilares, do gato 9, onde se observa a hipertrofia moderada do septo interventricular (6,6mm) (imagem gentilmente cedida por HVBV)...42 Figura 17 – Ecografia em modo B do plano paraesternal direito, em eixo longo, de 5 câmaras, do animal 2, em que se observa a hipertrofia da base do septo interventricular (6mm) (imagem gentilmente cedida por HVBV)...42 Figura 18 – Ecografia em modo B, do plano paraesternal direito, de eixo curto, ao nível da aorta, do animal 9, onde se observa, uma dilatação ligeira do átrio esquerdo (LA:Ao=1,7) (imagem gentilmente cedida por HVBV). ...43 Figura 19 – Ecografia em modo Doppler pulsátil da velocidade do fluxo sanguíneo através da aorta, do animal 4, em que a velocidade máxima do fluxo é de 2,74m/s, que corresponde a um grau de obstrução ligeiro do trato de saída do ventrículo esquerdo (imagem gentilmente cedida por HVBV). ...43 Figura 20 – Ecografia em modo B, do plano paraesternal direito, de eixo curto ao nível do átrio esquerdo, do animal 13, onde se observa a presença de um trombo (seta) (imagem gentilmente cedida por HVBV). ...44 Figura 21 – Coração do gato 13 com cardiomiopatia hipertrófica. Na imagem observa-se o aumento da espessura das paredes do ventrículo esquerdo (hipertrofia concêntrica) (espessura máxima de 7mm), com diminuição do diâmetro da cavidade ventricular (imagem gentilmente cedida por HVBV). ...47 Figura 22 – Derrame pleural à abertura do tórax do gato 13 com cardiomiopatia hipertrófica. Durante a necropsia, observou-se a acumulação de fluido (seta), no interior da cavidade pleural (imagem gentilmente cedida por HVBV). ...47
Índice de tabelas
xiii
Índice de tabelas
Tabela 1 – Identificação dos animais relativamente ao género, idade aquando do
diagnóstico, raça e peso vivo. ...38
Tabela 2 – Distribuição dos animais segundo o estímulo iatrotrópico. ...39
Tabela 3 – Distribuição dos animais com e sem doenças concomitantes ou pregressas. ....39
Tabela 4 – Frequência absoluta e relativa das alterações referidas pelo tutor. ...39
Tabela 5 – Distribuição dos animais segundo as alterações ao exame físico. ...40
Tabela 6 – Resultado dos animais com alteração das bioquímicas séricas. ...40
Tabela 7 – Frequência absoluta e relativa das alterações radiográficas encontradas nos animais. ...41
Tabela 8 – Distribuição dos animais segundo o grau e a localização da hipertrofia ventricular esquerda. ...42
Tabela 9 – Distribuição dos animais segundo o grau de dilatação atrial esquerda. ...42
Tabela 10 – Distribuição dos animais segundo o grau de obstrução do trato de saída do ventrículo esquerdo. ...43
Tabela 11 – Distribuição dos animais segundo o grau de disfunção diastólica. ...43
Tabela 12 – Diagnóstico obtido para cada animal. ...45
Tabela 13 – Frequência absoluta e relativa dos fármacos utilizados nos animais ...45
Lista de abreviaturas, siglas, símbolos e acrónimos
xiv
Lista de abreviaturas, siglas, símbolos e acrónimos
% - porcento < - menor que > - maior que ± - mais ou menos ≤ - menor ou igual que ≥ - maior ou igual que
A - enchimento diastólico devido à contração atrial (atrial filling)
A’ - movimento do miocárdio durante o enchimento diastólico devido à contração atrial ALT – Alanina aminotransferase
Ao - diâmetro da aorta
ATE - tromboembolismo arterial B - bidimensional
BID - duas vezes por dia (de 12 em 12 horas) BNP - péptido natriurético cerebral
bpm - batimentos cardíacos por minuto CMH - cardiomiopatia hipertrófica
CMHO - cardiomiopatia hipertrófica obstrutiva CRI - infusão contínua (continuous-rate infusion) dL - decilitro
DT - tempo de desaceleração
E -enchimento diastólico precoce (early filling)
E:A - rácio entre a velocidade de enchimento diastólico inicial e a velocidade de enchimento diastólico devido à contração atrial
E’ - movimento do miocárdio durante o enchimento diastólico precoce ECG - eletrocardiograma
ELISA - Ensaio de imunoabsorção enzimática (Enzyme-Linked Immunosorbent Assay) g - grama
GGT – Gama glutamiltransferase h - hora
HVBV - Hospital Veterinário do Baixo Vouga ICC - insuficiência cardíaca congestiva
IECA - inibidor da enzima de conversão da angiotensina IM - administração intramuscular
Lista de abreviaturas, siglas, símbolos e acrónimos
xv IVRT - tempo de relaxamento isovolumétrico (isovolumic relaxation time)
IVS - septo interventricular Kg - kilograma
LA - diâmetro do átrio esquerdo
LA:Ao - rácio entre o diâmetro do átrio esquerdo e o diâmetro da aorta LV - ventrículo esquerdo
LVOT - Obstrução do trato de saída do ventrículo esquerdo (left ventricular outflow tract) M - movimento
m/s - metro por segundo
MBPC - proteína C de ligação à miosina (myosin binding protein C) mEq/L - miliequivalentes por litro
mg - miligrama
mg/kg - miligrama por kilo de peso vivo min - minuto mm - milímetro mmHg – milímetro de mercúrio ms - milissegundo mv - milivolts MV - válvula mitral
NT-proBNP - Fragmento da forma inativa do péptido natriurético cerebral PO - administração oral
PVa - fluxo retrógrado da veia pulmonar (pulmonar vein in atrial systole)
PW-TDI - Doppler de tecido associado ao doppler pulsátil (pulsed wave-tissue Doppler
imaging)
rpm - respirações por minuto
S - movimento do miocárdio durante a sístole ventricular s - segundos
SAM - movimento sistólico anterior (systolic anterior motion) SC - administração subcutânea
SID - uma vez por dia (de 24 em 24 horas)
smoke - contraste ecográfico espontâneo
SRAA - sistema renina-angiotensina-aldosterona T4 - tiroxina
TDI - Doppler de tecidos (tissue Doppler imaging) TID - três vezes por dia (de 8 em 8 horas)
Lista de abreviaturas, siglas, símbolos e acrónimos
xvi UI – unidades internacionais x - multiplicar μg - micrograma μl - microlitroIntrodução
1
Capitulo I – Introdução
As cardiomiopatias são um grupo de doenças que provocam a alteração do funcionamento e estrutura do músculo cardíaco. Estas doenças podem ser divididas em cardiomiopatia hipertrófica, cardiomiopatia dilatada, cardiomiopatia restritiva, cardiomiopatia arritmogénica do ventrículo direito e cardiomiopatia não classificada (Richardson et al., 1996; Fox, 1999).
As doenças do miocárdio podem ser idiopáticas ou secundárias a outras causas sistémicas (Ware, 2007). Um exemplo de uma cardiomiopatia primária é a cardiomiopatia hipertrófica, caracterizada pelo aumento de massa cardíaca na ausência de outras causas que provocam a hipertrofia concêntrica do ventrículo esquerdo (Chetboul 2017).
A cardiomiopatia hipertrófica é a doença cardíaca mais frequentemente diagnosticada no gato (Ferasin et al., 2003), possui um número variado de apresentações clinicas e morfológicas (Fox, 2003a), e é a maior causa de mortalidade e morbilidade, associada a morte súbita, insuficiência cardíaca e tromboembolismo arterial (Chetboul et al., 2006). A ecocardiografia permite obter o diagnóstico da doença e avaliar as alterações cardíacas associadas de forma precisa e não invasiva (Häggström et al., 2015). O tratamento destes animais deve ser realizado individualmente para cada caso, não sendo um assunto consensual entre os Médicos Veterinários (Rishniw e Pion, 2011; Fox e Schober, 2015).
Esta dissertação foi realizada no sentido de contribuir para o conhecimento da realidade da cardiomiopatia hipertrófica em gatos. Ela inicia-se com uma revisão bibliográfica sobre o tema proposto, verificando em que ponto se encontra o conhecimento sobre esta doença, seguindo-se de vários casos clínicos, caracterizando os animais que são afetados pela cardiomiopatia hipertrófica, demonstrando a variabilidade de manifestações clínicas que caracterizam esta doença e expondo a abordagem diagnóstica e terapêutica seguida nestes casos.
Cardiomiopatia Hipertrófica do gato
2
Capitulo II – Cardiomiopatia Hipertrófica do gato
1. Definição
A cardiomiopatia hipertrófica (CMH) é caracterizada por uma hipertrofia concêntrica do ventrículo esquerdo, sem haver dilatação do mesmo (Chetboul, 2017). É uma doença primária do miocárdio, por isso, outras causas cardíacas, sistémicas ou metabólicas que provoquem hipertrofia concêntrica do ventrículo esquerdo como a estenose aórtica, a hipertensão sistémica, o hipertiroidismo ou a acromegalia, não podem existir aquando do diagnóstico da doença (Ware, 2007). Ao contrário de uma doença primária, o tratamento ou controlo das causas sistémicas de hipertrofia concêntrica do ventrículo esquerdo pode levar a uma melhoria dos problemas cardíacos (Nelson e Couto, 2014).
Em alguns animais além da hipertrofia concêntrica do ventrículo esquerdo existe também uma obstrução do trato de saída do ventrículo esquerdo devido ao movimento anterior da válvula mitral durante a sístole (SAM) (Fox et al., 1995; Fox, 2003a). Para denominar esta particularidade dentro da CMH foi criado o termo cardiomiopatia hipertrófica obstrutiva (CMHO) (Côté et al., 2011).
2. Epidemiologia
A CMH é a doença cardíaca adquirida mais frequente em gatos (Rush et al., 2002), com uma prevalência de 14,5% a 34% em gatos assintomáticos (Paige et al., 2009; Wagner
et al., 2010), e de 58% quando comparada com outras cardiomiopatias (Ferasin et al.,
2003).
Quanto ao género, alguns estudos indicam que os machos são os mais afetados, sendo diagnosticados a uma idade mais jovem e normalmente com uma forma grave da doença, mas nenhum padrão de transmissão hereditário ligado ao sexo foi encontrado
(Rush et al., 2002; Payne et al., 2010; Trehiou-Sechi et al., 2012; Spalla et al., 2015).
No que diz respeito à raça, os gatos sem raça definida e Persa são onde se verifica maior número de animais com a doença. Mas também existem outras raças onde se verifica elevada prevalência da CMH, nomeadamente em gatos: Maine Coon, Ragdoll, British Shorthair, Chartreux e Sphynx (Riesen et al., 2007a; Granstrom et al., 2011; Trehiou-Sechi
et al., 2012; Spalla et al., 2015). Já em relação à CMHO, o estudo realizado por
Trehiou-Sechi et al. (2012) verificou que esta era mais frequente em gatos Persas e Chartreux, com uma prevalência de 48% em relação a outros gatos.
Cardiomiopatia Hipertrófica do gato
3 A maioria dos animais aquando do diagnóstico tem uma idade média entre os 5 e os 7 anos de vida, mas há casos descritos em animais dos 2 meses aos 17 anos (Fujii et al., 2001; Rush et al., 2002). Gatos Sphynx, Maine Coon e Ragdoll costumam ser mais jovens no momento do diagnóstico (Payne et al., 2010; Trehiou-Sechi et al., 2012). A deteção da doença é mais precoce em animais com SAM da válvula mitral (uma vez que costuma estar associado a um sopro) (DeFrancesco et al., 2005).
3. Fenótipos
A CMH do gato é caracterizada por uma marcada variabilidade fenotípica podendo observar-se hipertrofia concêntrica do ventrículo esquerdo ligeira a grave, difusa ou segmentar (Liu et al., 1981; Fox et al., 1995; Fox, 2003a) (Figura 1).
Na forma difusa, a hipertrofia do ventrículo esquerdo afeta a parede livre e o septo interventricular na sua totalidade ou apenas porções de ambos, além de haver espessamento dos músculos papilares (Fox et al., 1995; Fox, 2003a). Considera-se hipertrofia difusa: assimétrica, quando a parede livre é mais afetada que o septo ou vice-versa; e simétrica, quando ambos são afetados de igual forma (Chetboul, 2017). Já na forma segmentar apenas uma parte do ventrículo esquerdo está hipertrofiada, sendo o espessamento da porção basal do septo interventricular a apresentação mais frequente, seguindo-se do espessamento ao nível do ápex (Fox et al., 1995; Fox, 2003a).
Mais de dois terços dos casos de CMH são hipertrofias difusas, enquanto que a hipertrofia segmentar afeta apenas um terço dos gatos com esta doença (Fox et al., 1995; Fox, 2003a).
O átrio esquerdo geralmente não está alterado nas formas ligeira a moderada, podendo encontrar-se aumentado na forma grave da doença (Fox, 2003a). Em alguns animais existe, também, hipertrofia do ventrículo direito, associado ou não a um aumento do átrio direito (Chetboul, 2017).
Cardiomiopatia Hipertrófica do gato
4 Figura 1 – Representação dos diferentes fenótipos
cardíacos existentes na cardiomiopatia hipertrófica do gato. A: hipertrofia difusa simétrica; B: hipertrofia difusa assimétrica, predominante no septo interventricular; C: hipertrofia difusa assimétrica, predominante na parede livre do ventrículo esquerdo; D, E e F: hipertrofia segmentar, onde se observa maior espessura do miocárdio ao nível da base do septo interventricular (adaptado de Fox, 2003a).
4. Etiologia
A causa da CMH em gatos é desconhecida em muitos casos, mas em algumas famílias há uma forte probabilidade de ser um defeito hereditário, já tendo sido identificadas algumas formas de herança da doença em gatos Maine Coon e Ragdoll (Martin et al., 1994; Kittleson et al., 1999; Meurs et al., 1997; Meurs et al., 2005; Chetboul et al., 2012; März et
al., 2015).
Até ao momento não se conhece nenhum fator nutricional, ambiental, infecioso ou imunológico que possa desencadear a doença (Côté et al., 2011). Num estudo realizado por Meurs et al. (2000) o vírus da panleucopenia felina estava presente na maioria dos gatos com CMH, mas não foi encontrada nenhuma relação causal com o desenvolvimento da cardiomiopatia.
Cardiomiopatia Hipertrófica do gato
5 4.1. Causas genéticas
Existem raças como Maine Coon, Ragdoll, American e British Shorthair, Bosques da Noruega, Scotish fold, Sphynx e outras raças puras predispostas à CMH em que há evidência de ser uma doença hereditária (Martin et al., 1994; Meurs et al., 1997; Kittleson et
al., 1999; Meurs et al., 2005; Meurs et al., 2007; März et al., 2015; Chetboul et al., 2012).
Nos Maine Coon com CMH hereditária descobriu-se que no gene que codifica a proteína C de ligação à miosina (MBPC) existe uma mutação missense (troca de um nucleótido por outro), no codão A31P, alterando a base azotada guanina pela base citosina, o que leva à codificação do aminoácido prolina em vez de alanina (Meurs et al., 2005). A prevalência da mutação nesta raça é de 42% na Europa, 31% na América do Norte e na Asia, e de 46% na Austrália; e a maior parte dos animais é heterozigótico para este defeito (Fries et al., 2008; Mary et al., 2010; Longeri et al., 2013). Nestes gatos sabe-se que a forma hereditária da doença tem um padrão de transmissão autossómico dominante e que possui penetrância incompleta (Kittleson et al., 1999), sendo o risco de desenvolvimento da CMH maior em gatos homozigóticos para a mutação e com o avançar da idade (Mary et al., 2010; Longeri et al., 2013).
Nos gatos Ragdoll com CMH hereditária existe também uma mutação missense (troca da citosina pela tiamina), no gene que codifica a MBPC, mas no codão R820W, que leva à codificação do aminoácido triptofano em vez da arginina (Meurs et al., 2007). Num estudo realizado, a prevalência da mutação nesta raça foi de 34%, sendo a maioria dos animais heterozigóticos para esta mutação (Borgeat et al., 2014a).
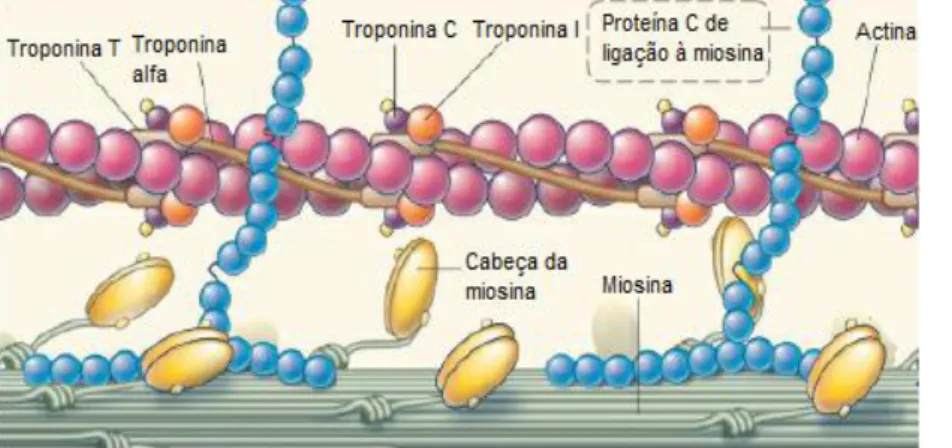
Estas mutações alteram a conformação final da MBPC, uma proteína presente nos sarcómeros (Figura 2), com uma função estrutural e reguladora (Marian e Roberts, 2001; Harris et al., 2002). Ela permite o alinhamento axial do sarcómero e a conexão/desconexão dos filamentos de actina e miosina, ou seja o relaxamento e contração do miócito, contribuindo para a função sistólica e diastólica do coração (Tong et al., 2014).
Figura 2 – Esquema das proteínas que compõem os sarcómeros dos miócitos cardíacos. Em alguns gatos Ragdoll e Maine Coon com cardiomiopatia hipertrófica hereditária sabe-se que a proteína C de ligação à miosina se encontra mutada (adaptado de Côté et al., 2011).
Cardiomiopatia Hipertrófica do gato
6 Com a presença da mutação há um aumento da sensibilidade ao cálcio, da força de contração e do tempo de relaxamento dos miócitos ventriculares (Calaghan et al., 2000). O desenvolvimento de sarcómeros disfuncionais leva ao aumento do número de sarcómeros como forma de compensação, aumentando a rigidez muscular e diminuindo o relaxamento ventricular durante a diástole (Figura 3) (Côté et al., 2011).
Figura 3 – Esquema do mecanismo fisiopatológico da cardiomiopatia hipertrófica, desde a mutação na proteína do sarcómero até à disfunção cardíaca (adaptado de Côté et al., 2011).
Em gatos American Shorthair observou-se que havia um padrão de transmissão autossómico dominante da CMHO (Meurs et al., 1997). Já em gatos Sphynx observou-se um padrão de transmissão autossómico dominante com penetrância incompleta (Chetboul et
al., 2012).
O aparecimento de mutações de novo no sarcómero podem explicar o aparecimento espontâneo da CMH sem ser de forma hereditária. E essas mutações de novo podem ainda ser depois transmitidas à descendência passando a fazer parte da CMH hereditária (Marian e Roberts, 2001).
5. Fisiopatologia
A hipótese proposta para explicar as alterações iniciais que promovem o desenvolvimento da doença é a presença de defeitos ao nível da unidade contrátil dos miócitos cardíacos, os sarcómeros. Esta alteração leva à ativação de mecanismos de
Cardiomiopatia Hipertrófica do gato
7 stresse dentro da célula, provocando a hipertrofia e desorganização dos miócitos e aumento da produção de colagénio, provocando hipertrofia e aumento da rigidez do ventrículo esquerdo. Sendo assim, o relaxamento do miocárdio fica comprometido, principalmente se houver isquemia ou maior sensibilidade ao cálcio, originando alterações da função diastólica e sistólica (Figura 4) (MacDonald, 2010; Nelson e Couto, 2014).
O fenótipo final pensa-se ser influenciado por fatores ambientais, genéticos e outras doenças concomitantes, mas não se sabe quais ou como (MacDonald, 2010).
Figura 4 – Esquema da fisiopatologia da cardiomiopatia hipertrófica e das suas consequências (adaptado de Chetboul, 2017).
ATE: tromboembolismo arterial; CMH: cardiomiopatia hipertrófica; CMHO: cardiomiopatia hipertrófica obstrutiva; ICC: insuficiência cardíaca congestiva; LA: átrio esquerdo; LV: ventrículo esquerdo; LVOT: trato de saída do ventrículo esquerdo; MV: válvula mitral.
5.1. Diástole
5.1.1. Disfunção diastólica
Nos animais com CMH verifica-se que existe diminuição na dinâmica de enchimento cardíaco (disfunção diastólica), devido à rigidez e atraso no relaxamento do ventrículo esquerdo (Fox, 1999). Os principais desencadeadores do défice de relaxamento são: a fibrose e a isquemia do miocárdio; a desorganização dos miócitos; as alterações na concentração intracelular e na sensibilidade ao cálcio (Liu et al., 1993; Fox et al., 1995). Esta alteração na dinâmica de enchimento provoca aumento das pressões diastólicas do lado
Cardiomiopatia Hipertrófica do gato
8 esquerdo do coração, o que leva à dilatação do átrio esquerdo e elevação da pressão nas veias pulmonares, provocando o desenvolvimento de derrame pleural; transudação de plasma para os alvéolos pulmonares (edema pulmonar); e em alguns animais com CMH mais grave, insuficiência cardíaca congestiva (ICC) (Fox, 1999).
A rigidez muscular associada à hipertrofia concêntrica leva à diminuição do volume de sangue bombeado por cada batimento cardíaco e consequentemente à redução da perfusão renal, ativando o sistema renina-angiotensina-aldosterona (SRAA). Isto faz com que o volume circulante aumente e por sua vez as pressões diastólicas se tornem ainda maiores (Taugner, 2001).
Em animais com CMHO a SAM da válvula mitral pode originar regurgitação do sangue para o átrio esquerdo, o que aumenta ainda mais a pressão diastólica (Côté et al., 2011).
5.1.2. Taquiarritmias
A taquicardia leva a uma maior concentração de cálcio dentro da célula cardíaca, o que resulta no aumento da tensão no miocárdio durante a diástole, exacerbando a disfunção diastólica existente e diminuindo ainda mais o débito cardíaco (Gwathmey et al., 1991; Fox, 1999). Também durante os episódios de taquicardia pode haver isquemia do miocárdio se as necessidades em oxigénio das células cardíacas não forem suprimidas (Boerth et al., 1969).
Além disso, a fibrose que existe na CMH contribui para o aumento do aparecimento de arritmias, porque altera a arquitetura do sistema de condução elétrico cardíaco, principalmente em corações com isquemia (Peters e Wit, 1998).
5.1.3. Isquemia do miocárdio
Os gatos com CMH possuem artérias coronárias com paredes espessas que reduzem o diâmetro do lúmen. A arteriosclerose, associada à hipertrofia ventricular, leva ao comprometimento da circulação nas coronárias, provocando isquemia do miocárdio (Liu et
al., 1993).
Outras causas que contribuem para a isquemia são a obstrução do trato de saída do ventrículo esquerdo e a presença de taquiarritmias (Liu et al., 1993; Fox et al., 1995).
Cardiomiopatia Hipertrófica do gato
9 5.2. Sístole
5.2.1. Obstrução dinâmica do trato de saída do ventrículo esquerdo
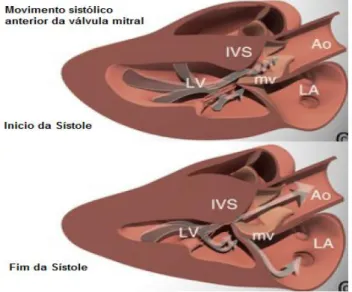
O SAM da válvula mitral é uma alteração frequente em gatos com CMH, aparecendo em 67% dos animais com esta doença (Fox et al., 1995). Este fenómeno é caracterizado pelo deslocamento anterior do folheto anterior da válvula mitral, obstruindo a passagem de sangue pelo trato de saída do ventrículo esquerdo, durante a sístole (Figura 5). Esta obstrução pode ir de ligeira a grave (Côté et al., 2011).
Figura 5 – Esquema da obstrução do trato de saída do ventrículo esquerdo num gato com cardiomiopatia hipertrófica. Neste esquema há movimento da válvula mitral em direção ao septo interventricular, causando a obstrução da saída do sangue para a aorta, durante a sístole e o retorno do sangue para o átrio esquerdo (regurgitação mitral) (adaptado de Chetboul, 2017).
Ao: artéria aorta; IVS: septo interventricular; LA: átrio esquerdo; LV: ventrículo esquerdo; mv: válvula mitral.
Várias teorias foram criadas para tentar explicar este fenómeno: a teoria de Venturi, diz que, devido ao aumento da velocidade da ejeção do sangue pelo trato de saída do ventrículo esquerdo estenosado, o folheto da válvula mitral é aspirado, mas esta teoria foi ultrapassada pela teoria do “deslocamento”, que diz que, a hipertrofia dos músculos papilares provoca o deslocamento anterior das cordas tendinosas que estão ligadas aos folhetos da válvula mitral, obstruindo assim a saída do sangue do ventrículo (Levine et al., 1995; Sherrid et al., 2000).
Quando existe hipertrofia da porção basal do septo interventricular, há uma maior obstrução do trato de saída do ventrículo esquerdo (Sherrid et al., 2000). A obstrução do trato de saída leva: ao aumento da pressão sistólica ventricular, o que aumenta o stresse sob o miocárdio; ao aumento das necessidades em oxigénio do miocárdio; à isquemia do miocárdio; e estimula a hipertrofia ventricular (Fox, 1999).
Cardiomiopatia Hipertrófica do gato
10 5.2.2. Regurgitação da válvula mitral
A regurgitação da válvula mitral é frequente em gatos com CMHO, devido ao deslocamento do seu folheto anterior quando o SAM é evidente (Fox et al., 1995), e esta pode ser ligeira a moderada e provocar o aumento da pressão dentro do átrio esquerdo (Côté et al., 2011).
5.2.3. Disfunção sistólica regional do ventrículo esquerdo
A função sistólica não é afetada, na maioria dos gatos com CMH, mas foi demonstrado, através de estudos ecográficos (Koffas et al., 2006; Sampedrano et al., 2006; Chetboul et al., 2012), que em alguns animais, a função sistólica do miocárdio está diminuída, em alguns dos seus segmentos, provavelmente devido à fibrose, à desorganização dos miócitos e à alteração da sensibilidade ao cálcio (Fox, 1999; Chetboul, 2017).
5.3. Cardiomiopatia hipertrófica em fase-terminal
Em alguns animais com CMH, a doença evolui para uma forma terminal, onde se observa disfunção sistólica, dilatação do ventrículo esquerdo e diminuição da espessura do septo interventricular e da parede livre do ventrículo esquerdo (Cesta et al., 2005). A presença de insuficiência cardíaca, com ou sem derrame pleural ou edema pulmonar é frequente nestes animais, assim como a presença de trombos intracardíacos ou tromboembolismo arterial (Fox e Schober, 2015). Além disso, nestes gatos também existem lesões no miocárdio e nas artérias coronárias (Fox, 1999), que nos humanos são explicadas pela morte celular e pela má circulação coronária provocando isquemia do miocárdio (Maron e Spirito, 1998).
5.4. Tromboembolismo arterial
A incidência de tromboembolismo arterial em gatos com CMH é de 12-17% (Atkins et
al.,1992; Rush et al., 2002). A formação de trombos ocorre quando um ou mais
componentes do triângulo de Virchow está presente: estase sanguínea, hipercoagulabilidade ou lesão do endotélio (Hogan e Brainard, 2015).
Em gatos com esta cardiomiopatia, devido à dilatação do átrio esquerdo há diminuição da velocidade sanguínea no local (estase sanguínea) o que leva à agregação
Cardiomiopatia Hipertrófica do gato
11 celular e ativação das plaquetas, provocando a formação de trombos no local (Hogan e Brainard, 2015); além disso também se verificou, durante a necropsia destes animais, a existência de lesão endotelial e aderências de fibrina (Liu, 1970).
O trombo formado pode deslocar-se do seu local inicial e entrar em circulação, alojando-se numa artéria, sendo o local mais frequente a trifurcação da aorta. A obstrução física e a libertação de substâncias vasoconstritoras por parte do trombo levam à diminuição da perfusão do membro (Hogan, 2017).
5.5. Morte súbita
A morte súbita pode estar ou não relacionada com o aumento da gravidade da doença, e a sua incidência em gatos com CMH não é conhecida. Pensa-se que esta poderá estar relacionada com trombos que ocluam a aorta proximal ou fibrilações (Côté et al., 2011).
6. Diagnóstico
6.1. Apresentação clínica
A maioria dos animais é assintomático, mas existem gatos que desenvolvem sintomas graves ou morrem subitamente. Além disso, as apresentações clínicas da doença são muito variáveis. Torna-se, por isso, muito importante realizar uma anamnese e exame físico completo, para obter o diagnóstico o mais rapidamente possível (Ferasin, 2009).
6.1.1. Anamnese
Entre 35% a 55% dos animais diagnosticados com CMH são assintomáticos, e por isso os tutores não mencionam nenhum sinal clínico, durante a anamnese. Muitas vezes estes gatos são identificados em consultas de rotina, onde é auscultado um sopro ou galope, ao exame físico (Atkins et al., 1992; Rush et al., 2002).
A dispneia é o sinal clínico mais encontrado em animais sintomáticos (32-46%), e normalmente é devido à ICC (Atkins et al., 1992; Rush et al., 2002). Outros sinais que, também, indicam ICC são: a letargia, a anorexia, o vómito e a perda de peso (Côté et al., 2011). Já a sincope e fraqueza ocorrem em 1-6% dos animais e normalmente acontecem após uma arritmia, insuficiência cardíaca grave ou um trombo intracardíaco. Em gatos com tromboembolismo arterial devido à CMH, os tutores podem indicar história de claudicação,
Cardiomiopatia Hipertrófica do gato
12 paralisia ou dor do membro, mais frequentemente nos membros posteriores (Payne et al., 2010; Trehiou-Sechi et al., 2012; Payne et al., 2013).
A morte súbita pode ser a única manifestação clínica encontrada e o diagnóstico é feito durante a necropsia. Esta costuma ser mais frequente em gatos mais jovens (com menos de 5 anos), mas pode ocorrer em qualquer idade (Côté et al., 2011).
Informações acerca de doenças concomitantes que possam interferir no tratamento e monitorização da doença, devem ser tidas em conta durante a anamnese (Côté et al., 2011). Assim como alguns fatores que podem desencadear o aparecimento de insuficiência cardíaca congestiva nestes animais, como a fluidoterapia, a anestesia/cirurgia, ou corticoterapia recente (Rush et al., 2002).
6.1.2. Exame físico
O sopro sistólico é a alteração mais frequente em animais com CMH (Ferasin et al., 2003; Wagner et al., 2010). A principal causa de sopro nestes gatos é a presença de obstrução do trato de saída do ventrículo esquerdo (Nakamura et al., 2011). O sopro devido à obstrução é normalmente auscultado do lado esquerdo, é holossistólico e quanto maior for a frequência cardíaca, maior é a sua intensidade (Paige et al., 2009). Os gatos com SAM da válvula mitral possuem sopros de maior intensidade do que gatos sem obstrução dinâmica (Rush et al., 2002). No entanto, a presença de sopro não é patognomónico de CMH, pois ele pode existir associado a outra cardiomiopatia ou devido à obstrução dinâmica do trato de saída do ventrículo direito (sopro benigno) (Ferasin et al., 2003; Paige et al., 2009; Wagner
et al., 2010). O sopro benigno é normalmente de baixa intensidade (III/IV ou menor) e
aumenta com a frequência cardíaca (Rishniw e Thomas, 2002).
O ritmo de galope é a segunda alteração mais detetada na auscultação cardíaca. Em gatos com CMH este acontece quando se dá o enchimento do ventrículo esquerdo hipertrofiado e rígido, provocando a reverberação das suas paredes. No entanto, o galope não está apenas presente em gatos com CMH, pode também aparecer em animais anémicos ou com outras cardiomiopatias (Côté et al., 2011).
A taquicardia está presente em alguns dos animais com CMH, mas não é um bom parâmetro de auxílio ao diagnóstico da doença, já que a frequência cardíaca pode elevar-se com fatores ambientais ou de stresse (Ferasin et al., 2003).
O pulso femoral pode ou não estar alterado em animais que tenham sofrido de tromboembolismo. Mas muitas vezes estes animais têm o pulso femoral diminuído e as extremidades frias. E apesar dos membros posteriores serem os mais afetados, o tromboembolismo também ocorre nos membros anteriores, mais frequentemente no lado
Cardiomiopatia Hipertrófica do gato
13 direito. Os animais podem, até, vocalizar de dor se o episódio ocorreu nas últimas 24 horas (Hogan, 2017).
Os animais com ICC podem apresentar taquipneia, dispneia, estertores ou encontrarem-se em posição ortopneica. Em gatos que desenvolveram derrame pleural, dependendo do volume de fluidos acumulados, os sons pulmonares podem estar diminuídos ventralmente e podem apresentar taquipneia (Ferasin et al., 2003). No entanto, a ascite ou caquexia costumam estar presentes nos animais com ICC crónica ou CMH em fase-terminal (Atkins et al., 1992; Fox, 1999). Alguns gatos com CMH em fase-terminal costumam estar desorientados, fracos e hipotensos (Côté et al., 2011).
6.2. Exames complementares de diagnóstico
A ecocardiografia é o gold standard para diagnóstico de CMH em gatos. No entanto, os resultados de outros exames complementares podem conduzir à suspeita de CMH, ou evidenciar outras alterações sistémicas, por exemplo: a radiografa torácica pode ser útil para verificar se existe ICC; a eletrocardiografia serve para identificar arritmias; e as análises sanguíneas ou a medição da pressão arterial permitem verificar a existência de doenças concomitantes (Häggström et al., 2015).
6.2.1. Análises sanguíneas e medição da pressão arterial
As análises sanguíneas não permitem diagnosticar a CMH, mas servem para fazer uma avaliação sistémica do animal e perceber se existem outras doenças concomitantes. Em gatos doentes ou geriátricos está aconselhado a realização de hemograma, análises bioquímicas, análise de urina e medição da tiroxina (T4), para verificar o estado de saúde destes animais e observar se existe alguma alteração que condiciona o tratamento a realizar (Häggström et al., 2015).
A realização de um hemograma nestes animais é importante para verificar a existência de anemia significativa (hematócrito ≤22%) pois esta contribui para o desenvolvimento de insuficiência cardíaca, alteração do ritmo cardíaco em gatos com CMH e disfunção diastólica grave (Côté et al., 2011).
A determinação da concentração sérica da T4 total ou livre é importante para descartar o hipertiroidismo, uma causa reversível de hipertrofia do ventrículo esquerdo. Já a medição da pressão sistémica é necessária para distinguir hipertrofia concêntrica do ventrículo esquerdo provocada por hipertensão sistémica ou por CMH (Fox e Schober, 2015). Além disso, a hormona de crescimento tem um efeito endócrino sobre o coração que
Cardiomiopatia Hipertrófica do gato
14 leva ao crescimento dos miócitos cardíacos, e por isso em animais com acromegalia pode encontrar-se hipertrofia concêntrica ventricular. Assim, em gatos com sinais de acromegalia deve ser medida a concentração sérica da hormona de crescimento, já que a hipertrofia cardíaca pode ser reduzida tratando a doença inicial (Myers et al., 2014).
6.2.2. Eletrocardiograma
O eletrocardiograma (ECG) não é um teste sensível na deteção de CMH (Häggström
et al., 2015), mas é muito útil para identificar arritmias e estabelecer qual o melhor
tratamento a aplicar (Côté et al., 2011).
Um estudo onde foi utilizada a monitorização Holter em animais com CMH assintomáticos e gatos normais, demonstrou que apesar de ambos os grupos terem frequências cardíacas semelhantes, a presença de arritmias era maior em gatos com CMH (Jackson et al., 2014), no entanto a presença de arritmias em animais com CMH não é constante (Riesen et al., 2007b).
Algumas das arritmias mais presentes em gatos com CMH são os complexos prematuros ventriculares, a taquicardia ventricular e os complexos prematuros atriais (Ferasin et al., 2003; Trehiou-Sechi et al., 2012; Payne et al., 2013; Jackson et al., 2014). Os complexos prematuros ventriculares são mais frequentes em animais que sofreram de tromboembolismo arterial (Fox, 1999). Já a fibrilação atrial leva à suspeita de um estado mais avançado de doença, pois indica que existe dilatação atrial esquerda grave (Côté et al., 2004). As taquiarritmias, acima dos 240-260bpm, provocam uma maior disfunção diastólica, que pode desencadear ICC (Gwathmey et al., 1991). Além disso, os bloqueios atrioventriculares de terceiro grau também podem ocorrer devido à fibrose do sistema de condução elétrica (Kaneshige et al., 2006).
Se na leitura do ECG houverem alterações do complexo QRS (amplitude >0,9mv e duração >0,04s), pode indicar aumento da espessura do ventrículo esquerdo (Ferasin et al., 2003); já o aumento da duração da onda P e do intervalo PR indicam que há dilatação atrial esquerda (Chetboul, 2017).
6.2.3. Radiografia torácica
Na maioria dos animais com CMH ligeira a moderada e sem dilatação atrial não se encontram alterações cardíacas nas radiografias, no entanto em casos mais graves e com dilatação atrial torna-se um exame mais útil (Winter et al., 2015).
Cardiomiopatia Hipertrófica do gato
15 Quando existe dilatação atrial esquerda, esta é melhor identificada em projeções ventrodorsais ou dorsoventrais, onde a silhueta cardíaca adquire uma forma denominada de “coração de São Valentim” (Figura 6). Este tipo de silhueta cardíaca pode estar presente em outras cardiomiopatias e não só na CMH (Winter et al., 2015). Também a presença de cardiomegalia (Vertebral Heart Size >7.5 ± 0.3) pode indicar doença cardíaca, mas na CMH como existe hipertrofia concêntrica é pouco frequente acontecer (Côté et al., 2011).
As radiografias torácicas são úteis para verificar a existência de ICC e monitorizar a resposta ao tratamento da mesma (Häggström et al., 2015). A insuficiência cardíaca pode identificar-se através da presença de edema pulmonar (mais frequente) e/ou de derrame pleural (Figura 7); também pode haver presença de dilatação das veias pulmonares quando existe aumento da pressão no átrio esquerdo (Rush et al., 2002; Ferasin et al., 2003).
Figura 6 – Coração de “São Valentim” em gato
com cardiomiopatia hipertrófica. Nesta
radiografia da projeção dorsoventral a seta evidencia a dilatação atrial esquerda que faz com que o coração adquira a forma de coração de “São Valentim” (adaptado de Côté et al., 2011).
Figura 7 – Radiografia de um gato com insuficiência cardíaca congestiva. Nesta radiografia torácica (projeção lateral) de um gato com cardiomiopatia hipertrófica obstrutiva, observa-se a presença de derrame pleural (limites do pulmão encontram-se bem definidos) e principalmente nos lobos ventrais observa-se um padrão compatível com edema pulmonar (imagem gentilmente cedida por HVBV).
6.2.4. Ecocardiografia
O diagnóstico de CMH é confirmado através de ecocardiografia, quando existe hipertrofia concêntrica do ventrículo esquerdo (Fox, 2003a). A ecocardiografia é importante não só para o diagnóstico, mas também para monitorizar os animais e determinar a abordagem terapêutica a adotar (Fox e Schober, 2015) . Segundo Paige et al. (2009) e Nakamura et al. (2011) o aumento da espessura do ventrículo esquerdo, devido à CMH, é a alteração ecocardiográfica mais frequentemente encontrada em gatos aparentemente saudáveis.
Cardiomiopatia Hipertrófica do gato
16 Deve ser feita uma ecocardiografia completa em animais com suspeita de CMH para verificar a espessura das paredes, tamanho das câmaras cardíacas, função diastólica e sistólica e investigar se existe obstrução do trato de saída do ventrículo esquerdo (Fox e Schober, 2015).
6.2.4.1. Hipertrofia ventricular esquerda
Considera-se que existe hipertrofia concêntrica quando o septo ventricular ou/e parede livre do ventrículo esquerdo, no fim da diástole, têm uma espessura ≥6mm, e considera-se duvidoso se a espessura estiver entre 5,5 e 5,9mm (Fox et al., 1995). Uma das classificações utilizadas para indicar a gravidade da CMH segundo a espessura da parede do ventrículo esquerdo, está representada no quadro 1.
Quadro 1 – Classificação da gravidade da cardiomiopatia hipertrófica em gatos segundo a espessura da parede do ventrículo esquerdo, medida através de ecocardiografia (adaptado de Côté et al., 2011).
Espessura da parede do ventrículo esquerdo (mm)
Valor normal <5,5 Valor duvidoso 5,5-5,9 CMH ligeira 6-6,5 CMH moderada 6,6-7,5 CMH grave >7,5 CMH: cardiomiopatia hipertrófica
Estudos feitos em diferentes raças mencionam que o peso vivo pode ter alguma influência sobre o valor inicial da espessura da parede do ventrículo esquerdo, e que por isso devia haver limites diferentes dependendo do peso do animal (Gundler et al., 2008). Existem já alguns autores que mencionam intervalos de referência para a espessura do ventrículo esquerdo específicos em determinadas raças (Granstrom et al., 2011; Chetboul et
al., 2012; Mottet et al., 2012).
A realização das medições é efetuada no modo bidimensional (B), no plano paraesternal direito de eixo curto, abaixo das cordas tendinosas, no fim da diástole, ou seja, quando o maior diâmetro interno do ventrículo esquerdo estiver presente. As medições são realizadas nos locais de maior espessura do septo interventricular e parede livre do ventrículo esquerdo, evitando os músculos papilares (Figura 8) (Häggström et al., 2015). No entanto, para avaliar a hipertrofia da base do septo interventricular as medições devem ser feitas no plano paraesternal direito, de eixo longo, de 4 ou 5 câmaras, colocando o cursor na região mais espessa do septo interventricular (Côté et al., 2011).
Cardiomiopatia Hipertrófica do gato
17 O modo movimento (M) também pode ser utilizado, mas existe mais dificuldade no posicionamento do cursor, e com o modo B consegue-se ter uma avaliação mais global da espessura das paredes (Bonagura, 2000).
Figura 8 – Hipertrofia ventricular num gato com cardiomiopatia hipertrófica. Esta ecocardiografia em modo B, do plano paraesternal direito de eixo curto, mostra o coração de um gato, em diástole, onde se observa o aumento da espessura do
septo interventricular (6,6mm) (imagem
gentilmente cedida por HVBV). IVS: septo interventricular.
A hipertrofia dos músculos papilares pode ser o único sinal presente e a hipertrofia concêntrica pode só desenvolver-se mais tarde. Esta hipertrofia é avaliada de forma subjetiva; normalmente os músculos papilares têm um formato mais fino, enquanto que, quando há presença de CMH os músculos papilares têm uma base mais larga e são hiperecóicos (Adin e Diley-Poston, 2007; Schober e Todd, 2010).
A obliteração da câmara ventricular esquerda durante a contração cardíaca é frequente em gatos com CMH. Este fenómeno acontece quando há uma hipertrofia grave dos músculos papilares e das paredes ventriculares, provocando, no fim da sístole, o desaparecimento total do lúmen do ventrículo esquerdo da imagem ecográfica (Kittleson et
al., 1999; Adin e Diley-Poston, 2007).
Em algumas regiões hipertróficas do miocárdio e subendocardio aparecem áreas hiperecóicas devido há fibrose. E quando há SAM da válvula mitral é frequente aparecer na base do septo interventricular uma placa fibrótica, identificada, à ecografia, como uma região espessada hiperecóica (Fox, 2003a).
6.2.4.2. Dilatação atrial esquerda
Devido à disfunção diastólica há aumento da pressão no átrio esquerdo provocando a sua dilatação; a presença de regurgitação da válvula mitral aumenta ainda mais o volume e pressão sanguínea dentro do átrio, agravando a dilatação. Em alguns gatos pode-se verificar fibrose do miocárdio do átrio esquerdo que leva a uma maior dilatação e disfunção do átrio (Côté et al., 2011).
Cardiomiopatia Hipertrófica do gato
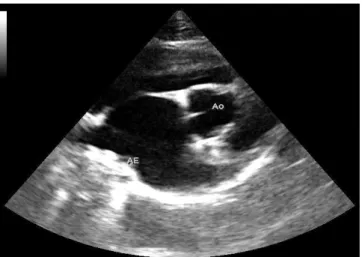
18 Para medir o diâmetro do átrio esquerdo (LA) é utilizado o plano paraesternal direito de eixo curto a nível da válvula aórtica (Figura 9). Essa medida é depois comparada com o diâmetro da aorta (Ao), obtendo-se o rácio LA:Ao que permite eliminar a influência da massa corporal sobre o diâmetro atrial e comparar medidas realizadas entre diferentes animais com tamanhos díspares (Abbott e MacLean, 2006; Schober et al., 2007a).
Figura 9 – Dilatação atrial num gato com cardiomiopatia hipertrófica. Nesta ecografia em modo B, do plano paraesternal direito, de eixo curto, ao nível a artéria aorta, observa-se que existe o aumento do tamanho do átrio esquerdo. O diâmetro da aorta é de 8,7mm e o diâmetro do átrio esquerdo é de 14,8mm, obtendo-se um rácio LA:Ao de 1,7 (imagem gentilmente cedida por HVBV).
Ao: artéria aorta; LA: átrio direito; LA:Ao: rácio entre o diâmetro do átrio esquerdo e da artéria aorta.
Ao contrário dos cães, os gatos, não têm tanta variação na conformação corporal, por isso alguns clínicos usam o diâmetro do átrio esquerdo absoluto, para avaliar a dilatação atrial esquerda. As medições devem ser realizadas quando as cúspides aórticas estão fechadas, e o diâmetro não deve incluir as paredes (Schober et al., 2007a). Esta medição pode ser feita utilizando o modo M ou do modo B, mas o alinhamento do cursor é mais difícil no modo M (Abbott e MacLean, 2006).
Segundo as medições obtidas pode-se classificar o grau de dilatação quanto à sua gravidade, como demonstrado no quadro 2.
Quadro 2 – Classificação do grau de dilatação do átrio esquerdo, segundo o rácio LA:Ao e o diâmetro absoluto do átrio esquerdo (adaptado de Côté et al., 2011).
LA:Ao LA (mm)
Valor normal <1,5 <16
Dilatação ligeira do átrio esquerdo 1,51-1,79 16-19,9
Dilatação moderada do átrio esquerdo 1,8-1,99 20-24
Dilatação grave do átrio esquerdo >2 >24
LA:Ao: rácio entre o diâmetro do átrio esquerdo e o diâmetro da aorta; LA: diâmetro do átrio esquerdo A dilatação atrial pode levar à agregação de células sanguíneas, devido à diminuição da velocidade dentro da câmara cardíaca, e este fenómeno pode ser identificado através da presença de contraste ecográfico espontâneo (smoke) no átrio esquerdo, durante a ecocardiografia (Schober e Maerz, 2006).
Cardiomiopatia Hipertrófica do gato
19 6.2.4.3. Movimento sistólico anterior da válvula mitral
O SAM da válvula mitral pode ser observado a nível ecográfico, durante a sístole, em que se verifica o movimento do folheto valvular aproximando-se do septo interventricular; utilizando o Doppler colorido observa-se a saída de fluxo turbulento a partir da válvula mitral (que indica regurgitação) e do trato de saída do sangue do ventrículo esquerdo (que indica uma ejeção turbulenta do sangue durante a sístole) (Figura 10) (Abbott, 2010; Schober e Todd, 2010).
Este fenómeno pode ser observado no modo B através do plano paraesternal direito, de eixo longo, de 5 câmaras ou no plano apical esquerdo de 5 câmaras. O modo M também pode ser utilizado para verificar o posicionamento errático do folheto da válvula mitral durante a sístole (Fuentes, 2010).
Figura 10 – Ecocardiografias de gato com cardiomiopatia hipertrófica obstrutiva, com movimento sistólico anterior da válvula mitral. Na imagem da esquerda a seta indica a obstrução no trato de saída do ventrículo esquerdo, criada pelo folheto da válvula mitral que toca o septo interventricular durante a sístole. Na imagem da direita (ecografia com doppler colorido) observa-se o fluxo turbulento ao longo do trato de saída do ventrículo esquerdo e a regurgitação da válvula mitral, criado devido ao movimento sistólico anterior da válvula mitral. São ambas ecografias no modo B, do plano paraesternal direito, de eixo longo, de 5 câmaras (adaptado de Côté et al., 2011).
Ao: artéria aorta; IVS: septo interventricular; LA: átrio direito.
A obstrução provocada pelo SAM da válvula mitral faz aumentar a resistência da passagem do sangue no trato de saída do ventrículo esquerdo, e para medir a gravidade da obstrução, é necessário calcular a diferença de pressão (gradiente de pressão) entre o ventrículo esquerdo e a aorta. O gradiente é estimado a partir da velocidade do fluxo sanguíneo que passa na aorta, utilizando a equação de Bernouilli modificada (gradiente de pressão = 4 x velocidade2). A velocidade é obtida através do Doppler contínuo, colocando o cursor alinhado, paralelamente ao fluxo de ejeção do sangue do ventrículo esquerdo para a aorta, utilizando o plano apical esquerdo, de 5 câmaras (Côté et al., 2011). Os graus de obstrução do trato de saída estão resumidos no quadro 3.
Cardiomiopatia Hipertrófica do gato
20 Quadro 3 - Classificação do grau de obstrução do trato de saída do ventrículo esquerdo (adaptado de Côté et al., 2011).
Gradiente de pressão entre o ventrículo esquerdo e a aorta (mmHg)
Obstrução ligeira <50
Obstrução moderada 50-80
Obstrução grave >80
Com a utilização do Doppler contínuo também se verifica que o padrão da velocidade do sangue através da aorta não tem uma forma cónica normal, mas sim uma forma côncava, assimétrica, chamada de forma de “adaga”, quando há presença de SAM da válvula mitral (Figura 11) (Fuentes, 2010).
Figura 11 – Doppler contínuo do
coração de um gato com
cardiomiopatia hipertrófica
obstrutiva. Nesta ecocardiografia observa-se a concavidade (seta) no padrão de velocidade do sangue da aorta (forma de “adaga”), formada devido ao movimento sistólico anterior da válvula mitral. Esta onda é obtida utilizando o plano apical esquerdo de 5 câmaras, (adaptado de Côté et al., 2011).
Os animais com obstrução moderada ou grave podem beneficiar de tratamento para diminuir a ocorrência de SAM da válvula mitral. E esse tratamento tem de ter em conta o temperamento do animal já que este fenómeno é dinâmico, aumentado com a elevação da frequência cardíaca (Côté et al., 2011).
6.2.4.4. Disfunção diastólica
6.2.4.4.1. Doppler pulsátil
O Doppler pulsátil é utilizado em gatos e outros animais para avaliar a função diastólica (Bright et al., 1999). Para obter o padrão de enchimento diastólico é utilizado o plano apical esquerdo, de 4 câmaras e o cursor é colocado ao nível do anel mitral paralelo ao fluxo sanguíneo (Fuentes, 2010). O padrão de enchimento diastólico normal é caracterizado por: um tempo de relaxamento isovolumétrico (IVRT) curto; uma onda de enchimento diastólico precoce (E) dominante em relação à onda de enchimento diastólico devido à contração atrial (A), criando o rácio E:A > 1 (Bright et al., 1999).
O atraso no relaxamento diastólico provoca alterações no padrão como: IVRT prolongado; redução da velocidade da onda E e aumento do tempo de desaceleração (DT)