2018
UNIVERSIDADE DE LISBOA
FACULDADE DE CIÊNCIAS
DEPARTAMENTO DE QUIMICA E BIOQUIMICA
Desenvolvimento de recetores heteroaromáticos para o
reconhecimento de aniões
Paulo Jorge Cruz Vieira
Mestrado em Química
Especialização em Química
Dissertação orientada por:
Cristina Moiteiro
2
Esta tese é dedicada à minha querida avó Josefina que infelizmente
faleceu meses antes da conclusão desta tese.
Onde quer que estejas espero que estejas feliz e orgulhosa
pelo teu neto minha querida avó
3
Agradecimentos
Em primeiro lugar queria agradecer ao projeto P2020 PTDC/QEQ-SUP/4283/2014 financiado pela Fundação para a Ciência e Tecnologia I. P (FCT) e ao Fundo Europeu de Desenvolvimento Regional (FEDER) pelo financiamento que proporcionou desenvolver este trabalho.
Em segundo lugar queria agradecer com um especial obrigado à Dra. Cristina Moiteiro por todo o apoio, conselhos e ensinamentos dados em mais uma etapa da minha vida académica e científica, neste caso, a realização desta tese de mestrado. Agradeço com grande amizade a oportunidade de poder dar continuidade ao trabalho desenvolvido na minha tese de licenciatura e assim ter a chance de continuar a trabalhar num laboratório onde fui muito bem acolhido e que muitas vezes foi uma segunda casa. Além disso e sem dúvida mais importante, a oportunidade de enriquecer o meu conhecimento em áreas científicas, como a química supramolecular, que me foi suscitando cada vez mais interesse ao longo da minha vida académica.
Em terceiro lugar agradeço à Dra. Sílvia Carvalho, que me orientou e ensinou no que diz respeito à técnica de titulação por RMN. Obrigado por todos os concelhos e ensinamentos dados em relação a uma metodologia que desconhecia totalmente em termos práticos.
Agradeço à Dra. Helena Gaspar e à Prof. Maria José Brito por toda a ajuda que me deram durante o desenvolvimento do meu trabalho de mestrado no que diz respeito à parte de RMN.
Agradeço a todos os colaboradores e intervenientes que direta ou indiretamente fizeram com que este trabalho fosse possível ser realizado nomeadamente ao grupo do Prof. Phil Gale pelos testes de transporte realizados no seu grupo em Sidney.
Um grande obrigado aos meus pais por todo o apoio emocional e financeiro que me deram para poder realizar este mestrado em química o melhor possível. Por fim e não menos importante um especial e carinhoso obrigado à minha namorada Patrícia por toda a paciência, e compreensão dada, quando partilhei momentos bons e maus do trabalho que desenvolvi.
4
Resumo
Esta tese de mestrado insere-se no campo da química supramolecular, no âmbito do projeto P2020 PTDC/QEQ-SUP/4283/2014, designadamente na síntese de recetores neutros com unidades ureias e tioureias para o reconhecimento e transporte de aniões com interesse biológico.
No capítulo 1 é efetuada uma revisão bibliográfica dos desenvolvimentos recentes na síntese de moléculas com propriedades de reconhecimento e transporte aniónico através das membranas fosfolipídicas. A revisão centra-se nos trabalhos de três grupos de investigação, R. Quesada, A. Davis e P. Gale, tentando mostrar abordagens diferentes em relação à construção de recetores do tipo (tio)ureia capazes de transportar e reconhecer aniões. R. Quesada e A. Davis utilizam estruturas baseadas em produtos naturais, com plataformas do tipo alcaloides e esteroide respetivamente, enquanto que P. Gale constrói recetores a partir de pequenas moléculas aromáticas (e.g. 1,2-fenilenodiamina) e/ou alifáticas ligadas por unidades (tio)ureias.
No segundo capítulo é apresentada a síntese de treze novos recetores com estruturas centrais de 1,2-fenilnodiamina e 4,5-difluoro-1,2-fenilenodiamina, com unidades ureia e correspondente tioureia ligados a diferentes grupos aromáticos de reconhecimento aniónico, como tiofeno, furano, oxadiazole e benzeno substituído. A síntese de moléculas com grupos ureia e tioureia deve-se à possibilidade de ocorrência de interações por ligações de hidrogénio com os aniões preteridos, como por exemplo o anião cloreto. A síntese dos recetores com grupos ureia e tioureia correspondente foram efetuadas usando metodologias com um ou dois passos reacionais e reagentes, como (tio)isocianatos e aminas, de custo reduzido. Ambos os recetores contêm na sua estrutura diferentes tipos de anéis aromáticos nomeadamente anéis de tiofeno furano, oxadiazole e benzénicos. Os recetores foram caracterizados através de técnicas espectroscópicas de IV, RMN (1D e 2D), ESI-MS.
No capítulo 3, é avaliada as propriedades de reconhecimento aniónico dos recetores com os iões halogeneto (fluoreto, cloreto, brometo e iodeto) e com os oxoaniões nitrato e hidrogenocarbonato. As propriedades de reconhecimento aniónico foram avaliadas através de titulação de 1H RMN em solução
sendo determinadas para cada par recetor-anião as respetivas constantes de associação, Ka. Através das
constantes conclui-se que os recetores apresentam uma afinidade muito superior para o cloreto relativamente aos outros halogenetos, observando-se inclusivamente desprotonação com o anião fluoreto. Observou-se ainda, que as ureias apresentam constates de associação superiores na interação com o anião cloreto comparativamente às tioureias correspondentes. O recetor diureia (99) com o heterociclos aromáticos tienilos diretamente ligados ao anel central aromático é o que apresenta maior constante de associação, Ka de 58.88 M-1, com o anião cloreto. Em relação aos oxoaniões estudados
observou-se que ocorre uma forte interação do recetor (97) com o anião hidrogenocarbonato (Ka >1200
M-1), contrariamente ao anião nitrato em que não há interação.
No capítulo 4 é apresentada as propriedades de transporte dos recetores relativamente ao cloreto em modelos de membranas fosfolipídicas com elétrodo seletivo para este ião. Os testes em que foi avaliado o efluxo de Cl-/NO3- foram desenvolvidos no laboratório do Prof. P. Gale. Foi possível
observar que a maioria das moléculas não apresentam elevada propriedades de transporte, contudo o recetor (100) apresentam propriedades de transporte de ca. de 70%, seguindo-se o recetor (126) com ca. de 75%.
Nos capítulos finais, 5 e 6 encontram-se as conclusões e os procedimentos experimentais respetivamente, deste trabalho.
Palavras Chave: Reconhecimento de aniões, (Tio)ureias, Titulações por RMN, Química
5
Abstract
This master’s thesis inserts us on the field of supramolecular chemistry, following the project P2020 PTDC/QEQ-SUP/4283/2014, namely the synthesis of neutral anion receptors with urea and thiourea units capable to transport anions with biological interest.
In chapter 1, it was made a bibliographic review following the recent developments made in the area of anion receptors synthesis. This review focus on R. Quesada, A. Davis and P. Gale’s works, trying to show different approaches on the construction of anion receptors with transport activity. R. Quesada and A. Davis utilize structures based on natural products, with alkaloids and sterol platforms respectively, while P. Gale uses small aromatic (1.2-phenylenodiamine-based receptors) or aliphatic molecules linked by (thio)urea units.
The next chapter presents the synthesis of thirteen new 1.2-phenylenodiamine and 4,5-difluoro-1.2-phenylenodiamine-based anion receptors, with urea and correspondent thiourea units connected to different aromatic rings, as thiophene, furan, oxadiazole and substituted benzene. The presence of (thio)urea units permits the occurrence of hydrogen bonds between anions and receptors. To develop these molecules, were used methodologies with one or two synthetic reactional steps and low-cost reagents such as (thio)isocyanates and amines. All receptors were characterized through diverse spectroscopic techniques (IR, NMR, ESI-MS).
In chapter 3, it is evaluated the anion recognition properties of receptors with halides anions (fluorine, chlorine, bromide and iodide) and oxoanions (nitrate and hydrogenocarbonate). This evaluation was made through the 1H NMR titration, being determined for each receptor-anion the
respectively association constant. With the constant values, it was possible to conclude that the synthetized receptors presented a much stronger interaction with chloride anion than other halides, noticing the deprotonation with fluorine. It was also observed that ureas interact better than thioureas with anions. The bisurea (99) with 2-thienyl groups is the receptor that shows the highest Ka value with
chlorine, Ka = 58.88 M-1. About oxoanions, a strong interaction was observed with hydrogenocarbonate,
while there wasn’t one with nitrate.
In chapter 4, it was assessed the chloride anion transport properties in phospholipidic membrane models with chloride selective electrode. The tests in which it was measured the Cl-/NO
3- efflux were
developed on Prof. P. Gale’s lab. It was possible to note that almost all molecules were inactive, although receptor (100) and (126) present 70% and 75%, respectively, chance of efflux activity.
The two last chapters were dedicated to final considerations and experimental procedures.
Keywords: Anion Recognition, (Thio)ureas, 1H NMR titration, Supramolecular Chemistry, Anion
6
Símbolos e Abreviaturas
Símbolos
ºC
Graus Celsiusδ Desvio químico
Δ δ Variação de desvio químico
ΧR Fração molar de recetor
Abreviaturas
C
13C APT Attached Proton Test
CACTI Centro de Apoio Científico-Tecnolóxico á Investigación
ccf Cromatografia em camada fina
CDCl3 Clorofórmio deuterado
CD2Cl2 Diclorometano deuterado
CFTR Cystic Fibrosis Transmembrane Regulator
CH3CN Acetonitrilo
Cl- Anião cloreto
COSY Correlation Spetroscopy
D
d dupleto
DCM Diclorometano
DMSO-d6 Dimetilsulfóxido deuterado
E
eq. equivalentes
ENaC Epithelium Sodium Channel
ESI-MS Electrospray Ionization Mass Spetrometry
7
F
FDA Food and Drugs Administration
FQ Fibrose Quística
H
H0 Concentração de recetor em solução
1H RMN Experiência de protão em ressonância nuclear magnética
h horas
HG Espécie supramolecular recetor-anião (host-guest) HMBC Heteronuclear Multiple-Bond Correlation spectroscopy
HSQC Heteronuclear Single-Quantum Correlation spectroscopy
Hz Hertz
I
IV Infravermelho
J
nJ
C-F Constante de acoplamento C-F a n ligações
nJ
H-F Constante de acoplamento H-F a n ligações
nJ
H-H Constante de acoplamento H-H a n ligações
K
K Kelvin
Ka Constante de associação
L
log(Ka) Logaritmo da constante de associação
M
m multipleto
8 [M] Concentração molar m/z Razão massa/carga MeOH Metanol mg miligramas min minutos mL mililitros mm milimetros mmol milimol N NH’s Ligações Nitrogénio-Hidrogénio nm nanómetros P POPC ppm Fosfatidilcolina partes por milhão
S
s singuleto
sl singuleto largo
T
t tripleto
t.a. temperatura ambiente
TCP 1,1’-Tiocarbonildi-2-(1H)-piridona
THF Tetra-hidrofurano
tren tris(2-aminoetil)amina
U
9
Índice
1. Introdução………. Pag. 1 1.1 Fibrose Quística ………...……….. Pag. 3 1.2 Recetores e transportadores de aniões biologicamente relevantes………. Pag. 6 2. Síntese e caracterização dos recetores de aniões……….. Pag. 17
2.1 Síntese de derivados de 1,2-fenilenodiamina (94)……….. Pag. 20 2.2 Síntese de derivados de 4,5-difluoro-1,2-fenilenodiamina (95)………. Pag. 38 3. Interações recetor-anião: Titulações por RNM……… Pag. 44 3.1 Titulações com o anião cloreto………... Pag. 48 3.2 Titulações com outros halogenetos………. Pag. 54 3.3 Titulações com oxoaniões……….. Pag. 56 3.4 Determinação da estequiometria do complexo supramolecular pelos
diagramas de Job……… Pag. 57 4. Testes de transporte membranar………... Pag. 58 4.1 Técnicas de monitorização do fluxo de aniões………... Pag. 60 4.2 Resultados de transporte de alguns dos recetores sintetizados………... Pag. 61 5. Conclusões……… Pag. 64 6. Parte experimental……… Pag. 68 7. Bibliografia………... Pag. 80 8. Anexos……….. Pag. 84
8.1 Estruturas com duas unidades (tio)ureia baseadas em 1,2-fenilenodiamina e
reportadas na literatura com valores de Ka para o anião cloreto……… Pag. 84 8.2 Estruturas com duas unidades (tio)ureia baseadas em 1,2-fenilenodiamina
desenvolvidas nesta tese com valores de Ka para o anião cloreto.……… Pag. 85 8.3 Espectros de IV, RMN e ESI dos compostos sintetizados.……… Pag. 86 8.4 Curvas de titulação com o anião brometo ………. Pag. 111 8.5 Espetros de 1H RMN adquiridos ao longo da titulação do recetor (97) com o
10
Índice de tabelas
Tabela 1.1 Alguns exemplos de possíveis fármacos corretores e potenciadores em
diferentes fases clínicas………. Pag. 5 Tabela 2.1 Rendimentos das diureias e ditioureias sintetizadas……….. Pag. 21 Tabela 2.2 Valores de 1H RMN dos protões dos derivados (96-104), (124-127)………. Pag. 22
Tabela 2.3 Valores de 13C APT RMN dos carbonos dos derivados (96-104), (124-127)….… Pag. 23
Tabela 2.4 Caracterização dos compostos (114) e (118) através de 1H e 13C APT RMN em
DMSO-d6. Indicação do átomo correspondente, desvio químico, multiplicidade
do sinal e constante de acoplamento……….. Pag. 34 Tabela 2.5 Caracterização do macrociclo (120) através de 1H e 13C APT RMN em
DMSO-d6. Indicação do átomo correspondente, desvio químico, multiplicidade do sinal
e constante de acoplamento………... Pag. 35 Tabela 2.6 Caracterização do isotiocianato (121) através de 1H e 13C APT RMN em CD
2Cl2.
Indicação do átomo correspondente, desvio químico, multiplicidade do sinal e
constante de acoplamento..………..., Pag. 35 Tabela 2.7 Caracterização do isotiocianato (123) através de 1H e 13C APT RMN em
DMSO-d6. Indicação do átomo correspondente, desvio químico, multiplicidade do sinal
e constante de acoplamento……… Pag. 37 Tabela 2.8 Rendimentos dos compostos obtidos a partir da 4,5-difluoro-1,2-fenilenodiamina
(95)………. Pag. 39
Tabela 3.1 Concentrações das soluções de recetor e cloreto utilizadas nas titulações…….... Pag. 48 Tabela 3.2 Valores de constante de associação dos recetores com o anião cloreto em
DMSO-d6………... Pag. 48
Tabela 3.3 Concentrações de fluoreto e recetores (102 e 125) utilizadas na titulação por
RMN em DMSO-d6………... Pag. 54
Tabela 3.4 Concentrações de aniões brometo e recetores (97-98, 102, 124-125, 127)
utilizadas na titulação por RMN em DMSO-d6………. Pag. 55
Tabela 3.5 Concentrações de iões hidrogenocarbonato, nitrato e recetor (97) utilizadas na
titulação por RMN em DMSO-d6……….. Pag. 56
11 Tabela 4.1 Resultados de transporte dos recetores (96-98), (100). (102-104), (124-126)
12
Índice de Figuras
Figura 1.1 Estruturas das bases componentes da dupla hélice de ADN……….. Pag. 3 Figura 1.2 Estruturas moleculares do Ivacaftor e Lumacaftor………. Pag. 4 Figura 1.3 Estrutura química do ataluren (PTC 124)……….. Pag. 5 Figura 1.4 Estrutura genérica de um recetor sintético decorado com unidades (tio)ureia a
interatuar com um anião de geometria esférica………. Pag. 6 Figura 1.5 Representação esquemática do transporte de cloreto por um recetor num modelo
de uma membrana fosfolipídica………... Pag. 7 Figura 1.6 Mecanismos de transporte aniónico……… Pag. 7 Figura 1.7 Exemplos de recetores sintéticos baseados em prodigininas (1-4) e tambjeminas
(5-8)……… Pag. 8
Figura 1.8 Exemplos de recetores de aniões baseados no ácido cólico decorados com grupos (tio)ureia………. Pag. 9 Figura 1.9 Exemplos de recetores aniónicos baseados em decalina com unidades
(tio)ureia……….… Pag. 10 Figura 1.10 Exemplos de recetores de aniões baseados em mono-(tio)ureia……….…... Pag. 11 Figura 1.11 Exemplos de recetores bis(tio)ureia baseados em tren……….…. Pag. 12 Figura 1.12 Exemplos de recetores com core central variado……….….. Pag. 12 Figura 1.13 Exemplos de recetores bis(tio)ureia com core central de 1,2-fenilenodiamina…. Pag. 13 Figura 1.14 Exemplos de recetores com core central de 1,2-fenilenodiamina……….…. Pag. 13 Figura 1.15 Exemplos de recetores de aniões baseados em squaramida………... Pag. 14 Figura 1.16 Mecanismo de transporte on/off das tiosquaramidas reportadas por Gale et
al………..….. Pag. 15
Figura 2.1 Plataformas centrais utilizadas na síntese dos recetores de aniões……… Pag. 19 Figura 2.2 Estrutura geral das moléculas sintetizadas………. Pag. 19 Figura 2.3 Esquema de retrossintese das moléculas sintetizadas……… Pag. 20
13 Figura 2.4 Novas diureias e ditioureias simétricas derivadas de 1,2-fenilenodiamina
(94)………. Pag. 20
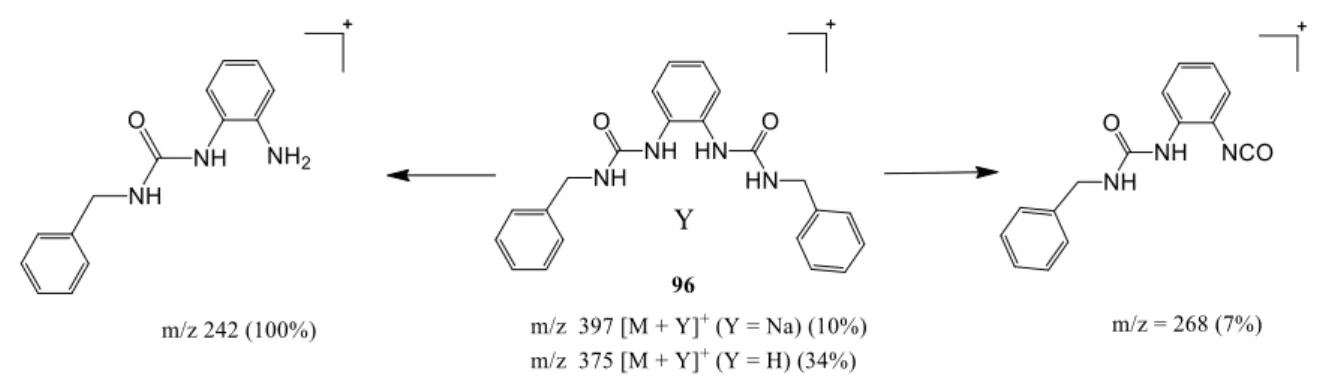
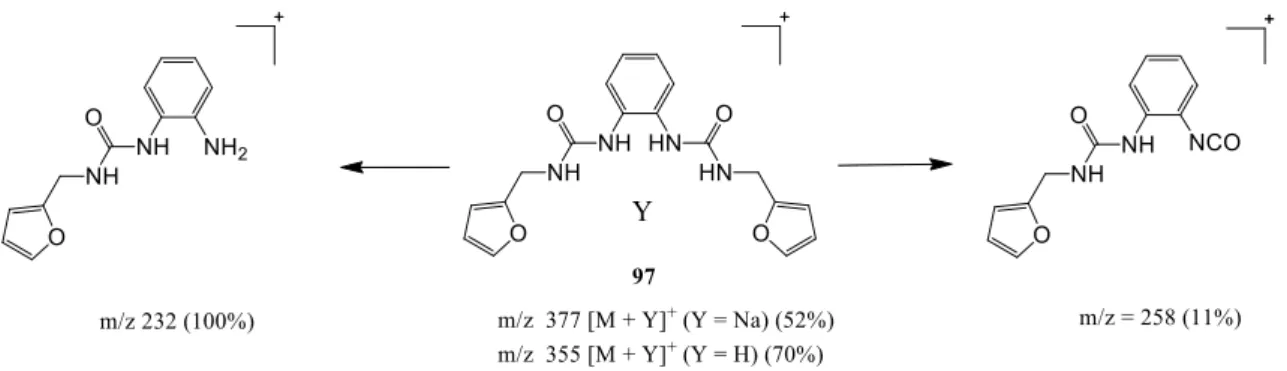
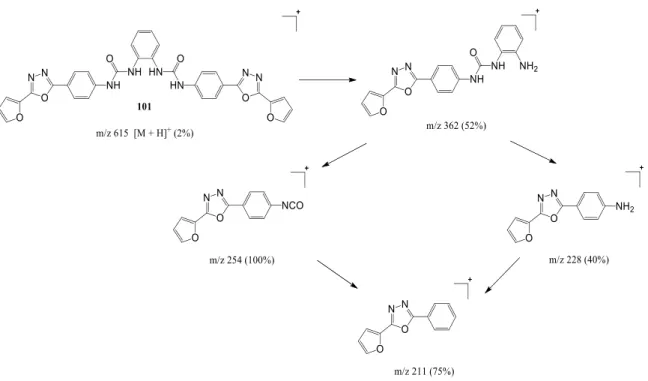
Figura 2.5 Esquema reacional da síntese da diureia (96)………. Pag. 24 Figura 2.6 Proposta de fragmentação da diureia (96) por ESI-MS………. Pag. 25 Figura 2.7 Esquema reacional da síntese da diureia (97)………. Pag. 25 Figura 2.8 Proposta de fragmentação da diureia (97) por ESI-MS………..……… Pag. 26 Figura 2.9 Esquema reacional da síntese da diureia (98)……….……… Pag. 27 Figura 2.10 Esquema reacional da síntese da diureia (99)……….………… Pag. 28 Figura 2.11 Esquema reacional da síntese da diureia (100)……….……….. Pag. 29 Figura 2.12 Esquema reacional da síntese do isocianato (110)………. Pag. 30 Figura 2.13 Esquema reacional da síntese da diureia (101)……….………. Pag. 31 Figura 2.14 Proposta de fragmentação da diureia (101) por ESI-MS……….………... Pag. 32 Figura 2.15 Esquema reacional da síntese da ditioureia (102)……….………. Pag. 32
Figura 2.16 Esquema reacional da síntese do isotiocianato (114)……….…….... Pag. 33 Figura 2.17 Esquema reacional da síntese da ditioureia (117)……….………. Pag. 34 Figura 2.18 Esquema reacional para sintetizar a ditioureia (117)……….……… Pag. 34 Figura 2.19 Esquema reacional da síntese do isotiocianato (121). ……….. Pag. 35 Figura 2.20 Esquema reacional da síntese da ditioureia (103)……….…………. Pag. 36 Figura 2.21 Proposta de fragmentação da ditioureia (103) através de ESI-MS………….…… Pag. 36 Figura 2.22 Esquema reacional da síntese do isotiocianato (123)………. Pag. 36 Figura 2.23 Esquema reacional da síntese da ditioureia (104)……….……. Pag. 37 Figura 2.24 Proposta de fragmentação da ditioureia (104) através de ESI-MS……… Pag. 38 Figura 2.25 Ureias e tioureia derivadas de 4,5-difluoro-1,2-fenilenodiamina (95)…………... Pag. 38 Figura 2.26 Esquema reacional da síntese da diureia (124)……….. Pag. 39
14 Figura 2.27 Proposta de fragmentação da diureia (124) em ESI-MS……… Pag. 40 Figura 2.28 Esquema reacional da síntese da diureia (125)……….. Pag. 40 Figura 2.29 Esquema reacional da síntese da diureia (126)……….. Pag. 41 Figura 2.30 Esquema reacional da síntese da diureia (127)……….. Pag. 42 Figura 2.31 Proposta de estruturas para os fragmentos observados em ESI-MS da diureia
(127)……… Pag. 43
Figura 3.1 Equilíbrio da interação entre substrato (Guest) e recetor (Host)……….... Pag. 46 Figura 3.2 Aniões utilizados nas titulações por RMN………. Pag. 47 Figura 3.3 Espetros de 1H RMN adquiridos ao longo da titulação do recetor (96) com o anião
cloreto………. Pag. 49
Figura 3.4 Curvas de titulação dos recetores (96-99) com o anião cloreto………. Pag. 50 Figura 3.5 Curvas de titulação dos recetores (100-101) com o anião cloreto……….…. Pag. 51 Figura 3.6 Curvas de titulação dos recetores (124-126) com o anião cloreto………..… Pag. 52 Figura 3.7 Curvas de titulação dos recetores (102-104, 127) com o anião cloreto……….…. Pag. 53 Figura 3.8 Espetros de 1H RMN da titulação da ditioureia (102) com o anião fluoreto…….. Pag. 55
Figura 3.9 Curva de titulação do recetor (97) com o anião hidrogenocarbonato………. Pag. 56 Figura 3.10 Gráficos de Job para os recetores (97) e (124) com o anião cloreto………….…. Pag. 57
15
1.Introdução
16 Esta tese insere-se no âmbito da Química Supramolecular, nomeadamente no tema de reconhecimento e transporte aniónico de moléculas orgânicas sintéticas. No século XIX e primeira metade do sec. XX, a química molecular baseada na ligação covalente, desenvolveu-se bastante com a criação de estruturas moleculares cada vez mais complexas, através da quebra e formação de novas ligações covalentes. Devido a isto, áreas como a química orgânica sofreram um profundo desenvolvimento durante esta época. Na segunda metade do sec. XX, mais precisamente em 1978, foi definida uma nova área dentro da química, designada Química Supramolecular. Para o crescimento desta área muito contribuiu o Nobel da Química de 1987, Jean Marie Lehn, que designa a Química Supramolecular como “a área da química que estuda para além da molécula, dedicando-se às entidades
organizadas de maior complexidade que resultam da associação de duas ou mais espécies químicas
ligadas por forças intermoleculares”.[1] A associação de duas ou mais espécies numa entidade
supramolecular pode ocorrer através de forças intermoleculares do tipo: electroestáticas (ião, ião-dipolo e ião-dipolo-ião-dipolo), ligações por pontes de hidrogénio, interações π-π, forças de dispersão, forças induzidas (forças de van der Waals), efeitos hidrofóbicos, solvatofóbicos e ligações de halogénio.[2]
Estas interações estão presentes em diversos sistemas físico-químicos, como materiais semicondutores, e/ou sistemas biológicos como por exemplo, o caso da associação imunológica antigene-anticorpo, leitura, tradução e transcrição do código genético, reconhecimento celular ou transporte membranar e na constituição de estruturas fundamentais há existência da vida como é o caso do ADN, onde moléculas de adenina-timina, citosina-guanina interatuam entre si por ligações de hidrogénio. (Figura 1.1). [1]
Figura 1.1 - Estruturas das bases componentes da dupla hélice de ADN.
Assim, podemos considerar a Química Supramolecular como uma área de domínio científico interdisciplinar, estudando conceitos químicos associados a sistemas físicos-químicos e biológicos complexos que se organizam por meio de forças intermoleculares.
Atualmente, são conhecidas diversas doenças, designadas canalopatias, que estão associadas ao mau funcionamento de canais iónicos presentes no nosso organismo, normalmente devido a mutações genéticas. Estes canais regulam o fluxo de aniões através de estímulos eletroquímicos e interações não covalentes sendo responsáveis pelo equilíbrio de diversos processos biológicos originando patologias graves quando se encontram disfuncionais.
1.1 Fibrose Quística
Uma das canalopatias mais conhecidas, a Fibrose Quística (FQ), é uma doença genética causada pela mutação de um gene na glicoproteína CFTR (cystic fibrosis transmembrane regulator) que desempenha a função de canal iónico.[3] Esta proteína encontra-se nas membranas plasmáticas de
diversos órgãos como os pulmões, o intestino e as células exócrinas, tendo como uma das principais funções manter a homeostasia na superfície das vias respiratórias através do transporte de cloreto, gluconato, hidrogenocarbonato e tiocianato.[4] Ao ocorrer mutação, o gene da CFTR faz com que a
17 hidrogenocarbonato não seja realizado corretamente e o canal ENaC seja regulado adequadamente.[5]
Este mau funcionamento leva a uma reabsorção dos iões sódio na superfície pulmonar e à secreção defeituosa de iões cloreto resultando na formação de muco patogénico espesso e desidratado. Esse muco origina a obstrução das vias respiratórias e consequente colonização das mesmas por colónias de bactérias da espécie Pseudomonas aeruginosa.[5] Com o passar do tempo vão surgindo infeções e
inflamações pulmonares crónicas, resultantes da presença das bactérias nos pulmões, e bronquiectasias fazendo com que ao fim de alguns anos, haja a falência do sistema respiratório e respetiva morte dos doentes.[6-8] Além dos danos a nível do sistema pulmonar existem outros órgãos afetados pela doença,
nomeadamente as glândulas sudoríparas, o pâncreas, a vesicula biliar, o intestino e o trato reprodutivo masculino, ocorrendo, por exemplo, problemas de má absorção a nível intestinal e insuficiência pancreática. Apesar desses órgãos também serem afetados os problemas respiratórios são o principal dano para a saúde dos doentes com fibrose quística provocando a morte em 80% dos casos.[7-9]
Até aos dias de hoje esta doença permanece sem cura, o que tem levado diversos grupos de investigação a nível mundial a unir esforços no entendimento das mutações e da própria doença com o objetivo de desenvolver terapias eficazes para a mesma. Alguns especialistas defendem que o ideal será desenvolver a terapia génica permitindo tratar a fibrose quística em todas as classes de mutações de forma generalizada, enquanto outros defendem que o progresso no tratamento desta doença, só é possível se for feito um acompanhamento e tratamento personalizado a cada doente. Como ambas as terapias se encontram ainda com diversas questões por responder, e “atrasadas” em relação à farmacoterapia, a indústria farmacêutica tem-se dedicado à terapia química como forma de tratamento da FQ. Dentro da farmacoterapia existem algumas abordagens em diferentes fases de desenvolvimento como o desenvolvimento: de anti-inflamatórios eficazes para combater as infeções pulmonares graves,[10] de corretores e potenciadores da CFTR,[10], de ativadores de canais biológicos de cloreto
alternativos,[7,11-12] a criação de canais sintéticos de iões capazes de substituir os canais danificados da
CFTR[13-18] e o desenvolvimento de transportadores sintéticos de iões capazes de mediar o transporte
de iões, mimetizando a CFTR.[19]
As abordagens que se encontram em fase mais avançada são a utilização de moléculas capazes de corrigir as mutações presentes na proteína CFTR ou que, de alguma forma, consigam potenciar o desempenho da proteína que se encontra deficiente nos doentes.
No que diz respeito à recuperação da proteína CFTR, em doentes com fibrose quística, existem no momento duas moléculas, um potenciador e um corretor, que estão a ser utilizadas como terapêutica conjunta. O ivacaftor (potenciador) (Fig. 1.2) tem como função “aumentar” o canal iónico na CFTR potenciando assim, o transporte de iões através da mesma. O lumacaftor (corretor) (Fig.1.2) tem como função corrigir a mutação que impede o tráfego da proteína através da membrana plasmática sendo então designado como um corretor da CFTR. Esta terapia conjunta é muito utilizada em doentes cujas mutações estão agrupadas na classe II podendo ser utilizada em doentes com mutações de outras classes.[7]
18 Além destas duas únicas moléculas enunciadas anteriormente, existem muitos outros potenciadores e corretores em fases clínicas distintas (Tabela 1.1). [7,10]
Tabela 1.1 – Alguns exemplos de possíveis fármacos corretores e potenciadores em diferentes fases clínicas. [10]
Corretores Potenciadores
VRT-325 CTP-656 b)
KM11060 QBW251 a)
VX-661 --- ---
GLPG-2222 --- ---
a) Estruturas químicas não acessíveis. b) Derivado presente patenteado, WO2017053455A1, 30 de Março de 2017
Em conjunto com o ivacaftor e o lumacaftor existiu uma molécula bastante promissora na terapia da fibrose quística, em doentes com mutações da classe I, que foi retirada recentemente do mercado pela FDA devido aos efeitos secundários atribuídos à mesma, permanecendo assim um desafio arranjar uma terapêutica capaz de corrigir as mutações desta classe.[8] Essa molécula é designada genericamente como
ataluren (PTC 124) (Fig. 1.3) e tinha como função corrigir a paragem prematura da síntese da proteína CFTR e consequentemente regenerar a funcionalidade da mesma.[20] Esta molécula contem na sua
estrutura um heterociclo aromático de oxadiazole, aos quais têm sido atribuídos uma vasta atividade biológica.[21]
Figura 1.3 – Estrutura química do ataluren (PTC 124).
Como a FQ, muitas das canalopatias conhecidas são doenças genéticas complexas e a cura das mesmas ainda permanece incerta. A utilização de corretores e potenciadores da CFTR não permite ainda a cura da doença, nem permite um tratamento eficaz sobre todas as classes de mutações continuando a pesquisa e desenvolvimento de alternativas eficazes ao tratamento atual.
É aqui que a Química Supramolecular, tem contribuído para a tentativa de desenvolvimento de pequenas moléculas, assentes em estruturas moleculares capazes de interatuarem com os iões, principalmente o cloreto e o hidrogenocarbonato, transportando-os através das membranas fosfolipídicas, e assim criar uma terapia de substituição dos canais iónicos onde ocorre mutação genética.
19
1.2 Recetores e transportadores de aniões biologicamente relevantes
Nas últimas duas décadas, o desenvolvimento de recetores e transportadores, capazes de interatuar com aniões, formando espécies supramoleculares recetor-anião (host-guest), tem sido cada vez mais estudado. Para tal, muito contribui a vasta aplicabilidade deste tipo de estruturas desde sensores óticos,[22] materiais funcionais,[23] catalisadores[24] além de recetores e transportadores de aniões em
sistemas biológicos.[19] A construção destas estruturas sintéticas está assente nos princípios da Química
Supramolecular, como já referido, sendo a sua construção uma tarefa árdua, mas desafiante. Alguns parâmetros fundamentais na construção destas moléculas são: geometria do ião, rigidez/flexibilidade e tamanho da cavidade do recetor de modo a ocorrer uma maior interação entre o recetor e o anião. Estas estruturas podem ser normalmente desenvolvidas a partir de uma plataforma central, a qual é decorada com grupos funcionais capazes de interatuar com os aniões através de forças intermoleculares. Neste capitulo introdutório apenas serão abordados recetores sintéticos neutros contendo grupos amina, amida e (tio)ureia, capazes de interatuar com aniões através de ligações de hidrogénio (Figura 1.4).
Figura 1.4 – Estrutura genérica de um recetor sintético decorado com unidades (tio)ureia a interatuar com um anião de geometria esférica.
Como já referido, uma das aplicabilidades dos recetores de aniões prende-se com o transporte destas espécies através das membranas fosfolipídicas. No que diz respeito ao transporte de aniões, devido à complexidade da estrutura da membrana, todas as moléculas candidatas a transportadores de aniões têm de possuir características particulares na sua estrutura química. Segundo J. M. Lehn “(…)
uma molécula transportadora deve ser extremamente seletiva, mas não ligar o seu substrato muito fortemente, ser suficientemente flexível para permitir a carga e descarga com velocidades de troca elevadas, e evitar a saturação do transportador, além disso o transportador deve possuir um equilíbrio lipofílico-hidrofílico adequado, de modo a ser rapidamente solúvel numa fase membranar e ao mesmo tempo ser capaz de alcançar a interface e entrar em contacto com a fase aquosa; o transportador não
deverá ser demasiado volumoso para se difundir rapidamente (…)”.[1]
Assim, o design de moléculas transportadoras de aniões torna-se uma tarefa desafiante onde diversos parâmetros têm de estar em equilíbrio de modo a maximizar as propriedades de transporte da molécula. A lipofilia é um dos parâmetros estruturais mais importantes da molécula existindo inclusive diversas evidências disso na literatura onde a lipofilia é relacionada com as propriedades de transporte das moléculas.[25-26]
O transporte mediado por parte destas moléculas sintéticas é “um transporte por difusão
facilitada que consiste na transferência de um substrato através de uma membrana, facilitada por uma
molécula transportadora localizada na mesma”.[1] Esse transporte é constituído por quatro passos:
formação do complexo transportador-substrato; difusão através da fase membranar; libertação do substrato na outra interface da membrana e difusão inversa do transportador livre (Figura 1.5).
20
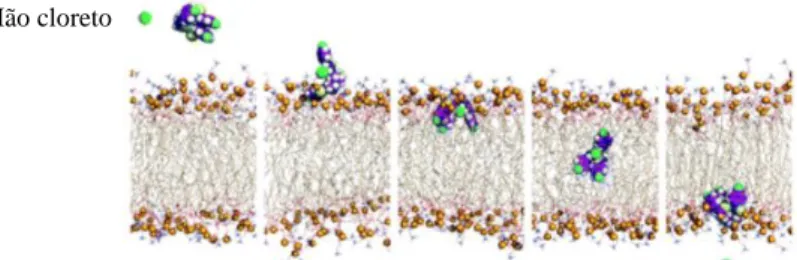
Figura 1.5 – Representação esquemática do transporte de cloreto por um recetor num modelo de uma membrana fosfolipídica. [27]
O transporte por difusão facilitada pode ser realizado de forma normal (uniporte), associado a um fluxo de iões na mesma direção do transporte (simporte) ou em direção oposta (antiporte) (Figura 1.6).
Figura 1.6 – Mecanismos de transporte aniónico. [28]
Como referido anteriormente, o número de exemplos de recetores para reconhecimento e transporte aniónico presente na literatura é vasto.[19,22,29-38] Assim, neste ponto introdutório,
selecionaram-se trabalhos desenvolvidos por grupos relevantes nesta área, nomeadamente os grupos de R. Quesada,[19] A. Davis[39] e P. A. Gale[19] que se têm dedicado a desenvolver, avaliar e a melhorar as
propriedades de reconhecimento e transporte de recetores aniónicos. Teve-se o cuidado de escolher exemplos cujo trabalho focou-se no estudo de reconhecimento e transporte aniónico de aniões biologicamente relevantes nomeadamente o cloreto e o hidrogenocarbonato, aniões esses que se relacionam com a FQ. Fundamentalmente, neste capítulo introdutório são referidos também recetores nos quais a estrutura se assemelha à dos recetores desenvolvidos no âmbito desta tese e que serviram de comparação aos resultados obtidos.
A análise quantitativa da interação recetor-anião (host-guest) processa-se normalmente em solução através de titulação por 1H RMN, UV-vis. e/ou fluorescência. O valor da constante de
associação, Ka, determinada através da titulação, dá a medida da força da interação entre o recetor e o
anião. Em relação às propriedades de transporte aniónico os recetores são testados em modelos de vesiculas de POPC através de métodos de fluorescência ou através de elétrodos seletivos de iões sensíveis à presença do anião em estudo.
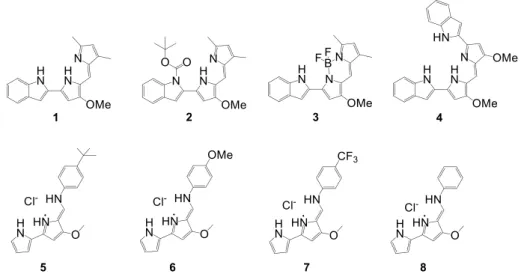
O grupo de R. Quesada tem vindo a desenvolver recetores aniónicos, principalmente para o anião cloreto, baseados em moléculas de origem natural, nomeadamente alcalóides, derivados de prodigininas (1-4)[40-42] e de tambjeminas (5-8)[43] (Fig.1.7).O derivado(1) apresenta afinidade para o
Ião cloreto
Uniporte Simporte Antiporte
21 anião cloreto, com valoresde constante de associação de 42 M-1 e de 96 M-1 para o hidrogenocarbonato
em CDCl3. Os derivados (5-8) apresentam uma maior afinidade para o anião cloreto, com Ka entre 1428
e 1990 M-1, em d6. Mesmo utilizando um solvente mais competitivo, como é o caso do
DMSO-d6 que hidrata facilmente e compete com o anião pelo recetor, a constante de associação é superior nos
recetores (5-8) em relação à do recetor (1) devido aos primeiros recetores terem carga positiva, ou seja adicionalmente à interação por ligação de hidrogénio entre o anião e o recetor existe também uma interação electroestática o que contribui fortemente para que as constantes de associação recetor-anião das moléculas (5-8) sejam mais elevadas. J. F. Davis e J. Sessler et al. também sintetizaram moléculas deste tipo capazes de reconhecer e transportar iões cloreto através das membranas.[44-46] Em relação à
capacidade de transporte das prodigininas e tambjaminas, R. Quesada constatou que os derivados (1, e
6) apresentaram valores de transporte acima de 80%. [41,43]
Figura 1.7 – Exemplos de recetores sintéticos baseados em prodigininas (1-4) e tambjeminas (5-8). [41,43]
Ao contrario de Quesada, A. Davis tem desenvolvido recetores para o anião cloreto, baseados em estruturas de massa molecular elevada, como o ácido cólico (cholapods)[47-54]. Nesta plataforma
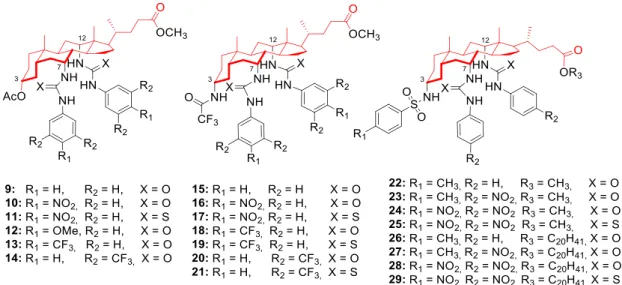
introduziu unidades (tio)ureia nas posições 7 e 12, variando estruturalmente o grupo hidroxilo em posição 3 e o ácido da cadeia terminal (9-29). O grupo hidroxilo em posição 3α foi derivatizado na forma de éster ou amida, entre outros, [47] enquanto que o ácido da cadeia terminal foi esterificado com
22
Figura 1.8 – Exemplos de recetores de aniões baseados no ácido cólico decorados com grupos (tio)ureia. [47-54]
Em termos de interação com aniões, todos os derivados apresentam constantes de associação elevadas para o anião cloreto, sendo estas da ordem de grandeza de 107 a 1011 M-1, em CDCl
3. É de
salientar que estas constantes foram calculadas através de 1H RMN, no entanto a metodologia utilizada
não foi a de titulação.[47-48,51-53] Davis utiliza a metodologia de extração baseada no método de Cram
[48,55] para determinar a força da interação entre o recetor e o anião contrariamente à metodologia de
titulação por 1H RMN utilizada por R. Quesada e P. A Gale. Davis avaliou também a capacidade de
interação de alguns destes cholapods com aniões como o brometo, iodeto, acetato e nitrato.[48] Os
derivados (10, 16, 26-29) apresentam valores de Ka entre 107 M-1 e 1010 M-1 para o anião brometo, no
entanto estes valores são inferiores aos valores de Ka dos mesmos recetores com o anião cloreto. Em
relação ao iodeto os valores de Ka dos mesmos recetores com o anião encontram-se entre 106 M-1 e 109
M-1 sendo estes inferiores aos valores de K
a com o anião brometo e cloreto. No que diz respeito aos
valores de constante de associação dos cholapods (10, 16, 26-29) com os halogenetos, o autor justifica os resultados com base na basicidade dos aniões. Devido aos recetores terem grupos eletroatratores, que possibilitam a retirada de densidade eletrónica dos grupos (tio)ureia, tornando os NH’s destes mais acídicos, a interação do recetor com o anião cloreto vai ser maior, pois este anião apresenta uma basicidade superior à do anião brometo e iodeto. Em relação ao acetato os valores de Ka estão na ordem
dos 108 M-1 a 1011 M-1. Com o anião nitrato foram avaliados os derivados (10-11; 15-16; 26-29)
observando-se valores de Ka na ordem dos 107 M-1 a 1011 M-1.
Ao variar estruturalmente os cholapods na posição 3α, éster, amida ou sulfonamida, Davis tentou estabelecer uma relação “estrutura-atividade”, entre a afinidade do recetor com o anião cloreto e as propriedades de transporte do recetor.[47] Com esta variação, concluiu que não existe uma relação
direta entre as duas propriedades quando o recetor é modificado somente na posição 3α, ao contrario do verificado anteriormente quando variou apenas a estrutura dos cholapods nas posições 7 e 12 em simultâneo.[47] Em relação à afinidade do recetor com o anião o grupo p-nitrofenilsulfonamida é
preferencial para o anião cloreto e nitrato, observando-se valores de Ka superiores aos restantes
derivados enquanto que, a utilização de grupos trifluorometilacetamida na posição 3α melhoraram as propriedades de transporte dos cholapods.[47] Além disso, é de notar que a variação da cadeia terminal
com ésteres de cadeia alifática com diferentes tamanhos provoca na molécula uma variação de lipofilia aumentando a hidrofobicidade da molécula. No entanto, ao variar o tamanho da cadeia alifática não se obteve grande variação nas propriedades de transporte como seria espectável, concluindo-se que o
23 aumento da cadeia neste tipo de compostos não aumenta significativamente as propriedades de transporte, como exemplo comparando os derivados (25) e (29).[47]
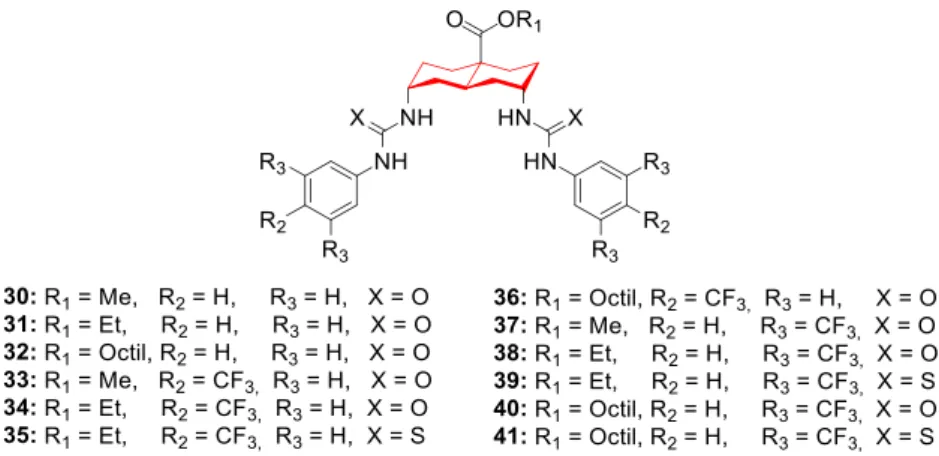
À semelhança dos cholapods, Davis também estudou derivados da decalina (30-41) decorados com unidades (tio)ureia (Figura 1.9).[52-53,56]
Figura 1.9 – Exemplos de recetores aniónicos baseados em decalina com unidades (tio)ureia.[52-53, 58]
Em relação a estes derivados foram determinadas constantes de associação com o anião cloreto através de duas metodologias. Para os derivados (35, 38-41), foram determinadas contantes entre 102
M-1 a 103 M-1 em DMSO-d6 através do método de titulação de 1H RMN[53] e constantes muito superiores,
entre 106 a 109 M-1 para todos os derivados (30-41) em CDCl
3[52-53] através do método de Cram já
referenciado anteriormente para os derivados (9-26).Davis observou que a utilização de substituintes eletroatratores, como anéis substituídos com grupos CF3, torna os NH’s das ureias mais acídicas
potenciando a interação entre o recetor e o anião. Além do anião cloreto, os derivados (32, 35-38) também foram avaliados em relação à sua interação com o anião nitrato observando-se contantes de associação entre 107 M-1 a 108 M-1 em CDCl
3 através do método de Cram.[53]
Nos derivados de decalina, Davis foi constatando que o aumento da cadeia alifática aumenta significativamente as propriedades de transporte das decalinas contrariamente ao sucedido com os
cholapods, já referenciados anteriormente.[52] Além de potenciar a interação do recetor com o anião, a
utilização de grupos fluorados, como CF3, aumenta as propriedades de transporte das moléculas em
relação aos derivados estruturalmente semelhantes que não contêm esses grupos. Essa conclusão foi retirada através da comparação dos resultados de transporte de moléculas baseados em cholapds
(17-21) em relação aos derivados estruturalmente semelhantes, (derivado (11)), e derivados de decalina (35, 38-41) comparativamente aos derivados (30-32). [53] Adicionalmente, a presença de grupos tioureia em
substituição de grupos ureia provoca um aumento nas propriedades de transporte deste tipo de recetores.[53]
Relacionando os derivados de cholapods e decalina, o autor concluiu que o recetor (38) é o mais seletivo, ou seja, apresenta melhores propriedades de transporte para o anião cloreto o que indica também que a utilização de uma plataforma central mais pequena como é ocaso da decalina em detrimento do ácido cólico é preferencial para otimizar as propriedades de transporte destes recetores.
[53]
Contrariamente a R. Quesada e A. Davis que desenvolveram recetores aniónicos baseados em estruturas naturais e plataformas rígidas de ácido cólico e decalina, P. Gale tem desenvolvido recetores aniónicos com uma ou mais unidades (tio)ureia alifáticas ou aromáticas utilizando plataformas mais ou menos rígidas.
24 Em relação a recetores mais flexíveis, recetores (42-47), com uma unidade (tio)ureia central (Figura 1.10) foram apresentados valores de Ka para o anião cloreto entre 10 M-1 e 96 M-1 em
DMSO-d6. É possível observar que os recetores com grupos ureia (42, 44, e 46) apresentam valores de Ka iguais
ou superiores às correspondentes tioureias (43, 45 e 47). O que sugere existir uma interação mais forte nas moléculas que apresentam na sua estrutura unidades ureia em detrimento de unidades tioureia. Com o anião nitrato não foi observada interação, contudo com o anião hidrogenocarbonato ocorre interação com valores de Ka entre 18 M-1 e 1170 M-1 em DMSO-d6.[57] Em relação às propriedades de transporte
destes recetores os derivados (43), (45) e (47) são os únicos que apresentam propriedades de transporte variando entre os 60 e os 80%.[57] Além das tioureias (42-47) têm sido desenvolvidos outros recetores
com uma unidade central (tio)ureia.[57-59]
Figura 1.10 – Exemplos de recetores de aniões baseados em mono-(tio)ureia. [57]
Gale et al. têm desenvolvido recetores com plataforma central flexível baseados na estrutura tris(2-aminoetil)amina (tren)[60] (48-57), com unidades ureia e tioureia (Figura 1.11). A utilização deste
tipo de estruturas, com um grau de flexibilidade elevado, foi estudada devido a existir evidências na literatura de que este tipo de recetores interatua fortemente com oxoaniões como o sulfato por exemplo,[61] e que era efetivo no transporte de aniões e outros substratos como HCl.[62]
Com este tipo de recetores, Gale concluiu que a presença de grupos com átomos de flúor na estrutura dos recetores em posições especificas é uma das característica estruturalmente importante para o aumento da interação entre os aniões e os recetores. A introdução destes grupos em posição orto ou
para aos grupos (tio)ureia provoca uma maior acidez nos NH’s das (tio)ureias potenciando assim a
interação destes hidrogénios com o anião.[60] Além disso, a introdução destes grupos faz com que as
estruturas dos recetores se tornem mais lipofílicas o que também influencia positivamente as propriedades de transporte dos recetores. Observando os valores de Ka dos recetores (48-57) é possível
observar valores de Ka entre 128 M-1 e 882 M-1 para o anião cloreto, em DMSO-d6. Outros aniões foram
também estudados nomeadamente, sulfato, nitrato e hidrogenocarbonato, não se observando interação para o nitrato, desprotonação do grupo (tio)ureia para o hidrogenocarbonato e uma interação superior a 104 M-1 em todos os recetores para o sulfato em DMSO-d6.[60]
Em relação às propriedades de transporte, estes derivados apresentam valores elevados à exceção do derivado (49). À semelhança de outro tipo de recetores, os derivados de tren com grupos tioureias e grupos fluorados apresentam valores de transporte superior aos restantes recetores estruturalmente semelhantes, estando estas conclusões concordantes com o trabalho de Davis referente aos cholapods [47-54] e derivados de decalina [52-53, 56] já mencionados.
Durante a avaliação das propriedades de transporte deste tipo de recetores o autor refere que este tipo de moléculas realiza o transporte de cloreto através de um mecanismo de troca do tipo antiporte dependendo fortemente das características do anião que troca com o anião cloreto afirmando o transporte ser mais eficiente quando existe uma troca Cl-/NO
25
Figura 1.11 – Exemplos de recetores bis(tio)ureia baseados em tren. [60]
Utilizando uma estrutura central semi-rígida Gale reportou um conjunto de 1,3-bis-metilureias baseadas em 1,3-bismetilaminobenzeno e 1,3-bismetilaminopiridina (Figura 1.12). Ao introduzir grupos metileno entre a plataforma central e o grupo ureia o recetor adquire uma certa flexibilidade fazendo com que este seja capaz de se reorganizar em solução e na presença do anião. Para estes derivados o autor reporta constantes de associação para o anião cloreto entre 32 M-1 e 229 M-1 enquanto que os
valores da constante para o anião hidrogenocarbonato variam entre 124 M-1 e 793 M-1. Em relação ao
ião nitrato não é observado qualquer tipo de interação entre o recetor e o anião. Além destes aniões os derivados foram estudados com os aniões acetato, benzoato, fluoreto e hidrogenofosfato observando-se uma interação superior com o anião sulfato (Ka > 104).[63]
Figura 1.12 – Exemplos de recetores com core central variado. [63]
Os derivados (61-63) apresentam propriedades de transporte acima de 50% com o anião cloreto, contudo apenas o derivado (63) apresenta propriedades de transporte de 90%. Os restantes derivados
(58-60) não apresentam propriedades de transporte significativas.[63]
No que diz respeito aos derivados com uma plataforma rígida central, Gale reportou os recetores da figura 1.13 (64-74) onde a molécula de 1,2-fenilenodiamina foi utilizada como plataforma central sendo decorada com duas unidades (tioureia) e os recetores da figura 1.14 (75-83) onde a cavidade central do recetor foi aumentada tendo sido utilizada uma plataforma central baseada em anéis de 1,2-fenilenodiamina com uma unidade ureia central, decorada com unidades ureia.[64-69] A mesma
plataforma central foi utilizada para desenvolver recetores com outros grupos funcionais (84-85) capazes de interatuar com os aniões como grupos amida e amina.
A utilização de grupos e átomos eletroatratores como trifluorometilo e flúor, na estrutura dos recetores, está de acordo com as conclusões retiradas pelo autor durante o estudo dos derivados baseados no tren onde constata que a utilização destes grupos melhora as propriedades de reconhecimento e transporte aniónico.[60] Estes recetores foram estudados com os aniões cloreto, nitrato e
hidrogenocarbonato em DMSO-d6. Para além dos aniões acima citados somente os recetores (64,
26
Figura 1.13 – Exemplos de recetores bis(tio)ureia com core central de 1,2-fenilenodiamina. [64-69]
Figura 1.14 – Exemplos de recetores com core central de 1,2-fenilenodiamina. [65,69]
A interação entre os recetores (64-74) e o anião cloreto foi avaliada através de titulação por 1H
RMN tendo sido obtidos valores de Ka, inferiores a 100 M-1, em DMSO-d6,enquanto que para o anião
hidrogenocarbonato, foram observados valores de Ka entre 836 M-1 e 7330 M-1. Em relação ao ião nitrato
não ocorreram interações significativas com este tipo de derivados.[66-67]
No caso dos recetores (75-79) em que o core central é constituído por um grupo ureia ligado a duas unidades de 1,2-fenilenodiamina os valores de Ka, para o anião cloreto, são da mesma ordem de
grandeza dos derivados anteriores, contudo os derivados (80-83) apresentam uma interação mais forte refletindo-se em valores bastante mais elevados nas constantes de associação. Embora a cavidade dos recetores seja consideravelmente maior em relação aos derivados (64-74), e se esperasse uma interação inferior com o anião cloreto devido ao seu tamanho, o facto de existirem seis NH’s a interatuarem com o anião pode ser justificativo de a interação recetor anião ter aumentado em comparação com os derivados (64-74). Com o anião hidrogenocarbonato são observados valores de Ka entre 203 M-1 e 802
M-1 para os derivados (75-83), valores estes que são inferiores aos observados para os derivados
(64-74). Para o anião nitrato não é observada qualquer interação com todos os recetores.[69]
A interação de recetores com unidades amida (84) e amida-amina (85) foi comparada com recetores com unidades ureia estruturalmente semelhantes (recetor 64) e já referido anteriormente.[65]
Ao comparar estes recetores. Gale comprovou que a utilização de recetores com grupos amida e/ou amina relativamente aos grupos ureia reduz o valor da constante de associação com o anião cloreto, devido à existência de menos locais de interação através de ligações de hidrogénio.
27 Em conjunto com o estudo de reconhecimento aniónico, Gale et al. apresenta também para alguns dos recetores as propriedades de transporte essencialmente com cloreto e hidrogenocarbonato. De um modo geral, os derivados de 1,2-fenilenodiamina (64-74) apresentaram propriedades de transporte acima dos 50%, à exceção do recetor (64) que é praticamente inativo.[66-67] Além da avaliação
da capacidade de transporte de cloreto alguns destes derivados foram também testados em relação ás suas propriedades de transporte para os ácidos fumárico e maleico (carboxilatos presentes no ciclo de krebs).[66] Quando a cavidade do recetor é aumentada substancialmente as propriedades de transporte
variam com maior amplitude. Os derivados (76-79) apresentam valores de transporte elevado (ca. de 100%), enquanto os restantes derivados (75, 80-83) apresentam valores inferiores (< que 50%). Ao comparar os recetores (66, 68) e (77, 79) conclui que o aumento da cavidade não provoca uma variação significativa em termos de transporte transmembranar mantendo-se este elevado. Em relação aos recetores com valores de transporte inferiores (75, 80-83) não existe referências na literatura de derivados do tipo das indicadas na figura 1.13, impossibilitando a comparação do efeito provocado pelo aumento da cavidade nestes recetores em concreto. No entanto, é possível concluir através da comparação dos recetores (77-81) que a utilização de substituintes como o OCH3 e CH3, reduz as
propriedades de transporte dos recetores em relação a grupos eletroatratores como já constatado anteriormente em diversos casos.
Por fim Gale tem desenvolvido derivados do tipo squaramida avaliando as propriedades de reconhecimento e transporte aniónico de moléculas do tipo squaramida[70-71] (Figura. 1.15).Em relação
a estes derivados foram reportados valores de Ka para ao anião cloreto entre 60 M-1 e 643 M-1 em
DMSO-d6. [71]
Figura 1.15 – Exemplos de recetores de aniões baseados em squaramida. [71]
Em relação às propriedades de transporte das (tio)squaramidas foi reportado que as tiosquaramidas apresentam melhores propriedades de transporte de cloreto do que as squaramidas com grupos ureia, estando assim os resultados concordantes com as conclusões retiradas noutros estudos semelhantes com outros recetores já referenciados.[60] Além disso verificou-se que o mecanismo de
transporte deste tipo de moléculas é o mecanismo antiporte havendo uma troca Cl-/NO
3- a nível da
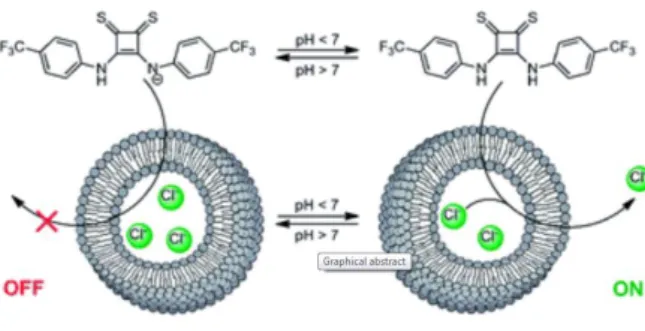
membrana fosfolipídica. Adicionalmente verificou-se que, neste tipo de moléculas as tiosquaramidas têm propriedades de transporte sensíveis ao pH do meio, constatando-se que a pH inferior a 7 as suas propriedades de transporte são consideravelmente superiores. Tal facto, deve-se ao pKa das moléculas
em questão, sendo que a pH superior a 7 a maioria das mesmas encontra-se na forma desprotonada o que faz com que o transporte de cloreto seja dificultado, havendo assim uma repulsão de cargas negativas a dificultar o transporte do anião. A pH inferior a 7 as tiosquaramidas encontram-se na sua forma neutra o que facilita o transporte de cloreto através das membranas pois a repulsão de cargas entre anião e recetor é mínima ou nula.[71]
28
Figura 1.16 – Mecanismo de transporte on/off das tiosquaramidas reportadas por Gale et al. [71]
Através dos conceitos da química supramolecular, e tendo como suporte os trabalhos de R. Quesada, A. Davis e P. Gale, no âmbito desta tese pretendeu-se desenvolver recetores supramoleculares capazes de transportar iões cloreto através das membranas fosfolipídicas, contribuindo assim para o desenvolvimento de uma possível terapia de substituição dos canais iónicos disfuncionais na FQ que, continua hoje em dia um tema bastante atual como é possível constatar na literatura de 2018.[72-74] Mais
concretamente o trabalho científico desenvolvido para esta tese de mestrado prende-se com a construção de pequenas moléculas baseadas em plataformas de 1,2-fenilenodiamina (94) e 4,5-difluoro-1,2-fenilenodiamina (95), decoradas com anéis heteroaromáticos e unidades (tio)ureia para posterior avaliação da sua interação com aniões de interesse biológico. Os recetores sintetizados estão a ser testados em modelos de vesiculas de membranas fosfolipídicas, de modo a averiguar as suas propriedades de transporte com o anião cloreto.
29
2. Síntese e caracterização
dos recetores
30 Este segundo capítulo, contempla a apresentação das vias sintéticas utilizadas para a obtenção de recetores neutros com unidades (tio)ureia com afinidade para aniões biologicamente relevantes.
As moléculas sintetizadas possuem uma estrutura central rígida baseadas em unidades de 1,2-fenilenodiamina (94) e 4,5-difluoro-1,2-1,2-fenilenodiamina (95), (Figura 2.1). Sabe-se que, a presença de grupos eletroatractores no anel benzénico, em posição para aos grupos amina provoca alterações nas propriedades de reconhecimento aniónico dos recetores. [60] Deste modo, a escolha da diamina (95) vai
permitir averiguar o efeito que os átomos de flúor vão provocar nos recetores desta série comparativamente aos derivados da série de 1,2-fenilenodiamina (94).
Figura 2.1 – Plataformas centrais utilizadas na síntese dos recetores de aniões.
As plataformas centrais (94) e (95) foram ligadas através de unidades ureia ou tioureia a diferentes substituintes R1 (Figura 2.2) entre eles, anéis aromáticos substituídos ou anéis
heteroaromáticos distintos. A existência de grupos (tio)ureia possibilita a formação de ligações de hidrogénio entre o recetor e os aniões através das ligações N-H destes grupos. A utilização de diferentes substituintes R1 permitiu estudar, não somente o efeito da variação estrutural, como a influência da
aromaticidade dos substituintes nos grupos (tio)ureia do recetor, e assim concluir qual o efeito destas alterações estruturais na interação destes recetores com os aniões. Através da medição da força da interação recetor-anião foi possível observar se estes recetores são seletivos para o anião cloreto em relação à série dos halogenetos. Essa avaliação será descrita no capítulo 3.
Figura 2.2 – Estrutura geral das moléculas sintetizadas.
Por retrossíntese das diureias (X = O) ou ditioureias (X = S) simétricas da figura 2.2 resultam as diaminas (94) e (95) e os respetivos isocianatos ou tiocianatos (Figura 2.3). As diaminas e os iso(tio)cianatos foram adquiridos na sua maioria comercialmente, com exceção de alguns iso(tio)cianatos que não existiam e que tiveram de ser sintetizados. Quando necessário para obter os isocianatos procedeu-se à reação das aminas substituídas em R1 com o reagente trifosgénio, enquanto
que na síntese de isotiocianatos foram utilizadas aminas substituídas e o agente oxidante, 1,1-tiocarbonildi-2-(1H)-piridona (TCP). Assim, utilizando uma metodologia rápida e simples, com um ou dois passos reacionais, obtiveram-se os recetores pretendidos a partir de reagentes de baixo custo.
31
Figura 2.3 – Esquema de retrossintese das moléculas sintetizadas.
2.1 Síntese de derivados de 1,2-fenilenodiamina (94)
Inicialmente foram sintetizadas seis ureias (96-101), e três tioureias (102-104) derivadas da 1,2-fenilenodiamina (94) decoradas com grupos: benzilo, 2-furfurilo, 2-tienilmetilo, 2-tienilo e arilo (Figura 2.4). Na literatura encontram-se descritos recetores com esta plataforma rígida ligados através de (tio)ureias a anéis benzénicos substituídos em diferentes posições com substituintes eletroactatores (capítulo 1, pag.12). [66-67] Os derivados de 1,2-fenilenodiamina (94) sintetizados (Figura 2.4) inovam na
introdução de diferentes sistemas aromáticos (heterociclos aromáticos de furano e tiofeno) e novos substituintes em posição para do anel benzénico (flúor, oxadiazole e furano). A introdução de sistemas aromáticos como benzilo, fufurilo, 2-tienilmetilo e 2-tienilo permite avaliar o efeito que esta variação estrutural provoca na acidez dos hidrogénios dos grupos (tio) ureia e consequentemente nas propriedades de reconhecimento aniónico. A introdução de novos substituintes em posição para no grupo fenilo, em relação ao já referido na literatura, possibilitou estudar também o efeito da presença de sistemas aromáticos conjugados com o anel aromático, como o oxadiazole e o furano, avaliando também o impacto na acidez dos NH’s dos grupos (tio)ureia e consequentemente no reconhecimento aniónico.
32 De um modo geral, as diureias foram obtidas por reação da 1,2-fenilenodiamina (94) com os isocianatos respetivos à temperatura de 0 ºC, durante uma a quatro horas, dependendo do isocianato utilizado. Após induzir a precipitação dos produtos estes foram filtrados obtendo-se assim as diureias com rendimentos variados (Tabela 2.1). Em relação às ditioureias, embora a adição dos isotiocianatos à 1,2-fenilenodiamina (94) tivesse sido também efetuada à temperatura de 0 ºC, foi necessário pelo menos 24h de reação à temperatura ambiente para a formação total das ditioureias. Pelo facto de estas não precipitarem, as ditioureias só se obtiveram após a evaporação do solvente e posterior precipitação com um solvente adequado (tabela 2.1).
Todos os derivados diureias e ditioureias foram caraterizados por IV, RMN (experiências 1D e 2D) em DMSO-d6 (Tabelas 2.2 e 2.3) e por espetrometria de massa (ESI-MS).
Tabela 2.1 Rendimentos das diureias e ditioureias sintetizadas.
Composto Rendimento (%) 96 85 97 61 98 52 99 95 100 53 101 28 102 60 103 35 104 39
33 Tab ela 2.2 – V alo re s d e 1 H R MN d os pro tõ es d os d eri vado s (96 -104) , (124 -127) . 1 H R M N δ (p pm) Á to mo C omp ost o (9 6) (9 7) (9 8) (9 9) (1 00 ) (1 01 ) (1 02 ) (1 03 ) (1 04 ) (1 24 ) (1 25 ) (1 26 ) (1 27 ) 1 ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- 2 7,5 3-7 ,5 0 (m, 2H ) 7,5 2-7 ,4 9 (m, 2H ,) 7,5 2-7, 50 (m, 2H ) 7,6 2-7 ,5 9 (m, 2H ) 7,5 8-7 ,5 6 (m, 2H ) 7,4 8 ( d, 3 J H -H = 7, 4 H z, 2 H ) 7,5 0-7 ,4 3 (m, 2H ) 7,5 5-7 ,5 3 (m, 2H ) 7,5 7-7 ,5 5 (m, 2H ) 7,6 4-7 ,5 8 (m, 2H ) 7,5 9 ( t, 3 J H -F = 10 ,7 H z, 2 H ) 7,7 3 ( t, 3 J H -F = 10 ,5 H z 2 H ) 7,7 0 (sl , 2 H ) 3 6,9 9-6 ,9 7 (m, 2H ) 6,9 8-6 ,9 6 (m, 2H ) 7,0 0-6 ,9 8 (m, 4H ) 7,1 2-7 ,1 0 (m, 2H ) 7,1 3-7 ,0 7 (m, 2H ) 7,2 3 ( d, 3 J H -H = 7, 4 H z, 2 H ) 7,2 2-7 ,1 9 (m, 2H ) 7,3 1-7 ,2 8 (m, 2H ) 7,3 2-7, 30 (m, 2H ) --- --- ---- --- 4 7,9 1 (s, 2H ) 7,8 4 (s, 2H ) 7, 90 (s, 2H ) 8,1 0 (s, 2H ) 8,0 5 (s, 2H ) 9,2 6 (s, 2H ) 9,0 6 (s, 2H ) 9,4 8 (s, 2H ) 9,4 8 (s, 2H ) 7,9 2 (s, 2H ) 7,9 7 (s, 2H ) 8,1 9 (s, 2H ) 9,0 4 (s, 2H ) 5 ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- 6 7,0 2 ( t, 3 J H -H = 5,9 H z, 2 H ) 6,9 4 ( t, 3 J H -H = 5,6 H z, 2 H ) 7,0 8 ( t, 3 J H -H = 5,8 H z, 2 H ) 10 ,0 4 (s, 2H ) 9,1 2 (s, 2H ) 10 ,0 9 (s, 2H ) 8,2 1 (sl , 2 H ) 10 ,3 9 (s, 2H ) 10 ,4 1 (s, 2H ) 7,0 3 ( t, 3 J H -H = 5,5 H z, 2 H ) 7,1 5 ( t, 3 J H -H = 5,8 H z, 2 H ) 10 ,0 9 (s, 2H ) 8,4 6 (s, 2H ) 7 4,2 9 ( d, 3 J H -H = 5 ,9 H z, 4 H ) 4,2 7 ( d, 3 J H -H = 5 ,6 H z, 4 H ) 4,4 5 (d , 3 J H -H = 5 ,8 H z, 4 H ) ---- ---- ---- 4, 67 (sl , 4 H ) ---- ---- 4,2 7 ( d, 3 J H -H = 5 ,5 H z, 4 H ) 4,4 2 ( d, 3 J H -H = 5 ,8 H z, 4 H ) ---- 4,6 9 (d , 3 J H -H = 3 ,0 H z, 4 H ) 8 ---- --- ---- ---- 7,4 9-7, 46 (m, 4H ) 7,7 3 ( d, 3 J H -H = 8,3 H z, 4 H ) --- 7,7 8 ( d, 3 J H -H = 8 ,7 H z, 4 H ) 7,7 8 ( d, 3 J H -H = 8 ,7 H z, 4 H ) --- --- --- --- 9 7,3 4-7 ,3 0 (m, 8H ) 6,2 6 ( d, 3 J H -H = 3 ,0 H z, 2 H ) 7,0 0-6 ,9 8 (m, 2H ) 6,8 6-6 ,8 4 (m, 2H ) 7,1 3-7 ,0 7 (m, 4H ) 8,0 1 ( d, 3 J H -H = 8,3 H z, 4 H ) 6,3 2 ( d, 3 J H -H = 2 ,7 H z, 2 H ) 7,9 4 ( d, 3 J H -H = 8 ,7 H z, 4 H ) 7,9 7 (d , 3 J H -H = 8 ,7 H z, 4 H ) 6,2 7 ( d, 3 J H -H = 2 ,9 H z, 2 H ) 6,9 8 ( d, 3 J H -H = 2 ,4 H z, 2 H ) 6, 88 -6 ,8 6 (m, 2H ) 6,3 5 ( d, 3 J H -H = 3 ,0 H z, 2 H ) 10 6, 40 (sl , 2 H ) 6,9 7-6 ,9 5 (m, 2H ) 6,5 4-6 ,5 3 (m, 2H ) ---- ---- 6,4 1 (s, 2H ) ---- ---- 6,3 9 (sl , 2 H ) 6,9 5-6 ,9 3 (m, 2H ) 6,5 6-6 ,5 5 (m, 2H ) 6,4 2 (sl , 2 H ) 11 7,2 6-7 ,2 1 (m, 2H ) 7,5 9 (s, 2H ) 7,3 9 ( d, 3 J H -H = 3 ,9 H z, 2 H ) 6,8 1-6 ,7 9 (m, 2H ) ---- ---- 7, 61 (s, 2H ) --- ---- 7,5 8 (s, 2H ) 7,3 7 ( d, 3 J H -H = 5 ,0 H z 2 H ) 6,8 1-6 ,7 9 (m, 2H ) 7,6 2 (s, 2H ) 12 ---- ---- ---- ---- ---- ---- ---- 9,2 9 (s, 2H ) ---- ---- ---- ---- ---- 13 ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- ---- 14 ---- ---- ---- ---- ---- 7,4 2 (sl , 2 H ) ---- ---- 7,3 9 ( d, 3 J H -H = 3 ,5 H z) ---- ---- ---- ---- 15 ---- ---- ---- ---- ---- 6,8 2 (sl , 2 H ) ---- ---- 6,8 0-6 ,7 9 (m, 2H ) ---- ---- ---- ---- 16 ---- ---- ---- ---- ---- 8,0 8 (sl , 2 H ) ---- ---- 8,0 5 (s, 2H ) ---- ---- ---- ----