Nívia do Nascimento Marques
PARTÍCULAS INTELIGENTES DE POLI (
N
-ISOPROPILACRILAMIDA),
QUITOSANA E POLI (ÁCIDO ACRÍLICO): efeito da temperatura e
do pH sobre suas propriedades em suspensões aquosas
_______________________________________
Dissertação de Mestrado
Natal/RN, julho de 2012
INSTITUTO DE QUÍMICA
PARTÍCULAS INTELIGENTES DE POLI (N-ISOPROPILACRILAMIDA), QUITOSANA
E POLI (ÁCIDO ACRÍLICO): efeito da temperatura e do pH sobre suas propriedades em suspensões aquosas
PARTÍCULAS INTELIGENTES DE POLI (N-ISOPROPILACRILAMIDA), QUITOSANA
E POLI (ÁCIDO ACRÍLICO): efeito da temperatura e do pH sobre suas propriedades em suspensões aquosas
Dissertação apresentada como requisito para obtenção do título de Mestre, pelo Programa de Pós-Graduação em Química da Universidade Federal do Rio Grande do Norte
Orientadora: Profa. Dra. Rosangela de Carvalho Balaban (UFRN)
Co-orientadora: Dra. Ana Maria da Silva Maia (UFRN)
Natal, RN
UFRN / Biblioteca Central Zila Mamede Catalogação da Publicação na Fonte Marques, Nívia do Nascimento.
PARTÍCULAS INTELIGENTES DE POLI (N -ISOPROPILACRILAMIDA), QUITOSANA E POLI (ÁCIDO ACRÍLICO): efeito da temperatura e do pH sobre suas em suspensões aquosas / Nívia do Nascimento Marques. – Natal, RN, 2012.
95 f. : il.
Orientadora: Rosangela de Carvalho Balaban. Co-orientadora: Ana Maria da Silva Maia.
Dissertação (Mestrado) – Universidade Federal do Rio Grande do Norte. Centro de Ciências Exatas e da Terra. Instituto de Química. Programa de Pós-Graduação em Química.
1. Termossensibilidade – Dissertação. 2. pH-sensibilidade – Dissertação. 3. Polissacarídeo – Dissertação. 4. Copolimerização – Dissertação. 5. Estabilidade – Dissertação. 6. Reologia – Dissertação. I. Balaban, Rosangela de Carvalho. II. Maia, Ana Maria da Silva. III. Universidade Federal do Rio Grande do Norte. IV. Título.
Esse estudo descreve a estabilidade e o comportamento reológico de suspensões aquosas de partículas reticuladas sensitivas de poli (N-isopropilacrilamida) (PNIPAM), poli
(N-isopropilacrilamida)-quitosana (PNIPAM-QS) e poli (N-isopropilacrilamida)-quitosana-
poli (ácido acrílico) (PNIPAM-CS-PAA). A obtenção dos materiais foi realizada por polimerização por precipitação, via radicais livres, utilizando persulfato de potássio como iniciador e N,N’-metilenobisacrilamida (MBA) como agente reticulante. A incorporação dos precursores nas partículas reticuladas foi confirmada por análise elementar e espectroscopia na região do infravermelho. A influência de estímulos externos, como pH, temperatura, ou ambos, no comportamento das partículas, foi investigado por medidas reológicas, estabilidade visual e centrifugação analítica. As partículas de PNIPAM-QS apresentaram maior estabilidade em meios ácido e neutro, enquanto que as partículas de PNIPAM-QS-PAA foram mais estáveis em meios neutro e alcalino, tanto abaixo quanto acima da LCST da PNIPAM
(dados de estabilidade). Isso ocorreu devido às diferentes interações interpartículas e entre as partículas e o meio (também evidenciadas pelos dados reológicos), que foi influenciada pelo pH e temperatura do meio. Baseando-se nos resultados obtidos, observou-se que a introdução de polímeros sensíveis ao pH nas partículas reticuladas de poli (N-isopropilacrilamida),
resultou não apenas na síntese de copolímeros reticulados com dupla sensibilidade, mas em partículas passíveis de ajuste de estabilidade, ou seja, que podem sofrer separação de fases mais ou menos rápida, dependendo da aplicação desejada. Dessa forma, é possível adaptar as partículas sintetizadas aos mais diversos meios.
poly (N-isopropylacrylamide) (PNIPAM), poly (N-isopropylacrylamide)-chitosan
(PNIPAM-CS), and poly (N-isopropylacrylamide)-chitosan-poly (acrylic acid) (PNIPAM-CS-PAA)
crosslinked particles sensitive to pH and temperature. These dual-sensitive materials were simply obtained by one-pot method, via free-radical precipitation copolymerization with potassium persulfate, using N,N’-methylenebisacrylamide (MBA) as a crosslinking agent. Incorporation of the precursor materials into the chemical networks was confirmed by elementary analysis and infrared spectroscopy. The influence of external stimuli such as pH and temperature, or both, on particle behavior was investigated through rheological measurements, visual stability tests and analytical centrifugation. The PNIPAM-CS particles showed higher stability in acid and neutral media, whereas PNIPAM-CS-PAA particles were more stable in neutral and alkaline media, both below and above the LCST of poly (N
-isopropylacrylamide) (stability data). This is due to different interparticle interactions, as well as those between the particles and the medium (also evidenced by rheological data), which were also influenced by the pH and temperature of the medium. Based on the results obtained, we found that the introduction of pH-sensitive polymers to crosslinked poly (N
-isopropylacrylamide) particles not only produced dual-sensitive materials, but allowed particle stability to be adjusted, making phase separation faster or slower, depending on the desired application. Thus, it is possible to adapt the material to different media.
Keywords: thermosensibility; pH-sensibility; polysaccharide; copolymerization; stability;
1 INTRODUÇÃO _________________________________________________________ 7
2 OBJETIVOS ____________________________________________________________ 9
2.1 OBJETIVO GERAL ______________________________________________________ 9
2.2 OBJETIVOS ESPECÍFICOS _______________________________________________ 9
3 REVISÃO BIBLIOGRÁFICA _____________________________________________ 10
3.1 POLÍMEROS INTELIGENTES ___________________________________________ 10
3.1.1 Polímeros Sensíveis à Temperatura ______________________________________ 13
3.1.1.1 Poli (N-isopropilacrilamida) (PNIPAM) __________________________________ 17 3.1.1.2 Aplicações _________________________________________________________ 19
3.1.2 Polímeros sensíveis ao pH ______________________________________________ 23
3.1.2.1 Poliácidos __________________________________________________________ 25 3.1.2.2 Polibases ___________________________________________________________ 26
3.1.2.2.1 Quitosana ________________________________________________________ 26
3.1.2.3 Polímeros anfóteros ou esquizofrênicos ___________________________________ 28 3.1.2.4 Aplicações _________________________________________________________ 29
3.2 COMBINAÇÃO DAS PROPRIEDADES pH E TERMORRESPONSIVAS _________ 32
3.3.1 Reologia ____________________________________________________________ 43 3.3.2 Estabilidade _________________________________________________________ 47
3.3.2.1 Centrifugação Analítica _______________________________________________ 47
4 REFERÊNCIAS BIBLIOGRÁFICAS ______________________________________ 54
1 INTRODUÇÃO
O desenvolvimento de partículas responsivas a estímulos tem ganhado considerável notoriedade nos últimos anos (Gil e Hudson, 2004; Motornov, Roiter et al., 2010; Roy,
Cambre et al., 2010; Zhao, Nie et al., 2011), devido à capacidade em alterar as suas
estruturas/propriedades em resposta a pequenas mudanças no meio, como variações no pH (Gil e Hudson, 2004; Yang, Chen et al., 2009; Motornov, Roiter et al., 2010; Roy, Cambre et
al., 2010; Mihai, Stoica et al., 2011; Zhao, Nie et al., 2011), temperatura (Curti, Moura et al.,
2005; Liu, Fraylich et al., 2009; Bao, Li, Leong et al., 2010; Yang, Liang et al., 2011), força
iônica (Zhou, Wang et al., 2006; Li, Lai et al., 2009; Costa, Custõdio et al., 2011; Liu, 2011),
e campos magnéticos e/ou elétricos (Riskin, Basnar et al., 2007; Fernández-Barbero, Suárez
et al., 2009; Huang e Juang, 2011).
Partículas sensíveis à temperatura e ao pH, em particular, têm sido extensivamente investigadas em virtude da sua importância em sistemas químicos e fisiológicos típicos (Taşdelen, Kayaman-Apohan et al., 2004; Aguilar, Elvira et al., 2007; Dimitrov, Trzebicka et al., 2007). As partículas inteligentes mais exploradas são baseadas na termossensibilidade da
poli (N-isopropilacrilamida) (PNIPAM) em água (Thorne, Vine et al., 2011). A PNIPAM
apresenta uma temperatura consoluta inferior (lower critical solution temperature - LCST) em
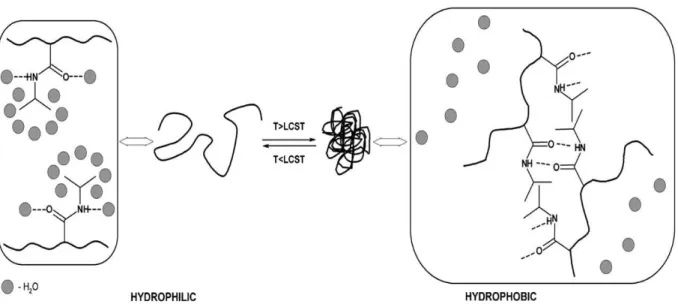
água por volta de 32 °C, em virtude do balanço hidrofílico/hidrofóbico existente em sua estrutura. Isso significa que abaixo da LCST partículas reticuladas intumescem, devido às interações de hidrogênio entre os segmentos hidrofílicos do polímero e a água, enquanto que contraem quando acima da LCST, devido à predominância de interações hidrofóbicas entre os grupos isopropil (Han, Wang et al., 2009; Hamcerencu, Desbrieres et al., 2011; Martins,
Mano et al., 2011). Muitos trabalhos exploram a hidrofobicidade da PNIPAM acima de sua
LCST para incorporar materiais hidrofóbicos, como vários fármacos (Wei, Cheng et al.,
2009). Quando quimicamente reticuladas, essas partículas não são totalmente solúveis, mas podem se manter dispersas no meio (Murray e Snowden, 1995).
Quitosana (QS) e poli (ácido acrílico) (PAA) são polímeros pH-sensitivos comumente empregados para modificar partículas de PNIPAM (Mi Kyong, Yong Kiel et al., 1997;
Schilli, Zhang et al., 2004; Al-Manasir, Zhu et al., 2009; Recillas, Silva et al., 2009; Wang,
Chen et al., 2009; Bao, Li, Leong et al., 2010; Recillas, Silva et al., 2011; Sanoj Rejinold,
Sreerekha et al., 2011) e produzir materiais com dupla sensibilidade. PAA torna-se
possui grupos –NH2 e, dessa forma, torna-se positivamente carregada em meio ácido (pKa
~6,3) (Glampedaki, Petzold et al., 2012). Além disso, a quitosana é um polímero de fonte
natural, derivado da quitina, o segundo polissacarídeo mais abundante da natureza. Essa característica é importante para diversas áreas, principalmente a biomédica (Carreira, Goncalves et al., 2010). Suspensões compostas por essas partículas de dupla sensibilidade
têm sido investigadas para aplicações em diversas áreas, tais como remoção de contaminantes de águas, funcionalização de superfícies, processos de liberação controlada de fármacos (Saitoh, Sugiura et al., 2009; Parasuraman e Serpe, 2011b; a; Saitoh, T., Asano, K. et al.,
2011; Parasuraman, Leung et al., 2012; Saitoh, Asano et al., 2012), entre outras.
Propriedades como morfologia, cinética de intumescimento, capacidade de incorporação e liberação de substâncias, têm sido extensivamente abordadas na literatura (Lee, Wen et al., 2003; Lee, Wen et al., 2004; De Moura, Rubira et al., 2008; Han, Wang et
al., 2009; Hua, Jiang et al., 2011; Mihai, Stoica et al., 2011; Recillas, Silva et al., 2011; Sun,
Shi et al., 2011; Elsaeed, Farag et al., 2012; Hamcerencu, Desbrieres et al., 2012). Outra
característica importante é a estabilização e agregação dessas partículas em diversos meios (Al-Manasir, Zhu et al., 2009). Essas propriedades são de conhecimento fundamental para a
escolha de um material para determinada aplicação (Thorne, Vine et al., 2011) e podem ser
convenientemente investigadas através de medidas reológicas e de sedimentação.
Nesse sentido, foi feita a síntese de partículas reticuladas inteligentes a partir de: N
-isopropilacrilamida (NIPAM) e N,N’-metilenobisacrilamida (MBA); NIPAM, QS e MBA; e
2 OBJETIVOS
2.1 OBJETIVO GERAL
Esta dissertação tem como objetivo principal a obtenção de polímeros com dupla sensibilidade, especificamente ao pH e à temperatura, visando avaliar a estabilização/agregação das partículas obtidas.
2.2 OBJETIVOS ESPECÍFICOS
Obter partículas através da reação de copolimerização por enxertia sobre a quitosana, via radicais livres, com N-isopropilacrilamida ou com N-isopropilacrilamida e ácido acrílico,
utilizando N,N’-metilenobisacrilamida como agente reticulante;
Investigar o comportamento de suspensões aquosas obtidas com as partículas pH e termorresponsivas por: (i) testes de estabilidade visual, (ii) testes de estabilidade acelerada e (iii) análises reológicas;
Avaliar o comportamento em diversos pHs e temperaturas;
3 REVISÃO BIBLIOGRÁFICA
3.1 POLÍMEROS INTELIGENTES
A vida é polimérica em sua essência: alguns dos componentes mais importantes dos organismos vivos são polímeros, como proteínas, carboidratos e ácidos nucleicos, que são utilizados tanto como materiais estruturais quanto como componentes principais na regulação de funções celulares. Uma característica desses biopolímeros funcionais é a resposta não linear a estímulos externos (Galaev e Mattiasson, 1999; Gil e Hudson, 2004; Kumar, Srivastava et al., 2007; Mano, 2008), isto é: pequenas mudanças ocorrem em resposta a um
parâmetro externo que esteja variando até que um ponto crítico seja atingido, quando uma ampla mudança ocorre como resultado de uma pequena variação do parâmetro; após a completa transição, não ocorre mais resposta significativa do sistema. Esse fenômeno é causado por uma grande quantidade de interações cooperativas. Apesar da aparente fragilidade das interações que ocorrem em cada mero da cadeia polimérica, quando somadas a centenas e milhares de unidades, essas interações promovem a força motora para o processo de resposta não linear (Galaev e Mattiasson, 1999; Mano, 2008).
Na tentativa de mimetizar esse comportamento, muitos cientistas têm desenvolvido os chamados polímeros inteligentes (smart polymers or intelligent polymers) (Chaterji, Kwon et
al., 2007; Kumar, Srivastava et al., 2007; Maharjan, Woonton et al., 2008; Wang e Zhou,
2011), que são conhecidos pela capacidade de responder a pequenos estímulos externos de maneira rápida, ampla e reversível (Kumar, Srivastava et al., 2007). Os estímulos podem ser:
físicos, tais como temperatura (Brun-Graeppi, Richard et al., 2010; Pelton, 2010; Beija, Marty
et al., 2011), campo elétrico/magnético (Riskin, Basnar et al., 2007; Fernández-Barbero,
Suárez et al., 2009) e luz (Zhao, 2012); químicos, como pH (Li, Heo et al., 2011; Zhao, Nie et
al., 2011) e força iônica (Zhou, Wang et al., 2006); bioquímicos, como a enzimas específicas
(Ulijn, 2006) e antígenos (Miyata, Asami et al., 1999). Os polímeros inteligentes também são
intitulados como: responsivos (responsive polymers) (Inoue, Noda et al., 2012), sensitivos
(sensitive polymers) (Schwarz, Ponce-Vargas et al., 2012), sensíveis a estímulos (
stimuli-sensitive polymers) (Hamcerencu, Desbrieres et al., 2012), responsivos a estímulos (
stimuli-responsive polymers) (Sá-Lima, Caridade et al., 2010), sensíveis ao meio (environmentally
sensitive polymers) (Seal e Panitch, 2006) ou mesmo responsivos ao meio (environmentally
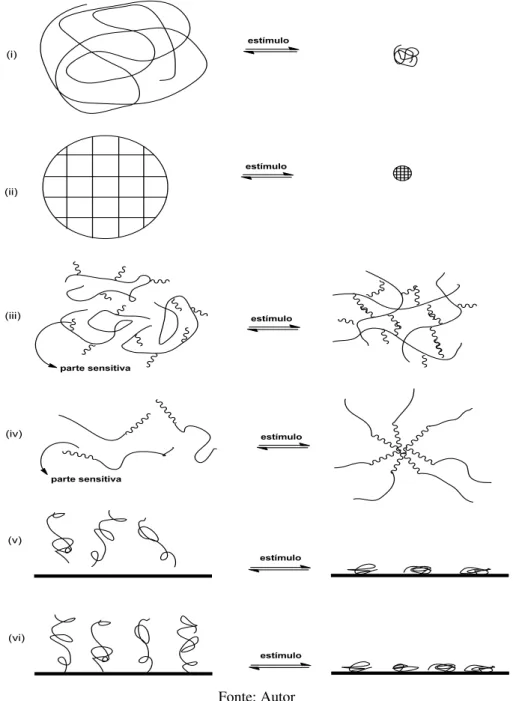
Quanto à forma física (Figura 1), os polímeros sensitivos podem ser classificados como: (i) cadeias em solução, em que o polímero sofre um colapso reversível após um estímulo ser aplicado; (ii) géis reticulados covalentemente, que intumescem ou contraem em resposta a um estímulo; (iii) géis físicos, que se formam reversivelmente, quando o estímulo é aplicado, ou seja, que apresentam uma transição sol-gel (solução-gelificação); (iv) micelas poliméricas, formadas através da agregação de polímeros anfifílicos em bloco ou polímeros modificados terminalmente; (v) cadeias imobilizadas ou (iv) enxertadas em uma superfície, em que os polímeros contraem ou se expandem reversivelmente na superfície, convertendo a interface de hidrofílica para hidrofóbica e vice-versa, quando um parâmetro externo específico é modificado (Gil e Hudson, 2004; Kumar, Srivastava et al., 2007; Maharjan,
Woonton et al., 2008). Ainda, as estruturas micelares podem formar géis físicos reversíveis,
quando acima de uma concentração micelar crítica (concentração micelar de gelificação) (Gil e Hudson, 2004).
Além disso, os polímeros inteligentes, nas mais diversas formas físicas, podem ser conjugados com biomoléculas ou materiais sintéticos, sendo que a atividade do conjugado vai depender da resposta do polímero em relação a um estímulo aplicado (Gil e Hudson, 2004; Kumar, Srivastava et al., 2007).
Em virtude dessas características peculiares, os polímeros sensitivos têm atraído a atenção dos pesquisadores para o estudo e aplicação em diversas áreas, como liberação controlada de fármacos (Ankareddi e Brazel, 2007), separação cromatográfica (Kanazawa, Yamamoto et al., 1996; Maharjan, Woonton et al., 2008), purificação de água (Parasuraman e
Serpe, 2011a), recuperação aumentada de petróleo (Wang, Lu et al., 2011), catálise (Yan,
Zhang et al., 2010), imobilização de enzimas e cultura de células (Nie, He et al., 2012).
Grande parte dessas aplicações utiliza-se do polímero termossensitivo PNIPAM.
Ultimamente, muitos sistemas têm sido desenvolvidos com o intuito de combinar dois ou mais mecanismos de resposta em um único material (Bhattacharya, Eckert et al., 2007; Li,
Xing et al., 2012). Isto porque, através da aplicação simultânea de dois ou mais sinais, são
induzidos diferentes tipos de resposta, o que amplia a aplicabilidade dos materiais sensitivos (Dimitrov, Trzebicka et al., 2007; Kumar, Srivastava et al., 2007). Em particular, existe um
crescente interesse na obtenção de materiais inteligentes nos quais as propriedades em meio aquoso mudem abrupta e reversivelmente em resposta a mudanças simultâneas no pH e na temperatura (Sun, Zhang et al., 2007; Bao, Li, Gan et al., 2010). A combinação das
interesse tecnológico e científico, devido a grande importância dessas variáveis em sistemas químicos e fisiológicos típicos (Taşdelen, Kayaman-Apohan et al., 2004; Medeiros, Santos et
al., 2011).
Figura 1– Ilustração de diferentes formas físicas dos polímeros responsivos: (i) cadeias em solução; (ii) géis reticulados covalentemente; (iii) géis físicos; (iv) micelas poliméricas; (v) cadeias adsorvidas ou (vi) graftizadas
em uma superfície
3.1.1 Polímeros Sensíveis à Temperatura
A sensibilidade à temperatura é uma das características mais interessantes (Wei, Cheng et al., 2009) e a propriedade mais estudada em sistemas poliméricos responsivos
(Maharjan, Woonton et al., 2008). Isto porque a mudança na temperatura é algo simples de
ser controlado e de fácil aplicação em sistemas in vitro e in vivo (Gil e Hudson, 2004; He,
Kim et al., 2008; Brun-Graeppi, Richard et al., 2010; Chen, Ferris et al., 2010).
Quando um polímero é dissolvido em um solvente adequado, ele pode tornar-se insolúvel com o aumento ou a diminuição da temperatura, precipitando da solução (Weber, Hoogenboom et al., 2012). A solubilidade da maioria dos polímeros aumenta quando a
temperatura é elevada (Chaterji, Kwon et al., 2007; Dimitrov, Trzebicka et al., 2007). Quando
a separação de fases ocorre com a diminuição da temperatura, o sistema apresenta uma temperatura consoluta superior (Lucas, Soares et al., 2001) (upper critical solution
temperature – USCT) (Schmaljohann, 2006). Entretanto, alguns polímeros exibem um
comportamento peculiar em solução, no qual uma elevação na temperatura resulta em uma separação de fases, e o sistema exibe uma temperatura consoluta inferior (Lucas, Soares et al.,
2001) (lower critical solution temperature – LSCT) (Dimitrov, Trzebicka et al., 2007; Kumar,
Srivastava et al., 2007; Maharjan, Woonton et al., 2008). Mais precisamente, são formadas
duas fases em equilíbrio, em que uma tem uma alta concentração de polímero e a outra uma baixa concentração de polímero. A LCST representa o ponto mínimo da curva composição
versus temperatura e a UCST o ponto máximo (Figura 2) (Weber, Hoogenboom et al., 2012).
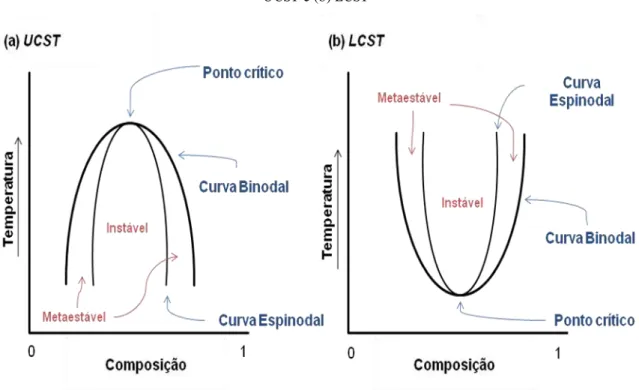
A figura 2 exibe a representação do diagrama de fases para um sistema binário polímero-solvente apresentando UCST ou LCST. A curva binodal separa a região homogênea
da região heterogênea. Na região bifásica, um sistema polímero-solvente apresenta uma separação de fases tipo líquido–líquido, na qual se encontram uma fase líquida rica em polímero (fase gel) e outra fase líquida pobre em polímero (fase sol). A curva espinodal divide a região heterogênea nas regiões instável, localizada dentro da curva espinodal, e metaestável, que fica entre as curvas binodal e a espinodal (Meier, 2004).
(separação lenta), enquanto que na região instável a separação de fases ocorre pelo mecanismo de decomposição espinodal (separação rápida).
A separação de fases por nucleação e crescimento é um processo iniciado com flutuações locais de densidade ou concentração nas soluções poliméricas, formando núcleos de crescimento dispersos na solução. A formação do núcleo é favorecida quando a sua energia superficial livre (responsável pela formação de uma superfície líquida dentro de uma fase homogênea) for maior que a barreira de ativação para sua formação. Já o mecanismo de decomposição espinodal inicia-se, não a partir de um núcleo, mas sim com flutuações deslocalizadas de concentração, com a modulação da composição variando de forma senoidal. As flutuações aumentam nos estágios intermediários e a coalescência das fases ocorre no último estágio. O processo é espontâneo, que não requer energia de ativação e que ocorre com um coeficiente de difusão negativo (Olabisi, Robeson et al., 1979).
Figura 2– Representação de um diagrama de fases para um sistema binário polímero-solvente apresentando (a)
UCST e (b) LCST
Fonte: Adaptado de (Olabisi, Robeson et al., 1979; Kamide, 1990)
Especificamente, a LCST pode ser definida como a temperatura na qual a solução
2007; Bajpai, Shukla et al., 2008; Bajpai, Shukla et al., 2010; Brun-Graeppi, Richard et al.,
2010). Essa transição de fases é reversível, pois quando o estímulo é removido, ou seja, a temperatura é diminuída para um valor inferior à LCST do polímero, o mesmo volta a ser
solúvel no meio (Bajpai, Shukla et al., 2010).
A temperatura consoluta inferior é governada pelo balanço entre as interações hidrofílicas e hidrofóbicas (Eeckman, Moës et al., 2002). Em temperaturas abaixo da
temperatura crítica, em que se tem apenas uma fase, as ligações de hidrogênio formadas entre os segmentos hidrofílicos do polímero e as moléculas de solvente são dominantes, levando, assim, a sua dissolução em água. Com o aumento da temperatura, as ligações de hidrogênio enfraquecem, enquanto que as interações entre os segmentos hidrofóbicos tornam-se mais fortes, levando a uma contração das cadeias (Bajpai, Shukla et al., 2010). Esse
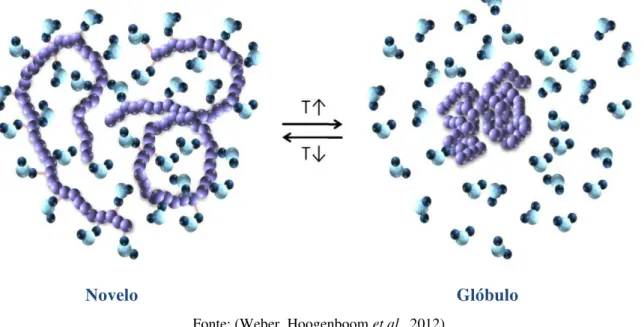
comportamento é ilustrado na Figura 3, em que uma cadeia polimérica em meio aquoso passa de um estado expandido a baixas temperaturas (novelo), para um estado contraído (glóbulo) acima da LCST.
Figura 3– Representação da transição de fases de um polímero linear que apresenta LCST em água
Novelo Glóbulo
Fonte: (Weber, Hoogenboom et al., 2012)
Observando a LCST de um ponto de vista termodinâmico, o processo de solubilização
que ocorram essas interações de hidrogênio é desfavorável (entropia negativa). Dessa forma, a energia livre de dissolução, ΔG, dada por ΔH-TΔS, pode mudar de negativa (solução) para positiva (transição de fases) com o aumento da temperatura (Costa e Freitas, 2002; Vieira, 2006; Dimitrov, Trzebicka et al., 2007; Weber, Hoogenboom et al., 2012).
Uma importante família dos polímeros termorresponsivos com LCST são as
poliacrilamidas N-alquilsubstituídas, tendo como representante principal a poli (N
-isopropilacrilamida) (Gil e Hudson, 2004; Liu, Fraylich et al., 2009; Bajpai, Shukla et al.,
2010; Medeiros, Santos et al., 2011), que será abordada mais detalhadamente no decorrer do
texto. Outros polímeros da família são: poli (N,N-dietilacrilamida) (Gil e Hudson, 2004;
Dimitrov, Trzebicka et al., 2007; Bajpai, Shukla et al., 2010; Medeiros, Santos et al., 2011),
poli (2-carboxiisopropilacrilamida), poli (N-(L)-(1-hidroximetil) propilmetacrilamida), poli
(N-acriloil-N’-propilpiperazina) (Gil e Hudson, 2004), poli (N-etilacrilamida), poli (N,N
-etilmetilacrilamida), poli (N-n-propilacrilamida) (Liu, Fraylich et al., 2009; Medeiros, Santos
et al., 2011), poli (N-etilmetacrilamida), poli (N-metil-N-isopropilacrilamida), poli (N
-isopropilmetacrilamida), poli (N-n-propilmetacrilamida), poli (N-metil-N-n-propilacrilamida),
poli (N-ciclopropilacrilamida), poli (N-ciclopropimetacrilamida) (Medeiros, Santos et al.,
2011), poli (N,N-bis(2-metoxietil) acrilamida), poli (N-(3-metoxipropil)acrilamida), poli
(etoxipropilacrilamida) (Liu, Fraylich et al., 2009) e poli (aminoetoxipropilacrilamida)
(Uğuzdoğan e Kabasakal, 2010).
Polímeros sensíveis à temperatura que não são poliacrilamidas N-alquilsubstituídas,
também têm chamado considerável atenção. Dentre eles, podem ser citados: poli (N
-vinilcaprolactama) (Dimitrov, Trzebicka et al., 2007; Liu, Fraylich et al., 2009; Bajpai,
Shukla et al., 2010), poli (2-etil-2-oxazolina) (Liu, Fraylich et al., 2009), poli (vinil metil éter)
(Dimitrov, Trzebicka et al., 2007; Liu, Fraylich et al., 2009), poli (2-isopropil-2-oxazolina),
poli ((2-dimetilamino) metacrilato de etila), poli (óxido de propileno) (Liu, Fraylich et al.,
2009) e poli (N-acriloilpiperidina) (Medeiros, Santos et al., 2011).
Outro grupo de polímeros que apresentam LCST são macromoléculas de celulose
alquil-substituídas, como metilcelulose, etil(hidroxietil)celulose, e hidroxipropilcelulose, que são potencialmente importantes para aplicação biomédica, já que são polímeros naturais modificados. Esses polímeros podem ser dissolvidos em água a baixas temperaturas por causa da presença de hidroxilas e de éteres nas unidades repetidas (Liu, Fraylich et al., 2009).
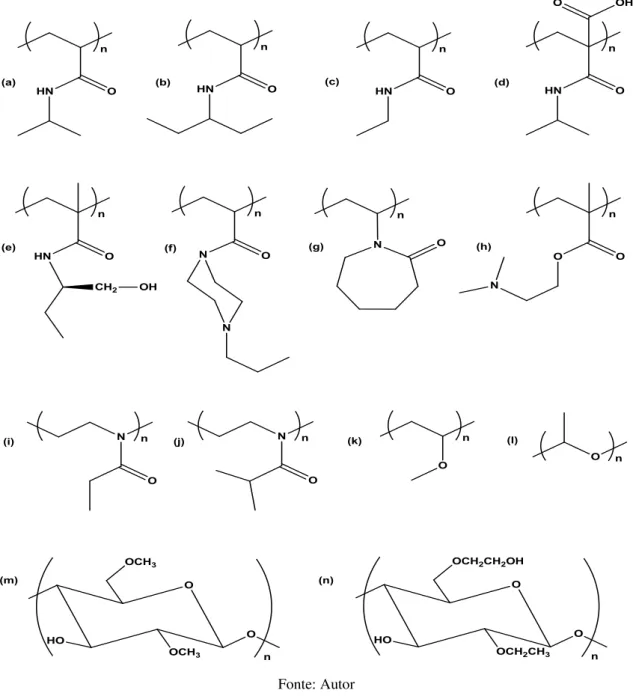
Figura 4– Estrutura química de alguns polímeros termorresponsivos: (a) poli (N-isopropilacrilamida); (b) poli
(N,N-dietilacrilamida); (c) poli (N-etilacrilamida); (d) poli (2-carboxiisopropilacrilamida); (e) poli (N-(L
)-(1-hidroximetil) propilmetacrilamida); (f) poli (N-acriloil-N’-propillpiperazina); (g) poli (N-vinilcaprolactama); (h)
poli ((2-dimetilamino) metacrilato de etila); (i) poli (2-etil-2-oxazolina); (j) poli (2-isopropil-2-oxazolina); (k) poli (vinil metil éter); (l) poli (óxido de propileno); (m) metilcelulose; (n) etil(hidroxietil)celulose
Fonte: Autor
3.1.1.1 Poli (N-isopropilacrilamida) (PNIPAM)
O polímero termossensitivo que tem sido mais extensivamente estudado é a poli (N
-isopropilacrilamida) (PNIPAM) (De Las Heras Alarcón, Pennadam et al., 2005; Dimitrov,
Piantanida et al., 2009; Wei, Cheng et al., 2009; Medeiros, Santos et al., 2011), o qual
apresenta uma temperatura consoluta inferior de aproximadamente 32 °C em água (Sun, Shi
et al., 2011). Abaixo dessa temperatura, as ligações de hidrogênio entre os grupos amida do
polímero e as moléculas de água são dominantes, levando à dissolução em água (Recillas, Silva et al., 2009). Com o aumento da temperatura, as ligações de hidrogênio
polímero-solvente enfraquecem, enquanto que as interações entre os grupos hidrofóbicos isopropil do polímero tornam-se mais fortes, levando a uma contração das cadeias (Al-Manasir, Zhu et al.,
2009; Han, Wang et al., 2009). Acima da LCST, soluções muito diluídas geram agregados
com poucas cadeias de PNIPAM, enquanto que soluções mais concentradas levam a formação de partículas com tamanho coloidal ou precipitados macroscópicos (Pelton, 2010). A Figura 5 ilustra a transição de fase da PNIPAM.
Figura 5– Transição de fase para a poli (N-isopropilacrilamida)
Fonte: (Dimitrov, Trzebicka et al., 2007)
A natureza abrupta e reversível da transição de fase da PNIPAM (Recillas, Silva et al.,
2009), assim como a biocompatibilidade e a proximidade entre os valores da LCST e a
temperatura do corpo humano, têm atraído diversos pesquisadores para o estudo desse polímero termossensitivo (Brun-Graeppi, Richard et al., 2010), principalmente para a
aplicação na área biomédica (Cole, Voelcker et al., 2009).
Além disso, como a LCST é governada pelo balanço entre as interações atrativas
polímero-polímero diminuem a LCST (Liu, Fraylich et al., 2009; Brun-Graeppi, Richard et
al., 2010). Dessa forma, é possível controlar a temperatura de transição por modificação
(copolimerização) com comonômeros hidrofílicos (aumento na LCST) ou hidrofóbicos
(diminuição na LCST).
A LCST depende também da massa molar e da concentração. Foi relatado na literatura
que um aumento no comprimento da cadeia polimérica ou na concentração de polímero leva a uma diminuição da LCST da poli (N-isopropilacrilamida) (Bajpai, Shukla et al., 2010). Com
relação à massa molar, pode-se dizer que quanto menor for a cadeia do polímero, menor o seu caráter hidrofóbico e, dessa forma, maior será a sua LCST. Da mesma forma, quanto menor a concentração de polímero, menor a quantidade de grupos capazes de realizarem associações, o que aumenta a LCST (Durand e Hourdet, 1999). Outra abordagem para modificar a
temperatura de transição de fases da PNIPAM é a presença de sais, tensoativos e co-solventes no meio (Brun-Graeppi, Richard et al., 2010).
3.1.1.2 Aplicações
Existe um crescente interesse em polímeros que apresentam LCST em água devido ao
enorme número de possíveis aplicações (Weber, Hoogenboom et al., 2012). Principalmente
na liberação controlada de fármacos, em que a contração-expansão dos hidrogéis ocorre por causa da LCST, próxima à temperatura do corpo humano (Bajpai, Shukla et al., 2008; He,
Kim et al., 2008; Bajpai, Shukla et al., 2010; An, Zhang et al., 2012). Outras aplicações
incluem: purificação de substâncias, engenharia de tecidos, imobilização de enzimas, cromatografia, recuperação avançada de petróleo.
Em processos de separação cromatográfica, por exemplo, PNIPAM e seus copolímeros têm sido empregados no desenvolvimento de fases estacionárias termorresponsivas para cromatografia por interações hidrofóbicas e interações iônicas, com a utilização de vários materiais como suporte (Maharjan, Woonton et al., 2008). PNIPAM
suportada em sílica foi utilizada como fase estacionária para cromatografia líquida de alta eficiência. Água foi utilizada como única fase móvel para a uma mistura de benzeno com cinco esteróides diferentes. Abaixo da LCST, os solutos não foram bem separados, enquanto
Figura 6– Cromatogramas que mostram a separação de uma mistura de benzeno com 5 esteróides em uma coluna de sílica-PNIPAM, utilizando água como fase móvel, em diferentes temperaturas: (a) 5, (b) 25, (c) 35, e
(d) 50 °C. Picos: (1) benzeno; (2) hidrocortisona; (3) prednisolona; (4) dexametasona; (5) acetato de hidrocortisona; (6) testosterona
Fonte: (Kanazawa, Yamamoto et al., 1996)
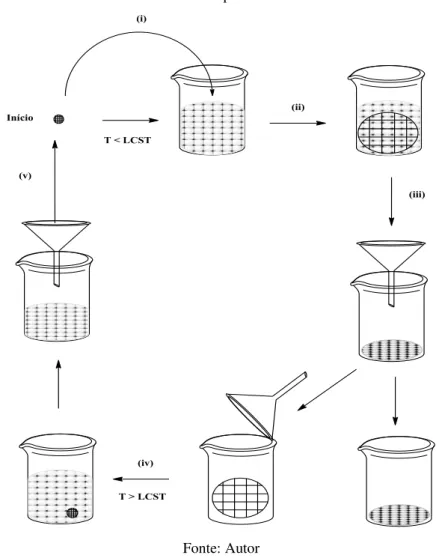
moléculas de pequena massa molar (extrato); (v) esse hidrogel contraído, após ser separado do extrato, está pronto para ser utilizado novamente. Esse processo combina a seletividade dos hidrogéis, devido ao entrelaçamento das moléculas e a densidade das ligações cruzadas, juntamente com sua sensitividade, responsável pela variação abrupta do volume com a temperatura. Uma vantagem desse processo de separação em relação a outros é justamente o fato do gel poder ser reutilizado. Quando se usa materiais para a confecção do gel que não permitem sua restauração, o material utilizado para separação tem que ser descartado após o uso, e desse modo torna os processos inviáveis economicamente (Teixeira, 2005; Silva, 2006).
Figura 7– Ilustração do processo de purificação de macromoléculas através da utilização de macrogéis termorresponsivos
Fonte: Autor
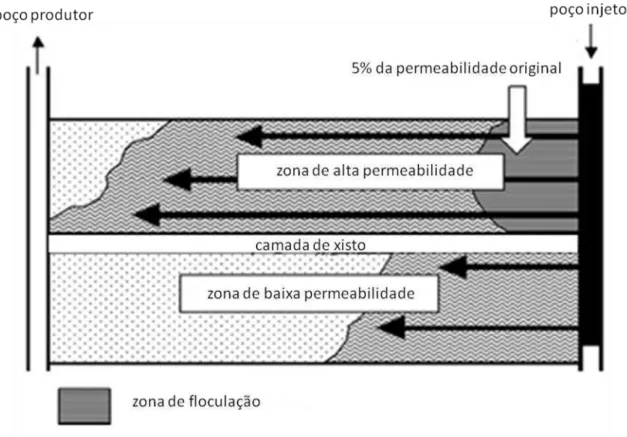
zonas de alta permeabilidade, fazendo com que a água de injeção, de baixa viscosidade, seja forçada a passar por zonas de permeabilidade mais baixa, deslocando até a superfície o óleo viscoso contido nessa zona. O mecanismo de bloqueio se dá pela ativação térmica, já que os reservatórios possuem temperaturas elevadas, promovendo a agregação das partículas. Ao contrário, antes de serem injetados no poço, os microgéis encontram-se dispersos no solvente, já que a temperatura é abaixo da temperatura de transição (Figura 8) (Thorne, Vine et al.,
2011).
Figura 8– Modelo de recuperação aumentada de petróleo pela injeção de microgéis
3.1.2 Polímeros sensíveis ao pH
Para os polímeros inteligentes que são sensíveis ao pH, as interações polímero-polímero e polímero-polímero-solvente experimentam abruptos reajustes devido a pequenas mudanças no pH do meio (Bajpai, Shukla et al., 2008). Isso é atribuído ao fato de que os polímeros
pH-responsivos são polieletrólitos com grupos laterais de bases e/ou ácidos fracos, que recebem ou liberam prótons, respectivamente, em resposta a mudanças no pH do sistema polimérico (Bajpai, Shukla et al., 2010). Isto ocorre porque o grau de ionização de ácidos ou bases fracas
é significativamente alterado em virtude de uma variação no pH, próximo ao valor do pKa
desses grupos. Uma mudança rápida na carga dos grupos pendentes causa uma alteração no volume hidrodinâmico das cadeias dos polímeros (Gil e Hudson, 2004; Chaterji, Kwon et al.,
2007).
Um polieletrólito é uma macromolécula que, quando dissolvida em meio aquoso ou outro solvente ionizante, se ioniza gerando íons. Consequentemente, em virtude da repulsão eletrostática entre as cargas de mesmo sinal presentes nas cadeias poliméricas, a macromolécula se expande. Entretanto, se o solvente não permitir a ionização do polieletrólito, a cadeia solúvel permanece em um estado compacto. Se as cadeias do polieletrólito possuírem caráter hidrofóbico quando não ionizadas, elas colapsam em forma de glóbulos e precipitam da solução aquosa. Já que o grau de ionização de um polieletrólito fraco é controlado através do pH do meio aquoso, os polímeros pH-responsivos mudam abruptamente de conformação em resposta a pequenas mudanças no pH do meio aquoso (Bajpai, Shukla et al., 2008).
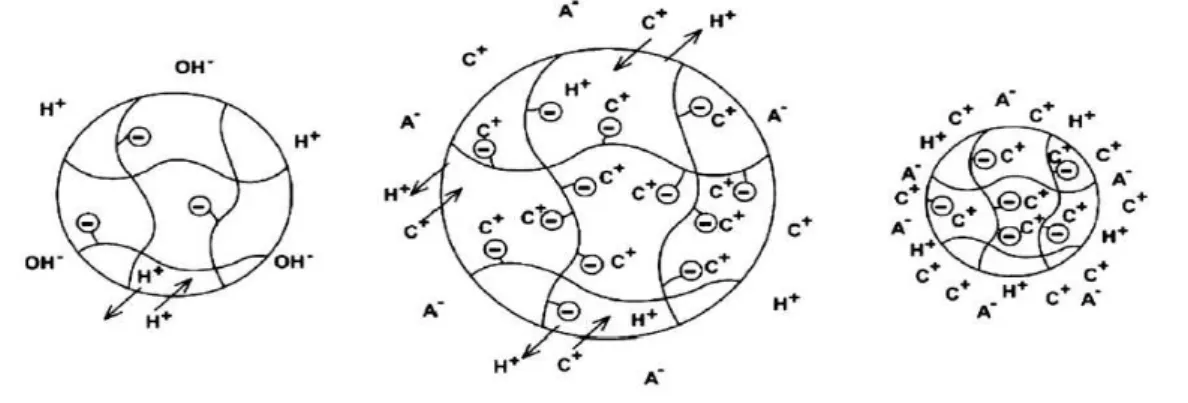
No caso de hidrogéis pH-responsivos que são quimicamente reticulados, o material passa de um estado contraído para intumescido em resposta a uma pequena variação no pH do meio, que depende do grau de ionização dos grupos funcionais de ácidos ou bases fracos. A diferença na concentração de contraíons no interior do hidrogel em relação à solução externa, que varia em função do pH do solvente, gera uma pressão osmótica, a qual governa a mudança no volume e, consequentemente, o processo de contração/intumescimento (Gil e Hudson, 2004). Ainda, é importante salientar que, a extensão do intumescimento do hidrogel também depende das interações entre as cadeias poliméricas reticuladas com o solvente e da força elástica restauradora do gel (Figura 9) (Chaterji, Kwon et al., 2007; Bajpai, Shukla et
Por exemplo, em soluções básicas, grupos ácidos presentes em um hidrogel sofrem desprotonação. Os hidrogênios ácidos gerados se combinam com os OH- do meio, formando moléculas de água. A neutralidade de cargas no hidrogel é mantida pela entrada de cátions (contraíons móveis) na rede tridimensional. A densidade de cargas de mesmo sinal (que, para os hidrogéis aniônicos é negativa) dentro da rede polimérica é aumentada, acompanhada pelo aumento na concentração de cátions no hidrogel, o que dá origem a uma pressão osmótica, promovendo a entrada de água no interior da rede polimérica, aumentando as interações entre o polímero e o solvente, resultando no intumescimento do hidrogel. O intumescimento chega ao equilibro com o balanço das pressões interna e externa, juntamente com as interações polímero-polímero na rede, que limitam o intumescimento do hidrogel (Chaterji, Kwon et al.,
2007; Bajpai, Shukla et al., 2010).
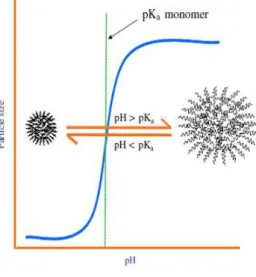
Figura 9– Mudança no tamanho de um microgel polieletrólito em função do pH do meio
Fonte: (Thorne, Vine et al., 2011)
A reversibilidade do processo pode ser observada quando o pH do meio fica ácido. Nesse caso, o hidrogel aniônico é protonado, resultando em uma diminuição tanto na densidade de cargas negativas quanto na quantidade de contraíons dentro do hidrogel, levando à contração do mesmo. Também, é importante salientar que, se o hidrogel com grupos ácidos já estiver completamente desprotonado em um meio básico, e o pH for elevado a valores ainda maiores (aumento da força iônica), ocorrerá uma contração do hidrogel, devido à geração de uma pressão osmótica no sentido contrário (Figura 10) (Bajpai, Shukla et al.,
Figura 10– Intumescimento/contração de um hidrogel pH-sensitivo aniônico em função da força iônica do meio
Fonte: (Bajpai, Shukla et al., 2008)
Os polímeros responsivos ao pH podem ser divididos em polibases, poliácidos (Gil e Hudson, 2004; Maharjan, Woonton et al., 2008), ou, ainda, anfóteros (Bajpai, Shukla et al.,
2010).
3.1.2.1 Poliácidos
Os poliácidos possuem grupos ácidos (-COOH, -SO3H) nas cadeias poliméricas, que
são desprotonados quando o pH fica acima do pKa, gerando poliânions; quando o pH do meio
fica abaixo do pKa, os grupos são protonados (Gil e Hudson, 2004; Bajpai, Shukla et al.,
2010; Medeiros, Santos et al., 2011; Samchenko, Ulberg et al., 2011). A maioria dos
polímeros aniônicos sensitivos ao pH é baseada no poli (ácido acrílico) (PAA) ou seus derivados (Figura 11) (Bajpai, Shukla et al., 2008).
Figura 11– Polímeros aniônicos sensíveis ao pH: (a) poli (ácido acrílico); (b) poli (ácido metacrílico); (c) poli (ácido 2-etil acrílico); (d) poli (ácido 2-propil acrílico)
3.1.2.2 Polibases
As polibases possuem grupos básicos (-NH2) em sua estrutura, os quais são
protonados em valores de pH inferiores ao pKa dos grupos, gerando policátions; quando o pH
do meio fica acima do pKa, os grupos desprotonam. Alguns policátions estão representados na
Figura 12 (Gil e Hudson, 2004; Liu e Urban, 2010).
Figura 12– Polímeros catiônicos sensíveis ao pH: (a) poli (metacrilatode N,N’-dimetil aminoetila), (b) poli (metacrilatode N,N-dietil aminoetila), (c) poli (4 ou 2-vinilpiridina), (d) poli (vinil imidazol)
Adaptado de: (Gil e Hudson, 2004)
3.1.2.2.1 Quitosana
A quitosana (QS) é um dos polímeros de fonte renovável que têm chamado mais atenção, principalmente para a área biomédica, por causa de suas propriedades biológicas favoráveis como biocompatibilidade, biodegradabilidade, mucoadesividade, atividade antimicrobiana e baixo custo. Além disso, seus produtos de degradação são não tóxicos, não imunogênicos e não carcinogênicos (Alves e Mano, 2008; Bajpai, Shukla et al., 2010). Esse
polissacarídeo tem sido extensivamente obtido através da desacetilação da quitina (Carreira, Goncalves et al., 2010), o segundo polissacarídeo mais abundante da natureza, perdendo
apenas para a celulose (Dos Santos Alves, Lima Vidal et al., 2009; Dash, Chiellini et al.,
Figura 13– Estruturas químicas da (a) celulose; (b) quitina e (c) quitosana
Fonte: Autor
A quitina é constituída predominantemente por unidades repetitivas de 2-acetamido-2-desoxi-D-glicopiranose unidas por ligações glicosídicas β-(1→4). É uma estrutura semelhante
à da celulose, sendo que, nesta última, ao invés dos grupos acetamido existem hidroxilas (unidades β-(1→4)-2-desoxi-D-glicopiranose). A quitina pode ser encontrada no exoesqueleto
A obtenção da quitosana a partir da desacetilação termoquímica da quitina ocorre em meio básico, sendo que a maioria dos métodos propostos envolve a hidrólise na posição acetilada por meio de soluções de hidróxido de sódio ou de potássio, ou a mistura de hidrazina anidra e sulfato de hidrazina. O tratamento da quitina em solução aquosa de NaOH a 40-45 % (m/v), a temperaturas na faixa de 90-120 °C, por 4-5 horas, resulta na N-desacetilação da
quitina. As condições utilizadas para a desacetilação determinam a massa molar média e o grau de desacetilação da quitosana (Dash, Chiellini et al., 2011).
A quitosana é um copolímero linear composto de unidades 2-amino-2-desoxi-D
-glicopiranose (em maior proporção) e 2-acetamida-2-desoxi-D-glicopiranose, interligadas por
ligações glicosídicas β-(1→4) (Garcia, Costa et al., 2008; Dash, Chiellini et al., 2011). A
quantidade de grupos 2-amino-2-desoxi-D-glicopiranose determina o grau de desacetilação do
copolímero. De maneira geral, é considerado que quando o grau de desacetilação (GD) da quitina é maior que 50 % (dependendo da origem do polímero e da distribuição dos grupos acetil ao longo das cadeias), o polímero se torna solúvel em meio aquoso ácido e é nomeado quitosana (Alves e Mano, 2008).
A presença dos grupos amino (-NH2), com pKa em torno de 6-6,5, nas cadeias de QS,
possibilita a sua solubilização em soluções aquosas ácidas diluídas (pH < 6). Essa propriedade faz da quitosana um polímero pH-responsivo. A baixos valores de pH, os grupos amino ficam protonados (positivamente carregados), fazendo da quitosana um polieletrólito catiônico solúvel em água. Quando o pH aumenta acima do pKa dos grupos amino, a quitosana
desprotona e o polímero deixa de estar carregado, tornando-se insolúvel (Dash, Chiellini et
al., 2011).
3.1.2.3 Polímeros anfóteros ou esquizofrênicos
Os polímeros anfóteros são polímeros pH sensitivos que possuem tanto grupos ácidos quanto grupos básicos ao longo da cadeia (Guo e Gao, 2007). Eles também são chamados de esquizofrênicos, por causa da presença de grupos catiônicos e aniônicos num mesmo material. Dessa forma, a carga resultante do material pode ser modulada, para a obtenção de propriedades desejadas, através da mudança na proporção entre grupos ácidos ou básicos durante a síntese e do pH do meio (Bajpai, Shukla et al., 2010). Sendo assim, a seleção
3.1.2.4 Aplicações
A variação abrupta no volume em função do pH é particularmente interessante para aplicações biomédicas. Isto porque o corpo humano exibe variações no pH ao longo do trato gastrointestinal, assim como em áreas específicas como certos tecidos (áreas tumorais) e compartimentos subcelulares (Bajpai, Shukla et al., 2008; Bajpai, Shukla et al., 2010;
Brun-Graeppi, Richard et al., 2010). Por exemplo, o estômago possui um valor de pH de 1,2,
enquanto que o pH do intestino delgado é de 7,4. Além disso, é sabido que o pH extracelular de tumores (6,8-6,9) é mais ácido do que o pH intracelular de tumores (7,2) e do que pH extracelular de tecidos (7,4) (Schmaljohann, 2006; Medeiros, Santos et al., 2011). Nesse
sentido, hidrogéis sensíveis ao pH são os mais frequentemente utilizados no desenvolvimento de sistemas de liberação controlada de fármacos (Samchenko, Ulberg et al., 2011). Outras
aplicações dos polímeros pH-sensitivos incluem cultura de células (Patil, Chaudhury et al.,
2012), inibidores de corrosão (Chen e Fu, 2012) e regeneração de tecidos (Sá-Lima, Caridade
et al., 2010; Tan, Rubin et al., 2010).
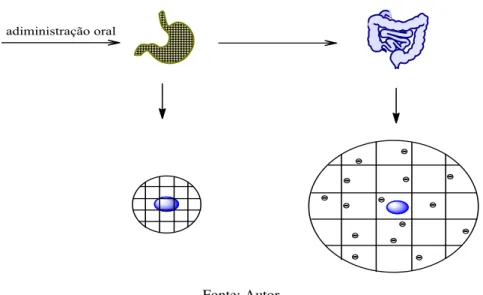
Geralmente, peptídeos e proteínas, como a insulina, por exemplo, não podem ser administrados por via oral, por causa da degradação dessas substâncias por enzimas proteolíticas no trato gastrointestinal e por causa da taxa extremamente baixa de transporte através da mucosa intestinal. Para superar essas barreiras na liberação por via oral, diversas estratégias têm sido investigadas, como o uso de agentes promotores de absorção e de inibidores de protease, que tem levado a uma melhor assimilação das proteínas (Lowman, Morishita et al., 1999; Nakamura, Murray et al., 2004; Bajpai, Shukla et al., 2010).
A avaliação de hidrogéis pH-responsivos graftizados como veículos para liberação de insulina por via oral foi relatada na literatura. Esses géis, nomeados poli (ácido metacrílico-g
-etileno glicol), foram feitos a partir de cadeias de poli (ácido metacrílico) enxertadas com poli (etileno glicol) (PEG), utilizando dimetilacrilato de etilenoglicol como agente reticulante. Estudos in vitro (Morishita, Lowman et al., 2002) mostraram que todas as formulações foram
que a insulina possui maior afinidade com as cadeias do PEG, fazendo com o que maior incorporação de fármaco fosse observada no copolímero com maior quantidade de PEG.
A liberação da insulina, em função do pH, também foi estudada (Morishita, Lowman
et al., 2002). Em meio ácido (pH=1,2), a insulina teve liberação de apenas 6% para o hidrogel
na proporção de 1:1, enquanto que os hidrogéis de poli (ácido metacrílico-g-etileno glicol)
(ácido: PEG de 4:1) e de poli (ácido metacrílico) tiveram uma liberação de 50% da insulina em um período de 2 horas. O comportamento em meio ácido, similar ao do estômago, foi atribuído à formação de ligações de hidrogênio entre os prótons ácidos do poli (ácido metacrílico) e o oxigênio do PEG. Essas reticulações físicas promoveram uma diminuição do tamanho do poro dos géis, o que impede a liberação da insulina, protegendo-a do meio ácido. Assim, quanto maior a quantidade de PEG no gel, maior a formação de ligações de hidrogênio, menor o tamanho dos poros, e menor a liberação. No caso do hidrogel sem PEG, o poli (ácido metacrílico), em meio ácido, a diminuição do tamanho do poro ocorre apenas em função da hidrofobicidade do material nessas condições; mas, por causa da ausência das reticulações físicas com o PEG, o tamanho do poro é suficiente para a passagem da insulina. Já em um valor mais elevado de pH (6,8), devido à rápida dissociação dos grupos ácidos, a insulina foi rapidamente liberada em todos os hidrogéis. Contudo, um pequeno retardamento na liberação foi observado para o hidrogel com proporções equimolares de ácido e PEG, quando comparado aos outros géis, devido à interação da insulina com as cadeias de PEG (Figura 14).
Em outro estudo (Lowman, Morishita et al., 1999), a insulina foi incorporada nos
hidrogéis pH-sensíveis de poli (ácido metacrílico-g-etileno glicol) e administrada oralmente
em ratos saudáveis e diabéticos. No ambiente ácido no estômago, os géis não intumesceram devido à formação de complexos intermoleculares. Dessa forma, a insulina ficou retida nos géis e protegida da degradação proteolítica. No ambiente básico do intestino, os complexos intermoleculares foram desfeitos, o que resultou em rápido intumescimento dos hidrogéis e liberação da insulina. Dentro de 2 horas de administração dos copolímeros com insulina incorporada foi observado um forte efeito hipoglicemiante, tanto nos ratos saudáveis quanto nos diabéticos, sendo que os efeitos duraram por até 8 horas.
Também, foi investigado o efeito do tamanho das partículas de poli (ácido
metacrílico-g-etileno glicol) na liberação de insulina no intestino (Morishita, Goto et al., 2004), sendo
hipoglicemiantes, sem danos detectáveis à mucosa. A mucoadesividade dos hidrogéis foi conferida através da presença das cadeias laterais do PEG. Além disso, a presença dos grupos carboxílicos pode blindar o Ca2+, inibindo a ação de enzimas dependentes desse metal, o que contribuiu para a proteção da insulina da degradação por proteazes.
Figura 14– Liberação de insulina por via oral, e sua liberação no intestino a partir de partículas de poli (ácido metacrílico-g-etileno glicol)
Fonte: Autor
Contudo, uma das limitações inerentes ao uso de polímeros sintéticos pH-responsivos, quando se trata da aplicação biomédica, é a não biodegradabilidade desses materiais. Em alguns casos, se o polímero não degrada dentro do corpo, ele deve ser cirurgicamente removido, implicando em alto custo e risco para o paciente (Samchenko, Ulberg et al., 2011).
A biodegradabilidade é uma propriedade que faz com que materiais degradem in vivo em
3.2 COMBINAÇÃO DAS PROPRIEDADES pH E TERMORRESPONSIVAS
Existe um interesse crescente no desenvolvimento de materiais que apresentem sensibilidade tanto ao pH quanto à temperatura em meio aquoso, em virtude da facilidade de controle dessas propriedades e da grande aplicabilidade desses materiais, como em biotecnologia, processamentos químicos e áreas médicas. Como mencionado previamente, dentre os polímeros termorresponsivos, o mais extensivamente investigado é a PNIPAM. Hidrogéis poliméricos pH e termorresponsivos têm sido frequentemente sintetizados a partir da copolimerização radicalar da NIPAM com monômeros do tipo ácido acrílico, na presença de um agente de reticulação, comumente a N,N’-metilenobisacrilamida (MBA) (Duan, Zhang
et al., 2011). De fato, o ácido acrílico é o monômero mais utilizado para a produção de
copolímeros com a NIPAM, a fim de obter materiais com pH e termossensibilidade (Dimitrov, Trzebicka et al., 2007).
Citando um exemplo, microgéis de PNIPAM quimicamente reticulados e de PNIPAM com diferentes quantidades de ácido acrílico (PNIPAM-co-PAA) foram sintetizados por
polimerização por precipitação por radicais livres, utilizando persulfato de amônio como iniciador e N,N’-metilenobisacrilamida (MBA) como agente reticulante (Figura 15). O estudo
revelou que a estabilização dos microgéis em diferentes pHs e temperaturas pode ser afetada por fatores como: concentração polimérica, adição de surfactantes iônicos e quantidade de grupos carregados no polímero (Al-Manasir, Zhu et al., 2009).
Figura 15– Esquema do processo de síntese de microgéis de PNIPAM-co-PAA, por polimerização por
precipitação, usando um iniciador radicalar (persulfato) e MBA como agente de reticulação
Com o intuito de incorporar, aos polímeros de dupla sensibilidade, propriedades biológicas favoráveis, tais como biodegradabilidade, biocompatibilidade e baixa toxicidade, tem sido sugerido a introdução de polissacarídeos, entre os quais se destaca a quitosana, que também é pH-sensitiva. Várias maneiras de unir as cadeias de quitosana com as de PNIPAM têm sido propostas. Han e colaboradores (2009), por exemplo, desenvolveram hidrogéis de quitosana funcionalizada com metacrilato de glicidila (QS-MAG) e copolimerizada com NIPAM, utilizando N,N’-metilenobisacrilamida (MBA) como agente reticulante. A
copolimerização foi realizada via fotopolimerização. A solução de QS-MAG com os demais reagentes foi irradiada com luz na faixa do ultravioleta, fazendo com o que fotoiniciador 2959 sofresse quebra homolítica nas suas ligações C-C, gerando radicais livres, que promoveram a clivagem das duplas ligações (C=C) do monômero, do agente reticulante e do derivado de quitosana. Esse processo gerou hidrogéis nos quais as cadeias de PNIPAM e de quitosana estão covalentemente ligadas (Figura16).
Figura 16– Esquema de preparação dos hidrogéis
A liberação de um fármaco modelo, o ácido laranja 8 (AL8), foi avaliado em meio ácido (pH = 2,2) e meio neutro (pH = 7,4), a uma temperatura de 37 °C. Em meio neutro, o AL8 foi liberado gradualmente do hidrogel; enquanto que, em meio ácido, a taxa de liberação foi extremamente baixa (Figura 17). Esse comportamento foi atribuído ao fato das interações do AL8 com o hidrogel ser dependente do pH do meio. Isso porque, em meio ácido, os grupos amino da quitosana encontram-se positivamente carregados, enquanto que em meio neutro eles encontram-se na forma não ionizada. Dessa forma, em pH ácido, existe uma forte interação eletrostática atrativa entre os grupos amino protonados da quitosana (-NH3+) com o
grupo SO3- do AL8, que dificulta a liberação do AL8. A falta de interação em pH neutro
promoveu a liberação gradual do fármaco modelo nesse meio (Han, Wang et al., 2009).
Figura 17– Perfil de liberação cumulativa do ácido laranja 8 do hidrogel em diferentes valores de pH de soluções tampão
Fonte: (Han, Wang et al., 2009)
Hua e colaboradores (2011) sintetizaram copolímeros de quitosana-g-PNIPAM
conjugados com Lilial (3-(4-terc-butilfenil) isobutiraldeído) e verificaram a liberação desse último em função do pH e da temperatura do meio. A formação do conjugado foi realizada através da reação do grupo aldeído do lilial com o –NH2 da quitosana, em meio iônico líquido
PNIPAM foi feita por reações de esterificação. Isso foi possível porque a PNIPAM foi previamente funcionalizada com grupos carboxílicos terminais (Figura 18).
Figura 18– Representação esquemática da rota sintética para a obtenção do copolímero conjugado
PNIPAM-quitosana-Lilial
Fonte: (Hua, Jiang et al., 2011)
O conjugado PNIPAM-quitosana-Lilial associou-se na forma de estruturas núcleo-corona (core-shell) em meio aquoso de pH = 7,4, à temperatura ambiente, sendo o núcleo
Figura 19– (A) Perfil de liberação do Lilial simulado em: (a) 25 °C e pH = 7,4; (b) 37 °C e pH = 4,5. (B) Representação esquemática da dupla responsividade do nanocarreador conjugado auto-associativo
PNIPAM-quitosana-Lilial. A PNIPAM está representada em vermelho, a quitosana em azul e o lilial em amarelo
Fonte: (Hua, Jiang et al., 2011)
Nas últimas décadas, a copolimerização por enxertia de monômeros vinílicos nas cadeias de polissacarídeos através da iniciação por radicais livres tem atraído o interesse de muitos cientistas. Esse tipo de síntese possibilita a produção de materiais que agregam e melhoram as propriedades dos polímeros em relação aos seus precursores, ampliando a aplicabilidade. Por exemplo, hidrogéis contendo apenas quitosana mostram rápida dissolução no estômago e, assim, capacidade limitada de controle de liberação de fármacos. A enxertia de PNIPAM permite um maior controle no processo de liberação. A enxertia de NIPAM na quitosana também melhora as propriedades mecânicas da PNIPAM (Prabaharan e Mano, 2006; Alves e Mano, 2008; Carreira, Goncalves et al., 2010).
Entre os iniciadores dessa polimerização, tem-se o nitrato de cério amoniacal (NCA), persulfatos em geral (XPS) e a 2,2’-azoisobutironitrila (AIBN), comumente ativados termicamente ou ainda por sistemas redox, em que se adicionam o N,N,N’,N’- tetrametilenodiamina (TEMED) (Prabaharan e Mano, 2006; Alves e Mano, 2008; Carreira, Goncalves et al., 2010).
Com relação ao mecanismo para a reação de copolimerização de monômeros vinílicos nas cadeias de quitosana, usando NCA ou XPS como iniciador, por exemplo, várias hipóteses têm sido propostas quanto ao ponto da cadeia de quitosana em que ocorrerá a formação de radicais livres para iniciar a reação.
duplas ligações do anidrido itacônico e as hidroxilas secundárias das cadeias de QS, como apresentado no esquema da Figura 20 (Gaffar, El-Rafie et al., 2004).
Figura 20– Esquema de enxertia de monômero vinílico nas cadeias de quitosana
Fonte: (Alves e Mano, 2008)
Chung e colaboradores (2006) propõem que o NCA abstrai um hidrogênio do grupo CH2 ligado à hidroxila primária da glucosamina, conforme apresentado no esquema da Figura
21, a seguir (Chung, Bae et al., 2005).
Figura 21– Esquema da reação para a síntese da QS-g-PNIPAM
Recillas e colaboradores (2009) sugerem que a copolimerização da PNIPAM, iniciada por NCA, ocorre nos grupos amina das cadeias de quitosana, como mostrado no esquema da Figura 22 (Recillas, Silva et al., 2009).
Figura 22– Esquema da reação de modificação das cadeias de QS, iniciada por NCA, formando os copolímeros
de QS-g-PNIPAM
Fonte: (Recillas, Silva et al., 2009)
Tabela 1 – Exemplos de mecanismos propostos para a iniciação da enxertia de monômeros vinílicos sobre a cadeia de quitosana, utilizando persulfato como iniciador
Mecanismo proposto Referência
(Najjar, Yunus et al., 2000)
(Prashanth e Tharanathan, 2003)
(Mahdavinia, Pourjavadi et
al., 2004)
(Mun, Nurkeeva et al.,
2008)
Duan e colaboradores (2011) sintetizaram copolímeros de CS-g-PNIPAM, por
polimerização por precipitação, utilizando persulfato de amônio como iniciador e MBA como agente reticulante (Figura 23). As nanopartículas obtidas foram carregadas com oridonin, um potente agente anticancerígeno na medicina chinesa tradicional, e que tem se mostrado eficaz contra diversos tumores, por ensaios farmacológicos e clínicos. Testes de liberação in vitro a
37 °C demonstraram que a liberação do oridonin foi maior em pH mais ácidos e menor em pH de 7,4 (Duan, Zhang et al., 2011).
Figura 23– Esquema de síntese dos copolímeros
Fonte: (Duan, Zhang et al., 2011)
negativamente carregadas com PNIPAM-co-PAA como corona, em meio alcalino (Fei, Yang
et al., 2010).
Figura 24– Esquema de síntese do copolímero quitosana-g-P(NIPAM-co-AA) por polimerzação por graftização
radicalar
Fonte: (Fei, Yang et al., 2010)
Jung e colaboradores (2009) prepararam nanopartículas termorresponsivas, tendo PNIPAM-co-PAA como núcleo e quitosana como corona. Inicialmente, partículas de
PNIPAM-co-PAA foram sintetizadas na presença de um tensoativo (dodecilsulfato de sódio –
polimerização em emulsão) e reticuladas com MBA, utilizando persulfato de potássio como iniciador, ativado termicamente (75 °C). Após purificação por diálise, as partículas foram adicionadas a uma solução contendo quitosana, e 1-etil-3-dimetilamino-propil-carbodiimida (EDC) foi adicionado, promovendo a reação entre o grupo amina da quitosana e o carboxílico da partícula. O tamanho das partículas variou de 380 a 25 nm com o aumento da temperatura do meio disperso. As nanopartículas com quitosana mantiveram comportamento termossensitivo, como LCST e contração das partículas por causa da presença do núcleo com
PNIPAM, induzindo agregação por volta da LCST. Esse comportamento não foi observado
para as partículas de PNIPAM-co-PAA (sem quitosana). Além disso, as partículas de
quitosana devem apresentar maior biocompatibilidade por causa da presença do polissacarídeo (Jung, Jang et al., 2009).
O potencial de aplicação desses materiais pH e termossensitivos baseados em PNIPAM não se restringe apenas à área farmacêutica. Parasuraman e colaboradores publicaram alguns trabalhos sobre a síntese de microgéis de PNIPAM-co-PAA para
descontaminação de água (Parasuraman e Serpe, 2011b; a; Parasuraman, Leung et al., 2012).
MBA, com diferentes quantidades de ácido acrílico, mas mantendo a concentração total de monômero igual para todos os microgéis (140 mM), foram preparadas por polimerização por precipitação, iniciada por radicais livres (persulfato de amônio). Foi avaliada a eficiência desses microgéis na remoção de corantes orgânicos da água. Eles observaram que, em temperatura ambiente, a quantidade de corante removida aumentou com o aumento na concentração das partículas e na quantidade de ácido acrílico na partícula, sendo este comportamento atribuído ao aumento no tamanho das partículas (determinado por espalhamento de luz dinâmico) com o aumento na concentração de AA. Também, a remoção do corante foi maior a maiores temperaturas, muito provavelmente por causa da termossensibilidade da PNIPAM, que expele água, retendo o corante por interação hidrofóbica. Com a aplicação de ciclos de temperatura, a remoção do corante orgânico foi aumentada, embora tenha sido limitada em dois ciclos de aquecimento, provavelmente, porque os microgéis saturaram após o segundo aquecimento, não conseguindo reter mais nenhum material (Parasuraman e Serpe, 2011b).
Outro grupo de pesquisa, formado por Saitoh e colaboradores, tem publicado artigos sobre a preparação de copolímeros contendo quitosana, PNIPAM e PAA para purificação de água contaminada (Saitoh, Sugiura et al., 2009; Saitoh, Tohru, Asano, Kotaro et al., 2011;
Saitoh, Asano et al., 2012). Os copolímeros de PNIPAM-co-PAA foram sintetizados
previamente por polimerização redox (persulfato de amônio/TEMED) da mistura de NIPAM com AA. Então, PNIPAM-co-PAA foram ligados à quitosana por reação posterior de um
3.3 O ESTUDO DE PROPRIEDADES FÍSICO-QUÍMICAS DE PARTÍCULAS POLIMÉRICAS INTELIGENTES
3.3.1 Reologia
A reologia descreve a deformação de sólidos, líquidos ou gases sob a influência de tensões. Sólidos ideais deformam-se elasticamente, ou seja, a energia necessária para a deformação é totalmente recuperada quando a tensão é removida. Fluidos ideais (líquidos e gases) deformam-se irreversivelmente, ou seja, fluem. Sendo assim, a energia requerida para a deformação é dissipada sob a forma de calor e não pode ser recuperada através da remoção da tensão.
Os corpos reais não são sólidos ideais nem fluidos ideais. Os sólidos reais também podem se deformar de forma irreversível (fluir) quando sob a influência de forças de magnitude suficiente. Também, somente alguns líquidos de importância técnica ou prática se aproximam dos líquidos com comportamento ideal. A grande maioria dos líquidos apresenta comportamento reológico que os classifica numa região entre os líquidos e os sólidos: eles são elásticos e viscosos e, por essa razão, são chamados viscoelásticos.
Os equipamentos que medem as propriedades viscoelásticas de materiais são chamados reômetros. Em particular, os sistemas de medição, que envolvem a utilização de cilindros coaxiais em reômetros, resultam do “dobramento” de ambos os pratos do modelo de placas paralelas (Figura 25), formando um cilindro externo e outro interno. Uma amostra líquida preenche o espaço anular entre os dois cilindros e é submetida a um cisalhamento, em que o cilindro externo (copo) é fixo e o interno (rotor) gira (Schramm, 2006).
diretamente proporcional ao gradiente de velocidade através do líquido. Assim, o coeficiente de proporcionalidade é igual à viscosidade (η) (Ferreira, Brandão et al., 2005).
Figura 25– Fluxo entre duas placas paralelas
Fonte: Autor
F dv
A dx (1)
A força por unidade de área é conhecida como tensão de cisalhamento (σ) e o
gradiente de velocidade é conhecido como taxa de cisalhamento (.). Substituindo (F/A) por
(σ) e (dv/dx) por (. ), tem-se a equação de Newton (Equação 2) para a viscosidade de um fluido.
.
(2)
Os fluidos chamados Newtonianos apresentam uma relação linear entre a taxa de cisalhamento e a tensão de cisalhamento, ou seja, a viscosidade mantém-se constante com a variação na taxa de cisalhamento. Ao contrário dos fluidos Newtonianos, os fluidos não-Newtonianos não apresentam uma relação linear entre a tensão de cisalhamento e a taxa de cisalhamento, isto é, os valores da viscosidade variam com a variação nos valores da taxa de cisalhamento.