ANA PAULA SANTANA LOURES
TRATAMENTO ANAERÓBIO DE EFLUENTES DE MÁQUINA DE PAPEL POR
BIORREATOR CONVENCIONAL E BIORREATOR DE MEMBRANAS
Tese apresentada à Universidade
Federal de Viçosa, como parte das
exigências do Programa de
Pós-Graduação em Ciência Florestal, para
obtenção do título de Doctor Scientiae.
VIÇOSA
ANA PAULA SANTANA LOURES
TRATAMENTO ANAERÓBIO DE EFLUENTES DE MÁQUINA DE PAPEL POR
BIORREATOR CONVENCIONAL E BIORREATOR DE MEMBRANAS
Tese apresentada à Universidade
Federal de Viçosa, como parte das
exigências do Programa de
Pós-Graduação em Ciência Florestal, para
obtenção do título de Doctor Scientiae.
APROVADA: 8 de outubro de 2007.
______________________________
Profa. Ann Honor Mounteer
(Co-Orientadora)
______________________________
Prof. Carlos Augusto de
Lemos Chernicharo
(Co-Orientador)
______________________________
Prof. Hilário Cuquetto Mantovani
______________________________
Prof. João Carlos Teixeira Dias
______________________________
A meus pais,
Lívia e Emílio,
meus irmãos,
Dany e Emílio,
minha cunhada,
Luciana,
e meus sobrinhos,
Cecília e Gabriel
AGRADECIMENTOS
À Universidade Federal de Viçosa (UFV) e ao Departamento de Engenharia Florestal (DEF), pela
oportunidade de realizar o Curso de Doutorado, ao Conselho Nacional de Desenvolvimento Científico e
Tecnológico (CNPq) e à Fundação de Amparo à Pesquisa do Estado de Minas Gerais (FAPEMIG), pelo
financiamento desta pesquisa e pela concessão das bolsas de doutorado e de iniciação científica.
À Zenon Environmental Inc. (Canadá), pelo módulo de membrana de ultrafiltração, à Suzano Papel e
Celulose e à Klabin S.A., pelo fornecimento da água branca.
Ao professor Cláudio Mudado Silva, pela orientação, ensinamentos, incentivo em diversos momentos
apreensivos durante estes quatro anos, confiança, contribuições e sugestões oportunas e, acima de
tudo, pela amizade.
Aos professores Ann Honor Mounteer e Carlos Augusto de Lemos Chernicharo, pelo apoio durante a
realização deste trabalho, contribuições e sugestões oportunas.
Aos professores Hilário Cuquetto Mantovani e João Carlos Teixeira Dias, pelo apoio durante a
realização deste trabalho, sugestões e amizade.
Aos professores José Lívio Gomide, Jorge Luiz Colodette e Rubens Chaves de Oliveira, pelos
ensinamentos e pela franca disposição com que sempre me receberam.
Aos meus estagiários, Matheus e Ismarley, pela competência na realização das análises
laboratoriais, paciência durante a operação de manutenção dos biorreatores, imprescindível ajuda em
buscar água branca na câmera fria, constante bom-humor e amizade.
À Ana Augusta, Mônica e Sandra, pelos momentos de descontração e amizade.
À Valéria, pela dedicação ao laboratório, conversas bem-humoradas e amizade.
A todos no Laboratório de Meio Ambiente, pelo intenso intercâmbio de informações e risadas
compartilhadas.
Aos funcionários do Laboratório de Celulose e Papel, Bittencourt, Cirinho e Edinho, companheiros
fiéis nas madrugadas no laboratório, apoio durante a realização deste trabalho e simpatia com que
sempre me receberam.
Aos demais funcionários do LCP e colegas do programa de pós-graduação, sem os quais o
laboratório não seria minha segunda casa e pela amizade sem a qual nada valeria a pena.
A todos que, de alguma forma, contribuíram para a realização deste trabalho.
Aos amigos e familiares distantes que souberam compreender meus momentos de exílio no curso
das disciplinas, no laboratório e em frente ao computador.
A Deus, pelo zelo com o qual sempre cuidou de mim e por trazer para a minha vida todas essas
BIOGRAFIA
ANA PAULA SANTANA LOURES, filha de Lívia Helena Rebouças Santana Loures e Emílio Gomide
Loures, nasceu na cidade de Belo Horizonte, Estado de Minas Gerais, em 17 de setembro de 1968.
Em janeiro de 1997, graduou-se em Engenharia Civil pela Escola de Engenharia da Universidade
Federal de Minas Gerais (UFMG), em Belo Horizonte, MG.
Em agosto de 2002, obteve o título de “Magister Scientiae” em Engenharia Agrícola na Universidade
Federal de Viçosa (UFV), Viçosa, MG, tendo concentrado seus estudos na Área de Recursos Hídricos e
Ambientais e sendo o título da tese "Modelos de remoção de parâmetros qualitativos em sistema para
tratamento de esgoto doméstico por escoamento superficial utilizando o capim-coastcross (Cynodon
dactylon (L.) Pers.)".
Em abril de 2003, iniciou o Programa de Pós-Graduação, em nível de Doutorado, em Ciência
Florestal na Universidade Federal de Viçosa, tendo concentrado seus estudos na Área de Tecnologia de
Celulose e Papel, realizando pesquisa direcionada ao tratamento de efluente da máquina de papel por
biorreator anaeróbio com acoplamento de membranas de ultrafiltração e submetendo-se à defesa de
SUMÁRIO
Página
LISTA DE FIGURAS... viii
LISTA DE TABELAS... xii
LISTA DE ABREVIATURAS... xvi
RESUMO... xviii
ABSTRACT... xx
1. INTRODUÇÃO GERAL... 1
2. REVISÃO BIBLIOGRÁFICA... 3
2.1. FABRICAÇÃO DE PAPEL... 3
2.2. REATORES ANAERÓBIOS... 6
2.2.1. Fundamentos da digestão anaeróbia... 7
2.2.1.1. Hidrólise... 8
2.2.1.2. Acidogênese... 9
2.2.1.3. Acetogênese... 9
2.2.1.4. Metanogênese... 11
2.2.2. Condições de operação dos reatores anaeróbios... 13
2.3. MEMBRANAS... 18
2.3.1. Fundamentos da tecnologia de membrana... 18
2.3.2. Características das membranas... 20
2.4. BIORREATORES ANAERÓBIOS DE MEMBRANAS... 21
2.5. EFEITOS DA TEMPERATURA... 24
3. OBJETIVOS... 29
4. BIORREATOR ANAERÓBIO CONVENCIONAL (BRAC) E BIORREATOR ANAERÓBIO DE MEMBRANAS (BRAM), TRATANDO A ÁGUA BRANCA DA MÁQUINA DE PAPEL PRODUZINDO PAPEL KRAFT BRANQUEADO (ETAPA 1)... 30
4.1. MATERIAL E MÉTODOS……...………... 31
4.1.1. Sistema de tratamento... 31
4.1.2. Alimentação... 33
4.1.3. Lodo... 33
4.1.4. Condições operacionais... 34
4.1.5. Análises físico-químicas... 34
4.1.6. Equações utilizadas... 35
Página
4.1.6.2. Carga hidráulica volumétrica (CHV) e carga orgânica volumétrica (COV).. 36
4.1.6.3. Taxa alimento/microrganismo (A/M) e taxa de utilização do substrato (U).. 36
4.2. RESULTADOS E DISCUSSÃO... 38
4.2.1. Condições operacionais... 38
4.2.2. Monitoramento da estabilidade... 38
4.2.3. Monitoramento da eficiência... 41
4.2.4. Monitoramento do lodo... 51
4.2.5. Reutilização do efluente tratado... 53
4.3. CONCLUSÃO DA ETAPA 1…... 54
5. BIORREATOR ANAERÓBIO CONVENCIONAL (BRAC) E BIORREATOR ANAERÓBIO DE MEMBRANAS (BRAM), TRATANDO A ÁGUA BRANCA DA MÁQUINA DE PAPEL PRODUZINDO PAPEL RECICLADO (ETAPA 2)... 55
5.1. MATERIAL E MÉTODOS……...………... 56
5.1.1. Sistema de tratamento... 56
5.1.2. Alimentação... 58
5.1.3. Lodo... 58
5.1.4. Condições operacionais... 59
5.1.5. Análises físico-químicas... 59
5.1.6. Equações utilizadas... 60
5.2. RESULTADOS E DISCUSSÃO... 61
5.2.1. Condições operacionais... 61
5.2.2. Monitoramento da estabilidade... 62
5.2.3. Monitoramento da eficiência... 67
5.2.4. Monitoramento do lodo... 76
5.3. CONCLUSÃO DA ETAPA 2…... 78
6. BIORREATOR ANAERÓBIO DE MEMBRANAS MESOFÍLICO (BRAM 35°C) E BIORREATOR ANAERÓBIO DE MEMBRANAS TERMOFÍLICO (BRAM 55°C), TRATANDO A ÁGUA BRANCA DA MÁQUINA DE PAPEL PRODUZINDO PAPEL KRAFT BRANQUEADO (ETAPA 3)... 79
6.1. MATERIAL E MÉTODOS……...………... 80
6.1.1. Sistema de tratamento... 80
6.1.2. Alimentação... 82
6.1.3. Lodo... 82
6.1.4. Condições operacionais... 83
6.1.5. Análises físico-químicas... 83
6.1.6. Equações utilizadas... 84
6.2. RESULTADOS E DISCUSSÃO... 85
6.2.1. Condições operacionais... 85
6.2.2. Monitoramento da estabilidade... 85
6.2.3. Monitoramento da eficiência... 89
6.2.4. Monitoramento do lodo... 95
Página
6.3. CONCLUSÃO DA ETAPA 3…... 98
7. CONCLUSÕES GERAIS….………...………...……….. 99
8. RECOMENDAÇÕES... 100
LISTA DE FIGURAS
Págin a
2.1. Principais etapas na fabricação de papel... 4
2.2. Sistema de água branca... 5
2.3. Seqüências metabólicas envolvidas na digestão anaeróbia... 8
2.4. As três vias para a metanogênese: via hidrogenotrófica, via metilotrófica e via acetoclástica... 11
2.5. Via hidrogenotrófica... 12
2.6. Esquema básico de uma membrana... 18
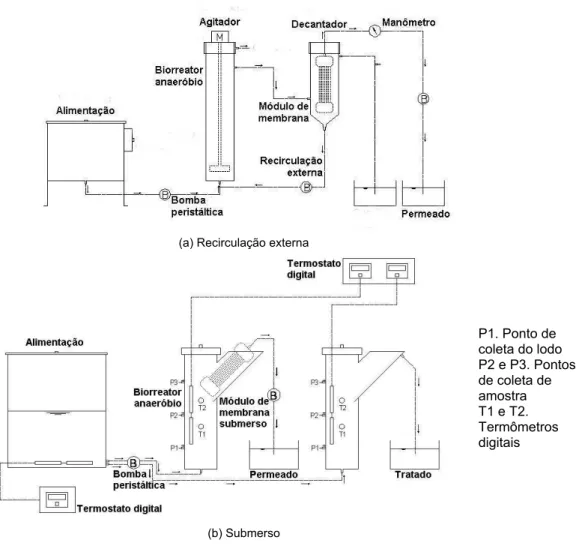
2.7. Esquemas dos sistemas de biorreator de membranas com (a) recirculação externa e (b) submerso... 19
2.8. Operações em (a) pressão transmembrana (PTM) e (b) fluxo constantes... 19
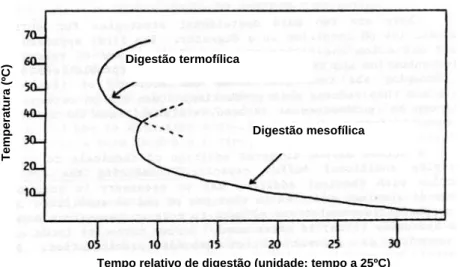
2.9. Tempo relativo de digestão de lodo de sedimentação plena digerido às temperaturas de 10ºC a 70ºC... 25
2.10. Efeito da temperatura em Archaea metanogênicas... 25
2.11. Eficiência de remoção de DQO no efluente em (a) reator I e (b) reator II... 27
2.12. Parâmetros de desempenho do reator durante o experimento: ( ) pH e (●) ácidos orgânicos voláteis totais... 27
4.1. Sistema de tratamento biológico... 31
4.2. Sistema de aquecimento da entrada... 32
4.3. Módulo de membrana de ultrafiltração... 33
4.4. pH, durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel kraft branqueado (Etapa 1).. 39
4.5. Ácidos orgânicos voláteis (AOV), durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel kraft branqueado (Etapa 1)... 40
4.6. Alcalinidade total (AT), durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel kraft branqueado (Etapa 1)... 41
Págin a
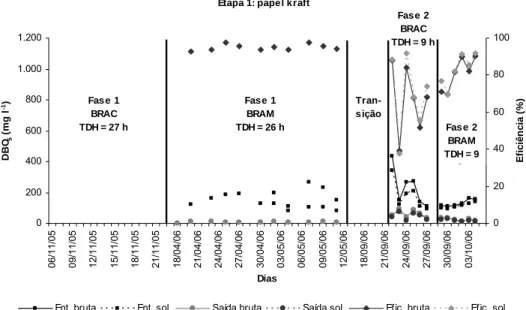
4.8. Demanda química de oxigênio (DQO), bruta e solúvel, e eficiência de remoção, durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água
branca da máquina de papel produzindo papel kraft branqueado (Etapa 1)... 43
4.9. Demanda bioquímica de oxigênio (DBO5), bruta e solúvel, e eficiência de remoção,
durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM),
tratando água branca da máquina de papel produzindo papel kraft branqueado (Etapa 1).. 43
4.10. Sólidos suspensos totais (SST) e eficiência de remoção, durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de
papel produzindo papel kraft branqueado (Etapa 1)... 45
4.11. Turbidez e eficiência de remoção, durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 1)... 46
4.12. Dureza total (DT) e eficiência de remoção, durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 1)... 49
4.13. Dureza cálcio (DCa) e eficiência de remoção, durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 1)... 50
4.14. Condutividade elétrica (C.E.), durante as Fases 1 e 2 e o período de transição, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel kraft
branqueado (Etapa 1)... 51
4.15. Sólidos suspensos totais (SST), sólidos suspensos fixos (SSF) e sólidos suspensos voláteis (SSV) no lodo anaeróbio, durante as Fases 1 e 2 e o período de transição, para o biorreator anaeróbio convencional (BRAC) e para o biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel kraft branqueado
(Etapa 1)... 52
5.1. Sistema de tratamento biológico... 56
5.2. Detalhe dos aquecedores de aquário utilizados no sistema de aquecimento dos
biorreatores... 57
5.3. Módulo de membrana de ultrafiltração... 58
5.4. pH, durante as Fases 2 e 3, na entrada, no biorreator anaeróbio convencional (BRAC) e no biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de
papel produzindo papel reciclado (Etapa 2)... 63
5.5. pH, durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio
convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água
branca da máquina de papel produzindo papel reciclado (Etapa 2)... 64
5.6. Ácidos orgânicos voláteis (AOV), durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas
(BRAM), tratando água branca da máquina de papel produzindo papel reciclado (Etapa 2) 65
5.7. Alcalinidade total (AT), durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM),
tratando água branca da máquina de papel produzindo papel reciclado (Etapa 2)... 66
5.8. Alcalinidade bicarbonato (AB), durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas
Págin a
5.9. Demanda química de oxigênio bruta (DQO bruta) e eficiência de remoção, durante as
Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel reciclado (Etapa 2)... 68
5.10. Demanda química de oxigênio solúvel (DQO solúvel) e eficiência de remoção, durante as
Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel reciclado (Etapa 2)... 68
5.11. Sólidos suspensos totais (SST) e eficiência de remoção, durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel reciclado (Etapa 2)... 69
5.12. Turbidez, durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água
branca da máquina de papel produzindo papel reciclado (Etapa 2)... 71
5.13. Turbidez e cor aparente, durante a Fase 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água
branca da máquina de papel produzindo papel reciclado (Etapa 2)... 71
5.14. Dureza total (DT) e eficiência de remoção, durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel
reciclado (Etapa 2)... 73
5.15. Dureza cálcio (DCa) e eficiência de remoção, durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de
membranas (BRAM), tratando água branca da máquina de papel produzindo papel
reciclado (Etapa 2)... 74
5.16. Condutividade elétrica (C.E.), durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas
(BRAM), tratando água branca da máquina de papel produzindo papel reciclado (Etapa 2)... 75
5.17. Cor real, durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água
branca da máquina de papel produzindo papel reciclado (Etapa 2)... 76
5.18. Sólidos suspensos totais (SST), sólidos suspensos fixos (SSF) e sólidos suspensos voláteis (SSV) no lodo anaeróbio, durante as Fases 1, 2 e 3, para o biorreator anaeróbio convencional (BRAC) e para o biorreator anaeróbio de membranas (BRAM), tratando
água branca da máquina de papel produzindo papel reciclado (Etapa 2)... 77
6.1. Sistema de tratamento biológico... 80
6.2. Detalhe dos aquecedores de aquário utilizados no sistema de aquecimento dos
biorreatores... 81
6.3. Módulo de membrana de ultrafiltração... 82
6.4. pH para o biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e para o biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da
máquina de papel produzindo papel kraft branqueado (Etapa 3)... 86
6.5. pH, na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água
branca da máquina de papel produzindo papel kraft branqueado (Etapa 3)... 87
6.6. Ácidos orgânicos voláteis (AOV), na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel produzindo papel kraft
Págin a
6.7. Alcalinidade total (AT), na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel produzindo papel kraft branqueado
(Etapa 3)... 88
6.8. Alcalinidade bicarbonato (AB), na entrada e na saída do biorreator anaeróbio de
membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel produzindo papel kraft
branqueado (Etapa 3)... 89
6.9. Demanda química de oxigênio (DQO) e eficiência de remoção, na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 3)... 90
6.10. Sólidos suspensos totais (SST) e eficiência de remoção, na entrada e na saída do
biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 3)... 91
6.11. Turbidez e eficiência de remoção, na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel produzindo papel kraft
branqueado (Etapa 3)... 92
6.12. Dureza total (DT) e eficiência de remoção, na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel produzindo papel
kraft branqueado (Etapa 3)... 93
6.13. Condutividade elétrica (C.E.), na entrada e na saída do biorreator anaeróbio de
membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel produzindo papel kraft
branqueado (Etapa 3)... 94
6.14. Cor real, na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água
branca da máquina de papel produzindo papel kraft branqueado (Etapa 3)... 95
6.15. Sólidos totais (ST), sólidos totais fixos (STF) e sólidos totais voláteis (STV) no lodo anaeróbio, para o biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e para o biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da
LISTA DE TABELAS
Página
2.1. Exemplos de grupos bacterianos envolvidos na digestão anaeróbia, segundo diferentes
autores... 9
2.2. Valores da energia livre padrão de algumas reações catabólicas da digestão anaeróbia,
segundo diferentes autores... 10
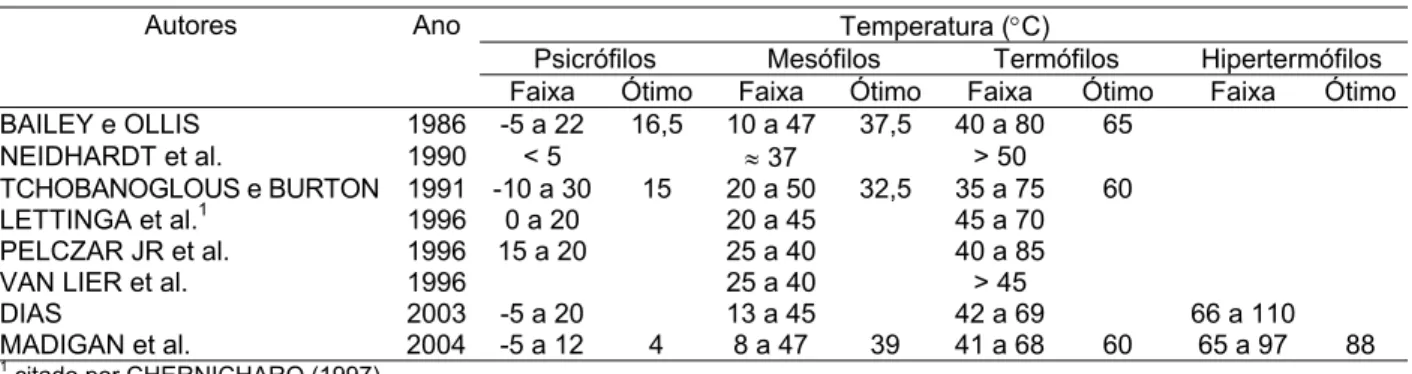
2.3. Variação de temperatura para quatro grupos de microrganismos, segundo diferentes
autores... 15
2.4. Condições ótimas de operação de reatores anaeróbios para os parâmetros pH,
temperatura, alcalinidade e ácidos voláteis, segundo diferentes autores... 15
2.5. Remoção de espécies de acordo com a membrana... 20
2.6. Características das membranas utilizadas para o tratamento de água
residuária... 20
2.7. Resumo de alguns parâmetros operacionais e de projeto de sistemas de tratamento de
efluentes, reportados na literatura... 22
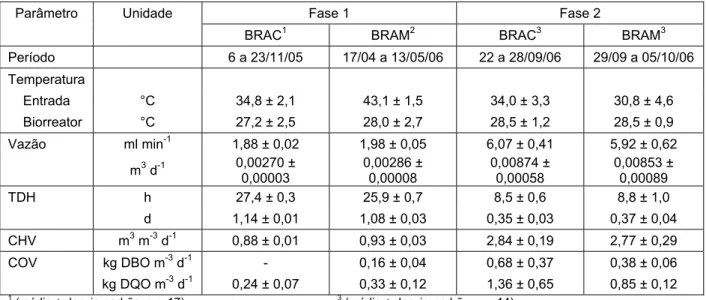
4.1. Período, temperatura, vazão, tempo de detenção hidráulica (TDH), carga hidráulica volumétrica (CHV) e carga orgânica volumétrica (COV) do sistema de tratamento durante as Fases 1 e 2, para o biorreator anaeróbio convencional (BRAC) e para o biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 1)... 34
4.2. Análises físico-químicas da entrada, da saída e do lodo... 35
4.3. pH, ácidos orgânicos voláteis (AOV), alcalinidade total (AT) e alcalinidade bicarbonato (AB), durante as Fases 1 e 2, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da
máquina de papel produzindo papel kraft branqueado (Etapa 1)... 39
4.4. Demanda química de oxigênio (DQO), bruta e solúvel, demanda bioquímica de oxigênio (DBO5), bruta e solúvel, sólidos suspensos totais (SST) e turbidez, durante as Fases 1 e
2, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 1)... 42
4.5. Eficiências médias de remoção de demanda química de oxigênio (DQO), para o
biorreator anaeróbio convencional (BRAC) e para o biorreator anaeróbio de membranas (BRAM), sob diferentes tempos de detenção hidráulica (TDH) estimados, tratando água branca da máquina de papel produzindo papel kraft branqueado (Etapa
1)... 44
4.6. Eficiências médias de remoção de demanda química de oxigênio (DQO), para diferentes tempos de detenção hidráulica (TDH) estimados, sob as configurações de sistema biorreator anaeróbio convencional (BRAC) e biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel kraft branqueado
(Etapa 1).. 45
4.7. Eficiências médias de remoção de sólidos suspensos totais (SST), sob diferentes tempos
produzindo papel kraft branqueado (Etapa 1)...
Página
4.8. Eficiências médias de remoção de sólidos suspensos totais (SST), sob as configurações de sistema biorreator anaeróbio convencional (BRAC) e biorreator anaeróbio de
membranas (BRAM), tratando água branca da máquina de papel produzindo papel kraft
branqueado (Etapa 1)... 47
4.9. Eficiências médias de remoção de turbidez, para o biorreator anaeróbio convencional (BRAC) e para o biorreator anaeróbio de membranas (BRAM), sob diferentes tempos de detenção hidráulica (TDH) estimados, tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 1)... 47
4.10. Eficiências médias de remoção de turbidez, para os diferentes tempos de detenção hidráulica (TDH) estimados, sob as configurações de sistema biorreator anaeróbio convencional (BRAC) e biorreator anaeróbio de membranas (BRAM), tratando água
branca da máquina de papel produzindo papel kraft branqueado (Etapa 1)... 47
4.11. Dureza total (DT), dureza cálcio (DCa) e condutividade elétrica (C.E.), durante as Fases 1 e 2, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 1)... 48
4.12. Eficiências médias de remoção de dureza total (DT), sob diferentes tempos de detenção hidráulica (TDH) estimados, tratando água branca da máquina de papel produzindo papel
kraft branqueado (Etapa 1)... 49
4.13. Eficiências médias de remoção de dureza total (DT), sob as configurações de sistema biorreator anaeróbio convencional (BRAC) e biorreator anaeróbio a membranas (BRAM),
tratando água branca da máquina de papel produzindo papel kraft branqueado (Etapa 1).. 49
4.14. Sólidos suspensos totais (SST), sólidos suspensos fixos (SSF), sólidos suspensos voláteis (SSV), relação alimento/microrganismo (A/M) e taxa de utilização do substrato (U), durante as Fases 1 e 2, para o biorreator anaeróbio convencional (BRAC) e para o biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 1)... 51
5.1. Período, temperatura, vazão, tempo de detenção hidráulica (TDH), carga hidráulica volumétrica (CHV) e carga orgânica volumétrica (COV) do sistema de tratamento, durante as Fases 1, 2 e 3, para o biorreator anaeróbio convencional (BRAC) e para o biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel reciclado (Etapa 2)……….. 59
5.2. Análises físico-químicas da entrada e da saída...…….. 60
5.3. pH, ácidos orgânicos voláteis (AOV), alcalinidade total (AT) e alcalinidade bicarbonato (AB), durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio
convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água
branca da máquina de papel produzindo papel reciclado (Etapa 2)...……….. 64
5.4. Demanda química de oxigênio (DQO), bruta e solúvel, sólidos suspensos totais (SST) e turbidez, durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água
branca da máquina de papel produzindo papel reciclado (Etapa 2)……….. 67
5.5. Eficiências médias de remoção de demanda química de oxigênio (DQO), sob diferentes tempos de detenção hidráulica (TDH) estimados, tratando água branca da máquina de
papel produzindo papel reciclado (Etapa 2)...……….. 69
5.6. Eficiências médias de remoção de demanda química de oxigênio (DQO), sob as configurações de sistema biorreator anaeróbio convencional (BRAC) e biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel reciclado (Etapa
2)...………. 69
anaeróbio convencional (BRAC) e no biorreator anaeróbio de membranas (BRAM), sob diferentes tempos de detenção hidráulica (TDH) estimados, tratando água branca da máquina de papel produzindo papel reciclado (Etapa 2)...………...
Página
5.8. Eficiências médias de remoção de sólidos suspensos totais (SST), nos diferentes tempos de detenção hidráulica (TDH) estimados, sob as configurações de sistema biorreator anaeróbio convencional (BRAC) e no biorreator anaeróbio de membranas (BRAM),
tratando água branca da máquina de papel produzindo papel reciclado (Etapa 2)………… 70
5.9. Eficiências médias de remoção de turbidez, sob diferentes tempos de detenção hidráulica (TDH) estimados, tratando água branca da máquina de papel produzindo papel reciclado (Etapa
2)...………. 72
5.10. Eficiências médias de remoção de turbidez, sob as configurações de sistema biorreator anaeróbio convencional (BRAC) e biorreator anaeróbio de membranas (BRAM), tratando
água branca da máquina de papel produzindo papel reciclado (Etapa 2)...………. 72
5.11. Dureza total (DT), dureza cálcio (DCa), condutividade elétrica (C.E.) e cor real, durante as Fases 1, 2 e 3, na entrada e na saída do biorreator anaeróbio convencional (BRAC) e do biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel reciclado (Etapa
2)....……….. 73
5.12. Eficiências médias de remoção de dureza total (DT), sob diferentes tempos de detenção hidráulica (TDH) estimados, tratando água branca da máquina de papel produzindo papel
reciclado (Etapa 2)...………... 74
5.13. Eficiências médias de remoção de dureza total (DT), sob as configurações de sistema biorreator anaeróbio convencional (BRAC) e biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel produzindo papel reciclado (Etapa
2)... 74
5.14. Sólidos suspensos totais (SST), sólidos suspensos fixos (SSF), sólidos suspensos voláteis (SSV), relação alimento/microrganismo (A/M) e taxa de utilização do substrato (U), durante as Fases 1, 2 e 3, para o biorreator anaeróbio convencional (BRAC) e para o biorreator anaeróbio de membranas (BRAM), tratando água branca da máquina de papel
produzindo papel reciclado (Etapa 2)……….. 77
6.1. Período, temperatura, vazão, tempo de detenção hidráulica (TDH), carga hidráulica volumétrica (CHV) e carga orgânica volumétrica (COV) do sistema de tratamento para o biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e para o biorreator
anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de
papel produzindo papel kraft branqueado (Etapa 3)... 83
6.2. pH, ácidos orgânicos voláteis (AOV), alcalinidade total (AT) e alcalinidade bicarbonato (AB) na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água
branca da máquina de papel produzindo papel kraft branqueado (Etapa 3)... 86
6.3. Demanda química de oxigênio (DQO), sólidos suspensos totais (SST) e turbidez, na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da
máquina de papel produzindo papel kraft branqueado (Etapa 3)... 89
6.4. Eficiências médias de remoção de demanda química de oxigênio (DQO), sob diferentes temperaturas, tratando água branca da máquina de papel produzindo papel kraft
branqueado (Etapa 3)... 90
6.5. Eficiências médias de remoção de sólidos suspensos totais (SST), sob diferentes temperaturas, tratando água branca da máquina de papel produzindo papel kraft
branqueado (Etapa 3)... 91
6.6. Eficiências médias de remoção de turbidez, sob diferentes temperaturas, tratando água
6.7. Dureza total (DT), condutividade elétrica (C.E.) e cor real, na entrada e na saída do biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e do biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel
produzindo papel kraft branqueado (Etapa 3)... 93
6.8. Eficiências médias de remoção de dureza total (DT), sob diferentes temperaturas,
tratando água branca da máquina de papel produzindo papel kraft branqueado (Etapa 3).. 93
Página
6.9. Sólidos totais (ST), sólidos totais fixos (STF), sólidos totais voláteis (STV), relação alimento/microrganismo (A/M) e taxa de utilização do substrato (U), para o biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e para o biorreator anaeróbio de membranas termofílico (BRAM 55ºC), tratando água branca da máquina de papel
LISTA DE ABREVIATURAS
AB: Alcalinidade bicarbonato, mg CaCO3 l-1
Al: Alumínio
A/M: Taxa alimento/microrganismo, kg DBO kg SSV-1 d-1 ou kg DQO kg SSV-1 d-1
AOV: Ácidos orgânicos voláteis, mg HAc l-1
AT: Alcalinidade total, mg CaCO3 l -1
BRAC: Biorreator anaeróbio convencional
BRAM: Biorreator anaeróbio de membranas
CE: Condutividade elétrica, μS cm-1
CHV: Carga hidráulica volumétrica, m3 m-3 d-1
COT Carbono orgânico total, mg l-1 ou kg m-3
COV: Carga orgânica volumétrica, kg DBO m-3 d-1 ou kg DQO m-3 d-1
Cu: Cobre
DBO: Demanda bioquímica de oxigênio, mg l-1 ou kg m-3
DCa: Dureza cálcio, mg CaCO3 l -1
DQO: Demanda química de oxigênio, mg l-1 ou kg m-3
DT: Dureza total, mg CaCO3 l -1
Fe: Ferro
K: Potássio
MAP: Mono-amônio fosfato
Mn: Manganês
N: Nitrogênio
Na: Sódio
P: Fósforo
PVC: Policloreto de vinila
Q: Vazão, ml min-1 ou m3 d-1
SSF: Sólidos suspensos fixos, mg l-1
SST: Sólidos suspensos totais, mg l-1
SSV: Sólidos suspensos voláteis, mg l-1
ST: Sólidos totais, mg l-1
STF: Sólidos totais fixos, mg l-1
STV: Sólidos totais voláteis, mg l-1
TRS Tempo de retenção dos sólidos, h ou d
tsa: Tonelada seca ao ar
U: Taxa de utilização de substrato, kg DBO kg SSV-1 d-1 ou kg DQO kg SSV-1 d-1
UASB Upflow anaerobic sludge blanket
UC: Unidade de cor
UNT: Unidade nefelométrica de turbidez
Vr: Volume útil do biorreator, m3
RESUMO
LOURES, Ana Paula Santana, D.Sc., Universidade Federal de Viçosa, outubro de 2007. Tratamento anaeróbio de efluentes de máquina de papel por biorreator convencional e biorreator de membranas. Orientador: Cláudio Mudado Silva. Co-Orientadores: Ann Honor Mounteer e Carlos Augusto de Lemos Chernicharo.
O consumo de água fresca em fábricas de papel varia de acordo com o tipo de papel produzido,
podendo atingir 100 m3 por tonelada de papel. Assim, a recuperação da água branca torna-se uma
opção atrativa para reduzir o consumo de água fresca nas fábricas. Entretanto, nem sempre é possível
recuperar completamente a água branca em um circuito fechado devido à sua qualidade inadequada e
aos possíveis problemas causados pelo acúmulo de contaminantes. Uma forma de superar estes
problemas é a remoção destes contaminantes antes do reciclo da água. Na Etapa 1, este trabalho
comparou a eficiência de tratamento e a exeqüibilidade do reúso da água branca de um biorreator
anaeróbio convencional (BRAC) e de um biorreator anaeróbio de membranas (BRAM), sendo utilizada a
água branca coletada em uma fábrica de papel para imprimir e escrever. Na Fase 1, o sistema
convencional operou com um tempo de detenção hidráulica (TDH) de 27 h e uma carga orgânica
volumétrica (COV) de 0,24 kg DQO m-3 d-1; e, na Fase 2, com um TDH de 9 h e uma COV de
1,36 kg DQO m-3 d-1. Já o BRAM operou, na Fase 1, com um TDH de 26 h e uma COV de 0,33 kg DQO m-3 d-1,
e, na Fase 2, com um TDH de 9 h e uma COV de 0,85 kg DQO m-3 d-1. O BRAC alcançou eficiências de
remoção de 66% e 74% para demanda química de oxigênio (DQO), de 97% e 83% para sólidos
suspensos totais (SST) e 99% e 49% para turbidez, nas Fases 1 e 2, respectivamente. O BRAM
alcançou eficiências de remoção de 92% e 79% para DQO, de 99% e 90% para SST e 100% e 92%
para turbidez, nas Fases 1 e 2, respectivamente. Ambas as configurações apresentaram boa remoção
de dureza total. Um ligeiro aumento no pH e na condutividade elétrica foi observado. Estes resultados
indicam que o BRAM tem vantagens sobre o tratamento anaeróbio convencional na recuperação da
água branca tratada, especialmente devido à alta remoção dos sólidos suspensos e ao conteúdo
orgânico muito baixo presente no efluente tratado. Entretanto, os altos valores de dureza total e
condutividade elétrica no efluente, não removidas pelo processo biológico, podem tornar-se um
empecilho para um circuito de água branca completamente fechado. Na Etapa 2, esta pesquisa
comparou a eficiência de tratamento da água branca por um BRAC e por um BRAM, sendo utilizada a
água branca coletada em uma fábrica de papel reciclado. Na Fase 1, o sistema convencional operou
com um TDH de 7 h e COV de 14,8 kg DQO m-3 d-1; na Fase 2, com um TDH de 14 h e uma COV de
8,1 kg DQO m-3 d-1; e, na Fase 3, com um TDH de 24 h e uma COV de 4,7 kg DQO m-3 d-1. Já o BRAM
operou, na Fase 1, com um TDH de 8 h e uma COV de 13,4 kg DQO m-3 d-1; na Fase 2, com um
DQO m-3 d-1. O tratamento anaeróbio da água branca da máquina de papel produzindo papel reciclado
apresentou altas concentrações de ácidos orgânicos voláteis, refletindo em baixa eficiência de remoção
da DQO, turbidez e dureza total. Para SST, observou-se que o BRAM apresentou desempenho superior
ao BRAC. Na Etapa 3, este trabalho comparou a eficiência de tratamento e a exeqüibilidade do reúso da
água branca de um biorreator anaeróbio de membranas mesofílico (BRAM 35ºC) e de um biorreator
anaeróbio de membranas termofílico (BRAM 55ºC), sendo utilizada a água branca coletada em uma
fábrica de papel para imprimir e escrever. O BRAM 35ºC alcançou eficiências de remoção de 70% para
DQO, 95% para SST e 68% para turbidez, operando com um TDH de 10,1 h e uma COV de 1,41 kg
DQO m-3 d-1. Já o BRAM 55ºC alcançou eficiências de remoção de 55% para DQO, 97% para SST e
77% para turbidez, operando com um TDH de 9,8 h e uma COV de 1,46 kg DQO m-3 d-1. Ambas as
configurações apresentaram ligeira remoção de dureza total e aumento na condutividade elétrica e na
cor real. Embora o BRAM 55ºC tenha alcançado uma menor eficiência de remoção da DQO, ele tem
vantagens sobre o tratamento anaeróbio mesofílico, principalmente, por não necessitar do resfriamento
da água branca. Com os recentes desenvolvimentos nos materiais para membrana, pode ser possível
utilizar membranas poliméricas a uma temperatura de operação de 55ºC. A maior desvantagem
associada ao uso de membranas de fibras poliméricas ocas submersas é que sua utilização, a longo
ABSTRACT
LOURES, Ana Paula Santana, D.Sc., Universidade Federal de Viçosa, October of 2007. Anaerobic treatment of paper machine effluents by conventional bioreactor and membrane bioreactor. Adviser: Cláudio Mudado Silva. Co-Advisers: Ann Honor Mounteer and Carlos Augusto de Lemos Chernicharo.
Fresh water use in paper mills varies according to the type of paper produced, but it can be as high as
100 m3 per ton of paper. In order to reduce water use in paper mills, the reclamation of whitewater is an
attractive option. However, it is not always possible to completely recover the whitewater in a
closed-cycle manner due to the poor quality of this stream and the possible problems caused by the
accumulation of contaminants in the mill. One way to overcome this problem is to remove these
contaminants prior to water recycling. The first part of this work compared the efficiency of treatment and
the feasibility of whitewater reuse of an anaerobic conventional bioreactor (ACBR) and an anaerobic
membrane bioreactor (AMBR), using the whitewater collected from a writing and printing paper mill. In
Phase 1, the conventional system operated with a hydraulic retention time (HRT) of 27 h and a chemical
oxygen demand (COD) load of 0.24 kg COD m-3 d-1; and in Phase 2, with a HRT of 9 h and a COD
load of 1.36 kg COD m-3 d-1. In Phase 1, the AMBR operated with a HRT of 26 h and a COD load of 0.33 kg COD
m-3 d-1; and in Phase 2, with a HRT of 9 h and a COD load of 0.85 kg COD m-3 d-1. In the ACBR
configuration the removal efficiencies were 66% and 74% for COD, 97% and 83% for total suspended
solids (TSS) and 99% and 49% for turbidity, in Phases 1 and 2, respectively. In the AMBR configuration
the removal efficiencies were 92% and 79% for COD, 99% and 90% for TSS and 100% and 92% for
turbidity, in Phases 1 and 2, respectively. Both configurations showed good removal of total hardness. A
slight increase in pH and in electric conductivity was observed. These results indicated that the AMBR
has advantages over the conventional anaerobic treatment for reclaiming the treated whitewater,
especially due to the high removal of suspended solids and the very low organic content present in the
AMBR effluent. However, high values of hardness and electric conductivity in the effluent, not removed by
the biological process, might become a drawback for a fully closed whitewater circuit. The second part of
this research compared the efficiency of treatment of an ACBR and an AMBR, using the whitewater
collected from a recycling paper mill (Old Corrugated Cardboard). The conventional system operated, in
Phase 1, with HRT of 7 h and a COD load of 14.8 kg COD m-3 d-1; in Phase 2, with a HRT of 14 h and a
COD load of 8.1 kg COD m-3 d-1; and in Phase 3, with a HRT of 24 h and a COD load of 4.7 kg COD m-3
d-1. The AMBR operated, in Phase 1, with a HRT of 8 h and a COD load of 13.4 kg COD m-3 d-1; in Phase
2, with a HRT of 15 h and a COD load of 8.0 kg COD m-3 d-1; and in Phase 3, with a HRT of 23 h and a
COD load of 4.8 kg COD m-3 d-1. The anaerobic treatment of the whitewater from OCC paper machine
hardness. For TSS, the AMBR showed a better performance than the ACBR. The third part of this work
compared the efficiency of treatment and the feasibility of whitewater reuse of a mesophilic anaerobic
membrane bioreactor (35ºC AMBR) and a thermophilic anaerobic membrane bioreactor (55ºC AMBR),
using the whitewater collected from a writing and printing paper mill. In the 35ºC AMBR configuration, the
removal efficiencies were 70% for COD, 95% for TSS and 68% for turbidity, operating with a HRT of 10.1 h
and a COD load of 1.41 kg COD m-3 d-1. In the 55ºC AMBR configuration, the removal efficiencies were
55% for COD, 97% for TSS and 77% for turbidity, operating with a HRT of 9.8 h and a COD load of
1.46 kg COD m-3 d-1. Both configurations showed slight removal of total hardness and an increase in
electric conductivity and real colour. Although COD removal at 55ºC was lower than at 35ºC, the 55ºC
AMBR has advantages over the mesophilic anaerobic treatment mainly because it does not need the
whitewater cooling. With recent developments in membrane materials, it may be possible to use
polymeric membranes at an operating temperature of 55ºC. The major disadvantage associated with
using polymeric submerged hollow fiber membranes is that their long-term use at elevated temperatures
1. INTRODUÇÃO GERAL
As fábricas de papel utilizam grandes quantidades de água fresca em comparação a outros tipos
de processos industriais. A água é utilizada em vários setores da fábrica, como meio de transporte de
fibras, formação da folha de papel e a preparação de aditivos e também nos processos auxiliares, como
resfriamento, selagem de equipamentos, limpeza, lubrificação, dentre outros.
Os despejos líquidos da fabricação de papel originam-se, principalmente, na máquina de papel,
nos refinadores, nas caixas de regulagem de consistência e na mistura de massa nas peneiras
depuradoras, sendo chamada de água branca. As cargas poluidoras dependem, fundamentalmente, do
tipo de papel fabricado e da prática ou não da recirculação da água branca. De modo geral, este efluente
contém fibras celulósicas, finos e outros aditivos químicos específicos como amido, cola,
anti-espumantes e caulim.
Diversos são os motivos que tornam a recirculação de água branca vantajosa. A reciclagem de
água dentro da fábrica permite a recuperação de matéria prima e reagentes químicos (DEXTER, 1996;
THOMPSON et al., 2001), além de reduzir os custos no descarte do resíduo sólido. A maior parte destes
sólidos é constituída por fibras que representam 5% do total de fibras para papéis pesados (CPRH,
1998). Portanto, sem recuperação, uma fábrica que produz 200 t d-1 de papel perde diariamente 10 t d-1
de material fibroso. Para papéis finos, tal perda pode chegar a 50%.
A recuperação do efluente é economicamente mais atrativa já que o consumo de água na
indústria é alto, bem como os investimentos das instalações e dos equipamentos das estações de
tratamento de água fresca. O consumo de água varia com o tipo de papel sendo produzido e pode ser
tão alto quanto 60 m3 por tonelada de papel produzido, mesmo com as técnicas operacionais mais
modernas e eficientes. Na Alemanha, o volume de efluente gerado pela indústria de papel varia de 5 a
22 m3 t-1 de papel, com exceção das indústrias que produzem papéis especiais, cujo consumo pode ser
acima de 100 m3 t-1 de papel (HAMM e SCHABEL, 2006). No Brasil, as fábricas modernas já possuem
consumo de água em torno de 30 m3 tsa-1, enquanto as fábricas mais antigas podem consumir até
100 m3 tsa-1. A média atual de consumo de água está na faixa de 50 m3 tsa-1.
O custo do tratamento para toda a água residuária na indústria é elevado devido aos custos de
instalação e de operação das estações de tratamento de efluentes. No Brasil, onde existem muitas
empresas operando com máquinas de papel usadas e/ou adquiridas de fabricantes maiores, a vazão
dos despejos é extremamente variável, por exemplo, na fabricação de papéis para impressão e/ou
escrita com colagem alcalina, a vazão é de 15 m3 t-1; para impressão e/ou escrita com colagem
ácida, de 23 m3 t-1; para jornal, de 11 m3 t-1; e para cartão duplex, de 18 m3 t-1 (CPRH, 1998).
No caso de projetos de expansão de fábricas, a capacidade limitada da estação de tratamento
de água fresca e de efluente, bem como as crescentes exigências impostas pela legislação em relação à
vazão de água bruta passível de ser captada pela indústria e à qualidade do efluente a ser lançado no
corpo d’água receptor, podem constituir um obstáculo. Assim, a reciclagem do efluente da máquina de
papel pode ser uma alternativa e/ou solução viáveis. Isto implica em trabalhar com um circuito mais
fechado de água branca, ou seja, buscar operar com uma geração mínima de efluente.
água branca reciclada. Em algumas situações, estes custos podem sobrepor as economias citadas
anteriormente, especialmente onde se realiza um sistema com alto grau de fechamento de circuito de
água branca. Mesmo não havendo uma vantagem econômica, o reúso da água oferece uma vantagem
de marketing a longo prazo, simplesmente porque a água fresca será o objeto de utilidade mais precioso
no mundo inteiro. Assim, um alto consumo de água será considerado uma agressão ao meio ambiente.
A remoção da matéria orgânica biodegradável com processos anaeróbios une o tratamento de
despejo com a produção de energia, oferecendo uma rara oportunidade de um retorno potencialmente
positivo do capital investido no tratamento, assim como de minimização dos custos operacionais. Ambas
as características e a quantidade de compostos orgânicos biodegradáveis nos efluentes da indústria de
papel tornam o tratamento anaeróbio uma alternativa economicamente atrativa em relação aos
processos de tratamento aeróbios tradicionalmente empregados (LEE, 1993).
O sucesso dos reatores anaeróbios de alta taxa é atribuído à sua capacidade de retenção de
biomassa através de uma separação efetiva do tempo de retenção dos sólidos (TRS) do tempo de
detenção hidráulica (TDH), permitindo altas cargas e baixos TDH. O consórcio bacteriano anaeróbio é
essencial, sendo imobilizado dentro dos grânulos. A diversidade e a distribuição das bactérias são
determinadas por diversos fatores físico-químicos e biológicos (LEPISTÖ e RINTALA, 1999).
Membranas de micro ou ultrafiltração podem ser convenientemente acopladas a um reator
biológico para permitir o aumento do TRS e melhorar a eficiência do tratamento. Em particular, as
Archaea metanogênicas têm velocidades de crescimento mais lentas que os microrganismos aeróbios e,
assim, produzem menores quantidades de lodo residual, porém, requerem um espaço de tempo
relativamente longo através de um reator de mistura completa clássico para evitar sua remoção não
intencional do mesmo. Além disso, a emissão de gás residual e a conseqüente flotação de sólidos
tornam a separação completa impraticável no clarificador final. Assim, reatores anaeróbios, incorporando
micro ou ultrafiltração como etapa de separação, têm sido aplicados para reter os sólidos
completamente e melhorar o efluente (CHOO e LEE, 1996; ELMALEH e ABDELMOUMNI, 1998).
Os efluentes da máquina de papel podem possuir temperaturas superiores a 40ºC, ou seja, fora
da faixa ideal para o tratamento mesofílico. Atualmente, algumas fábricas que possuem um nível alto de
reúso de água necessitam de resfriamento, o qual é realizado em torres de resfriamento e/ou trocadores
de calor. O tratamento biológico em temperatura termofílica vem sendo estudado por não necessitar do
prévio resfriamento do afluente, economizando energia.
Verificando a lacuna existente em relação à operacionalidade e viabilidade de um sistema de
tratamento anaeróbio, especificamente para o efluente da máquina de papel, principalmente, em
condições típicas e reais de operação de uma fábrica nacional, buscou-se, com o presente trabalho,
comparar os desempenhos de um biorreator anaeróbio convencional (BRAC) e de um biorreator
anaeróbio de membranas (BRAM), sob diferentes cargas de aplicação e tempos de detenção hidráulica.
Estudou-se, igualmente, os tratamentos anaeróbios mesofílico e termofílico, procurando adequar-se às
condições de temperatura do citado efluente. Além disso, cabe ressaltar que este experimento foi
conduzido paralelamente ao experimento do sistema de tratamento aeróbio, com o objetivo de se
2. REVISÃO BIBLIOGRÁFICA
2.1. FABRICAÇÃO DE PAPEL
Desde os primórdios da história e ao longo das civilizações que se sucederam ou conviveram no
nosso planeta, pode ser observada uma preocupação ininterrupta visando conseguir um registro das
idéias, dos pensamentos e das experiências de vida que configuraram alguns fatos históricos relevantes,
dignos de serem preservados para o benefício de futuras gerações. O homem começou a registrar sua
história por volta de 6.000 a.C., e a escrita surgiu independentemente no Egito, na Mesopotâmia e na
China. Pedra, madeira, placas de barro, papiro, pergaminho, cânhamo, capim, palha, trapos velhos,
todos foram materiais para escrita usados pela humanidade durante séculos (ARACRUZ, 2007).
Oficialmente, o papel foi fabricado pela primeira vez na China, no ano de 105 d.C., por Ts'Ai Lun
que fragmentou, em uma tina com água, cascas de amoreira, pedaços de bambu, rami, redes de pesca,
roupas usadas e cal para ajudar no desfibramento. Na pasta formada, submergiu uma forma de madeira
revestida por um fino tecido de seda - a forma manual - como seria conhecida. Esta forma coberta de
pasta era retirada da tina e, com a água escorrendo, deixava sobre a tela uma fina folha que era
removida e estendida sobre uma mesa. Esta operação era repetida e as novas folhas eram colocadas
sobre as anteriores, separadas por algum material. As folhas, então, eram prensadas para perder mais
água e, posteriormente, colocadas uma a uma, em muros aquecidos para a secagem (BRACELPA,
2007).
A idéia de Ts'Ai Lun, "a desintegração de fibras vegetais por fracionamento, a formação da folha
retirando a pasta da tina por meio de forma manual, procedendo-se ao deságüe e posterior aquecimento
para secagem", continua válida até hoje (BRACELPA, 2007).
O crescimento do uso do papel conduziu a uma procura por matérias primas novas. Em 1840,
um alemão chamado Keller teve a idéia de moer a madeira em um moinho para extrair a fibra. Isto
produziu a primeira polpa de madeira. A tecnologia de fabricação de papel fez grandes avanços desde
então, sendo as principais fases deste processo representadas na Figura 2.1 (CELULOSEONLINE,
2007).
A madeira é a matéria prima na fabricação de papel, sendo o eucalipto a principal árvore usada
neste processo no Brasil. Devido às condições climáticas favoráveis no país, após sete anos em média,
as árvores estão prontas para serem cortadas. Após o corte, as toras são descascadas e picadas para
serem transformadas em cavacos, os quais são separados pelo tamanho na peneira (Figura 2.1). As
cascas são separadas e usadas como combustível em caldeira de biomassa para produzir vapor e
Figura 2.1. Principais etapas na fabricação de papel (PAPER MACHINE, 2007).
A madeira é composta, principalmente, de fibras celulósicas aderidas umas às outras com uma
"cola" chamada lignina. Para converter madeira em polpa, deve-se separar estas fibras, ou seja,
remover a lignina. A polpação ou separação das fibras é realizada por meios químicos ou mecânicos ou
por uma combinação de ambos. A polpação química tem como objetivo a remoção seletiva da lignina,
retirando-a em diferentes intensidades e procurando-se preservar ao máximo a celulose e as
hemiceluloses (GOMIDE, 1979).
No Brasil, o processo mais comumente empregado é a polpação química pelo processo "kraft"
que, em alemão, quer dizer "forte". No processo kraft, a celulose e a lignina são separadas no digestor
(Figura 2.1) com o auxílio dos reagentes químicos hidróxido de sódio (NaOH) e sulfeto de sódio (Na2S),
a temperaturas entre 160 e 180ºC, sendo a lignina despolimerizada e dissolvida. O processo de
polpação termina quando a polpa ainda contém entre 5 e 10% de lignina, pois uma deslignificação mais
extensa pode danificar a fibra e prejudicar a qualidade da polpa (NOLASCO et al., 2000, 2001; SOUZA,
2001).
O licor resultante, contendo os reagentes químicos e os subprodutos gerados na decomposição
dos constituintes da madeira (NaOH + Na2S + lignina + H2O), é chamado licor negro fraco. Este licor
possui muita água na sua composição (15% de sólidos), assim sendo, após o digestor, o mesmo é
concentrado através do processo de evaporação, depois do qual, passa a ser denominado licor negro
forte (> 70% de sólidos) (CASSIM, 2004). Em uma etapa posterior, este licor é incinerado na caldeira de
recuperação (Figura 2.1) com o objetivo de gerar vapor e energia e recuperar compostos inorgânicos
para reutilização no processo industrial. Desta forma, é também eliminada uma fonte potencial de
poluição da água e o processo torna-se mais econômico (NOLASCO et al., 2000, 2001; SOUZA, 2001).
Para a fabricação de certos tipos de papel, a celulose resultante deve ser branqueada (Figura
dissolver ou eliminar a lignina restante. A polpa final não só é mais branca, como também tem uma
tendência menor de amarelar com o passar do tempo, ou seja, de sofrer reversão de alvura.
Quando a polpa chega à caixa de entrada da máquina de papel (Figura 2.1), seu conteúdo de
água excede 99%. A mistura é lançada sob a forma de um jato fino e uniforme sobre uma tela móvel
denominada tela formadora. A ação filtrante desta tela formadora, combinada com um sistema de vácuo,
extrai a maior parte da água contida na polpa formando, assim, a folha de papel. A folha é prensada
entre rolos para remover mais água e, então, atravessa a seção de secagem, onde entra em contato
com cilindros geralmente aquecidos com vapor, extraindo a maior parte da água restante através da
evaporação. No final da máquina, o papel é enrolado em rolo jumbo, os quais são rebobinados e
segmentados em rolos menores, seguindo para a seção de conversão ou de acabamento.
Quando a massa é lançada na tela da máquina, a água de drenagem (água branca) é,
geralmente, colhida em bandejas colocadas abaixo da tela (Figura 2.2). ROMERO (2001) caracterizou a
água branca como a água do desaguamento da máquina de papel, com teores de fibras entre 700 e
4.000 mg l-1, com temperatura de 40 a 50ºC e com alta concentração de produtos químicos (cola, carga
mineral, alumínio, alvejante óptico). Após a coleta, a água passa por equipamentos de recuperação de
fibras, sendo usada para a diluição da massa. A água proveniente das caixas de sucção é coletada em
recipiente diferente da água da tela e utilizada, em geral, para a lavagem desta. Uma maior proporção
de água branca volta a ser permanentemente usada, o que diminui a poluição hídrica e possibilita a
economia de matéria fibrosa e de produtos químicos. As cargas poluidoras dos despejos líquidos da
fabricação de papel dependem fundamentalmente do tipo de papel fabricado e da prática ou não da
recirculação do efluente gerado na máquina de papel pela formação e prensagem da folha.
Figura 2.2. Sistema de água branca (D’ALMEIDA, 1988).
Tradicionalmente, os programas de controle dos efluentes hídricos enfocam apenas as estações
de tratamento. No entanto, as fábricas mais modernas têm adotado o controle na própria fonte de
2.2. REATORES ANAERÓBIOS
Há anos, a digestão anaeróbia tem sido utilizada para a estabilização de lodos de águas
residuárias. Em anos mais recentes, entretanto, tem sido empregada com sucesso para o tratamento de
efluentes doméstico e industrial. Isto se tornou possível através de uma melhor compreensão da
microbiologia do processo e do aperfeiçoamento do projeto dos reatores. O processo anaeróbio
apresenta diversas vantagens em relação ao processo aeróbio (RINTALA e PUHAKKA, 1994;
CHERNICHARO, 1997; BITTON, 1999; FORESTI et al., 1999; BERNI e BAJAY, 2001; THOMPSON et
al., 2001):
1. A digestão anaeróbia usa o dióxido de carbono (CO2) prontamente disponível como aceptor de
elétrons, não requerendo oxigênio elementar (O2), cujo suprimento aumenta substancialmente
os custos do tratamento do efluente.
2. A digestão anaeróbia produz menores quantidades de lodo estabilizado (3 a 20 vezes menos
que nos processos aeróbios), pois o rendimento energético dos microrganismos anaeróbios é
relativamente baixo. A maioria da energia derivada da quebra do substrato é encontrada no
produto final, o metano (CH4). Em relação ao crescimento celular, 50% do carbono orgânico é
convertido em biomassa sob condições aeróbias enquanto apenas 5% é convertido em
biomassa sob condições anaeróbias.
3. A digestão anaeróbia produz um gás combustível, o metano, que contém cerca de 90% de
energia, tem um teor calorífico de aproximadamente 9.000 kcal m-3 e pode ser queimado para
fornecer aquecimento aos digestores ou para gerar eletricidade. Uma pequena quantidade de
energia (3 a 5%) é perdida na forma de calor. A produção de metano contribui na redução da
demanda bioquímica de oxigênio (DBO) no lodo digerido.
4. A energia requerida para o tratamento de efluente é menor que nos processos aeróbios.
5. A digestão anaeróbia é adequada para efluentes industriais com alta carga orgânica.
6. Há a possibilidade de aplicação de altas taxas de carregamento no digestor.
7. A atividade dos microrganismos anaeróbios é preservada, mesmo que o digestor não receba
alimentação por longos períodos de tempo.
8. A demanda de área para a instalação do sistema de tratamento é baixa.
9. O consumo de nutrientes é baixo.
Algumas desvantagens da digestão anaeróbia são:
1. É um processo mais lento que a digestão aeróbia.
2. É sensível à inibição por diversos compostos tóxicos.
3. A partida do processo requer longos períodos, embora a utilização de inóculo de alta qualidade
(por exemplo, lodo granular) possa aumentar a velocidade do processo.
4. Há a possibilidade de geração de maus odores.
2.2.1. Fundamentos da digestão anaeróbia
A digestão anaeróbia é um processo biológico no qual um consórcio de diferentes tipos de
microrganismos, na ausência de oxigênio (O2), promove a transformação de compostos orgânicos
complexos (carboidratos, proteínas e lipídeos) em produtos mais simples como metano (CH4) e dióxido
de carbono (CO2) (FORESTI et al., 1999).
Em um digestor anaeróbio, as duas principais vias envolvidas na formação de CH4 são (1) a
conversão do hidrogênio (H2) e do dióxido de carbono (CO2) a CH4 e água (H2O) e (2) a conversão do
acetato (CH3COO
-) a CH4 e CO2 (TCHOBANOGLOUS e BURTON, 1991). A formação de CH4 não
ocorre em ambientes onde O2, nitrato (NO3
-) ou sulfato (SO4
2-) encontram-se prontamente disponíveis
como aceptores inorgânicos de elétrons (CHERNICHARO, 1997).
CHERNICHARO (1997) relata que a digestão anaeróbia de compostos orgânicos complexos é
normalmente considerada um processo de dois estágios. No primeiro estágio, um grupo de bactérias
facultativas e anaeróbias, denominadas formadoras de ácidos ou fermentativas, converte os orgânicos
complexos em outros compostos. Compostos orgânicos complexos como carboidratos, proteínas e
lipídeos são biologicamente convertidos em materiais orgânicos mais simples, principalmente ácidos
voláteis. No segundo estágio, ocorre a conversão dos ácidos orgânicos, CO2 e H2 em produtos finais
gasosos, o CH4 e o CO2. Esta conversão é efetuada por um grupo especial de bactérias, denominadas
formadoras de metano, as quais são estritamente anaeróbias.
TCHOBANOGLOUS e BURTON (1991) citam que as Archaea metanogênicas são capazes de
utilizar o hidrogênio produzido pelas acidogênicas devido à sua eficiente hidrogenase. Como as
metanogênicas são capazes de manter uma pressão parcial de H2 extremamente baixa, o equilíbrio das
reações de fermentação é deslocado para a formação de mais produtos finais oxidados (por exemplo,
formato e acetato).
As Archaea metanogênicas dependem do substrato fornecido pelas acidogênicas, e estas, por
sua vez, dependem das primeiras para a remoção dos compostos que poderiam inibir o seu
crescimento, configurando, portanto, uma interação sintrófica (mutuamente benéfica)
(TCHOBANOGLOUS e BURTON, 1991; CHERNICHARO, 1997).
Uma vez que as Archaea metanogênicas são responsáveis pela etapa final da degradação do
resíduo, a sua baixa taxa de crescimento e de utilização dos ácidos orgânicos, normalmente, representa
o fator limitante no processo de digestão como um todo (TCHOBANOGLOUS e BURTON, 1991;
CHERNICHARO, 1997). A degradação sintrófica de butirato, propionato ou ácidos graxos de cadeia
ramificada acontece sob condições que deixam somente a quantidade mínima de energia para o
organismo parceiro e isto pode explicar porque estes têm o crescimento lento, executando todas as suas
reações biossintéticas na dependência da energia fornecida por estes incrementos mínimos de energia
(SCHINK, 2002).
FORESTI et al. (1999) relatam que, nos reatores anaeróbios, a formação de CH4 é altamente
desejável, uma vez que a matéria orgânica, geralmente medida como demanda química de oxigênio
(DQO), é efetivamente removida da fase líquida, pois o CH4 apresenta baixa solubilidade em água
(TCHOBANOGLOUS e BURTON, 1991). Assim, a conversão dos compostos orgânicos em CH4 é eficaz
na remoção do material orgânico, apesar de não promover a sua oxidação completa, a exemplo de
Os diferentes grupos de bactérias e Archaea que transformam o material orgânico afluente têm
todos atividade catabólica e anabólica. Deste modo, paralelo à liberação dos diferentes produtos de
fermentação, há a formação de novas células, dando origem a quatro populações bacterianas no
digestor anaeróbio. Para conveniência, muitas vezes os três primeiros processos juntos são chamados
de fermentação ácida, que deve ser completada com a metanogênese (VAN HAANDEL e LETTINGA,
1994).
Uma representação esquemática das fases da digestão anaeróbia é apresentada na Figura 2.3.
Figura 2.3. Seqüências metabólicas envolvidas na digestão anaeróbia (os números referem-se a percentagens da DQO) (VAN HAANDEL e LETTINGA, 1994; FORESTI et al., 1999).
2.2.1.1. Hidrólise
Diversos autores (TCHOBANOGLOUS e BURTON, 1991; LEE, 1993; VAN HAANDEL e
LETTINGA, 1994; CHERNICHARO, 1997; FORESTI et al., 1999) registram que, nesta etapa, o material
orgânico particulado é convertido em compostos dissolvidos de menor peso molecular (Figura 2.3). O
processo requer a interferência das chamadas exoenzimas – enzimas proteolíticas, lipolíticas, ureolíticas
ou celulolíticas – que são excretadas pelas bactérias fermentativas. As proteínas são degradadas em
polipeptídeos para formarem aminoácidos; os carboidratos, transformados em açúcares solúveis (mono
e dissacarídeos); e os lipídeos, convertidos a ácidos graxos de cadeia longa (C13 a C27) e glicerina, os
quais podem atravessar as paredes celulares das bactérias fermentativas. Na prática de tratamento de
efluente, a velocidade de hidrólise pode ser a etapa limitante para todo o processo da digestão
anaeróbia.
MATERIAL ORGÂNICO EM SUSPENSÃO PROTEÍNAS, CARBOIDRATOS, LIPÍDEOS
AMINOÁCIDOS, AÇÚCARES ÁCIDOS GRAXOS
CH3COCOO
-(piruvato)
CH3CH2COO
-(propionato) OUTROS
ÁCIDOS ORGÂNICOS
CH3COO
(acetato) H2 + CO2
CH4 + CO2
21 40
34 39 5
34 66
46 5
15
35 11 9 6 4 1 23 11
70 30
Hidrólise
Acidogênese
Acetogênese
Metanogênese
Acetotrófica Hidrogenotrófica
2.2.1.2. Acidogênese
Segundo diferentes autores (TCHOBANOGLOUS e BURTON, 1991; LEE, 1993; VAN HAANDEL
e LETTINGA, 1994; CHERNICHARO, 1997; FORESTI et al., 1999), os compostos dissolvidos, gerados
no processo de hidrólise ou liquefação, são absorvidos nas células das bactérias fermentativas e, após a
acidogênese (Figura 2.3), excretados como substâncias orgânicas simples como ácidos orgânicos
voláteis de cadeia curta (AOV) – tais como ácidos acético, butírico, lático, propiônico etc. –, álcoois – tais
como etanol, butanol, metanol – e compostos minerais como amônia (NH3), sulfeto de hidrogênio (H2S).
A acidogênese é realizada por um grupo diversificado de bactérias (Tabela 2.1), das quais a maioria é
estritamente anaeróbia. Entretanto, algumas espécies são facultativas e podem metabolizar o material
orgânico por via oxidativa. Isto é importante nos sistemas de tratamento anaeróbio de efluentes porque o
oxigênio dissolvido, eventualmente presente, poderia se tornar uma substância tóxica para as Archaea
metanogênicas se não fosse removido pelas bactérias acidogênicas facultativas.
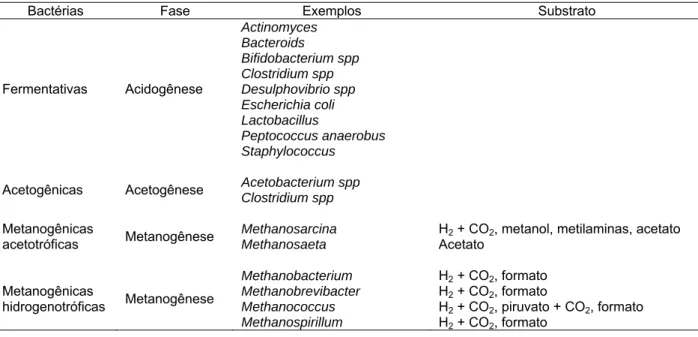
Tabela 2.1. Exemplos de grupos bacterianos envolvidos na digestão anaeróbia, segundo diferentes autores (TCHOBANOGLOUS e BURTON, 1991; LEE, 1993; CHERNICHARO, 1997; MADIGAN et al., 2004)
Bactérias Fase Exemplos Substrato
Fermentativas Acidogênese
Actinomyces Bacteroids
Bifidobacterium spp Clostridium spp Desulphovibrio spp Escherichia coli Lactobacillus
Peptococcus anaerobus Staphylococcus
Acetogênicas Acetogênese Acetobacterium spp
Clostridium spp
Metanogênicas
acetotróficas Metanogênese
Methanosarcina Methanosaeta
H2 + CO2, metanol, metilaminas, acetato
Acetato
Metanogênicas
hidrogenotróficas Metanogênese
Methanobacterium Methanobrevibacter Methanococcus Methanospirillum
H2 + CO2, formato
H2 + CO2, formato
H2 + CO2, piruvato + CO2, formato
H2 + CO2, formato
2.2.1.3. Acetogênese
De acordo com diversos autores (TCHOBANOGLOUS e BURTON, 1991; LEE, 1993; VAN
HAANDEL e LETTINGA, 1994; CHERNICHARO, 1997; FORESTI et al., 1999), as bactérias
acetogênicas são responsáveis pela oxidação dos produtos gerados na fase acidogênica em substrato
apropriado para as Archaea metanogênicas, ou seja, os ácidos orgânicos mais elaborados – tais como
ácidos propiônico e butírico – são, subseqüentemente, transformados a hidrogênio, dióxido de carbono e
acetato pelas bactérias acetogênicas (Figura 2.3). Dessa forma, as bactérias acetogênicas fazem parte
de um grupo metabólico intermediário, que produz substrato para as metanogênicas.
A acetogênese, etapa essencial na conversão de compostos intermediários em acetato, é