PROF. DELBY FERNANDES DE MEDEIROS
PROGRAMA DE PÓS-GRADUAÇÃO EM PRODUTOS NATURAIS E SINTÉTICOS BIOATIVOS
AVALIAÇÃO DA UTILIDADE DE UM SOFTWARE DE SIMULAÇÃO CROMATOGRÁFICA NA SEPARAÇÃO DE FLAVONÓIDES POR CLAE-DAD DE
FASE REVERSA
JOSÉ WILSON FIGUEIREDO JÚNIOR
UNIVERSIDADE FEDERAL DA PARAÍBA
LABORATÓRIO DE TECNOLOGIA FARMACÊUTICA PROF. DELBY FERNANDES DE MEDEIROS
PROGRAMA DE PÓS-GRADUAÇÃO EM PRODUTOS NATURAIS E SINTÉTICOS BIOATIVOS
AVALIAÇÃO DA UTILIDADE DE UM SOFTWARE DE SIMULAÇÃO CROMATOGRÁFICA NA SEPARAÇÃO DE FLAVONÓIDES POR CLAE-DAD DE
FASE REVERSA
JOSÉ WILSON FIGUEIREDO JÚNIOR
Orientação: Prof. Dr. Eduardo de Jesus Oliveira
Dissertação submetida como requisito parcial para obtenção do grau de Mestre em Produtos Naturais e Sintéticos Bioativos. Área de concentração em Farmacoquímica.
Ficha Catalográfica
F475a Figueiredo Júnior, José Wilson.
Avaliação da utilidade de um software de simulação cromatográfica na separação de Flavonóides por CLAE-DAD de fase reversa / José Wilson Figueiredo Junior. - - João Pessoa: UFPB, 2008.
129 f.: il.
Orientador: Eduardo de Jesus Oliveira.
Dissertação (Mestrado) – UFPB, CCS, LTF, Pós- Graduação em Produtos Naturais e Sintéticos Bioativos.
1. Substâncias naturais. 2. CLAE- Cromatografia Líquida de Alta Eficiência. 3. Software- simulação. 4. Flavonóides - separação
AVALIAÇÃO DA UTILIDADE DE UM SOFTWARE DE SIMULAÇÃO CROMATOGRÁFICA NA SEPARAÇÃO DE FLAVONÓIDES POR CLAE-DAD DE
FASE REVERSA
JOSÉ WILSON FIGUEIREDO JÚNIOR
Aprovada em 24 de ABRIL DE 2008
Prof. Dr. Eduardo de Jesus Oliveira__________________________________ (CCS-LTF-UFPB)
(Orientador)
Profa. Dra. Fernanda Nervo Raffin __________________________________ (DTFA-CCS-UFRN)
Membro externo
Prof. Dr. José Marcelino Oliveira Cavalheiro___________________________ (DTQA-CT-UFPB)
Membro Interno
Dedico este trabalho aos meus pais José Wilson Figueiredo (in memorian) e Nelma Dorian Cavalcante por todo o amor, carinho e incentivo em todas as descobertas e conquistas da minha vida.
AGRADECIMENTOS
- Ao Criador que continua escrevendo e narrando minha estória neste mundo;
- Aos meus Pais, irmãs e familiares que sempre me apoiaram na minha carreira acadêmica. - Ao Professor Dr. Eduardo de Jesus Oliveira, por ter me aceito em sua equipe de pesquisas. Por sua amizade, compreensão e paciência ao guiar-me nas lições que moldaram minha visão do mundo científico.
- A Dra. Eliete Nascimento Borges, Diretora-Presidente da Policia Técnica Cientifica do Amapá pela amizade, sensibilidade, compreensão e incentivo que permitiram me realizar este trabalho de pesquisa.
Ao amigo e colega de equipe de pesquisa Roberto Jefferson Bezerra de Nascimento, pelo companheirismo e amizade em todo o percurso da pesquisa sem o qual não poderia ter tido êxito.
- Ao LTF, UFPB e CNPq, pela oportunidade, acolhimento e apoio financeiro.
- Aos amigos e colegas de laboratório, Antonio Cláudio, Adriana Fernandes, Cibele Cabral, Francinalva Medeiros, Gustavo de Castro, Ionaldo Diniz, Kiriaki Nurit, Kristerson Reinaldo, Marajane Medeiros, Sócrates Golzio e Stanley Chavéz cuja parceria e apoio me foram essenciais na conclusão deste trabalho.
RESUMO
AVALIAÇÃO DA UTILIDADE DE UM SOFTWARE DE SIMULAÇÃO CROMATOGRÁFICA NA SEPARAÇÃO DE FLAVONÓIDES POR CLAE-DAD DE
FASE REVERSA José Wilson Figueiredo Júnior
Mestrado em Produtos Naturais e Sintéticos Bioativos (Farmacoquímica)
Laboratório de Tecnologia Farmacêutica, UFPB, Caixa Postal 5009, Cep 58051-970 João Pessoa, Paraíba, Brasil. (w.figueiredojr@gmail.com)
A Cromatografia Líquida de Alta Eficiência (CLAE) permite análises químicas qualitativas e quantitativas, separando e identificando substâncias em misturas com rapidez e eficiência. Entretanto, os fatores que governam a retenção cromatográfica são complexos e a fase de desenvolvimento de métodos consome muitos recursos. Em nosso trabalho nós avaliamos um pacote de softwares de simulação cromatográfica (HIPAC-G, HIPAC-B e HIPAC-S, Phenomenex, Torrance, USA) para otimização da separação cromatográfica de oito padrões de flavonóides: (3-O-[β-D-glicopiranosil-(1→6)-α-L-ramnopiranosil]-7-O-α-L -ramnopiranosilkanferol; hesperidina; kanferol; tilirosideo; quercetina; 3,4’,7,8-tetra-O -metil-gossipetina; 3,3’,4’,7,8-penta-O-metil-gossipetina; 3,3’,4’,7-tetra-O-metil-quercetina). O modelo de retenção do HIPAC se baseia na conhecida relação linear entre o fator de retenção de um analito e a porcentagem de solvente orgânico na fase móvel para simulação de dados de retenção. Utilizando eluição em modo gradiente, três corridas preliminares foram realizadas (corridas preliminares são usadas para inserir dados de retenção para o software). A primeira corrida preliminar usou uma coluna C18 (250 x 4,6 mm, 5 m) e como fase móvel um gradiente de 5 a 95% de acetonitrila (solvente B) e acido fórmico a 0,1% (solvente A) a um fluxo de 1 mL/min com detecção no ultravioleta a 264 nm. A primeira corrida preliminar foi composta de duas corridas em modo gradiente usando as mesmas condições cromatográficas, mas com diferentes durações de tempo de gradiente (30 e 60 minutos respectivamente). A segunda corrida preliminar utilizou as mesmas condições cromatográficas da primeira, mas como modificador orgânico usou metanol ao invés de acetonitrila e %B inicial e final de 10% e 100%, respectivamente. A terceira corrida preliminar foi feita com as mesmas condições cromatográficas da segunda corrida, mas utilizando uma coluna com fase estacionária e dimensões diferentes (C8, 150 x 4,6 mm, 5 m). Os dados de retenção das três corridas preliminares foram usados para alimentar o software de simulação, utilizando o módulo HIPAC-G. Para simulação em modo isocrático usou-se o módulo HIPAC-B, tanto com uma coluna C8 (150 x 4,6 mm, 5 m) quanto C18 (250 x 4,6 mm 5 m) e misturas binárias de MeOH (Solvente B) em 0,1% de ácido fórmico (Solvente A). Duas corridas preliminares com 60% e 70%B foram realizadas para cada coluna e os dados de retenção resultantes foram usados para alimentar a simulação. As condições otimizadas de separação sugeridas pelo HIPAC-B foram usadas como dados para inserção no HIPAC-S para otimizar as condições do sistema cromatográfico. O critério de otimização utilizado para todas as simulações foi a resolução média global para todos os picos no cromatograma. No total, doze simulações em modo gradiente e quatro simulações em modo isocrático foram realizadas. Os dados de retenção simulados foram comparados com os dados experimentalmente obtidos para os oito flavonóides padrões. O coeficiente de correlação (r2) entre os tempos simulados e observados para analitos
eluídos em modo gradiente variaram de 0,9416 a 0,9992 (n=12). O coeficiente de correlação em modo isocrático variou de 0.9999 a 1 (n=4), indicando excelente eficiência em predizer dados de retenção para a mistura testada. Tomados em conjunto, nossos resultados mostram que o uso de softwares de simulação cromatográfica tal como HIPAC-G, HIPAC-B e HIPAC-S podem constituir uma importante ferramenta na otimização das condições de separação de misturas complexas, tais como as que são encontradas no campo de produtos naturais.
ABSTRACT
USEFULNESS OF A CHROMATOGRAPHY SIMULATION SOFTWARE ON THE REVERSED-PHASE SEPARATION OF FLAVONOIDS BY HPLC-DAD
José Wilson Figueiredo Júnior
Mestrado em Produtos Naturais e Sintéticos Bioativos (Farmacoquímica)
Laboratório de Tecnologia Farmacêutica, UFPB, Caixa Postal 5009, Cep 58051-970 João Pessoa, Paraíba, Brasil. (w.figueiredojr@gmail.com)
High Performance Liquid Chromatography (HPLC) allows both qualitative and quantitative chemical analysis, separating and identifying substances in mixtures with speed and efficiency. However, factors governing chromatographic retention are complex and the method development phase consumes a lot of resources. In our work we evaluated a chromatographic simulation software package (HIPAC-G, HIPAC-B e HIPAC-S, Phenomenex, Torrance, USA) for optimizing the chromatographic separation of eight flavonoid standards (3-O-[β-D -glucopyranosyl-(1→6)-α-L-ramnopyranosyl]-7-O-α-L-ramnopyranosyl kampferol; hesperidine; kampferol; tiliroside; quercetin; 3,4’,7,8-tetra-O-methyl-gossypetine; 3,3’,4’,7,8-penta-O -methyl-gossypetine and 3,3’,4’,7-tetra-O-methyl-quercetin). The HIPAC model of retention is based on the known linear relationship that exists between the retention factor of an analyte and the percentage of organic solvent in the mobile phase, to simulate retention data. Using gradient elution, three trial runs were done (preliminary runs that are used to input retention data to the software). The first trial run used a C18 column (250 x 4,6 mm, 5 m) and as mobile phase a gradient from 5 to 95% of acetonitrile (solvent B) in 0,1% formic acid (solvent A) at a flow rate of 1 mL/min with UV detection at 264 nm. The first trial run was comprised of two gradient runs using the same chromatographic conditions but different gradient duration times (30 and 60 minutes respectively). The second trial run used the same chromatographic conditions as the first one, but methanol instead of acetonitrile as the organic modifier and 10% and 100% as the initial and final %B, respectively. The third trial run was done with the same chromatographic conditions as the second one, but using a column with different stationary phase and dimensions (C8, 150 x 4,6 mm, 5 m). The retention data of the three trial runs were used as input to the simulation software, using the HIPAC-G module. For isocratic mode simulation using the HIPAC-B module, both a C8 (150 x 4,6 mm, 5 m) and a C18 (250 x 4,6 mm 5 m) column was used with binary mixtures of MeOH (solvent B) in 0,1% formic acid (solvent A). Two trial runs with 60% and 70%B were done for each column and the resulting retention data used as input for simulation. The optimized separation conditions as suggested by HIPAC-B were used as input for HIPAC-S to optimize the system chromatographic conditions. The optimization criterion used for all simulations was the average global resolution for all peaks in the chromatogram. Altogether twelve simulations in gradient elution mode and four isocratic simulations were done. The simulated retention data was then confronted with experimentally obtained retention data for the eight flavonoid standards. The correlation coefficient (r2) between simulated and observed
retention times for the analytes when eluted in gradient mode varied from 0,9416 to 0,9992 (n=12). The correlation coefficient in isocratic mode varied from 0.9999 to 1 (n=4), indicating an excellent efficiency in predicting retention data for the mixture tested. Taken together our results show that the use of chromatographic simulation software such as G, B e HIPAC-S can constitute an important tool in the optimization of separation conditions of complex mixtures, such as those found in the field of natural products.
““Se olharmos para qualquer ponto
do universo, encontraremos algo de
estupendo. A ntes de mais nada,
encontraremos
um
universo
extremamente belo, construído de
maneira sutil e intrincada.”
SUMÁRIO
1.INTRODUÇÃO ... 25
2.REFERENCIALTEÓRICO ... 33
2.1 Princípios Teóricos do Processo Cromatográfico ... 33
2.1.1 Definição ... 33
2.1.2 Representação gráfica do processo de separação. ... 33
1.1.3 Alargamento de banda ... 34
1.1.3.1 Primeira causa:Difusão de Eddy ... 35
1.1.3.2 Segunda causa: Distribuição de fluxo ... 35
1.1.3.3 Terceira causa: Difusão da amostra da molécula na fase móvel. ... 36
1.1.3.4 Quarta causa: Transferência de massa entre fase móvel e fase estacionária. ... 36
1.1.4 O cromatograma e seu propósito ... 37
1.2. Interfaces do Programa ... 45
A) Módulo HIPAC-G ... 45
A.1) HIPAC-G, manual ícones. ... 45
A.2) Interfaces do módulo HIPAC-G ... 47
B) Módulo HIPAC-B ... 49
B.1) HIPAC-B, manual ícones... 49
C) Módulo HIPAC-S ... 52
C.1) HIPAC-S, manual ícones ... 52
C.2) Interfaces do Módulo HIPAC-S. ... 53
2.OBJETIVOS ... 59
2.1 Geral ... 59
2.2 Específicos... 59
3.METODOLOGIA ... 60
3.1 Instrumental ... 60
3.2 Substâncias e Solventes ... 60
3.3 Uso do Software de Simulação ... 60
3.3.1 Determinação do Tempo de Retardo do Sistema (System Delay Time) ... 61
3.3.2 Obtenção dos dados de retenção nas corridas preliminares (trial runs) ... 62
4.RESULTADOSEDISCUSSÃO ... 64
4.1 Calculo do Tempo de Retardo (System Delay Time) ... 64
4.2 Separação de Flavonóides com o auxílio do módulo HIPAC-G, Utilizando acetonitrila. ... 64
4.2.1. Identificação dos analitos e inserção dos dados no módulo HIPAC-G. ... 64
4.3 Análise com HIPAC-G (“Sigle Step” e “Multi Step”) – ACN, C18, 25 cm. ... 71
4.4 Análise com HIPAC-G (“Sigle Step” e “Multi Step”) – MeOH, C18, 25 cm. ... 110
4.5 Análise com HIPAC-B – MeOH, C18, 25 cm. ... 120
4.6 Análise com HIPAC-S – MeOH, C18, 25 cm. ... 126
4.8. ANÁLISE COM HIPAC-B – MeOH, C8, 15 cm. ... 139
5.CONCLUSÕES ... 152
Lista de Figuras
FIGURA 1. USANDO A INFORMAÇÃO SOBRE A AMOSTRA PARA SELECIONAR CONDIÇÕES
EXPERIMENTAIS PARA SEPARAÇÃO INICIAL (SNYDER,KIRKLAND,GLAJCH,1997). ... 29
FIGURA 2.PRINCIPIOS DE UM DETECTOR DE ARRANJO DE DIODOS. ... 32
FIGURA 3.ESQUEMA ILUSTRANDO OS COMPONENTES BÁSICOS DE UM CROMATÓGRAFO LÍQUIDO DE ALTA EFICIÊNCIA. ... 32
FIGURA 4.REPRESENTAÇÃO DE UMA SEPARAÇÃO CROMATOGRÁFICA. ... 34
FIGURA 5.DIFUSÃO DE EDDY EM UMA COLUNA CROMATOGRÁFICA. ... 35
FIGURA 6.DISTRIBUIÇÃO DO FLUXO EM UM LEITO CROMATOGRÁFICO. ... 35
FIGURA 7.ALARGAMENTO DA BANDA POR DIFUSÃO LONGITUDINAL. ... 36
FIGURA 8.ESTRUTURA DE UM PORO DE PARTÍCULA DE FASE ESTACIONÁRIA. ... 36
FIGURA 9.FORMA DO PICO. ... 37
FIGURA 10.CROMATOGRAMA E SUAS PRINCIPAIS CARACTERÍSTICAS. ... 38
FIGURA 11.PLOTAGEM DA RETENÇÃO DE COMPOSTOS (LOG K) VS. FORÇA DA FASE MÓVEL (%B). ... 44
FIGURA 12.TELA DE CONTROLE PARA OPERAÇÃO DO HIPAC-G... 47
FIGURA 13.TABELA DE INSERÇÃO DOS DADOS HIPAC-G. ... 47
FIGURA 14. TELA PARA INSERÇÃO DOS DADOS REFERENTES ÀS DUAS CORRIDAS CROMATOGRÁFICAS INICIAIS E O TEMPO MORTO DO SISTEMA,HIPAC-G. ... 47
FIGURA 15.TELA MOSTRA O MODO SIGLE STEP, ONDE É FEITA A ESCOLHA DOS LIMITES MÁXIMO E MÍNIMO DE TEMPO E CONCENTRAÇÃO DE ELUENTE B,HIPAC-G. ... 48
FIGURA 16.TELA MOSTRA O MODO MULTI STEP, ONDE É FEITA A ESCOLHA DE UMA RESOLUÇÃO ALVO, E A DEFINIÇÃO DOS TRECHOS DO CROMATOGRAMA, PARA SER EFETUADA A MELHOR OTIMIZAÇÃO COM BASE NESTA RESOLUÇÃO,HIPAC-G. ... 48
FIGURA 17. (A) CROMATOGRAMA PREDITO PELO SOFTWARE, (B) SUMÁRIO DOS DADOS DE PREDIÇÃO, E (C) E (D), MAPAS QUE RELACIONAM A MELHOR RELAÇÃO ENTRE A CONCENTRAÇÃO E O TEMPO DE GRADIENTE HIPAC-G. ... 48
FIGURA 18.INTERFACE DO SISTEMA DE CONTROLE (SYSOP) ACIONA A INTERFACE DO MÓDULO HIPAC-S;(MPOP) ACIONA A INTERFACE DO HIPAC-B;(ISOEL) FERRAMENTA QUE AUXILIA NO CÁLCULO DA FORÇA ELUOTRÓPICA;(N,RS) FERRAMENTA PARA O CÁLCULO DOS NÚMEROS DE PRATOS TEÓRICOS E RESOLUÇÃO; (SCAN) FERRAMENTA DE AUXÍLIO DE VERIFICAÇÃO SE A AMOSTRA DA MISTURA É ADEQUADA PARA USO DO MODO GRADIENTE. ... 50
FIGURA 20.TABELA DE INSERÇÃO DOS DADOS HIPAC-B. ... 50
FIGURA 21. TELA DE ESCOLHA DOS LIMITES DA CONCENTRAÇÃO DE B A SER OTIMIMIZADA HIPAC-B. ... 51
FIGURA 22.TELA DE INSERÇÃO DOS DADOS DA COLUNA E FLUXO, PARA O CÁLCULO DO TEMPO QUE LEVA UMA AMOSTRA NÃO RETIDA PARA ATRAVESSAR SEU COMPRIMENTO,HIPAC-B. ... 51
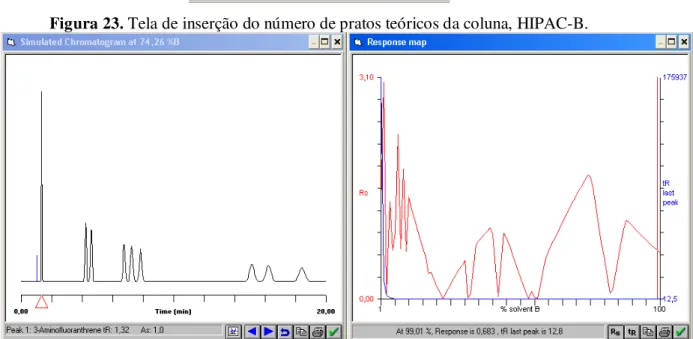
FIGURA 23.TELA DE INSERÇÃO DO NÚMERO DE PRATOS TEÓRICOS DA COLUNA,HIPAC-B. .... 51
FIGURA 24.CROMATOGRAMA E GRÁFICO DO MAPA DE RESPOSTA,HIPAC-B. ... 51
FIGURA 25.SUMÁRIO COM OS DADOS DE PREDIÇÃO DO HIPAC-B. ... 52
FIGURA 26.INTERFACE DO SISTEMA DE CONTROLE PARA O MÓDULO HIPAC-S. ... 53
FIGURA 27.TABELA DE INSERÇÃO DOS DADOS HIPAC-S. ... 53
FIGURA 28.TELA DE INSERÇÃO DOS DADOS REFERENTES AO SISTEMA, DO HIPAC-S... 54
FIGURA 29.TELA DE INSERÇÃO DO TIPO E CONCENTRAÇÃO DA FASE MÓVEL DO HIPAC-S. ... 54
FIGURA 30. LISTA DE DADOS COMPUTADOS DO SISTEMA DEPOIS DE INSERIDOS INFORMAÇÃO PERTINENTE AO CORRENTE SISTEMA CROMATOGRÁFICO. ... 54
FIGURA 31.TELA DE ESCOLHA DOS PARÂMETROS QUE SE DESEJA OTIMIZAR DE FORMA SIMPLES OU COMBINADA COMO O FLUXO, FLUXO E TAMANHO DA COLUNA, FLUXO, TAMANHO DA COLUNA E PARTÍCULA. ... 54
FIGURA 32. TELA DE INSERÇÃO DE DADOS, ONDE SE PODE COMBINAR OS PARÂMETROS DO SISTEMA MANUALMENTE PARA SE OBTER UMA OTIMIZAÇÃO ADEQUADA. ... 55
FIGURA 33. CROMATOGRAMA OBTIDO A PARTIR DA OTIMIZAÇÃO EFETUADA PELO MÓDULO HIPAC-S. ... 55
FIGURA 34. A)NÚCLEO FLAVONOÍDICO, B)NÚCLEO 4-OXO-FLAVONÓIDE ... 57
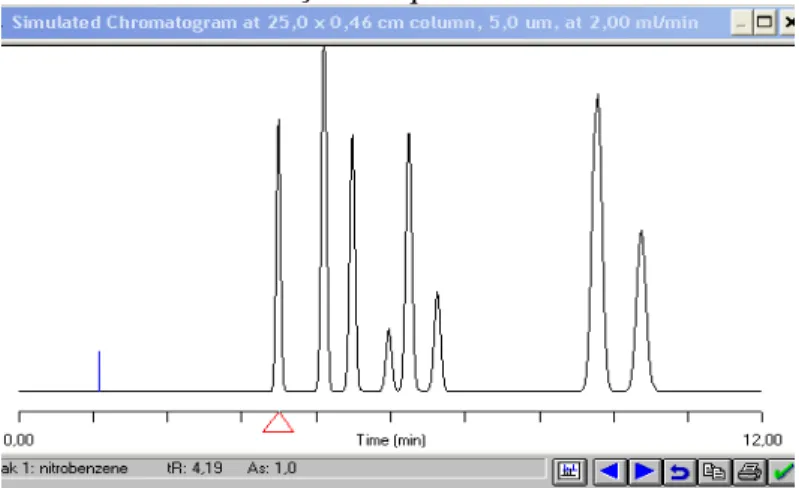
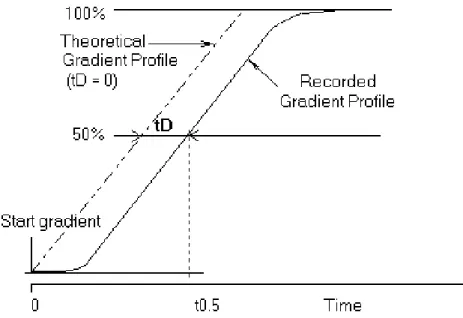
FIGURA 35.GRÁFICO DEMONSTRATIVO DA MEDIÇÃO PARA O CÁLCULO DO TEMPO MORTO. ... 61
FIGURA 36.CROMATOGRAMA OBTIDO PARA O CÁLCULO DO TEMPO MORTO DO APARELHO. ... 64
FIGURA 37.CORRIDA DE GRADIENTE DE 30 MINUTOS 5 A 95%B(ACN), COLUNA 25 CM,C18,1 ML/MIN (GRADIENTE 01). ... 65
FIGURA 38.CORRIDA DE GRADIENTE DE 60 MINUTOS 5 A 95%B(ACN), COLUNA 25 CM,C18,1 ML/MIN.(GRADIENTE 02). ... 65
FIGURA 39. CROMATOGRAMA DO PADRÃO 3-O-[Β-D-GLICOPIRANOSIL-(1→6)-Α-L -RAMNOPIRANOSIL]-7-O-Α-L RAMNOPIRANOSILKANFEROL (SAS1336). ... 66
FIGURA 40.CROMATOGRAMA DO PADRÃO HESPERIDINA ... 66
FIGURA 41.CROMATOGRAMA DO PADRÃO KANFEROL. ... 66
FIGURA 42.CROMATOGRAMA DO PADRÃO TILIROSÍDEO. ... 67
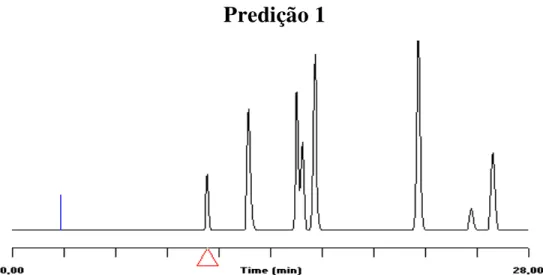
FIGURA 44.CROMATOGRAMA DO PADRÃO 3,7,8,4'- TETRA-O-METILGOSSIPETINA (SPEA01). ... 67 FIGURA 45. CROMATOGRAMA DO PADRÃO 3, 7, 8, 3', 4'-PENTA-O-METILGOSSIPETINA (SPEA01ME). ... 67 FIGURA 46.CROMATOGRAMA DO PADRÃO 3,7,3',4'-TETRA-O-METILQUERCETINA (SPEH01). 68 FIGURA 47. SIMULAÇÃO COM HIPAC-G PARA OTIMIZAÇÃO DE SEPARAÇÃO (RESOLUÇÃO GLOBAL MÍNIMA) IMPONDO O LIMITE DE CONCENTRAÇÃO INICIAL MAX DE 10% PARA O SOLVENTE ORGÂNICO (%B).CONDIÇÕES:250 X 4,6MM,5M C18;;ACN-ÁGUA, GRADIENTE DE 10 A 85%B EM 25MIN. ... 72 FIGURA 48.CROMATOGRAMA OBTIDO BASEADO NA SIMULAÇÃO DA PREDIÇÃO 1. ... 72 FIGURA 49.MAPAS DE RESOLUÇÃO EM FUNÇÃO DA %B INICIAL (INITIAL %B) E DURAÇÃO DO GRADIENTE (GRADIENT TIME/MIN)(PREDIÇÃO 1). ... 72 FIGURA 50.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O QUE FOI PREVISTO PELO HIPAC-G E O OBTIDO NO APARELHO DE CLAE-DAD(PREDIÇÃO 1). ... 73 FIGURA 51.RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
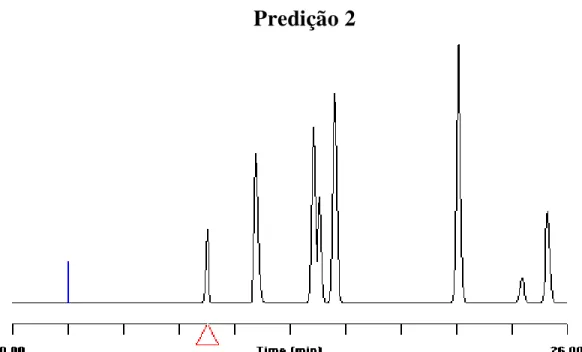
CLAE-DAD A PARTIR DA PREDIÇÃO 1. ... 74 FIGURA 52. SIMULAÇÃO COM HIPAC-G PARA OTIMIZAÇÃO DE SEPARAÇÃO (RESOLUÇÃO GLOBAL MÍNIMA) IMPONDO O LIMITE DE CONCENTRAÇÃO INICIAL MAX DE 15% PARA O SOLVENTE ORGÂNICO (%B).CONDIÇÕES:250 X 4,6MM,5M C18;;ACN-ÁGUA, GRADIENTE DE 15 A 84%B EM 24 MIN... 76 FIGURA 53.CROMATOGRAMA OBTIDO BASEADO NA SIMULAÇÃO CORRESPONDENTE A PREDIÇÃO 2. ... 76 FIGURA 54. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS GRADIENTE (PREDIÇÃO 2). ... 76 FIGURA 55.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (PREDIÇÃO 2). ... 77 FIGURA 56.RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
SOLVENTE ORGÂNICO (%B).CONDIÇÕES:250 X 4,6MM,5M C18;;ACN-ÁGUA, GRADIENTE DE 20 A 82%B EM 23MIN. ... 80 FIGURA 58.CROMATOGRAMA OBTIDO BASEADO NA SIMULAÇÃO CORRESPONDENTE A PREDIÇÃO 3.. ... 80 FIGURA 59. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS DE GRADIENTE (PREDIÇÃO 3). ... 80 FIGURA 60.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (PREDIÇÃO 3). ... 81 FIGURA 61.RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
CLAE-DAD A PARTIR DA PREDIÇÃO 3. ... 82 FIGURA 62. SIMULAÇÃO COM HIPAC-G PARA OTIMIZAÇÃO DE SEPARAÇÃO (RESOLUÇÃO GLOBAL MÍNIMA) IMPONDO O LIMITE DE CONCENTRAÇÃO INICIAL MAX DE 25% PARA O SOLVENTE ORGÂNICO (%B).CONDIÇÕES:250 X 4,6MM,5M C18;;ACN-ÁGUA, GRADIENTE DE 25 A 81%B EM 22MIN. ... 84 FIGURA 63.CROMATOGRAMA OBTIDO BASEADO NA SIMULAÇÃO DA PREDIÇÃO 4. ... 84 FIGURA 64. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS DE GRADIENTE (PREDIÇÃO 4). ... 84 FIGURA 65.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (PREDIÇÃO 4). ... 85 FIGURA 66.RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
FIGURA 70.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (OTIMIZAÇÃO 5). ... 89 FIGURA 71.RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
CLAE-DAD A PARTIR DA PREDIÇÃO 5. ... 90 FIGURA 72. SIMULAÇÃO COM HIPAC-G PARA OTIMIZAÇÃO DE SEPARAÇÃO (RESOLUÇÃO GLOBAL MÍNIMA) IMPONDO O LIMITE DE CONCENTRAÇÃO INICIAL MAX DE 35% PARA O SOLVENTE ORGÂNICO (%B).CONDIÇÕES:250 X 4,6MM,5M C18;;ACN-ÁGUA, GRADIENTE DE 32 A 80%B EM 21MIN. ... 92 FIGURA 73.CROMATOGRAMA OBTIDO BASEADO NA SIMULAÇÃO CORRESPONDENTE A PREDIÇÃO 6. ... 92 FIGURA 74. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS DE GRADIENTE (PREDIÇÃO 6). ... 92 FIGURA 75.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (PREDIÇÃO 6). ... 93 FIGURA 76.RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
CLAE-DAD A PARTIR DA PREDIÇÃO 6. ... 94 FIGURA 77. SIMULAÇÃO COM HIPAC-G PARA OTIMIZAÇÃO DE SEPARAÇÃO (RESOLUÇÃO GLOBAL MÍNIMA) IMPONDO O LIMITE DE CONCENTRAÇÃO INICIAL MAX DE 5% PARA O SOLVENTE ORGÂNICO (%B).CONDIÇÕES:250 X 4,6MM,5M C18;;ACN-ÁGUA, GRADIENTE DE 5 A 86%B EM 26MIN. ... 96 FIGURA 78.CROMATOGRAMA OBTIDO BASEADO NA SIMULAÇÃO DA PREDIÇÃO 7. ... 96 FIGURA 79. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS DE GRADIENTE (PREDIÇÃO 7). ... 96 FIGURA 80.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (PREDIÇÃO 7). ... 97 FIGURA 81RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
FIGURA 82. SIMULAÇÃO COM HIPAC-G PARA OTIMIZAÇÃO DE SEPARAÇÃO (RESOLUÇÃO GLOBAL MÍNIMA) IMPONDO O LIMITE DE CONCENTRAÇÃO INICIAL MAX DE 99% PARA O SOLVENTE ORGÂNICO (%B).CONDIÇÕES:250 X 4,6MM,5M C18;;ACN-ÁGUA, GRADIENTE DE 26 A 61%B EM 47MIN. ... 100 FIGURA 83.CROMATOGRAMA OBTIDO BASEADO SIMULAÇÃO DA PREDIÇÃO 8. ... 100 FIGURA 84. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS DE GRADIENTE (PREDIÇÃO 8). ... 100 FIGURA 85.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (PREDIÇÃO 8). ... 101 FIGURA 86RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
CLAE-DAD A PARTIR DA PREDIÇÃO 8. ... 102 FIGURA 87. SIMULAÇÃO COM HIPAC-G PARA OTIMIZAÇÃO DE SEPARAÇÃO (RESOLUÇÃO GLOBAL MÍNIMA) IMPONDO O LIMITE DE CONCENTRAÇÃO INICIAL MAX DE 99% PARA O SOLVENTE ORGÂNICO (%B).CONDIÇÕES:250 X 4,6MM,5M C18;;ACN-ÁGUA, GRADIENTE EM MODO MULTISTEP COM OS SEGUINTES PASSOS:1 A 36% EM 6MIN,36 A 36% EM 9 MIN,36-99% EM 6MIN. ... 105 FIGURA 88.CROMATOGRAMA OBTIDO BASEADO NA SIMULAÇÃO EM MODO GRADIENTE “MULTI
STEP” DA PREDIÇÃO 9. ... 105 FIGURA 89. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS DE GRADIENTE (PREDIÇÃO 9). ... 105 FIGURA 90.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (PREDIÇÃO 9). ... 107 FIGURA 91RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM DUPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
ORGÂNICO (%B). CONDIÇÕES: 250 X 4,6MM, 5 M C18;; MEOH-ÁGUA, GRADIENTE “SINGLE STEP” DE 62% A 75%B EM 34MIN. ... 112 FIGURA 95. CROMATOGRAMA OBTIDO BASEADO NA SIMULAÇÃO MODO GRADIENTE “SINGLE STEP” NAS CONDIÇÕES DA PREDIÇÃO 10. ... 112 FIGURA 96. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS DE GRADIENTE (GRADIENTE “SINGLE STEP”,PREDIÇÃO 10). ... 112 FIGURA 97.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (PREDIÇÃO 10; MODO GRADIENTE “SINGLE STEP”) ... 113
FIGURA 98RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
CLAE-DAD A PARTIR DA PREDIÇÃO DO MODO GRADIENTE “SINGLE STEP”(PREDIÇÃO 10). .. 114 FIGURA 99. SIMULAÇÃO COM HIPAC-G PARA OTIMIZAÇÃO DE SEPARAÇÃO (RS) IMPONDO O LIMITE DE CONCENTRAÇÃO INICIAL MAX DE 99% PARA SOLVENTE ORGÂNICO (%B). CONDIÇÕES:250 X 4,6 MM,5M C18;MEOH-ÁGUA, GRADIENTE “MULTI STEP” COM 3 PASSOS NESTAS CONDIÇÕES:57 A 58% DE B EM 3 MINUTOS;58 A 60% DE B EM 7 MINUTOS E 60 A 99% DE B EM 3 MINUTOS. ... 116 FIGURA 100. CROMATOGRAMA OBTIDO BASEADO NA SIMULAÇÃO MODO GRADIENTE “MULTI
STEP” NAS CONDIÇÕES DA PREDIÇÃO 11. ... 116 FIGURA 101. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS DE GRADIENTE (MODO GRADIENTE “MULTI STEP”, PREDIÇÃO 11). ... 116 FIGURA 102.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-G E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (PREDIÇÃO EM MODO GRADIENTE “MULTI STEP”.PREDIÇÃO 11) ... 117 FIGURA 103RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
FIGURA 106.SIMULAÇÃO COM HIPAC-B USANDO AS SEGUINTES CONDIÇÕES:250 X 4,6 MM,5
M C18;; MODO ISOCRÁTICO COM 57% DE B EM 100 MINUTOS E FLUXO DE 1 ML/MIN. ... 121 FIGURA 107.CROMATOGRAMA BASEADO NA PREDIÇÃO 12 COM HIPAC-B. ... 121 FIGURA 108.GRÁFICO QUE REPRESENTA O MAPA DE RESPOSTA QUE MOSTRA A RELAÇÃO ENTRE A RESOLUÇÃO E A CONCENTRAÇÃO DO ELUENTE B.(PREDIÇÃO 12) ... 122 FIGURA 109. GRÁFICO QUE REPRESENTA O MAPA DE RETENÇÃO COM TEMPO DE RETENÇÃO VARIANDO EM FUNÇÃO DA CONCENTRAÇÃO DO ELUENTE B.(PREDIÇÃO 12) ... 122 FIGURA 110.DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-B E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (OTIMIZAÇÃO MODO ISOCRÁTICO 57% EM 100 MIN, FLUXO DE 1 ML/MIN.)... 123 FIGURA 111RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
CLAE-DAD A PARTIR DA OTIMIZAÇÃO ISSO.57%B EM 100 MIN.(PREDIÇÃO 12) ... 124 FIGURA 112. SIMULAÇÃO COM HIPAC-S USANDO CONDIÇÕES: 250 X 4,6 MM, 5 M C18;; MEOH-ÁGUA MEOH, EM MODO ISOCRÁTICO COM 57% DE B EM 150 MINUTOS E FLUXO DE 0,7 ML/MIN. ... 126 FIGURA 113.CROMATOGRAMA BASEADO NA PREDIÇÃO 13 COM HIPAC-S. ... 126 FIGURA 114. DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC-S E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (OTIMIZAÇÃO MODO ISOCRÁTICO 57% EM 150 MIN, FLUXO DE 0,7 ML/MIN.PREDIÇÃO 13) ... 127 FIGURA 115RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
FIGURA 121. DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (OTIMIZAÇÃO MODO GRADIENTE “SINGLE STEP” EM 6 MIN, 1ML/MIM, MEOH, COLUNA C8, 15CM).PREDIÇÃO 14. ... 132 FIGURA 122RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
CLAE-DAD A PARTIR DA OTIMIZAÇÃO LIVRE C815CM HIPAC-G. ... 133 FIGURA 123. SIMULAÇÃO PARA OTIMIZAÇÃO DE SEPARAÇÃO (RS) IMPONDO O LIMITE DE CONCENTRAÇÃO INICIAL MAX DE 99% PARA SOLVENTE ORGÂNICO (%B). CONDIÇÕES:150 X 4,6MM,5M C8;;MEOH-ÁGUA, GRADIENTE “MULTI STEP” COM 3 PASSOS NESTAS CONDIÇÕES: 53 A 63% DE B EM 1 MINUTO,63 A 63% DE B EM 4 MINUTOS E 63 A 99% DE B EM 3 MINUTOS, MANTEVE-SE POR MAIS 3 MINUTOS A 99% DE B. ... 135 FIGURA 124.CROMATOGRAMA BASEADO NA PREDIÇÃO 15. ... 135 FIGURA 125. MAPAS DEMONSTRATIVOS EXPRESSÃO A VARIAÇÃO DA CONCENTRAÇÃO DE B (SOLVENTE ORGÂNICO) E SUA INFLUÊNCIA NOS TEMPOS DE GRADIENTE (OTIMIZAÇÃO COM MEOH,“MULTI STEP”). ... 135 FIGURA 126.OTIMIZAÇÃO MULTI STEP: VARIAÇÃO DO SOLVENTE B INICIAL DE NO MAX 99%,53 A 63%B EM 1 MIN,63 A 63% EM 4 MIN E 63 A 99% EM 3 MIN, MANTEVE-SE POR MAIS 3 MIN A 99%.PREDIÇÃO 15. ... 136 FIGURA 127RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
CLAE-DAD A PARTIR DA OTIMIZAÇÃO OTI.LIVRE C8-15CM,HIPAC-GMULTISTEP... 137 FIGURA 128.CORRIDAS ISOCRÁTICAS DE 60% PARA COLUNA C8,15 CM.MEOH. ... 139 FIGURA 129.CORRIDAS ISOCRATICAS DE 70% PARA COLUNA C8,15 CM.MEOH. ... 139 FIGURA 130..SIMULAÇÃO COM HIPAC-B USANDO AS SEGUINTES CONDIÇÕES:150 X 4,6MM,5
(CORRIDA OTIMIZADA SUGERIDA EM MODO ISOCRATICO A 54%B EM 70 MINUTOS).PREDIÇÃO 16... 142 FIGURA 135RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
CLAE-DAD A PARTIR DA OTIMIZAÇÃO HIPAC-B. ... 143 FIGURA 136. SIMULAÇÃO COM HIPAC-S USANDO AS SEGUINTES CONDIÇÕES:150 X 4,6MM,5
M C8;; MODO ISOCRÁTICO COM 54% DE B EM 50 MINUTOS E FLUXO DE 1,5 ML/MIN. ... 145 FIGURA 137.CROMATOGRAMA BASEADO NA PREDIÇÃO 17. ... 145 FIGURA 138. DADOS CROMATOGRÁFICOS E SEUS RESPECTIVOS GRÁFICOS DE CORRELAÇÃO ENTRE O PREVISTO PELO HIPAC E O OBTIDO DE FORMA REAL NO APARELHO DE CLAE-DAD (CORRIDA OTIMIZADA SUGERIDA EM MODO ISOCRATICO A 54%B EM 70 MINUTOS).PREDIÇÃO 17... 146 FIGURA 139RESULTADOS SUMARIZADOS DOS DADOS OBTIDOS EM TRIPLICATA COM OS DESVIOS PADRÕES E ERROS PADRÕES DA MÉDIA REFERENTES AOS DADOS OBTIDOS NO EXPERIMENTO EM
Lista de Tabelas
Lista de Quadros
ABREVIATURAS E SÍMBOLOS
ACN acetonitrila
CLAE Cromatografia Líquida de Alta Eficiência DAD Detector com Arranjo de Diodos
MeOH metanol
SAS1336 3-O-[β-D-glicopiranosil-(1→6)-α-L-ramnopiranosil]
-7-O-α-L ramnopiranosilkanferol
SPEA01 3, 7, 8, 4'- tetra-O-metilgossipetina SPEA01Me 3, 7, 8, 3', 4'-penta-O-metilgossipetina SPEH01 3, 7, 3', 4'-tetra-O-metilquercetina
C18, C8 número de carbonos na fase ligada UV Ultra Violeta
K coeficiente de distribuição
t0 tempo morto
u velocidade linear do fluxo “n”, “N” número de pratos teóricos
W largura do pico na linha de base
W1/2 largura do pico a meia altura.
Rs resolução global
r2 coeficiente de correlação
1. INTRODUÇÃO
A ciência avança a passos largos a cada momento, levando a humanidade a novos patamares tecnológicos. O mundo constantemente volta seu olhar para trás e pergunta: Como vivíamos antigamente sem todos estes avanços? Para muitos, é difícil imaginar um tempo sem todas as vantagens da vida moderna como celulares, carros, computadores, medicamentos entre outras tantas invenções que melhoraram a qualidade de vida da sociedade em que vivemos. O uso da tecnologia iniciou-se com pequenas ferramentas simples criadas usando recursos encontrados na natureza, e a partir deste começo tímido a humanidade atravessou os séculos galgando degrau a degrau utilizando suas ferramentas para compreender e mudar o ambiente em que vive. Em um ciclo infindável de construção de conhecimento, desenvolvimento de tese, antítese e síntese, a sociedade combinou recursos para produzir produtos, resolver problemas, preencher necessidades, e satisfazer desejos.
A distinção entre ciência, engenharia e tecnologia nem sempre é clara. Enquanto ciência é o estudo ou investigação racional de fenômenos naturais utilizando técnicas formais como o método científico, objetivando descobertas de princípios estáveis entre os variados elementos dos fenômenos da natureza (http://dictionary.reference.com/browse/science). A engenharia é o processo objetivo e orientado de design e feitura de ferramentas e sistemas para exploração de fenômenos naturais para meios práticos humanos, freqüentemente (mas
nem sempre) usando resultados e técnicas da ciência
(http://en.wikipedia.org/wiki/Technology).. Por fim, a tecnologia freqüentemente é
A curiosidade humana derivada da necessidade fez com que Mikhail Semenovich Tswett desenvolvesse em 1901 os primórdios das técnicas cromatográficas durante sua pesquisa com pigmentos de plantas. Tswett usou em seu método, uma coluna cromatográfica de adsorção preenchida com carbonato de cálcio como adsorvente e uma mistura de éter de petróleo/ etanol como eluente para separar a clorofila e carotenóides. O método de Tsweet foi descrito em 30 de dezembro de 1901 no XI Congress of Naturalists and Physicians em San Petersburgo (http://www.uni-kiel.de/anorg/lagaly/group/klausSchiver/Feigl.pdf -23/01/2008). Entretanto, o trabalho de Tswett foi ignorado por algumas décadas, sendo retomado somente 10 anos após sua morte graças aos esforços do cientista alemão Edgar Lederer. Desde então novas técnicas cromatográficas e equipamentos de análise foram desenvolvidos por diversos cientistas e colaboradores. Martin e Synge na década de 40 desenvolveram a cromatografia por partição. Em 1952 surgiu a cromatografia gasosa desenvolvida por Martin. Em 1957, Golay aperfeiçoa a técnica de cromatografia gasosa com a introdução das colunas capilares. E a partir de 1967 Snyder e vários outros teóricos desenvolveram o que viria a ser a técnica de Cromatografia Líquida de Alta Eficiência (CLAE) para análise química (KEVIN ROBARDS; HADDAD, 1994). Até a atualidade a comunidade científica ainda se deslumbra com o interminável potencial de desenvolvimento da técnica para análises cada vez mais precisas.
A técnica de High Performance Liquid Cromatography (HPLC) ou como também é conhecida Cromatografia Líquida de Alta Eficiência (CLAE) é uma forma de cromatografia que encontra amplo espectro de aplicabilidade em campos muito diversos como análises farmacêuticas, indústria de alimentos, indústria química e petroquímica, química orgânica, química de produtos naturais, criminalística entre outras tantas (KEVIN ROBARDS; HADDAD, 1994). A CLAE é usada para separar, identificar, isolar e quantificar componentes de uma mistura pela utilização de uma variedade de interações químicas entre substância analisada (analito), os solventes e a coluna cromatográfica.
móvel. O tempo entre a introdução da amostra no sistema cromatográfico e o momento em que um analito específico elui e é detectado ao fim da coluna é denominado Tempo de Retenção (tR), sendo considerado uma característica identificadora de um dado analito. Os
“inventores” da cromatografia líquida moderna, Martin e Synge (MARTIN, 1941), tiveram consciência por volta de 1941 que, em teoria, para aumentar o poder de separação de uma coluna, a fase estacionária requer partículas muito pequenas, e por isso uma pressão elevada é necessária para forçar a fase móvel através da coluna. O uso da pressão aumenta a velocidade linear e permite o uso de partículas de sílica peliculares (com diâmetros de 5 m e menores, dando aos constituintes menos tempo para difundir-se na coluna e levando à melhora da resolução no cromatograma resultante. Solventes comumente utilizados em CLAE incluem qualquer combinação miscível de água ou vários líquidos orgânicos (metanol, acetonitrila, tetrahidrofurano, metanol, etc.). A água pode ainda conter soluções tampões ou outros modificadores como ácidos, reagentes de pareamento iônico, surfactantes e outros, para
auxiliar na separação de componentes da mistura
(http://www.chromedia.org/chromedia?waxtrapp=yqegzCsHqnOxmOlIEcCxB).
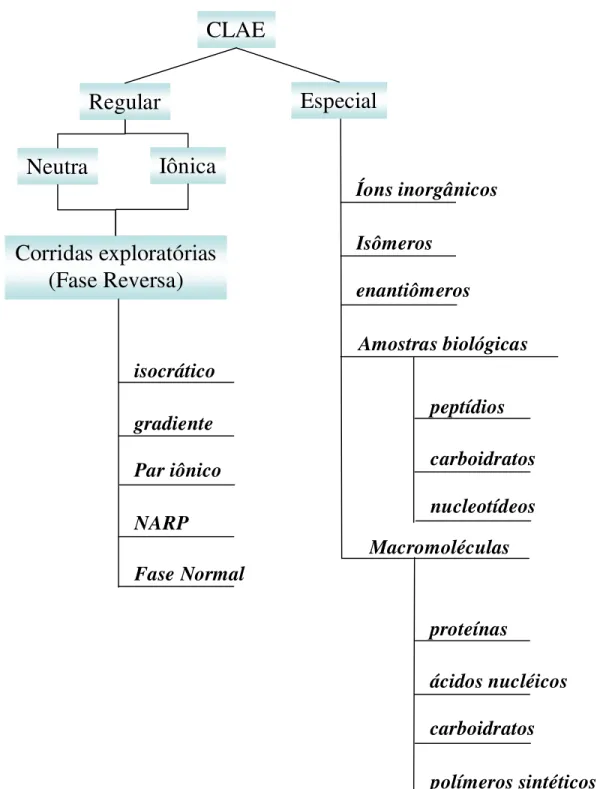
Figura 1. Usando a informação sobre a amostra para selecionar condições experimentais para separação inicial (SNYDER, KIRKLAND, GLAJCH, 1997).
CLAE
Regular
Especial
Neutra
Iônica
Corridas exploratórias
(Fase Reversa)
isocrático
gradiente
NARP
Fase Normal
Par iônico
Íons inorgânicos
Isômeros
Amostras biológicas
Macromoléculas
enantiômeros
peptídios
carboidratos
nucleotídeos
proteínas
ácidos nucléicos
Quadro 1. Condições experimentais preferidas para separação inicial de CLAE
Variável da separação Escolha inicial preferida
Coluna
Dimensões (comprimento, Diâmetro Interno ID) Tamanho da partícula
Fase estacionária
15 x 0,46 cm 5 µm (a) C8 ou C18
Fase Móvel
Solventes A e B %B
Tampão (composto, pH, concentração) Aditivos (amina modificadoras,
reagentes pareadores iônicos)
Tampão-Acetonitrila 80-100% (b) 25 mM fosfato de potássio,
2.0 , pH , 3.0 (c) Não utilizado inicialmente
Fluxo 1.5-2.0 mL/min
Temperatura 35-45ºC
Tamanho da amostra
Volume (d)
Peso (d) < 100 µg. < 25µL a) Partículas de 3.5-um são uma alternativa, ao usar uma coluna de 7,5 cm.
b) Para uma corrida isocratica inicial, uma corrida inicial por gradiente é preferida.
c) Tampão não é requerido para amostras Neutras, para pH <2,5, colunas pH-estaveis são recomendadas. d) Valores menores requeridos para colunas de volume menores (ex.: 7,5 x 0,46cm, coluna de 3.5 µm
Fonte:(LLOYD, JOSEPH, SNYDER, 1997).
O método relacionado no Quadro 1 mostra-se um ótimo ponto de partida para o desenvolvimento do método de separação. Entretanto, não se tem uma noção precisa de como será conduzida a separação. Unindo estas informações com o poder de um software de predição e otimização da separação cromatográfica, pode-se esperar a aquisição de inúmeras vantagens para o cromatografista.
butil ou C4, octil ou C8, entre outras formas poliméricas ou baseadas em sílica pelicular (KEVIN ROBARDS; HADDAD, 1994).
O fluxo da fase móvel é geralmente ajustado em função do diâmetro da coluna cromatográfica, de forma a respeitar uma velocidade linear da fase móvel ideal para minimizar a altura equivalente a um prato teórico (máxima eficiência de separação): 1-2 mL/minuto para colunas de 0,46 mm, 0,5-1,0 mL/min para colunas de 3 mm e 0,3-,0,5 mL/minuto para colunas de 2 mm. A modalidade de separação mais amplamente usada em CLAE é a cromatografia de fase reversa, a qual apresenta uma fase estácionária apolar e fase móvel polar, sendo o método de separação baseado em um processo de partição do analito entre a fase móvel e a fase estacionária.
A detecção é realizada por um transdutor que converte uma mudança na concentração da amostra em um sinal elétrico que é registrado por um processador de dados. Interpretação deste registro fornece dados qualitativos e quantitativos da amostra. Os fotômetros de UV são os detectores mais utilizados em cromatografia liquida. Estes medem mudanças de absorbância da luz nas regiões de 190 – 350 nm quando o eluente da coluna passa através do detector da célula de fluxo. O detector é composto por lâmpada, célula de fluxo e sensor luminoso. Adicionalmente, um filtro pode ser utilizado para um especifico comprimento de luz.
Figura 2. Principios de um detector de arranjo de diodos. Fonte: MEYER, 2004.
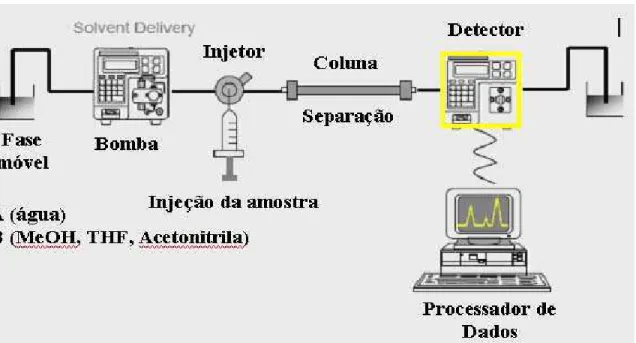
O cromatógrafo de alta eficiência é composto por um grupo de módulos individuais ou elementos, como ilustrado na Figura 2. Os módulos apresentam funções diferenciadas, como módulos de controle do sistema, bomba propriamente dita, detector, forno ou sistemas para injeção automática.
Figura 3.Esquema ilustrando os componentes básicos de um Cromatógrafo Líquido de Alta Eficiência.
2. REFERENCIAL TEÓRICO
2.1 Princípios Teóricos do Processo Cromatográfico
2.1.1 Definição
A cromatografia é um processo de separação em que os constituintes de uma mistura são distribuídos entre duas fases no leito cromatográfico (coluna ou plano). Uma fase é estacionária enquanto a outra passa através do leito cromatográfico. A fase estacionária pode ser um material sólido, poroso, ativo superficialmente na forma de uma pequena partícula, ou um fino filme de líquido revestindo um suporte sólido, como uma partícula de sílica. A fase móvel é um líquido.
Compostos que tendem a residir na fase móvel movem-se mais rápido que aqueles que preferem a fase estacionária. A preferência pela fase pode ser expressa pelo coeficiente de distribuição KX (distribution coefficient, K):
Aonde cstat é a concentração (na realidade atividade) do composto X na fase estacionária e cmob é a concentração de X na fase móvel, ou o fator de retenção, k (formalmente denominado capacity factor k) :
Aonde nstat é o número de moles de X na fase estacionária e nmob é o numero de moles na fase móvel. A fase móvel e estacionária precisam estar, obviamente, em contato íntimo uma com a outra para garantir uma distribuição balanceada. Os vários constituintes precisam ter diferentes coeficientes de distribuição e, portanto, diferentes fatores de capacidade (capacity factors) no sistema cromatográfico para que a mistura possa ser separada (MEYER, 2004).
2.1.2 Representação gráfica do processo de separação.
(b) O constituinte X tem maior afinidade pela fase estacionária e o constituinte Y maior afinidade pela fase móvel (Figura 3b). Aqui, Kx=5/2 = 2.5 e Ky = 2/5 = 0,4.
(c) Um novo equilíbrio se segue com a adição de um novo eluente: moléculas da amostra na fase móvel são parcialmente adsorvidas pela superfície da fase estacionária “nua” de acordo com os seus respectivos coeficientes de distribuição, e em um segundo momento ocorre transferência de massa das moléculas de volta à fase móvel renovada, em um movimento em sentido contrário. Assim, a retenção ocorrerá através de inúmeros passos de transferência de massa da fase móvel à fase estacionária e de volta àquela. (Figura 3c)
(d) Depois de repetir este processo muitas vezes, os dois constituintes são finalmente separados. O constituinte Y prefere a fase móvel e migra mais rapidamente que o componente X, que tende a “grudar” (ficar mais retido) na fase estacionária. (Figura. 3d).
Como o diagrama mostra, aqui o novo balanço é encontrado ao longo da seção correspondente a 3 ½ de diâmetro de partícula da fase estacionária. Assim, esta distância representa os Pratos Teóricos. Quanto mais comprido é o leito cromatográfico, mais pratos teóricos este contem e melhor é o grau de separação de mistura. Este efeito é parcialmente compensado pelo alargamento da banda. Nos experimentos, mostram zonas de substância que se tornam cada vez mais largas de acordo com o aumento do comprimento da coluna e mais longo é o tempo de retenção (MEYER, 2004).
Figura 4. Representação de uma separação cromatográfica. Fonte: MEYER, 2004.
1.1.3 Alargamento de banda
1.1.3.1 Primeira causa:Difusão de Eddy
A coluna é empacotada com pequenas partículas de fase estacionária. A fase móvel passa através desta e arrasta as moléculas da amostra (Fig. 4). Algumas moléculas são “afortunadas” e deixam a coluna antes de muitas das outras, após viagem aleatória mais ou menos em linha reta através do leito cromatográfico. Outras moléculas saem posteriormente, passando por vários desvios ao longo do caminho (MEYER, 2004).
Figura 5. Difusão de Eddy em uma coluna cromatográfica. Fonte:MEYER, 2004.
1.1.3.2 Segunda causa: Distribuição de fluxo
A fase móvel é um fluxo laminar entre as partículas da fase estacionária (Figura 5). O fluxo é mais rápido no “canal” central próximo à partícula. As flechas da Figura 5 representam os vetores de velocidade da fase móvel (Quanto mais comprida a flecha, mais rápida). A difusão de Eddy e distribuição de fluxo podem ser reduzidos pelo empacotamento da coluna com partículas perfeitamente uniformes (MEYER, 2004).
Figura 6. Distribuição do fluxo em um leito cromatográfico. Fonte: MEYER, 2004.
Partícula da fase estacionária
1.1.3.3 Terceira causa: Difusão da amostra da molécula na fase móvel.
Moléculas da amostra se espalham no solvente sem qualquer influência externa (tal qual açúcar que se dissolve se difundindo lentamente em água mesmo sem misturar o liquido). Esta é a chamada difusão longitudinal (Figura 6) e tem um desvantajoso efeito sobre a altura do prato apenas se:
(a) partículas pequenas da fase estacionária são utilizadas,
(b) A velocidade da fase móvel é muito lenta em relação ao diâmetro da partícula, e (c) O coeficiente de difusão da amostra é relativamente grande (MEYER, 2004)
Figura 7. Alargamento da banda por difusão longitudinal. Fonte: MEYER, 2004.
1.1.3.4 Quarta causa: Transferência de massa entre fase móvel e fase estacionária.
A Figura 7 mostra a estrutura de uma partícula de fase estacionária: os canais são tanto largos quanto apertados, e alguns passam diretamente através da partícula inteira e outros são fechados (MEYER, 2004).
Os poros são preenchidos com a fase móvel que não se move (está estagnada). Uma molécula da amostra ao entrar neste poro cessa de ser transportada pelo fluxo do solvente e muda sua posição apenas por processo de difusão. De qualquer forma, duas possibilidades se apresentam:
(a) A molécula se difunde de volta para o fluxo da fase móvel. Este processo leva mais tempo do que moléculas que não foram retidas nos poros, que consequentemente se movem ligeiramente mais rápidas. O alargamento de banda é menor quanto mais curtos são os poros, isto é, quando menores são as partículas de fase estacionária. Além disso, a taxa de difusão das moléculas da amostra em um solvente é maior sob condições de baixa viscosidade (eles se difundem mais rápido dentro e fora dos poros) que em um meio mais viscoso.
(b) A molécula interage com a fase estacionária (adsorvente ou filme líquido) e é adsorvida por um tempo, esta forma retida na fase estacionária, até que um novo processo de transferência de massa se inicie.
Em ambos os casos, o alargamento de banda aumenta com o aumento do fluxo de fase móvel, uma vez que as moléculas estagnadas ficam rapidamente distantes das moléculas não estagnadas que permanecem mais tempo na fase móvel com velocidade linear alta (MEYER, 2004).
1.1.4 O cromatograma e seu propósito
Os compostos eluídos são transportados pela fase móvel até o detector e registrados em curvas gaussianas (formato de um sino). Estes sinais são conhecidos como picos (Figura 8) e a representação gráfica dos picos (do sinal analíico) em função do tempo ou do volume de fase móvel é conhecido como cromatograma.
O pico fornece informações qualitativas e quantitativas da mistura em questão:
(a) Qualitativa: O tempo de retenção de um componente é sempre constante sob condições idênticas cromatográficas. O tempo de retenção é o período compreendido entre a injeção da amostra e o ponto máximo (ápex) do pico cromatográfico referente àquela substância. As dimensões da coluna, tipo de fase estacionária, composição de fase móvel, velocidade de fluxo, tamanho da amostra e temperatura influenciam de forma única a retenção de dado analito. Por isso, um pico pode ser identificado ao injetar a amostra e um padrão de referência autêntico da substância em questão.
(b) Quantitativo: Tanto a área quanto a altura do pico podem ser proporcionais à quantidade do composto injetado. Um gráfico de calibração pode ser derivado das áreas dos picos ou alturas obtidas para várias soluções de amostras com concentrações conhecidas, e uma comparação de tamanho de picos pode ser usada para determinar a concentração de uma amostra desconhecida.
O cromatograma pode ser usado para prover informação de eficiência de separação (Figura 9). Aqui w é a largura do pico na linha de base, t0 é o tempo morto ou tempo de
retenção de um soluto não retido, (o tempo requerido para a fase móvel atravessar a coluna). Assim, a velocidade linear do fluxo, u, pode ser calculada:
Figura 10. Cromatograma e suas principais características. Fonte: MEYER, 2004.
A coluna cromatográfica pode ser imaginada como composta de várias divisões chamadas de “pratos teóricos”. O soluto ao mover-se por estas divisões realiza sucessivos equilíbrios entra a fase estacionária e a fase móvel. Assim, quanto maior o número de pratos teóricos de uma coluna maior será sua eficiência (MEYER, 2004).
O número de pratos teóricos “n” ou “N” de uma coluna se define por:
n = (t
r/σ)²
(2)
Onde “tr” é o tempo de retenção do soluto e “σ” é o desvio padrão do mesmo pico (parâmetro difícil de ser medido). Vários métodos baseados em aproximações e extrapolações das partícularidades de um pico gaussiano são disponíveis, permitindo-nos calcular “N” da seguinte forma:
N
= 16 (
t
R/
w
)² ou
N
= 5.54 (
t
R/
W
1/2)²
(3)
Onde “W” é a largura do pico na linha de base e W1/2 é a largura do pico a meia altura. Assim, “N” (numero de pratos teóricos) é um parâmetro adimensional, em decorrência das duas variáveis tempo de retenção e largura de pico serem medidas em unidades de tempo. Pode-se ainda calcular “n” com as seguintes equações:
n = 16 (
t
r/Wb)² ou ainda n=5.54 (t
r/Wh/2)²
(4)Com picos com tempo de retenção pequenos o volume morto da coluna colabora de uma forma significativa para a retenção total de um soluto. Assim, tendo em vista este fato outra equação pode ser usada para obter um parâmetro denominado número de pratos teóricos efetivos (N, efective plate number):
N=16 [(
t
r-tm)/Wb]² ou N=5.54 [(tr-tm)/W
h/2]²
(5)N = 41.7 (t
r/W
0.1)²/As+1.25
(6)Onde As é um fator de assimetria para o pico de interesse e W0.1 é a largura do pico a 10% da altura.
Tanto o número de pratos teóricos (n) quanto o número de pratos teóricos efetivos (N) dependem do comprimento de coluna. Para facilitar a comparação da eficiência de colunas um parâmetro foi determinado de altura equivalente a um prato teórico (h) definido como
h=L/n
(7)ou analogamente com o número de pratos teóricos efetivos:
H=L/N
(8)Mais um dado importante é a resolução do cromatograma (Rs), que é o principal parâmetro usado para descrever o grau de separação de picos adjacentes, sendo que valores acima de 1.2 são considerados adequados para picos bem resolvidos.
Estes valores são determinados pela seguinte equação:
Rs = (tr
b-tr
a) / ½. (Wa+Wb)
(9)Onde são usados tempos de retenção e largura de dois picos adjacentes.
O cálculo de pratos teóricos não pode ser realizado através de uma única corrida por método de gradiente. Resultados de pelo menos duas corridas (para gradientes lineares) com diferentes tempos de gradiente são requeridos, e até então a computação destes dados está longe de ser simples. Em muitos casos, é seguro assumir que o número de pratos teóricos de uma corrida em modo isócratico para uma dada coluna pode ser aplicado para uma separação
por método em modo de gradiente.
(http://www.lcresources.com/wiki/index.php?title=ChromFAQ:TheoreticalPlates).
A utilização de programas de computadores para facilitar o desenvolvimento de método em CLAE tem recebido atenção desde os anos setenta (SNYDER, KIRKLAND, GLAJCH, 1997). Inúmeros trabalhos têm sido publicados até hoje. Os softwares para desenvolvimento de métodos comercialmente disponíveis, podem ser classificados de acordo com sua capacidade ou função.
Quadro 2. Métodos de microcomputadores ou otimização de fase móvel de CLAE ajudada por microprocessadores.
Método Sistema Tipo Autores
COF Off-line Isocrático Glajch et al (1980)
Window Diagram Off-line Isocrático Sachok e al (1980) ORM (SENTINEL) Integral Isocrático Glajch et al (1982)
ISOORPT Integral Isocrático Berridge (1982)
TERNOPT Integral Isocrático Berridge (1982)
GRADOPT Integral Gradiente Berridge (1982)
Search and Stop Off-line Isocrático Drouen et al (1982) OPTIM (I) Integral Isocrático Bradley and Gillen (1983) OPTIM (G) Integral Gradiente Bradley and Gillen (1984)
OPEX Off-line Gradiente Sabate et al (1983)
IMGE Off-line Gradiente Kirkland and Glajch (1983) SMGE Off-line Gradiente Kirkland and Glajch (1983)
PEAKIN/SAS Off-line Isocrático Issaq (1984)
RPS Off-line Isocrático Jinno and Kawasaki (1984) CCSM-I Off-line Isocrático D’agostino et al. (1984) Fonte: D'AGOSTINO, 1985.
Otimizar parâmetros envolvidos nos métodos de desenvolvimento de separações cromatográficas na década de 80 só era possível com a ajuda de computadores e microprocessadores. Mesmo com o auxílio destas ferramentas o procedimento requeria várias corridas experimentais (que aumentavam em número a medida que novas variáveis eram adicionadas aos cálculos). Os processadores do período gastavam muito tempo em computação das predições (4 a 6 horas), mesmo sendo otimizações de problemas cromatográficos simples. Os programas citados acima na tabela, eram comercialmente disponíveis na época e são revisados com certa minúcia na literatura especializada (D'AGOSTINO, 1985).
Cada programa citado na lista auxiliava em um aspecto de desenvolvimento de CLAE, sendo necessário o uso de dois ou mais programas para cobrir as variadas possibilidades de exames como os modos de análise isocrático, uso de fases ternárias ou quaternárias, modo gradiente, modo gradiente não linear com/ ou sem passos isocráticos.
Na década seguinte o mercado já possuía novos e mais eficazes softwares de predição, tanto em conseqüência da presença de máquinas com processadores mais potentes e velozes quanto pelo maior conhecimento obtido em modelos matemáticos para predição do comportamento cromatográfico em função das mudanças das variáveis de separação.
Destes podemos destacar o software Drylab (SNYDER, 1989; SNYDER, KIRKLAND, GLAJCH, 1997) que possui ampla literatura especializada relacionada ao seu desempenho, bem como outros disponíveis no mercado e citados em quadro abaixo, com suas respectivas finalidades descritas (SNYDER, KIRKLAND, GLAJCH , 1997).
Quadro 3. Classificação de softwares comerciais de desenvolvimento de método de acordo com sua capacidade.
1- Mudança de uma variável de retenção por vez, predizendo a separação como função desta variável. (Drylab b***)
2- Mudança de uma ou mais variáveis por vez predizendo separação como função dessas variáveis. (ICOS c**, DIAMOND d**)
3- Mudança de condições de coluna (Dimensões da coluna, tamanho da partícula, fluxo,) predizer separação para qualquer condições da coluna. (Drylab b***, ENHANCER d**)
4- Mudanças de condições de gradiente, predizer separações para quaisquer condições de gradiente. (Drylab b***)
5- Mudança de uma ou mais condições, examinar cromatogramas experimentais pela melhor separação (Pesos e***)
6- Experts systems. Sistemas especializados para predizer as melhores iniciais de separação sobre a base de amostra de compostos moleculares estruturais (?) (ELUEX f*, CHROMDREAM g*, HPLC-METABOLEXPERT f*, ProDigest-LC h*)
7- Sistemas especializados para aconselhar em outros aspectos de desenvolvimento de método de HPLC.
a) Exemplos de cada programa de computador é dado entre parênteses. Estes programas eram avaliados comercialmente em 1996. * software Stand-alone; ** Software integrado a sistemas; *** Encontrando tanto no formato stand-alone quanto integrado a sistemas. b) LC Resources, Walnut Creek, CA. (Mudança de duas variaveis possiveis com DryLab 2.0 introduzida em 1997)
Os métodos aplicados cobrem tanto situações estáticas quanto dinâmicas. Em todos os casos o tempo de computação aumenta rapidamente de acordo com o tamanho do sistema a ser estudado. O sistema pode ser uma simples molécula, um grupo de moléculas relacionadas ou um grupo de moléculas estruturalmente não relacionadas. Em geral, os métodos são baseados em teorias que fornecem previsões muito acuradas, mas aplicáveis apenas a sistemas menores, ou aquelas que fornecem previsões aproximadas para sistemas maiores. Os métodos acurados são denominados métodos ab initio, já que são baseados inteiramente na teoria desde os primeiros cálculos. Os métodos menos acurados são denominados empíricos ou semi empíricos devido ao uso de resultados experimentais juntamente com a teoria, frequentemente obtidos a partir de moléculas relacionadas. (LIPKOWITZ, 2007). Os métodos semi-empíricos demonstram predições mais confiáveis e robustas, frente aos variados problemas cromatográficos em rotinas laboratoriais (SNYDER, KIRKLAND, GLAJCH, 1997; DOLAN, 1992).
Muitas das regras e relações em que se baseiam os métodos semi-empíricos são quantitativas, e então se torna necessário o uso de cálculos precisos para obter as melhores predições para a próxima análise.
Um exemplo é a retenção como função de %B em HPLC de fase reversa, que é descrita pela equação:
log
K
= log K
w
–
S Φ
(10)
A %B também pode ser descrita como equivalente a 100 Φ, onde Φ é a fração do volume de
solvente orgânico na fase móvel. Os valores de Kw e S são constantes para um determinado analito e condições de separação específicas. Se dois experimentos são realizados em que apenas a %B varia, é possível determinar os valores de Kw e S para cada componente da amostra, e então utilizar a relação acima para calcular a retenção dos componentes da amostra para qualquer valor de Φ (%B). Uma conseqüência desta equação é que K aumenta
substâncias que são separadas em fase reversa é conhecido como a “regra do 3”. Estes resultados podem ser demonstrados em qualquer formato tais como tabelas, gráficos, cromatogramas, cada um destes pode ajudar o cromatografista a selecionar mais rapidamente as melhores condições para uma dada amostra. A habilidade de predizer uma separação iniciando apenas com um número limitado de experimentos “reais” se torna especialmente útil em desenvolvimentos de métodos, se um grande número de corridas (>10) for necessário. Geralmente este tipo de análise é realizada em amostras contendo meia dúzia de compostos quimicamente similares e/ou separações que envolvam eluição por gradiente ou requeiram a otimização de 2 ou mais variáveis. (SNYDER, KIRKLAND, GLAJCH, 1997).
Figura 11. Plotagem da retenção de compostos (log k) vs. força da fase móvel (%B). Fonte: SNYDER, KIRKLAND, GLAJCH. (1997)
1.2. Interfaces do Programa
A) Módulo HIPAC-G
A.1) HIPAC-G, manual ícones.
New File: Para remover todos os dados e iniciar nova pesquisa com um novo problema de separação.
Open File: Para abrir um arquivo.
Import: Importa dados de outros programas de aquisição de dados cromatográficos.
Save File. Salva os dados (arquivo com até 8 caracteres, na extensão .HGM inserida automaticamente).
Enter Peak Data: Opção que abre interface permitindo inserir dados cromatográficos (tempo de retenção, área, assimetria e denominação dos picos cromatográficos) em uma caixa de texto e posicioná-las nas células das colunas. Pode-se editar, copiar e colar, bem como apagar linhas específicas de dados.
Enter Trial Data: Caixa de diálogo para selecionar as condições dos experimentos preliminares (trial runs). O valor do tempo de retardo do sistema (System Delay time) irá ter um significante impacto na precisão dos cálculos dos tempos de retenção; um valor incorreto acarretará simulações imprecisas.
Enter Hold UpTime: Insere o valor de t0. Pode ser calculado a partir dos valores informados para especificações do sistema (comprimento da coluna, diâmetro interno, porosidade e fluxo).
Optimize: Interface onde seleciona-se o tipo de otimização, os limites da otimização (valor inicial de %B mínimo e máximo, tempo de gradiente mínimo e máximo), os critérios de otimização (Resolução global mínima, tempo de corrida limitado, uso de picos assimétricos e etc...).
Contour Response Map: Indica o gradiente e a resposta correspondente (resolução). Mapas de resposta são selecionados após otimização “single step” (um gradiente com um único trecho) ter sido encontrada. Não são avaliados para otimizações multistep (gradientes com mais de um trecho).
Surface Response Map: Permite melhor visualização (gráfico tridimensional) das variáveis demonstradas no mapa de resposta.
Simulation: Permite demonstrar um cromatograma simulado ou dados de retenção. A opção “set gradiente” permite desenvolver um novo perfil de gradiente diretamente.
Summary: As tabelas do sumário listam os resultados de todas as simulações realizadas desde a última vez em que os dados do novo teste foram carregados, inseridos ou após o uso de novo critério de otimização.
A.2) Interfaces do módulo HIPAC-G
O HIPAC-G apresenta um panorama simples e prático de ser utilizado o que é demonstrado em suas interfaces reproduzidas nas Figuras 13-18. A forma de inserção dos dados está demonstrada nas imagens subseqüentes.
Figura 12. Tela de controle para operação do HIPAC-G.
Figura 13. Tabela de inserção dos dados HIPAC-G.
Figura 15. Tela mostra o modo sigle step, onde é feita a escolha dos limites máximo e mínimo de tempo e concentração de eluente B, HIPAC-G.
Figura 16. Tela mostra o modo Multi step, onde é feita a escolha de uma resolução alvo, e a definição dos trechos do cromatograma, para ser efetuada a melhor otimização com base nesta resolução, HIPAC-G.
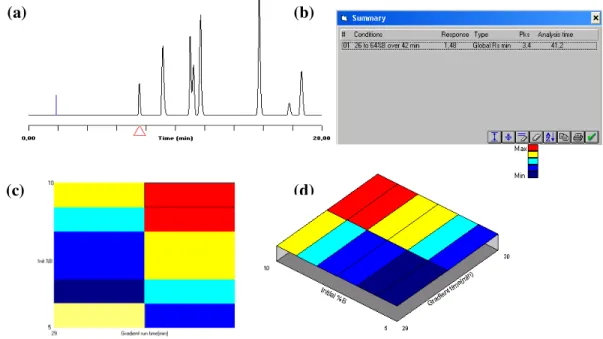
Figura 17. (a) Cromatograma predito pelo software, (b) sumário dos dados de predição, e (c) e (d), mapas que relacionam a melhor relação entre a concentração e o tempo de gradiente HIPAC-G.
(a) (b)
B) Módulo HIPAC-B
B.1) HIPAC-B, manual ícones
New File: Para remover todos os dados e iniciar nova pesquisa com um novo problema de separação.
Open File: Para abrir um arquivo.
Import: Importa dados de outros programas de aquisição de dados cromatográficos.
Save File. Salva os dados (arquivo com até 8 caracteres, na extensão .HBM inserida automaticamente).
Enter Peak Data: Opção que abre interface permitindo inserir dados cromatográficos (tempo de retenção, área, assimetria e denominação dos picos cromatográficos) em uma caixa de texto e posicioná-las nas células das colunas. Pode-se editar, copiar e colar, bem como apagar linhas específicas de dados.
Enter Mobile Phase: Insere as condições utilizadas nas corridas preliminares. (trial runs) Enter Hold Up Time: Insere o valor de t0. Pode ser calculado ao inserir-se as especificações do sistema ( comprimento da coluna, diâmetro interno, porosidade e fluxo).
Enter plate Count: Uma estimativa do número de pratos teóricos é requerida para o programa calcular larguras dos picos (peak Widths), e em conseqüência resolução. O valor padrão (Default) é de 10.000, podendo ser alterado de acordo com as características da coluna e amostra utilizadas, para simulações mais precisas.
Optimize: Ícone que abre a interface aonde se insere os limites da otimização e os critérios escolhidos para serem melhorados durante as simulações.