Desenvolvimento da aplica¸c˜
ao
inform´
atica InterPharm para
estudar a intera¸c˜
ao entre f´
armacos
Por
Ana Rita Fernandes de Sousa
Orientador: Doutor Lio Fidalgo Gon¸calves
Disserta¸c˜ao submetida `a
UNIVERSIDADE DE TR ´AS-OS-MONTES E ALTO DOURO para obten¸c˜ao do grau de
MESTRE
em Engenharia Electrot´ecnica e de Computadores, de acordo com o disposto no DR – I s´erie–A, Decreto-Lei no
74/2006 de 24 de Mar¸co e no Regulamento de Estudos P´os-Graduados da UTAD
DR, 2a
s´erie – Delibera¸c˜ao no
Desenvolvimento da aplica¸c˜
ao
inform´
atica InterPharm para
estudar a intera¸c˜
ao entre f´
armacos
Por
Ana Rita Fernandes de Sousa
Orientador: Doutor Lio Fidalgo Gon¸calves
Disserta¸c˜ao submetida `a
UNIVERSIDADE DE TR ´AS-OS-MONTES E ALTO DOURO para obten¸c˜ao do grau de
MESTRE
em Engenharia Electrot´ecnica e de Computadores, de acordo com o disposto no DR – I s´erie–A, Decreto-Lei no
74/2006 de 24 de Mar¸co e no Regulamento de Estudos P´os-Graduados da UTAD
DR, 2a
s´erie – Delibera¸c˜ao no
Orienta¸c˜ao Cient´ıfica :
Doutor Lio Fidalgo Gon¸calves
Professor Auxiliar do Departamento de Engenharias
Universidade de Tr´as-os-Montes e Alto Douro
”A imagina¸c˜ao ´e mais importante que a ciˆencia, porque a ciˆencia ´e limitada, ao passo que a imagina¸c˜ao abrange o mundo inteiro.”
Albert Einstein (1879 – 1955)
UNIVERSIDADE DE TR ´AS-OS-MONTES E ALTO DOURO Mestrado em Engenharia Electrot´ecnica e de Computadores
Os membros do J´uri recomendam `a Universidade de Tr´as-os-Montes e Alto Douro a aceita¸c˜ao da disserta¸c˜ao intitulada “ Desenvolvimento da aplica¸c˜ao inform´atica InterPharm para estudar a intera¸c˜ao entre f´armacos ” realizada por Ana Rita Fernandes de Sousa para satisfa¸c˜ao parcial dos requisitos do grau de Mestre.
Dezembro 2015
Presidente: Doutor Jo˜ao Agostinho Batista de Lacerda Pav˜ao,
Professor Auxiliar da Universidade de Tr´as-os-Montes e Alto Douro
Vogais do J´uri: Doutora Teresa Maria de Gouveia Torres Feio Mendon¸ca,
Professor Auxiliar da Universidade de Aveiro
Doutor Lio Fidalgo Gon¸calves,
Professor Auxiliar do Departamento de Engenharias da Universidade de Tr´as-os-Montes e Alto Douro
Desenvolvimento da aplica¸c˜ao
inform´atica InterPharm para
estudar a intera¸c˜ao entre f´armacos
Ana Rita Fernandes de Sousa
Submetido na Universidade de Tr´as-os-Montes e Alto Douro para o preenchimento dos requisitos parciais para obten¸c˜ao do grau de
Mestre em Engenharia Electrot´ecnica e de Computadores
Resumo — A intera¸c˜ao de f´armacos ´e uma ´area da farmacologia com bastante interesse de estudo, pois ´e poss´ıvel combinar f´armacos no sentido de descobrir novas terapias mais eficientes com menor toxicidade para o doente. O efeito da mistura de dois componentes pode ser aditivo (o efeito da combina¸c˜ao ´e igual `a soma dos efeitos dos f´armacos isolados), antag´onico (´e necess´aria maior quantidade de f´armacos na mistura para atingir o mesmo efeito isoladamente), ou sin´ergico (para obter o mesmo efeito, na mistura a dose dos f´armacos ´e menor que a dose isolada de cada f´armaco). Para a determina¸c˜ao do efeito existente na combina¸c˜ao de f´armacos existem v´arios m´etodos desenvolvidos, como por exemplo o princ´ıpio do efeito mediano de Chou e Talalay e o m´etodo de Greco que combina m´etodos mais antigos num novo m´etodo mais completo. Na presente disserta¸c˜ao ´e apresentada uma nova aplica¸c˜ao inform´atica, InterPharm, desenvolvida em Matlab R
, que permite aos investigadores analisar o efeito existente na combina¸c˜ao de dois f´armacos em determinada terapia. Foram feitas experiˆencias para diferentes combina¸c˜oes de f´armacos e os resultados produzidos s˜ao semelhantes aos obtidos por outros softwares j´a existentes.
Palavras Chave: Intera¸c˜ao de f´armacos, aplica¸c˜oes inform´aticas, sinergismo, antagonismo, aditividade, superf´ıcie de ajuste, efeito mediano.
Development of a software application
InterPharm to study drug-drug interaction
Ana Rita Fernandes de Sousa
Submitted to the University of Tr´as-os-Montes and Alto Douro in partial fulfillment of the requirements for the degree of Master of Science in Electrical Engineering and Computers
Abstract — The drug-drug interaction is an area of pharmacology with great interest of study because it is possible to combine drugs in order to discover new therapies more effective with less toxicity to the patient. The effect of the mixture of two components may be additive (the effect of the combination is equal to the sum of the effects of the individual drugs), antagonistic (requires more amount of drug in the mixture to achieve the same effect alone) or synergistic (for the same effect in mixing the dose of drugs is less than the dose of each drug alone). To determine the effect of drug combination there are several developed methods such as the principle of the median-effect of Chou and Talalay and Greco’s method that combines the oldest methods in a new and more complete method. In this thesis is presented a new software application, InterPharm developed in MATLAB, which allows researchers to analyze the effect on the combination of two drugs in certain therapy. Experiments were made for different drug combinations, and the results are similar to those obtained by other existing software.
Key Words: Drug-drug interaction, software application, synergism, antagonism, additivity, surface fit, median-effect.
Agradecimentos
Este espa¸co ´e dedicado `aqueles que deram a sua contribui¸c˜ao para que esta disserta¸c˜ao fosse realizada. A todos eles deixo aqui os meus sinceros agradecimentos.
Os meus agradecimentos ao Professor Doutor Lio Gon¸calves, Professor Auxiliar do Departamento de Engenharias da Universidade de Tr´as-os-Montes e Alto Douro, pela orienta¸c˜ao, pela sua motiva¸c˜ao, pela confian¸ca na minha capacidade de trabalho, e pelas suas sugest˜oes e ensinamentos fundamentais para a realiza¸c˜ao da disserta¸c˜ao. Aos meus colegas do Mestrado em Engenharia Electrot´ecnica e de Computadores da Universidade de Tr´as-os-Montes e Alto Douro pelo seu acolhimento e simpatia e aos meus amigos pelo apoio.
Ao Jo˜ao, um agradecimento especial pelo apoio e carinho di´arios, pelas palavras doces e pela transmiss˜ao de confian¸ca e de for¸ca, em todos os momentos. Pelo companheirismo e amizade, e pelo modo como me aturou ao longo desta ´ardua etapa.
Por ´ultimo, um agradecimento especial aos meus pais, Am´elia e Henrique, pelo modelo que s˜ao de esfor¸co e dedica¸c˜ao, por tudo o que sou hoje, por n˜ao medirem esfor¸cos, apesar das dificuldades, para que eu chegasse a esta etapa da minha vida que sempre souberam ser um dos meus maiores objetivos, pelo carinho, apoio e for¸ca, pela paciˆencia e por me darem a confian¸ca necess´aria para realizar os meus sonhos.
Aos meus irm˜aos, Diogo e Eduardo, pelo apoio e carinho, e pela preocupa¸c˜ao pelo meu bem-estar.
A todos que acreditaram em mim, que sempre me apoiaram e ajudaram, prometo n˜ao desiludir. Um sincero obrigado!
UTAD, Ana Rita Fernandes de Sousa
Barcelos, 1 de Setembro de 2015
´Indice geral
Resumo xi
Abstract xiii
Agradecimentos xv
´Indice de tabelas xix
´Indice de figuras xxi
Gloss´ario, acr´onimos e abreviaturas xxv
1 Introdu¸c˜ao 1 1.1 Motiva¸c˜ao . . . 2 1.2 Objetivos . . . 4 1.3 Organiza¸c˜ao da Disserta¸c˜ao . . . 4 2 Estado da Arte 7 2.1 Intera¸c˜ao de f´armacos. . . 8 2.1.1 Farmacocin´etica . . . 9 2.1.2 Farmacodinˆamica . . . 10
2.1.3 Intera¸c˜ao a n´ıvel molecular . . . 11
2.2 M´etodos de an´alise do efeito . . . 13
2.2.1 Aditividade de Loewe. . . 14
2.2.2 Independˆencia de Bliss . . . 15 xvii
2.2.3 Princ´ıpio do Efeito Mediano . . . 16
2.2.4 Isobolograma . . . 20
2.2.5 Modelo de Greco . . . 24
2.2.6 Resposta em superf´ıcie . . . 26
2.3 Ferramentas Computacionais: MATLAB R , GUIDE e Report Generator . . . 28
2.4 Aplica¸c˜oes Inform´aticas. . . 30
2.4.1 CompuSyn. . . 30
2.4.2 CalcuSyn . . . 31
2.4.3 Curve Fitting toolbox . . . 32
3 Desenvolvimento da aplica¸c˜ao InterPharm 35 3.1 Algoritmos do programa Interpharm . . . 35
3.2 Metodologia utilizada . . . 36
3.2.1 Figura 1 - InterPharm . . . 36
3.2.2 Figura 2 - Nova experiˆencia . . . 37
3.2.3 Figura 3 - Novo f´armaco . . . 37
3.2.4 Figura 4 - Nova combina¸c˜ao de f´armacos . . . 38
3.2.5 Figura 5 - Nova combina¸c˜ao de f´armacos . . . 39
3.2.6 Figura 6 - Salvar Experiˆencia . . . 39
3.2.7 Figura 7 - Calcular Parˆametros . . . 40
3.2.8 Figura 8 - Gerar o Relat´orio . . . 41
3.2.9 Figura 9 - Superf´ıcie de Ajuste. . . 42
3.2.10 Figura 10 - Isobolograma . . . 43
3.2.11 Figura 11 - Relat´orio . . . 44
4 Apresenta¸c˜ao e discuss˜ao dos resultados 45 4.1 Caso de estudo I- Rotenone e Pyrethrins . . . 45
4.2 Caso de estudo II - ADP e o-PAL . . . 49
4.3 Caso de estudo III - MTX e Ara-C . . . 52
4.4 Caso de estudo IV- Sunitinib malate e Meloxicam . . . 56
5 Conclus˜ao e trabalho futuro 67
Referˆencias bibliogr´aficas 69
´Indice de tabelas
4.1 Toxicidade letal de Rotenone e Pyrethrins para as moscas: r´acio constante da Combina¸c˜ao R:P de 1:5 e 1:15 (Adotado da Tabela 18 de Pharmcol Rev. 58: 621-681, 2006). . . 46
4.2 Resultados obtidos pelo CompuSyn e InterPharm no caso de estudo I 46
4.3 Inibi¸c˜ao da enzima ´alcool desidrogenase de f´ıgado de cavalo com inibidor competitivo (ADP) e n˜ao competitivo (o-PAL). R´acio constante da Combina¸c˜ao 1:17.4 apenas na diagonal (Adotado da Tabela 9 de Pharmacol Rev. 58: 621-681, 2006). . . 49
4.4 Resultados obtidos pelo CompuSyn e InterPharm no caso de estudo II 50
4.5 Inibi¸c˜ao da incorpora¸c˜ao de [6-H]dUrd no ADN de c´elulas leuc´emicas L1210 por MTX e Ara-C. R´acio constante da Combina¸c˜ao 1:0.782 (Adotado da Tabela 19 de Pharmacol Rev. 58: 621-681, 2006). . . 53
4.6 Resultados obtidos pelo CompuSyn e Interpharm no caso de estudo III 54
4.7 Meloxicam aumenta sinergicamente o efeito in vitro de Sunitinib malate (T24). . . 57
4.8 Meloxicam aumenta sinergicamente o efeito in vitro de Sunitinib malate (5637). . . 58
4.9 Meloxicam aumenta sinergicamente o efeito in vitro de Sunitinib malate (HT1376). . . 58
4.10 Resultados obtidos pelo InterPharm no caso de estudo IV . . . 59
´Indice de figuras
1.1 Fotomicrografia representativa que mostra a morfologia das c´elulas da bexiga de linhas celulares HCV29, T24, 5637 e HT1376. S˜ao observados corpos apopt´oticos (seta preta), citoplasma (aster´ısco) e c´elulas apopt´oticas (triˆangulo) (Arantes-Rodrigues et al.,2013a).. . . 3
2.1 Representa¸c˜ao esquem´atica do comportamento farmacocin´etico de um f´armaco (Kwon, 2002). . . 10
2.2 Representa¸c˜ao esquem´atica de farmacocin´etica, farmacodinˆamica e rela¸c˜ao farmacocin´etica/farmacodinˆamica de um f´armaco. Cp(t) e
Ce(t) s˜ao as concentra¸c˜oes de f´armaco no plasma e no local de atua¸c˜ao,
respetivamente (Kwon,2002). . . 11
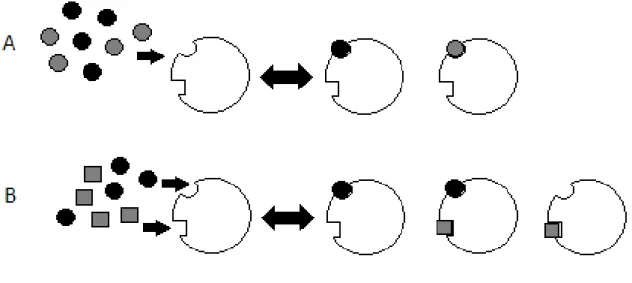
2.3 Representa¸c˜ao esquem´atica dos mecanismos de inibi¸c˜ao. (A) Inibi¸c˜ao competitiva, inibidor (c´ırculos cinzentos) e f´armaco (c´ırculos pretos) ligam-se ao mesmo s´ıtio. (B) Inibi¸c˜ao n˜ao competitiva, inibidor (quadrados cinzentos) e f´armaco ligam-se a locais diferentes (Lee and Kong, 2009). 12
2.4 Esquema da rea¸c˜ao de dois inibidores (quadrados) n˜ao competitivos ligando-se no mesmo local (Breitinger, 2012).. . . 13
2.5 Esquema da rea¸c˜ao de dois inibidores (quadrados e triˆangulos) mutuamente n˜ao exclusivos e n˜ao competitivos ligando-se a locais diferentes (Breitinger,
2012). . . 13
2.6 Ilustra¸c˜ao do ´ındice de intera¸c˜ao. P = (Dy,1,0) representa a dose de
f´armaco 1 que produz o efeito y, Q = (0, Dy,2) representa a dose de
f´armaco 2 que produz o efeito y e U = (d1,d2) representa a dose na
combina¸c˜ao que produz o mesmo efeito y. O caso A representa a situa¸c˜ao de sinergismo e o caso B antagonismo (Lee and Kong,2009). 15
2.7 Exemplo t´ıpico de um gr´afico Fa-CI (Chou, 2006). . . 19
2.8 Exemplo t´ıpico de um gr´afico Fa-DRI (Chou,2006). . . 21
2.9 Equa¸c˜ao do efeito mediano como a conjuga¸c˜ao das teorias de Michaelis-Menten, Hill, Scatchard e de Henderson-Hasselbalch (Chou, 2006). . . 21
2.10 Isobolograma para um determinado efeito, onde a dose de f´armaco A isolado ´e A=20 e de f´armaco B ´e B=100. O ponto Q ´e um par de doses que obtˆem o mesmo efeito com menores quantidades de f´armaco, ou seja ´e sin´ergico, enquanto que o ponto R ´e antag´onico (´e necess´aria mais quantidade de f´armaco). O ponto P aparece muito perto da linha de aditividade, o que pode indicar aditividade (Tallarida,2001). 22
2.11 Isobolas aditivas de uma combina¸c˜ao de f´armacos para diferentes n´ıveis de efeito (Tallarida, 2006). . . 25
2.12 Superf´ıcie tridimensional de dose-efeito, obtida pela experiˆencia de Greco (Greco et al., 1990). . . 26
2.13 Superf´ıcie de ajuste aos pares de doses ao longo do efeito. Ilustra¸c˜ao de um ponto acima da superf´ıcie que indica sinergismo (Tallarida,
2001). . . 27
2.14 Janela do software MATLAB R
GUIDE (mat). . . 29
2.15 Janela resultante da compila¸c˜ao (mat). . . 29
2.16 Interface do software CalcuSyn (bio). . . 31
2.17 Interface da aplica¸c˜ao Curve Fitting toolbox da MathWorks. . . 32
3.1 Interface do InterPharm - Primeira janela gerada pelo programa. . . . 36
3.2 Interface do InterPharm - Janela principal da experiˆencia. . . 37 xxii
3.3 Interface do InterPharm - Cria¸c˜ao de um f´armaco isolado. . . 38
3.4 Interface do InterPharm - Escolha dos f´armacos constituintes da combina¸c˜ao. 38
3.5 Interface do InterPharm - Cria¸c˜ao da combina¸c˜ao de dois f´armacos. . 39
3.6 Interface do InterPharm - Sele¸c˜ao da pasta onde se salva a experiˆencia. 40
3.7 Interface do InterPharm - C´alculo de Dm, CI e DRI para determinado valor de Fa. . . 41
3.8 Interface do InterPharm - Escolha dos f´armacos, combina¸c˜oes e informa¸c˜ao presente no relat´orio. . . 42
3.9 Interface do InterPharm - Introdu¸c˜ao da matriz de dados para gerar a superf´ıcie. . . 43
3.10 Interface do InterPharm - Escolha dos n´ıveis de efeito. . . 43
3.11 Interface do InterPharm - Relat´orio em HTML. . . 44
4.1 Curva dose-efeito. . . 47
4.2 Gr´afico efeito mediano. . . 47
4.3 Gr´afico CI.. . . 47 4.4 Gr´afico log(CI). . . 47 4.5 Gr´afico DRI.. . . 48 4.6 Gr´afico log(DRI). . . 48 4.7 Isobolograma. . . 48 4.8 Curva dose-efeito. . . 50
4.9 Gr´afico efeito mediano. . . 50
4.10 Gr´afico CI.. . . 51 4.11 Gr´afico log(CI). . . 51 4.12 Gr´afico DRI. . . 51 4.13 Gr´afico log(DRI). . . 51 4.14 Isobolograma. . . 52 4.15 Superf´ıcie de ajuste. . . 52 4.16 Curva dose-efeito. . . 54
4.17 Gr´afico efeito mediano. . . 54
4.18 Gr´afico CI.. . . 55
4.19 Gr´afico log(CI). . . 55 xxiii
4.20 Gr´afico DRI. . . 55
4.21 Gr´afico log(DRI). . . 55
4.22 MTX e Ara-C - Isobolograma. . . 56
4.23 An´alise Imunofluorescente. Apoptose celular apresenta-se a fluorescente (Arantes-Rodrigues et al., 2013a). . . 57
4.24 Curva dose-efeito. . . 59
4.25 Gr´afico efeito mediano. . . 59
4.26 Gr´afico CI.. . . 60
4.27 Gr´afico log(CI). . . 60
4.28 T24 - Isobolograma. . . 60
4.29 T24 - Superf´ıcie de ajuste. . . 61
4.30 Curva dose-efeito. . . 61
4.31 Gr´afico efeito mediano. . . 61
4.32 Gr´afico CI.. . . 62
4.33 Gr´afico log(CI). . . 62
4.34 5637 - Isobolograma. . . 63
4.35 5637 - Superf´ıcie de ajuste. . . 63
4.36 Curva dose-efeito. . . 64
4.37 Gr´afico efeito mediano. . . 64
4.38 Gr´afico CI.. . . 64
4.39 Gr´afico log(CI). . . 64
4.40 HT1376 - Isobolograma. . . 65
4.41 HT1376 - Superf´ıcie de ajuste. . . 65
Gloss´
ario, acr´
onimos e
abreviaturas
Lista de acr´
onimos
Sigla Expans˜ao 2D Bidimensional 3D Tridimensional
ADN Acido Desoxirribonucleico´ Ara-C 1-β-D-arabinofuranosilcitosina
α Parˆametro de intera¸c˜ao que indica a magnitude do efeito C50A Concentra¸c˜ao do f´armaco A que produz 50% do efeito
CI Combination Index (´Indice de Combina¸c˜ao) DOM Document Object Model
DRI Dose-reduction index (´Indice de redu¸c˜ao da dose) Dm Dose necess´aria para produzir o efeito mediano
m Coeficiente de Hill que confere sigmoicidade `a curva dose-efeito
dx Dose do f´armaco x na combina¸c˜ao que produz o efeito E
Dx Dose isolada do f´armaco x que produz o efeito E
Sigla Expans˜ao
EDx,y Dose isolada do f´armaco y que produz x% do efeito
E Efeito
Emax Efeito m´aximo
fa Fra¸c˜ao afetada fu Fra¸c˜ao n˜ao afetada
γ coeficiente de Hill (declive da curva dose-efeito) GUI Graphical user interface
GUIDE Graphical user interface design environment IC50 Concentra¸c˜ao de f´armaco para inibir 50%
LD50 Dose letal
p e q Coeficientes de Hill
r Qualidade da reta de ajuste R R´acio entre dois f´armacos RMSE Root mean squared error SSE Sum of squares due to error
Lista de abreviaturas
Abreviatura Significado(s) a.C. antes de Cristo e.g. por exemplo et al. e outros (autores) i.e. isto ´e, por conseguinte
1
Introdu¸c˜
ao
O uso de produtos medicinais pelos humanos j´a ´e bastante antigo, devido `a necessidade de combater doen¸cas e pelo instinto de sobrevivˆencia.
No s´eculo 16 a.C., Papiro de Ebers (Egipto) utilizou v´arios f´armacos, como sangue de lagarto, ´opio, gordura de castor, no desenvolvimento de diversas terapias de cura. Hip´ocrates inaugurou uma nova era para a cura de doen¸cas, atrav´es de leis naturais e afirmou que o corpo tem amplos recursos naturais para a recupera¸c˜ao e o papel do m´edico ´e remover ou reduzir os impedimentos da defesa natural (Levine et al.,
2004).
Com o tempo novas terapias surgiram utilizando a combina¸c˜ao de f´armacos para melhorar a efic´acia dos tratamentos, o que se denomina por intera¸c˜ao de f´armacos. A avalia¸c˜ao destas intera¸c˜oes mudaram drasticamente ao longo da ´ultima d´ecada devido ao desenvolvimento dos medicamentos, o aumento do conhecimento de enzimas que metabolizam os f´armacos e pelo desenvolvimento de ferramentas para estudar a intera¸c˜ao de f´armacos (Huang et al., 2008).
2 CAP´ITULO 1. INTRODUC¸ ˜AO
1.1
Motiva¸c˜
ao
O fen´omeno das intera¸c˜oes de f´armacos constitui na atualidade um dos temas mais importantes e debatidos da farmacologia. A prescri¸c˜ao simultˆanea de v´arios f´armacos e consequente administra¸c˜ao ´e uma pr´atica comummente utilizada em terapias cl´assicas, com a finalidade de aumentar a efic´acia dos tratamentos, reduzir a toxicidade, e/ou tratar doen¸cas coexistentes.
Os f´armacos s˜ao substˆancias qu´ımicas e podem interagir entre si, com nutrientes ou agentes qu´ımicos ambientais, desencadeando respostas ben´eficas, para ampliar os efeitos da terapia, ou indesejadas, como a redu¸c˜ao do efeito. ´E necess´ario desenvolver m´etodos para verificar o efeito da combina¸c˜ao de diferentes componentes de forma a ajudar os profissionais da sa´ude aquando da prescri¸c˜ao a doentes, ou em experiˆencias para a descoberta de novas terapias.
Ao longo dos anos foram desenvolvidos v´arios m´etodos para an´alise da intera¸c˜ao de f´armacos e com a evolu¸c˜ao da tecnologia foi poss´ıvel automatiz´a-los. J´a existe algum software comercial nesta ´area, por´em, s˜ao produtos com pre¸cos bastante avultados. Investigadores desta ´area sem conhecimentos profundos de matem´atica e inform´atica tˆem dificuldades na an´alise do efeito se n˜ao tiverem oportunidade de comprar um software comercial.
Na Universidade de Tr´as-os-Montes e Alto Douro, no departamento de Ciˆencias Veterin´arias foram realizados v´arios estudos na ´area da farmacologia no sentido de descobrir novas terapias. Assim, houve necessidade de verificar o efeito existente atrav´es de m´etodos matem´aticos j´a existentes, analisando os dados obtidos pelas experiˆencias realizadas.
Visando este ´ultimo argumento, pretende-se contribuir com um software, InterPharm, desenvolvido em MATLAB R
, visto ser um software bastante popular em ambiente acad´emico e pela facilidade de uso, com o intuito de melhorar e facilitar a an´alise de dados de combina¸c˜oes de componentes atrav´es de algoritmos e m´etodos cl´assicos
1.1. MOTIVAC¸ ˜AO 3
inclu´ıdos nos software comerciais.
A principal motiva¸c˜ao para este trabalho foi o facto de investigadores da UTAD na ´area da farmacologia terem identificado esta lacuna - de n˜ao ter dispin´ıvel um software gratuito que possam usar sempre que fazem combina¸c˜ao de f´armacos e pretendam inferir se o efeito combinado ´e sin´ergico/aditivo/antag´onico. Alguns artigos foram publicados no seguimento destes estudos pelo departamento de Ciˆencias Veterin´arias (Arantes-Rodrigues et al.,2013a,b) e serviram de casos de estudo para testar a aplica¸c˜ao desenvolvida (Figura 1.1).
Figura 1.1– Fotomicrografia representativa que mostra a morfologia das c´elulas da bexiga de linhas celulares HCV29, T24, 5637 e HT1376. S˜ao observados corpos apopt´oticos (seta preta), citoplasma (aster´ısco) e c´elulas apopt´oticas (triˆangulo) (Arantes-Rodrigues et al.,2013a).
4 CAP´ITULO 1. INTRODUC¸ ˜AO
1.2
Objetivos
O objetivo principal da presente disserta¸c˜ao ´e o desenvolvimento de um programa para o estudo do efeito da intera¸c˜ao de f´armacos, denominado InterPharm, que permita efetuar a an´alise do efeito da combina¸c˜ao de dois componentes, com a possibilidade de escolher se os f´armacos s˜ao mutuamente exclusivos ou n˜ao exclusivos e quais os m´etodos de estudo. Tamb´em permite o c´alculo do ´ındice de combina¸c˜ao, CI, o ´ındice de redu¸c˜ao da dose, DRI, a dose mediana, DM, e apresenta gr´aficos e
tabelas com os dados simulados.
Para al´em deste objetivo principal pretende-se:
• Entender e apresentar os fundamentos da intera¸c˜ao de f´armacos.
• Familiarizar-se com as metodologias e algoritmos existentes da intera¸c˜ao de f´armacos.
• Familiarizar-se e estabelecer comunica¸c˜ao entre as aplica¸c˜oes MATLAB R, GUIDE e Report Generator.
• Testar a fiabilidade do programa InterPharm, atrav´es de diferentes casos de estudo, para cada um dos efeitos.
• Comparar os parˆametros obtidos na aplica¸c˜ao desenvolvida com software j´a existentes.
1.3
Organiza¸c˜
ao da Disserta¸c˜
ao
Esta disserta¸c˜ao encontra-se estruturada em cinco cap´ıtulos. Neste Cap´ıtulo fornece-se uma introdu¸c˜ao de enquadramento e aprefornece-senta-fornece-se a motiva¸c˜ao e objetivos da disserta¸c˜ao.
1.3. ORGANIZAC¸ ˜AO DA DISSERTAC¸ ˜AO 5
No Cap´ıtulo 2 ´e feita uma revis˜ao da literatura, onde se exp˜oem os conceitos relacionados com a intera¸c˜ao de f´armacos e quais os efeitos existentes. Seguidamente faz-se um levantamento dos m´etodos de an´alise do efeito e as ferramentas computacionais j´a desenvolvidas nesta ´area.
No Cap´ıtulo 3 ´e apresentada a aplica¸c˜ao desenvolvida nesta disserta¸c˜ao, bem como os m´etodos utilizados e a explica¸c˜ao das funcionalidades existentes.
O Cap´ıtulo 4 cont´em os resultados de v´arios casos de estudo para cada um dos efeitos poss´ıveis (antagonismo, sinergismo e aditividade).
No Cap´ıtulo 5 s˜ao apresentadas as conclus˜oes baseadas nos resultados obtidos no Cap´ıtulo 4 e faz-se uma discuss˜ao destes. Tamb´em se perspetivam desenvolvimentos futuros.
2
Estado da Arte
Neste cap´ıtulo apresentam-se os principais conceitos referentes `a intera¸c˜ao de f´armacos, os m´etodos existentes para inferir que tipo de efeito existe e a evolu¸c˜ao hist´orica desta ´area da farmacologia.
Ao longo da vida do Homem sempre houve uma procura pelo tratamento de doen¸cas atrav´es da utiliza¸c˜ao de plantas, animais e extratos de solo. Com o avan¸co da tecnologia, farmacologia, isolamento e s´ıntese de f´armacos foi poss´ıvel descobrir v´arias terapias (Breitinger, 2012).
H´a mais de 100 anos que a intera¸c˜ao de f´armacos e os seus efeitos s˜ao estudados. V´arios m´etodos foram criados para analisar os dados por´em ao longo dos anos mudaram drasticamente (Prichard and Shipman, 1990). Com o aparecimento de princ´ıpios de an´alise de f´armacos e o avan¸co da tecnologia foi poss´ıvel implementar estes algor´ıtmos, criando assim aplica¸c˜oes inform´aticas que s˜ao mais r´apidas e precisas no c´alculo dos efeitos de determinadas combina¸c˜oes de componentes, melhorando esta ´area da farmacologia.
O uso de m´ultiplos f´armacos com diferentes modelos e mecanismos de a¸c˜ao pode direcionar o efeito para um ´unico alvo ou doen¸ca de forma a ser tratado mais
8 CAP´ITULO 2. ESTADO DA ARTE
eficientemente. Os resultados favor´aveis do sinergismo incluem o aumento da efic´acia do efeito do tratamento, a diminui¸c˜ao da dosagem mas mantendo ou aumentando a efic´acia evitando toxicidade, minimizar ou diminuir a resistˆencia aos f´armacos e fornecer sinergismo seletivo contra o alvo. Estes benef´ıcios da intera¸c˜ao de f´armacos tˆem levado a este ser o tratamento mais utilizado para as doen¸cas mort´ıferas, como o cancro e doen¸cas infeciosas (por exemplo a SIDA) (Chou, 2006).
2.1
Intera¸c˜
ao de f´
armacos
As intera¸c˜oes biol´ogicas de agentes ativos s˜ao um aspeto importante da farmacologia e da biomedicina. A intera¸c˜ao de f´armacos descreve a atividade biol´ogica que resulta da presen¸ca de v´arios f´armacos ao mesmo tempo no organismo (Breitinger, 2012). Existem v´arias situa¸c˜oes cl´ınicas em que tal fen´omeno ocorre deliberadamente de forma a melhorar os tratamentos, como por exemplo:
• A combina¸c˜ao de f´armacos citot´oxicos no tratamento de tumores e infe¸c˜oes, requerem baixas concentra¸c˜oes de cada f´armaco de forma a obter melhores efeitos com menores efeitos colaterais.
• A combina¸c˜ao de antibi´oticos ´e um exemplo de combina¸c˜ao de melhores efeitos com menores efeitos secund´arios e redu¸c˜ao do desenvolvimento da resistˆencia.
• Muitas situa¸c˜oes cl´ınicas requerem a administra¸c˜ao de v´arios f´armacos devido a v´arias doen¸cas. Por´em nestes casos n˜ao s˜ao estudados os efeitos do conjunto de f´armacos, e tal deveria ser avaliado.
• O efeito de um f´armaco quando por sua vez n˜ao consegue atingir o efeito desejado, pode ser aumentando pela combina¸c˜ao com outro f´armaco.
Existem trˆes classes diferentes de intera¸c˜ao de f´armacos: aditividade, antagonismo e sinergismo, por´em n˜ao existe consenso quanto `a terminologia da intera¸c˜ao de f´armacos por parte dos cientistas. Aditividade ´e quando a resposta `a combina¸c˜ao
2.1. INTERAC¸ ˜AO DE F ´ARMACOS 9
dos f´armacos ´e igual `a esperada dada pela rela¸c˜ao dose-efeito dos f´armacos, ou seja ´e a soma dos efeitos. Antagonismo verifica-se quando a resposta ´e menor que a esperada, isto ´e o resultado ´e menor que a soma dos efeitos individuais. Sinergismo ocorre quando a resposta ´e maior que a esperada (Breitinger, 2012; il Lee,2010).
O efeito antag´onico pode tamb´em ser designado por: intera¸c˜ao negativa, sub-aditiva e sinergismo negativo. Sin´onimos para intera¸c˜ao sin´ergica s˜ao positiva, potencia¸c˜ao e aumento. O termo aditividade tem como sin´onimos zero, intera¸c˜ao nula, indiferen¸ca e independˆencia (Bliss) (il Lee, 2010).
2.1.1
Farmacocin´
etica
A farmacocin´etica ´e uma disciplina do ˆambito da farmacologia e esclarece a a¸c˜ao farmacol´ogica, in vivo, de um f´armaco em diferentes ´org˜aos e tecidos do organismo tendo em conta a dose administrada. Tem um papel importante para prever as quantidades dos f´armacos e suas concentra¸c˜oes em fun¸c˜ao do tempo nos diferentes tecidos.
Os processos b´asicos que um f´armaco sofre no organismo s˜ao absor¸c˜ao, distribui¸c˜ao, metabolismo e excre¸c˜ao (Figura 2.1) (Kwon, 2002), estes eventos sequenciais s˜ao designados por processos ADME.
• Absor¸c˜ao: ´e a primeira etapa e inicia-se com a escolha do tipo de administra¸c˜ao at´e ao momento em que o f´armaco entra na corrente sangu´ınea. Caso a administra¸c˜ao seja intravenosa ou intra-arterial n˜ao existe esta etapa, se o medicamento for administrado por via oral ´e aqui onde se verificam as intera¸c˜oes (S.Rodrigues, 2009). Alguns fatores que interferem nesta etapa s˜ao o pH do meio, patologias (p.e., ´ulceras), dose do f´armaco administrado, concentra¸c˜ao do f´armaco na circula¸c˜ao sist´emica e no local de a¸c˜ao, caracter´ısticas qu´ımicas do f´armaco, entre outros.
• Distribui¸c˜ao: o f´armaco ´e distribu´ıdo pelo organismo atrav´es da circula¸c˜ao. O f´armaco passa inicialmente por ´org˜aos de maior vasculariza¸c˜ao (p.e. pulm˜oes
10 CAP´ITULO 2. ESTADO DA ARTE
Figura 2.1– Representa¸c˜ao esquem´atica do comportamento farmacocin´etico de um f´armaco (Kwon,2002).
e cora¸c˜ao) e depois sofre redistribui¸c˜ao por tecidos menos irrigados (p.e. tecido adiposo). Nesta fase ´e onde o f´armaco chega `a zona de atua¸c˜ao (Kwon,2002).
• Metabolismo: fase onde o f´armaco ´e transformado num composto mais hidrossol´uvel para posterior excre¸c˜ao. Existem duas fases, a primeira onde existe oxida¸c˜ao, redu¸c˜ao e hidr´olise e a fase de conjuga¸c˜ao com substˆancias end´ogenas (S.Rodrigues, 2009).
• Excre¸c˜ao: o f´ıgado ´e o ´org˜ao respons´avel pela prepara¸c˜ao do f´armaco para a excre¸c˜ao. Os compostos s˜ao removidos do organismo para o meio externo (S.Rodrigues, 2009).
2.1.2
Farmacodinˆ
amica
A farmacodinˆamica ´e a fase onde h´a intera¸c˜ao do f´armaco com o recetor, o resultado desta intera¸c˜ao produz o efeito terapˆeutico. A maioria dos f´armacos atua sobre recetores espec´ıficos para desencadear a sua a¸c˜ao farmacol´ogica (S.Rodrigues,2009).
2.1. INTERAC¸ ˜AO DE F ´ARMACOS 11
Figura 2.2 – Representa¸c˜ao esquem´atica de farmacocin´etica, farmacodinˆamica e rela¸c˜ao farmacocin´etica/farmacodinˆamica de um f´armaco. Cp(t) e Ce(t) s˜ao as concentra¸c˜oes de
f´armaco no plasma e no local de atua¸c˜ao, respetivamente (Kwon,2002).
A farmacodinˆamica ´e o estudo da rela¸c˜ao entre a concentra¸c˜ao de um f´armaco no local de atua¸c˜ao, onde os recetores est˜ao localizados, e a magnitude da sua efic´acia farmacol´ogica (Kwon, 2002).
Quando o local de atua¸c˜ao do f´armaco n˜ao ´e no plasma, a concentra¸c˜ao de f´armaco no plasma ´e diferente do local de atua¸c˜ao, ´e necess´ario desenvolver um modelo para estabelecer a rela¸c˜ao entre a chamada concentra¸c˜ao efeito, Ce(t), e a concentra¸c˜ao
plasm´atica, Cp(t), e um modelo farmacodinˆamico que estabelece a rela¸c˜ao entre o
efeito induzido pelo f´armaco e a concentra¸c˜ao efeito, Ce(t) (Figura 2.2) .
2.1.3
Intera¸c˜
ao a n´ıvel molecular
Ao n´ıvel molecular os f´armacos interagem com enzimas e podemos ter dois tipos de intera¸c˜ao: inibi¸c˜ao competitiva e inibi¸c˜ao n˜ao competitiva.
Na inibi¸c˜ao competitiva, a enzima tem uma zona ativa onde o substrato ser´a convertido em produto. Aquando da apresenta¸c˜ao de uma mistura `a zona ativa o f´armaco e o substrato natural da enzima competem pelo s´ıtio ativo da enzima (Figura 2.3A). Este fen´omeno ´e conhecido por liga¸c˜ao mutuamente exclusiva. `A medida que a concentra¸c˜ao de substrato se torna superior ao inibidor, o substrato passa a deslocar o inibidor do s´ıtio ativo da enzima reativando-a (Breitinger, 2012).
No caso da inibi¸c˜ao n˜ao competitiva, a enzima possui uma zona ativa, onde se liga o substrato, e uma outra zona diferente onde se liga o inibidor, assim n˜ao h´a interferˆencia por parte do inibidor e a enzima fica ativa (Figura 2.3B) (Breitinger,
12 CAP´ITULO 2. ESTADO DA ARTE
Figura 2.3 – Representa¸c˜ao esquem´atica dos mecanismos de inibi¸c˜ao. (A) Inibi¸c˜ao competitiva, inibidor (c´ırculos cinzentos) e f´armaco (c´ırculos pretos) ligam-se ao mesmo s´ıtio. (B) Inibi¸c˜ao n˜ao competitiva, inibidor (quadrados cinzentos) e f´armaco ligam-se a locais diferentes (Lee and Kong,2009).
Tanto no caso da inibi¸c˜ao competitiva como na inibi¸c˜ao n˜ao competitiva existe um efeito sin´ergico pois a enzima est´a ativa (Breitinger,2012).
Se dois inibidores n˜ao competitivos se ligam ao mesmo s´ıtio na enzima este s´ıtio s´o pode estar ocupado pelo inibidor A ou B, mas nunca pelos dois inibidores ao mesmo tempo (Figura 2.4). Se um inibidor est´a presente e o outro ´e adicionado pode-se observar uma grande inibi¸c˜ao do efeito, assim existe um efeito aditivo.
No caso de existirem dois locais diferentes de liga¸c˜ao para inibidores n˜ao competitivos, os dois inibidores podem-se ligar simultaneamente `a enzima (Figura 2.5), assim existe liga¸c˜ao mutuamente n˜ao exclusiva. Neste tipo de inibi¸c˜ao n˜ao haver´a um efeito aditivo mas sim superaditivo, ou antag´onico, devido `a grande inibi¸c˜ao das enzimas por parte dos dois inibidores (Breitinger, 2012).
2.2. M´ETODOS DE AN ´ALISE DO EFEITO 13
Figura 2.4– Esquema da rea¸c˜ao de dois inibidores (quadrados) n˜ao competitivos ligando-se no mesmo local (Breitinger,2012).
Figura 2.5 – Esquema da rea¸c˜ao de dois inibidores (quadrados e triˆangulos) mutuamente n˜ao exclusivos e n˜ao competitivos ligando-se a locais diferentes (Breitinger,2012).
2.2
M´
etodos de an´
alise do efeito
O primeiro modelo para descrever a intera¸c˜ao entre f´armacos foi proposto por Fraser em 1872 e era um modelo te´orico que descrevia o antagonismo entre atropina1
e fisostigmina2 (Prichard and Shipman, 1990). Este modelo teve problemas na
representa¸c˜ao em trˆes dimens˜oes. Ap´os 50 anos, um farmacologista alem˜ao, Loewe,
1
F´armaco alcal´oide que age inibindo a atividade do neurotransmissor acetilcolina. 2´
14 CAP´ITULO 2. ESTADO DA ARTE
explorou as alternativas `a representa¸c˜ao deste modelo.
Historicamente, existem trˆes modelos de intera¸c˜ao mais utilizados: independˆencia de Bliss, aditividade de Loewe e princ´ıpio do efeito mediano (il Lee, 2010), m´etodos que ser˜ao abordados mais `a frente.
2.2.1
Aditividade de Loewe
O modelo de aditividade de Loewe foi descrito pela primeira vez em 1926. Este trabalho ´e a base de modelos contemporˆaneos utilizados para analisar a intera¸c˜ao de dois componentes diferentes (Zhao et al., 2010).
A equa¸c˜ao geral de aditividade de Loewe ´e definida por (Lee et al., 2010; il Lee,
2010; Lee and Kong, 2009):
´Indice de Intera¸c˜ao = d1 D1 + d2 D2 < 1, sinergismo = 1, aditividade > 1, antagonismo (2.1)
A forma espec´ıfica ´e:
´Indice de Intera¸c˜ao = d1
ED50,1.(EE−Emax−E0 )1/Y1
+ d2
ED50,2.(EE−Emax−E0 )1/Y2
(2.2)
onde d1 e d2 s˜ao as doses de cada f´armaco na mistura que permite um efeito, E,
e D1 e D2 s˜ao as doses isoladas de cada f´armaco que produzem o mesmo efeito, E
(Figura 2.6).
Devido `as dificuldades em expressar o seu m´etodo atrav´es de superf´ıcies tridimensionais, atendendo a que n˜ao dispunha de meios computacionais, o farmacologista alem˜ao criou o termo isobola, que significa linha de igual eleva¸c˜ao e foi copiada dos cart´ografos. As isobolas s˜ao proje¸c˜oes bidimensionais de superf´ıcies tridimensionais (Prichard and
2.2. M´ETODOS DE AN ´ALISE DO EFEITO 15
Figura 2.6 – Ilustra¸c˜ao do ´ındice de intera¸c˜ao. P = (Dy,1,0) representa a dose de f´armaco
1 que produz o efeito y, Q = (0, Dy,2) representa a dose de f´armaco 2 que produz o efeito
y e U = (d1,d2) representa a dose na combina¸c˜ao que produz o mesmo efeito y. O caso A
representa a situa¸c˜ao de sinergismo e o caso B antagonismo (Lee and Kong,2009).
Shipman, 1990).
Loewe utiliza uma isobola reta para intera¸c˜oes zero quando os f´armacos combinados tˆem mecanismos de a¸c˜ao e rela¸c˜ao dose-efeito semelhantes. Este m´etodo ´e a base do m´etodo do Isobolograma que ser´a abordado mais `a frente (il Lee, 2010).
2.2.2
Independˆ
encia de Bliss
A independˆencia de Bliss (1939) ´e um modelo que implica que dois f´armacos n˜ao cooperem farmacol´ogica ou fisiologicamente um com o outro de forma a que cada componente se comporte de maneira independente. A equa¸c˜ao geral da independˆencia de Bliss (Equa¸c˜ao (2.3)) e a equa¸c˜ao espec´ıfica (Equa¸c˜ao (2.4)) s˜ao as seguintes (il Lee, 2010):
16 CAP´ITULO 2. ESTADO DA ARTE E − E0 Emax− E0 = 1 (1 + ( d1 ED50,1) −γ1)(1 + ( d2 ED50,2)−γ2) (2.4)
Na equa¸c˜ao (2.3), f u13 , f u2 e f u12 s˜ao as fra¸c˜oes de tecido n˜ao afetadas pelo
tratamento para os f´armacos 1 e 2 e na combina¸c˜ao. Na equa¸c˜ao (2.4), a primeira fra¸c˜ao ´e a fra¸c˜ao do efeito resultante da mistura de d1 e d2. d1 e d2 s˜ao as doses de
cada f´armaco na mistura que corresponde ao efeito E. ED50,ii = 1, 2 ´e a dose isolada
dos f´armacos que produzem 50% do efeito m´aximo (Emax) e γ1 e γ2 s˜ao coeficientes
de Hill (declive da curva dose-efeito) (il Lee, 2010).
A independˆencia de Bliss apresenta como vantagem o facto de poder ser diretamente calculado a partir de dados de experiˆencias minimamente amostrados sem interpola¸c˜ao da curva de resposta ou itera¸c˜oes para encontrar as ra´ızes (Prichard and Shipman,
1990).
2.2.3
Princ´ıpio do Efeito Mediano
O princ´ıpio do efeito mediano (Equa¸c˜ao (2.5)) ´e origin´ario de Chou e Talalay em 1984 (Chou and Talalay, 1984), este m´etodo da intera¸c˜ao de f´armacos foi desenvolvido atrav´es da combina¸c˜ao do princ´ıpio f´ısico-qu´ımico da lei da massa-a¸c˜ao com o princ´ıpio matem´atico de indu¸c˜ao e dedu¸c˜ao (Chou and Talalay, 1977;Chou, 2006).
A equa¸c˜ao do efeito mediano ´e dada por (Chou and Talalay, 1984):
fa/fu = (D/Dm)m (2.5)
onde D ´e a dose, fa e fu s˜ao as fra¸c˜oes afetadas e n˜ao afetadas do sistema pela
dose D, respetivamente, Dm ´e a dose necess´aria para produzir o efeito mediano e
m ´e o coeficiente de Hill que confere sigmoicidade `a curva dose-efeito. Se fa+fu=1,
podem-se obter v´arias formas da equa¸c˜ao (2.5) (Chou and Talalay,1984):
3
fa - fra¸c˜ao afetada, por exemplo para um carcinog´enico ´e a fra¸c˜ao de c´elulas cancer´ıgenas que n˜ao sobrevive; fu - fra¸c˜ao n˜ao afetada, fra¸c˜ao de c´elulas que sobrevive.
2.2. M´ETODOS DE AN ´ALISE DO EFEITO 17
fa/(1 − fa) = [(fa)−1− 1]−1 = [(fu)−1− 1] = (D/Dm)m
fa= 1/[1 + (D/Dm)]m
D = Dm[f a/(1 − fa)]1/m
A equa¸c˜ao do efeito mediano (equa¸c˜ao (2.5)) pode ser linearizada aplicando logaritmos de ambos os lados,
log(fa/fu) = m.log(D) − m.log(Dm)
O gr´afico obtido por esta equa¸c˜ao permite saber qual o declive, m, e a interce¸c˜ao do gr´afico dose-efeito com o eixo efeito mediano, ou seja quando fa=fu, fa/fu=1
e consequentemente y=log(fa/fu)=0, que permite determinar log(Dm) e o valor de
Dm (Chou and Talalay, 1984).
Para analisar o efeito de m´ultiplos f´armacos e verificar se existe sinergismo, antagonismo ou aditividade ´e essencial a seguinte informa¸c˜ao:
• ´E necess´aria uma defini¸c˜ao quantitativa de soma uma vez que o sinergismo implica mais do que a soma e o antagonismo ´e menos que a soma dos efeitos.
• ´E preciso saber a rela¸c˜ao dose-efeito para o f´armaco 1, f´armaco 2 e a sua mistura, ou seja o r´acio do f´armaco 1 em rela¸c˜ao ao f´armaco 2 (Chou and Talalay, 1984).
Se dois f´armacos (e.g., D1 e D2) tˆem efeitos que s˜ao mutuamente exclusivos, isto ´e os
f´armacos da combina¸c˜ao atuam de forma dependente um do outro, ent˜ao a soma dos efeitos combinados (fa)1,2 pode ser calculado atrav´es de (Chou and Talalay, 1984):
18 CAP´ITULO 2. ESTADO DA ARTE (fa)1,2 (fu)1,2 = (fa)1 (fu)1 + (fa)2 (fu)2 = = (D)1 (ED50)1 + (D)2 (ED50)2 (2.6)
onde fa ´e a fra¸c˜ao afetada e fu ´e a fra¸c˜ao n˜ao afetada, ED50 ´e a concentra¸c˜ao do
f´armaco que ´e necess´aria para produzir 50% do efeito. Note que fa+ fu=1 ou fa
=1-fu (Chou and Talalay,1984).
Se o efeito de dois f´armacos (e.g., D1 e D2) s˜ao mutuamente n˜ao exclusivos, isto ´e
tˆem modos diferentes de a¸c˜ao e tˆem um local espec´ıfico e independente de intera¸c˜ao, a soma dos efeitos combinados (fa)1,2 pode ser calculado atrav´es de (Chou and
Talalay, 1984): (fa)1,2 (fu)1,2 = (fa)1 (fu)1 +(fa)2 (fu)2 + (fa)1.(fa)2 (fu)1.(fu)2 = = (D)1 (ED50)1 + (D)2 (ED50)2 + (D)1.(D)2 (ED50)1.(ED50)2 (2.7)
Quando s˜ao colocados os resultados experimentais nas equa¸c˜oes (2.6) ou (2.7), se a soma dos dois termos na equa¸c˜ao (2.6) ou a soma dos trˆes termos na equa¸c˜ao (2.7) ´e maior, igual ou menor que 1, ent˜ao pode-se inferir que existe antagonismo, aditividade ou sinergismo, respetivamente. Para quantificar estes efeitos foi necess´ario haver uma designa¸c˜ao, assim criou-se o termo Combination index (CI) (Figura2.7). Para f´armacos mutuamente exclusivos, CI ´e dado por (Chou and Talalay, 1984):
CI = (D)1 (Dx)1
+ (D)2 (Dx)2
(2.8)
2.2. M´ETODOS DE AN ´ALISE DO EFEITO 19
Figura 2.7 – Exemplo t´ıpico de um gr´afico Fa-CI (Chou,2006).
CI = (D)1 (Dx)1 + (D)2 (Dx)2 + (D)1.(D)2 (Dx)1.(Dx)2 (2.9)
Para os dois casos, quando CI: < 1, sinergismo = 1, aditividade > 1, antagonismo
Um dos maiores objetivos do efeito sin´ergico de uma combina¸c˜ao ´e a possibilidade de reduzir as doses dos f´armacos que s˜ao utilizados, mantendo a efic´acia. Neste sentido foi criado o termo Dose-reduction index (DRI) por Chou em 1988. O ´ındice de redu¸c˜ao da dose ´e uma medida que indica a quantidade de cada dose que pode ser diminu´ıda, numa combina¸c˜ao sin´ergica, comparando com as doses de cada f´armaco isolado (Equa¸c˜ao (2.11)) (Chou, 2006).
20 CAP´ITULO 2. ESTADO DA ARTE
diminui¸c˜ao da toxicidade mantendo a efic´acia da terapia. Quanto maior o valor de DRI maior ´e a diminui¸c˜ao da dose para um determinado efeito mas n˜ao garante, necess´ariamente, que haja sinergismo, como se pode verificar pela rela¸c˜ao de CI e DRI na equa¸c˜ao (2.10) (Figura 2.8) (Chou,2006).
CI = (D)1 (Dx)1 + (D)2 (Dx)2 = 1 (DRI)1 + 1 (DRI)2 (2.10) Assim, (DRI)1 = (Dx)1 (D)1 , (DRI)2 = (Dx)2 (D)2 (DRI)1 = (Dm)1[fa/(1 − fa)]1/m1 (D)1 , (DRI)2 = (Dm)2[fa/(1 − fa)]1/m2 (D)2 (2.11)
Este m´etodo de Chou ´e uma teoria baseada em quatro resultados fundamentais das ciˆencias biom´edicas: a equa¸c˜ao de Michaelis-Menten, a equa¸c˜ao de Hill, a equa¸c˜ao de Scatchard e a equa¸c˜ao de Henderson-Hasselbalch (Figura 2.9). Em 2005 Chou e Martin desenvolveram um software , CompuSyn, para facilitar a simula¸c˜ao e os c´alculos autom´aticos dos parˆametros, atrav´es dos dados dose-efeito (Chou, 2006;
Berenbaum, 1977).
2.2.4
Isobolograma
O termos isobola foi utilizado pela primeira vez por Loewe e Muischnek (1926) (Berenbaum,1977). O isobolograma ´e um m´etodo gr´afico que existe h´a v´arios anos com o prop´osito de avaliar se existe sinergismo ou antagonismo em combina¸c˜oes de f´armacos. Este m´etodo ´e aplicado a pares de f´armacos que produzem efeitos semelhantes e quantific´aveis que foram testados como uma fun¸c˜ao das respetivas doses ou concentra¸c˜oes. No caso de se pretender estudar mais do que dois f´armacos o isobolograma n˜ao ´e aplicado (Tallarida, 2012).
2.2. M´ETODOS DE AN ´ALISE DO EFEITO 21
Figura 2.8– Exemplo t´ıpico de um gr´afico Fa-DRI (Chou,2006).
Figura 2.9– Equa¸c˜ao do efeito mediano como a conjuga¸c˜ao das teorias de Michaelis-Menten, Hill, Scatchard e de Henderson-Hasselbalch (Chou,2006).
22 CAP´ITULO 2. ESTADO DA ARTE
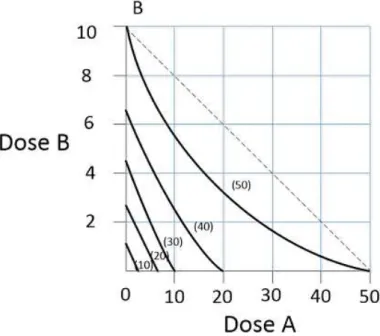
Figura 2.10– Isobolograma para um determinado efeito, onde a dose de f´armaco A isolado ´e A=20 e de f´armaco B ´e B=100. O ponto Q ´e um par de doses que obtˆem o mesmo efeito com menores quantidades de f´armaco, ou seja ´e sin´ergico, enquanto que o ponto R ´e antag´onico (´e necess´aria mais quantidade de f´armaco). O ponto P aparece muito perto da linha de aditividade, o que pode indicar aditividade (Tallarida,2001).
Para criar um isobolograma ´e necess´ario haver r´acio constante4, onde as curvas
de dose-efeito de cada f´armaco permitem a determina¸c˜ao de cada dose que cria um determinado efeito, como a metade do efeito m´aximo (E50). A dose E50´e desenhada
para cada f´armaco como a interce¸c˜ao no sistema de coordenadas cartesianas, em que cada eixo representa as doses individuais de cada f´armaco e as duas interce¸c˜oes definem uma linha reta que se designa por linha de aditividade (Figura2.10). Todos os pontos (a,b) nesta linha s˜ao pares de doses (Grabovsky and Tallarida, 2004). Quando a isobola para determinado efeito estiver determinada, o par de doses da combina¸c˜ao que experimentalmente produz este efeito pode ser desenhado no gr´afico como um ponto. Este ponto vai estar a cima ou abaixo da linha de aditividade e assim determina-se se existe sinergismo ou antagonismo, respetivamente (Grabovsky and Tallarida, 2004).
E = EmaxA/(A + A50)
4
r´acio nas doses dos dois f´armacos. Exemplo: se dose A=[100 200 300 400] e dose B=[10 20 30 40] o r´acio ´e constante e igual a 10:1.
2.2. M´ETODOS DE AN ´ALISE DO EFEITO 23
e
E = EmaxB/(B + B50)
Neste caso o r´acio, R, ´e R = A/B = A50/B50. Quando os dois componentes
est˜ao presentes em quantidades a e b ´e poss´ıvel expressar a quantidade de a em equivalˆencia do componente B, designado por b’, e dado por b’ = a/R. Para determinado efeito em que se pretende a dose B, a combina¸c˜ao equivalente ´e b + b’ = B, ou b + a/R = B. ´E comum expressar o ´ultimo na interce¸c˜ao de forma a criar uma linha reta que intercepta A e B (Figura 2.11) (Grabovsky and Tallarida,2004).
a A +
b B = 1
Quando os efeitos (m´aximos) produzidos pelos f´armacos s˜ao distintos a an´alise a efetuar ´e necessariamente diferente. Considere-se, por conveniˆencia, que o efeito m´aximo (Ec) para B ser´a de 100 (Grabovsky and Tallarida, 2004).
E = 100B/B + B50
e
E = EcA/A + Ac
A dose da combina¸c˜ao (a,b) dos f´armacos A e B s˜ao equivalentes `a dose b + b’ do f´armaco B, onde b’ ´e obtido pela equa¸c˜ao
b’ = 100 B50
Ec(1 + Ac
a ) − 1
(2.12)
A isobola para um efeito espec´ıfico ´e dada por b + b’ = B ou
b + 100 B50
Ec(1 + Ac
a) − 1
24 CAP´ITULO 2. ESTADO DA ARTE
Para casos em que as curvas dose-efeito n˜ao s˜ao descritas por hip´erboles, mas s˜ao ajustadas por
E = EbBp/(Bp+ B50p )
e
E = EcAq/(Aq+ Aqc)
os coeficientes de Hill (p e q) s˜ao utilizados nas equa¸c˜oes dose-efeito e o isobolograma da equa¸c˜ao (2.12) generaliza-se (Tallarida, 2012):
b = Bi− B50 [Eb Ec(1 + Aqc aq) − 1] 1/p (2.14)
Este m´etodo de an´alise permaneceu como padr˜ao nos campos da quimioterapia antiviral e anticancer´ıgena durante mais de 25 anos, devido `a sua especificidade de mostrar o efeito para diferentes concentra¸c˜oes de f´armaco (Prichard and Shipman,
1990).
2.2.5
Modelo de Greco
Greco et al em 1990 apresentou uma nova abordagem para qualificar o efeito numa combina¸c˜ao de f´armacos, utilizando cisplatina e 1-β-D-arabinofuranosilcitosina (ara-C) (Figura 2.12). Este m´etodo foi desenvolvido adaptando e combinando outros modelos j´a existentes, como o conceito fundamental dos isobologramas de Loewe, equa¸c˜oes e s´ımbolos foram adaptados de Chou e Talalay, entre outros (Greco et al.,
1990).
A equa¸c˜ao (2.15) cont´em as concentra¸c˜oes dos f´armacos (d1 e d2) como valores de
entrada e α ´e o parˆametro de intera¸c˜ao, que indica a magnitude do sinergismo, aditividade e antagonismo (il Lee, 2010).
2.2. M´ETODOS DE AN ´ALISE DO EFEITO 25
Figura 2.11 – Isobolas aditivas de uma combina¸c˜ao de f´armacos para diferentes n´ıveis de efeito (Tallarida,2006).
1 = d1
ED50,1.(EE−Emax−E0 )1/γ1
+ d2
ED50,2.(EE−Emax−E0 )1/γ2
+ αxd1xd2
ED50,1xED50,2.(EE−Emax−E0 )(1/2γ1+ 1/2γ2)
(2.15)
A equa¸c˜ao (2.16) define o ´ındice de intera¸c˜ao para a combina¸c˜ao de dois f´armacos (il Lee, 2010). ´ındice de Intera¸c˜ao = d1 D1 + d2 D2 = = 1 − α.d1.d2
ED50,1.ED50,2.(EE−Emax−E0 )(1/2γ1+ 1/2γ2)
26 CAP´ITULO 2. ESTADO DA ARTE
Quando α > 0, o ´ındice de intera¸c˜ao ´e menor que um, logo h´a sinergismo; quando α < 0 o ´ındice de intera¸c˜ao ´e maior que um, logo h´a antagonismo; quando α = 0, o efeito ´e aditivo (il Lee,2010).
Figura 2.12 – Superf´ıcie tridimensional de dose-efeito, obtida pela experiˆencia de Greco (Greco et al.,1990).
2.2.6
Resposta em superf´ıcie
Outro m´etodo de avalia¸c˜ao da resposta da combina¸c˜ao de dois f´armacos ´e a resposta atrav´es de uma superf´ıcie. ´E poss´ıvel mostrar a rela¸c˜ao da combina¸c˜ao de dois componentes num gr´afico tridimensional, onde as doses representam as coordenadas cartesianas no plano xOy e o efeito ´e desenhado como a distˆancia vertical acima do plano xOy. Este conjunto de pontos espaciais permite visualizar a rela¸c˜ao dose-efeito na combina¸c˜ao (Tallarida, 2001).
Utilizando os pontos espaciais pode-se criar uma superf´ıcie lisa de ajuste, que representa a aditividade da combina¸c˜ao. Esta superf´ıcie de aditividade ´e a superf´ıcie de referˆencia utilizada para inferir qual o efeito de combina¸c˜ao presente. Um ponto
2.2. M´ETODOS DE AN ´ALISE DO EFEITO 27
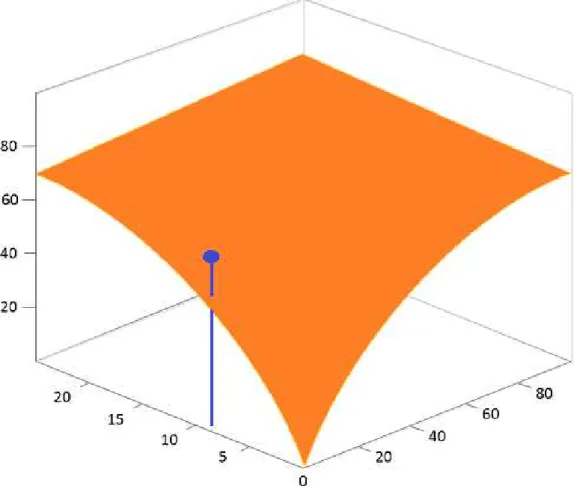
que esteja significativamente acima da superf´ıcie indica sinergismo, por´em se um ponto estiver abaixo da superf´ıcie est´a-se perante um efeito antag´onico (Figura2.13) (Tallarida,2001).
Figura 2.13– Superf´ıcie de ajuste aos pares de doses ao longo do efeito. Ilustra¸c˜ao de um ponto acima da superf´ıcie que indica sinergismo (Tallarida,2001).
Os m´etodos tridimensionais atualmente utilizados para examinar as intera¸c˜oes de f´armacos tˆem muitas vantagens em rela¸c˜ao `as aproxima¸c˜oes bidimensionais. Nos modelos tridimensionais ´e poss´ıvel visualizar a superf´ıcie de resposta; nos modelos 2D quando se pretende analisar o mesmo h´a uma vari´avel que fica constante tornando a an´alise incompleta. Tamb´em nos modelos 3D ´e poss´ıvel quantificar o sinergismo e antagonismo, podendo-se assim comparar diferentes combina¸c˜oes e a forma da curva de sinergismo ´e caracter´ıstica de cada combina¸c˜ao de f´armacos.
28 CAP´ITULO 2. ESTADO DA ARTE
2.3
Ferramentas Computacionais: MATLAB
R,
GUIDE e Report Generator
MATLAB R
(matrix laboratory) foi lan¸cado em 1984. No seu site a MathWorks R
define o software MATLAB R
como um ambiente interativo para computa¸c˜ao num´erica, visualiza¸c˜ao e programa¸c˜ao e ´e a linguagem de alto n´ıvel utilizada por muitos engenheiros e cientistas no mundo.
As ferramentas, a linguagem e as fun¸c˜oes matem´aticas permitem explorar diversas abordagens e chegar a uma solu¸c˜ao mais r´apida do que com outras linguagens de programa¸c˜ao tradicionais (e.g. C/C++).
Este software possibilita explorar e visualizar ideias, analisar dados, criar algoritmos e modelos. O MATLAB R
pode ser utilizado em v´arias ´areas, como o processamento de imagem e sinal, comunica¸c˜ao, sistemas de controlo, teste e medi¸c˜ao, biologia computacional, finan¸cas computacionais, entre outros, atrav´es de novos produtos que s˜ao criados para estender as capacidades deste produto, as toolboxes.
O MATLAB R
possui duas ferramentas computacionais relevantes para este trabalho, o GUIDE e o Report Generator. O GUIDE (do inglˆes graphical user interface design environment) ´e um ambiente de desenvolvimento de interfaces gr´aficas por parte do utilizador em MATLAB R
, que oferece ferramentas para criar interfaces gr´aficas para aplica˜oes, as GUIs (sigla do inglˆes graphical user interface) (Lent, 2013).
A GUI ´e uma representa¸c˜ao gr´afica de uma ou mais janelas que contˆem componentes, que tornam a aplica¸c˜ao interativa. O GUIDE codifica automaticamente em MATLAB R
a constru¸c˜ao das GUIs, caso o utilizador pretenda maior controlo sobre o design e desenvolvimento da interface pode criar a fun¸c˜ao que define o comportamento e propriedades de cada componente e, assim, desenvolver a GUI programaticamente.
Os componentes da GUI podem incluir bot˜oes, bot˜oes de r´adio, menus, barras de slide, listas, paineis de bot˜oes e exibir dados em tabelas ou gr´aficos (Figura2.14).
2.3. FERRAMENTAS COMPUTACIONAIS: MATLAB R,
GUIDE E REPORT GENERATOR 29
Figura 2.14– Janela do software MATLAB R GUIDE (mat).
30 CAP´ITULO 2. ESTADO DA ARTE
O produto Report Generator do MATLAB R
permite criar um relat´orio formatado em Microsoft R
Word, HTML ou PDF onde se apresentam os resultados dos programas ou aplica¸c˜oes criados em MATLAB R
. Podem-se utilizar modelos j´a existentes para criar os relat´orios atrav´es da aplica¸c˜ao Report Explorer ou ent˜ao conceber um programaticamente usando DOM(Document Object Model ) (Mathworks,2014).
2.4
Aplica¸c˜
oes Inform´
aticas
A Inform´atica M´edica ´e uma ´area da Engenharia Biom´edica que intersecta as ciˆencias
da informa¸c˜ao, as ciˆencias da computa¸c˜ao e a medicina, com a finalidade de desenvolvimento de m´etodos, tecnologias e dispositivos necess´arios para a optimiza¸c˜ao de aquisi¸c˜ao,
armazenamento e utiliza¸c˜ao de informa¸c˜ao nas atividades relacionadas com a presta¸c˜ao de servi¸cos m´edicos e com investiga¸c˜ao biom´edica.
Cada vez mais s˜ao desenvolvidas aplica¸c˜oes de Inform´atica M´edica adotadas a diferentes n´ıveis de cuidados de sa´ude devido ao desenvolvimento das tecnologias e `a crescente necessidade por parte das institui¸c˜oes de sa´ude, de racionalizar recursos, de cruzar dados cl´ınicos, controlar as ´areas administrativa e financeira e haver um planeamento.
2.4.1
CompuSyn
O software CompuSyn foi desenvolvido em 2005 por Chou e Martin, no seguimento de v´arios estudos realizados pelos cientistas no desenvolvimento de m´etodos sobre a intera¸c˜ao de f´armacos. Este software utiliza o princ´ıpio de efeito mediano da lei de massa-a¸c˜ao (Chou, 2006; Chou and Talalay, 1977) e o seu m´etodo de ´ındice de combina¸c˜ao (Chou and Talalay, 1984).
O CompuSyn ´e um programa para quantificar o sinergismo e antagonismo em combina¸c˜oes de f´armacos e na determina¸c˜ao dos valores de IC50, ED50e LD50. Este
2.4. APLICAC¸ ˜OES INFORM ´ATICAS 31
Figura 2.16– Interface do software CalcuSyn (bio).
determina¸c˜ao autom´atica dos valores de CI e DRI, pode ser usado para casos de r´acio constante e casos de r´acio n˜ao constante, tamb´em se pode fazer um relat´orio com toda a informa¸c˜ao, tabelas e gr´aficos acerca da an´alise da intera¸c˜ao dos f´armacos.
2.4.2
CalcuSyn
O CalcuSyn ´e um software desenvolvido pela Biosoft e permite analisar a dose-efeito para um ou m´ultiplos f´armacos. Utiliza o m´etodo do efeito mediano de Chou e Talalay (Chou, 2006; Chou and Talalay, 1977).
Neste programa os dados podem ser introduzidos atrav´es do teclado ou pela importa¸c˜ao de um ficheiro e podem ser processados para f´armacos isolados ou combina¸c˜oes com r´acios constante ou n˜ao constante. O CalcuSyn gera automaticamente gr´aficos dos dados, como a dose-efeito, efeito mediano, isobolograma e CI-efeito (Figura 2.16) e um relat´orio com informa¸c˜ao estat´ıstica dos dados, os valores de CI e EDX e os
32 CAP´ITULO 2. ESTADO DA ARTE
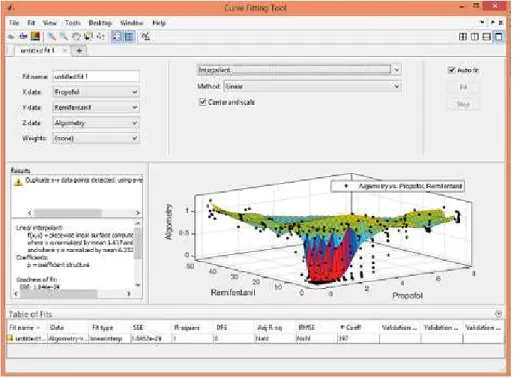
Figura 2.17– Interface da aplica¸c˜ao Curve Fitting toolbox da MathWorks.
2.4.3
Curve Fitting toolbox
A MathWorks criou uma toolbox onde ´e poss´ıvel analisar que tipo de efeito existe, na combina¸c˜ao de dois componentes, atrav´es da superf´ıcie de ajuste designada por Curve Fitting toolbox. Nesta toolbox ´e necess´ario introduzir uma matriz de doses e efeitos, com dados das doses isoladas e na combina¸c˜ao para assim criar uma malha de pontos que v˜ao ser dispostos tridimensionalmente. Tamb´em existem v´arios m´etodos poss´ıveis para se fazer o ajuste da superf´ıcie, como m´etodos de interpola¸c˜ao, regress˜oes lineares e n˜ao-lineares e suaviza¸c˜ao (Figura 2.17), tamb´em ´e poss´ıvel fazer o ajuste da superf´ıcie atrav´es de uma equa¸c˜ao determinada e introduzida pelo utilizador. Quando ´e feito o ajuste s˜ao apresentadas as informa¸c˜oes da qualidade do ajuste como os valores de SSE (sum of squares due to error ), de R-quadrado, de R-quadrado ajustado e de RMSE (Root mean squared error ).
Esta aplica¸c˜ao baseia-se no modelo de intera¸c˜ao de Greco et al. (Greco et al.,1990), que se representa pela seguinte rela¸c˜ao:
2.4. APLICAC¸ ˜OES INFORM ´ATICAS 33 E = Emax.( C′ A C50A + C′ B C50B + α. C′ A C50A + C′ B C50B) n ( CA′ C50A + C′ B C50B + α. C′ A C50A + C′ B C50B) n+ 1 (2.17)
onde Emax ´e o efeito m´aximo do f´armaco A e do f´armaco B, C50A e C50B s˜ao as
concentra¸c˜oes individuais que produzem 50% do efeito m´aximo, n ´e o declive da curva de resposta de farmacodinˆamica e α ´e o ´unico parˆametro que caracteriza a natureza da intera¸c˜ao entre dois f´armacos para determinado efeito (Kern et al.,
3
Desenvolvimento da aplica¸c˜
ao
InterPharm
A proposta central deste trabalho versa sobre o desenvolvimento de uma ferramenta computacional a partir de trˆes outras: o MATLAB R
(vers˜ao R2014a), o GUIDE e o Report Generator.
O programa InterPharm permite efetuar a an´alise do efeito da combina¸c˜ao de dois f´armacos bidimensional e tridimensionalmente, com r´acios constantes e para componentes mutuamente exclusivos e n˜ao exclusivos, para v´arios n´ıveis de efeito. Neste cap´ıtulo apresentam-se as etapas necess´arias para desenvolver a aplica¸c˜ao InterPharm e os algoritmos utilizados.
3.1
Algoritmos do programa InterPharm
Os algoritmos utilizados no programa InterPharm para a an´alise da rea¸c˜ao de dois f´armacos em combina¸c˜ao s˜ao o Princ´ıpio do Efeito Mediano de Chou e Talalay (1984) (Cap´ıtulo 2.2.3), o m´etodo do Isobolograma (Cap´ıtulo 2.2.4) e o m´etodo da Resposta em Superf´ıcie baseado no modelo de Greco et al. (1990) (Cap´ıtulo 2.2.5).
36 CAP´ITULO 3. DESENVOLVIMENTO DA APLICAC¸ ˜AO INTERPHARM
3.2
Metodologia utilizada
Uma vez encontrados os algoritmos pretendidos para implementar na aplica¸c˜ao, iniciou-se o desenvolvimento da interface em MATLAB R
.
A interface gr´afica da aplica¸c˜ao desenvolvida foi realizada atrav´es de programa¸c˜ao. Utiliza os algoritmos descritos nesta disserta¸c˜ao bem como a interface propriamente dita. Quase tudo ´e transparente para o investigador que n˜ao ´e programador. A interface permite introduzir os dados das doses de f´armaco, o tipo de combina¸c˜ao e caracter´ısticas espec´ıficas e no final ´e poss´ıvel gerar um relat´orio em formato HTML/PDF/WORD com conslus˜oes obtidas atrav´es de diferentes m´etodos.
O software InterPharm possibilita a implementa¸c˜ao de um sistema de an´alise ajustado por inteligˆencia computacional de maneira mais simplificada e interativa.
3.2.1
Figura 1 - InterPharm
Quando o utilizador executa a aplica¸c˜ao InterPharm a primeira interface gr´afica que ´e mostrada est´a representada na figura3.1.
Figura 3.1 – Interface do InterPharm - Primeira janela gerada pelo programa.
A ferramenta desenvolvida permite que o utilizador selecione se pretende realizar uma nova experiˆencia ou uma j´a efetuada (figura3.1).
3.2. METODOLOGIA UTILIZADA 37
3.2.2
Figura 2 - Nova experiˆ
encia
No caso do utilizador pretender realizar uma nova experiˆencia ´e apresentada uma outa janela para ser preenchida com o nome da experiˆencia, data, descri¸c˜ao e os f´armacos (figura 3.2).
Figura 3.2 – Interface do InterPharm - Janela principal da experiˆencia.
3.2.3
Figura 3 - Novo f´
armaco
Para a introdu¸c˜ao de um novo f´armaco aparece uma terceira janela onde o utilizador coloca as informa¸c˜oes gerais do f´armaco, como o nome, a abreviatura, as unidades, e as doses e respetivos efeitos (figura 3.3). Caso os dados introduzidos na tabela dose-efeito estejam incorretos, o utilizador tem a op¸c˜ao de limpar a tabela e colocar novamente os dados, ou ent˜ao ir `a tabela e clicar sobre o valor incorreto e substitu´ı-lo. Tamb´em existe o bot˜ao de cancelar a cria¸c˜ao do novo f´armaco. Quando o utilizador pretender salvar os dados introduzidos e voltar `a janela anterior, clica no bot˜ao ’Finished’.
38 CAP´ITULO 3. DESENVOLVIMENTO DA APLICAC¸ ˜AO INTERPHARM
Figura 3.3– Interface do InterPharm - Cria¸c˜ao de um f´armaco isolado.
3.2.4
Figura 4 - Nova combina¸c˜
ao de f´
armacos
Ap´os o utilizador preencher a lista dos f´armacos isolados com pelo menos dois f´armacos, este pode fazer a combina¸c˜ao de f´armacos escolhendo quais os que pretende combinar (figura 3.4), atrav´es de dupla sele¸c˜ao na lista apresentada com os nomes dos f´armacos. Depois o utilizador tem de selecionar clicando no bot˜ao de r´adio se os f´armacos tˆem r´acio constante ou n˜ao. Termina esta fase selecionando o bot˜ao ’Ok’. Caso queira voltar `a janela anterior seleciona o bot˜ao ’Cancel’.
3.2. METODOLOGIA UTILIZADA 39
3.2.5
Figura 5 - Nova combina¸c˜
ao de f´
armacos
Nesta fase aparece uma nova janela onde o utilizador pode introduzir o nome da combina¸c˜ao, a abreviatura, os valores de r´acio de cada f´armaco e as doses e efeitos correspondentes (figura 3.5). Para preencher a tabela dose-efeito basta apenas introduzir a dose de um dos f´armacos ou a dose total e automaticamente s˜ao gerados e apresentados nos devidos locais os valores das outras duas doses, depois introduz-se o valor do efeito e ao fazer ’Enter’ os dados s˜ao colocados na tabela. Aqui tamb´em h´a a possibilidade de limpar os dados da tabela dose-efeito e cancelar a nova combina¸c˜ao de f´armacos. Para salvar pressiona-se o bot˜ao ’Finished’.
Figura 3.5 – Interface do InterPharm - Cria¸c˜ao da combina¸c˜ao de dois f´armacos.
3.2.6
Figura 6 - Salvar Experiˆ
encia
Ap´os introduzida toda a informa¸c˜ao ´e aconselh´avel que o utilizador salve a experiˆencia, selecionando o bot˜ao ’Save Experiment’. Depois ser´a apresentada uma janela (figura
3.6) onde o utilizador poder´a selecionar onde quer salvar a experiˆencia e com que nome (este dever´a ser sem espa¸cos), preferencialmente deve-se salvar na pasta que ´e apresentada (cujo nome ´e InterPharm). Depois de ser salva a experiˆencia o software cria uma pasta com o nome da mesma onde colocar´a toda a informa¸c˜ao gerada acerca desta.
40 CAP´ITULO 3. DESENVOLVIMENTO DA APLICAC¸ ˜AO INTERPHARM
Figura 3.6 – Interface do InterPharm - Sele¸c˜ao da pasta onde se salva a experiˆencia.
3.2.7
Figura 7 - Calcular Parˆ
ametros
Ap´os se salvar a experiˆencia o utilizador seleciona o bot˜ao ’Recall Experiment’ na janela da figura 3.1 e a janela correspondente `a figura 3.2 ser´a preenchida com os dados. Nesta fase o utilizador pode pretender mais ou menos informa¸c˜ao, no caso de pretender menos informa¸c˜ao acerca da intera¸c˜ao da combina¸c˜ao dos f´armacos, seleciona o bot˜ao ’Calculate Parameters’. Nesta sec¸c˜ao ´e apresentada a dose m´edia, Dm, para cada f´armaco e combina¸c˜ao, o ´ındice de combina¸c˜ao, CI, e o ´ındice de redu¸c˜ao da dose, DRI, para cada f´armaco, pr´e-definido para 50% do efeito (figura
3.2. METODOLOGIA UTILIZADA 41
Figura 3.7– Interface do InterPharm - C´alculo de Dm, CI e DRI para determinado valor de Fa.
3.2.8
Figura 8 - Gerar o Relat´
orio
Quando o utilizador pretende uma informa¸c˜ao mais detalhada, este pressiona o bot˜ao ’Generate Report’. Primariamente seleciona quais os f´armacos que pretende colocar no relat´orio (m´aximo dois) e clica ’Ok’, de seguida ´e apresentada uma nova janela onde seleciona qual a combina¸c˜ao de f´armacos pretendida (m´aximo uma) e clica em ’Ok’. Nesta fase s˜ao poss´ıveis as seguintes combina¸c˜oes: apenas um f´armaco, a combina¸c˜ao dos dois f´armacos, ou os f´armacos intervenientes e a combina¸c˜ao (figura
3.8). Ap´os escolher os dados que pretende, selecciona qual a informa¸c˜ao que necessita para a sua an´alise, que s˜ao as seguintes:
• Dose Effect Table • Dose Effect Plot • Median Effect Plot • CI Table
42 CAP´ITULO 3. DESENVOLVIMENTO DA APLICAC¸ ˜AO INTERPHARM • Fa-CI Plot • Fa-Log(CI) Plot • DRI Table • Fa-DRI Plot • Fa-Log(DRI) Plot • Isobologram • Surface Fit
Figura 3.8 – Interface do InterPharm - Escolha dos f´armacos, combina¸c˜oes e informa¸c˜ao presente no relat´orio.
3.2.9
Figura 9 - Superf´ıcie de Ajuste
No caso de ser selecionado o t´opico Suface Fit aparece uma janela onde o utilizador introduzir´a os v´arios valores de efeitos para as doses indicadas e assim ser´a produzida uma matriz de pontos necess´aria para gerar a superf´ıcie de ajuste da resposta (figura
3.2. METODOLOGIA UTILIZADA 43
Figura 3.9– Interface do InterPharm - Introdu¸c˜ao da matriz de dados para gerar a superf´ıcie.
3.2.10
Figura 10 - Isobolograma
Para desenhar o isobolograma s˜ao necess´arios trˆes n´ıveis de efeito, por defeito est˜ao os valores de 0.5, 0.75 e 0.9 mas o utilizador pode alterar estes valores pelos que pretender, numa janela que aparecer´a ap´os selecionar o ´ıtem Isobologram (figura
3.10).
44 CAP´ITULO 3. DESENVOLVIMENTO DA APLICAC¸ ˜AO INTERPHARM
3.2.11
Figura 11 - Relat´
orio
No final ´e gerado e apresentado um relat´orio em HTML com tabelas e gr´aficos pretendidos pelo utilizador (figura3.11). Esta informa¸c˜ao gerada, figuras e relat´orios em HTML e Word, ´e guardada na pasta criada aquando do salvamento da experiˆencia.
4
Apresenta¸c˜
ao e discuss˜
ao dos
resultados
No sentido de validar a aplica¸c˜ao desenvolvida foram realizados alguns testes com f´armacos isolados e em combina¸c˜ao que j´a foram implementados em outros softwares. Os resultados e discuss˜oes de cada um destes casos de estudo s˜ao tratados neste cap´ıtulo a seguir.
4.1
Caso de estudo I- Rotenone e Pyrethrins
Neste primeiro caso de estudo pretendeu-se verificar o efeito existente numa experiˆencia in vivo com a combina¸c˜ao de dois f´armacos anti-moscas. Os dados utilizados para o caso de estudo apresentam-se na Tabela 4.1.
Estes dados foram compilados na aplica¸c˜ao InterPharm e no software CompuSyn e os resultados obtidos dos parˆametros dose-efeito, CI e DRI est˜ao presentes na tabela 4.2. Pode-se verificar que os valores obtidos na aplica¸c˜ao desenvolvida s˜ao semelhantes aos do CompuSyn.