UNIVERSIDADE FEDERAL DO CEARÁ
CENTRO DE CIÊNCIAS
DEPARTAMENTO DE QUÍMICA ORGÂNICA E INORGÂNICA
Contribuição para a Padronização Química de Espécies do
Gênero
Plectranthus
: Derivatização e Validação de Métodos
Analíticos para a Quantificação de Marcadores Químicos
LEANDRO BEZERRA DE LIMA
Tese Submetida à Coordenação do Curso de Pós Graduação em Química como Requisito Parcial para a Obtenção do Título de Doutor.
Orientador: Profa. Dra. Maria Goretti de Vasconcelos Silva
Dedico Aos meus pais,
AGRADECIMENTOS
À professora Dra. Maria Goretti, pela valiosa orientação, confiança depositada, pela liberdade dada para o desenvolvimento deste trabalho, pelo conhecimento compartilhado e pela amizade, o que foi de grande importância para meu crescimento pessoal e profissional.
Aos professores Dr. Marcos Carlos e Dr. Maria Conceição por todos os ensinamentos, atenção, colaboração e pelo espaço que me foi cedido e que tornaram possível a conclusão dos meus experimentos.
Aos professores Dr. Alberto J. Cavalheiro e Dra. Eveline S. B. Cavalcanti por participarem da banca examinadora e por contribuírem com a conclusão deste trabalho.
Ao professor Dr. Daniel Esdras pela atenção e auxílio na obtenção dos espectros de ressonância magnética nuclear das minhas amostras.
À professora Dra. Maria Teresa por toda atenção e colaboração.
A todos os amigos do Laboratório de Produtos Naturais e do Laboratório de Biotecnologia e Síntese Orgânica em especial ao Edângelo, Tiago Augusto, Tiago Correia, Thiago Fonseca, Ricardo Marques, Ricardo Araújo, Emanuela, Reinaldo, Carol, Daniely, Natália, Tasso Gabriel, Bárbara, Caroline, Juliana, Elayne, Daniel Marcos, Francisco Sales, Amélia, Rogério e Roberto, por terem me ajudado e incentivado ao longo da minha vida acadêmica na UFC.
Aos meus pais, Raimundo e Francisca, aos meus irmãos, Douglas e Danilo, por todo o amor, suporte, compreensão, dedicação e atenção, por estarem sempre do meu lado em todos os momentos, principalmente nos mais adversos.
À Fernanda, por todo apoio, compreensão, incentivo e amor, tornando os momentos mais difíceis apenas em pequenos obstáculos.
Ao Fernando, Regina e Samuel, pelo apoio, confiança e amizade, desde o meu ingresso na graduação até a conclusão do meu doutorado.
LISTA DE TABELAS
Tabela 1 - Diterpenos abietanos - perfil químico-farmacológico de Labiatae ... 12
Tabela 2 - Representação estrutural dos diterpenos abietanos identificados em Labiatae nos últimos 40 anos (numeração referente à Tabela 1) ... 23
Tabela 3 - Deslocamento químico de RMN 13C ( δ) (125 MHz, CDCl3) para PGD-1, com padrão de hidrogenação obtido por comparação com DEPT-135° ... 35
Tabela 4 - Comparação dos dados de RMN 1H e de 13C de PGD-1 com valores da literatura (Albuquerque, 2007) para a substância barbatusina. ... 36
Tabela 5 - Comparação dos dados de RMN 1H e de 13C de PGD-2 com valores da literatura (Albuquerque, 2004). ... 40
Tabela 6 - Comparação dos dados de RMN 1H e de 13C de DB-1 com valores da literatura (Albuquerque, 2004). ... 42
Tabela 7 - Deslocamento químico de RMN 13C (δ) (125 MHz, CDCl3) para OXB, com padrão de hidrogenação obtido por comparação com DEPT-135°. ... 45
Tabela 8 - Comparação dos dados de RMN 1H e de 13C de OXB com valores da literatura (Albuquerque et al, 2007) para a substância barbatusina. ... 46
Tabela 9 - Recuperação do analito em função da concentração. ... 65
Tabela 10 - Coeficientes de variação em função da concentração do analito. ... 66
Tabela 11 – Condições de eluição estabelecidas para cada marcador químico... 68
Tabela 12 - Concentrações dos analitos injetados em triplicadas e as áreas correspondentes para cada curva analítica. ... 75
Tabela 13 - Resultados da regressão linear para as duas curvas analíticas. ... 75
Tabela 14 - Teores dos marcadores químicos nos extratos etanoicos das folhas de P. grandis, P. barbatus, P. ornatus e P. amboinicus. ... 76
Tabela 15 - Percentuais de recuperação de BARB e DEBARB em P. grandis, P. barbatus, P. ornatus e P amboinicus. ... 77
Tabela 16 – Determinação da precisão intradia... 78
Tabela 17 - Terminação da precisão interdias para três níveis de concentração de BARB e DEBARB. ... 79
Tabela 18 - Limite de detecção dos marcadores químicos obtido pelos parâmetros da curva analítica. ... 80
Tabela 19 - Limite de detecção obtida pela injeção em decaplicata. ... 80
Tabela 20 - Limite de quantificação dos marcadores químicos obtido pelos parâmetros da curva analítica. ... 81
Tabela 21 - Limite de quantificação obtida pela injeção em decaplicata. ... 81
Tabela 22 - Inibição do crescimento celular (IC%) das amostras em três linhagens tumorais testadas na dose única de 25µM. ... 83
Tabela 23 - IC50 para a barbatusina, 3-β-hidroxi-3-deoxobarbatusina e OXB. ... 84
Tabela 24 - Número de larvas mortas para as espécies de Plectranthus. ... 85
Tabela 25 - Valores de concentração letal para a mortalidade de 50 e 99% das larvas do mosquito Aedes aegypti para as espécies de Plectranthus. ... 86
Tabela 26 - Fracionamento de PGE por partição líquido-líquido. ... 90
LISTA DE FIGURAS
Figura 1 - Representação estrutural dos compostos isolados e identificados de
Plectranthus barbatus e Plectranthus forskohlii ... 2
Figura 2 - Representação estrutural de compostos com atividade gastroprotetora ... 3
Figura 3 - Representação estrutural dos constituintes químicos do óleo essencial de Plectranthus grandis ... 4
Figura 4 - Registro fotográfico de espécies do gênero Plecthanthus: P grandis (a), P. barbatus (b), P. ornatus (c) e P amboinicus (d) (Fonte: MGVSilva) ... 7
Figura 5 - Representação estrutural dos esqueletos abietanos ... 23
Figura 6 - Espécies de Labiatae produtoras de diterpenos abietanos... 33
Figura 7 - Espectro de massas de alta resolução de PGD-1 ... 35
Figura 8 – Representação estrutural do diterpeno barbatusina ... 36
Figura 9 - Espectro de RMN 1H de PGD-1 ... 37
Figura 10 - Espectro de RMN 13C de PGD-1 ... 37
Figura 11 - Espectro de RMN 13C DEPT-135º de PGD-1 ... 38
Figura 12 - Espectro na região do infravermelho de PGD-1 ... 38
Figura 13 - Representação estrutural do diterpeno 3β-hidroxi-3-deoxobarbatusina ... 39
Figura 14 - Espectro de massas de alta resolução de PGD-2 ... 39
Figura 15 - Espectro de RMN 1H de PGD-2 ... 40
Figura 16 - Espectro de RMN 13C de PGD-2 ... 41
Figura 17 - Representação estrutural do diterpeno 3-hidroxi-3-deoxobarbatusina ... 42
Figura 18 - Espectro de RMN 1H de DB-1 ... 43
Figura 19 - Espectro de RMN 13C de DB-1 ... 43
Figura 20 - Espectro de RMN 13C DEPT de DB-1 ... 44
Figura 21 - Espectro de massas de alta resolução de OXB ... 45
Figura 22 - Representação estrutural de OXB ... 46
Figura 23 - Espectro de RMN 1H de OXB ... 48
Figura 24 - Espectro de RMN 13C BB de OXB ... 48
Figura 25 - Espectro de RMN 13C DEPT-135° ... 49
Figura 26 - Espectro bidimensional de correlação heteronuclear 1H x 13C HSQC de OXB ... 49
Figura 27 - Expansão 1 do espectro bidimensional de correlação heteronuclear 1H x 13C HSQC de OXB. ... 50
Figura 28 - Expansão 2 do espectro bidimensional de correlação heteronuclear 1H x 13C HSQC de OXB. ... 50
Figura 29 - Espectro bidimensional de correlação homonuclear 1H x 1H COSY de OXB ... 51
Figura 30 - Expansão 1 do espectro bidimensional de correlação homonuclear 1H x 1H COSY de OXB. ... 52
Figura 32 – Expansão 1 do espectro bidimensional de correlação heteronuclear 1H x 13C
à longa distancia (HMBC) de OXB. ... 54
Figura 33 - Expansão 2 do espectro bidimensional de correlação heteronuclear 1H x 13C à longa distancia (HMBC) de OXB. ... 55
Figura 34 - Expansão 3 do espectro bidimensional de correlação heteronuclear 1H x 13C à longa distancia (HMBC) de OXB. ... 56
Figura 35 - Expansão 4 do espectro bidimensional de correlação heteronuclear 1H x 13C à longa distancia (HMBC) de OXB. ... 57
Figura 36 - Expansão 5 do espectro bidimensional de correlação heteronuclear 1H x 13C à longa distancia (HMBC) de OXB ... 58
Figura 37 - Expansão 6 do espectro bidimensional de correlação heteronuclear 1H x 13C à longa distancia (HMBC) de OXB. ... 59
Figura 38 - Espectro de RMN 1H de PDB ... 60
Figura 39 - Espectro de RMN 1H da Barbatusina (PGD-1) ... 61
Figura 40 - Cromatograma de BARB na concentração de 25 ppm ... 72
Figura 41 - Cromatograma de BARB na concentração de 50 ppm ... 72
Figura 42 - Cromatograma de BARB na concentração de 100 ppm ... 72
Figura 43 - Cromatograma de BARB na concentração de 250 ppm ... 73
Figura 44 - Cromatograma de BARB na concentração de 500 ppm ... 73
Figura 45 - Cromatograma de DEBARB na concentração de 25 ppm ... 73
Figura 46 - Cromatograma de DEBARB na concentração de 50 ppm ... 74
Figura 47 - Cromatograma de DEBARB na concentração de 100 ppm ... 74
Figura 48 - Cromatograma de DEBARB na concentração de 250 ppm ... 74
Figura 49 - Cromatograma de DEBARB na concentração de 500 ppm ... 74
Figura 50 – Registro fotográfico dos cristais obtidos da fração diclorometano de PGEPD ... 91
LISTA DE ESQUEMAS
Esquema 1 - Esquema biossintético via mevalonato de terpenoides (SIMÕES, 2001).. 10
Esquema 2 - Semi-rota biossintética para formação do esqueleto abieta-7,13-dieno (MACMILLAN, 1999). ... 11
Esquema 3 - Reação de redução da barbatusina. ... 94
Esquema 4 - Reação de hidrólise ácida da Barbatusina ... 94
Esquema 5 - Reação de hidrólise alcalina, em metanol, da Barbatusina ... 94
Esquema 6 - Reação de hidrólise ácida, em metanol, da Barbatusina ... 95
Esquema 7 - Reação de metilação da Barbatusina com base fraca ... 95
Esquema 8 - Reação de metilação da Barbatusina com base forte ... 96
Esquema 9 - Reação de metilação da Barbatusina com éter coroa... 96
Esquema 10 - Reação de benzilação da Barbatusina ... 97
LISTA DE FLUXOGRAMAS
LISTA DE GRÁFICOS
LISTA DE ABREVIATURAS
BARB Barbatusina
BB - Broudband
CCD - Cromatografia em Camada Delgada CDCl
3 - Clorofórmio
CLAE-DAD Cromatografia Líquida de Alta Eficiência Acoplada a Detector de Arranjo de Diodos
COSY - Correlation Spectroscopy
DB-1 Substância derivada da barbatusina
DEBARB 3β-hidróxi-3-deoxobarbatusina
DEPT - Distortionless Enhancement by
Polarization Transfer
DPE Desvio Padrão Relativo
HMBC - Heteronuclear Multiple Bond
Connectivity
HPM/FJAM - Horto de Plantas Medicinais Francisco José Abreu Matos.
HSQC - Heteronuclear Single Quantum
Correlated
J - Constante de Acoplamento
LD Limite de Detecção
LPN - Laboratório de Produtos Naturais
LQ Limite de Quantificação
OXB Substância derivada da barbatusina
P.F. - Ponto de Fusão
PGD-1 Substância obtida da fração
diclorometano de P. grandis
PGD-2 Substância obtida da fração
diclorometano de P. grandis
PGEPA Fração acetato de etila da partição do extrato etanoico de P. grandis
PGEPB Fração n-butanol da partição do extrato etanoico de P.grandis
PGEPD Fração diclorometano da partição do extrato etanoico de P. grandis
PGEPH Fração hexano da partição do extrato etanoico de P. grandis
RMN-13
C - Ressonância Magnética Nuclear de
Carbono-13
RMN-1H - Ressonância Magnética Nuclear de Hidrogênio
RSD Relative Standard Deviation
UFC - Universidade Federal do Ceará
RESUMO
Plectranthus grandis (Cramer) R. H. Willense é uma planta medicinal conhecida popularmente no Ceará como boldo-grande, utilizada pela população em substituição a P. barbatus (boldo), que apresenta atividade gastroprotetora já comprovada para a planta, atividade esta, atribuída a diterpenos que foram isolados desta planta, validando cientificamente seu uso popular. Este trabalho descreve alguns procedimentos analíticos visando contribuir para a padronização química de quatro espécies de Plectranthus. Os diterpenos barbatusina e 3β-hidroxi-3-deoxobarbatusina foram isolados através de
técnicas cromatográficas, sendo possível desenvolver um método de extração seletiva para a barbatusina, o que possibilitou obter quantidade significativa desta substância. Foram realizadas reações de derivatização, obtendo-se a 3-hidroxi-3-deoxobarbatusina, que possui atividade gastroprotetora, in vivo, já reportada na literatura, e a oxima da barbatusina, inédita na literatura, com atividade citotóxica mais potente do que sua precursora. As elucidações estruturais foram realizadas através de espectroscopia na região do infravermelho (IV), RMN 1H, RMN 13C, DEPT-135º, COSY, HMBC e HSQC em comparação com dados da literatura. Utilizando a técnica de cromatografia líquida de alta eficiência com detector de arranjo de diodos (CLAE-DAD) desenvolveu-se métodos para a quantificação de barbatusina e 3β-hidroxi-3-deoxobarbatusina, em
que foram encontrados parâmetros adequados de linearidade (r2 > 0,99), para as duas substâncias analisadas. O método foi validado e apresentou linearidade (r2 = 0,9931 para a barbatusina e r2 = 0,9966 para a 3β-hidroxi-3-deoxobarbatusina), seletividade,
precisão intra-dia (DPR (desvio padrão relativo) < 2,8% para a barbatusina e DPR < 3,5% para a 3β-hidroxi-3-deoxobarbatusina), exatidão (recuperação entre 81,7% e
ABSTRACT
Plectranthus grandis (Cramer) Willense is a medicinal plant popularly known in Ceará as boldo-grande, used by population in substitution of P. barbatus (boldo). It shows gastroprotective activity and this activity is attributed to diterpenes have been isolated from this plant, scientifically validating its popular use. This work describes the analytical procedures used and obtained results, aiming to contribute for chemical standardization of four Plectranthus species. Barbatusin and 3β
-hydroxy-3-deoxobarbatusin diterpenes were isolated by chromatographic techniques, being possible to develop selective extraction method of barbatusin, which enabled to obtain significant amount of this substance. Derivatization reactions were performed, getting 3-hydroxy-3-deoxobarbatusin, having gastroprotective activity, in vivo, already reported in the literature, and oxyimine product of barbatusin, unpublished in the literature, with cytotoxic activity more potent than its precursor. Structural elucidation were performed by infra-red spectroscopy, NMR 1H and NMR 13C, compared with literature data. Using HPLC-DAD, methods were developed for quantification of barbatusin and 3β
-hydroxy-3-deoxobarbatusin, in wich suitable parameters have been found of linearty (r2 > 0,99), for both analytes. The method was validated and presented linearity (r2 = 0.9931 for barbatusin and r2 = 0.9966 for 3β-hydroxy-3-deoxobarbatusin), selectivity, within-day
precision (RSD < 2.8% for barbatusin and RSD < 3.5% for 3β
CAPíTULO 1... 1
INTRODUÇÃO ... 1
CAPÍTULO 2: ... 6
CONSIDERAÇÕES BOTÂNICAS ... 6
2.1 - A Família Lamiaceae. ... 6
2.2 - Considerações Botânicas sobre Plectranthus grandis. ... 8
2.3 - Considerações Botânicas sobre Plectranthus barbatus. ... 8
2.4 - Considerações Botânicas sobre Plectranthus amboinicus. ... 8
2.5 - Considerações Botânicas sobre Plectranthus ornatus. ... 9
CAPÍTULO 3 ... 10
DITERPENOS ABIETANOS DE LABIATAE NOS ÚLTIMOS 40 ANOS (revisão bibliográfica) ... 10
CAPÍTULO 4 ... 34
RESULTADOS E DISCUSSÃO ... 34
4.1- Determinação Estrutural ... 34
4.1.1--Obtenção e Determinação Estrutural de PGD-1 ... 34
4.1.2 - Obtenção e Determinação Estrutural de PGD-2... 38
4.1.3–Produtos de derivatização da Barbatusina ... 41
4.1.3.1 – Obtenção e Determinação Estrutural de DB-1 ... 41
4.1.3.2 – Obtenção e Determinação Estrutural de OXB-1 ... 44
4.1.3.2 – Produtos de hidrólise, metilação e benzilação da barbatusina ... 60
4.1.3.3 – Avaliação do produto de Degradação da Barbatusina em Meio Alcalino (PDB). 60 4.2 – Reatividade biocatalítica da barbatusina... 61
4.2.1-Triagem com Enzimas ... 61
4.2.2-Triagem com Fungos ... 61
CAPÍTULO 5 ... 62
DESENVOLVIMENTO E VALIDAÇÃO DE MÉTODOS ANALÍTICOS POR CROMATOGRAFIA LÍQUIDA DE ALTA EFICIÊNCIA COM DETECTOR DE ARRANJO DE DIODOS PARA DETERMINAÇÃO DOS MARCADORES QUÍMICOS, BARBATUSINA (BARB) E 3-Β-HIDROXI-3-DEOXOBARBATUSINA (DEBARB) EM QUATRO ESPÉCIES DO GÊNERO PLECTRANTHUS ... 62
5.1 - Validação e Parâmetros de Validação ... 62
5.2 - Parâmetros de Validação ... 63
5.2.1 - Linearidade ... 63
5.2.3 - Precisão ... 65
5.2.4 - Limite de Detecção ... 66
5.2.5 - Limite de Quantificação ... 67
5.3- Análise Quantitativa por CLAE-DAD para os marcadores (BARB) e (DEBARB) em quatro espécies do gênero Plectranthus: P. grandis, P. barbatus, P. ornatus e P. amboinicus. ... 67
5.3.1- Desenvolvimento do método ... 67
Condições cromatográficas utilizadas ... 67
Preparação das amostras ... 68
Preparação das soluções padrões ... 68
Estimativa das Faixas de Concentração de Trabalho ... 69
Construção das Curvas Analíticas ... 69
5.3.2- Validação do método ... 69
Seletividade ... 69
Linearidade ... 70
Limite de Detecção (LD) ... 70
Limite de Quantificação (LQ) ... 70
Exatidão ... 71
Precisão ... 71
5.4 - RESULTADOS ... 71
5.4.1-Desenvolvimento do método ... 71
Obtenção das Curvas Analíticas ... 71
5.4.2- Validação do método ... 76
Exatidão ... 76
Precisão ... 78
Precisão intradia... 78
Precisão interdias ... 79
Limite de Detecção (LD) ... 80
Limite de quantificação (LQ)... 81
CAPÍTULO 6 ... 83
ATIVIDADES BIOLÓGICAS DOS EXTRATOS DE Plectranthus E BARBATUSINA ... 83
6.1.-Avaliação da Citotoxicidade In Vitro ... 83
6.2-Potencial larvicida dos extratos de Plectranthus frente a Aedes aegypti... 85
CAPíTULO 7... 87
PARTE EXPERIMENTAL ... 87
7.3 – Ponto de Fusão... 89
7.4 – Coleta das Plantas Estudadas. ... 89
7.5 - Isolamento dos Constituintes Químicos de Plectranthus grandis. ... 89
7.5.1 - Obtenção do Extrato Etanoico das Folhas de Plectranthus grandis. ... 89
7.5.2-Fracionamento do Extrato Etanoico (PGE) ... 90
7.5.3-Isolamento de PGD-1. ... 91
7.5.4 - Isolamento de PGD-2 ... 93
7.6 - Derivatização da Barbatusina ... 93
7.6.1 - Obtenção de 3β-hidroxi-3-deoxobarbatusina (DB-1) ... 93
7.6.2 – Obtenção do produto de hidrólise ... 94
7.6.3 – Obtenção do produto de metilação ... 95
7.6.4 – Obtenção do produto de benzilação ... 97
7.6.5- Reação de Formação da oxima (OXB) ... 97
7.6.6 – Avaliação da Decomposição da Barbatusina em Meio Alcalino ... 97
7.6.7.-Reatividade da Barbatusina em Reações Biocatalisadas e de Biotransformações ... 98
I - Triagem com enzimas ... 98
II - Triagem com fungos ... 98
7.7 - Atividades Biológicas ... 98
7.7.1 - Avaliação da Citotoxicidade in vitro da Barbatusina ... 98
7.7.2 - Avaliação do Potencial Larvicida (utilizando as larvas de Aedes aegypti) ... 99
CAPITULO 8 ... 100
CONCLUSÃO ... 100
CAPÍTULO 9 ... 102
CONSTANTES FÍSICAS E DADOS ESPECTROMÉTRICOS DOS CONSTITUINTES QUÍMICOS OBTIDOS DE Plectranthus grandis ... 102
PGD-1 ... 102
PGD-2 ... 103
DB-1 ... 104
OXB ... 105
CAPÍTULO 10 ... 106
CAPíTULO 1
INTRODUÇÃO
O gênero Plectranthus (sin. Coleus) pertencente à família Labiatae (sin. Lamiaceae) engloba cerca de 300 espécies, das quais muitas são usadas como ornamentais e ou medicinais, ocorrendo de forma nativa na África, Ásia e Austrália (Ascensão et al, 1998).
Espécies do gênero Plectranthus apresentam capacidade biossintética para produzir metabólitos secundários em diversidade, destacando-se entre estes, os diterpenos, inclusive alguns com propriedades biológicas comprovadas (Marques et al, 2006; Buznego e Perez-Saad, 1999; Abdel-mogib et al, 2002; Hagiwara et al, 2003). São constituintes identificados em P. barbatus (falso boldo), Ciclobutatusina (Zelnik et al, 1977), 6β-hidroxicarnosol (Kelecom, 1983), barbatusol (Kelecom, 1983), plectrina
(Kubo, 1984), cariocal (Kelecom, 1985), coleon E, coleon F, plectrinona A e plectrinona B (Ruedi, 1986), e apresentam importância farmacológica. Por sua vez, o estudo do óleo essencial da parte aérea e raízes da espécie P. barbatus apresentou β
-cariofileno, α-pineno, β-felandreno, β-(z)-ocimeno, manool e abietatrieno (Kerntopf,
2002; Albuquerque, 2006).
Dentre as várias espécies de Plectranthus de interesse químico-biológico podemos citar também Plectranthus forskohlii, cuja análise cromatográfica forneceu um diterpeno labdano de alta importância farmacológica, que foi denominada forskolina (7β-acetoxi-8,13-epoxi-1α, 6β,9α-triidroxi-labd-14-en-11-ona), que apresenta atividade
anti-hipertensiva, anti-glaucoma, antiinflamatória, inibidor da agregação plaquetária, bronco dilatador e ativador da adenilase ciclase (SHAH, 1980). Assim, só em 2001 foram encontradas mais de 1500 citações no Chemical Abstracts (HAGIWARA, 2003) sobre forskolina, que é disponível comercialmente na concentração de 10% a U$ 49,00 (60 cápsulas), para uso humano sem comprovação, como auxiliar na queima de gorduras e aumento da testosterona.
Figura 1 - Representação estrutural dos compostos isolados e identificados de Plectranthus barbatus e Plectranthus forskohlii
CH2 β-Cariofileno OAc O OH O H OH H Ciclobutatusina O OH O
6β-Hidroxi-carnosol
OH HO Barbatusol CHO O O OH OH Cariocal O O OAc OH OH Plectrina O H O OH OAc Coleon E O H O OAc Coleon F O O HO OH OH OH Plectrinona A O O HO OH OH
Plectrinona B α-Pineno β-Felandreno β-(z)-Ocimeno
HO
H
Manool Abietatrieno
Plectranthus grandis (Cramer) Willense é uma planta aromática morfologicamente semelhante à P. barbatus (malva santa), diferindo basicamente no tamanho do porte arbustivo e das partes aéreas sendo popularmente conhecida como boldo grande. Entre os fatores divergentes marcantes das duas espécies, está o fato de que P. grandis florescer até duas vezes ao ano em regiões não serranas e apresentar amargor de caules e folhas enquanto P. barbatus apresenta amargor apenas nas folhas e floresce apenas uma única vez por ano (MATOS, 2000). A semelhança entre as duas espécies é suficiente para que, algumas pesquisas encontradas na literatura sobre P. barbatus, especialmente aquelas baseadas em estudos etnofarmacológicos, possam ter sido realizadas com P. grandis, por engano de identificação botânica (MATOS, 2000).
A população utiliza P. grandis em substituição a P. barbatus, planta que apresenta atividade hipossecretora gástrica já comprovada (LAPA et al, 1991) e estudos anteriores demonstraram propriedade gastroprotetora de vários diterpenos isolados da planta (SCHMEDA-HIRSCHMANN et al, 2002; MELO et al, 2003; RODRÍGUEZ et al, 2006), validando desta forma o uso popular desta planta, no combate às doenças relacionadas ao aparelho digestivo. O óleo essencial de Plectranthus grandis é rico em
β-cariofileno, e relatos recentes comprovam a atividade antioxidante do óleo
(ALBUQUERQUE et al, 2006).
A busca realizada utilizando a ferramenta de busca Scifinder, em março de 2013, apresenta apenas dez artigos publicados sobre a espécie Plectranthus grandis, dos quais somente quatro versam sobre sua constituição química. Albuquerque e col. (2010) relatam o efeito protetor contra lesões gástricas induzidas pela ingestão de etanol em ratos, com a administração oral de 3β-hidroxi-3-deoxobarbatusina (5 e 10 mg/kg) e barbatusina (5 e 10 mg/kg) (figura 2). Para as respectivas doses empregadas, a redução da lesão foi de 53, 58 e 96% para a 3β-hidroxi-3-deoxobarbatusina e 32 e 76% para barbatusina.
Figura 2 - Representação estrutural de compostos com atividade gastroprotetora
OAc
OAc OH O
O O
H
OAc
OAc OH HO
O O
H
essenciais das folhas de P. grandis cultivada no Ceará, apresenta majoritariamente trans-β-cariofileno (31,3-40,2%), germacreno-D (12,5-24,5%) e eugenol (15,4%)
(figura 3). O ensaio do DPPH que mede a capacidade sequestrante de radicais livres do substrato realizado com o óleo essencial das folhas desta planta, apresentou um índice de varredura de DPPH (2,2-difenil-1-picril-hidrazil) de 83,28% (ALBUQUERQUE, 2006).
Figura 3 - Representação estrutural dos constituintes químicos do óleo essencial de Plectranthus grandis
As investigações em busca de biocompostos oriundos de plantas herbáceas, tais como as espécies de Plectranthus, apresentam a vantagem da disponibilidade do material vegetal, sem impacto das floras nativas, pois muitas se propagam facilmente permitindo cultivos, inclusive para fins comerciais. A variabilidade qualitativa e quantitativa dos constituintes bioativos pode influenciar a ação terapêutica apresentada pela planta, sendo necessário um conhecimento mais completo possível, dos parâmetros que envolvem e promovem esta quimiodiversidade.
Para Plectranthus grandis, os dados encontrados na pesquisa bibliográfica, até então, são insuficientes para promover o uso racional desta planta e validar seu uso medicinal popular de modo que esta espécie foi selecionada para o desenvolvimento deste trabalho. A presença relatada de diterpenos de esqueleto abietanos em P. grandis, que são conhecidos por sua diversidade de atividades farmacológicas, notadamente barbatusina, justifica a continuação de estudo da espécie, com o desenvolvimento de extração seletiva de barbatusina, desenvolvimento e validação de métodos analíticos
para a quantificação dos marcadores químicos barbatusina e 3β
-hidroxi-3-deoxobarbatusina visando contribuir para a padronização química de espécies do gênero
Plectranthus.
CH2
O
HO
Foram utilizadas no desenvolvimento deste trabalho, técnicas cromatográficas como cromatografia em coluna aberta, cromatografia em camada delgada, CLAE (cromatografia líquida de alta eficiência), além de técnicas de determinação estrutural como ressonância magnética nuclear (RMN1H), carbono (RMN13C) e 1H x 1H COSY, HMBC, HMQC e espectroscopia de infravermelho.
CAPÍTULO 2:
CONSIDERAÇÕES BOTÂNICAS 2.1 - A Família Lamiaceae.
A família Lamiaceae possui quase 4000 espécies contidas em aproximadamente 220 gêneros, entre eles estão Salvia, Ocimum, Mentha e Plectranthus, com uma rica diversidade de usos etnobotânicos, ampla diversidade morfológica e uma distribuição quase cosmopolita.
As espécies desta família evitam, em geral, florestas tropicais e os trópicos, e igualmente as regiões frias. Preferem os habitat livres, abertos, declives secos e pedregosos, matas da Córsega, ilhas mediterrâneas e cumes de montanhas ensolaradas. Nestes locais habitam as espécies mais características e mais nobres, enquanto variantes menos nobres são encontradas nas áreas mais úmidas dos prados à beira dos regatos e na sombra das florestas. As folhas das plantas são odoríferas, opostas duas a duas, mas a planta não se detém na fase vegetativa foliar, pois tendem a produzir flores o mais rápido possível. Flores são abundantes, têm formas marcantes, caracteres específicos e variados, próprio da família. Os frutos são pequenos do tipo aquênio, separando-se caracteristicamente em quatro frutículos parciais (núculas), onde cada um é uma pequena noz. Os tricomas glandulares multicelulares são responsáveis pela presença e o teor do óleo essencial, presentes principalmente nas folhas e nos cálices das flores. (LUKHOBA et al, 2006; HEDGE, 1992)
Plectranthus é um dos gêneros que compõem a família , e possui aproximadamente 300 espécies distribuídas na África tropical, apesar de as espécies da família Lamiaceae evitarem as regiões tropicais, Ásia e Austrália (LUKHOBA et al, 2006). O táxon Plectranthus inclui plantas ricas em diterpenos, que são substâncias responsáveis por variadas e importantes propriedades medicinais tais como antiviral, antifúngica, anti-hipertensiva, antioxidante, citotóxica entre outras. No Brasil, várias destas espécies foram introduzidas pelos colonizadores europeus a partir da África, provavelmente seguindo a rota do tráfego de escravos.
ocorrência mais comum no Brasil são P. grandis, P. barbatus, P. ornatus e P. amboinicus (Figura 4)
Figura 4 - Registro fotográfico de espécies do gênero Plecthanthus: P grandis (a), P. barbatus (b), P. ornatus (c) e P amboinicus (d) (Fonte: MGVSilva)
a) b)
A espécie Plectranthus grandis é popularmente conhecida no Brasil como boldo-grande, boldão, boldo-da-folha-boldo-grande, falsa malva-santa e boldo mexicano, sendo designado na literatura por Plectranthus grandis (Cramer) Willense.
Conforme dados da literatura (CRAMER, 1977), Plectranthus grandis é um arbusto com até 3 m de altura com folhas maiores do que 4,7 cm, racemo com 56 cm de comprimento, caule subquadrangular espesso e com pelos; inflorescência racemosa, com racemo simples erétil, 26 - 56 cm, pedúnculo rígido, portando flores com corola maior do que 2,0 cm de comprimento de coloração azul. Esta espécie é capaz de florescer no Nordeste nas regiões serranas, litorâneas ou sertão central, no que diferem das outras espécies que necessitam de clima mais ameno ou temperado como ocorre em regiões serranas com clima úmido.
2.3 - Considerações Botânicas sobre Plectranthus barbatus.
Popularmente conhecida no Brasil pelas denominações de malva-santa, boldo-nacional, boldo-falso ou sete-dores. Na literatura cientifica seu nome botânico é Plectranthus barbatus Andr., tendo sido referida anteriormente pela designação de Coleus barbatus.
Plectranthus barbatus é uma grande e ereta erva ou subarbusto flexível, atingindo até 1,75 m de altura, ramos densamente tormentosos, de folhas aromáticas pecioladas, limbo semissuculento, oval e largamente elíptico, densamente tormentoso, face inferior com glândulas, ápice obtuso e arredondado, base acuneada, margem regularmente crenado-denteada, pecíolo 10 - 20 mm de comprimento, bráctea oval acuminada, caduca, corola azul claro, 17 - 20 mm de comprimento no fruto tubo geniculado mais ou menos no meio e expandindo-se na base por 3 mm. Não floresce no Nordeste a não ser em regiões serranas com clima mais ameno (KERNTOPF, 1998).
2.4 - Considerações Botânicas sobre Plectranthus amboinicus.
A planta é popularmente conhecida no Brasil pelas designações de malvariço, malva do reino e hortelã da folha grande. Na literatura cientifica é referida pelo nome botânico de Plectranthus amboinicus (Lour) Spreng..
ao ser dobrado. As folhas são muito aromáticas e carnudas e se dispõem em pares opostos, duas a duas. No Nordeste não produz flores, a não ser em regiões serranas que apresentem climas mais amenos. É uma erva nativa da Índia, sendo encontrada em toda América tropical, desde as Antilhas até o sul do Brasil, onde são cultivadas em pequenos canteiros e jardins para fins medicinais e muitas vezes para como condimento em culinária. Apresenta ação antibacteriana e expectorante e são facilmente multiplicadas por estaquia.
P. amboinicus difere basicamente de Plectranthus barbatus Andr. por possuir folhas duras e quebradiças e sem sabor amargo. (MATOS, 1994)
2.5 - Considerações Botânicas sobre Plectranthus ornatus.
No Brasil esta espécie é popularmente conhecida pelos nomes populares boldo-gambá, boldo-pequeno ou boldo-miúdo e novalgina e cientificamente é designado como Plectranthus ornatus Codd.. As vezes é confundida com Plectranthus neochilus Schld espécie muito semelhante morfologicamente.
CAPÍTULO 3
DITERPENOS ABIETANOS DE LABIATAE NOS ÚLTIMOS 40 ANOS (revisão bibliográfica)
Os diterpenos são metabólitos secundários formados via mevalonato, em que o mevalonato é formado da condensação de uma unidade da acetoacetil- CoA com uma molécula da acetil-CoA. Após a condensação aldólica, ocorre uma hidrólise originando a 3-hidroxi-3-metilglutaril-CoA, que é reduzida a mevalonato numa reação irreversível. O mevalonato é então convertido em isopentenil-pirofosfato (IPP), ou isopreno ativo, a unidade básica na formação dos terpenos e esteroides. A polimerização do mevalonato origina moléculas de cadeias crescentes de cinco em cinco átomos de carbono. A molécula de isopentenil-pirofosfato e seu isômero dimetilalil-pirofosfato (DMAPP) formam trans-geranil-pirofosfato (GPP), a partir do qual se formam os demais terpenos (Esquema 1). Novas ligações cabeça-cauda entre o trans-geranil-pirofosfato e o isopentenil-pirofosfato resultarão em sesquiterpeno (C15) e diterpenos (C20). (Simões, 2001).
Esquema 1 - Esquema biossintético via mevalonato de terpenoides (SIMÕES, 2001)
S C o A
O O
S C o A O
C o A - S H
O O
O S C o A
O O
O H
3 - h i d r ó x i - 3 - m e t i l - g l u t a r il C o A
O H O H
O P P m e v a l o n a t o
g e r a n i l p i r o f o s f a t o ( G P P ) M O N O T E R P E N O S ( C 1 0 )
O P P f a r n e s i l p i r o f o s f a t o ( F P P ) S E S Q U I T E R P E N O S ( C 1 5 )
O P P
g e r a n i l g e r a n i l - p ir o f o s f a t o ( G G P P )
D I T E R P E N O S ( C 2 0 )
A partir do pirofosfato de geranil-geranila, a enzima abietadieno sintase catalisa a formação de abieta-7,13-dieno (Esquema 2) por uma série de etapas de ciclização, iniciada por uma ciclização próton-induzida e concluída pela saída do difosfato (MACMILLAN, 1999).
Esquema 2 - Semi-rota biossintética para formação do esqueleto abieta-7,13-dieno (MACMILLAN, 1999).
A presença dos diterpenos abietanos é frequentemente detectada em espécies da família Labiatae. A pesquisa bibliográfica realizada nos últimos quarenta anos (1972 a 2013) com as palavras-chave “abietane” e “Labiatae” indicou 110 e 175 registros, utilizando o software de busca SciFinder® e www.scopus.com, respectivamente. Todas as referências foram relatadas na forma de artigos publicados em jornais e revistas, e nenhuma patente foi encontrada. Observou-se uma modesta evolução no número de publicações (Gráfico 1), com um incremento no ano de 2010, mas com resultados bem expressivos com relação ao teor das publicações que relatam diversas atividades biológicas para as substâncias relatadas.
Gráfico 1 - Evolução dos relatos científicos para diterpenos abietanos de Labiatae
dispostos por ordem alfabética da espécie, seguido pelo nome dos compostos encontrados para cada planta, o órgão vegetal utilizado no estudo, a atividade farmacológica relatada e a referência bibliográfica.
Tabela 1 - Diterpenos abietanos - perfil químico-farmacológico de Labiatae
Planta Compostos isolados Fonte Atividade Referência Ajuga decumbens Ajudecumina A (1) Partes aéreas Citotóxica WANG et al, 2012
Ajudecumina B (2) Partes aéreas Citotóxica WANG et al, 2012
Ajudecumina C (3) Partes aéreas Citotóxica WANG et al, 2012
Ajudecumina D (4) Partes aéreas Citotóxica WANG et al, 2012
Ajuforrestina A (5) Partes aéreas Citotóxica WANG et al, 2012
Ajuforrestina B (6) Partes aéreas Citotóxica WANG et al, 2012 Coleus
xanthanthus
11-16-Diacetoxi-coleon U
(9) Partes aéreas -
MEI et al, 2002
11-Acetoxi-coleon U (10) Partes aéreas Citotóxica MEI et al, 2002
16-O-acetil coleon C (7) Partes aéreas - MEI et al, 2002
8a,9a-Epoxicoleon
U-quinona (8) Partes aéreas Citotóxica
MEI et al, 2002
Coleon U (11) Partes aéreas - MEI et al, 2002
Oxo-coleon U (12) Partes aéreas Citotóxica MEI et al, 2002
Xantatusina E (13) Partes aéreas Citotóxica MEI et al, 2002
Xantatusina F (14) Partes aéreas - MEI et al, 2002
Xantatusina G (15) Partes aéreas - MEI et al, 2002
Xantatusina H (16) Partes aéreas Citotóxica MEI et al, 2002
Xantatusina I (17) Partes aéreas - MEI et al, 2002
Xantatusina J (18) Partes aéreas - MEI et al, 2002
Xantatusina K (19) Partes aéreas - MEI et al, 2002 Dracocephalum
komarovi
Dracocephalona A (20) Planta inteira Tripanomicida UCHIYAMA et al,
2003
Fuerstia africana Ferruginol (21) Partes aéreas Antimalárica e
Citotóxica
KOCH et al, 2006
Hyptis carvalhoi 7α-Etoxi-rosmanol (22) Partes aéreas - LIMA et al, 2012
7α-Metoxi-rosmanol (23) Partes aéreas - LIMA et al, 2012
Galdosol (24) Partes aéreas - LIMA et al, 2012 Hyptis martiusii 7α
-Acetoxi-12-hidroxi- 11,14-dioxoabieta-8,12-dieno (25)
Raízes Genotóxica CAVALCANTI et al, 2008
7β -Hidroxi-11,14-dioxoabieta-8, 13-dieno (26)
Raízes Genotóxica CAVALCANTI et al, 2008
Hyptis suaveolens Deidro-abietinol (27) Partes aéreas Antimalárica ZIEGLER et al, 2002 Hyssopus
cuspidatus
19,20-Epoxi-12,19- dimetoxi-11,14,diidroxi-7-oxo-8,11,13-abietatrieno (28)
Planta inteira - FURUKAWA et al,
2011
19,20-Epoxi-12,metoxi- 11,14,19-triidroxi-7-oxo-8,11,13-abietatrieno (29)
Planta inteira Citotóxica FURUKAWA et al, 2011
19,20-epoxi-12-metoxi- 11,14,19-triidroxi-7-oxo-8,11,13-abietatrieno (30)
Tabela 1 – Diterpenos abietanos - perfil químico-farmacológico de Labiatae – cont.
Hyssopus cuspidatus
19,20-Epoxi- 11, 14-diidroxi-12, 20-dimetoxi-7-oxo-8, 11,
13-abietatrieno (31)
Planta inteira Antialérgica FURUKAWA et al, 2011
19,20-Epoxi- 11, 14- diidroxi-12-metoxi-7-20-dioxo-8, 11,
13-abietatrieno (32)
Planta inteira Citotóxica FURUKAWA et al, 2011
Isodon inflexus 3α,6β
-Diidroxi-7,17-dioxo-ent
-abieta-15(16)-eno (34)
Partes aéreas Antiinflamatória LEE et al, 2008
Isodon lophanthoides var. graciliflorus
15-hidroxi-1-oxosalvibretol (35) Partes aéreas Citotóxica
ZHOU et al, 2013
15-hidroxi-20-Desoxi-carnosol (36) Partes aéreas Citotóxica
ZHOU et al, 2013
15-O-Metilgraciliflorina F
(37) Partes aéreas -
ZHOU et al, 2013
16-Acetoxil-sugiol (38) Partes aéreas Citotóxica ZHOU et al, 2013
3α-Hinokiol (39) Partes aéreas Citotóxica ZHOU et al, 2013
3β-Hidroxi-sempervirol
(40) Partes aéreas Citotóxica
ZHOU et al, 2013
6,12,15-Triidroxi- 5,8,11,13-abietatetraen-7-ona (41)
Partes aéreas Citotóxica ZHOU et al, 2013
Abieta-8,11,13-trieno-14,19-diol (42) Partes aéreas Citotóxica
ZHOU et al, 2013
Graciliflorina E (43) Partes aéreas Citotóxica ZHOU et al, 2013
Graciliflorina F(44) Partes aéreas - ZHOU et al, 2013 Isodon
lophanthoids var. micranthus
16-acetoxi-7-α
-hidroxi-royleanona (33) Não informado
- ZHOU et al, 2013
16- Acetoxi-7 α
-metoxi-royleanona (45) Não informado
- ZHOU et al, 2013
Hiptol (46) Não informado
- ZHOU et al, 2013
Micranthina C (47) Não informado
- ZHOU et al, 2013
Isodon rubescens Hebeiabinina A (48) Folhas Citotóxica HUANG et al, 2007
Hebeiabinina B (49) Folhas - HUANG et al, 2007
Hebeiabinina C (50) Folhas - HUANG et al, 2007
Hebeiabinina D (51) Folhas Citotóxica HUANG et al, 2007
Hebeiabinina E (52) Folhas Citotóxica HUANG et al, 2007
Rubescensina I (53) Folhas - HUANG et al, 2007
Rubescensina J (54) Folhas - HUANG et al, 2007
Rubescensina P (55) Folhas - HUANG et al, 2007 Isodon xerophilus Xeropilusins R (56) Folhas -
Xeropilusins S (57) Folhas - NIU, 2004 Leucas cephalotes Leucastrina C(58) Planta inteira - MYIAICHI, 2006 Lycopus
europaeus
Euroabienol (59) Frutos Antibacteriana, antifúngica
RADULOVIC, 2010
Meriandra benghalensis
Cryptotanshinona (60) Não
informado -
RODRÍGUEZ, 2003
17-Hidroxi-cryptotanshinona (61) Não informado -
Peltodon longipes
12-Hidroxi-11- metoxiabieta-8,11,13-trien-7-ona (62)
Raízes Citotóxica FRONZA et al, 2011
7α-Acetoxi-royleanona
(63) Raízes Citotóxica
FRONZA et al, 2011
7α-Etoxi-royleanona (64) Raízes Citotóxica FRONZA et al, 2011
7α-Hidroxi-royleanona
(65) Raízes Citotóxica
FRONZA et al, 2011
7-Oxo-royleanona (66) Raízes Citotóxica FRONZA et al, 2011
Cryptojaponol (67) Raízes Citotóxica FRONZA et al, 2011
Deoxi-neocriptotanshinona (69) Raízes Citotóxica
FRONZA et al, 2011
Iguestol (70) Raízes Citotóxica FRONZA et al, 2011
Inuroileanol (71) Raízes Citotóxica FRONZA et al, 2011
Ortosifonol (72) Raízes Citotóxica FRONZA et al, 2011
Royleanona (73) Raízes Citotóxica FRONZA et al, 2011
Sugiol (74) Raízes Citotóxica FRONZA et al, 2011 Perovskia
abrotanoides
7-Epi-7-O-metilrosmanol
(75) Partes aéreas Citotóxica
AOYAGI et al, 2006
7-O-Metil-rosmanol (76) Partes aéreas Citotóxica AOYAGI et al, 2006
Ácido
11-O-acetil-carnósico (77) Partes aéreas Citotóxica
AOYAGI et al, 2006
Ácido
12-O-metil-carnosico (78) Partes aéreas Citotóxica
AOYAGI et al, 2006
Ácido carnósico (79) Partes aéreas Citotóxica AOYAGI et al, 2006
Carnosol (80) Partes aéreas Citotóxica AOYAGI et al, 2006
Isorosmanol (81) Partes aéreas Citotóxica AOYAGI et al, 2006
Rosmanol (82) Partes aéreas Citotóxica AOYAGI et al, 2006 Perovskia
scrophularifolia
Ácido
12-O-metil-carnosico (78) Partes aéreas -
TAKEDA et al, 2007
Carnosol (80) Partes aéreas - TAKEDA et al, 2007
Epirosmanol (83) Partes aéreas -
Rosmanol (82) Partes aéreas - TAKEDA et al, 2007 Plectranthus aff.
puberulentus
Coleon A (84) Folhas Inseticida, bactericida
WELLSOW et al, 2006
Coleon B (85) Folhas Inseticida, bactericida
WELLSOW et al, 2006
Plectranthus barbatus
Coleon O (68) Folhas ALASBAHI et al,
2010
(+)-Allil-roileanona (86) Folhas ALASBAHI et al, 2010
11-Hidroxi-sugiol (87) Raízes ALASBAHI et al, 2010
14-Deoxi-coleon U (88) Raízes ALASBAHI et al, 2010
20-Desoxi-carnosol (185) Ramos ALASBAHI et al, 2010
3β
-Hidroxi-3-deoxibarbatusina (89) Folhas
ALASBAHI et al, 2010
6,7-Secoabietano I (90) Ramos ALASBAHI et al, 2010
6,7-Secoabietano II (91) Ramos ALASBAHI et al, 2010
Tabela 1 – Diterpenos abietanos - perfil químico-farmacológico de Labiatae – cont.
Plectranthus barbatus
7β
-Acetil-12-deacetoxi-ciclobutatusina (93) Folhas -
ALASBAHI et al, 2010;
ALBUQUERQUE, 2007
Abietatrieno (94) Raízes - ALASBAHI et al, 2010
Barbatusina (95) Folhas Citotóxica ALASBAHI et al, 2010;
ALBUQUERQUE, 2007
Barbatusol (96) Ramos Anti-hipertensiva ALASBAHI et al, 2010
Cariocal (97) Ramos - ALASBAHI et al,
2010
Ciclobutatusina (98) Folhas - ALASBAHI et al, 2010;
ALBUQUERQUE, 2007
Coleon C (99) Planta inteira Citotóxica ALASBAHI et al, 2010
Coleon E (100) Folhas Antiacetilcolines-terásica
FALÉ et al, 2011
Coleon F (101) Folhas - ALASBAHI et al, 2010
Coleon S (102) Folhas - ALASBAHI et al,
2010
Coleon T (103) Folhas - ALASBAHI et al,
2010
Ferruginol (21) Hastes - ALASBAHI et al,
2010
Plectrina (104) Folhas Antialimentar para insetos
ALASBAHI et al, 2010
Plectrinon a (105) Folhas Gastroprotetora ALASBAHI et al, 2010
Plectrinona B(106) Folhas - ALASBAHI et al, 2010
Plectrinone A Folhas Gastroprotetora SCHULTZ et al, 2007
Sugiol (74) Planta inteira - ALASBAHI et al, 2010
Plectranthus bishopianus
6,7-Deidro-royleanona
(107) Partes aéreas -
SYAMASUNDAR et al, 2012
6β,7α
-Diidroxi-royleanona (108) Partes aéreas -
SYAMASUNDAR et al, 2012
6β-Didroxi-7α
-metoxi-royleanona (109) Partes aéreas -
SYAMASUNDAR et al, 2012 Plectranthus
elegans
11-hidroxi-12-oxo-7,9(11),13-abietatrieno (110)
Partes aéreas Antibacteriana DELLAR et al, 1996
7,11-diidroxi-12-metoxi-8,11,13-abietatrieno (111) Partes aéreas Antibacteriana
DELLAR et al, 1996
Plectranthus grandidentatus
14-O-Acetil-coleon U
(112) Partes aéreas -
RIJO et al, 2007
Plectranthus ornatus
Sugiol (74) Partes aéreas - RIJO et al, 2011
Plectranthus porcatus
(13S,15S)-6b,7ª,12ª,19- tetraidroxi-13b,16-ciclo-8-abieteno-11,14-diona (113)
Plectranthus puberulentus
Coleon A lactona (114) Folhas Inseticida, bactericida
WELLSOW et al, 2006
Oxo-coleon U (12) Folhas Inseticida, bactericida
WELLSOW et al, 2006
Coleon U (11) Folhas Inseticida, bactericida,
fungicida
WELLSOW et al, 2006
Rosmarinus officinalis
7-O-Metil-rosmanol (76) Planta inteira Antioxidante MASUDA et al, 2002
Ácido
12-O-metil-carnosico (78) Folhas Antioxidante
DEL BAÑO et al, 2003
Ácido carnósico (79) Planta inteira Antioxidante, Citotóxica Hipolipemiante Antiinflamatória
MUNNÉ-BOSCH et al, 2003; HUANG, et al 2005; POECKEL et al, 2008; IBARRA et al, 2011,
MASUDA et al, 2002
Ácido dioxo-carnósico
(115) Planta inteira Antioxidante
MASUDA et al, 2002
Carnosico 8-lactona (116) Planta inteira Antioxidante MASUDA et al, 2002
Carnosol (80) Folhas Citotóxica; Antioxidante, Antiinflamatória
HUANG et al, 2005; DEL BAÑO et al, 2003; POECKEL et al, 2008;
Rosmanol (82) Planta inteira Antioxidante MASUDA et al, 2002
Seco-hinokiol (117) Folhas - CANTRELL et al, 2005
Salvia aegyptiaca 6-Metilcriptotanshinona
(121) Planta inteira -
YOUSUF et al, 2002
Salvia africana-lutea
Ácido carnósico (79) Partes aéreas Antimicobacterian o, Citotóxica
HUSSEIN et al, 2007
Carnosol (80) Partes aéreas - HUSSEIN et al, 2007
Rosmadial (122) Partes aéreas - HUSSEIN et al, 2007 Salvia
anastomosans
6-Epidemetil-esquirolina
D (123) Raízes -
ESQUIVEL et al, 2005
Arucadiol (124) Raízes - ESQUIVEL et al,
2005
Cariocal (97) Raízes - ESQUIVEL et al,
2005
Deacetilnemorona (125) Raízes - ESQUIVEL et al, 2005
Deacetoxi-nemorona
(126) Raízes -
ESQUIVEL et al, 2005
Royleanona (73) Raízes - ESQUIVEL et al,
2005 Salvia barrelieri
7a-Acetoxi-royleanone-12-metil eter (127) Raízes Antioxidante
KABOUCHE et al, 2007
7-epi-Salviviridinol (128) Raízes Antioxidante KOLAK et al, 2009
7-O-Acetil-horminona
(129) Raízes Antioxidante
KABOUCHE et al, 2007
7-Oxoroyleanona-12-metil
eter (130) Raízes Antioxidante
KABOUCHE et al, 2007
Tabela 1 – Diterpenos abietanos - perfil químico-farmacológico de Labiatae – cont.
Salvia barrelieri Cryptojaponol (67) Raízes Antioxidante KABOUCHE et al, 2007
Demetil-inuroileanol
(132) Raízes Antioxidante
KOLAK et al, 2009
Ferruginol (21) Raízes Antioxidante KOLAK et al, 2009
Horminona (133) Raízes Antioxidante KABOUCHE et al, 2007
Iguestol (70) Raízes Antioxidante KOLAK et al, 2009
Inuroyleanol (134) Raízes Antioxidante KABOUCHE et al, 2007
Royleanona (73) Raízes Antioxidante KABOUCHE et al, 2007
Royleanona-12-metil eter
(135) Raízes Antioxidante
KOLAK et al, 2009
Taxodiona (136) Raízes Antioxidante KOLAK et al, 2009
Viridona (137) Raízes Antioxidante KOLAK et al, 2009 Salvia castanea Castanol A (138) Planta inteira Citotóxica PAN et al, 2012
Castanol B (139) Planta inteira Citotóxica PAN et al, 2012
Castanol C (140) Planta inteira Citotóxica PAN et al, 2012
Castanolideo (141) Planta inteira - PAN et al, 2012
Cryptotanshinona (60) Planta inteira Citotóxica PAN et al, 2012
Danshenspirocetallactona
(142) Planta inteira Citotóxica
PAN et al, 2012
Diidro-tanshinona I (118) Planta inteira Citotóxica PAN et al, 2012 epi-Castanolideo (143) Planta inteira - PAN et al, 2012 epi
-Danshenspirocetallactona (144)
Planta inteira Citotóxica PAN et al, 2012
Ferruginol (21) Planta inteira Citotóxica PAN et al, 2012
Metil-enetanshinquinona
(145) Planta inteira Citotóxica
PAN et al, 2012
Metileno
diidrotanshinquinona (146)
Planta inteira Citotóxica PAN et al, 2012
Metil-tanshinoato (147) Planta inteira Citotóxica PAN et al, 2012
Neo-tanshinlactona (148) Planta inteira Citotóxica PAN et al, 2012
Przewalskina (149) Planta inteira Citotóxica PAN et al, 2012
Salvicanol (150) Planta inteira Citotóxica PAN et al, 2012
Tanshinona I (151) Planta inteira Citotóxica PAN et al, 2012
Tanshinone IIA (152) Planta inteira Citotóxica PAN et al, 2012
Tanshinone IIB (153) Planta inteira Citotóxica PAN et al, 2012 Salvia chionantha 7-O-Acetil-horminona
(154) Partes aéreas -
OZTEKIN et al, 2010
Horminona (133) Partes aéreas - OZTEKIN et al, 2010 Salvia deserta 7-O-Acetil-horminona
(154) Raízes -
TEZUKA et al, 1998
Deidro-royleanona (156) Raízes - TEZUKA et al, 1998
Ferruginol (21) Raízes - TEZUKA et al, 1998
Horminona (133) Raízes - TEZUKA et al, 1998
Metil-horminona (157) Raízes - TEZUKA, 1998
Royleanona (73) Raízes - TEZUKA, 1998
Taxodiona (136) Raízes - TEZUKA, 1998
Salvia digitaloides
Salviatalin A (158) Raízes Antiinflamatória WU et al, 2010
Salvia dorrii 7α-Metoxi-rosmanol(23) Partes aéreas - AHMED et al, 2006
7β-Metoxi-rosmanol(160) Partes aéreas - AHMED et al, 2006
Salvidorol (161) Partes aéreas - AHMED et al, 2006 Salvia eriophora 12-Hidroxisapriparaquinona
(162) Raízes -
ULUBELEN et al, 2002
3,12- Diidroxisapriparaquinona-1-eno (163)
Raízes - ULUBELEN et al,
2002
4,12-Diidroxisapriparaquinona (164)
Raízes Cardioprotetora ULUBELEN et al, 2002
4,14-Diidroxisapriortoquinona (165)
Raízes Cardioprotetora ULUBELEN et al, 2002
6,7-Deidro-royleanona
(107) Raízes Cardioprotetora
ULUBELEN et al, 2002
Aethiopinona (166) Raízes Cardioprotetora ULUBELEN et al, 2002
Ferruginol (21) Raízes Cardioprotetora ULUBELEN et al, 2002
Salvilimbinol (167) Raízes - ULUBELEN et al, 2002
Salvipisona (168) Raízes - ULUBELEN et al, 2002
Salvia hydrangea 6,7-Deidro-royleanona
(107) Raízes -
SAIRAFIANPOUR et al, 2003
7α-Acetoxi-royleanona
(63) Raízes -
SAIRAFIANPOUR et al, 2003
7,8-Dimetil-2-(1-metiletil)
fenantren-3-ol (169) Raízes -
SAIRAFIANPOUR et al, 2003
9,10-Diidro-7,8-dimetil-2-(1-metiletil) fenantren-3-ol (170)
Raízes - SAIRAFIANPOUR
et al, 2003
Salvia hypargeia 14-Deoxi-coleon U (88) Raízes Citotóxica TOPCU et al, 2008
Ácido salvicanarico (171) Raízes - TOPCU et al, 2008
Dideidro-7-hidroxitaxodona (172) Raízes -
TOPCU et al, 2008
Salvia kronenburgii
7-O-Acetil-horminona
(154) Partes aéreas -
OZTEKIN et al, 2010
Horminona (133) Partes aéreas - OZTEKIN et al, 2010 Salvia
milthiorriza
Cryptotanshinona (60) Raízes, Rizoma Hipolipemiante, Citotóxica, Antiosteoporose, Antialérgica, Antidiabética, Hepatoprotetora, Antiamnésica, Citotóxica,
JANG et al, 2012; TRINH et al, 2010; JUNG et al, 2009; MANOLESCU et al, 2009; PARK et al, 2007; KIM et al, 2007;LEE et al, 2005
Ferruginol (21) Raízes - LEE et al, 2005
Tanshinona IIA (152) Raízes Citotóxica, Antialérgica, Cardioprotetora, Neuroprotetora, Antioxidante, Hepatoprotetora
FRONZA et al, 2011; TRINH et al, 2010; ZHU et al, 2010; WANG et al, 2005; LEE et al, 2005; CHOI, 2004; LAM, 2003
Salvia milthiorriza
Isocriptotanshinona(119) Raízes Inibidor de PTP1B (Antidiabética tipo
2)
HAN et al, 2005
Isotanshinona (120) Raízes Inibidor de PTP1B (Antidiabética tipo
2)
HAN et al, 2005
1,2-Diidro-tanshinona
(173) Raízes Citotóxica
FRONZA et al, 2011
15, 16- Diidrotanshinona I
(174) Raízes Antiamnésica, Antidiabética, Antialérgica, Antiosteoporose, Antioxidante, Vasorrelaxante, Hipolipemiante, Citotóxica
JANG et al, 2012;TRINH et al, 2010; JUNG et al, 2009; LAM et al, 2008; KIM et al, 2007; LEE et al, 2005, CHOI et al, 2004
1-Oxo-miltirona (175) Raízes Citotóxica FRONZA et al, 2011
Cripto-tanshinona (176) Raízes Citotóxica, Cardioprotetoraa,
Antioxidante
FRONZA et al, 2011; WANG et al, 2005; CHOI et al, 2004
Danshenspirocetallactona
(177) Raízes Hipolipemiante, Citotóxica
JANG et al, 2012
Diidro-isotanshinona I
(118) Raízes Inibidor de PTP1B
(Antidiabética tipo 2), Citotóxica
MANOLESCU et al, 2009; HAN et al, 2005
Miltiodiol
(178) Raízes Citotóxica
FRONZA et al, 2011
Miltirona (179) Raízes Citotóxica FRONZA et al, 2011
Sibiriquinona A (180) Raízes Citotóxica MANOLESCU et al, 2009
Sibiriquinona B(181) Raízes Citotóxica MANOLESCU et al, 2009
Tanshinona I (151) Raízes Hipolipemiante, Citotóxica, Antialérgica, Cardioprotetora, Antidiabética, Antiosteoporose, Antioxidante, Hepatoprotetora; Antiamnésica
JANG et al, 2012; FRONZA et al, 2011; TRINH et al, 2010; PARK et al, JUNG et al, 2009; KIM et al, 2007; WANG et al, 2005; LEE et al, 2005; CHOI et al, 2004
TanshinonaVI (182) Raízes Cardioprotetora ARINO et al, 2008 Salvia montbretii 14-Deoxi-coleon U (88) Não
informado
- RODRÍGUEZ, 2003
Salvia nipponica var. formosana
Taxodiona (136) Raízes e folhas
Anticolinesterá-sica
CHAN et al, 2011
Salvia officinalis 7-O-Metil-rosmanol (76) Planta inteira Antioxidante MASUDA et al, 2002
Ácido
12-O-metil-carnosico (78) Hastes e folhas Antidiabética
CHRISTENSEN et al, 2010
Ácido 12-O-metil-carnosico-epirosmanol ester (183)
Hastes e folhas
Ácido carnósico (79) Planta inteira Antioxidante, Hipolipemiante
CHRISTENSEN et al, 2010;
NINOMIYA et al, 2004; MUNNÉ-BOSCH et al, 2003
Ácido dioxo-carnósico
(115) Planta inteira Antioxidante
MASUDA et al, 2002
Carnosico8-lactona (116) Planta inteira Antioxidante MASUDA et al, 2002
Rosmanol (82) Planta inteira Antioxidante MASUDA et al, 2002
11,12,20-Triidroxi-abieta-8,11,13-trieno (184) Hastes e folhas -
CHRISTENSEN et al, 2010
20-Desoxi-carnosol (185) Hastes e folhas
- CHRISTENSEN et al, 2010
20-HidroxiFerruginol
(186) Hastes e folhas -
CHRISTENSEN et al, 2010
Carnosol (80) Hastes e folhas
- CHRISTENSEN et al, 2010
Salvia phlomoides 14-Deoxi-coleon U (88) Não
informado
- RODRÍGUEZ, 2003
Cryptojaponol (67) Não
informado -
RODRÍGUEZ, 2003
Royleanona (73) Não informado
- RODRÍGUEZ, 2003
Sugiol (74) Não
informado -
RODRÍGUEZ, 2003
Taxodiona (136) Não informado
- RODRÍGUEZ, 2003
Taxodona (187) Não
informado -
RODRÍGUEZ, 2003
Salvia prionitis Bisprioterona A (188) Raízes - XU et al, 2006
Bisprioterona B (189 Raízes - XU et l, 2006
Bisprioterona C (190) Raízes - XU et al, 2006
Prionoid A (191 Raízes - CHANG et al, 2005
Prionoid B (192) Raízes - CHANG et al, 2005
Prionoid C (193) Raízes - CHANG et al, 2005
Prionoid D (194) Raízes Citotóxica CHANG et al, 2005
Prionoid E (195) Raízes Citotóxica CHANG et al, 2005
Prionoid F (196) Raízes - CHANG et al, 2005 Salvia sahendica Ferruginol (21) Raízes Citotóxica FRONZA et al, 2011
Sahandinona (197) Raízes Citotóxica FRONZA et al, 2011 Salvia sclarea 1-Oxoaethiopinona (198) Raízes Antibiótica KUZMA et al, 2007
Aethiopinona (199) Raízes Antibiótica KUZMA et al, 2007
Ferruginol (21) Raízes Antibiótica KUZMA et al, 2007
Salvipisona (168) Raízes Antibiótica KUZMA et al, 2007 Salvia semiatrata 20-Nor-inuroyleanol (200) Raízes - ESQUIVEL et al,
2005
Horminona (133) Raízes - ESQUIVEL et al,
2005
Salvifolanona (201) Raízes Citotóxica ESQUIVEL et al, 2005
Salvia silicia 12-Deoxi-royleanona
(202) Raízes Leishmanicida
TAN et al, 2002
Tabela 1 – Diterpenos abietanos - perfil químico-farmacológico de Labiatae – cont.
Salvia silicia Cryptanol (204) Raízes - TAN et al, 2002
7-Hidroxi-12-metoxi-20-nor- abieta-1,5(10),7,9,12-pentaen-6,14-diona (203)
Raízes - TAN et al, 2002
Inuroyleanol (134) Raízes - TAN et al, 2002 Salvia
yunnanensis
Salviamine A (205) Raízes - LIN et al, 2006
Salviamine B (206) Raízes - LIN et al, 2006
Salviamine C (207) Raízes - LIN et al, 2006
Salviamine D (208) Raízes - LIN et al, 2006 Sideritis
canariensis
Deidro-abietano (209) - - GIANNONI et
al, 2010
Sideritis discolor Deidro-abietano (209) - - GIANNONI et al, 2010
Sideritis lotsyi Deidro-abietano (209) - - GIANNONIet
al, 2010 Sideritis
massoniana
Deidro-abietano (209) - - GIANNONI et
al, 2010
Sideritis soluta Deidro-abietano (209) - - GIANNONI et
al, 2010 Teucrium
fruticans
Teuvincenona E (210) Raízes - RODRÍGUEZ, 2002;CUADRA DO et al, 1992
Teuvincenona F (211) Raízes - CUADRADO et al, 1992
Teuvincenona G (212) Raízes - CUADRADO et al, 1992 Teucrium
lanigerum
Teuvincenona A (213) Raizes - RODRÍGUEZ et al, 2009
Teucrium lanigerum
Teuvincenona B (214) Raízes - RODRÍGUEZ et al, 2009
Teuvincenona C (215) Raízes - RODRÍGUEZ et al, 2009
Teuvincenona D (216) Raízes - RODRÍGUEZ et al, 2009
Teuvincenona J (217) Raízes - RODRÍGUEZ et al, 2009 Teucrium polium
12,16-Epoxi-6,11,14,15-tetraidroxi-17(15→ 16)-abeo- 3a,18-ciclo-5,8,11,13-abietatetraen-7-ona (218)
Raízes Antioxidante FIORENTINO et al, 2010
12,16-Epoxi-6,11,14,15-tetraidroxi-17(15→ 16)-abeo-5,8,11,13-abietatetraen-7-ona (219)
Raízes Antioxidante FIORENTINO et al, 2010
12,16-Epoxi-6,11,14,17-tetraidroxi-17(15→ 16)-abeo- 3a,18-ciclo-5,8,11,13,15-abietapentaen-7-ona (220)
Raízes Antioxidante FIORENTINO et al, 2010
12,16-epoxi-6,11,14,17-tetraidroxi-17(15→ 16)-abeo- 5,8,11,13,15-abietapentaen-7-ona (221)
Raízes Antioxidante FIORENTINO et al, 2010
12,16-epoxi-6,11,14-triidroxi-17(15→ 16)-abeo- 3a,18-ciclo-5,8,11,13,15-abietapentaen-7-ona (222)
Teucrium polium
12,16-Epoxi-6,11,14-triidroxi-17(15→
16)-abeo- 5,8,11,13,15-abietapentaen-7-ona (223)
Raízes Antioxidante FIORENTINO et al, 2010
Deidro-hidroxi-teuvincenona
A (224) Raízes Antioxidante
FIORENTINO et al, 2010
Diidro-hidroxi-teuvincenona
J (225) Raízes Antioxidante
FIORENTINO et al, 2010
Teuvincenona A (213) Raízes Antioxidante FIORENTINO et al, 2010
Teuvincenona B (214) Raízes Antioxidante FIORENTINO et al, 2010
Teuvincenona C (215) Raízes Antioxidante FIORENTINO et al, 2010
Teuvincenona D (216) Raízes Antioxidante FIORENTINO et al, 2010
Villosin C (226) Raízes Antioxidante FIORENTINO et al, 2010
Teuvincenona A 11,14-diona
(227) Raízes -
RODRÍGUEZ, 2002
Teuvincenona D (216) Raízes - RODRÍGUEZ, 2002
Teucrium polium subsp. expansum
Ferruginol (21) Raízes - CUADRADO et
al, 1992
Teuvincenona A (213) Raízes - CUADRADO et al, 1992
Teuvincenona B (214) Raízes - CUADRADO et al, 1992
Teuvincenona H (228) Raízes - CUADRADO et al, 1992
Teuvincenona I (229) Raízes - CUADRADO et al, 1992 Teucrium polium
subsp. uincentinum
Di-deidroxi-dioxo-teuvincenona A(230) Derivado -
CUADRADO et al, 1992
Teuvincenona A (213) Raízes - CUADRADO et al, 1992
Teuvincenona B (214) Raízes - CUADRADO et al, 1992
Figura 5 - Representação estrutural dos esqueletos abietanos
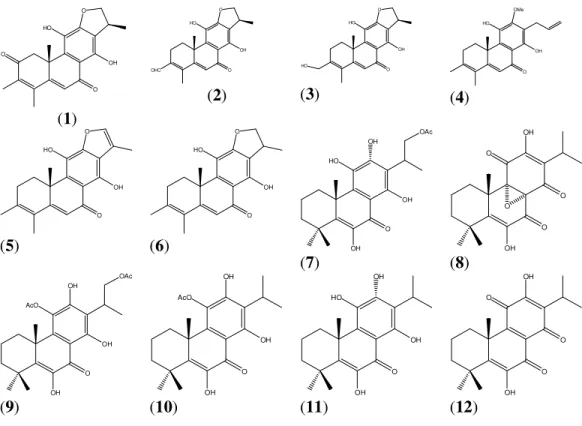
Tabela 2 - Representação estrutural dos diterpenos abietanos identificados em Labiatae nos últimos 40 anos (numeração referente à Tabela 1)
O O O OH HO (1) O OHC O OH HO (2) O O OH HO HO (3) OMe O OH HO (4) O OH HO O (5) O OH HO O
(6) OH
OH OH HO
O OAc
(7) OH
O OH O O O (8) O OH OH OH AcO OAc (9) O OH OH OH AcO
(10) OH
OH OH
HO
O
(11) OH
O OH
O
O
Labiatae nos últimos 40 anos – cont. O O OH O COOH (13) O OH OH OH AcO AcO OH (14) O OH OH OH AcO AcO O (15) O OH O OH O OAc (16) O OH O OAc O AcO
(17) O
O OAc
O
AcO
OH
(18) O
O OAc O OH (19) OMe HO OH O H O (20) H OH H
(21) (22)
HO OH H OH H O O OMe (23) H O O O HO OH (24) H O O O HO OH (24) O O OAc H (25) O O OH H
(26) CH2OH
H (27) HO OH OCH3 O O H3CO (28) HO OH OCH3 O O HO (29) HO OCH3 O OH O HO (30) HO OCH3 O OH O
H3CO
(31) HO OH OCH3 O O O (32) O O H OH OH CH2OAc
Tabela 2 - Representação estrutural dos diterpenos abietanos identificados em Labiatae nos últimos 40 anos – cont.
HO OH OH O H (36) O OH OMe OH O O
(37) H
O OH O O (38) HO H (39) H OH (40) OH O OH OH (41') H HO OH (42) O OH OCH3 OH (43) O OH OH OH O O (44) O O H OMe OH CH2OAc
(45) O OH HO O H (46) O H OH HO H O O (47) CHO CHO OH H OH O H (48) H OH OH OH H HO HO
(49) OHC
H H HO O (50) H H HO OH OH OH O H OH OH OH O H O OH (51) H H HO O H OH OH OH O H O OH O (52) HO HO H H OH OH (53) HO HO H H O (54) HO HO H H OH OH (55) CHO OH O H O O (56) CHO OH O H O O
CH2OH
nos últimos 40 anos – cont.
(60) (61)
O OH O (62) O O OH O O (63) O O OH O (64) O O OH OH (65) O O OH O (66) O O HO (67) O OH H OAc OH H O (68) O OH OH O (69) HO O OH (70) HO O O OH (71) OH O O OH (72) O O OH (73) OH O (74) HO OH H O O OMe (75) HO OH H O O OMe (76) AcO COOH OH H (77) HO COOH OMe (78) HO COOH OH (79) HO OH H O O (80) HO OH H O O OH (81) HO OH H O O OH (82) O HO OH O OH (83) O CH3 O O
H3C CH3
O OH O O
Tabela 2 - Representação estrutural dos diterpenos abietanos identificados em Labiatae nos últimos 40 anos – cont.
O H HO OH O O OH (84) O HO H OH O O OH (85) O OH H OH OAc O O (86) O HO OH (87) HO OH O OH (88) O OAc H OH OAc O HO (89) O OHC OH OH H (90) O OHC OH OH H (91) OH H O OH O HO (92) HO OH H OAc OAc O O H H (93) (94) O OAc H OH OAc O O (95) OH HO H (96) O OH OH H O OH CHO OH (97) HO OAc H OH OAc O O H OH (98) HO OH O OH OH OH (99) O OH O HO OH (100) HO O OH O (101) O OH H OH OH H O OEt (102) O OH H OH OH H O (103) O OH H OH OAc O O (104) HO OH OH O O OH H (105) HO OH OH O O
(106) H
O O OH (107) H O O OH OH OH (108) H OH OMe O O OH
(109) (110) (111)
CH3 CH3 HO
H3C CH3 O CH3 CH3 OH HO O CH3
nos últimos 40 anos – cont. OH O HO OH OAc (112) O O OH CH2 H OH OH HO H (113) O OH O O OH O (114) COOH O O (115) O O HO O (116) HOOC H OH (117) O O O (119) O O O (120) O O O (121) CHO CHO O O OH (122) OH HO HO OH H O (123) OH HO O (124) OH O O OH O H (125) OH O O O H (126) O O OCOCH3 OMe (127) OCH3 HO OH OH (128) O O OCOCH3 OH (129) O O O OMe (130) O O HO OH (131) OH HO OH O (132) O OH H OH O (133) (134) OMe O O (135) HO O H H O (136) CH3 CH3 OH O HO CH3
H3C CH3 O