Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
Artigo Original (Química)
Solange Aparecida Camargo Pivotto
Licenciada em Química pela Faculdade de Educação e Meio Ambiente. E-mail: solangecamargo28@hotmail.com.
Bruno de Oliveira Poletto
Licenciado em Química pela Faculdade de Educação e Meio Ambiente (FAEMA). E-mail: bruno-opoletto@hotmail.com.
Filomena Maria Minetto Brondani
Professora do curso de Licenciatura em Química da FAEMA e Diretora do Instituto Superior de Educação - ISE/FAEMA. E-mail: filomenabrondani@yahoo.com.br.
Andressa dos Santos Cruz
Graduada em Biomedicina da Faculdade São Paulo - Rolim de Moura/RO. E-mail: andressasantos752@gmail.com.
Jhonattas Muniz de Souza
Mestre em Engenharia de Processos e Tecnologia. Prof. da Fundação Universidade Federal de Rondônia (UNIR). E-mail: Muniz_jhonattas@hotmail.com.
Resumo:
O presente trabalho tem por objetivo, analisar a concentração de cálcio, magnésio, Poder de Neutralização, Reatividade e Poder Relativo de Neutralização Total em calcário da região Norte. Foram determinados os teores totais de óxidos de cálcio (CaO) e magnésio (MgO) por volumetria utilizando o EDTA (ácido etilenodiaminotetracético) como agente complexante, solução tampão em pH = 10, e como indicador complexométrico, o corante orgânico Negro de eriocromo T. As análises foram realizadas em dez amostras de calcários, em que cada amostra corresponde a jazidas distintas. As amostras encontram-se dentro dos parâmetros que as classificam como calcário. Na classificação pelo teor de MgO, constatou-se que, das dez amostras analisadas, todas podem ser classificadas como calcário dolomítico, além de apresentar as quantidades mínimas de PRNT admitidas pela legislação.Palavras-chave:
Calcário, Carbonatos, Poder Relativo.CARACTERÍSTICAS FÍSICAS, QUÍMICAS E
FÍSICO-QUÍMICAS DE CALCÁRIO EXTRAIDO DO
SULDOESTE DA REGIÃO AMAZÔNICA
PHYSICAL, CHEMICAL AND PHYSICAL-CHEMICAL
CHARACTERISTICS OF LIMESTONE EXTRACTED
FROM SOUTHWEST OF THE AMAZON REGION
10.31072/rcf.v10i2.813Submetido:
03 jun. 2019.
Aprovado:
02 dez. 2019.Publicado:
29 maio. 2020.solangecamargo28@hotmail.com:
Este é um artigo de acesso aberto e distribuído sob os Termos da
Creative Commons Attribution License. A licença permite o
uso, a distribuição e a reprodução irrestrita, em qualquer meio, desde que creditado as fontes originais.
Imagem: StockPhotos (Todos os direitos reservados).
Open Access
1
95
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
Abstract:
The present work aims to analyze the concentration of calcium, magnesium, Power of Neutralization, Reactivity and Relative Power of Total Neutralization in limestone of the northern region. Total calcium oxide (CaO) and magnesium (MgO) contents were determined by volume using EDTA (ethylenediaminetetraacetic acid) as a complexing agent, buffer solution at pH = 10, and as a complexometric indicator, the erythromic black organic dye T. The analyzes were performed in ten limestone samples, where each sample corresponds to distinct deposits. The samples are within the parameters that classify them as limestone. In the classification by MgO content, it was found that, of the ten samples analyzed, all can be classified as dolomitic limestone, besides presenting the minimum amounts of PRNT allowed by the legislation.Keywords
: Limestone, Carbonates, Relative Power.Introdução
Rochas carbonatadas ou calcário é a denominação de minerais constituído em maior percentual de a calcita (CaCO3) e/ou a dolomita (CaCO3.MgCO3), contendo outros carbonatos como os de magnésio, ferro, manganês e mais raramente de zinco e bário (1,2). A formação dos calcários magnesianos e dolomíticos ocorreram pela substituição do cálcio pelo magnésio, vindo de águas com elevado teor de magnésio. Entretanto, vários depósitos de dolomita baseiam ter origem na co-precipitação de ambos os carbonatos e na substituição dos metais (3,4).
Atualmente existe diversas aplicações industriais para o calcário, como exemplo ser utilizado na produção de diversos produtos como papel, tintas, plásticos, cerâmicas, metalúrgica, vidros e alimentação de animais, purificação da água e amplamente aplicação no processo de calagem (5). O principal consumo da produção de calcário brasileiro, em meados de 2014, foi na fabricação de cimento que representou 43,94% da produção beneficiada e 64% da produção bruta.
O consumo da calcita em uso agrícola foi de 1,22% enquanto que o dolomito 31,5% da produção bruta (6, 7).A produção brasileira entre os anos de 2010 a 2014 teve o maior índice em 2014, produzindo aproximadamente 1137000 t de calcário calcíta e a produção de calcário dolomítico 6172000 t no mesmo ano, uma queda de 15,4% se comparado ao ano de 2013 (7).
Os estados que se destacaram na produção de calcário são MG, MS, PR e GO que representam juntos aproximadamente 60% da produção brasileira. Conforme apresentado, Rondônia, estado onde foi extraído o calcário para análise deste artigo, não se destaca na produção de calcário, possui uma usina de extração e processamento. Em contrapartida, o estado está em grande desenvolvimento nas áreas de agricultura e pecuária. São áreas que necessitam de consumo de calcário para correção dos solos através do processo denominado calagem.
A calagem, consiste na aplicação de calcário a acidez do a partir da reação de neutralização. Para a efetiva reação de neutralização ou poder de neutralização (PN) é importante, além dos teores de CaO e MgO, analisar a granulometria das partículas, pois influenciam diretamente na reatividade (RE). O PN do carbonato de cálcio vem a ser a conversão equivalente de CaO e MgO em CaCO3. Como base, considera-se o PN de CaCO3 sendo 100%. Assim, os respectivos PN equivalentes de CaO e MgO são de 1,7884 e 2,48 vezes maior se comparado ao PN do CaCO3(8).
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
O processo de calagem se faz necessária pois, sabe-se que a acidez do solo tende a aumentar gradativamente considerando o efeito das chuvas ácidas geradas a partir de óxidos ácidos (9). Assim, havendo a demanda cada vez maior na extração e processamento do calcário dolomítico para o consumo agrícola (8).
Considerando que a aplicação do calcário na agricultura está relacionada às características dele, evidencia-se aqui a importância de analisar as propriedades químicas, físicas e físico-químicas. Assim, o objetivo deste trabalho é determinar o Poder de Neutralização (PN) do Oxido de Cálcio (CaO), Oxido de Magnésio (MgO), o Poder Relativo de Neutralização Total (PRNT) e a Granulometria do Calcário extraído no sudoeste amazônico.
Material e Métodos
As análises foram realizadas de acordo com as metodologias do “Manual de métodos analíticos oficiais para fertilizantes e corretivos”, do Ministério da agricultura pecuária e abastecimento – MAPA (10).
A extração das amostras foi realizada no município de Parecis, distante aproximadamente 564 km da capital Porto Velho, estado de Rondônia. No município há a Usina de Calcário César Cassol, localizada na linha 70, lote 31, na qual disponibilizou as amostras. Parecis, cuja altitude é 292 metros, está localizada nas seguintes coordenadas geográficas: latitude: 12° 10' 31'' Sul, longitude: 61° 36' 13'' Oeste (11).
Foram analisadas dez amostras de duas jazidas distintas. As amostras numeradas de 1 a 5 são para uma jazida e amostras numeradas de 6 a 10 são para outra jazida. A Figura 1 apresenta o minério na sua forma bruta, recém extraído das jazidas e a Figura 2 apresenta a característica física da amostra após o processo de trituração.
Figura 1. Calcário em rocha. Figura 2. Amostra triturada.
Fonte: Elaborado pelos autores.
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
Granulometria
Pesou-se 100 gramas de calcário em um Becker que foi transferido para as peneiras de n° 50 (ABNT) que corresponde valor < 0,30mm, n° 20 (ABNT) que corresponde de 0,84mm a 0,30mm e n° 10 (ABNT) que equivale 2mm a 0,84mm. Posteriormente foram agitadas aproximadamente por 5 minutos, depois pesou-se cada resultado e realizou-se os cálculos das frações retida em cada peneiro.
Onde:
A % da amostra passante na peneira > 0.30 mm (ABNT 50) =100-(R1 + R2 + R3) x 100/Gr
A % da amostra passante na peneira 0.84 mm (ABNT 20)=100-(R1 + R2) x 100/Gr
A % da amostra passante na peneira 2 mm (ABNT 10)=100-(R1) x 100/Gr G= massa da amostra analisada
R1= massa retida da peneira 2 mm (ABNT 10) R2= massa retida da peneira de 0.84 mm (ABNT 20) R3= massa retida da peneira > 0.30 mm (ABNT 50)
Determinações do poder de neutralização PN
Secou-se a amostra de calcário em estufa até massa constante, depois a triturou e posteriormente pesou-se exatamente 1,0 g de calcário já seca em estufa até massa constate seca, moída e peneirada (0,3 mm) e transferir para erlenmeyer de 125 mL. Adicionar à amostra 50 mL de ácido clorídrico 0,5 mol.L-1, tampar com um vidro relógio e aquecer a 110 ºC por 2 min e homogeneizar. Retirar da fonte de calor, deixar esfriar a temperatura ambiente. Transferir para um balão volumétrico de 100 mL e completar com água destilada até o menisco.
Realizar a filtragem com um papel filtro que apresenta porosidade média de 3 micras e 12,5 cm. Utilizar o filtrado para análise do PN, do óxido de cálcio e do óxido de magnésio.
Com auxílio de uma pipeta, retirou 50,0 mL do filtrado, transferiu para um erlenmeyer de 125 mL, acrescentou de 2 a 3 gotas de indicador fenolftaleína e procedeu a titulação com NaOH 0,25 mol.L-1. O volume consumido foi denominado de V2. Para a determinação do PN procedeu-se a seguinte Equação 1:
Eq. 1 - Determinação do PN
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
Onde:
M1= concentração do HCl, em mol.L-1 M2= concentração do NaOH, em mol.L-1
V2= refere-se ao volume utilizado de hidróxido de sódio (NaOH), em mL durante a titulação.
G= refere-se à massa inicial da amostra, mencionada em gramas.
DeterminaçãO CaO
Preparou-se uma solução contendo hidróxido de potássio com cianeto de potássio dissolvendo 140,0 g de KOH e 1,0 g de KCN em 500 mL de água destilada.
Como indicador, foi preparado uma solução denominada Calcon (ácido calconcarbônico): transferindo 0,10 g de calcon para um béquer de 100 mL, mais 10 mL de trietanolamina além de 10 mL de álcool metílico e homogeneizou-se até dissolver por completo. Transferir a solução para um frasco plástico e manter refrigerado a aproximadamente 4,2 ºC. Na titulação, evidencia-se a mudança de cor do vermelho claro para violeta intenso.
O preparo da solução de EDTA foi iniciado secando-o, primeiramente, em estufa a 75 ºC durante 2 horas, em sequência foi preparado uma solução a 0,020 mol.L-1.
Para a titulação complexométrica com EDTA, foi utilizado o extrato armazenado da análise do PN. Assim, foi transferido 5,0 mL do filtrado para um erlenmeyer com capacidade de 125 mL, além de 5,0 mL da solução KOH-KCN seguido da adição de 6 gotas do indicador calcon e procedeu a titulação. Foi desenvolvido também um teste em branco com água deionizada no lugar da amostra, anotando a quantidade utilizada de EDTA (V2). Os cálculos foram realizados conforme Equação 2.
Eq. 2 - Quantificação do percentual do CaO Cálculo
Onde:
V1 - é o volume, em mL, da solução EDTA utilizado na titulação.
V2 - é volume consumido, em mL, da solução EDTA, durante a titulação do teste em branco.
G – Representa a massa, em gramas, da amostra inicial. M – Concentração do EDTA, em mol/L.
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
Determinação MgO
Em um frasco erlenmeyer de 125 mL foi transferido 5 mL do extrato, seguido da adição de 50 mL de água destilada, juntamente com a adição de 5 mL de solução tampão com pH 10 e adição de 10 gotas do indicador eriocromo T. Na sequência, após a homogeneização, foi titulado com solução 0,20 mol.L-1 padronizada. Para os respectivos cálculos, anotou-se o volume consumido de EDTA (V3). Realizar uma prova em branco, sem o extrato, desenvolvendo os mesmos procedimentos e anotar o volume de EDTA consumido (V4).
O cálculo para o percentual de MgO desenvolveu-se conforme apresentado na Equação 3.
Eq. 3 - Quantificação do percentual de MgO.
Onde:
V1= Volume (mL) da solução EDTA padronizada utilizadona titulação do cálcio V2= Volume (mL) da solução EDTA padronizada utilizadona titulação da prova branco do cálcio.
V3= Volume consumido, em mL, da solução de EDTA utilizado da titulação com extrato contendo Ca2+ e Mg2+.
V4= Volume, em mL, da solução de EDTA consumido na titulação da prova em branco.
G = representa a massa inicial (g) da amostra.
O cálculo da Reatividade nos Corretivos segue: RE= 0,2 (P1 – P2) +0,6 (P2 – P3) +P3 obtidos na análise granulométrica, em que P1, P2, P3 são os valores percentuais das frações que passaram nas peneiras, com os respectivos números na ABNT 10, 20 e 50. A Equação 4 refere-se à determinação do Poder Relativo de Neutralização Total.
Eq. 4 – Fórmula para quantificação do PRNT
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
Resultados e discussão
As principais análises que permitem quantificar a concentração de calcário são: a soma dos teores de CaO e MgO, em uma concentração mínima de 38% e o PRNT. A qualidade do calcário está relacionada aos altos teores de CaO ou de MgO e que se solubilize no solo, e que essa solubilidade está relacionada ao PRNT em que quanto maior o PRNT será melhor a qualidade do calcário (12).
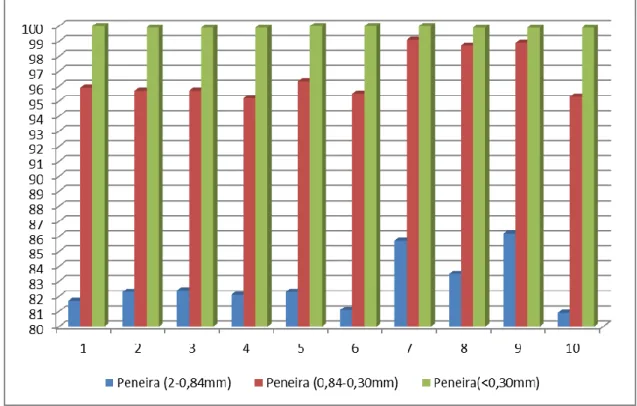
O Poder Relativo de Neutralização Total – PRNT que calcula a eficiência de calcários para corretivos agrícolas, é estabelecido em relação ao PN e RE. A reatividade é calculada a partir da granulometria do corretivo. Reatividade zero para a fração retida na peneira ABNT n.º 10; reatividade 20% para a fração que passa na peneira ABNT n.º 10 e fica retida na peneira ABNT n.º 20; reatividade 60% para a fração que passa na peneira ABNT n.º 20 e fica retida na peneira ABNT n.º 50; e reatividade 100% para a fração que passa na peneira ABNT n.º 50.
As análises granulométricas das dez amostras foram realizadas nas peneiras de 2-0,84mm, 0,84-0,30mm e menor que 0,30mm. Os resultados estão apresentados no gráfico 1.
Gráfico 1. Resultados percentuais da granulometria nas 10 amostras analisadas.
Fonte: Elaborado pelos autores.
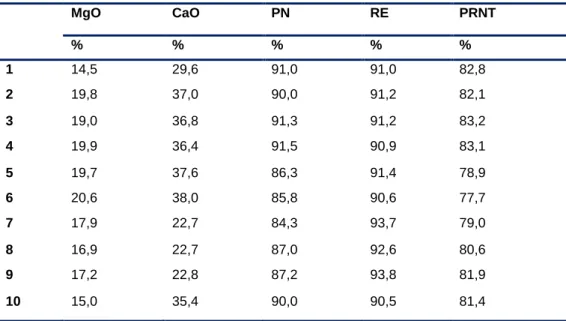
A Tabela 1 apresenta os resultados das análises químicas em cada amostra de calcário, possibilitando o entendimento dos teores de Ca e Mg, PN, RE e PRNT do calcário analisado.
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
Tabela 1 - Resultados das análises químicas, físico-químicas do calcário.
Fonte: Elaborado pelos autores.
A concentração de MgO encontra-se acima de 12%, caracterizando-o como dolomítico. Demais classificações são os calcíticos e magnesiano quando apresentado menos 5% de óxido de magnésio MgO e de 5% a 12% de MgO respectivamente.
As características químicas do Calcário dolomítico constam variações de 35 a 38% de óxido de cálcio, 12 a 15% de MgO, 98 a 102% é a variação do PN e 85% a 90% é a variação do PRNT.
Conforme consta no Ministério da Agricultura, Pecuária e Abastecimento (MAPA) é estabelecido quatro variações percentuais do PRNT para classificação e fins comerciais do calcário, a saber: faixa A o PRNT varia de 45 a 60%, faixa B entre 60,1% a 75%, faixa C de 75,1% a 90% e faixa D quando apresentado PRNT acima de 90%.
As impurezas dos calcários afetam em sua reatividade e consequentemente na qualidade, variando muito em tipo e quantidade, precisando ser examinadas em vista ao aspecto econômico, além da verificação se tais impurezas afetam a utilidade da rocha. Estas impurezas acompanham o processo de deposição do CaCO3 ou ocorreram em estágios posteriores à deposição.
O calcário com pouco PRNT e que não atende a determinadas especificações é redirecionado e aproveitado em outros fins, como exemplo, utilizado na construção
MgO CaO PN RE PRNT % % % % % 1 14,5 29,6 91,0 91,0 82,8 2 19,8 37,0 90,0 91,2 82,1 3 19,0 36,8 91,3 91,2 83,2 4 19,9 36,4 91,5 90,9 83,1 5 19,7 37,6 86,3 91,4 78,9 6 20,6 38,0 85,8 90,6 77,7 7 17,9 22,7 84,3 93,7 79,0 8 16,9 22,7 87,0 92,6 80,6 9 17,2 22,8 87,2 93,8 81,9 10 15,0 35,4 90,0 90,5 81,4
102
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
civil como agregados em massas. Desta forma, mesmo sendo um calcário de baixa qualidade na utilização do solo o mesmo tem saída comercial, uma vez que pode ser utilizado na produção de cimento (2).
No Brasil, toda classificação para calcários agrícolas é baseada na Instrução Normativa SDA/ nº 35, de 04 de julho de 2006. Na qual, define o calcário calcítico com fórmula molecular CaCO3, calcário magnesiano e dolomítico com a fórmula molecular CaMg (CO3)2. Esses calcários são comumente explorados a partir de minerações a céu aberto. A qualidade depende dos níveis de impurezas, sendo a argila uma das impurezas que se destaca. Seu poder de neutralização (equivalente em CaCO3) usualmente varia de 65% a 70%.
Entretanto, sabe-se que solos com pH ácido diminui a eficiência das bactérias nitrificadoras e fixadoras de nitrogênio, reduzindo assim a disponibilidade de nitrogênio. Além disso, plantas como as leguminosas são uma das mais afetadas com o aumento da acidez, pois diminui a capacidade de manter as reservas de nutrientes (13).
No conceito de ácidos, há a aceitação de teorias que evidenciam como sendo substâncias capazes de doar próton, sendo o mais comum a se apresentar é o H+. Entretanto, íons metálicos, como o Al3+ também apresentam características ácidas por enquadrar dentro do conceito de Lewis sobre ácidos, definido como substâncias capazes de receber par de elétrons (14). Os cátions Al3+ favorecem a elevação do pH do solo conforme descrito na equação química a seguir (15,16, 17, 18).
Eq. 5:
Al3+ + 3H
2O → Al(OH)3 + 3H+
Ademais, outro fator que ocasiona a elevação da acidez no solo, ocorre por meio da adubação com fertilizantes amoniacais e a ureia conforme as equações químicas 2 e 3, resultando em H+ e NH 4+(aq)(7). Eq. 6: 2NH4+ + 3O2 → 2NO2- + 2H2O + 4H+ Eq. 7: CO(NH2)2 + 2H2O → (NH4)2CO3
103
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
Os solos ácidos são inviáveis no desenvolvimento de plantas e produção de grãos. Assim, uma medida para neutralizar a acidez do solo é a utilização de óxidos básicos como os que são amplamente utilizados, o óxido de magnésio MgO e o óxido de cálcio (CaO), produzidos a partir da decomposição do CaCO3 e MgCO3, que são constituintes do calcário (7). As reações ocorrem quando o CaO se dissolve na água produzindo assim uma base, o hidróxido de cálcio Ca(OH)2, que por seguinte, neutraliza a acidez dos solo neutralizando o pH (19).
Braga(8) menciona que o equivalente PN do CaCO
3 está diretamente relacionado ao teor e a reatividade (RE) de CaO e MgO, é possível calcular com base na Equação 4.
Eq. 8. PN de CaCO3 X% de CaO x 1,7884 = C
Y% de MgO x 2,4800 = D
Onde X e Y representam os respectivos teores de cálcio e magnésio apresentados na amostra do minério. Desta maneira, o PN do calcário é a soma dos valores percentuais C e D.
Considerando o efeito direto do PRNT na correção da acidez de um determinado solo, assim usa-se menor percentual de calcário a medida em que o PRNT apresente valores maiores, conforme a necessidade de aplicação e correção. (20).
Conclusões
As características mais importantes do calcário são os teores de cálcio e magnésio, expressos respectivamente em percentagens CaO (óxido de cálcio) e MgO (óxido de magnésio), PN e RE do material, que depende principalmente da sua granulométria. O PN, juntamente com a reatividade do corretivo define o PRNT que é o índice muito utilizado na escolha de calcário.
Pode-se concluir que o calcário analisado classifica como dolomítico com uma concentração acima de 12% de MgO e com isso podendo ter significativo uso industrial destinado a áreas agrícolas para o processo de calagem e correção de solos.
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
Referências
1. Luz AB, Lins FAF (ed). Rochas & Minerais Industriais: usos e especificações. 2 ed. Rio de Janeiro: CETEM/MCT, 2008. 990p.
2. Sampaio JA, Almeida SLM. CT2005-132-00: Calcário e Dolomito. Cap. 15. 2005.
[Citado em 2018 setembro 20]. Disponível em
http://www.cetem.gov.br/publicacao/CTs/CT2005-132-00.pdf.
3. Guimarães JEP. A Cal: Fundamentos e aplicações na engenharia civil. 2 ed. São Paulo: Pini; 2002.
4. Šiler P, Kolářová I, Bednárek J, Janča M, Musil P, Opravil T. The possibilities of analysis of limestone chemical composition. IOP Conf. Series: Materials Science and Engineering. 2018;379(1)012033. [Citado em 2019 março 17]. Disponível em: https://iopscience.iop.org/article/10.1088/1757-899X/379/1/012033/pdf.
5. Sampaio JA, Almeida SL. Calcário e Dolomito. Centro de Tecnologia Mineral (CETEM), 2011. [Citado em 24 de Setembro de 2018]. Disponível em: http://www.cetem.gov.br/agrominerais/livros/16-agrominerais-calcariodolomito.pdf 6. Ambrosio A. Perfil analítico do cimento, Boletim nº 30, DNPM, Rio de Janeiro – RJ, 1974.
7. D’Avila AE, et al. Análise de competitividade do setor das Indústrias de moagem de calcário e mármore do estado do Espírito Santo. Instituto de desenvolvimento educacional e industrial do Espírito Santo – Ideies. Gerência executiva de economia criativa Sesi, Senai – ES. 2017. [citado em 2019 Março 12]. Disponível em: https://ideies.org.br/wp-content/uploads/2017/09/An%C3%A1lise-da-Competitividade-Moagem-de-Calc%C3%A1rio-2017-v2.pdf
8. Braga GNB. Poder de Neutralização e Reatividade do Calcário. 2012. [Citado em
2018 Outubro 16]. Disponível em:
https://agronomiacomgismonti.blogspot.com/2012/09/poder-de-neutralizacao-e-reatividade-do.html.
9. Braga GNB. A Acidez do Solo - Ativa e Potencial. [Citado em 2018 Outubro 16]. Disponível em: https://agronomiacomgismonti.blogspot.com/2010/04/acidez-do-solo-ativa-e-potencial.html
10. Ministério da Agricultura, Pecuária e Abastecimento (BR). Manual de métodos analíticos oficiais para fertilizantes minerais, orgânicos, organominerais e corretivos / Ministério da Agricultura, Pecuária e Abastecimento. 2014. 220 p. [Citado em 2018
Novembro 20]. Disponível em:
http://www.agricultura.gov.br/assuntos/laboratorios/arquivos-publicacoes-
laboratorio/manual-_in-5_-analiticos-oficiais-para-fertilizantes-e-corretivos_com_capa_final_03.pdf
Rev Cient da Fac Educ e Meio Ambiente: Revista da Faculdade de Educação e Meio Ambiente - FAEMA, Ariquemes, v10., n. 2 , p. 95-106, ago.-dez. 2019.
11. Cidade-Brasil. Município de Parecis. 2019. [citado em 2019 Fevereiro 11]. Disponível em: https://www.cidade-brasil.com.br/municipio-parecis.html
12. Filho MB, et al. Correção da acidez do solo. 2009. [Citado em 2018 Agosto].
Disponível em:
http://www.agencia.cnptia.embrapa.br/gestor/arroz/arvore/CONT000fuv6gg6802wyiv 80166sqfcgaqd10.html#
13. Pellegrini AE, Sucunza FA, Millán G, Vázquez ME. Comparación de metodologías analíticas para diagnosticar suelos con enmiendas básicas en el ámbito templado argentino. Rev Cienc Del Suelo. 2016;34(1):1-12.
14. Moreno EL, Martins E, Rajagopal K. Basicidade e acidez, da pré-história aos dias atuais. Rev Virtual Química, 2015;7(3):893-902.
15. Lopes AS, Silva MC, Guilherme LRG. Boletim técnico nº 1 acidez do solo e calagem. Associação Nacional para difusão de adubos – ANDA. São Paulo – SP, 1991. [Citado em 2018 Outubro 16]. Disponível em:
https://www.agencia.cnptia.embrapa.br/recursos/Calagem_boletim_tecnicoID-80pHHoncbJ.pdf.
16. Zambrosi FCB, Alleoni LRF, Caires EF. Teores de alumínio trocável e não trocável após calagem e gessagem em latossolo sob sistema plantio direto. Centro de Pesquisa e Desenvolvimento de Solos e Recursos Ambientais – IAC, Campinas (SP). 2007;66(3):487-495.
17. Amaral LA, Ascari JP, Duarte WM, Mendes IRN, Santos ES, Julio OLL. Efeito de doses de gesso agrícola na cultura do milho e alterações químicas no solo. Rev Agrarian. 2017;35(10):31-41.
18. Moreno EL, Martins E, Rajagopal K. Basicidade e acidez, da pré-história aos dias atuais. Rev Virtual Química, 2015;7(3):893-902.
19. Silva JO. Produto RT 55, Perfil do calcário agrícola. Ministério de Minas e Energia, J. Mendo Consultoria, Secretaria De Geologia, Mineração e Transformação Mineral, Banco Mundial: Projeto Estal, set. 2009. [Citado em 2018 Setembro 26].
Disponível em:
http://www.mme.gov.br/sgm/galerias/arquivos/plano_duo_decenal/a_mineracao _brasileira/P27_RT38_Perfil_do_Calcxrio.pdf.
20. Departamento Nacional de Produção Mineral – DNPM (BR). Anuário Mineral Brasileiro. 2006. [Citado em 2018 Setembro 19]. Disponível em http://www.dnpm.gov.br/dnpm/paginas/anuariomineral/ anuario-mineral-brasileiro-2006.