MINISTÉRIO DA EDUCAÇÃO E DO DESPORTO Escola de Minas da Universidade Federal de Ouro Preto
Departamento de Engenharia de Minas
Programa de Pós-Graduação em Engenharia Mineral – PPGEM
INFLUÊNCIA DA MINERALOGIA NA ETAPA DE SEPARAÇÃO DA
LAMA VERMELHA NO PROCESSO BAYER
Autor: ANGELA NAIR AVELAR
Orientador: Prof. Dr. GERALDO MAGELA DA COSTA
Dissertação apresentada ao Programa de Pós- Graduação do Departamento de Engenharia de Minas da Escola de Minas da Universidade Federal de Ouro Preto, como parte integrante dos requisitos para obtenção do título de Mestre em Engenharia de Minas.
A948i Avelar, Angela Nair.
Influência da mineralogia na etapa de separação da lama vermelha no processo Bayer [manuscrito] / Angela Nair Avelar – 2011.
xii, 84f.: il. color; grafs., tabs.
Orientador: Prof. Dr. Geraldo Magela da Costa.
Dissertação (Mestrado) - Universidade Federal de Ouro Preto. Escola de Minas. Departamento de Engenharia de Minas. Programa de Pós-graduação em
Engenharia Mineral.
Área de concentração: Tratamento de Minérios.
1. Minérios de ferro - Teses. 2. Bauxita - Teses. 3. Hematita - Teses. 4. Mösbauer, Espectroscopia de - Teses. I. Universidade Federal de Ouro Preto. II. Título.
CDU: 622.794.3
Agradecimentos
A Deus por me iluminar em todos os momentos da minha vida.
Aos meus professores Geraldo Magela, Eliomar Ferreira, Maria Beatriz Vieira e Rômulo Angélica pela atenção, orientação, incentivo e experiências trocadas para a realização deste trabalho;
Ao Centro de Desenvolvimento Mineral – CDM / Vale por todo apoio de infraestrutura, essenciais para a realização deste trabalho;
A toda equipe da GAESK pelo apoio e colaboração em todas as etapas desse trabalho. Em especial a Tamara Ribeiro e Daniel Moraes pela amizade, disponibilidade, discussões e apoio nas análises dos resultados de processo;
A Mineração Rio do Norte, em especial ao químico Jardel Oliveira, e a Mineração Paragominas S.A., em especial ao geólogo Clóvis Maurity;
Ao Professor Edison Tazava, do Departamento de Geologia da UFOP, pelo apoio logístico;
Ao Curso de Pós-Graduação em Engenharia de Minas/UFOP pelo apoio administrativo;
Resumo
Neste trabalho foi realizado um estudo de caracterização mineralógica em amostras bauxitas de forma a permitir uma melhor quantificação das espécies de ferro presentes nos minérios originais e nas lamas vermelha obtidas a partir da digestão alcalina em escala de laboratório. Esta caracterização permitiu identificar uma correlação entre a composição mineralógica e o desempenho na etapa de sedimentação da lama vermelha.
As amostras utilizadas nesse trabalho são provenientes de Trombetas (Mineração Rio do Norte) e de Paragominas (Mineração Paragominas S.A.) localizadas no Pará e também uma amostra de Gana.
Abstract
A mineralogical characterization of several bauxites was undertaken in order in order to improve the quantification of all iron-bearing species occurring in the beneficiated ores and in the red mud obtained from the alkaline digestion tests carried out on laboratory scale. A correlation between the mineralogical composition and the settling rate of red mud was derived.
The samples used in this work were from Trombetas (MRN) and Paragominas (Mineração Paragominas S.A.) located in the Para State and one sample from Ghana. The alkaline digestions were done at 145°C and pressure of 5.0 kgf/cm2. Both the initial samples and the red mud generated in these digestions were characterized by optical microscopy, scanning electron microscopy, thermogravimetric analysis, chemical analysis, X-ray diffraction and Mössbauer spectroscopy.
Sumário
1 – INTRODUÇÃO ... 1
2 – OBJETIVO... 2
3 – REVISÃO BIBLIOGRÁFICA... 3
3.1 – Histórico sobre bauxita, alumina e alumínio ... 3
3.2 – Mineração Rio do Norte e Mineração Paragominas S.A. ... 5
3.3 – Geologia ... 8
3.4 – Mineralogia da bauxita ... 12
3.5 – Beneficiamento ... 17
3.6 – Sedimentação da lama vermelha ... 19
3.7 – Métodos analíticos ... 23
4 – MATERIAS E MÉTODOS ... 28
4.1 – Preparação das amostras ... 28
4.2 – Digestão Bayer e determinação da velocidade de sedimentação ... 32
4.3 – Análises químicas ... 34
4.4 – Caracterização Mineralógica ... 35
5.1 – Análise química ... 37
5.2 – Difração de raios X... 38
5.3 – Microscopia ótica e microscopia eletrônica de varredura ... 45
5.4 – Análises termogravimétricas... 51
5.5 – Espectroscopia Mössbauer ... 53
5.6 – Velocidade de sedimentação... 67
6 – DISCUSSÃO ... 68
7 – CONCLUSÕES ... 78
8 – SUGESTÕES PARA TRABALHOS FUTUROS... 80
Lista de Figuras
Figura 1 – Principais reservas e produtores do mundo de bauxita (Fonte adaptado apresentação Marcio
Goto - Alcoa IBRAM 2007). ... 4
Figura 2 - Localização da Mineração Rio do Norte e Paragominas. ... 6
Figura 3 – Fluxograma da operação de extração de bauxita da MRN (fonte site www.mrn.com.br). ... 7
Figura 4 – Fluxograma do beneficiamento do minério de Paragominas (relatório interno - Vale). ... 8
Figura 5 – Zonas propícias para formação de depósitos de bauxita laterítica (Fonte adaptado apresentação Marcio Goto - Alcoa IBRAM 2007). ... 9
Figura 6 - Perfil laterítico bauxítico de Paragominas (fonte relatório interno Vale). ... 11
Figura 7 – Perfil litológico da Mineração Rio do Norte (fonte www.mrn.com). ... 12
Figura 8 – Fluxograma simplificado do Processo Bayer (relatório interno – Vale). ... 19
Figura 9- Diagrama de bloco de um espectrômetro Mössbauer (adaptado de Vanderbergue, 1991)... 26
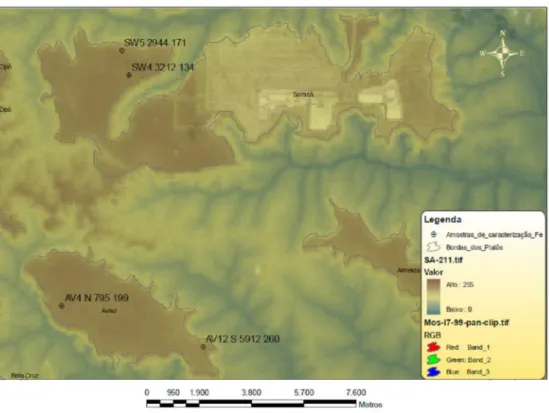
Figura 10 - Localização dos pontos de coleta das amostras na Mineração Rio do Norte. ... 29
Figura 11 - Fluxograma de análises das amostras utilizadas. ... 31
Figura 12 – Hotbox utilizado nos testes do CDM. ... 33
Figura 13 – Detalhe das provetas dentro do hotbox, após a sedimentação da lama vermelha. ... 33
Figura 14 - Difratogramas de raios X das amostras MBP. Caulinita (Cau); gibbsita (Gib); goethita (Goe); hematita (Hem) e anatásio (Ana). ... 39
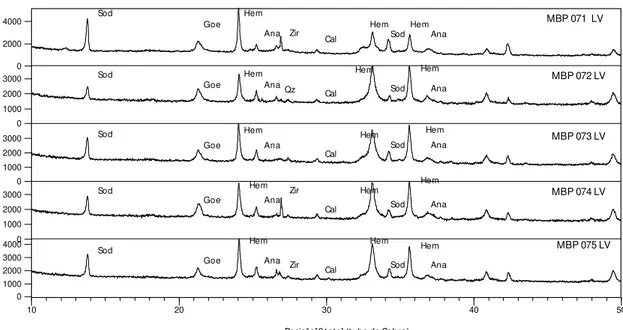
Figura 16 - Difratogramas de raios X das amostras de lama vermelha do minério da MBP. Sodalita
(Sod); goethita (Goe); hematita (Hem); gibbsita (Gib); quartzo (Qz); calcita (Cal) e anatásio (Ana). .... 40
Figura 17 - Difratogramas de raios X das amostras de lama vermelha da MRN. Sodalita (Sod); goethita (Goe); hematita (Hem); Gib (gibbsita); calcita (Cal); anatásio (Ana); Hydrotalcita (Hyd). ... 41
Figura 18 - Difratogramas de raios X das amostras de minério secundário da MBP. Caulinita (Cau); gibbsita (Gib); goethita (Goe) e hematita (Hm). ... 42
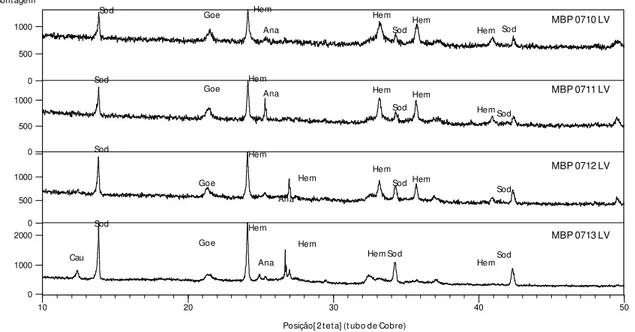
Figura 19 - Difratogramas de raios X das amostras de lama vermelha do minério secundário MBP. Sodalita (Sod); goethita (Goe); hematita (Hem); caulinita (Cau) e anatásio (Ana)... 42
Figura 20 - Difratograma de raios X da amostra de Gana. Gibbsita (Gib); goethita (Goe); hematita (Hem); (Ana) anatásio e sodalita (Sod). ... 43
Figura 21 – Tamanhos de cristalitos da hematita e goethita nas amostras de bauxita e de lama vermelha dos minérios da MBP e da MRN. ... 44
Figura 22 - Fotomicrografia da amostra MBP 073: (a) porções goethíticas e hematiticas bem distintas; (b) porções goethíticas com hematita microcristalina. Luz refletida. ... 45
Figura 23 - Fotomicrografia da amostra MRN 078 (a) porções goethíticas e hematiticas bem distintas; (b) porções goethíticas com hematita microcristalina. Luz refletida... 46
Figura 24 - Fotomicrografia da amostra MBP 071: (a) gibbsita microcristalina impregnada com ferro; (b) caulinita associada a gibbsita. Luz transmitida com polarizadores cruzados. ... 47
Figura 25 - Fotomicrografia da amostra MRN 079: (a) gibbsita granular com associação de ferro nas bordas. Luz transmitida com polarizadores cruzados. ... 48
Figura 26 –Imagens ao MEV das amostras de lama do minério da MBP. ... 49
Figura 27 - Imagens ao MEV das amostras lama do minério da MRN. ... 50
Figura 28 - Imagens ao MEV das amostras de lama do minério secundário MBP e de Gana. ... 51
Figura 30 - Curvas de TGA/DTG e DTA da amostra GAN 0714. ... 53
Figura 31 – Espectros Mössbauer das amostras MBP 071 e MBP 071 LV a 298 K e 77K. ... 54
Figura 32 - Espectros Mössbauer das amostras MBP 072 e MBP 072 LV a 298 K e 77K. ... 55
Figura 33 - Espectros Mössbauer das amostras MBP 073 e MBP 073 LV a 298 K e 77K. ... 55
Figura 34 - Espectros Mössbauer das amostras MBP 074 e MBP 074 LV a 298 K e 77K. ... 56
Figura 35 - Espectros Mössbauer das amostras MBP 075 e MBP 075 LV a 298 K e 77K. ... 56
Figura 36 - Espectros Mössbauer das amostras MRN 076 e MRN 076 LV a 298 K e 77K. ... 57
Figura 37 - Espectros Mössbauer das amostras MRN 077 e MRN 077 LV a 298 K e 77K. ... 57
Figura 38 - Espectros Mössbauer das amostras MRN 078 e MRN 078 LV a 298 K e 77K. ... 58
Figura 39 - Espectros Mössbauer das amostras MRN 079 e MRN 079 LV a 298 K e 77K. ... 58
Figura 40 - Espectros Mössbauer das amostras MBP 0710, MBP 0710 LV, MBP 0711 e MBP 0711 LV a 298 K, MBP 0712 e MBP 0712 LV, MBP 0713 e MBP 0713 LV. ... 63
Figura 41 - Espectros Mössbauer das amostras GAN 0714 e GAN 0714 LV a temperatura ambiente. .... 65
Figura 42 – Diagrama de dispersão do conteúdo de gibbsita nas amostras iniciais da MBP e MRN versus a velocidade de sedimentação. ... 70
Figura 43 - Diagrama de dispersão do conteúdo de caulinita nas amostras iniciais da MBP e MRN versus a velocidade de sedimentação. ... 71
Figura 44 - Diagrama de dispersão do fator de lama nas amostras iniciais da MBP e MRN versus a velocidade de sedimentação. ... 72
Figura 45 – Diagrama de dispersão do teor de ferro total nas amostras iniciais MBP e MRN versus a velocidade de sedimentação. ... 73
velocidade de sedimentação. ... 73
Figura 47 - Diagrama de dispersão do conteúdo de goethita das amostras iniciais MBP e MRN versus a
velocidade de sedimentação. ... 74
Figura 48- Diagrama de dispersão da razão hematita/goethita nas amostras inicias MBP e MRN versus
a velocidade de sedimentação. ... 75
Figura 49 - Diagrama de dispersão dos teores de goethita tipo 2 nas amostras iniciais MBP e da MRN
versus a velocidade de sedimentação. ... 76
Figura 50 - Diagrama de dispersão dos teores de goethita tipo 1 nas amostras de lama vermelha dos
minérios da MBP e da MRN versus a velocidade de sedimentação. ... 77
Figura 51 - Diagrama de dispersão dos valores de hematita nas amostras de lama vermelha dos minérios
Lista de Tabelas
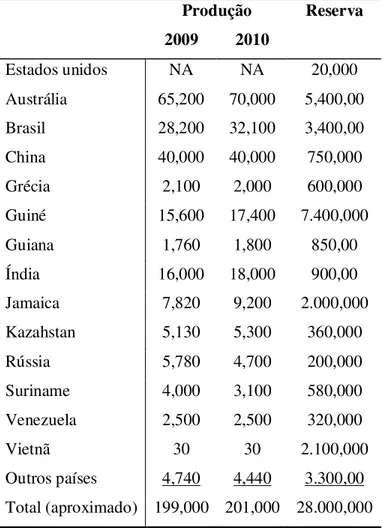
Tabela 1 - Distribuição mundial de reservas e sua produção de bauxita em 2009 e 2010 - unidade 1.000
t (fonte USGS 2011). ... 5
Tabela 2 - Composição mineralógica de bauxitas (adaptado de Ostap, 1984). ... 13
Tabela 3 - Raios iônicos e valores máximos de substituição dos cátions usualmente existentes na goethita (Cornell & Schwertmann 2000). ... 16
Tabela 4 - Localização dos pontos de coleta das amostras de minério da MRN. ... 29
Tabela 5 - Localização dos pontos de coleta das amostras de minério da MBP. ... 30
Tabela 6 - Localização dos pontos de coleta das amostras de minério secundário da MBP. ... 30
Tabela 7 – Resultados de análises químicas das amostras de bauxita (%). ... 37
Tabela 8 - Resultados de análises químicas das amostras de lama vermelha (%.) ... 38
Tabela 9 - Parâmetros obtidos das análises termogravimétricas... 52
Tabela 10 - Parâmetros experimentais obtidos dos espectros Mössbauer (298 K) das amostras iniciais. Hhf (kOe) = campo magnético hiperfino; 2εQ(mm/s) = deslocamento quadrupolar; δ (mm/s) = desvio isomérico; S = área relativa; ΔEQ (mm/s) = desdobramento quadrupolar. ... 60
Tabela 11 - Parâmetros experimentais obtidos dos espectros Mössbauer (77 K) das amostras iniciais de minério. Hhf (kOe) = campo magnético hiperfino; 2εQ(mm/s) = deslocamento quadrupolar; δ (mm/s) = desvio isomérico; S = área relativa; ΔEQ (mm/s) = desdobramento quadrupolar. ... 61
Tabela 13 – Quantificação dos minerais de ferro presentes nas amostras iniciais e de lama da MBP,
MRN e Gana. ... 66
Tabela 14 – Velocidade de sedimentação e fator de lama obtidos nos resultados de digestão. ... 67
Tabela 15 – Composição mineralógica das amostras de minério da MBP... 68
Tabela 16 - Composição mineralógica das amostras de minério secundário da MBP. ... 68
1 – INTRODUÇÃO
A bauxita compõe-se principalmente de minerais de alumínio, sendo a gibbsita (γ-Al(OH)3), diásporo (-AlOOH) e boehmita (γ-AlOOH) os mais importantes. As suas proporções na rocha variam muito entre os depósitos, bem como o tipo e a quantidade das impurezas do minério na forma de óxi-hidróxidos de ferro, silicatos, óxido de titânio, entre outras. (Sampaio et al., 2005).
Os minerais de ferro são responsáveis pela coloração da bauxita. O vermelho indica a presença de hematita (Fe2O3) enquanto o amarelo pode indicar a presença da goethita e/ou Al-goethita (Fe1-xAlxOOH).
O processo Bayer para obtenção de alumina a partir da bauxita foi desenvolvido e patenteado por Karl Joseph Bayer em 1888. Este método consiste na extração do óxido de alumínio de minério de bauxita, através da lixiviação alcalina utilizando soda cáustica como reagente. Atualmente este é o único processo viável para a produção de alumina metalúrgica (“Smelter Grade Alumina”).
No final do processo de lixiviação alcalina obtém-se uma polpa constituída por um licor rico em alumina (industrialmente denominado licor rico) contendo sílica e uma lama vermelha constituída pelos minerais inertes ao processo de digestão. Os minerais mais frequentes são hematita, goethita, magnetita, ilmenita, anatásio, rutilo, quartzo, mica, turmalina, zircão, carbonato. Também pode ocorrer à presença de ferro no licor rico, entretanto sua forma ainda é desconhecida.
Alguns estudos avaliaram os efeitos dos principais contaminantes do minério de bauxita sobre as variáveis desse processo (Ostap 1984, Li & Rutherford 1996, Authier-Martin et al., 2001 e Ribeiro et al., 2009). Dentre essas variáveis, a velocidade de
Nesse trabalho será dada ênfase às fases minerais portadoras de ferro, pois é conhecido que dependendo da forma como ocorrem os minerais portadores de ferro, se como goethita (incluindo o tipo Al-goethita), hematita ou na forma de espécie coloidal, haverá um efeito sobre a sedimentação da lama vermelha e, em alguns casos, contaminação do licor rico.
Até então, a grande maioria dos trabalhos realizados para a caracterização tecnológica de bauxita da mina de Paragominas feitos na Vale concentraram-se em identificar as principais propriedades do minério, dando ênfase aos aspectos de extração de alumina, consumo de soda e velocidade de sedimentação da lama vermelha. Alguns trabalhos tentaram identificar o efeito da presença e quantidade dos minerais contaminantes na sedimentação da lama vermelha, porém os resultados foram apenas de caráter qualitativo. Isso ocorreu principalmente devido à dificuldade de se identificar de forma precisa o percentual da hematita e goethita ou alumino-goethita.
As técnicas mais usadas em caracterização mineralógica, como microscopia ótica, microscopia eletrônica de varredura e difração de raios X podem apresentar problemas na quantificação das fases de ferro nas amostras de bauxita, devido a seu pequeno tamanho de cristal e defeitos na estrutura cristalina. A utilização da espectroscopia Mössbauer possibilitou a quantificação precisa os minerais portadores de ferro e suas possíveis substituições.
2 – OBJETIVO
3 – REVISÃO BIBLIOGRÁFICA
3.1 – Histórico sobre bauxita, alumina e alumínio
No passado, o alumínio era pouco conhecido e tinha um custo elevado de produção, e devido a isso esse metal só era utilizado em trabalhos ornamentais como em estatuetas e placas comemorativas. No final do Século XIX, com o aumento da produção e redução de preços, ele começou a ser usado em utensílios de cozinha e em alguns painéis de automóveis.
No início do século XX, as indústrias de alumínio começaram a trabalhar na produção de ligas de alumínio com propriedades mecânicas superiores. Como se trata de um metal que possui excelente combinação de propriedades úteis, foi fácil sua aplicação em um campo vasto da engenharia (www.abal.org.br).
No fim da primeira Guerra Mundial, com a expansão da mineração em meados de 1917, atingiu-se o primeiro milhão de toneladas de produção anual do minério. Especificamente no Brasil, os primeiros registros oficiais sobre a bauxita estão nos Anais de 1928 da Escola de Minas de Ouro Preto (fonte www.abal.org.br).
Arabia Saudita
DRC Gana Guiné
Aust ralia Brasil
Venezuela
India Viet nã China
Rússia
Jamaica
Grécia
Indonesia Camarões
M adagascar
Filipinas
Suriname Serra Leoa Colombia
Figura 1 – Principais reservas e produtores do mundo de bauxita (Fonte adaptado apresentação Marcio Goto - Alcoa IBRAM 2007).
O Brasil é o terceiro maior produtor de minério de bauxita (Tabela 1) com produção em 2010 de 32 milhões de toneladas, o que significa 15% da produção mundial, que foi de 201 milhões de ton. A Austrália é líder em produção, com 70 milhões de ton. em 2010, que correspondem a 34% da produção global, seguida da China com 19%.
As principais empresas produtoras no mundo são: Comalco, Alcan, Alcoa, RioTinto e BHP na Austrália, Chalco na China, CVG na Guiné, e MRN no Brasil.
Tabela 1 - Distribuição mundial de reservas e sua produção de bauxita em 2009 e 2010 -
unidade 1.000 t (fonte USGS 2011).
Produção Reserva
2009 2010
Estados unidos NA NA 20,000
Austrália 65,200 70,000 5,400,00
Brasil 28,200 32,100 3,400,00
China 40,000 40,000 750,000
Grécia 2,100 2,000 600,000
Guiné 15,600 17,400 7.400,000
Guiana 1,760 1,800 850,00
Índia 16,000 18,000 900,00
Jamaica 7,820 9,200 2.000,000
Kazahstan 5,130 5,300 360,000
Rússia 5,780 4,700 200,000
Suriname 4,000 3,100 580,000
Venezuela 2,500 2,500 320,000
Vietnã 30 30 2.100,000
Outros países 4,740 4,440 3.300,00 Total (aproximado) 199,000 201,000 28.000,000
* NA – Não disponível
3.2 – Mineração Rio do Norte e Mineração Paragominas S.A.
A maior parte das amostras que foram utilizadas nesse trabalho são do minério de Trombetas (MRN) e do minério (e minério secundário) de Paragominas (MBP), provenientes do norte do Brasil no estado do Pará.
microrregião do Baixo Amazonas (Figura 2).
Figura 2 - Localização da Mineração Rio do Norte e Paragominas.
Lavra
Escavação e transporte
Disposição do rejeito
Reflorestamento
Britagem Bauxita britada
Escrubagem
Bauxita lavada
Carregamento Transporte ferroviário
Descarregamento
de vagões Bauxita úmida Secagem Bauxita seca
Carregamento de navios
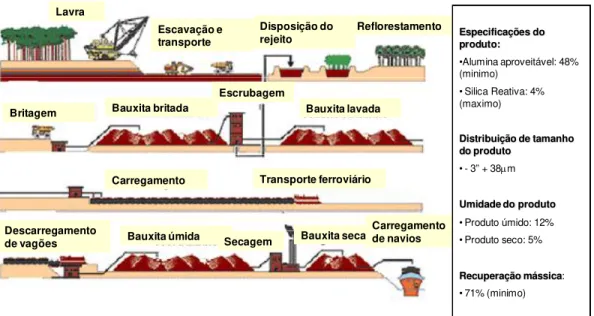
Especificações do produto:
•Alumina aproveitável: 48% (minimo)
• Silica Reativa: 4% (maximo)
Distribuição de tamanho do produto
• - 3” + 38m
Umidade do produto
• Produto úmido: 12% • Produto seco: 5%
Recuperação mássica:
• 71% (minimo)
Figura 3 – Fluxograma da operação de extração de bauxita da MRN (fonte site www.mrn.com.br).
A capacidade anual de produção da MRN é de 16,3 milhões de toneladas de bauxita com teor médio de 50% de alumina aproveitável, 4% de sílica reativa, granulometria abaixo de 3" e umidade de 5 a 12%.
A segunda maior produtora de bauxita do Brasil é a Mineração Paragominas S.A., localizada no leste do Estado do Pará. A fase de produção comercial da mina teve início em março de 2007, com capacidade anual de 5,4 milhões de toneladas, para suportar a segunda expansão da Alunorte (refinaria).
Especificações do
produto: Alumina
aproveitável: 48% / Sílica reativa: 4%
Distribuição de tamanho
do produto: 98-100%<300
m e 42-47%< 38m
Sólidos na polpa: 50%
Recuperação mássica:
70% (miínimo)
Figura 4 – Fluxograma do beneficiamento do minério de Paragominas (relatório interno - Vale).
3.3 – Geologia
A bauxita é uma rocha de coloração avermelhada que foi descoberta em 1821 por Berthier na localidade de Les Baux, no sul da França. Sua composição está
associada a quatro elementos principais: Al, Fe, Si e Ti (Schobbenhaus & Coelho, 1988). Segundo a definição de Bardossay & Aleva (1990) as bauxitas “são rochas de origem lateritica formadas dominantemente por hidróxidos de alumínio (gibbsita e/ou boehmita e/ou diásporo), subordinadamente por hematita e/ou goethita, caulinita, anatásio e fosfatos de alumínio”.
A classificação das bauxitas é feita com base em sua composição química, mineralógica e em suas características petrográficas, a mais utilizada é aquela baseada na natureza da rocha-mãe e na gênese do depósito (Bardossy & Aleva, 1990):
- depósitos de bauxitas cársticas, que correspondem a dissolução de rochas carbonáticas e concentração residual do Al pelo intemperismo de aluminossilicatos;
- depósitos de bauxitas do tipo Tikhvin, que são bauxitas detríticas que recobrem superfícies erosivas de rochas aluminossilicatadas.
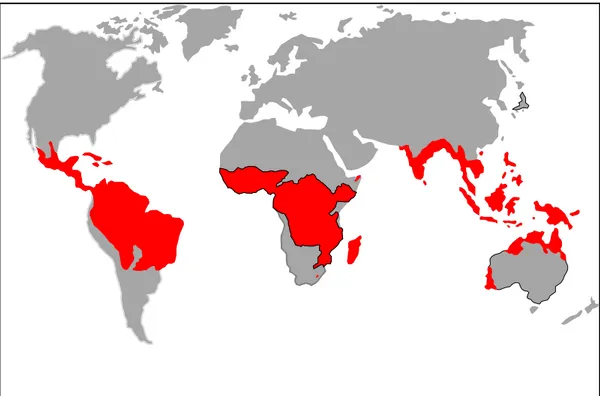
A bauxita laterítica está amplamente distribuída ao longo das zonas tropicais do mundo (Figura 5).
Figura 5 – Zonas propícias para formação de depósitos de bauxita laterítica (Fonte adaptado apresentação Marcio Goto - Alcoa IBRAM 2007).
A textura, estrutura, mineralogia, composição química e coloração das rochas lateríticas variam amplamente em seção vertical de um perfil laterítico em camadas sub-horizontais com variações químicas e físicas (Costa, 1991).
O teor de alumínio da rocha-mãe influencia o teor e a qualidade do minério: 30 a 35 % em algumas rochas sedimentares caulíniticas; 10 a 15% em granitos e basaltos, e podem se formar a partir de rochas com menos de 15%. A intensa lixiviação no perfil produz a migração e perda de elementos mais solúveis (sódio, potássio, cálcio e manganês) e ocorrem reações químicas para voltar-se ao equilíbrio nas quais são formados os minerais secundários. Costa (1991) explicou a evolução do perfil de bauxitas lateríticas da seguinte forma:
1. é formado sobre a rocha-mãe um horizonte saprolítico composto de caulinita, goethita e/ou hematita, e minerais residuais (como muscovita, quartzo, zircão, rutilo, ilmenita, turmalina, etc.). O horizonte saprolítico é a parte do perfil onde ainda é possível observar a espessura e a textura da rocha-mãe. Geralmente essa espessura está em torno de 5 a 15m.
2. No topo do horizonte saprolítico acontece a alteração e/ou transformação da caulinita em gibbsita, ou seja silício da caulinita é lixiviado e tem-se a formação da gibbsita. O novo horizonte formado é conhecido como bauxita, e tem poucos metros de espessura, mas altos valores de Al e baixo a médio de Fe.
3. Acima da bauxita pode desenvolver-se uma crosta ferruginosa bauxítica e até mesmo um horizonte argiloso. A crosta é um horizonte superficial, concrecionário e endurecido, formado normalmente por oxi-hidróxidos de Fe e de Al.
A espessura de todo o perfil depende da natureza da rocha-mãe (textura, mineralogia), tempo de formação e idade deste perfil, além da evolução da paisagem (do relevo).
em camadas, devido a alternância de horizontes ricos em Al ou Fe (Kotschoubey et al.,
2005).
Figura 6 - Perfil laterítico bauxítico de Paragominas (fonte relatório interno Vale).
Figura 7 – Perfil litológico da Mineração Rio do Norte (fonte www.mrn.com.br).
3.4 – Mineralogia da bauxita
Tabela 2 - Composição mineralógica de bauxitas (adaptado de Ostap, 1984).
Mineral Fórmula
Minerais predominantes
Gibbsita Al(OH)3
Boehmita -AlOOH
Diásporo -AlOOH
Hematita Fe2O3
Alumino-goethita (Al,Fe)OOH
Goethita FeOOH
Anatásio TiO2
Rutilo TiO2
Caulinita Al2Si2O5(OH)4
Quartzo SiO2
Minerais minoritários e elementos traços
Fosfatos (crandalita, apatita) CaAl3(PO4)2(OH)5(H2O) / Ca5(PO4)3F
Lithioforita (Li, Al) MnO2(OH)2
Calcita CaCO3
Carbono orgânico Materiais húmicos
Vanádio V2O5
Cromo Cr2O3
Arsênio As2O3
Traços F, S, Hg
O conteúdo e a morfologia dos minerais portadores de alumínio são fundamentais na extração da alumina (por exemplo, tipo de hidróxido de alumínio), qualidade do produto, quantidade de soda caústica (por exemplo, quantidade e tipo de caulinita), e consumo de energia (temperatura de digestão) (Authier-Martin et al.,
2001).
Na indústria de alumínio os tipos de bauxita mais utilizados para fins metalúrgicos são as bauxitas gibbsíticas, que são aquelas que contêm a maior parte do seu alumínio na forma de gibbsita, e menos de 2% como boehmita. As bauxitas boehmiticas são predominantemente compostas por boehmita mas contém cerca de 2% de diásporo. As bauxitas mistas são predominantes compostas de gibbsita.
da bauxita gibbsítica será baixa temperatura (100-150°C) e no caso de boehmítica as temperaturas são mais elevadas (235-250°C) .
Segundo Ostap (1984), a eficiência do processamento depende, em parte, da morfologia dos cristais do mineral portador de alumínio. Os tamanhos dos cristais de gibbsita na bauxita também podem variar de um depósito para o outro. Por exemplo, a gibbsita ocorre como uma mistura de agregados fracamente comprimidos e em prismas na bauxita da Guiana, ou como prismas hexagonais elongados na bauxita australiana, ou como agregados de prismas entrelaçados em Trombetas (Mineração Rio do Norte). Esse mesmo autor sugeriu que o impacto da mineralogia no processo Bayer pode ser observado na extração seletiva dos minerais solúveis e insolúveis presentes na bauxita, na precipitação das espécies desejadas (trihidratado) e indesejadas ao longo do processo Bayer, e nas especificações para produção de alumina smelter grade. Além de lidar com
as fases portadoras de alumínio na bauxita, o processo Bayer tem que lidar com espécies inertes que se tornarão resíduos do processo (lama vermelha).
Dos elementos presentes na bauxita, aqueles que possuem as propriedades químicas necessárias para acumular algum teor no licor recirculante são P, As, Mo, Ga, Cl, I, Br, K e Ge. Cinco elementos adicionais podem causas problemas específicos no processo: silício, enxofre, vanádio, flúor e carbono (na forma de carbono orgânico e como carbonato).
O quartzo, minerais de ferro (hematita, goethita, etc.), e minerais de titânio (anatásio e rutilo) são considerados inertes na digestão a baixa temperatura (100-150°C). Em digestão a alta temperatura (235-260°C) espera-se que todas essas fases, com exceção do rutilo e da hematita, sejam atacadas em diferentes proporções pela soda caústica (Authier-Martin et al., 2001).
estável em condições de alta temperatura na digestão alcalina no processo Bayer (Authier-Martin et al., 2001).
A estrutura da goethita consiste de uma matriz de ânions (O-2 e OH-) empilhados ao longo da direção [010] com íons FeIII ocupando metade dos interstícios octaédricos dentro de uma camada. Os íons de ferro estão arranjados em fileiras duplas de sítios vazios. Os difratogramas de raios X de goethita frequentemente mostram picos alargados, consequência do efeito de pequeno tamanho de cristais; em cristais maiores isso é causado por uma desordem do arranjo interno resultante de substituições isomórficas (Cornell & Schwertmann, 2000). A estrutura da hematita pode ser descrito como um empacotamento de íons de oxigênio empilhados ao longo da direção [001]. Dois terços dos sítios são preenchidos com íons de ferro, que são organizados regularmente sendo seguido por um site vazio no plano (001) (Cornell & Schwertmann, 2000).
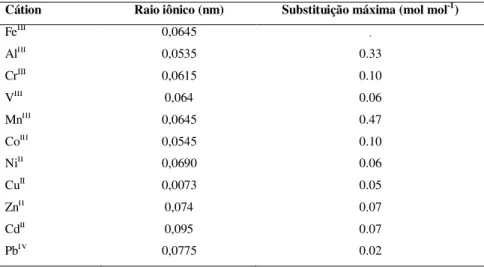
Tabela 3 - Raios iônicos e valores máximos de substituição dos cátions usualmente existentes
na goethita (Cornell & Schwertmann 2000).
Cátion Raio iônico (nm) Substituição máxima (mol mol-1)
FeIII 0,0645
-
AlIII 0,0535 0.33
CrIII 0,0615 0.10
VIII 0,064 0.06
MnIII 0,0645 0.47
CoIII 0,0545 0.10
NiII 0,0690 0.06
CuII 0,0073 0.05
ZnII 0,074 0.07
CdII 0,095 0.07
PbIV 0,0775 0.02
No processo Bayer as fases de alumínio são dissolvidas e os minerais de ferro permanecem como resíduo (lama vermelha). O comportamento da velocidade de sedimentação é um fator econômico importante para a produtividade da refinaria e controle da qualidade do produto final. Diversos são os fatores que influenciam a taxa de sedimentação da lama, dentre eles cita-se a composição mineralógica. Outros parâmetros como tamanho, área superficial, densidade, presença de fases amorfas ou criptocristalina também tem influências nessa sedimentação.
Murray et al. (2009) em um estudo com amostras sintéticas usaram pela
primeira vez a difração síncroton in-situ para acompanhar a transformação hidrotermal
necessário a presença de sementes de hematita. A análise cinética não mostrou nenhuma mudança nas temperatura entre 200° e 250°C.
E Kirwan et al. (2009) utilizaram a difração de raios X e a espectroscopia
Mössbauer para quantificar as fases minerais presentes nestas amostras. Foram identificadas a presença de hematita e alumino-goethita, e nenhuma fase amorfa nas amostras iniciais de bauxita. Estes autores conseguiram obter uma relação goethita/hematita para efeito de comparação dos resultados das técnicas, porém não correlacionaram esses resultados com os parâmetros do processo Bayer. O valor determinado via difração de raios X para a substituição isomórfica de alumínio foi de 15 mol%.
3.5 – Beneficiamento
Depois de extraída da mina, a bauxita é introduzida em um circuito de beneficiamento. O minério inicialmente passa por processos de cominuição (britagem/moagem) e, no caso específico do Brasil, têm-se uma etapa de deslamagem para eliminação de grande parte do mineral contaminante (caulinita) e para concentração dos minerais de alumínio. Após esses processos, o minério lavado é transportado até a refinaria, onde é submetido a um processo de lixiviação alcalina (digestão). Na digestão, a bauxita é lixiviada em uma solução aluminato de sódio com alta concentração de soda cáustica sob determinadas condições de concentração, pressão, temperatura e tempo de residência. Essas variáveis são dependentes das características mineralógicas da amostra inicial. Os minerais atacados na lixiviação são a gibbsita, boehmita e a caulinita, que são os principais minerais de alumínio presentes na bauxita. À medida em que ocorre a solubilização dos hidróxidos de alumínio e da caulinita, o licor é enriquecido em Al e Si, respectivamente. Porém, com o avanço da digestão, o licor passa a ficar saturado em sílica, que começa a precipitar na forma do chamado produto de dessilicação, ou sodalita Bayer que recebe esse nome devido a sua composição (Na, Al, Si) e sua estrutura de zeólita.
e uma lama vermelha constituída pelos minerais inertes ao processo de digestão, frequentemente são hematita, goethita, magnetita, ilmenita, anatásio, rutilo, quartzo, mica, turmalina, zircão, carbonato.
Após a lixiviação, o resíduo (lama vermelha) deve ser separado do licor enriquecido em alumínio por sedimentação/filtragem. Para auxiliar na sedimentação das impurezas presentes no licor é adicionado um floculante que gera um agregado mais pesado favorecendo uma decantação mais rápida e eficiente. A lama é então retirada do processo e a solução resultante (licor rico) segue para a precipitação e filtragem.
Moagem
Digestão
Expansão do DBO
Sedimentação de
lama Lavagem de lama
Deposição de
rejeitos Resfriamento
Precipitação
Aquecimento do licor
Classificação
Lavagem Calcinação
vapor vapor
Licor rico
Semente
Licor Licor
pobre
Bauxita
Alumina Calcinada NaOH
Hidrato de alumina
Lama
ura 5 – Fluxograma esquemático do processo Bayer.
3.6 – Sedimentação da lama vermelha
Ao final da etapa de digestão da bauxita, almeja-se um licor rico puro e com o mínimo de sólidos em suspensão, pois quanto mais puro o licor rico em aluminato melhor o produto final na forma de alumina. A separação do licor e da lama vermelha ocorre durante a etapa de sedimentação, na qual é interessante que as partículas sedimentem o mais rápidamente possível para não impactar na produtividade da refinaria.
As partículas em suspensão sofrem a ação de três tipos de força: gravitacional, hidrodinâmica e movimento browniano. A força da gravidade ao agir nas partículas é compensada pelas forças de empuxo e arrasto. A presença de outras partículas do mesmo tamanho caindo ao mesmo tempo também pode atrapalhar a sedimentação, por isso a concentração de sólidos também é importante para o bom desempenho dessa etapa. Essa concentração pode ser expressa como fator de lama, que representa a relação entre a massa da lama vermelha e a massa da bauxita que alimentou a digestão.
Alguns trabalhos foram publicados sobre a relação da presença dos minerais de ferro com o comportamento na sedimentação (Ostap 1984, Li & Rutherford 1996,
Gomes et al., 2005, Murray et al., 2009), assim como a solubilidade desses minerais no
processo Bayer (Basu 1983). Esses autores afirmaram que bauxitas com menor conteúdo de goethita têm um desempenho melhor na separação sólido-líquido, levando a uma taxa de velocidade de sedimentação mais alta.
Basu (1983) avaliou o impacto da solubilidade dos minerais de ferro na solução de aluminato de sódio. A autora fez o processo Bayer com amostras contendo mistura de minerais puros de goethita e hematita em uma solução de aluminato de sódio, para diferentes temperaturas e após a digestão avaliou-se a taxa de sedimentação e a qualidade da lama. Verificou-se nesse trabalho que amostras de bauxita com alto conteúdo de hematita apresentam taxa de velocidade de sedimentação consideravelmente mais altas do que amostras ricas em goethita. Segundo a autora, esse comportamento foi devido as propriedades de área superficial distintas desses minerais, já descritas anteriormente.
Além de observar um melhor uma melhor sedimentação das amostras com alto conteúdo de hematita a autora avaliou de duas maneiras a transformação da goethita em hematita, em amostras puras de goethita e amostras com misturas de hematita: por desidratação térmica no ar em uma faixa de temperatura de 300-550°C (por 96 horas); e por tratamento hidrometalúrgico (em uma solução de Na2O/Al2O3) em temperaturas acima de 175°C. Nos resultados de difração de raios X da hematita gerada na desidratação térmica, a autora observou uma desordem na estrutura da hematita formada a partir da goethita. O tratamento térmico da goethita resultou em aproximadamente 55, 60 e 80% de transformação em hematita à temperaturas de 350°, 400° e 550°C, respectivamente. Vale ressaltar que esses números são apenas de caráter qualitativo pois foram obtidos por comparações das áreas dos picos de difração em relação ao padrão puro da hematita cristalina.
à falta de locais de nucleação de hematita, e ao fato de que alguns componentes de licor podem ser prejudiciais para a reação.
A partir dos resultados dos ensaios de Basu (1983) e do gráfico gerado nesse trabalho observou-se que a solubilidade do ferro em função da temperatura é exponencial. Isso pode implicar na reprecipitação do ferro na etapa de clarificação ou na de sedimentação, se essas etapas forem realizadas a temperaturas mais baixas do que as utilizadas na digestão. É muito provável que o ferro precipite como partículas nanométricas de -FeOOH porque a formação dessa fases é cineticamente favorecida devido à elevada concentração de soda caústica. Baseado nestes resultados, pode-se esperar que a clarificação no processo a alta temperatura também seja afetada pelo mineral de ferro presente na amostra.
Ostap (1984) abordou em seu trabalho que a presença de cristais finos pode estar relacionada à Al-goethita, que tende a formar cristais de menor tamanho. Esta espécie mineral tem densidade menor do que a goethita ou hematita, o que não ajuda na sedimentação. Este autor também apontou uma questão que ainda não está bem definida, e que diz respeito à forma na qual o elemento ferro está presente no licor: não é conhecido se esse ferro remanescente no licor, e consequentemente no produto Bayer, está na forma de complexo orgânico (resultantes da reação do material orgânico que pode vir associado a bauxita na lavra) ou na forma coloidal.
As partículas de pequenos tamanhos podem ser extremamente significantes, mesmo em pequenas porcentagens devido ao efeito negativo que causam nas separações sólido-líquido. Acredita-se que mesmo uma quantidade pequena de material nanométrico (ou amorfo) poderia ter um efeito significativo na sedimentação. No passado, nada foi publicado sobre a determinação da fração de materiais nanométricos e/ou amorfos presentes nas lamas vermelhas e bauxitas, bem como do efeito destes materiais no comportamento da separação da lama vermelha.
formar mais partículas menores o que retarda a sedimentação das partículas. Orban (apud Li & Rutherford 1996) descreveu que a velocidade de sedimentação da lama
vermelha está relacionada com a área superficial das partículas e que quanto maior a superfície do mineral de ferro menor a taxa de sedimentação. O mineral de ferro com maior área é a alumino-goethita, seguida de goethita e hematita.
Roach & Jamieson (2002) voltaram a abordar o problema do ferro no licor, e segundo os autores existem muitas bauxitas que quando processadas, resultam em alto teor de ferro em solução no licor rico e consequentemente na alumina produzida. Esses autores apontaram que bauxitas com baixo teor de ferro são mais propensas a produzirem licor com alto ferro. A solubilidade do ferro no licor também foi estudada nesse trabalho em várias temperaturas e concentrações de soda cáustica, e a principal conclusão foi que a solubilidade dos óxidos de ferro aumenta com a temperatura e concentração de caústico.
Nesse mesmo trabalho de Roach & Jamieson (2002), foi sugerido que bauxitas podem conter ferro associado a gibbsita. Na dissolução desta fase o ferro liberado pode resultar num licor rico em ferro, o que não é desejável. Essa substituição do ferro na gibbsita pode ocorrer em baixas quantidades, o que já seria suficiente segundo os autores para explicar o ferro solúvel no licor. Foram apresentadas algumas hipóteses para explicar esse fenômeno, e a mais plausível é que essa gibbsita portadora de ferro poderia ser formada no licor antes de precipitação do ferro. Essa pode ser uma explicação, dentre outras, para o ferro contido no licor rico.
Gomes et al. (2005) exploraram, além da presença da hematita e goethita, a
forma como os minerais se aglomeram para sedimentação da lama vermelha. Nesse estudo percebeu-se que as amostras com maiores taxas de sedimentação apresentaram principalmente aglomerados compactos dos cristais, enquanto para a menor taxa de sedimentação a amostra é composta por sodalita Bayer de forma isolada ou com cristais que aparentam estar fracamente conectados.
Em um estudo mais atual, Ribeiro et al. (2009) realizaram um estudo de
lama vermelha) na digestão da bauxita gibbsítica a 145 º C durante 60 minutos, com o objetivo de reduzir o ferro no licor. Foi obtido uma redução do nível de ferro no licor rico de 0.027g/L a 0.004g /L de Fe2O3 usando areia de 10% de carga na digestão. A caracterização mineralógica preliminar dessa lama indicou uma grande quantidade de partículas finas e predomínio de sodalita, enquanto a areia apresentou partículas grossas e predominância de minerais de ferro na forma de hematita, quartzo e apenas traços de sodalita. Esses autores associaram o sucesso na redução dos níveis de ferro a areia adicionada devido as suas partículas grossas de hematita que podem ter atuado como sementes. A lama age no sentido oposto, com adição de partículas finas de sodalita, e quantidade significativa de goethita.
Em suma, a maioria dos trabalhos concorda que a velocidade de sedimentação é afetada pelo tipo e quantidade de minerais de ferro na bauxita e que a presença de goethita muito fina pode gerar problemas para sedimentação da lama vermelha, devido a baixa gravidade específica e alta área superficial desta espécie.
3.7 – Métodos analíticos
Na caracterização tecnológica de minérios, as análises mineralógicas são fundamentais para a identificação das fases constituintes, determinação das propriedades, texturas e associações entre as mesmas. Dessa maneira, são de suma importância as técnicas analíticas que permitam a quantificação das espécies minerais, viabilizando a determinação da composição mineral, mesmo que de forma estimada, e se possível do grau de liberação do mineral de interesse em relação a ganga (Sant’Agostino & Kahn, 1997).
3.7.1 Difração de raios X
para identificar os minerais e para determinar quantidades desses minerais. A técnica do método do pó envolve a montagem de uma pequena quantidade de pó em um porta amostras especial para essas análises. Os resultados dessas análises são difratogramas nos quais os picos dos minerais se distinguem do ‘background”. Esses picos no difratograma são lidos por um software de interpretação (no nosso caso HighScore Plus) que busca os minerais, com os picos próximos dos encontrados na análise, no banco de dados do ICDD (International Center Data Diffraction).
A radiação emitida pela amostra é difratada pelos planos da rede cristalina (com espaçamento conhecido d ) do cristal. De acordo com a lei de Bragg (nλ = 2d sen θ) a
radiação de um único comprimento de onda é difratada para cada posição angular do cristal e a intensidade desta radiação pode ser medida.
Antoniassi (2010) tentou quantificar os minerais de bauxita pelo método de Rietveld porém a autora encontrou limitações na quantificação dos minerais de ferro, e isso provavelmente ocorreu devido ao alargamento da goethita consequente da substituição isomórfica (modificação na estrutura cristalina) e/ou efeito de pequeno tamanho de cristal.
Devido a essas limitações na quantificação, optou-se por utilizar os resultados de difração de raios X apenas para identificar os minerais nas amostras analisadas. A quantificação das fases será feita através da combinação dos resultados das outras técnicas utilizadas.
3.7.2 - Microscopia
A utilização de microscopia ótica é limitada, pois como trata-se um minério de origem supergênica, esse é constituído essencialmente por minerais de pequeno tamanho de cristal.
possibilita a distinção entre hematita e goethita.
No MEV (Microscopia Eletrônica de Varredura) um feixe fino de elétrons de alta energia incide na superfície da amostra, parte do feixe é refletido e coletado por um detector que converte este sinal em imagem. Há uma interação entre o feixe incidente e a superfície analisada, e uma das consequências dessa interação é a produção de raios X que fornecem a composição química elementar de um ponto ou região da superfície, possibilitando a identificação de elementos com número atômico acima do sódio presentes nas amostras.
3.7.3 - Espectroscopia Mössbauer
A espectroscopia Mössbauer, quando comparada às outras técnicas espectroscópicas, é considerada uma das que tem a mais simples e barata coleta de dados (Vanderbergue, 1991). Uma grande vantagem dessa técnica é que a presença de outros elementos na amostra não alteram sua análise. É amplamente utilizada em mineralogia para examinar o estado de valência do ferro, que é encontrado na natureza como Fe0 (metal), Fe2+ e Fe3+, bem como o tipo de poliedro de coordenação ocupados por átomos de ferro (trigonal, tetraédrica , octaédrica, etc.)
A espectroscopia Mössbauer é também utilizada para auxiliar na identificação das fases de óxido e hidróxido de ferro em função das suas propriedades magnéticas. Esta técnica envolve a emissão e absorção sem recuo de raios gama. No modo de transmissão, uma fonte (57Co para espectros de ferro) que emite raios gama é movida, e a radiação transmitida pela amostra é registrada em função da velocidade da fonte. A espectroscopia Mössbauer é uma ferramenta poderosa para determinar e quantificar as fases de ferro no minério de bauxita, fornecendo informações complementares àquelas obtidas na difração de raios X. Além disso, tem o potencial de detectar as fases amorfas e de pequenos tamanhos de cristalito que podem não ser identificadas por DRX (Kirwan
et. al, 2009).
um equipamento de amplificação e separação para aquisição de dados e o dispositivo de armazenamento, como um analisador multicanal (Figura 9).
Figura 9- Diagrama de bloco de um espectrômetro Mössbauer (adaptado de Vanderbergue,
1991).
O efeito Mössbauer é uma técnica de absorção ressonante de radiação nuclear sem recuo, e foi descoberta em 1957 durante o trabalho de doutorado de R.L. Mössbauer. Um sistema quantizado, depois de ser excitado, pode voltar ao seu nível do inicial, emitindo radiação eletromagnética. Esta radiação é capaz de excitar um sistema similar. A perda de excitação da radiação incidente é observada. Este fenômeno é chamado de absorção ressonante e encontra aplicação em vários técnicas de espectroscopia. Neste caso a radiação emitida e absorvida é composta de luz visível/ultra violeta e o sistema quantizado tem origem nos níveis eletrônicos dos átomos (Vanderberghe 1991).
Os espectros Mössbauer são obtidos a partir das interações hiperfinas entre os núcleos e seus ambientes de ressonância elétrica e magnética, e são caracterizados por três parâmetros principais: desvio isomérico (δ); desdobramento quadrupolar (ΔEQ) e interação magnética hiperfina(HHF).
eletrônica dentro da região nuclear;
Desdobramento quadrupolar ocorre para estados nucleares com spin I > ½ que têm um momento quadrupolar Q que pode interagir com o campo elétrico local, removendo parcialmente a degenerescência dos níveis nucleares;
Interação magnética hiperfina é interação do momento de dipolo magnético nuclear com um campo magnético Hhf atuando no núcleo, removendo a degenerescência dos níveis nucleares;
A informação a respeito do estado de oxidação é obtida principalmente do valor do desvio isomérico. O ferro ocorre em dois estados de oxidação principais (+2 e +3), mas existem casos com estados de oxidação intermediários (magnetita). O valor do deslocamento isomérico para Fe3+ se situa entre 0,3-0,6 mm/s, enquanto para Fe2+ esta entre 0,7-1,2 mm/s.
Os óxidos e oxi-hidróxidos de ferro nos solos geralmente são de pequeno tamanho de partículas. Na espectroscopia Mössbauer estes óxidos de pequeno tamanho resultam num espectro consistindo de um dubleto superparamagnético. A obtenção do espectro em baixas temperaturas usualmente permite uma completa definição. Os óxidos de e hidróxidos de ferro apresentam ordenamento magnético em temperaturas que variam de 77 K para lepidocrocita até 955 K para hematita. A temperatura do ordenamento antiferromagnético é chamado de temperatura de Néel (TN) e a temperatura do ordenamento ferro-magnético é conhecida como temperatura de Curie (TC) (Murad, 1990). A presença de fases de baixa cristalinidade devido a defeitos estruturais e/ou presença de partículas pequenas afeta TN e TC, e portanto, também afeta o espectro Mössbauer.
3.7.4 – Análises térmicas
As análises térmicas são aplicáveis a qualquer tipo de amostra, independentemente do grau de cristalinidade, e são extremamente úteis no estudo de amorfos e materiais altamente desordenados. Existem métodos para melhorar as repostas das análises, como o controle da atmosfera, a extensão da faixa de temperatura, e o emprego de amostras muito pequenas. O potencial dos pré-tratamentos químicos na amostra a ser analisada auxilia em um resultado mais eficaz, como no caso das bauxitas onde pode-se tratar as amostras com o sistema ditionito-citrato-bicarbonato (DCB) para a remoção dos oxi-hidróxidos de ferro. Esta remoção é essencial para impedir a interferência da goethita na quantificação dos minerais de alumínio, como gibbsita, caulinita e boehmita.
4 – MATERIAS E MÉTODOS
4.1 – Preparação das amostras
As amostras utilizadas nesse trabalho foram selecionadas com base no seu conteúdo de ferro, com o intuito de avaliar o comportamento de amostras de baixos e altos teores de ferro na digestão, com ênfase na influência dos minerais portadores deste elemento na etapa de sedimentação.
Tabela 4 - Localização dos pontos de coleta das amostras de minério da MRN.
LOCALIZAÇÃO
ÁREA FAIXA CANALETA X Y
MRN 076 AV4 N 795 199 556807 9814822
MRN 077 AV 12 S 5912 260 556536 9815734
MRN 078 SW 4 3212 134 444360 9806460
MRN 079 SW 5 2944 171 559493 9804983
COORDENADAS DE LOCALIZAÇÃO DAS AMOSTRAS - MRN
NOMENCLATURA
Figura 10 - Localização dos pontos de coleta das amostras na Mineração Rio do Norte.
Tabela 5 - Localização dos pontos de coleta das amostras de minério da MBP.
LOCALIZAÇÃO
BLOCO FAIXA CANALETA X Y
MBP 071 2K 51 5 197938,3 9641973
MBP 072 2E 50 5 197263 9642252
MBP 073 2B 36 2 198801 9641138
MBP 074 B 105 2 197988,6 9637290
MBP 075 I 105 3 198402,3 9637760
NOMENCLATURA
COORDENADAS DE LOCALIZAÇÃO DAS AMOSTRAS RETIRADAS - MBP
As amostras de minério secundário (BN, BNC, BCBA e BA) também foram coletadas em Paragominas (Tabela 6). Elas são parte do perfil de um poço feito especialmente para estudos tecnológicos.
Tabela 6 - Localização dos pontos de coleta das amostras de minério secundário da MBP.
X Y
MBP 0710 BN 9637761 198911
MBP 0711 BNC 9637761 198911
MBP 0712 BCBA 9637761 198911
MBP 0713 BA 9637761 198911
NOMENCLATURA
CLASSIFICAÇÃO DO INTERVALO
COORDENADAS DE LOCALIZAÇÃO DAS
AMOSTRAS RETIRADAS
A amostra de Gana foi coletada em um poço (coordenadas E769146, N691479) no depósito de Kibi, situado na região leste de Gana, a cerca de 90 km de Acra.
Bauxita
Escrubagem
Bauxita lavada
Finos
Testes de sedimentação Licor rico
Lama Vermelha Moagem
Digestão
Análises mineralógicas
DRX, Mössbauer, ATG, MO AT, AA, SiT, SiR, PF,Fe2O3, TiO2
~44%<44um
<37 um
>37um
145, C, 1 hora, A/C = 0.75
90oC, 1L cilindro, HX200, 200g /ton
Análise química
Análise química
Análises mineralógicas
DRX, Mössbauer, ATG, MEV AT, AA, SiT, SiR, Na2O, CaO,
PF, Fe2O3, TiO2
Figura 11 - Fluxograma de análises das amostras utilizadas.
Foram recebidos 250 kg de cada amostra para os testes de digestão, análises químicas e mineralógicas. Dessa massa, 95% foi britada a <1,00mm e o restante foi arquivado.
A escrubagem foi realizada em bentoneiras, e o produto escrubado foi peneirado em 3,36 mm e em 400# (37µm). O passante em 400# foi desaguado, pesado e separado. Do restante do produto lavado, foram retiradas alíquotas para análise química e moagem, além de uma alíquota para análises mineralógicas.
100% < 20# e 40% a 47% <325# (amostras da MRN). Os produtos das moagens foram quarteados para digestão do processo Bayer.
4.2 – Digestão Bayer e determinação da velocidade de sedimentação
Todas amostras foram submetidas ao processo de lixiviação alcalina com licor sintético em autoclave da marca Parr a 145°C, pressão de 5,0 Kgf/cm2 e agitação de 500rpm durante 60min. Uma dosagem de cal de 2,63 kg/ton, que equivale a 0,25% da massa de bauxita foi adicionado com a finalidade de precipitar o fósforo presente na bauxita sob a forma de apatita (Ca5(PO4,CO3)3(OH)).
Após decorrido o tempo do ensaio de digestão descarregou-se o reator lentamente, retirou-se e transferiu-se a polpa para a cuba de lama vermelha. Quatro alíquotas representativas foram colocadas em quatro provetas de 1L que foram pesadas e transferidas para um Hotbox à temperatura de 90 a 95°C. Adicionou-se em cada
proveta uma massa de floculante (HX 200) equivalente a dosagem de 200g para cada tonelada de lama vermelha que passará pelo processo de sedimentação. Um plunger foi utilizado para garantir a homogeneização. E anotou-se o tempo inicial e final que a amostra demorou para passar entre as marcas de volume de 600 e 700mL da proveta (Figuras 12 e 13).
A equação abaixo foi utilizada para se chegar ao valor da velocidade de sedimentação, uma vez que é esperado que as forças citadas anteriormente agirão da mesma forma em todos os ensaios:
Vsed = hp x (Vi – Vf) x 0.036 (ti – tf)
Onde:
Vsed = velocidade de sedimentação (m/h)
hp – Altura da proveta (1000mL); Vi – Volume inicial (mL);
Vf – Volume final (mL);
Figura 12 – Hotbox utilizado nos testes do CDM.
Figura 13 – Detalhe das provetas dentro do hotbox, após a sedimentação da lama vermelha.
4.3 – Análises químicas
Os teores de Altotal, Si, Fe e Ti foram obtidos por ICP (Inductively Coupled Plasma) em um equipamento marca Spectro, após a fusão com Na2CO3 e Na2B4O7. O resultado das análises químicas é expresso em óxidos.
Foi utilizado um método específico para a determinação do alumínio oriundo da gibbsita, também conhecida como alumina aproveitável, e também para a determinação do silício presente no mineral caulinita, usualmente expresso como sílica reativa. Esse método baseia-se em uma digestão caústica a baixa temperatura. Uma batelada de até 16 amostras, incluindo branco, padrão e duplicata, foi digerida em solução de hidróxido de sódio a 150°C em bombas de 45 mL usando um bloco digestor para aquecer o sistema. A gibbsita dissolve conforme a reação:
O H NaAlO NaOH
OH
Al( )3 22 2
A sílica reativa reage com o hidróxido de sódio e vários ânions tais como sulfato, carbonato, nitrato e cloreto, e precipita na forma da “sodalita” Bayer, abaixo a reação de dissolução da sílica.
O H NaAlO SiO
Na NaOH
O H SiO O
Al2 3.2 2.2 2 6 2 2 3 2 2 5 2
A lama digerida na bomba foi transferida para um balão, e uma alíquota foi filtrada a quente. O alumínio dissolvido foi então complexado com um excesso de CDTA (Cyclohexanediaminetetraacetic Acid trans ou Ácido Ciclohexanodiamino 1,2 Tetraacético)em meio ácido, e este excesso foi titulado com ZnSO4 padrão.
O material insolúvel retido no papel de filtro foi dissolvido com a adição de ácido clorídrico. Após a adição de floculante para aglomerar a lama vermelha, a suspensão foi filtrada e o teor de silício no filtrado foi determinado via ICP.
4.4 – Caracterização Mineralógica
4.4.1 – Difração de raios X
As análises de difração de raios X (DRX) foram realizadas em um difratômetro modelo X´PERT PRO MPD (PW 1775) da PANalytical, equipado com tubo de raios X cerâmico e anodos de Cu (Kα1=1,540598 Å), filtro Kβ de níquel e Co (Kα1=1,789 Å) e detector X’Celerator. As condições instrumentais utilizadas foram: varredura de 3° a
75° em 2θ; voltagem de 40 kV e corrente de 40 mA; tamanho do passo de 0,02° (2θ) e tempo de contagem de 20s; fenda divergente de 1/8º e anti-espalhamento de 1/4º; máscara de 10 mm; amostra em movimentação circular com frequência de 1 rotação/s.
4.4.2 – Espectroscopia Mössbauer
Os espectros Mössbauer foram obtidos à temperatura ambiente (298 K) em um espectrômetro operando com 1024 canais com aceleração constante e um sinal triangular. A calibração de velocidade foi feita com um absorvedor de ferro metálico e os desvios isoméricos são relativos ao α-Fe. Os absorvedores foram preparados misturando-se uma quantidade apropriada da amostra com glucose a fim de se obter cerca de 10 mg de Fe por centímetro quadrado.
Os espectros foram ajustados através dos programas MOSF utilizando Lorentzianas e DIST3E, o qual é baseado em um modelo independente de distribuição dos campos hiperfinos e/ou desdobramentos quadrupolares (Vandenberghe 1991). Os resultados numéricos dos ajustes são reportados como parâmetros hiperfinos, os quais são:
-campo magnético hiperfino (Hhf) que é dado em kOe; -área sub-espectral relativa (S) em %;
-deslocamento e/ou desdobramento quadrupolar (2εQ, ΔEQ) e o desvio isomérico
(δ) dados em mm/s.
Nos casos em que os ajustes foram feitos com o programa DIST3E, os valores de Hhfe ΔEQ reportados são os de máxima probabilidade. Para dubletos, ΔEQ significa o valor do desdobramento quadrupolar.
concentrações de ferro determinados na análise química e pelas áreas relativas dos sextetos e dubletos para cada amostra.
4.4.3 – Análises termogravimétricas
Os ensaios de análises termogravimétrica (ATG) e de análise térmica diferencial (DTA) foram realizados em um aparelho Du Pont SDT2960 entre a temperatura ambiente e 1000 oC, com taxa de aquecimento de 20 oC/min-1 em atmosfera de ar sintético com fluxo de 100 mL. min-1.
As amostras passaram por um pré-tratamento químico, realizado com base no trabalho de Mehra & Jackson (1960). Os autores afirmaram que uma amostra contendo minerais de ferro pode ser deferrificada através do sistema Ditionito-Citrato-Bicarbonato (DCB), onde se reduz o Fe3+ para Fe2+ pelo ditionito e posterior complexação com o citrato em um meio ligeiramente alcalino tamponado pelo bicarbonato. Após a lavagem do resíduo da lixiviação seletiva, realizou-se as análises termogravimétricas. Todas as amostras foram tratadas com DCB no mínimo três vezes para assegurar a extração, mas conforme será mostrado a seguir, uma quantidade significativa de ferro ainda permaneceu em algumas amostras. Essa lixiviação foi feita porque a gibbsita e a goethita perdem água em temperaturas próximas, então se faz necessário a retirada da goethita para se garantir que a perda de água observada próximo a 300oC corresponda a gibbsita.
4.4.4 – Microscopia Eletrônica de Varredura
5 – RESULTADOS
A seguir serão exibidos os resultados das 14 amostras que foram objeto desse trabalho. Serão apresentados os resultados de caracterização mineralógica de nove amostras provenientes de Paragominas (MBP), quatro provenientes da Mineração Rio do Norte – MRN e uma amostra proveniente de Gana.
5.1 – Análise química
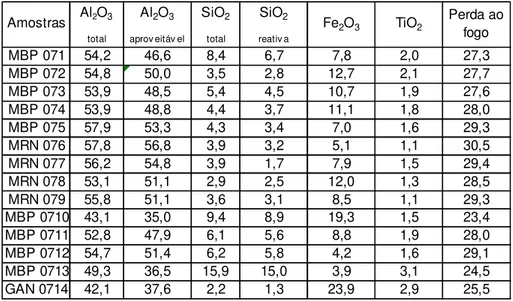
De acordo com os resultados das análises químicas (Tabela 7), as amostras apresentam teores de ferro variando de 5,1 a 12.7% para os minérios da MBP e MRN, e 3.9 a 19.3% para amostras de minério secundário. A amostra de Gana é a que apresenta maior teor de ferro, com 23.9%. Os maiores valores de sílica reativa são os equivalentes aos de minério secundário, e o de alumina aproveitável para as amostras de minério da MRN.
Tabela 7 – Resultados de análises químicas das amostras de bauxita (%).
MBP 071 54,2 46,6 8,4 6,7 7,8 2,0 27,3
MBP 072 54,8 50,0 3,5 2,8 12,7 2,1 27,7
MBP 073 53,9 48,5 5,4 4,5 10,7 1,9 27,6
MBP 074 53,9 48,8 4,4 3,7 11,1 1,8 28,0
MBP 075 57,9 53,3 4,3 3,4 7,0 1,6 29,3
MRN 076 57,8 56,8 3,9 3,2 5,1 1,1 30,5
MRN 077 56,2 54,8 3,9 1,7 7,9 1,5 29,4
MRN 078 53,1 51,1 2,9 2,5 12,0 1,3 28,5
MRN 079 55,8 51,1 3,6 3,1 8,5 1,1 29,3
MBP 0710 43,1 35,0 9,4 8,9 19,3 1,5 23,4
MBP 0711 52,8 47,9 6,1 5,6 8,8 1,9 28,0
MBP 0712 54,7 51,4 6,2 5,8 4,2 1,6 29,1
MBP 0713 49,3 36,5 15,9 15,0 3,9 3,1 24,5
GAN 0714 42,1 37,6 2,2 1,3 23,9 2,9 25,5
TiO2 Perda ao
fogo Amostras Al2O3
total
Al2O3 aprov eitáv el
SiO2 total
SiO2 reativ a
Fe2O3
Tabela 8 - Resultados de análises químicas das amostras de lama vermelha (%.)
MBP 071 LV 25,0 1,7 25,2 18,9 22,2 14,1 0,9 4,8 8,2
MBP 072 LV 14,2 1,8 13,4 10,9 48,3 7,8 1,2 7,4 6,5
MBP 073 LV 19,1 1,8 18,9 14,9 35,6 11,0 1,0 6,2 6,9
MBP 074 LV 17,8 1,9 16,6 14,0 40,4 9,9 1,1 5,8 7,4
MBP 075 LV 19,3 1,6 20,0 16,9 33,2 11,6 1,4 6,8 6,9
MRN 076 LV 21,5 1,3 22,7 19,4 26,7 13,3 1,6 6,0 7,7
MRN 077 LV 10,6 1,2 19,3 7,4 46,6 5,2 1,6 8,7 6,1
MRN 078 LV 14,2 1,5 12,9 10,7 50,5 7,7 1,2 5,8 6,4
MRN 079 LV 17.8 1,8 16,8 15,3 39,9 10,7 1,3 5,3 6,9
MBP 0710 LV 21,6 1,2 18,4 17,8 35,6 11,0 0,5 2,6 7,7
MBP 0711 LV 22,0 < 1,14 19,7 19,1 27,1 12,3 0,9 6,2 8,0 MBP 0712 LV 24,8 < 1,14 24,2 23,1 18,4 14,6 1,1 4,6 8,1 MBP 0713 LV 30,2 < 1,14 29,7 27,7 6,1 17,3 0,5 3,8 8,5
GAN 0714 LV 18,3 5,4 4,9 3,7 51,8 6,0 7,7 6,8 11,9
NaO2 CaO TiO2 Perda ao fogo Lama Vermelha Al2O3
total
Al2O3 aproveitável
SiO2 total
SiO2
reativa Fe2O3
Observa-se um aumento significativo nos teores de ferro e de sílica, às expensas da diminuição dos teores de alumínio. A amostra de Gana é a mais rica em alumina aproveitável, indicando uma ineficiência no processo Bayer.
5.2 – Difração de raios X
Position [°2Theta] (Copper (Cu))
10 20 30 40 50
0 10000 20000 0 10000 20000 0 10000 20000 30000 0 10000 20000 0 20000 40000 Hem Gib Cau MBP 071 Cau Goe Hem Gib Cau MBP 072 Hem Gib Cau MBP 073 Gib Cau MBP 074 Gib Gib Gib Gib Ana Ana Goe Cau
Posição[2 teta] (t ubo de Cobre) Cont agem MBP 075 Cau Gib Gib Cau Hem Cau Ana
Figura 14 - Difratogramas de raios X das amostras MBP. Caulinita (Cau); gibbsita (Gib);
goethita (Goe); hematita (Hem) e anatásio (Ana).
Position [°2Theta] (Copper (Cu))
10 20 30 40 50
0 20000 40000 60000 0 20000 40000 60000 0 10000 20000 30000 40000 0 50000 100000 Gib MRN 076 Gib Gib Hem Gib Ana MRN 077 MRN 078 MRN 079 Gib Gib Gib Gib
Posição[2 teta] (tubo de Cobre) Contagem
Figura 15 - Difratogramas de raios X das amostras MRN. Gibbsita (Gib); hematita (Hem) e anatásio (Ana).
identificou-se sodalita, hematita, goethita, gibbsita e anatásio, e subordinadamente calcita e rutilo. Os minerais majoritários nesse caso, são a sodalita, hematita e a goethita. As amostras são similares porém as amostras MBP 071 LV, MBP 074 LV e MBP 075 LV apresentaram gibbsita, indicando uma ineficiência na digestão Bayer. Todas amostras de lama vermelha da MRN são bem similares, com exceção da amostra MRN 078 LV que apresentou hydrotalcita (Mg6Al2(CO3)(OH)16•4(H2O)).
Position [°2Theta] (Copper (Cu))
10 20 30 40 50
0 2000 4000 0 1000 2000 3000 0 1000 2000 3000 0 1000 2000 3000 0 1000 2000 3000 4000 Goe Hem Ana Hem Hem Sod Goe Hem Ana Hem Hem Sod
Goe Ana Hem
Hem Hem
Sod
Goe Ana Hem
Hem Hem Sod Goe Hem Ana Hem Hem Sod
MBP 071 LV
MBP 072 LV
MBP 073 LV
MBP 074 LV
MBP 075 LV
Zir
Zir
Zir
Cal Sod Ana
Cal Cal Cal Cal Sod Ana Sod Ana Sod Ana Sod Ana Qz
Posição[2 teta] (t ubo de Cobre) Contagem
Figura 16 - Difratogramas de raios X das amostras de lama vermelha do minério da MBP.
Sodalita (Sod); goethita (Goe); hematita (Hem); gibbsita (Gib); quartzo (Qz); calcita (Cal) e