CENTRO DE TECNOLOGIA
DEPARTAMENTO DE ENGENHARIA QUÍMICA
PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA – PPGEQ
DISSERTAÇÃO DE MESTRADO
MODELAGEM DA DEGRADAÇÃO DE FENOL EM EFLUENTES
AQUOSOS ATRAVÉS DO PROCESSO DE FOTO-FENTON
Luiz Gonzaga Lopes Neto
Orientador: Osvaldo Chiavone Filho
DISSERTAÇÃO DE MESTRADO
MODELAGEM DA DEGRADAÇÃO DE FENOL EM EFLUENTES
AQUOSOS ATRAVÉS DO PROCESSO DE FOTO-FENTON
Dissertação apresentada ao Programa de Pós-graduação em Engenharia Química da Universidade Federal do Rio Grande do Norte como parte dos requisitos necessários à conclusão do curso de Mestrado.
Orientador: Osvaldo Chiavone Filho. Prof. Ph.D.
Catalogação da Publicação na Fonte. UFRN / CT / DEQ
Biblioteca Setorial “Professor Horácio Nícolás Sólimo”.
Lopes Neto, Luiz Gonzaga.
Modelagem da degradação de fenol em efluentes aquosos através do processo de foto-fenton / Luiz Gonzaga Lopes Neto. - Natal, 2016.
94 f.: il.
Orientador: Osvaldo Chiavone Filho. Coorientador: André Luís Novais Mota.
Dissertação (Mestrado) - Universidade Federal do Rio Grande do Norte. Centro de Tecnologia. Departamento de Engenharia Química. Programa de Pós-graduação em Engenharia Química.
1. Processos fotoquímicos - Dissertação. 2. Fenol - Dissertação. 3. Fotodegradação - Dissertação. 4. Efluentes industriais - Dissertação. 5. Redes neurais - Modelagem - Dissertação. I. Chiavone Filho, Osvaldo. II. Mota, André Luís Novais. III. Universidade Federal do Rio Grande do Norte. IV. Título.
i
Aos meus pais, Rosineide Soares e Luiz Lopes pelo apoio e dedicação de sempre, e pela educação moral imprescindível a meu crescimento.
Ao Professor Osvaldo Chiavone Filho pela orientação e companheirismo durante a realização deste trabalho.
Ao Professor André Mota por grande parte do conhecimento adquirido nesta jornada e pelos excelentes conselhos e sugestões para melhoria deste trabalho.
À minha família, irmãos, tios, primos e sobrinhos por todo auxílio emocional e por todas as palavras de carinho e motivação.
Aos amigos da Universidade, Iêda Mendes, Jéssica Câmara, Millene Caroline, Roger Williams e Tahyná Barbalho por estarem sempre presentes, mesmo distantes fisicamente.
Aos amigos Daniel Serafim, Débora Forte, Lorena Barbalho, Lucas Oliveira, Pedro da Silva, Thiego Moreira e Wallace Barros por estarem sempre dispostos a me ouvir e me auxiliar. A Joatã Soares por toda paciência e carinho, e por sempre ter me motivado a seguir em frente, mesmo nas piores circunstâncias.
À equipe de técnicos e trabalhadores do Núcleo de Ensino e Pesquisa em Petróleo e Gás, sobretudo Neide, Maria, Cristiane, Tayronne e Paulino por todo apoio prestado dentro do laboratório.
A Patrícia Puglia, Celyna Rackov, Daladiê Barreto e Francisco Sousa por toda a ajuda na etapa experimental e de análises, fundamental ao bom andamento deste trabalho.
À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES) e ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) pelo auxílio financeiro prestado em diversas etapas deste trabalho.
À toda equipe do Programa de Pós-Graduação em Engenharia Química da UFRN pelo auxílio prestado e pela eficiência na resolução dos problemas enfrentados.
ii
LOPES NETO, L. G. - Modelagem da Degradação de Fenol em Efluentes Aquosos Através do Processo de Foto-Fenton. Dissertação de Mestrado, UFRN. Programa de Pós-Graduação em Engenharia Química. Área de concentração: Engenharia Ambiental, Natal/RN, Brasil.
RESUMO: Os processos oxidativos avançados (POA) são técnicas que envolvem a formação de radicais hidroxila (HO•) com grande poder de oxidação de matéria orgânica. Esses processos têm encontrado cada vez mais aplicação na indústria por serem capazes de degradar substâncias recalcitrantes que não são removidas completamente por processos tradicionais de tratamento de efluentes. Nesse trabalho, estudou-se a modelagem da degradação do fenol pelo processo de foto-Fenton, baseado na adição de H2O2, Fe2+ e radiação luminosa. Um planejamento
experimental foi desenvolvido para analisar os efeitos das concentrações de fenol, H2O2 e Fe2+
na fração de carbono orgânico total (COT) degradada. Os experimentos foram realizados em um reator fotoquímico parabólico em batelada com 1,5 L de capacidade. Amostras do meio reacional foram retiradas em diferentes tempos de reação e analisadas em um medidor de COT da Shimadzu (TOC-VWP). Os resultados encontrados mostram efeito negativo da concentração de fenol, e positivo das outras duas variáveis na fração de COT degradado. Uma análise estatística do planejamento mostrou que a concentração de peróxido de hidrogênio era também a variável mais influente na fração de COT degradada em 45 minutos e gerou um modelo com R² = 0,82, que previu os pontos experimentais com pouca precisão. Utilizou-se o Visual Basic
for Applications para gerar um modelo por redes neurais e um banco de dados fotoquímicos.
Esse modelo apresentou R² = 0,96 e previu com precisão os valores de resposta utilizados para teste. Os resultados encontrados indicam a possível aplicação da ferramenta desenvolvida para indústria, principalmente pela simplicidade, baixo custo e facilidade de acesso ao programa.
PALAVRAS-CHAVE: fenol; foto-Fenton; tratamento de efluentes; modelagem; redes neurais artificiais; processos oxidativos avançados.
iii
LOPES NETO, L. G.–Modelling of Phenol Degradation in Aqueous Effluents by the Process of photo-Fenton. Thesis, UFRN. Programa de Pós-Graduação em Engenharia Química. Concentration area: Environmental Engineering, Natal/RN, Brazil.
ABSTRACT: Advanced Oxidation Processes (AOP) are techniques involving the formation of hydroxyl radical (HO•) with high organic matter oxidation rate. These processes application in industry have been increasing due to their capacity of degrading recalcitrant substances that cannot be completely removed by traditional processes of effluent treatment. In the present work, phenol degrading by photo-Fenton process based on addition of H2O2, Fe2+ and luminous
radiation was studied. An experimental design was developed to analyze the effect of phenol, H2O2 and Fe2+ concentration on the fraction of total organic carbon (TOC) degraded. The
experiments were performed in a batch photochemical parabolic reactor with 1.5 L of capacity. Samples of the reactional medium were collected at different reaction times and analyzed in a TOC measurement instrument from Shimadzu (TOC-VWP). The results showed a negative effect of phenol concentration and a positive effect of the two other variables in the TOC degraded fraction. A statistical analysis of the experimental design showed that the hydrogen peroxide concentration was the most influent variable in the TOC degraded fraction at 45 minutes and generated a model with R² = 0.82, which predicted the experimental data with low precision. The Visual Basic for Application (VBA) tool was used to generate a neural networks model and a photochemical database. The aforementioned model presented R² = 0.96 and precisely predicted the response data used for testing. The results found indicate the possible application of the developed tool for industry, mainly for its simplicity, low cost and easy access to the program.
KEY WORDS: phenol; photo-Fenton; effluent treatment; modelling; artificial neural networks; advanced oxidation processes.
1 Introdução ... 2
1.1 Objetivo Geral ... 4
1.2 Objetivos Específicos... 4
2 Aspectos teóricos ... 6
2.1 Processos Oxidativos Avançados ... 6
2.1.1 Sistema H2O2/Radiação UV ... 8
2.1.2 Sistema O3/Radiação UV ... 9
2.1.3 Sistema com reagente de Fenton e radiação (foto-Fenton) ... 10
2.2 Fenol ... 12
2.3 Degradação do fenol pelo processo de foto-Fenton ... 13
2.4 Modelagem de processos fotoquímicos ... 15
2.4.1 Redes Neurais ... 16
2.4.1.1 O perceptron ... 17
2.4.2 Modelos semi-empíricos ... 22
2.4.3 Modelos fenomenológicos ... 24
3 Estado da arte... 29
3.1 Processos oxidativos avançados ... 29
3.2 Degradação do fenol por POA ... 30
3.3 Modelagem da degradação em reatores fotoquímicos ... 32
3.3.1 Modelagem por redes neurais artificiais ... 32
3.3.2 Modelos de emissão de luz... 33
4 Metodologia ... 36
4.1 Planejamento experimental ... 36
4.2 Tratamento estatístico ... 38
4.4 Actinometria ... 40
4.5 Desenvolvimento do algoritmo de redes neurais ... 42
4.6 Desenvolvimento do banco de dados fotoquímicos... 48
5 Resultados e Discussões ... 51
5.1 Degradação fotoquímica ... 51
5.1.1 Efeito da concentração de fenol ... 52
5.1.2 Efeito da concentração de íons Fe2+ ... 54
5.1.3 Efeito da concentração de peróxido de hidrogênio ... 55
5.2 Actinometria ... 57
5.3 Modelo estatístico ... 57
5.4 Desenvolvimento de modelo empírico por redes neurais artificiais ... 62
5.4.1 Testes do algoritmo de treinamento ... 62
5.4.1.1 Análise de sensibilidade para o número de neurônios ... 65
5.4.1.2 Análise de sensibilidade para a taxa de aprendizagem ... 67
5.4.2 Aplicação ao planejamento ... 68
5.4.3 Modelo global para o reator parabólico ... 71
5.4.4 Banco de dados fotoquímicos ... 72
6 Conclusões ... 76
Figura 2.1 - Estrutura química do fenol. ... 12
Figura 2.2 - Reação de adição eletrofílica. Fonte: Nogueira et al. (2007). ... 14
Figura 2.3 - Esquema do mecanismo de mineralização do fenol (Fonte: Mota, 2010). ... 15
Figura 2.4 - Esquema de funcionamento de um neurônio artificial. ... 16
Figura 2.5 - Exemplo de uma rede neural artificial com duas camadas ocultas. ... 17
Figura 2.6 - Esquema para obtenção da taxa local volumétrica de absorção de energia. Fonte: Alfano et al. (1985). ... 25
Figura 4.1 - Esquema de montagem do reator fotoquímico utilizado nos experimentos...39
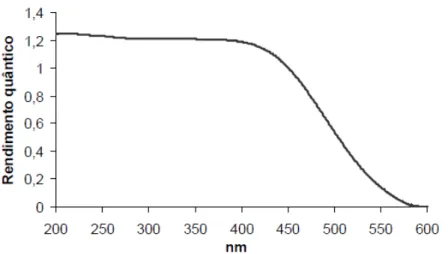
Figura 4.2 - Distribuição espectral da lâmpada utilizada no reator fotoquímico. Fonte: OSRAM SYLVANIA LTD (ecom.sylvania.com). ... 41
Figura 4.3 - Rendimento quântico para formação de Fe2+ a partir de [Fe(C 2O4)3]3+. Fonte: Mota (2005). ... 42
Figura 4.4 - Formulário desenvolvido em VBA que funciona como interface entre o usuário e o algoritmo de treinamento de redes neurais. ... 43
Figura 4.5 - Fluxograma de funcionamento do algoritmo de treinamento desenvolvido. ... 47
Figura 4.6 - Fluxograma de funcionamento do programa desenvolvido em VBA. ... 48
Figura 4.7 - Fluxograma de funcionamento do banco de dados desenvolvido em VBA. ... 49
Figura 5.1 - Perfil da fração de COT degradada para os níveis superior e inferior de concentração de fenol, com [Fe2+] = 2,5 mM e [H 2O2] = 200 mM. ... 53
Figura 5.2 - Perfil de COT para os níveis superior e inferior de concentração de fenol, com [Fe2+] = 2,5 mM e [H 2O2] = 200 mM. ... 53
Figura 5.3 - Perfil da fração de COT degradada para os níveis superior e inferior de concentração de íons ferrosos, com [Fenol] = 1000 ppm e [H2O2] = 200 mM. ... 54
Figura 5.4 - Perfil de COT para os níveis superior e inferior de concentração de íons ferrosos, com [Fenol] = 1000 ppm e [H2O2] = 200 mM. ... 55
Figura 5.5 - Perfil da fração COT degradada para os níveis superior e inferior de concentração de peróxido de hidrogênio, com [Fe2+] = 2,5 mM e [Fenol] = 1000 ppm. ... 56
Figura 5.6 - Perfil de COT para os níveis superior e inferior de concentração de peróxido de hidrogênio, com [Fe2+] = 2,5 mM e [Fenol] = 1000 ppm. ... 56
Figura 5.7 – Superfície de resposta para [Fe2+] e [Fenol], com [H 2O2] = 200 mM. ... 58
Figura 5.8 - Superfície de resposta para [H2O2] e [Fenol], com [Fe2+] = 2,5 mM ... 58
Figura 5.10 - Gráfico de Pareto para os efeitos das variáveis de entrada. ... 60 Figura 5.11 - Valores preditos pelo modelo versus valores experimentais. ... 61
Figura 5.12 - Valores preditos pelo modelo versus valores experimentais para os dados de
Mota (2005). ... 63 Figura 5.13 - Valores preditos pelo modelo versus valores experimentais para os dados de
Mota (2010). ... 65 Figura 5.14 - Valores preditos versus valores experimentais para diferentes quantidades de
neurônios ocultos. ... 66 Figura 5.15 - Valores preditos versus valores experimentais para diferentes taxas de
aprendizagem. ... 67 Figura 5.16 - Valores preditos versus valores experimentais para a série de treinamento e
para os pontos de teste. ... 70 Figura 5.17 - Erro relativo do modelo para cada experimento da série... 71 Figura 5.18 - Valores preditos versus valores experimentais para a série de treinamento e
Tabela 2.1 - Potencial de oxidação de alguns oxidantes. ... 7
Tabela 2.2 - Sistemas típicos de processos oxidativos avançados. ... 8
Tabela 2.3 - Alguns modelos de emissão de radiação e seus autores. ... 27
Tabela 4.1 - Níveis das variáveis para o planejamento composto central. ...36
Tabela 4.2 - Condições experimentais do planejamento composto central. ... 37
Tabela 5.1 - Resultados obtidos durante a execução do planejamento experimental... 51
Tabela 5.2 - Níveis utilizados para a parte fatorial do planejamento. ... 52
Tabela 5.3 – Análise de variância do modelo encontrado (ANOVA) ... 61
Tabela 5.4 - Resultado do treinamento para os dados presentes em Mota (2005). ... 62
Tabela 5.5 - Parâmetros utilizados no treinamento dos dados de Mota (2005). ... 63
Tabela 5.6 - Resultado do treinamento para os dados presentes em Mota (2010). ... 64
Tabela 5.7 - Coeficientes de determinação para diferentes quantidades de neurônios ocultos. ... 66
Tabela 5.8 - Coeficientes de determinação para diferentes taxas de aprendizagem. ... 67
Tabela 5.9 - Resultados do treinamento para o planejamento realizado. ... 69
Tabela 5.10 - Previsão do modelo obtido para os pontos de teste. ... 69
COT – Carbono orgânico total
CONAMA – Conselho Nacional do Meio Ambiente TOC – Total organic carbon
POA – Processo oxidativo avançado RNA – Rede Neural Artificial HO• - Radical hidroxila UV – Ultravioleta
VBA –Visual Basic for Applications
hv– Radiação luminosa
x – Entrada individual de uma rede neural
X – Matriz de entrada para todas as variáveis e experimentos em uma rede neural w – Peso individual ligando os neurônios de entrada aos neurônios da camada oculta b –Bias proveniente da camada de entrada de uma rede neural
W1 – Matriz com todos os pesos e bias que ligam a camada de entrada à camada oculta
u – Somatório em um neurônio oculto
U1 – Matriz com os somatórios de todos os neurônios da camada oculta, para todos os
experimentos
Y1 – Matriz com os resultados gerados nos neurônios ocultos
w’ – Peso individual ligando os neurônios ocultos aos neurônios da camada de saída em uma
b’ – Bias proveniente da camada oculta de uma rede neural
W2 - Matriz com todos os pesos e bias que ligam a camada oculta à camada de resposta
u’ – Somatório em um neurônio de resposta de uma rede neural
U2 – Matriz com os somatórios em todos os neurônios da camada de resposta, para todos os
experimentos
Y2 – Matriz com os resultados gerados nos neurônios de resposta
Yexp– Valores experimentais utilizados para o treinamento da rede neural
Err – Erro quadrático entre os valores experimentais e os valores calculados durante o treinamento da rede neural
Eac – Erro acumulado para todos os experimentos da série de treinamento da rede neural N – Número de experimentos de uma série utilizada para treinamento
nrpt – Número de respostas de uma série de experimentos aplicada a uma rede neural η – Taxa de aprendizagem
I – Intensidade de radiação (einstein.m-2.s-1.sr-1)
Ω – Ângulo sólido (sr)
ν – Frequência (s-1)
s – Coordenada linear (m) t – Tempo (s)
ν– Coeficiente de absorção volumétrica (m-1)
σν – Coeficiente de espalhamento volumétrico (m-1)
jνe– Taxa de emissão de radiação (einstein.m-3.s-1.sr-1)
eνa– Taxa local volumétrica de absorção de energia radiante (einstein.m-3.s-1)
[Fenol] – Concentração de fenol (ppm)
[H2O2] – Concentração de peróxido de hidrogênio (mM)
[Fe2+] – Concentração de íons ferrosos (mM)
Linc– Potência radiante incidente (W)
nF +- Taxa de formação de íons ferrosos (mol.s-1)
Se, – Potência relativa da lâmpada
A – Absorção espectral da solução Φ – Rendimento quântico
T – Transmitância do tubo E – Energia de um fóton (J) P0 – Taxa de incidência (fótons.s-1)
h – Constante de Planck (6,62.10-34 m².kg.s-1)
c – Velocidade da luz (3.108 m.s-1)
– Comprimento de onda (nm)
Sub índices:
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 2
1 Introdução
Assunto de grande interesse da indústria atual, os impactos ambientais vêm gerando um grande número de estudos e esforços no sentido de reduzir emissões, tratar efluentes e promover modificações em busca de processos mais limpos e sustentáveis. A crescente preocupação e o aumento da regulamentação por parte dos órgãos ambientais têm feito com que novas estratégias sejam desenvolvidas e, pouco a pouco, melhoram-se as perspectivas, promovem-se procedimentos cada vez mais eficientes.
Nesse contexto - há cerca de 30 anos – desenvolvem-se métodos para tratamento de efluentes baseados na degradação de poluentes orgânicos utilizando radicais com alto poder oxidante, com aumento sensível de eficiência através da adição de radiação luminosa. Estes são chamados de processos oxidativos avançados (POA) com radiação ou processos de fotodegradação. Essa é, de maneira geral, uma estratégia bastante eficiente, o que permite sua aplicação para um grande número de substâncias orgânicas.
A fotodegradação tem se mostrado uma estratégia viável na vertente de tratamento de efluentes e pode ser utilizada para complementar tratamentos convencionais, quando é necessário degradar completamente ou quase completamente um componente orgânico recalcitrante em substrato, transformando-o em substâncias menores não tóxicas, de baixa toxicidade ou de tratamento mais fácil.
O fenol é um composto orgânico de alta toxicidade encontrado em efluentes provenientes das indústrias de processamento de borrachas, colas e adesivos, resinas impregnantes, componentes elétricos, siderúrgicas, entre outras. Existem diversos métodos de tratamento físicos, químicos e biológicos que promovem uma retirada eficaz desse poluente, tendo a fotodegradação um espaço de destaque, na medida em que permite a transformação do fenol em compostos menos nocivos com elevada eficiência. Apresenta assim a vantagem da alta degradação aliada à não existência de problemas posteriores ligados à presença do fenol em outra matriz – como ocorre, por exemplo, em processos de adsorção.
Dentre diversos processos oxidativos avançados estudados, um apresenta resultados mais satisfatórios na degradação do fenol: o processo de foto-Fenton. Baseado na utilização de íons de Fe2+ e H
2O2 como reagentes, e em presença de luz, esse procedimento produz radicais
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 3 Entretanto, alguns estudos já mostram que a luz solar pode ser utilizada como alternativa à lâmpada UV, o que oferece uma economia maior para valores de eficiência semelhantes, principalmente em locais com abundância de luz solar durante o ano todo.
Com relação ao substrato, sendo o fenol um composto presente em efluentes de diversos tipos de indústria, e considerando a alta eficácia de sua degradação pelo processo de foto-Fenton, fica evidente o interesse industrial para estudos focados nesse aspecto. Uma vez que a luz solar pode ser utilizada como alternativa às lâmpadas de luz ultravioleta, correspondendo a custos menores, é bastante válido o estudo desse tipo de processo, principalmente em lugares com intensa incidência de luz durante todo ano, como é o caso de Natal e diversas outras cidades no Rio Grande do Norte e no Nordeste do Brasil.
Em paralelo aos problemas e busca de soluções nas questões ambientais, grande importância tem sido dada, nas pesquisas e em processos industriais, à busca de modelos matemáticos representativos de situações reais. Área crescente na Engenharia Química, a Modelagem e Simulação tem permitido reduzir o esforço operacional de plantas industriais ou piloto, facilitar a otimização das condições de processo, economizar tempo e dinheiro, além de auxiliar na reprodução de estudos em diversas áreas. Podem-se destacar dois tipos de modelo representativo: os empíricos, baseados em experimentos, e que geralmente são específicos para aquele tipo de operação; e os fenomenológicos, baseados nas equações e leis físicas de conservação de massa, momento e energia, cuja aplicação se estende a todos os sistemas. A escolha e aplicação de um modelo para um sistema dependem principalmente do grau de complexidade do mesmo e do esforço matemático e computacional associado. De maneira geral, quando a resolução analítica das equações se mostra muito complicada ou não convencional, é preferível optar por um modelo empírico – que não pode ser generalizado, mas é obtido de forma mais simples e representa bem a situação específica estudada.
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 4
1.1 Objetivo Geral
Desenvolver modelos matemáticos para a degradação de substratos fenólicos em meio aquoso através do processo de foto-Fenton homogêneo utilizando um reator com refletores parabólicos funcionando com luz UV.
1.2 Objetivos Específicos
Verificar a influência das variáveis de entrada na degradação do carbono orgânico total num reator fotoquímico;
Verificar o perfil de degradação em diferentes condições operacionais;
Verificar quantitativamente a influência dos parâmetros de entrada utilizando uma ferramenta estatística de tratamento de dados; Desenvolver uma ferramenta de redes neurais artificiais que permita a obtenção de modelos através de dados experimentais;
Analisar a influência dos parâmetros de funcionamento da rede neural na precisão da resposta e no esforço computacional necessário;
CAPÍTULO 2:
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 6
2 Aspectos teóricos
2.1 Processos Oxidativos Avançados
Processos Oxidativos Avançados são definidos como processos de oxidação que geram radicais hidroxila em quantidade suficiente para influenciar o tratamento de água (Glaze et al.,
1987), de solos ou do ar (Mota, 2010). Esses processos apresentam alta eficiência na degradação de matéria orgânica e podem ser classificados de acordo com o mecanismo de geração desses radicais: por meios fotoquímicos (incluindo luz solar), ou sem a utilização de fontes externas de energia (Domènech et al., 2001). Importante esclarecer que a utilização de oxidantes fortes
no tratamento de água é antiga, mas só a partir de 1973 popularizou-se a terminologia de “Tecnologias Oxidativas Avançadas” através de um trabalho que utilizava a combinação entre ozônio e radiação ultravioleta para degradar complexos de cianeto (Teixeira & Jardim, 2004).
Esse tipo de processo apresenta diversas vantagens, conforme listadas por Domènech (2001):
Vantagem das tecnologias avançadas de oxidação
Não transferem o contaminante de fase (como ocorre nos processos de arraste com ar e tratamento com carvão ativado), mas o transformam quimicamente;
Geralmente se obtém a mineralização completa (destruição) do contaminante. Em contrapartida, as tecnologias convencionais, que não utilizam espécies muito fortemente oxidantes, não conseguem oxidar completamente a matéria orgânica;
Usualmente, não geram lama, que por sua vez requerem um processo de tratamento/disposição;
São muito úteis para contaminantes recalcitrantes que resistem a outros métodos de tratamento;
Servem para tratar contaminantes a concentrações muito baixas (por exemplo, ppb);
São ideais para diminuir a concentração de compostos formados por pré-tratamentos alternativos, como a desinfecção;
Geralmente melhoram as propriedades organolépticas da água tratada;
Em muitos casos, consomem muito menos energia do que outros métodos;
Permite transformar contaminantes refratários em produtos tratáveis em seguida por métodos mais econômicos como o tratamento biológico;
Eliminam efeitos sobre a saúde de desinfetantes e oxidantes residuais como o cloro.
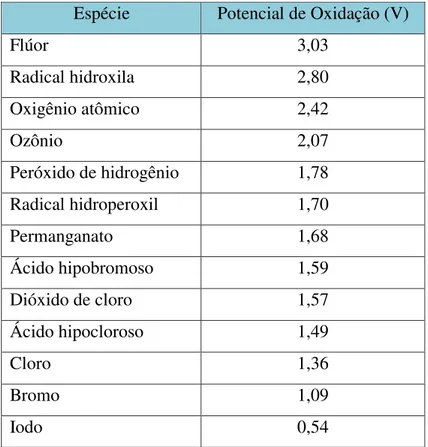
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 7 A alta eficiência desse tipo de processo pode ser justificada pelo elevado potencial de oxidação dos radicais hidroxila formados (Legrini et al., 1993). A Tabela 2.1 mostra o potencial
de oxidação dos principais oxidantes da natureza:
Tabela 2.1 - Potencial de oxidação de alguns oxidantes.
Espécie Potencial de Oxidação (V)
Flúor 3,03
Radical hidroxila 2,80
Oxigênio atômico 2,42
Ozônio 2,07
Peróxido de hidrogênio 1,78
Radical hidroperoxil 1,70
Permanganato 1,68
Ácido hipobromoso 1,59
Dióxido de cloro 1,57
Ácido hipocloroso 1,49
Cloro 1,36
Bromo 1,09
Iodo 0,54
Apesar de apresentar maior potencial de oxidação e fornecer, teoricamente, eficiências mais elevadas na degradação de contaminantes, a aplicação de flúor produz compostos halogenados, comprometendo o uso para um efluente industrial que será lançado em corpo hídrico. Destaca-se também o elevado poder oxidante do ozônio, justificando sua utilização em diversos processos de tratamento e os estudos iniciais de oxidação avançada realizados com essa espécie (Huang et al., 1993).
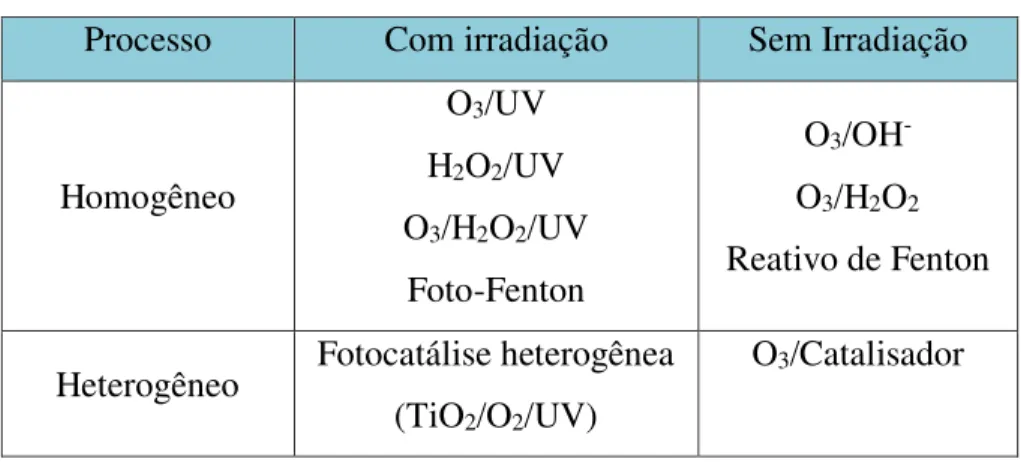
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 8 Tabela 2.2 - Sistemas típicos de processos oxidativos avançados.
Processo Com irradiação Sem Irradiação
Homogêneo
O3/UV
H2O2/UV
O3/H2O2/UV
Foto-Fenton
O3/OH
-O3/H2O2
Reativo de Fenton
Heterogêneo Fotocatálise heterogênea (TiO2/O2/UV)
O3/Catalisador
A seguir, são mostradas algumas das principais tecnologias para degradação fotocatalítica, e seus mecanismos.
2.1.1 Sistema H2O2/Radiação UV
Como destacado anteriormente, os processos oxidativos avançados se caracterizam por produzirem radicais hidroxila, de alto poder oxidante, e cuja geração pode se dar de forma eficiente a partir de sistemas que envolvam peróxido de hidrogênio (H2O2) e radiação
ultravioleta (Fioreze et al., 2014).
O mecanismo mais comumente aceito para a fotólise do H2O2 é a quebra da molécula,
com um rendimento de dois quanta de radicais hidroxila por quantum de radiação absorvida
(Legrini et al., 1993).
H O + ℎ� → HO• (1)
Deve-se atentar também à cadeia de reações que pode ocorrer ao incidir o meio com radiação num comprimento de onda abaixo de 365 nm (Hassemer, 2006):
HO•+ H O → H O + HO• (2)
HO• → H O + O (3)
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 9 Nos processos que utilizam esse tipo de tecnologia, são geralmente utilizadas lâmpadas UV de mercúrio de baixa e média pressão, com emissão máxima em 254 nm, uma vez que a absorção de luz pelo H2O2 se dá de forma mais intensa em 220 nm. Recomenda-se também o
estabelecimento de fluxo turbulento, além da observação das condições do meio reacional, de forma a realizar a operação da maneira mais eficiente (Ruas, 2008).
2.1.2 Sistema O3/Radiação UV
O ozônio é um agente oxidante poderoso e sua aplicação no tratamento de água tem ganhado destaque nos dias atuais, uma vez que esse método não produz compostos clorados que seriam resultantes do tratamento com cloro ou óxido de cloro. Na ausência de luz, o ozônio pode reagir diretamente com o substrato orgânico através de reações lentas e seletivas (Augugliaro et al., 2006):
O + S → S x (5)
Entretanto, o uso do ozônio só é caracterizado como POA quando o mesmo se decompõe para gerar radicais hidroxila (Mota, 2010). Os mecanismos envolvidos são diversos, mas destaca-se a utilização de radiação na obtenção de rendimentos maiores. Legrini et al. (1993)
propuseram dois mecanismos para geração de HO• pela fotólise do ozônio, mostrados nas Equações (6), (7) e (8).
O + ℎ� → O + O D (6)
O D + H O → HO• (7)
O + H O + ℎ� → H O + O (8)
Onde o peróxido de hidrogênio formado reagiria pelo mecanismo já mostrado na Equação (1).
Dentre as aplicações desta técnica, pode-se destacar, além do tratamento de água para consumo, a descontaminação de águas subterrâneas, a remediação de solos (Augugliaro et al.,
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 10 halogenados ou parcialmente halogenados e misturas contendo fenol, ácidos naftênicos, entre outros (Legrini et al.,1993).
2.1.3 Sistema com reagente de Fenton e radiação (foto-Fenton)
O reagente de Fenton consiste numa mistura de peróxido de hidrogênio com íons ferrosos. Na reação de Fenton, a geração de radicais hidroxila é feita por decomposição de H2O2
catalisada por Fe2+ em meio ácido (Teixeira & Jardim, 2004) segundo a Equação (9).
Fe ++ H O → Fe ++ HO•+ HO− (9)
Na ausência de substrato, o radical hidroxila oxida outra molécula de Fe2+:
Fe ++ HO• → Fe + + HO− (10)
Na década de 80, descobriu-se que a irradiação do reagente de Fenton provocava fotorredução dos íons férricos previamente formados, com geração de mais um mol de radical hidroxila (De Brito & Silva, 2012):
Fe ++ H O + ℎ� → Fe ++ H++ HO• (11)
A reação de fotorredução dos íons férricos, também conhecida por reação de foto‐ Fenton, é menos favorecida que a reação de Fenton, com uma constante k=0,02 M-1.s‐1. Na
prática, isso significa que, embora as duas reações ocorram concomitantemente em um meio reacional, há predominância de íons férricos, o que determina que o pH deve ser abaixo de 4,0 para evitar a precipitação de óxi‐hidróxidos férricos (De Brito & Silva, 2012).
Pignatello (1992) demonstra ainda que os íons Fe3+ decompõem cataliticamente o H 2O2
em H2O e O2 segundo um mecanismo de corrente de radical proposto para sistemas simples
contendo íons férricos. Trata-se de um conjunto de reações que envolve o radical HO• e a formação de radicais hidroperoxil (HO•).
Adicionalmente, em solução aquosa, íons férricos existem como aquo-complexos, como por exemplo, [Fe(H2O)6]3+ em pH 0, quando na ausência de outros ligantes. Com o aumento do
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 11
et al., 2007). A Equação (12) apresenta o primeiro equilíbrio de hidrólise, onde estão omitidas
as águas de hidratação.
Fe ++ H O → Fe OH ++ H+ (12)
Os complexos de ferro formados, quando irradiados, sofrem redução, gerando mais radicais hidroxila segundo a Equação (13).
Fe OH ++ ℎ� → Fe ++ HO• (13)
O Fe2+ gerado durante irradiação, quando na presença de peróxido de hidrogênio, reage
com este dando sequência à reação de Fenton (Equação 9). Neste contexto, a reação é catalítica e é estabelecido um ciclo em que Fe2+ é regenerado (Nogueira et al., 2007).
Uma das principais vantagens da utilização do processo de foto-Fenton em comparações com os outros processos oxidativos consiste no aproveitamento da luz solar em seu processo reacional (Mota, 2005). A absorbância de íons férricos pode se estender até a região do visível, dependendo do pH, pois o pH influencia a formação de espécies hidroxiladas, as quais apresentam maior absorção no visível. A espécie Fe(OH)2+ apresenta máximo de absorbância
em comprimento de onda de 300 nm, estendendo-se até aproximadamente 400 nm, o que permite que a irradiação solar seja utilizada na reação foto-Fenton (Nogueira et al., 2007).
Outros aspectos importantes envolvendo o processo de foto-Fenton incluem o cuidado em se trabalhar com a quantidade adequada de oxidante, a fim de impedir um residual de peróxido de hidrogênio, o que representaria custos mais elevados, interferência em análises subsequentes e eventuais perdas de eficiência em tratamentos biológicos posteriores (Teixeira & Jardim, 2004). Pode-se também destacar que reação ocorrer de forma mais eficiente num pH de 3,0, sendo necessário em alguns casos, acidificar o efluente a ser tratado e neutralizá-lo em seguida, adequando-o às condições de descarte. Esse fato pode também aumentar a salinidade e os custos operacionais de tratamento, o que determinaria a aplicação de um processo de foto-Fenton modificado, ou até mesmo de outra técnica de oxidação avançada (Klamerth et al.,
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 12
2.2 Fenol
O fenol (Figura 2.1) é um composto orgânico formado por um anel benzênico ligado a um radical hidroxila. Considerado um sério contaminante do meio ambiente, trata-se de uma substância tóxica que pode ser absorvida por vias orais ou respiratórias, e cuja exposição prolongada pode causar problemas como anorexia, perda progressiva de peso, diarreia, vertigem, salivação excessiva, além de problemas crônicos de sangue e fígado (EPA – EUA, 2000). Seu uso primário na indústria é de matéria-prima na produção de resinas fenólicas e adesivos, mas é também aplicado na manufatura de nylon e resinas de epóxi, na composição de desinfetantes, em produtos médicos, entre outros (PubChem, 2015).
Além de ser usado nas etapas de síntese, o fenol pode também ser encontrado nos efluentes de diversas plantas industriais. Coquearias, produtoras de fármacos, siderúrgicas, refinarias de petróleo, produtoras de papel e celulose, produtoras de resinas e diversos outros tipos de indústrias contém, frequentemente, fenol em seus efluentes (Nolasco, 2009), em concentrações que variam de acordo com as condições operacionais. Pode-se citar os exemplos quantitativos das indústrias de refinaria de petróleo (6-500 mg/L), as coquearias (28-3900 mg/L), as indústrias de processamento de carvão (9-6800 mg/L) e as que manufaturam produtos petroquímicos (2,8-1220 mg/L) (Busca et al., 2008).
Figura 2.1 - Estrutura química do fenol.
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 13 Apesar de se mineralizarem naturalmente em corpos hídricos (TOXNET, 2013), os compostos fenólicos apresentam caráter refratário, sendo bastante resistentes aos métodos de tratamento convencionais (Da Silveira, 2013). O tratamento biológico, por exemplo, é difícil de ser realizado de forma eficiente quando as concentrações de fenol ultrapassam 200 mg/L, uma vez que a toxicidade do composto compromete até mesmo a sobrevivência dos microrganismos (Mishra et al., 1995). Processos físicos como adsorção, por outro lado, geram muitos gastos com recuperação de adsorvente e com a manutenção de valores elevados de temperatura ou pressão (Muranaka, 2010).
Nesse contexto, intensificou-se a busca por alternativas viáveis no tratamento de efluentes fenólicos, tendo os processos oxidativos avançados ganhado cada vez mais destaque na aplicação para mineralização desse e de outros poluentes.
2.3 Degradação do fenol pelo processo de foto-Fenton
Nogueira (2007), de Brito & Silva (2012) e Fioreze (2014) demonstram três mecanismos pelos quais seria possível a degradação de matéria orgânica pelos radicais hidroxila:
Abstração do átomo de hidrogênio:
Os radicais hidroxila formados são capazes de oxidar compostos orgânicos por abstração de hidrogênio, gerando radicais orgânicos (Equação 14). Posteriormente ocorre adição de oxigênio molecular formando radicais peróxido (Equação 15), intermediários que iniciam reações térmicas em cadeia levando à degradação até CO2, água e sais inorgânicos. A
reação por abstração de hidrogênio ocorre geralmente com hidrocarbonetos alifáticos (Nogueira
et al., 2007).
RH + HO• → R•+ H O (14)
R•+ O → RO• (15)
Adição eletrofílica:
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 14 Figura 2.2 - Reação de adição eletrofílica. Fonte: Nogueira et al. (2007).
Transferência eletrônica:
Reações de transferência eletrônica ocorrem quando a adição eletrofílica e abstração de hidrogênio são desfavorecidas, como no caso de hidrocarbonetos clorados (Nogueira et al.,
2007). Esse tipo de reação é mostrado na Equação (16)
RX + HO•→ RX•++ HO− (16)
A oxidação do fenol foi estudada por Zazo et al. (2005), que propôs um mecanismo a
partir da adição eletrofílica da hidroxila ao anel aromático. O esquema da Figura 2.3, proposto por Zazo e modificado por Mota (2010) mostra todas as etapas seguintes, até a total mineralizado do contaminante em CO2, H2O e outros produtos menores.
Huang et al. (1993) e Esplugas et al. (2002)compararam a eficiência dos processos de
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 15 Figura 2.3 - Esquema do mecanismo de mineralização do fenol (Fonte: Mota, 2010).
2.4 Modelagem de processos fotoquímicos
A complexidade do mecanismo reacional de processos fotoquímicos gera imensas dificuldades para a determinação de modelos cinéticos fenomenológicos. Isto ocorre porque o radical hidroxila é não seletivo, dificultando a descrição por modelos que descrevam fenômenos cinéticos simples (Mota, 2005). Nesse contexto, a utilização de redes neurais artificiais (RNA) tem se mostrado uma alternativa eficiente na obtenção de modelos viáveis para diversas aplicações diferentes. Aliados a estudos de otimização através de técnicas de planejamento experimental, autores como Ayodele et al. (2012) e Kasiri et al. (2008) têm obtido resultados
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 16
2.4.1 Redes Neurais
Redes neurais é o nome dado a um conjunto de métodos matemáticos e algoritmos computacionais especialmente projetados para simular o processamento de informações e aquisição de conhecimento do cérebro humano. Operacionalmente podemos considerar uma rede neural como uma “caixa de processamento” que pode ser treinada para que, a partir de um conjunto de dados de entrada (inputs), possa gerar uma ou mais saídas (outputs) (Cerqueira et
al., 2001).
A técnica das redes neurais artificiais para estudos computacionais consiste em unidades de processamento simples chamadas neurônios (Figura 2.4), capazes de aplicar funções
matemáticas simples a dados inseridos como entrada (Miranda Junior, 2011). Cada neurônio fornece, assim, um valor de resposta baseado nas entradas, cujos sinais são propagados através de conexões associadas a pesos específicos, e uma função de ativação aplicada a um somatório ponderado dos valores de entrada (Silva, 1998).
Figura 2.4 - Esquema de funcionamento de um neurônio artificial.
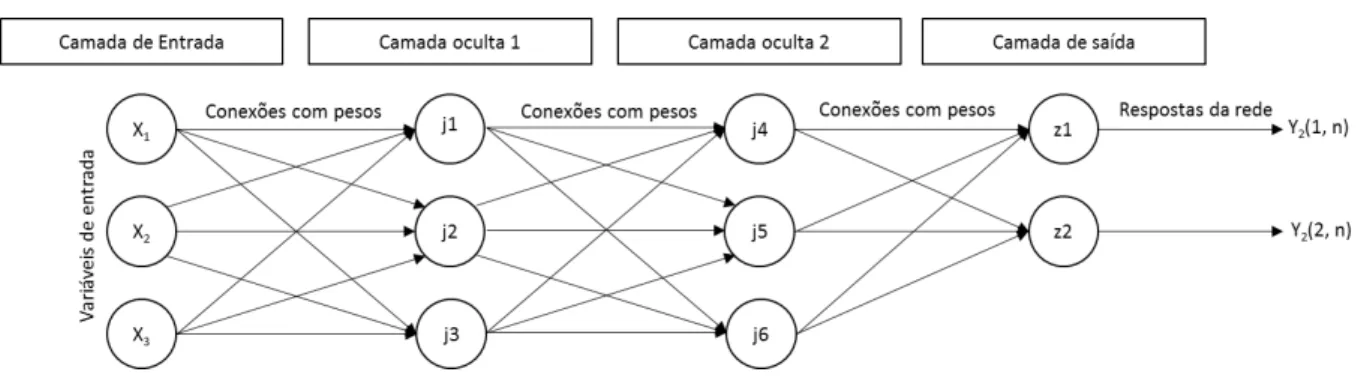
Uma rede neural, portanto, é composta de diversos neurônios artificiais, agrupados em camadas e postos em relação uns com os outros através de ligações paralelas (Figura 2.5). A força dessas interconexões é determinada pelo peso associado aos neurônios (Ayodele et al.,
2012). Para cada RNA, a primeira camada constitui a camada de entrada (variáveis independentes) e a última forma a camada de saída (variáveis dependentes). Entre elas, uma ou mais camadas de neurônios – chamadas camadas ocultas – podem ser localizadas (Kasiri et al.,
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 17 Figura 2.5 - Exemplo de uma rede neural artificial com duas camadas ocultas.
O número de variáveis utilizadas na predição e o número de variáveis a serem preditas são representadas, respectivamente, pelo número de neurônios de entrada e de saída. O grau de exatidão nas predições neurais é uma função do número de neurônios na camada oculta, os quais atuam como detectores de características. Na base da teoria da aproximação universal, com um número suficiente de neurônios, uma rede com uma única cama oculta pode interpretar qualquer estrutura de entrada-saída (Ayodele et al., 2012).
Para que possam representar um conjunto de dados num processo de modelagem, a RNA deve primeiramente passar por um processo de aprendizagem chamado treinamento. O aprendizado é geralmente implementado com ajuda de exemplos e seu processo se realiza com um ajuste iterativo dos pesos associados às conexões (Ding et al., 2013). Três tipos de
treinamento podem ser realizados em uma rede neural (Kumar & Thakur, 2012):
Treinamento supervisionado: nesse tipo de aprendizado, tanto os valores de entrada, quanto valores experimentais de saída são fornecidos à rede. Depois dos cálculos das respostas, os erros entre os valores desejados e obtidos em cada neurônio da camada de saída são utilizados para determinar mudanças nos pesos de acordo com uma regra de aprendizagem;
Treinamento não-supervisionado: para esse tipo de treinamento, as correções para os pesos da rede não são feitas por um agente externo, uma vez que em muitos casos não se sabe que solução se deve esperar. Nesse caso, a própria rede decide qual valor de saída é o melhor para um dado conjunto de valores de entrada, e os reorganiza de forma adequada (Rojas, 1996).
Treinamento por reforço: esse tipo de treinamento se baseia em aprender o que fazer, como mapear situações e ações, de maneira a maximizar um sinal numérico de recompensa. Não é dito à rede os passos específicos a seguir, mas ela os descobre quais ações resultam nos melhores ajustes. Contém, dessa forma, aspectos dos dois outros tipos de treinamento (Sutton & Barto, 2012; Kumar & Thakur, 2012).
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 18 Uma das estruturas mais conhecidas de treinamento supervisionado e de organização neurônios e de RNA, é chamada perceptron (Miranda Junior, 2011). Esse tipo de estrutura pode
ser do tipo monocamada, chamada MCP (Figura 2.4), ou multicamadas, chamada MLP (Figura 2.5). Uma estrutura MCP só é capaz de resolver problemas linearmente separáveis, ou seja, aqueles em que é possível utilizar uma reta ou hiperplano como fronteira de decisão (de Oliveira, 2002; Pádua, 2000). O funcionamento do algoritmo de aprendizagem é mostrado a seguir.
Um conjunto de entradas (matriz X) é inserido na entrada da rede, sendo aplicado aos neurônios artificiais da camada oculta subsequente. Cada variável k de entrada para cada série
de dados i, xk,i é multiplicada por um peso correspondente wi,j e somada para determinar o nível
de ativação do neurônio, este adicionado a um valor limite, conhecido por bias (polarização,
limiar de excitação, threshold) (Mota, 2005), conforme a Equação (17).
u, = ∑ w ,x , + b x
=
A cada neurônio oculto é aplicada uma função de ativação ao somatório, cujo objetivo será gerar uma resposta baseada nos dados de entrada. A escolha de qual função utilizar deve estar de acordo com a distribuição proposta para os dados e deve ser feita com a finalidade de facilitar a interpretação do modelo (Gomes & Ludermir, 2008). Em geral, existem três tipos de função de ativação: a função threshold (Equação 18), que assume valor de 0 ou 1 de acordo
com um limiar estabelecido; a função Linear-Piecewise (Equação 19), que também assume valores de 0 ou 1, mas pode receber valores entre esse intervalo dependendo do fator de amplificação em uma certa região linear; e a função sigmoide, cujos resultados variam no intervalo de 0 a 1 ou de -1 a 1 e pode se apresentar por diferentes expressões, dentre elas a mostrada na Equação (20) (Kumar & Thakur, 2012).
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 19 f u =
{
se u
u − u <
se u < −
f u = + e−
Os valores de saída dos neurônios da camada oculta são utilizados como entrada dos neurônios da camada subsequente, onde será realizada a mesma sequência de comandos, até que se obtenham os valores das respostas.
O algoritmo utilizado no modelo de MLP, chamado de Backpropagation é um tipo de
aprendizado supervisionado cujo critério de convergência é o valor do erro calculado após a geração dos valores de saída (Affonso et al., 2010). O nome recebido se refere à
retro-propagação do erro, da camada de saída até a de entrada, de maneira a ajustar os pesos até que se obtenha a resposta desejada.
A correção dos pesos acontece segundo a minimização do erro quadrático entre os valores calculados e os valores experimentais. Miranda Junior (2011) traz a formulação necessária para a obtenção dos fatores de correção:
Primeiramente, considerando a camada de saída e sua relação com a camada oculta, deseja-se minimizar o erro acumulado em todos os experimentos da série de dados utilizada:
Eac = ∗ ∑ ∑[Err z, i ]
z
Err z, i = Yexp z, i − f ∑ w′,zY j, i + b′z =
Uma vez que se deseja encontrar os valores dos pesos que minimizem o erro acumulado, deve-se procurar o valor da derivada do erro com relação aos pesos. A correção, então, se dá de acordo com esse valor de derivada, levando em conta também uma variável chamada taxa de
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 20 ∆w′,z= −η∂w′∂Eac
,z
Para encontrar o valor do gradiente, basta expandir somente o valor do somatório na Equação (22), pois todos os outros termos do somatório não são afetados pelos valores dos pesos. Pode-se escrever, então:
∂Eac ∂w′,z=
∂Eac ∂Err
∂Err
∂w′,z = Err
∂Err
∂w′,z
∂Eac
∂w′,z = Err
∂
∂w′,z[Yexp z, i − f ∑ w′= ,zY j, i + b′z ]
Finalmente:
∂Eac
∂w′,z= −Err f′ ∑ w′= ,zY j, i + b′z Y j, i
Definindo:
∆z= Err f′ ∑ w′,zY j, i + b′z =
Escreve-se:
∂Eac
∂w′,z= −Y j, i ∆z
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 21 Um procedimento análogo é realizado para a correção dos pesos que ligam a camada de entrada à camada oculta. Na definição do gradiente, entretanto, não se pode omitir o termo do somatório do número de respostas, uma vez que uma alteração nos pesos em questão altera todas as respostas da rede (Miranda Junior, 2011):
∂Eac
∂w , = ∑
∂Eac ∂Err
∂Err ∂w , z
= ∑ Err∂w∂Err
, z
∂Eac
∂w , = ∑ Err
∂
∂w , [Yexp z, i − f ∑ w′= ,zY j, i + b′z ] z
∂Eac
∂w , = − ∑ Err f′ ∑ w′= ,zY j, i + b′z
∂
∂w , ∑ w′= ,zY j, i + b′z z
Substituindo Δz:
∂Eac
∂w , = − ∑ ∆z
∂
∂w , ∑ w′= ,zY j, i + b′z z
∂Eac
∂w , = − ∑ ∆zw′,z
∂Y j, i ∂w , z
Sabendo que Y j, i = f(∑ w ,x , + b ):
∂Eac
∂w , = − ∑ ∆zw′,zf ′ z
(∑ w ,x , + b ) x ,
Finalmente, a expressão para correção dos pesos fica:
∆w , = −η∂w∂Eac
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 22 Os processos de propagação e retro-propagação são então repetidos até que o valor do erro seja mínimo.
2.4.2 Modelos semi-empíricos
A definição da cinética da reação de foto-Fenton foi possível de ser estudada a partir d estabelecimento de um mecanismo envolvendo radicais hidroxila (Wu et al., 2010). Segundo
Ayodele et al. (2012), um processo típico de foto-Fenton envolve três etapas reacionais
principais: a iniciação em cadeia, na qual são formados os radicais hidroxila; a propagação em cadeia, onde os substratos orgânicos serão atacados e degradados; e uma etapa de terminação, na qual os radicais hidroxila são consumidos por outros mecanismos. Cada etapa apresenta uma constante reacional e pode influenciar na expressão da cinética da degradação do contaminante. As reações e constantes reacionais envolvidas na degradação do fenol são mostradas a seguir com base nas reações e constantes cinéticas propostas por Ayodele et al. (2012) e Wu et
al. (2010).
Etapa 1: iniciação em cadeia
Fe + + H O → Fe ++ HO•+ HO− (36)
k1 = 70 M-1.s-1 Etapa 2: propagação em cadeia
C H O + HO•→ CO + H O + Produtos mineirais (37)
k2 depende das condições operacionais (Feng e Le-Cheng, 2004)
HO•+ H O → H O + HO• (38)
k3 = 3,3.107 M-1.s-1
H O + Fe + → Fe ++ HO• + H+ (39)
k4 = 0,01 M-1.s-1
Fe OH + + ℎ� → Fe ++ HO• (40)
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 23 Fe + + HO• → Fe ++ O + H+ (41)
k6 = 1,2.106 M-1.s-1
Etapa 3: terminação
Fe ++ HO•→ Fe ++ HO− (42)
k7 = 3,2.108 M-1.s-1
Fe ++ HO• → Fe ++ HO− (43)
k8 = 1,3.106 M-1.s-1
A velocidade de degradação do fenol seria dada por rC6H6 = k [C H O][HO•] (44).
Os procedimentos propostos por Wu et al. (2010) e Ayodele et al. (2012), utilizando os
mecanismos evidenciados acima, fornecem expressões semelhantes que representam bem a variação de concentração dos componentes estudados. A expressão final obtida está mostrada na Equação (45).
b ln [C H O][C H O] + a [C H O] − [C H O] =c − e−
Os parâmetros a, b e c correspondem às expressões abaixo:
a = k [H O ]
b =k [H O ] + k [Fek k [H O ] +]
c = +
= k [Fe +]
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 24 Os termos entre colchetes representam as concentrações das espécies químicas envolvidas, o sub índice “o” representa a concentração inicial utilizada e t é o tempo de reação. Sendo o HO• um radical livre altamente reativo com um período de vida extremamente curto de nano-segundos, sua concentração é normalmente considerada constante (Wu et al.,
2010). Dessa forma, as equações mostram que a degradação do fenol pelo processo de foto-Fenton depende principalmente das concentrações iniciais de ferro, peróxido de hidrogênio e do substrato, bem como do tempo de reação.
Feng e Le-Cheng (2004) propõem uma abordagem alternativa, considerando dois caminhos possíveis para a mineralização do fenol: um direto e um passando por intermediários tais qual o ácido acético. Três constantes de reação são propostas, cujos valores dependem das condições operacionais. O modelo proposto, expresso na Equação (51) relaciona diretamente a demanda química de oxigênio para um tempo t.
[DQO] = [DQO] [K + K − K eK −K + K − K
K + K − K e− K −K ]
A dificuldade de aplicação desses modelos está no fato das constantes variarem para diferentes condições operacionais, impedindo estender a aplicação a diversos sistemas e exigindo a utilização de dados experimentais. Alguns autores têm buscado a descrição fenomenológica através das leis da física que levem diretamente em consideração a quantidade de radiação emitida na operação de reatores fotoquímicos. Algumas das estratégias estudadas são mostradas na seção seguinte.
2.4.3 Modelos fenomenológicos
Como mostrado na seção anterior, a degradação fotoquímica do fenol ou de outras substâncias orgânicas está associada a um mecanismo complexo de reações, dificultando a análise cinética e o desenvolvimento de equações sem a utilização de dados experimentais. Apesar de não haver uma literatura abundante sobre a aplicação de modelos fenomenológicos em processos oxidativos avançados (em particular o de foto-Fenton), alguns estudos como os de Spadoni e Stramigioli (1979), Romero et al (1983), Alfano et al (1994, 1997 e 2000) e
Irazoqui et al (2000) obtiveram equações a partir das leis físicas de emissão e absorção da luz
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 25 Para expressar a taxa de uma reação fotoquímica, é necessário fazer a distinção entre as etapas escuras e as ativadas por radiação. O tratamento das etapas escuras utiliza a mesma metodologia de reatores convencionais, estando a principal dificuldade na avaliação das etapas de iniciação (Alfano et al., 1985). A taxa de uma reação ativada por radiação é proporcional a
um termo chamado LVREA, ou taxa volumétrica local de absorção de energia (Irazoqui et al.,
1973). A avaliação da LVREA é realizada explicitando primeiro um balanço de energia radiante em estado estacionário para um volume de controle homogêneo. Em seguida, é necessário incorporar um modelo para a fonte de radiação e a equação constitutiva de Lambert no termo de absorção (Alfano et al., 1985). A Figura 2.6 esquematiza a obtenção de um modelo para
sistemas fotoquímicos:
Figura 2.6 - Esquema para obtenção da taxa local volumétrica de absorção de energia. Fonte: Alfano et al. (1985).
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 26 vz∂C∂z = D rA ∂C∂r +A ∂ C∂zA + R
Para o caso de reações fotoquímicas, a taxa de reação dependerá diretamente da quantidade de energia emitida pela fonte e absorvida pelo meio, bem como do comprimento de onda utilizado. Se o campo de radiação é modelado corretamente, a taxa local de absorção de energia pode ter sua expressão obtida através de uma resolução formal de equação de balanço da energia radiante, uma vez que um modelo conveniente tenha sido assumido para emissão da lâmpada (Spadoni et al., 1979). A equação para transferência de radiação é dada por (Alfano
et al., 1994):
dIΩ,ν s, t
ds + [ ν s, t ]IΩ,ν s, t + σνIΩ,ν s, t
= jν s, t + πσν s, t ∫ p Ω′→ Ω IΩ′,ν s, t dΩ′
Ω′= π
Onde: [kν s, t ]IΩ,ν s, t – Termo de absorção, σνIΩ,ν s, t – Termo de espalhamento,
jν s, t – Termo de emissão, πσν s, t ∫Ω′= πp Ω′ → Ω IΩ′,ν s, t dΩ′ - termo de espalhamento
para dentro.
A LVREA para radiação monocromática pode então ser calculada pela Equação (54) (Alfano et al., 1994).
eνa s, t = ν s, t ∫ IνdΩ
Ω
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 27 Os primeiros modelos desenvolvidos aproximavam as lâmpadas como uma linha, e por isso recebem o nome de modelos line source. Os modelos mais recentes são mais rigorosos e
consideram a emissão esférica de cada um dos elementos diferenciais (modelo LSSE), bem como o raio da lâmpada como parâmetro de dimensionamento (modelos extense source),
eliminando a singularidade originada nos modelos lineares (Romero et al., 1983).
Na Tabela 2.3 são mostrados alguns dos principais modelos de emissão, bem como seus autores.
Tabela 2.3 - Alguns modelos de emissão de radiação e seus autores.
Modelo Autores Equação
Fonte linear com emissão em planos paralelos (LSPP)
Harris e Dranoff
(1965) jν s, t =
�,� exp[−�
�,� − �� ]
Fonte linear com emissão esférica (LSSE)
Jacob e Dranoff (1966)
jν s, t
= , ∑ ∑ �,�∆ exp {− [��,� �
− �� + ��,� ]}
Fonte extensa com emissão volumétrica (ESVE)
Irazoqui et al.
(1973)
jν s, t
= � ∫ ∫ ∫sen � cos � � �
� �
�
Fonte extensa com emissão superficial (ESSE)
Stramigioli et al.
(1975)
jν s, t
= �� ∫ ∫ � [− ∫ �� �� � ,�,� ] � � ∗ � �
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 29
3 Estado da arte
3.1 Processos oxidativos avançados
As chamadas tecnologias de oxidação avançadas são definidas como aquelas em que há a produção de radicais hidroxila, altamente reativos e não seletivos, responsáveis pela degradação de matéria orgânica em solução (Guimarães et al., 2012; Guo et al., 2014). Peróxido
de hidrogênio e ozônio tem sido as substâncias mais utilizadas para gerar radicais HO• em água (Cabrera-Codony et al., 2015), e podem ser usados em combinação com outros elementos como
catalisadores e radiação (Jin et al., 2012). Por se tratarem de operações de degradação com alta
eficiência, aplicáveis a várias substâncias, e com gasto de energia menores se comparado a processos tradicionais (Wols & Hofman-Caris, 2012; Tisa et al., 2014; Antonopoulou et al.,
2014), grande atenção tem sido dada a esse tipo de tecnologia, principalmente no tratamento de água.
Dentre os estudos envolvendo o processo oxidativo avançado com aplicação de H2O2
juntamente com radiação ultravioleta, destaca-se o grande número de substâncias orgânicas para o qual é possível empregar essa metodologia. Pode-se citar aqui os estudos envolvendo a degradação de EDTA (Ku et al., 1998), éter metil-terc-butílico (Stefan et al., 2000),
nitro-aromáticos (Einschlag et al., 2002), tricloroeteno (Li et al., 2007), e antibióticos (Jung et al.,
2012; Keen & Linden, 2013; Santos et al., 2015), evidenciando a extensa gama de aplicação
desse método.
Com relação aos POA envolvendo ozônio, pode-se citar os estudos envolvendo a degradação de 2,4-dicloro e 2,4-dimetil-fenol (Trapido et al., 1998), álcool terc-butílico
(Garoma & Gurol, 2004), ácidos orgânicos (Chang et al., 2012), e produtos farmacêuticos (Illés
et al., 2014).
Com relação aos processos de foto-Fenton, pode-se destacar as particularidades e conclusões obtidas por alguns estudos na degradação de compostos fenólicos ou outras substâncias orgânicas.
Zepp et al. (1992) utilizaram sondas de medição de traços de radicais HO• para provar
que eles se formam durante a foto-redução do Fe(III) quando H2O2 reage com Fe(II). Os
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 30 Ahmed et al. (2011) realizaram ensaios de degradação por reação de foto-Fenton em
efluentes vindos de agroindústrias produtoras de azeite de oliva, com concentrações de carbono orgânico total variando entre 180 e 300 mgC.L-1. Os experimentos foram feitos em um reator
fotoquímico em batelada, com uma lâmpada de mercúrio de 40W em seu centro e submetido a um banho termostático. O sistema serviu para avaliar a influência de algumas condições operacionais na eficiência do tratamento em questão. O aumento na concentração de peróxido de hidrogênio de 1,5 g.L-1 para 5 g.L-1 gerou aumento na degradação final de carbono orgânico
total de 50% para 80%. Para os íons Fe2+, o aumento de concentração de 10 mg.L-1 para 30
mg.L-1 também aumentou a degradação final de 60% para 80%; entretanto, aumentar sua
concentração para 60 mg.L-1 provocou diminuição na eficiência do processo. Os autores ainda
constataram que um pH de 3 e temperatura de 26°C eram os ideais para obter máxima eficiência. Na situação estudada, as concentrações ideais de peróxido de hidrogênio e de ferro foram de 30 g.L-1 e 30 mg.L-1, respectivamente.
Giri e Golder (2015) estudaram a degradação de misturas de drogas pelos processos de Fenton e foto-Fenton, simulando efluentes de indústrias farmacêuticas. Os procedimentos experimentais foram realizados em reatores cilíndricos em batelada, com uma concentração de efluente de 400 mL, temperatura entre 23°C e 25°C, e tinham como objetivo identificar a diferença na degradação das drogas individualmente ou em mistura. Não se observou mudança significativa no tratamento das drogas de forma individual ou em mistura para o sistema operando a pH 3, 2,25 mM de Fe2+ e 22,5 mM de H
2O2. A remoção do COT, no entanto, para
as drogas tratadas individualmente foi 17% menor no processo de foto-Fenton, com relação ao tratamento da mistura, indicando dependência da concentração de COT com o mecanismo de reação. No geral, as taxas de remoção das drogas foram sempre superiores a 70%, podendo chegar a mais de 90%, enquanto que as de COT foram maiores de 40%, podendo passar de 70%.
3.2 Degradação do fenol por POA
A literatura envolvendo a degradação de fenol por processos oxidativos avançados é extensa e contém estudos de diferentes processos de degradação, bem como dos fatores e parâmetros associados. Incluem-se nesses estudos os processos envolvendo radiação UV e H2O2 (Han et al., 2004; Edalatmanesh et al., 2007), fotocatálise heterogênea (Zhang et al.,
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 31 Em seu trabalho de 2002, Esplugas et al. compararam diversos processos de oxidação
avançada no tratamento de fenol em soluções aquosas, entre eles UV, UV/H2O2, UV/O3,
UV/H2O2/O3 e reagente de Fenton. Constatou-se que nenhum dos processos envolvendo
combinações com ozônio aumentaram de forma eficiente a degradação com relação ao emprego isolado de ozônio. Os processos com UV e peróxido de hidrogênio se mostraram cinco vezes mais eficientes do que o emprego apenas da luz UV, enquanto o processo com reagente de Fenton foi responsável pelas taxas de degradação mais elevadas.
Mota (2010) realizou comparações entre o emprego de radiação ultravioleta e radiação solar na degradação de fenol por foto-Fenton, e estudou a influência de diversos parâmetros operacionais como a concentração de Fe2+, de H
2O2, de fenol, o volume de efluente e a área
irradiada. O reator utilizado nesse trabalho operava em batelada e consistia em um tanque de mistura ligado a células contendo tubos de quartzo e refletores parabólicos, que poderiam ser irradiados por luz ultravioleta ou luz solar. O autor notou que a degradação de fenol era mais rápida à medida em se aumentava a área irradiada, com um valor máximo para área de 0,2 m². Além disso, a utilização de luz solar se mostrou mais eficiente do que as lâmpadas UV, havendo degradação máxima aos 45 minutos para uma área irradiada de 0,1 m², metade da necessária com luz ultravioleta. Com relação à concentração dos reagentes, os íons ferrosos apresentaram contribuição positiva até um valor intermediário, quando passaram a exercer efeito negativo devido ao aumento da turbidez da solução (que deixa mais difícil a absorção de luz) e do sequestro de radicais hidroxila. A concentração de peróxido de hidrogênio foi a variável que mais exerceu influência na degradação, apresentando também efeito positivo até um dado valor, e depois diminuindo a taxa de degradação pela ocorrência de reações paralelas. Os valores ótimos, para uma degradação de 98% de fenol, foram: 2,34 mM de Fe2+ e 135,33 mM de H
2O2.
Luna et al. (2012) estudaram a degradação de fenol em um efluente sintético pelo
processo de foto-Fenton em meio alcalino e com altas concentrações de íons cloreto. Os experimentos deste trabalho foram realizados em um reator anular de fluxo ascendente com uma lâmpada de mercúrio de média pressão de 450 W de potência. Os autores constataram que valores baixos de pH tinham efeito inibidor para as condições estudadas, devido à complexação competitiva dos íons Fe3+ promovida pelos íons cloreto. Por outro lado, as altas concentrações
Luiz Gonzaga Lopes Neto Dissertação de Mestrado 32 estudados têm caráter básico, podendo ser mais viável salinizar o meio a aumentar o pH, tornando a aplicação do processo de foto-Fenton mais eficiente.
3.3 Modelagem da degradação em reatores fotoquímicos
3.3.1 Modelagem por redes neurais artificiais
Redes Neurais Artificiais são descritas por Ding et al. (2013) como sistemas de
processamento de informações adaptativos e não-lineares que combinam várias unidades de processamento com uma série de características tais quais auto adaptação. Os modelos gerados por RNA têm como principal vantagem a capacidade de gerar não-linearidade (Vijayalakshmi & Girish, 2015), e têm sido adotados extensivamente na descrição e controle de processos químicos ou biológicos de tratamento de efluentes (Yu et al., 2009).
Nogueira et al. (2012) aplicaram uma estratégia de RNA para modelar a taxa de
degradação de carbono orgânico dissolvido em um efluente fenólico por foto-Fenton solar em um reator em batelada. A escolha desse tipo de abordagem se deu pela complexidade do problema avaliado, tanto nos mecanismos reacionais, quanto na utilização de luz solar, e pelo fato do modelo gerado ser capaz de prever as não-linearidades associadas. Foi utilizada uma rede neural do tipo feed-forward com 3 camadas e função de ativação do tipo sigmoide. As
variáveis de entrada foram: carbono orgânico dissolvido inicial, vazão de peróxido de hidrogênio, concentração de íons ferrosos, taxa de circulação, irradiância instantânea solar no instante t, carbono orgânico dissolvido no tempo t, e temperatura da solução. A variável de saída foi a taxa de remoção de carbono orgânico dissolvido no tempo t. Os autores obtiveram um modelo com coeficiente de determinação de 0,97 e identificaram que as variáveis mais importantes para os valores calculados eram o carbono orgânico dissolvido inicial, a concentração de íons ferrosos, a vazão de peróxido de hidrogênio e a taxa de remoção de carbono orgânico dissolvido.
Em um estudo realizado por Ayodele et al. (2012) foi utilizada uma rede neural artificial





![Figura 5.2 - Perfil de COT para os níveis superior e inferior de concentração de fenol, com [Fe 2+ ] = 2,5 mM e [H](https://thumb-eu.123doks.com/thumbv2/123dok_br/15652267.112775/67.893.194.743.543.866/figura-perfil-para-níveis-superior-inferior-concentração-fenol.webp)