www.jped.com.br
ARTIGO
ORIGINAL
Breast
milk
supplementation
and
preterm
infant
development
after
hospital
discharge:
a
randomized
clinical
trial
夽
,
夽夽
Roxana
Desterro
e
Silva
da
Cunha
a,b,∗,
Fernando
Lamy
Filho
c,
Eremita
Val
Rafael
a,b,
Zeni
Carvalho
Lamy
ce
André
Luiz
Guimarães
de
Queiroz
d,eaHospitalUniversitárioMaterno-Infantil,SãoLuís,MA,Brasil bUniversidadeFederaldoMaranhão(UFMA),SãoLuís,MA,Brasil
cDepartamentodeMedicina,UniversidadeFederaldoMaranhão(UFMA),SãoLuís,MA,Brasil dFaculdadedeMedicina,UniversidadeFederaldoMaranhão(UFMA),SãoLuís,MA,Brasil eProgramaInstitucionaldeBolsasdeIniciac¸ãoCientífica(PIBIC),Brasil
Recebidoem7dejaneirode2015;aceitoem6demaiode2015
KEYWORDS
Breastfeeding; Preterm;
Hospitaldischarge; Development; Humanmilk
Abstract
Objectives: Toassesstheeffectofmaternalbreastmilksupplementationonthedevelopment
ofexclusivelybreast-fedverylowbirthweightpreterminfantsat12monthsofcorrectedage.
Methods: Arandomizedclinicaltrialwith53infantsfollowed-upafterdischargefromthe
neo-natalunituntilacorrectedgestationalageof12months.Newbornsintheinterventiongroup werebreastfedexclusivelywithmaternalmilkandreceived2gofamultinutrientsupplement (Pré-Nan®,Nestlé,Vevey, Switzerland) added toexpressed breastmilk twice a dayuntil a correctedageof4to6months.Thecontrolgroupwasexclusivelybreastfedwithout supple-mentation.Aftermonthlyfollow-up,developmentalassessmentwasperformedusingtheBayley IIIScale.
Results: TherewasnostatisticallysignificantdifferenceontheBayleyIIIScalebetweenthe
interventionandcontrolgroupsinanyoftheassesseddomains:motor,cognitive,and commu-nication.However,scoresinthethreedomainswerealwayshigherinthegroupthatreceived thesupplement.Therewereasimilarnumberofcasesofdevelopmentaldelayinbothgroups: seven(28%)inthegroupthatreceivedthesupplementandnine(33.3%)inthegroupthatwas exclusivelybreastfed.
DOIserefereaoartigo:
http://dx.doi.org/10.1016/j.jped.2015.04.004
夽 Comocitaresteartigo:daCunhaRD,LamyFilhoF,RafaelEV,LamyZC,QueirozAL.Breastmilksupplementationandpreterminfant
developmentafterhospitaldischarge:arandomizedclinicaltrial.JPediatr(RioJ).2016;92:136---42.
夽夽EstudovinculadoàUniversidadeFederaldoMaranhão(UFMA),SãoLuís,MA,Brasil. ∗Autorparacorrespondência.
E-mail:roxanacunha@hotmail.com(R.D.e.S.d.Cunha).
Conclusions: Theresultsfailedtoshowanassociationbetweenpost-dischargemultinutrient supplementationanddevelopmentintheassessedinfants.
©2015SociedadeBrasileiradePediatria.PublishedbyElsevierEditoraLtda.Allrightsreserved.
PALAVRAS-CHAVE
Amamentac¸ão; Prematuro; Altahospitalar; Desenvolvimento; Leitematerno
Suplementac¸ãodoleitematernoedesenvolvimentodelactentespré-termoapósalta hospitalar:ensaioclínicorandomizado
Resumo
Objetivos: Avaliaroefeitodasuplementac¸ãodoaleitamentomaternoexclusivocomaditivo
multicomponentenodesenvolvimentodelactentesnascidospré-termodemuitobaixopesoaos 12mesesdeidadegestacionalcorrigida.
Método: Ensaioclínico randomizadocom53 lactentes, acompanhadosdaalta hospitalarna
UnidadeNeonatal atéo12◦ mêsdeidade gestacionalcorrigida. Aquelesalocados nogrupo intervenc¸ão permaneciam em aleitamento materno exclusivo e recebiam dois gramas de suplemento multicomponente em pó (Pré-Nan®, Nestlé,Vevey, Suíc¸a),adicionados ao leite ordenhadoduasvezesaodia,porquatroaseismesesdeidadegestacionalcorrigida.Ogrupo controlepermaneciaemaleitamentomaternoexclusivosemsuplementac¸ão.Após acompanha-mentomensal,foifeitaavaliac¸ãododesenvolvimentopormeiodaEscaladeBayleyIII.
Resultados: Na comparac¸ão do desenvolvimento pela Escala de Bayley III entre os grupos
intervenc¸ãoecontrole,nãohouvediferenc¸aestatísticasignificativanosdomíniosestudados: motor,cognitivoelinguagem.Porém,osvaloresdosescoresforamsempremaioresnogrupo intervenc¸ãodoquenogrupocontrolenostrêsdomínios.Oatrasodedesenvolvimentose dis-tribuiudeformasimilarnosgrupos:setecasos(28%)nogrupointervenc¸ãoenove(33,3%)no grupocontrole.
Conclusões: Osresultadosnão mostraramassociac¸ãoentresuplementac¸ãomulticomponente
pós-altaedesenvolvimentodoslactentesanalisadospelaEscaladeBayleyIII.
©2015SociedadeBrasileiradePediatria.PublicadoporElsevierEditoraLtda.Todososdireitos reservados.
Introduc
¸ão
O cérebro em desenvolvimento é particularmente vulne-rável a deficiências nutricionais por causa da trajetória rápida de vários processos neurológicos, como formac¸ão de sinapses e mielinizac¸ão. É regulado por nutrientes como proteínas, energia, gorduras,minerais e fatores de crescimento.1-3
A deficiência desses elementos pode refletir posteri-ormente e evoluir com disfunc¸ão cerebral associada a alterac¸ões futuras de desenvolvimento infantil.2 Dessa
forma, a nutric¸ão adequada, principalmente nos recém--nascidospré-termo(RNPT),édegrandeimportânciapara evitar, dentre outros danos, atrasos de desenvolvimento neurológico.4-6
Apesardeoleitematerno(LM)serconsideradoalimento idealnoperíodoneonatal,promoveramaturac¸ão gastroin-testinal,gerarbenefíciosimunológicoselevaraoaumento doníveldeácidodocosahexanoico,importantecomponente paraodesenvolvimentocerebral,5,7-9seuusoexclusivoem
determinadassituac¸õespodeacarretardeficiênciasde nutri-entesedesmineralizac¸ãoóssea.10,11
Operíododeinternac¸ão deRNPT, especialmente aque-lesdemuitobaixopeso,compõeumadessassituac¸õesque fazemcomqueasuplementac¸ãodoleitehumanoparaessas crianc¸assejaatualmenteumapráticabemestabelecidano períodointra-hospitalare promovamelhorganhodepeso,
aumento do comprimento e perímetro cefálico em curto prazoe melhoresíndicesdedesenvolvimentoem médioe longoprazos.12-14
Apesar de os benefícios da suplementac¸ão do leite humanoparaRNPTinternadosestarembemdocumentados na literatura, ainda não há consenso sobre a efetividade dessa prática após a alta hospitalar.6,10,15 Recentemente
o Comitê de Nutric¸ão da Sociedade Europeia de Gastro-enterologia Pediátrica, Hepatologia e Nutric¸ão (ESPGHAN Committee on Nutrition) recomendou que bebês alimen-tados exclusivamente com leite materno e que tivessem recebidoalta hospitalar com peso abaixo donormal para suaidade pós-conceptual recebessemaditivos para suprir suasnecessidadesnutricionais.16
Nosúltimos anosalguns autoresvêmtentando esclare-ceressaquestãoverificandoaefetividadedasuplementac¸ão pós-altaem estudos comdelineamento experimental. Em revisãosistemática,Youngetal.17selecionaramsomenteos
ensaiosrandomizadosdeO’Connor etal.18 e Zachariassen
etal.19 Essesmostrarambonsresultadosdasuplementac¸ão
Quanto aosefeitos dasuplementac¸ãodoleite materno sobreodesenvolvimentopós-alta,Aimoneetal.,20ao
estu-dara mesma populac¸ãode O’Connor etal.,19 mostraram
tendênciaamelhorganhodepesoemaiorescircunferências dacabec¸aemcrianc¸asdogruposuplementadoemrelac¸ão aosdogrupocontroleapós12semanas.Aoseremavaliados aos18mesesdeidadegestacionalcorrigida(IGC)osbebês dogrupointervenc¸ãoobtiverammelhoresescoresnaEscala Bayley II nos domínios dalinguagem e motor, porém sem significânciaestatística.
Diante da falta de evidências nessa área, o presente estudo se propôs a investigar se crianc¸as egressas de Unidade de Terapia Intensiva Neonatal (UTIN), nascidas prematuras e de muito baixo peso que se alimentam de leitematernosuplementadocomaditivomulticomponente apresentammelhoresescoresdedesenvolvimento neurop-sicomotorquandocomparadascomaquelasquefazemuso deleitematernonãosuplementado.
Métodos
Ensaio clínico randomizado feito de dezembro de 2010 até outubro de 2013 com 53 RNPT com peso de nasci-mento menor do que 1.500 g que estiveram internados naUTINdoHospitalUniversitárioUnidadeMaterno-Infantil daUniversidade Federal doMaranhão e que tiveram alta em aleitamento materno exclusivo. Após a alta, todas as crianc¸as que cumpriram esses critérios foram acom-panhadas até 12 meses de IGC. Não foram incluídos no estudoaquelesqueapresentaramcondic¸õesquepoderiam interferir no desenvolvimento neuropsicomotor (DNPM): malformac¸ões importantes, hidrocefalia, cromossomopa-tias,hidropsiafetal,infecc¸õescongênitas,usomaternode drogasilícitas,tabaco,álcooledecorticoidesdeforma con-tínua,gemelaridade,sequelasdeenterocolitenecrosantee paralisiacerebral.
Antes da alta as mães eram orientadas a oferecer o seioa seusfilhos,em livredemanda, e darprioridade ao leiteposterior.Seteadezdiasapósaaltaemaleitamento materno exclusivo, as díades retornavam para primeira avaliac¸ão. Caso continuassem em aleitamento materno exclusivo(AME),erafeitaarandomizac¸ão.Esseprocessose justificaporcausadograndenúmerodemãesque abando-namoAME,logoapósaalta,aosedepararcomassituac¸ões davidarealnodomicílio.
Foram gerados números aleatórios para alocac¸ão das crianc¸as nos grupos controle ou intervenc¸ão. Para a randomizac¸ão,usou-seenvelopeopacoeselado.Por ques-tõeséticas,nãofoipossívelusarplaceboehavercegamento dasmãesedosprofissionais.
Paraocálculodotamanhoamostralforamusadosos valo-resobtidosem estudo-piloto.Para issoassumiu-se ovalor médio(90pontos)obtidoparaodomíniolinguagemdaEscala deBayleyIIIdogrupocontroleaos12mesesdeIGCeescore dogrupointervenc¸ão10pontosmaior,comdesviopadrãode 12pontosnosdoisgrupos.Assumindo-setambémumpoder de80e probabilidadedeerrotipo1de0,05,calculou-se, comonecessários,23bebêsemcadagrupo.
A intervenc¸ão consistiu em suplementac¸ão do leite maternopor de quatro a seis meses e erafeita como se demonstraaseguir.
Apósarandomizac¸ão,demonstrava-seàsmãesdogrupo intervenc¸ão comoprocederparaadic¸ão dosuplemento ao leite materno.Eram retirados 10ml deleite por meiode ordenha manual e acrescentados 2g de pó da fórmula PRÉ-NAN® (Nestlé). Para isso era usado copo de plástico graduadode50ml.Apóshomogeneizac¸ão,amisturaera ofe-recidaà crianc¸a.O procedimentoerafeitoantesdeduas mamadasdodia,umanoturnodamanhãeoutraàtarde.O acréscimosignificouaumentode20kcalpordia.Emmédia esse acréscimo foi suficiente para elevar a taxa calórica da crianc¸a no momento daalta (considerando-se 1,8 a 2 kgdepesonaalta)paracercade140Kcal/kg/dia.21Além
disso, correspondia também ao aumento diário de 2,12g de carboidratos, 1,04g de gorduras, 0,56g de proteínas, 1,04g de gorduras totais, 0,44 g de gorduras saturadas, 0,164gdeácidolinoleico,19,6mgdeácidoalfalinolênico, 10,76gdesódio, 30,4mgdecálcio,0,4 mgdeferro,24,2 mgdepotássio,1,6mgdetaurinaevitaminas.
Oslactentestiveramacompanhamentomensaldoestado geral, nutricional e desenvolvimento em ambulatório de seguimento e incentivo aoaleitamento materno.AEscala de Bayley III foi aplicada para a avaliac¸ão do DNPM aos 12mesesdeidadegestacionalcorrigida.Aavaliac¸ãofoifeita porterapeutaocupacionalcomtreinamentoespecíficocom equipeautorizada,emsalaadequadamenteequipadapara aplicac¸ãodoteste.Oavaliadornãoerainformadosobreo grupoaoqualacrianc¸apertencia.
Paraaverificac¸ãodaefetividadedarandomizac¸ão,foram comparadas características dos lactentes estudados até a randomizac¸ão,emambososgrupos.Variáveiscomparadas: peso,sexo,idadegestacional,perímetrocefálico(PC), com-primento ao nascimento,peso na randomizac¸ão,peso em relac¸ãoàidadegestacional(PIG/AIG),tempodeinternac¸ão eescoredegravidade(SnappeII---ScoreforNeonatalAcute Physiology, Perinatal Extension,Version II).22 Não foi
apli-cadotestedehipótesenacomparac¸ãodessasvariáveis,em concordânciacomasnormas doConsolidatedStandardsof ReportingTrials(ConsortStatement).23
Osescoresdosdomíniosmotor,cognitivoedelinguagem avaliadospelaEscaladeBayleyIIIaocompletarem12meses deIGCtambémforamdescritos.
Foramcalculadasasmédiasdosescoresdecadadomínio dodesenvolvimento.
Usou-se análise multivariada (regressão linearsimples) apesar da randomizac¸ão, uma vez que algumas variáveis coletadas antes dela não se apresentavam balanceadas entreosdoisgrupos.Dentreelas,foramusadasnomodeloas variáveispesodenascimentoesexo,variáveiscom impor-tante influência no desenvolvimento futuro do RNPT.24,25
Apesar de não se mostrarem balanceadas, as variáveis SnappeIIetempodeinternac¸ãonãoforamusadasnomodelo porserconsideradascolinearescomopesodenascimento. Alémdisso,comoodesfechofoimedidováriosmesesapós o fim da intervenc¸ão, elementos presentes nesse período poderiaminfluenciarnoresultadofinal.
Apenasumavariávelpós-randomizac¸ãofoiescolhidapara comporomodeloporsuaimportânciaparadesenvolvimento da crianc¸a: ‘‘mãe como principal cuidador da crianc¸a’’ (categorias sim/não). Sabe-se que unidade familiar é um dosprincipaisfatoresdepromoc¸ãodedesenvolvimentoda crianc¸a.26Resegueetal.27dãoespecialenfoqueàpresenc¸a
RN com peso < 1.500g e IG < 37s (n = 293)
Excluídos (n = 211)
Não atendem aos critérios de inclusão (n = 33)
Óbitos (n = 93)
Aleitamento misto na alta (n = 85)
Randomizados (n = 82)
Grupo de intervenção (n = 45) Permaneceram no estudo até 1 ano de IGC (n = 27)
Grupo Controle (n = 37) Permaneceram no estudo até 1 ano de IGC (n = 27)
Perda de seguimento (n = 19)
• Introdução de outros alimentos (n =12) • Retorno ao trabalho (n = 02)
• Recusou-se a continuar (n=03) • Óbito (n=01)
• Alteração grave do BERA (n =1)
Perda de seguimento (n = 10)
• Introdução de outros alimentos (n = 08)
• Retorno ao trabalho (n = 01)
• Por internação prolongada (n = 01)
•Analisados (n = 26)
BB •
Analisados (n = 27)
Inclusão
Alocação
Seguimento
Análise
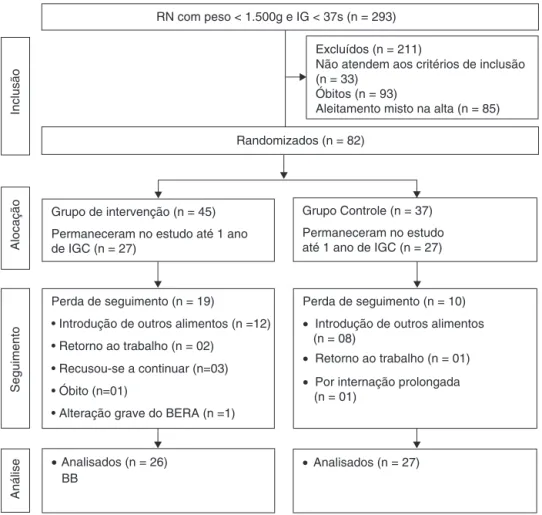
Figura1 Fluxogramadarandomizac¸ãodelactentesnascidospré-termoapósaaltahospitalar.23
RN,recém-nascido;IG,idadegestacional;IGC,idadegestacionalcorrigida;BERA,BrainEvokedResponseAudiometry.
econsideramaprivac¸ãomaternafatorderiscoparaatraso nodesenvolvimentoinfantil.
A escolaridade materna também foi entendida como essencial para o desenvolvimento,26 porém, tendo sido
coletada antes da randomizac¸ão, não mostrou diferenc¸a importantenasuadistribuic¸ãonosdoisgrupos.
Análise de regressão linear simples foi feita, a princí-pio,deformanãoajustadaapenascomasvariáveisgrupo (intervenc¸ãooucontrole)epontuac¸ãonaEscaladeBayley IIIparaostrêsdomíniosdedesenvolvimento(motor, cogni-tivoelinguagem). Emseguida fez-seumasegundaanálise deregressãolinearsimples,ajustadapelasvariáveissexo, pesoaonasceremãecomoprincipalcuidadordacrianc¸a.
AvariávelcorrespondenteaosescoresdaEscalade Bay-leyIIInostrêsdomíniostevesuanormalidadeverificadapelo testedeShapiro-Wilk.
Atabulac¸ãodosdadosfoifeitanoprogramaEpiInfo3.5 (Epi InfoTM, Centers for Disease Control and Prevention,
Atlanta,EUA)easanálisesestatísticasforamfeitasnoStata 11(StataCorp.2009.StataStatisticalSoftware:Release11. CollegeStation,TX:StataCorpLP).
Apesquisateveaprovac¸ãopormeiodoParecern◦302/10
doConselhodeÉticaemPesquisadoHospitalUniversitário daUniversidade Federal do Maranhão. O presenteestudo consiste num ensaio clínico randomizado que seguiu as normasinternacionaisestabelecidaspeloConsolidated Stan-dardsofReportingTrials(ConsortStatement).23Oestudofoi
registradonoRegistroBrasileirodeEnsaiosClínicos(Rebec)
doMinistériodaSaúdedoBrasilsobon◦U1111-1131-8413.
Baseou-senoprojetodepesquisa‘‘Fortificac¸ão multicom-ponente do leite humano para nutric¸ão, crescimento e desenvolvimentoderecém-nascidosprematurosegressosde UTI-Neonatal’’,editalMinistériodaSaúde,Conselho Naci-onaldeDesenvolvimento Científico e Tecnológico (CNPq), eFundac¸ão deAmparoà PesquisadoEstadodoMaranhão (Fapema),n.◦477848/2007-9.
Resultados
No período de estudo nasceram 293 crianc¸as pré-termo com menos de 1.500g. Não preencheram os critérios de inclusão 118 recém-nascidos (RN) e houve 93 óbi-tos. A randomizac¸ão foi feita em 82 recém-nascidos. Da randomizac¸ãoatéo fimdaintervenc¸ão 29 crianc¸as foram perdidas parao seguimento. Amaioria das perdas sedeu peladificuldadedamãedemanteroaleitamentomaterno exclusivo durante o período de intervenc¸ão. Essas per-das foram estatisticamente semelhantes nos dois grupos (p=0,12).Foramanalisadas53crianc¸aspelaEscalade Bay-ley III para avaliac¸ão do desenvolvimento. A média de durac¸ãodaintervenc¸ãofoisemelhanteentreosgrupos con-trole e intervenc¸ão: 5,84±0,54meses; 5,64±0,73meses; (p=0,42).
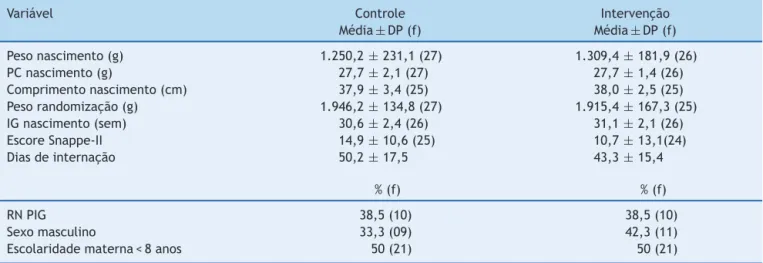
Tabela1 Distribuic¸ãodascaracterísticasperinataisdelactentesnascidospré-termoedemuitobaixopeso.SãoLuís,2010-2014
Variável Controle Intervenc¸ão
Média±DP(f) Média±DP(f)
Pesonascimento(g) 1.250,2±231,1(27) 1.309,4±181,9(26)
PCnascimento(g) 27,7±2,1(27) 27,7±1,4(26)
Comprimentonascimento(cm) 37,9±3,4(25) 38,0±2,5(25)
Pesorandomizac¸ão(g) 1.946,2±134,8(27) 1.915,4±167,3(25)
IGnascimento(sem) 30,6±2,4(26) 31,1±2,1(26)
EscoreSnappe-II 14,9±10,6(25) 10,7±13,1(24)
Diasdeinternac¸ão 50,2±17,5 43,3±15,4
%(f) %(f)
RNPIG 38,5(10) 38,5(10)
Sexomasculino 33,3(09) 42,3(11)
Escolaridadematerna<8anos 50(21) 50(21)
DP,desviopadrão;f,frequência;PC,perímetrocefálico;IG,idadegestacional;Snappe-II,ScoreforNeonatalAcutePhysiology,Perinatal
Extension,VersionII;RN,recém-nascido;PIG,pequenoparaaidadegestacional.
Dascrianc¸as queconcluíram aintervenc¸ão, 20 (37,7%) erammeninose33(62,3%)meninas;amaioriadoslactentes tinhamãesentre20e 30anos(60,4%)comoitoa11anos deestudo (69,2%) e paisque viviam em uniãoconsensual (60,4%).
A renda familiar predominante foi de um a três salá-riosmínimos(49%),porémcomaltopercentualdefamílias queviviamcomatéumsaláriomínimo(32%).Dasmãesque participaramdoestudo,apenas25%desenvolviamatividade remuneradaquandoseubebêcompletouumanodeIGC.
A mãe foi o principal cuidador da crianc¸a em 73,6% doscasos.Apenas18,9%das famíliastinham maisdeuma crianc¸aque moravam nomesmo domicílio. A maioria das casas(88,9%) tinharevestimento depiso, o que possibili-tavaque a crianc¸a brincasse nochão. Um poucomais da metadedapopulac¸ão(52,8%)tinhabrinquedos educativos (encaixe,empilhar).
Naanálisedascaracterísticaspré-randomizac¸ãoos lac-tentesdosgruposcontrole eintervenc¸ãomostraramperfil semelhante,excetoquantoàsvariáveispesodenascimento, SnappeII,tempodeinternac¸ãoesexo(tabela1).
Osresultadosdaavaliac¸ãofeitapelaEscaladeBayleyIII nostrêsdomíniosdedesenvolvimentoaos12mesesdeIGC em53crianc¸assãodemonstradosnatabela2.Em16casos (30,8%)foievidenciadoalgumatrasodoDNPM,nove(33,3%) nogrupocontroleesete(28%)nogrupointervenc¸ão.
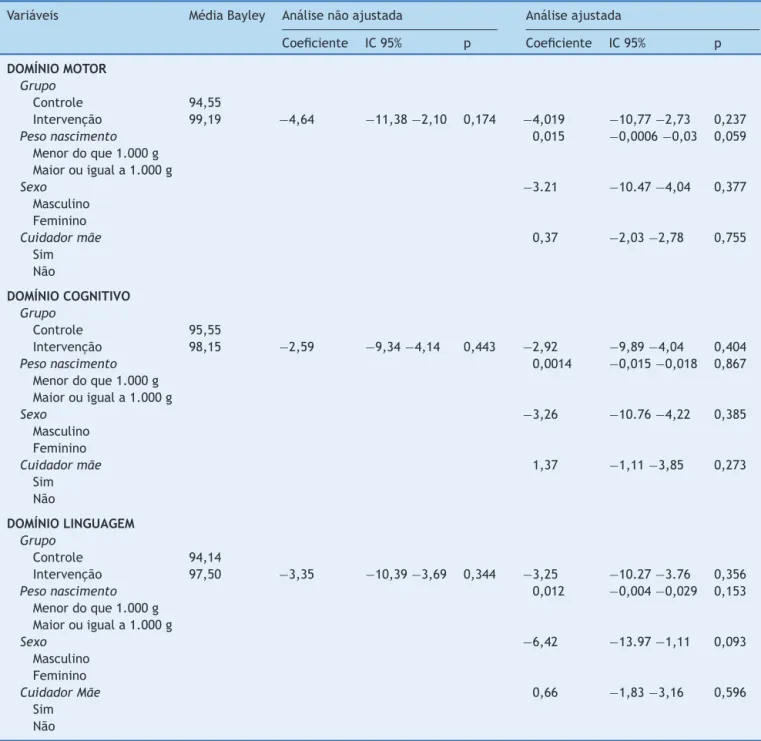
Naanáliseporregressãolinearsimples,emnenhumdos modeloscorrespondentesaostrêsdomíniosforam observa-das associac¸ões estatisticamente significativas, apesar de osvaloresmédios do EscoredaEscala de Bayley entreas crianc¸assuplementadasteremsidosempremaioresdoque osdasnãosuplementadas(tabela3).
Discussão
A comparac¸ão do DNPM avaliado pela Escala de Bayley III entre os grupos controle e intervenc¸ão não mostrou diferenc¸a estatísticasignificativanos domíniosestudados: motor,cognitivoelinguagem.Osvaloresdosescoresforam sempremaiores no grupointervenc¸ão do que nocontrole nostrêsdomínios.
Apenas um estudo semelhante ao presente ensaio foi identificado na literatura até o momento. Ambos estuda-rampopulac¸õessemelhantescompostasporRNPT,egressos de UTIN, com médias de peso de nascimento de 1.279g (presenteestudo)e1.287g20 emAMEnaaltahospitalar,e
tiveramcomoobjetivoasuplementac¸ãomultinutrientepara fornecermaisenergiaemaioraporteproteico.Noentanto,o modocomoasuplementac¸ãofoiadministradadiferiuentre eles. Diferentementedo presenteestudo,Aimone etal.20
adicionaram fortificante em cercade metadedaingestão diáriadeleitematerno,oque representou10%amaisde energiae20%amaisdeproteína.Nosdoisestudosoleite materno foi obtido por ordenha da própriamãe. No pre-senteensaio foi usadafórmula parapré-termo fracionada (Pré-Nan®,Nestlé,Vevey,Suíc¸a),diferentementedoestudo
citado,queusoufortificantemultinutrienteempódoleite humano(SimilacHMfortifier,AbbottNutrition®,Ohio,EUA).
Nosdoisensaiosnãohouveinfluênciadafortificac¸ãona durac¸ãodoaleitamentomaternoexclusivo.
OestudodeAimoneetal.20 avaliouodesenvolvimento
aos 18 meses de IGC por meio da escala de Bayley II e nãoencontrou diferenc¸asestatisticamente significativas
Tabela2 Classificac¸ãodanormalidadenostrêsdomínios dedesenvolvimentoavaliadospelaEscaladeBayleyIII.São Luís,2010-2014
Domínios Controle Intervenc¸ão
n % n %
Cognitivo
Normal(>85) 24 (88,9) 22 (84,6) Atrasado(<84) 3 (7,4) 4 (15,4)
Linguagem
Normal(>85) 21 (77,8) 23 (88,5) Atrasado(<84) 6 (22,2) 3 (11,5)
Motor
Tabela3 Análisesajustadaenãoajustadadarelac¸ãoentresuplementac¸ãodoleitematernoedesenvolvimentoavaliadopela EscaladeBayleyIIIparaosdomíniosmotor,cognitivoelinguagem.SãoLuís,2010-2014
Variáveis MédiaBayley Análisenãoajustada Análiseajustada
Coeficiente IC95% p Coeficiente IC95% p
DOMÍNIOMOTOR
Grupo
Controle 94,55
Intervenc¸ão 99,19 −4,64 −11,38−2,10 0,174 −4,019 −10,77−2,73 0,237
Pesonascimento 0,015 −0,0006−0,03 0,059
Menordoque1.000g Maiorouiguala1.000g
Sexo −3.21 −10.47−4,04 0,377
Masculino Feminino
Cuidadormãe 0,37 −2,03−2,78 0,755
Sim Não
DOMÍNIOCOGNITIVO
Grupo
Controle 95,55
Intervenc¸ão 98,15 −2,59 −9,34−4,14 0,443 −2,92 −9,89−4,04 0,404
Pesonascimento 0,0014 −0,015−0,018 0,867
Menordoque1.000g Maiorouiguala1.000g
Sexo −3,26 −10.76−4,22 0,385
Masculino Feminino
Cuidadormãe 1,37 −1,11−3,85 0,273
Sim Não
DOMÍNIOLINGUAGEM
Grupo
Controle 94,14
Intervenc¸ão 97,50 −3,35 −10,39−3,69 0,344 −3,25 −10.27−3.76 0,356
Pesonascimento 0,012 −0,004−0,029 0,153
Menordoque1.000g Maiorouiguala1.000g
Sexo −6,42 −13.97−1,11 0,093
Masculino Feminino
CuidadorMãe 0,66 −1,83−3,16 0,596
Sim Não
entre os grupos. Encontraram, porém, associac¸ões limí-trofes nos domínios linguagem (0,053) e motor (0,067). Foram encontrados percentuais semelhantes de crianc¸as comdesempenhoatrasadonosdoisgrupos.
Opresenteestudocorroborataisresultados,poisaoser feitaavaliac¸ãodoDNPMdelactentesaos12mesesdeIGC foram encontradasmédias do Escore daEscala deBayley III semelhantes nos dois grupos, nos três domínios avalia-dos,semdiferenc¸aestatísticasignificativa.Assimcomono trabalhodeAimoneetal.,20 atrasodedesenvolvimentose
distribuiudeformasimilarnosgrupos.
Alguns fatores podem ter contribuído para esse resul-tado. A não correc¸ão mensal da suplementac¸ão pode ter diminuído relativamente o efeito das quatro gramas de
suplementonodesenvolvimentodo lactente. Outro ponto quepodeterconcorridoparaareduc¸ãodadiferenc¸aentre osgrupos,queécaracterísticodostrabalhosdeintervenc¸ão comseguimento,éque,apesardocuidadosoesistemático acompanhamento das díades, é praticamente impossível garantir que a frequência correta da administrac¸ão do suplementodoleitematernodeusodomiciliar tenhasido obedecida.
tenderiam a se saciar mais precocemente e mamar por menostempodoqueogrupocontrole.
Porfim,apesardeocálculoamostralinicialterindicado queaquantidadedeindivíduoserasuficienteparadetectar diferenc¸a entre osgrupos, é possível que se tenha supe-restimado a dimensão dessas diferenc¸as. São necessárias amostrasmaioresparadetectá-las.
Ospontosfortesdesteestudoincluemodesenho expe-rimentalcomcegamentodoavaliadordoDNPMeofatode tersidoencontrado na literaturaapenasumtrabalhoque testavahipótesesimilar.
Opresenteestudoenfrentou algunsobstáculos.As difi-culdadesdoseguimentoeaintroduc¸ãodeoutrosalimentos fez com que não fosse possível acompanhar um maior número de crianc¸as. A possibilidade de vieses devido ao longotempoentreo fim daintervenc¸ão e a avaliac¸ão do desenvolvimentoeosdiferentespercentuaisdeperdasnos doisgruposforamminimizadospelousodeanáliseajustada. Diantedosresultadosdopresenteestudo,conclui-seque noatualestágiodeconhecimento,aindanãohá evidência deassociac¸ãoentresuplementac¸ãomulticomponente pós--alta e desenvolvimentodelactentes pré-termo demuito baixopesoaonascer.
Financiamento
Fonte financiadora de equipamento e material usados na pesquisa:MinistériodaSaúde,ConselhoNacionalde Desen-volvimento Científico e Tecnológico (CNPq) e Fundac¸ão de Amparo à Pesquisa do Estado do Maranhão (Fapema), n◦477848/2007-9.
Conflitos
de
interesse
Osautoresdeclaramnãohaverconflitosdeinteresse.
Referências
1.CaseyPH,Whiteside-MansellL,BarrettK,BradleyRH,Gargus R.Impactofprenataland/orpostnatalgrowthproblemsinlow birthweightpreterminfantsonschool-ageoutcomes:an8-year longitudinalevaluation.Pediatrics.2006;118:1078---86.
2.GeorgieffMK.Nutritionandthedevelopingbrain:nutrient pri-oritiesandmeasurement.AmJClinNutr.2007;85:614S---20S.
3.RodriguesMC,MelloRR,SilvaKS,CarvalhoML.Cognitive deve-lopment ofprematurechildrenatschoolage: aproposal for a hierarchical model to investigate risk factors. Cad Saude Publica.2011;27:1154---64.
4.StephensBE,WaldenRV,GargusRA,TuckerR,McKinleyL,Mance M,etal.First-weekproteinandenergyintakesareassociated with18-monthdevelopmentaloutcomesinextremelylowbirth weightinfants.Pediatrics.2009;123:1337---43.
5.EhrenkranzRA.EarlynutritionalsupportandoutcomesinELBW infants.EarlyHumDev.2010;86:21---5.
6.Bhatia J. Human milk and the premature infant. Ann Nutr Metab.2013;62:8---14.
7.Tanaka K, Kon N, Ohkawa N, Yoshikawa N, Shimizu T. Does breastfeedingin theneonatal periodinfluence thecognitive functionofvery-low-birth-weightinfantsat5yearsofage?Brain Dev.2009;31:288---93.
8.CameloJSJr,MartinezFE.Nutritionaldilemmasinextremely lowbirthweightinfantsandtheireffectsonchildhood, adoles-cenceandadulthood.JPediatr(RioJ).2005;81:S33---42.
9.LapillonneA,O’ConnorDL,WangD,RigoJ.Nutritional recom-mendationsforthelate-preterminfantandthepreterminfant afterhospitaldischarge.JPediatr.2013;162:S90---100.
10.ThomazDM, Serafim PO, PalharesDB, MelnikovP, Venhofen L, Vargas MO. Comparison between homologous human milk supplementsandacommercialsupplementforverylowbirth weightinfants.JPediatr(RioJ).2012;88:119---24.
11.Arslanoglu S,Moro GE,Ziegler EE, Wapm WorkingGroup On Nutrition.Optimizationofhumanmilkfortificationforpreterm infants:newconceptsand recommendations.JPerinat Med. 2010;38:233---8.
12.KuschelCA,HardingJE.Proteinsupplementationofhumanmilk forpromotinggrowth inpreterminfants. CochraneDatabase SystRev.2000;(2):CD000433.
13.HenriksenC,HaugholtK,LindgrenM,AurvågAK,RønnestadA, GrønnM,etal. Improvedcognitivedevelopmentamong pre-terminfantsattributabletoearlysupplementationofhuman milkwithdocosahexaenoicacid andarachidonic acid. Pedia-trics.2008;121:1137---45.
14.EhrenkranzRA,DusickAM,VohrBR,WrightLL,WrageLA,Poole WK.Growthintheneonatalintensivecareunitinfluences neu-rodevelopmentalandgrowthoutcomesofextremelylowbirth weightinfants.Pediatrics.2006;117:1253---61.
15.TudehopeDI.Humanmilkandthenutritionalneedsofpreterm infants.JPediatr.2013;162:S17---25.
16.AgostoniC,BuonocoreG,CarnielliVP,DeCurtisM,Darmaun D,DecsiT,etal.Enteralnutrientsupplyforpreterminfants: commentaryfromtheEuropeanSocietyofPaediatric Gastroen-terology,HepatologyandNutritionCommitteeonNutrition.J PediatrGastroenterolNutr.2010;50:85---91.
17.Young L, Embleton ND, McCormick FM, McGuireW. Multinu-trientfortificationofhuman breastmilkfor preterminfants following hospital discharge. Cochrane Database Syst Rev. 2013;2:CD004866.
18.O’ConnorDL,JacobsJ,HallR,AdamkinD,AuestadN,CastilloM, etal.Growthanddevelopmentofprematureinfantsfed predo-minantlyhumanmilk,predominantlyprematureinfantformula, oracombinationofhumanmilkandprematureformula.J Pedi-atrGastroenterolNutr.2003;37:437---46.
19.ZachariassenG, FaerkJ,GrytterC,EsbergBH,HjelmborgJ, MortensenS,etal.Nutrientenrichmentofmother’smilkand growthofverypreterminfantsafterhospitaldischarge. Pedia-trics.2011;127:e995---1003.
20.AimoneA,RovetJ,WardW,JefferiesA,CampbellDM,Asztalos E,etal.Growthandbodycompositionofhumanmilk-fed pre-matureinfantsprovidedwithextraenergyandnutrientsearly afterhospitaldischarge:1-yearfollow-up.JPediatr Gastroen-terolNutr.2009;49:456---66.
21.FalcãoMC.Nutritionsupport intheillorpremature newborn infant.RevMed(SãoPaulo).2003;82:11---21.
22.RichardsonDK,CorcoranJD, EscobarGJ,LeeSK.SNAP-IIand SNAPPE-II:Simplifiednewbornillnessseverityandmortalityrisk scores.JPediatr.2001;138:92---100.
23.SchulzKF,AltmanDG,MoherD,CONSORTGroup.CONSORT2010 statement:updatedguidelinesforreportingparallelgroup ran-domisedtrials.BMJ.2010;340:c332.
24.ArgolloN,LessaI,RibeiroS,AbreuKC,PintoJM,FariaRP,etal. Birthweightaspredictorfortheseverityofneonatalbrainwhite matterlesion.ArqNeuropsiquiatr.2006;64:287---94.
25.JohnstonMV,HagbergH.Sexandthepathogenesisofcerebral palsy.DevMedChildNeurol.2007;49:74---8.
26.Andrade SA, Santos DN, Bastos AC, Pedromônico MR, de Almeida-FilhoN,BarretoML.Familyenvironmentandchild’s cognitive development: an epidemiological approach. Rev SaudePublica.2005;39:606---11.