EKSPRESIJA PROTEINA
p53
KOD BOLESNIKA
SA MULTIPLIM MIJELOMOM
Olivera MARKOVIĆ1, Dragomir MARISAVQEVIĆ1, Vesna ČEMERIKIĆ2,
Maja PERUNIČIĆ2, Milica ČOLOVIĆ2
1Kliničkobolnički centar „Bežanijska kosa”, Beograd; 2Institut za hematologiju, Klinički centar Srbije, Beograd
KRATAK SADRŽAJ
Uvod Mutacije gena p53 su jedna od najčešćih stečenih genetskih aberacija i loš prognostički faktor kod bolesnika s
različitim malignim bolestima. Kod bolesnika sa multiplim mijelomom (MM) mutacije ovog gena su retke, a wihov uticaj na tok i prognozu bolesti nije jasan.
Ciq rada Ciq studije je bio da se utvrde učestalost i klinički značaj imunohistohemijske ekspresije proteina p53kod
bolesnika sa novootkrivenim multiplim mijelomom.
Metod rada U ispitivawe je ukqučeno 58 bolesnika sa novootkrivenim MM (26 žena i 32 muškarca), prosečne starosti
od 62 godine. Dijagnoza MM je postavqena na osnovu standardnih kriterijuma. Klinički stadijum bolesti je određen pre ma klasifikaciji Durija i Salmona (Durie – Salmon), histološki gradus na osnovu morfoloških osobina dominantne popu lacije plazmocita, a histološki stadijum na osnovu procenta plazmocita u kostnoj srži. Ekspresija p53 je ispitivana na
parafinskim isečcima kostne srži korišćewem standardne imunohistohemijske analize s antitelom prema proteinu p53. Uzorci su se smatrali pozitivnim ako je zabeležena jasna pozitivnost jedra u više od 5% plazmocita.
Rezultati Nukleusna ekspresija proteina p53 utvrđena je kod devet bolesnika (15,52%). Imunohistohemijska ekspresija
proteina p53 nije bila u značajnoj povezanosti sa kliničkim stadijumom bolesti (I+II prema III), koncentracijom β2mikroglo bulina u serumu (≤6 mg/l prema >6 mg/l), histološkim gradusom (I prema II+III), histološkim stadijumom (<20% prema 2150% prema >50%) i stepenom osteolitičkih lezija (≤3 prema >3). Medijana preživqavawa bolesnika s imunoreaktivnošću na
protein p53 bila je 10 meseci, a kod bolesnika s izostankom imunoreaktivnosti na p53 36 meseci. Međutim, ova razlika nije bila statistički značajna (p=0,2).
Zakqučak Učestalost imunohistohemijske ekspresije proteina p53 kod ispitanika sa novootkrivenim MM je relativno
mala. Nije utvrđena povezanost ekspresije ovog proteina s kliničkim i histološkim osobinama bolesti, niti sa vreme nom preživqavawa bolesnika.
Kqučne reči: multipli mijelom; imunohistohemija; p53; biologija; prognoza
UVOD
Gen p53 je jedan od kqučnih gena u složenoj mre
ži signalnih puteva odgovornih za regulaciju ćelij skog ciklusa i apoptoze. Wegov genski proizvod, pro tein p53, kontroliše ćelijski ciklus (u G1iG2 fa
zi) i apoptozu ćelija odgovarajući na nenormalne proliferacione signale i stres, ukqučujući ošte ćewe DNK [1]. Po svojoj strukturi je jedarni fosfo protein čiji se gen nalazi na kratkom kraku hromo zoma 17 [2]. U normalnim ćelijama koje nisu izlože ne stresu protein p53 se vezuje za MDM2, JNKili
Pirh2, koji promovišu wegovu degradaciju preko pu
ta ubikvitinproteozoma [3]. Posle izlagawa ćelije stresu ili oštećewa DNK različitim mehanizmima, dolazi do aktivacije gena p53, koji učestvuje u otkla
wawu nastalog oštećewa ili dela DNK kada je ošte ćewe veliko [3]. Čiwenice da je p53 najčešće deleti
ran ili mutiran gen u tumorima kod čoveka i da po rodice sa germinativnim mutacijama 53 imaju pove ćanu sklonost za malignitete u mlađem životnom do bu ukazuju na značajnu ulogu gena p53 u sprečavawu ma
lignog preobražaja [3, 4]. Inaktivacija proteina p53
može biti posledica mutacije wegovog gena ili gu bitka alela mehanizmom insercije i delecije. Muta cije gena p53 utiču na interakciju proteina p53sa
DNK, odnosno narušavaju wegov strukturni integri tet, vodeći delimičnom ili potpunom gubitku wego
ve funkcije [4]. Dosad je opisano 21.000 različitih mutacija gena p53 koje su zabeležene u različitim
tipovima tumora kod qudi, a oko 20% wih se nalazi u pet tzv. žarišnih (hotspot) kodona [46]. Mutaci
je gena p53 vode ekspresiji izmewenog proteina p53
(90%) ili potpunom izostanku proteina (10%). Ia ko najčešće mutacije gena p53 vode potpunom gubit
ku aktivnosti proteina, u više od 50% retkih muta cija ovog gena zadržava se značajna aktivnost prote ina [4]. Mutantni oblici proteina p53 predstavqaju
vrlo heterogenu grupu s različitim stepenom gubit ka aktivnosti, što može doprineti različitom kli ničkom ispoqavawu tumora, ali i teškoćama u utvr đivawu wihovog značaja u kliničkim studijama [4]. Do inaktivacije gena p53 može doći i inhibicijom
promotera gena p53, odnosno povećawem ekspresije
inhibitora proteina p53 [5]. Na primer, nagomila
vawe onkoproteina MDM2, koji pravi kompleks sa
proteinom p53, dovodi do gubitka aktivacione spo
sobnosti proteina p53. Slično tome, vezivawe za vi
rusne proteine može izazvati gubitak wegove aktiv nosti ili ubrzawe wegovog raspada. U nekim solid nim malignitetima opisana je i citoplazmatska lo kalizacija proteina p53, koja može doprineti gubit
ku aktivnosti proteina p53 [5].
Mutacije gena p53beleže se kod više od 50% so
lidnih tumora, a u nekima od wih (tumori pluća i dojke) su indikator loše prognoze bolesti[7, 8].
U hematološkim malignitetima mutacije gena p53
su ređe, ali, kada postoje, pokazateq su loše prog noze, naročito kod bolesnika s akutnom mijeloid nom leukemijom, mijelodisplastičnim sindromima i agresivnim nehočkinskim (nonHodgkin) limfo
mima [9]. Nastanak ovih mutacija je često povezan s recidivom ili pogoršawem hematoloških malig niteta, odnosno s agresivnijim tokom bolesti [9]. Mutacije gena p53 se retko otkrivaju i kod bolesni
ka sa multiplim mijelomom (MM) [1016], a wihov značaj u patogenezi i uticaj na tok bolesti nisu u potpunosti jasni.
CIQ RADA
Ciq rada je bio da se odrede učestalost imunohi stohemijske ekspresije proteina p53 i wegov klini
čki značaj kod bolesnika sa novootkrivenim MM.
METOD RADA
Ispitivawem je obuhvaćeno 58 bolesnika sa novo otkrivenim MM, dijagnostikovanih i lečenih u In stitutu za hematologiju Kliničkog centra Srbije u Beogradu. Ispitivawe je obavqeno od januara 1997. do januara 2000. godine. Ispitanici su nadgledani najmawe 27 meseci, a najviše 63 meseca (studija je za kqučena aprila 2002. godine). Kod svih bolesnika su u lokalnoj anesteziji urađene aspiraciona punkci ja i trepanaciona biopsija grebena ilijačne kosti. Dijagnoza MM postavqena je na osnovu kriterijuma
ChronicLeukemia-MyelomaTaskForce [17]. Klasifika
cija po kliničkim stadijumima izvršena je po siste mu Djurija i Salmona (Durie – Salmon) [18]. Analizi
rani su sledeći parametri: starost, kompletna krv na slika sa leukocitnom formulom, funkcija bubre ga (urea, kreatinin), kalcijum, fosfor i ukupni pro teini u serumu, elektroforeza i imunoelektrofore za proteina, CRP, β2mikroglobulin, proteini u 24
časovnom urinu (kvalitativno i kvantitativno) i prisustvo litičnih lezija kostiju. Histološka kla sifikacija je urađena prema modelu koji su predloži li Sejler (Sailer) i saradnici [19] 1995. godine, pre
ma kojem se klasifikacija obavqa na osnovu morfo loških osobina dominantne populacije plazmocita (gradus I – zreli, gradus II – intermedijarni, gradus III – plazmablastni mijelom). Prema stepenu infil
tracije kostne srži, bolesnici su svrstani u tri gru pe (stadijum I – mawe od 20% plazmocita, stadijum II
– 2050% plazmocita, stadijum III – više od 50% pla
zmocita u kostnoj srži) prema modelu Bartla (Bar tl) i saradnika [20]. Proliferaciona aktivnost mi
jelomskih ćelija ispitana je metodom imunohistohe mije uz korišćewe antitela prema Ki67, prema mode
lu Laja (Lai) i saradnika [21].
Svi bolesnici su lečeni konvencionalnom hemi oterapijom (32 bolesnika protokolom VAD, 14 bole
snika protokolom VMCP, 11 bolesnika protokolom
VBMCP i jedan bolesnik kombinacijom prednizona
i melfalana). Ukupno preživqavawe je računato od trenutka postavqawa dijagnoze bolesti.
Metod imunohistohemije
Ekspresija proteina p53 ispitivana je na parafin
skim isečcima kostne srži dobijenim trepanobiop sijom grebena ilijačne kosti, uz upotrebu trokara po Jamšidi (Jamshida) u lokalnoj anesteziji. Cilindri
kostne srži su fiksirani u B5 fiksativu, dekalci
fikovani u petoprocentnom vodenom rastvoru mra vqe kiseline u trajawu od šest sati i kalupqeni u parafinu. Sečewem parafinskih blokova, sa longitu dinalno usmerenom kosti, dobijeni su isečci debqi ne 3 µm, koji su zatim deparafinisani ksilolom i
rehidrirani alkoholima. S obzirom na to da su pre parati fiksirani u B5, pre započiwawa postupka
precipitati živinog pigmenta otklawani su sa de parafinisanih isečaka Lugolovim rastvorom i na trijumtiosulfatom. Za demaskirawe epitopa prime wen je mikrotalasni pretretman u 0,01 M citratnom puferu pH 6,0 (dva puta po pet minuta). Kao primar
no antitelo korišćeno je komercijalno monoklon sko antitelo prema proteinu p53 (DAKO, M7001 klon DO7). Za vizuelizaciju je korišćen LSAB2 (DAKO LSAB2 System, KO675), a kao hromogen upotrebqen je AEC (DAKO, K3464). Posle nanošewa hromogena pri
mewivano je kontrastno bojewe hematoksilinom po Majeru (Mayer). Svi uzorci kostne srži su pregleda
ni na uveličawu od 400 puta, koje su nezavisno ana lizirala dva autora. Ekspresija proteina p53 u mije
lomskim ćelijama utvrđena je na osnovu procenta pla zmocita (određenog brojawem najmawe 500 plazmoci ta na više različitih vidnih poqa), koji su pokazi vali imunoreaktivnost s antitelom p53. Uzorci su
smatrani pozitivnim kada je u 5% ili više plazmo cita zabeležena jasna pozitivnost jedra [22]. Kao po zitivna kontrola korišćeni su parafinski isečci kolorektumskog karcinoma u kojem je utvrđen visok stepen ekspresije ovog proteina, a kao negativna kon trola uzorci na kojima je umesto primarnog antite la korišćen pufer.
Statistička analiza podataka
Za statističku analizu podataka korišćen je pro gramski paket SPSS, verzija 8. Povezanost imunohi
stohemijske ekspresije proteina p53 sa kliničkim,
biohemijskim i patohistološkim parametrima bo lesti ispitivana je Spirmanovim (Spearman) koefi
cijentom korelacije ranga i χ2testom. Uticaj prisu
stva imunoekspresije proteina p53 na preživqava
we bolesnika procewivan je KaplanMajerovim (Ka plain-Meier) metodom (logrank test).
REZULTATI
Kliničke odlike ispitivanih bolesnika prika zane su u tabeli 1. Imunohistohemijska reaktivnost uzoraka na antitelo p53 utvrđena je kod devet od 58
bolesnika, ili 15,52% ispitanika (Slika 1). Prime nom Spirmanovog koeficijenta korelacije ranga i χ2testa nije utvrđena povezanost imunohistohemij
SLIKA 1. Isečak kostne srži bolesnika sa multiplim mijelo mom koji pokazuje imunoreaktivnost plazmaćelija s antitelom p53 (uveličawe ×400).
FIGURE 1. Section of paraffin-embedded bone marrow specimen in myeloma patient showing the immunoreactivity of plasma cells with anti-p53 antibody (magnification, ×400).
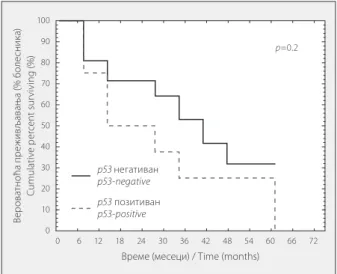
GRAFIKON 1. Verovatnoća preživqavawa bolesnika s imuno reaktivnošću p53 u 5% i više plazmocita (isprekidana linija) i bolesnika s imunoreaktivnošću p53 u do 5% plazmocita (pu na linija).
GRAPH 1. Probability of survival in patients with p53 immunoreactivity in ≥5% of plasma cells (broken line), compared to patients with p53 im-munoreactivity in <5% of plasma cells (full line) (log-rank test). TABELA 1. Kliničke odlike bolesnika sa multiplim mijelomom.
TABLE 1. Clinical features of patients with multiple myeloma on pres-entation.
Odlike
Variables
Broj bolesnika Numb
er of pa
tien
ts
Sredwa vrednos
t
M
ean v
alue
Medi
jana
M
edian
Ops
eg
R
ange
Starost (godine)
Age (years) 58 61.74 63 3880
Ukupni proteini (g/l)
Total proteins (g/l) 58 91.98 90 55147
Albumini (g/l)
Albumins (g/l) 58 34.76 35.05 17.1646.32 Hemoglobin (g/l)
Hemoglobin (g/l) 58 96.57 92.50 48165
Trombociti (×109/l)
Platelets (×109/l) 58 226.79 221 27690 CRP (mg/l)
CRP (mg/l) 38 16.14 9.50 0.0095
β2mikroglobulin (mg/l)
β2-microglobulin (mg/l) 25 7.12 3.87 1.2820.7 Kreatinin (µmol/l)
Creatinine (µmol/l) 58 186.14 118.65 56896
Kalcijum (mmol/l)
Calcium (mmol/l) 58 2.53 2.39 2.003.90
Proteinurija (g/24 h)
Urinary proteins (g/24 h) 57 1.79 1.20 0.106.70
Broj osteolitičkih lezija
Number of osteolytic lesions 58 3.43 3 0.008
Plazmociti u kostnoj srži (%)
Plasma cells in bone marrow (%) 58 48.61 44 1295
zmocita) je bila 10 meseci, a kod bolesnika s izostan kom imunoreaktivnosti na ovo antitelo (do 5% pla zmocita) 36 meseci, ali ova razlika nije bila stati stički značajna (Grafikon 1).
DISKUSIJA
Ćelije sa nedostatkom aktivnosti p53 nemaju spo
sobnost zaustavqawa ćelijskog ciklusa u fazi G1 po
sle oštećewa DNK, što dovodi do izostanka otklawa wa genetski oštećene ćelije mehanizmom programi rane ćelijske smrti (apoptozom) [1]. Gubitak funkci je proteina p53 najčešće je posledica “missense” muta
cije gena p53, zatim “nonsense” mutacije gena ili dele
cije regiona 17p13 [3]. Učestalost i distribucija me
sta mutacija se razlikuju između maligniteta koja po tiču od različitih vrsta tkiva. Mutacije gena p53 mo
gu biti locirane na različitim mestima, ali su naj češće između aminokiselinskih rezidua 130 i 290. Različiti mutirani oblici ovog gena imaju i razli čita biološka i biohemijska svojstva, zbog čega bo lesnici s različitim mutiranim oblicima protei
nap53 imaju i različitu prognozu [4].
Mutacije gena p53 se otkrivaju različitim moleku
larnim tehnikama (PCR, FISH, Southernblotting), ali i
tehnikom imunohistohemije, kojom se prisustvo mu tacija određuje indirektno. Naime, zbog kratkog po luživota (620 minuta) „divqi” tip proteina p53
se ne akumulira u normalnim tkivima u količina ma koje se mogu otkriti imunohistohemijskim meto dom. Mutirani oblici proteina imaju duži poluži vot od „divqeg” tipa, što dovodi do nakupqawa veli ke količine ovog proteina u malignim ćelijama, ko ji na taj način postaje detektabilan imunohistohe mijskim metodom [3]. Međutim, imunoreaktivnost na antitelo p53 nije u apsolutnoj korelaciji sa pri
sustvom mutacija gena p53 zbog toga što tzv. nonsense
mutacije ovog gena dovode do sinteze izmewenog pro lesnika, vrednošću ukupnih proteina, albumina, he
moglobina, CRP, β2mikroglobulina, kreatinina i
kalcijuma u serumu, brojem trombocita i odgovorom na terapiju. Imunohistohemijska ekspresija protei
nap53 nije bila statistički značajno povezana ni sa
kliničkim stadijumom bolesti (I+II prema III), histo
loškim gradusom (I prema II+III), histološkim stadi
jumom (I prema II prema III) i brojem osteolitičkih
lezija (≤3 prema >3).
Medijana preživqavawa bolesnika sa jedarnom imunoreaktivnošću na antitelo p53 (5% i više pla
Време (месеци) / Time (months)
Ве
ро
ва
тн
оћ
а
пр
еж
ив
љ
ав
ањ
а (% б
ол
ес
ни
ка
)
Cu
m
ul
at
ive p
er
ce
nt
s
ur
vi
vi
ng
(%
)
0 10 20 30 40 50 60 70 80 90 100
0 6 12 18 24 30 36 42 48 54 60 66 72
p=0.2
p53 негативан
p53-negative
teina koji gubi imunoreaktivnost s antitelom p53.
Takođe, ekspresija ovog proteina može biti reguli sana i drugim mehanizmima, nezavisnim od genskih mutacija [4].
U ovoj studiji ekspresija jedra proteina p53 zabe
ležena je kod 15,52% bolesnika sa novootkrivenim mijelomom. Mala učestalost ekspresije p53 (do 10%
bolesnika) [10, 11, 1316] ili čak izostanak mutacije gena p53 [13] opisani su u studijama koje su koristi
le molekularne tehnike dokazivawa mutacija (uglav nom PCR), iz čega je izveden zakqučak da mutacije
ovog gena nisu od većeg značaja za patogenezu MM. Za nimqivo je da znatno veću učestalost mutacija gena
p53 (16,639% bolesnika) opisuju autori studija u ko
jima je primewivana imunohistohemijska tehnika ko jom se mutacije gena p53 otkrivaju indirektno [12,
2125]. Pruneri (Pruneri) i saradnici [25] su utvrdi
li imunoreaktivnost na antitelo p53 kod čak 39,6%
ispitanika, dok su u istoj grupi bolesnika mutaci je PCR tehnikom dokazane kod svega 8,8% wih. Razli
ke u učestalosti mutacija gena p53 uslovqene kori
šćenom tehnikom otkrivawa pripisuju se nepotpu noj analizi svih regiona gena p53PCR tehnikom, od
nosno lažno pozitivnoj imunohistohemijskoj anali zi kao posledici povećane količine proteina p53u
normalnim tkivima sa brzom proliferacijom (ak tivirani Tlimfociti) ili vezivawa za neke pro
teine koji ga inaktiviraju, ali produžavaju wegov život [9]. S obzirom na to da nema optimalnog meto da za procenu aktivnosti proteina p53, kombinova
na primena različitih metoda otkrivawa, ali i ana liza transkripcione aktivnosti gena p53 određiva
wem aktivnosti gena koje aktivira gen p53 (MDM2, p21), mogla bi doprineti donošewu pouzdanijih za
kqučaka o značaju gubitka aktivnosti ovog gena u po jedinim malignim oboqewima.
Za razliku od bolesnika sa multiplim mijelomom, mutacije gena p53 se češće otkrivaju u plazmocitnoj
leukemiji (2040% bolesnika) [26]. Pretpostavqa se da su ove mutacije, kao „kasni događaj” u malignoj tran sformaciji plazmocita, možda odgovorne za prelazak u agresivniji oblik bolesti, tj. leukemijsku fazu.
U literaturi je malo podataka o uticaju mutacija gena p53 na kliničke odlike i tok bolesti. U našoj
studiji nije zabeležena značajna povezanost imuno histohemijske ekspresije proteina p53 sa kliničkim
i histološkim parametrima bolesti, što je u skla du s rezultatima studije Pajdaša (Paydaş) i saradni
ka [23]. S druge strane, Kanavaros (Kanavaros) i sarad
nici [24] su utvrdili da je povećana ekspresija pro teina p53 povezana sa visokim proliferacionim po
tencijalom malignih ćelija, plazmoblastnom morfo logijom i visokim stepenom infiltracije kostne sr ži. U literaturi postoje podaci da mutacije p53 ima
ju uticaj na razvoj rezistencije malignih ćelija na citotoksične lekove kod različitih vrsta solidnih i hematoloških maligniteta, što je u vezi sa wego vim značajem u očuvawu integriteta genoma i kquč noj ulozi u apoptozi. Međutim, postoji malo podata ka o povezanosti mutacija gena p53 sa rezistencijom
mijelomskih ćelija na ove lekove. U pojedinim studi jama je utvrđena povezanost delecije gena p53 sa re
zistencijom bolesti na terapiju [27, 28]. Međutim,
u našoj studiji, kao ni u studiji Pajdaša i saradni ka [23], nije utvrđena razlika u odgovoru na terapiju u odnosu na imunoekspresiju na antitelo p53. Opreč
ni podaci o značaju p53 za rezistenciju na terapiju
mogu se protumačiti kako različitim genetskim i negenetskim mehanizmima inaktivacije genap53, ta
ko i složenošću još nedovoqno razjašwenih meha nizama rezistencije na lekove [29].
U nekoliko studija je utvrđeno da su delecije gena
p53 nezavisan prognostički faktor u MM bez obzi
ra na to da li se primewuje konvencionalna hemio terapija ili visokodozna hemioterapija s autologom transplantacijom kostne srži [28, 30]. Kraće preži vqavawe bolesnika sa mijelomom i nukleusnom imu noekspresijom proteina p53 utvrdili su Pruneri i
saradnici [25] 2003. i Kumar (Kumar) i saradnici
[12] 2004. godine, zakqučujući da je imunohistohemij ska ekspresija proteina p53 pokazateq agresivnijeg
toka bolesti. Iako su naši bolesnici sa ekspresi jom jedra proteina p53 živeli u proseku tri i po pu
ta kraće nego bolesnici s izostankom imunoekspre sije ovog proteina (10 prema 36 meseci), ova razlika nije dostigla nivo statističke značajnosti.
ZAKQUČAK
Iako ova studija nije sa sigurnošću utvrdila kli nički značaj imunohistohemijske ekspresije protei
nap53 u multiplom mijelomu, nadamo se da će buduća
ispitivawa na većem broju ispitanika i praćewe prisustva mutacija u različitim fazama bolesti do neti pouzdanije zakqučke o ulozi mutacija gena p53
u ovoj bolesti.
LITERATURA
1. VogelsteinB,KinzlerKW.p53functionanddysfunction.Cell12; 70:523-5.
2. MartinACR,FacchianoAM,CuffAL,etal.Integratingmutation dataandstructuralanalysisofthep53tumour-suppressorprotein. HumanMutation2002;1:14-64.
3. PalmeroI,PetersG.Perturbationofcellcycleregulatorsinhuman cancer.CancerSurv16;27:351-67.
4. SoussiT,KatoS,LevyP,IshiokaC.ReassessmentoftheTP53muta-tiondatabaseinhumandiseasebydataminingwithalibraryof TP53missensemutations.HumMutat2005;25:6-17.
5. HamrounD,KatoS,IshiocaC,ClaustersM,BeroudC,SoussiT. TheUMDTP53databaseandwebsite:updateandrevisions.Hum Mutat2006;27(1):14-20.
6. SoussiT,LozanoG.p53mutationheterogeneityincancer.Biochem-icalandBiophysicalResearchCommunications2005;331:34-42. 7. HorioY,TakahashiT,KuroishiT,etal.Prognosticsignificanceof
p53mutationsand3pdeletionsinprimaryresectednon-smallcell lungcancer.CancerRes13;53:1-6.
. ThorlaciusS,BorresenAL,EufjordJE.Somaticp53mutationsin humanbreastcarcinomasinanIcelandicpopulation:Aprognos-ticfactor.CancerRes13;53:1637-40.
. ImamuraJ,MiyoshiI,KoefflerHP.p53inHematologicmalignan-cies.Blood14;4():2412-21.
10. OllikainenH,SyrjanenS,KoskelaK,etal.p53genemutationsare rareinpatientsbutcommoninpatient-originatingcelllinesinmul-tiplemyeloma.ScandJClinLabInvest17;57(4):21-. 11. NeriA,BaldiniL,TreccaL,etal.p53genemutationsinmultiple
myelomaareassociatedwithadvancedformsofmalignancy.Blood 13;1(1):12-35.
indicesexpressionofp53andmultidrugresistancegenesinmulti-plemyelomapatients.AnalQuantCytolHistol2004;26(5):271-7. 13. CorradiniP,InghiramiG,AstolfiM,etal.Inactivationoftumor
suppressorgenes,p53andRb1inplasmacelldyscrasias.Leuke-mia14;(5):75-67.
14. PreudhommeC,FaconT,ZandeckiM,etal.Rareoccurrenceofp53 genemutationsinmultiplemyeloma.BrJHaematol12;1(3): 440-3.
15. OwenRG,DavisSA,RandersonJ,etal.p53genemutationsinmul-tiplemyeloma.MolPathol17;50(1):1-20.
16. YasugaY,HirosawaS,YamamotoK,etal.N-rasandp53genemuta-tionsareveryrareeventsinmultiplemyeloma.IntJHematol15; 62(2):1-7.
17. ChronicLeukemiaandMyelomaTaskForceoftheNationalCan-cerInstitute.Proposedguidelinesforprotocolstudies.Plasmacell myeloma.CancerChemotherRep173;4:145-5.
1. DurieBG,SalmonSE.Aclinicalstagingsystemformultiplemye-loma.Cancer175;36:42-54.
1. SailerM,VykoupilKF,PeestD,etal.Prognosticrelevanceofa histologicclassificationsystemappliedinbonemarrowbiopsies frompatientswithmultiplemyeloma:Ahistopathologicalevalua-tionofbiopsiesfrom153untreatedpatients.EurJHaematol15; 54:137-46.
20. BartlR,FrischB,Fateh-MoghadamA,etal.Histologicclassifica- tionandstagingofmultiplemyeloma.Aretrospectiveandprospec-tivestudyof674cases.AmJClinPathol17;7:342-55. 21.
LaiMD,MedeirosQ,WilsonCS,etal.Expressionofthecell-cycle-relatedproteinsE2F-1,p53,mdm-2,p21waf-1,andKi-67 inmulti-plemyeloma:correlationwithcyclin-D1immunoreactivity.Mod Pathol1;11(7):642-7.
22. ElghetanyTM,AlterB.p53Proteinoverexpressioninbonemarow biopsiesofpatientswithShwaahman-DiamondSyndromehasa prevalencesimilartothatofpatientswithrefractoryanemia.Arch PatholLabMed2002;126:452-5.
23. PaydaşS,ŞahinB,SeyrekE,ZorludemirS.p53proteinexpression inmultiplemyeloma.AnnMedSci17;6:15-17.
24. KanavarosP,StefanakiK,VlachonikolisJ,etal.Immunohistochem-icalexpressionofthep53,p21/waf-1,Rb,p16andKi-67proteinsin multiplemyeloma.AnticancerRes2000;20(6):461-25.
25. PruneriG,CarboniN,BaldiniL,etal.Cellcycleregulatorsinmul-tiplemyeloma:prognosticimplicationofp53nuclearaccumulation. HumPathol2003;34(1):41-7.
26. HallekM,BergsagelPl,AndersonKC.Multiplemyeloma:Increas-ingevidenceforamultisteptransformationprocess.Blood1; 1(1):3-21.
27. ElnenaeiMo,Gruszka-WestwoodAM,A’HerntR,etal.Geneabnor-malitiesinmultiplemyeloma;therelevanceofTP53,MDM2,and CDKN2A.Haematologica2003;(5):52-37.
2. ChangH,QiC,YiQL,ReeceD,StewartAK.p53genedeletionby fluorescenceinsituhybridisationisanadverseprognosticfactor forpatientswithmultiplemyelomafollowingautologousstemcell transplantation.Blood2005;105(1):35-60.
2. LiuS,BishopRW,DasmahapatraB,WangY.Pharmacogenomicof thep53tumorsuppressoranditsroleincancerchemoresistance. DrugDevRes2004;62:254-72.
30. DrachJ,AckermannJ,FritzE,etal.Presenceofap53genedele-tioninpatientswithmultiplemyelomapredictsforshortsurvival afterconventional-dosechemotherapy.Blood1;2(3):02-.
Introduction Although mutations of p53 are one of the most often acquired genetic changes in malignant tumors, these mutations are rare events in patients with newly diagnosed multiple myeloma (MM). Moreover, there are a few literature data about clinical significance of p53 overexpression in mul-tiple myeloma.
Objective The aim of our study was to evaluate the clinical significance of p53 immunoexpression in multiple myeloma. Method A total of 58 patients with newly diagnosed MM (26 females and 32 males, mean age 62 years) were enrolled in the study. The diagnosis of MM was made according to criteria of Chronic Leukemia-Myeloma Task Force. Clinical staging was done according to Durie and Salmon classification (4 patients had disease stage I, 15 patients stage II and 39 patients stage III). The histological grade and histological stage were determined according to predominant plasma cell morphology and vol-ume of myeloma infiltration, respectively. Standard immuno-histochemical analysis with p53 antibody in B5-fixed and par-affin-embedded bone marrow specimens was used to eval-uate the expression of p53 in myeloma cells. The specimens were considered positive when ≥5% of plasma cells exhibited clear nuclear positivity.
Results Out of 58 patients, p53 expression was detected in 9 (15.52%). No significant correlation was found between p53
expression and clinical stage (I+II vs. III), ß2-microglobulin level (≤6 mg/L vs. >6mg/L), histological grade (I vs. II+III), histologi-cal stage (<20% vs. 21-50% vs. >50%) and the extent of osteo-lytic lesions (≤3 vs. >3 lesions). Median survival of patients with p53 immunoreactivity in =>5% of plasma cells was 10 months, whilst median survival of patients with p53 immunoreactivi-ty in <5% of plasma cells was 36 months. However, such differ-ence was not significant (p=0.2).
Conclusion The frequency of p53 immunoexpression in our group of newly diagnosed MM was relatively low. Although p53 immunoexpression was not associated with clinical and histological features of more aggressive disease, or with short-er survival, furthshort-er investigations of largshort-er group of patients will lead to final conclusions.
Key words: multiple myeloma; p53; immunohistochemistry; clinical significance; prognosis
Olivera MARKOVIĆ
Kliničko-bolnički centar „Bežanijska kosa” Auto put bb, 11080 Zemun
Tel.: 011 559 896 Faks: 011 699 937 E-mail: [email protected]
THE EXPRESSION OF p53 PROTEIN IN PATIENTS WITH MULTIPLE MYELOMA
Olivera MARKOVIĆ1, Dragomir MARISAVLJEVIĆ1, Vesna ČEMERIKIĆ2, Maja PERUNIČIĆ2, Milica ČOLOVIĆ2 1Medical Training Center “Bežanijska kosa”, Belgrade; 2Institute of Hematology, Clinical Center of Serbia, Belgrade