1 -Foto: Bruno Collaço
BRUNO JORGE RODRIGUES COLLAÇO
HIERARQUIA DE DOMINÂNCIA DURANTE A OBTENÇÃO DE
ALIMENTO EM
CEBUS APELLA
E
CEBUS LIBIDINOSUS
EM
CATIVEIRO
Universidade Federal do Rio Grande do Norte
Centro de Biociências
Programa de Pós-graduação em Psicobiologia
BRUNO JORGE RODRIGUES COLLAÇO
HIERARQUIA DE DOMINÂNCIA DURANTE A OBTENÇÃO DE
ALIMENTO EM
CEBUS APELLA
E
CEBUS LIBIDINOSUS
EM
CATIVEIRO
Dissertação apresentada ao Programa de Pós-Graduação em Psicobiologia no Departamento de Fisiologia da Universidade Federal do Rio Grande do Norte, como parte dos requisitos para a obtenção do título de Mestre.
Orientador: Prof. Arrilton Araújo
3
Divisão de Serviços Técnicos
Catalogação da Publicação na Fonte. UFRN / Biblioteca Central Zila Mamede
Collaço, Bruno Jorge Rodrigues.
Hierarquia de dominância durante a obtenção de alimento em Cebus Apella e Cebus Libidinosus / Bruno Jorge Rodrigues Collaço. – Natal,
RN, 2008.
57 f.
Orientador: Arrilton Araújo.
Dissertação (Mestrado) – Universidade Federal do Rio Grande do Norte. Centro de Biociências. Programa de Pós-Graduação em Psicobiologia.
1. Cebus – Dissertação. 2. Hierarquia de dominância– Dissertação. 3. Comportamento alimentar – Dissertação. I. Araújo, Arrilton. II. Universidade Federal do Rio Grande do Norte. III. Título.
RN/UF/BCZM CDU 599.822(043.3)
5
Por você, antes um e agora dois.
AGRADECIMENTOS
Acredito que devemos agradecer a cada minuto sobre tudo que recebemos de todos, por isso talvez neste momento precise na verdade não mais agradecer, mas tornar público a quem não esteve no dia-a-dia deste trabalho, quantas pessoas contribuíram para sua conclusão.
Talvez as pessoas que menos apareceram e que na verdade determinaram a possibilidade real de tudo, abrindo suas portas e corações para receber um desconhecido, que hoje deve um degrau significativo de sua vida acadêmica a elas: Dona Fátima; Daniela; Max e todos da sua família, a vocês meus respeitos e gratidão.
Arrilton Araújo, meu orientador, com sua paciência a confiança, talvez eu mesmo não a tivesse!, que se materializaram em liberdade e troca, talvez mais de lições pessoais que acadêmicas, Fátima Arruda, que sem saber, acabou me levando a uma experiência que teria mais na frente, se tornado uma luz no fim do túnel, Fívia Lopes, com apoio e amizade em momentos importantes e Simone Porfírio, que sem saber deu início a retomada do meu caminho acadêmico.
Lembro que este projeto somente pode ser realizado através da minha aceitação pelo Programa de Pós-Graduação em Psicobiologia da UFRN, onde pude contar com o apoio financeiro da Bolsa de Mestrado do sistema CAPES.
Mário Daniel e toda a equipe do IBAMA – Alagoas, que mantiveram os animais de minha pesquisa a minha disposição por todo o tempo que solicitei, mesmo passando por pressões internas.
7 -Meu compadre-irmão Ubiratan Gonçalves (Bira), quando dedicou seu apoio, força e companheirismo, mesmo estando no mesmo barco.
A todos os familiares e amigos, antigos e novos, quando às vezes, de forma direita ou torta tornaram-me um pouco mais forte, para o que havia de vir.
E finalmente, Karlla Lima (agora Collaço!),... Que todos os dias foi parte da preparação de todo o processo, auxiliar singular, colega admirável, esposa especial, companheira e defensora.
SUMÁRIO
LISTA DE FIGURAS ix
LISTA DE TABELAS x
INTRODUÇÃO GERAL 11
OBJETIVOS 15
Objetivos Gerais 15
Objetivos Específicos 15
ARTIGO 16
Resumo 18
Abstract 19
Introdução 20
Materiais e Métodos 22
Sujeitos de Estudo 22
Local de Estudo 22
Métodos de Observação 25
Análise dos Dados 27
Resultados 28
Estrutura Hierárquica 28
Teste de Obtenção de Recurso Alimentar 32
Discussão 38
Conclusão 42
Agradecimentos 43
Referências 43
REFERÊNCIAS BIBLIOGRÁFICAS 48
ANEXOS – PLANILHAS DE OBSERVAÇÃO NORMAS PARA PUBLICAÇÃO
9
-LISTA DE FIGURAS
Figura 1 – Vista externa do recinto (a) e portas de acesso aos recintos de cada
grupo (b). 24
Quadro I – Etograma de identificação para tipos de interação física e não-física, e padrões comportamentais em Cebus. Adaptado dos etogramas de Visalberghi et al. (2006), Mendonça - Furtado (2006). 25 Figura 2 – Objeto utilizado para o TORA (teste de obtenção de recurso alimentar), montado a esquerda e desmontado a direita. 26 Figura 3 – Freqüência dos padrões comportamentais executados pelos
membros agressores do Grupo de C. apella. 31
Figura 4 – Freqüência dos padrões comportamentais recebidos pelos membros
agredidos do Grupo de C. apella. 31
Figura 5 – Freqüência dos padrões comportamentais recebidos pelos membros
agredidos do Grupo de C. libidinosus. 33
Figura 6 – Árvores hierárquicas dos Grupos de C. apella e C. libidinosus, onde, o membro hierarquicamente dominante, encontra-se na base da árvore. 34 Figura 7a – Tempo total de interação em minutos, com o objeto teste, de cada membro do grupo de C. apella nos padrões comportamentais descritos. 35 Figura 7b - Tempo total de interação em minutos, com o objeto teste, de cada membro do grupo de C. libidinosus nos padrões comportamentais descritos. 35 Figura 8 – Freqüência de interação com o objeto teste, de cada membro do
grupo de C. apella durante o período de testes. 37
Figura 9 – Freqüência de interação com o objeto teste, de cada membro do grupo de C. libidinosus durante o período de testes. 37
LISTA DE TABELAS
Tabela 1 – Composição e identificação dos grupos de Cebus apella e Cebus
libidinosus. 23
Tabela 2 – Resultados quantitativos de cada evento comportamental apresentado pelos animais do Grupo de C. apella, separando membros agressores (I.D.A. – Indivíduo Agressor) e membros agredidos (I.D.R. –
Indivíduo Receptor). 29
Tabela 3 – Resultados quantitativos de cada evento comportamental apresentado pelos animais do Grupo de C. libidinosus, separando membros agressores (I.D.A.) e membros agredidos (I.D.R.). 29 Tabela 4 – Matriz de direcionamento das interações agonísticas e índice de Landau (h) do Grupo de C. apella, com o somatório total das interações de
cada membro e sua posição. 33
Tabela 5 – Matriz de direcionamento das interações agonísticas e índice de Landau (h) do Grupo de C. libidinosus, com o somatório total das interações
11
-INTRODUÇÃO GERAL
Algumas espécies sociais mantêm relações assimétricas, que podem por vezes ser estáveis, quanto ao comportamento agonístico. Nesse caso um indivíduo termina suplantando outro quando estes competem seja por alimento, abrigo ou parceiros (Dewsbury, 1982; Drews, 1993; Reed et al., 1997), uma vez que na rede sócio-ecológica a competição é um momento crítico. Destas competições é determinado um indivíduo dominante e outro subordinado, sem muitas vezes serem devidamente notados os indivíduos constituintes das faixas intermediárias (Reader e Laland, 2001).
Assim a hierarquia determinada pode ter algumas formas de organização. A consistência e previsibilidade na interação indicam que uma dominância pode ser estável linear, reversa, assimétrica ou transitiva (Martin e Bateson, 1993; Reed et al., 1997).
Em termos adaptativos, a hierarquia seria um regulador para um sistema de privilégios, usualmente medida pela observação de atos agonísticos direcionados entre as díades, na determinação de liderança, para resolver conflitos ou mesmo para evitar excessos de agressividade. Outra linha procura entendê-la como expressão de liberdade de um animal permitida em um encontro com outro. A hierarquia pode não ser um traço individual, mas um reflexo da assimetria e dinâmica entre os indivíduos, variando no tempo e contexto (Poisbleau et al., 2005; Fatjó et al., 2007; Wittermyer e Getz, 2007).
A hierarquia de dominância é normalmente determinada por fatores sócio-estruturais do grupo, além de sofrer influências genéticas (Vekovishcheva et al., 2000).
Um alto grau de dominância confere benefícios para machos e fêmeas, principalmente quando a relação de acesso aos recursos é competitiva (Reed et al., 1997). Há, porém um preço a se pagar pela posição ocupada, uma vez que, apesar da posição de dominância ser vantajosa, requer uma constante atenção e é muitas vezes dependente da agressividade (Poisbleau et al., 2005).
Uma vez que a hierarquia de dominância ocorre em diversas espécies, a posição ocupada pode influenciar muito a qualidade de vida de um animal, indivíduos altamente ranqueados são responsáveis pela maioria dos agonismos durante a alimentação. Já os indivíduos que ocupam as posições hierarquias médias ou baixas se equivalem (Sapolsky, 2005; Vogel, 2005).
Nas espécies em que a estrutura social se faz sobre uma condição de grande quantidade e ampla distribuição de recursos, como em elefantes africanos, a hierarquia de dominância não é ligada a altos níveis de agressividade. Os custos e benefícios são equivalentes para todos os integrantes, ao contrário das linhas hierárquicas fortes, nas quais alguns indivíduos acumulam os benefícios, como em lebres européias (Vehrencamp, 1983; Archie et al., 2006).
Em espécies como Helogale parvula – mangustos, Lycaon pictus – cães selvagens africanos e Lemur catta - lêmures cauda-anelada, os indivíduos dominantes se envolvem em interações agressivas muito mais que subordinados, isto leva a uma condição desgastante fisicamente e pode gerar também um aumento do nível de estresse, reflexo da freqüente demanda física para competições por recursos alimentares (Creel et al., 1996; Sapolsky, 2005).
13 -particularmente ligados à disputa por posições hierárquicas, podendo ser expressos por todos os indivíduos do grupo (Fatjó et al., 2007). Outro exemplo de que a hierarquia de dominância não esta diretamente ligada à agressão, são as interações ritualísticas, como em Pecari tajacu (queixadas), que utilizam rituais com posicionamento de corpo, olhares fixos, perseguições e odores.
Nos modelos sócio-ecológicos, originalmente aplicados em primatas, a relação de dominância ocorre (Wittermyer e Getz, 2007), mas a alta posição hierárquica em primatas não-humanos gregários é algumas vezes associada à posição central na rede social do grupo, muito mais ligada à estrutura de relações com outros membros, do que propriamente com a disputa por recursos alimentares. Encontramos exemplos como os do mico-de-cheiro – Saimiri sp., onde a posição de macho dominante se estabelece pelo volume do corpo e idade. Fêmeas de Saimiri podem promover alianças para forrageio, porém se há possibilidade de monopolizar o recurso os indivíduos dominantes serão agressivos.
As espécies do gênero Cebus são variáveis quanto aos padrões sociais e adaptabilidade comportamental, assim entende-se a flexibilidade das relações intragrupo (Fragaszy et al., 1990; Manson et al., 1999).
Quanto às questões de relações de dominância entre macacos-prego – Cebus
Em macacos-prego – Cebus olivaceus, o macho dominante é preferido pelas fêmeas como parceiro de catação, reprodutor (em Cebus olivaceus é o pai da maioria da prole), e também é o macho central do grupo (Perry, 1998). Em Cebus albifrons e
Cebus capucinus, nem sempre os machos dominantes ocupam a posição central no grupo, relativa a outros machos (Fedigan, 1993), isto porque as relações entre as díades do grupo independem diretamente das relações hierárquicas de organização do grupo.
Estudos de reconciliação em macacos-prego (Cebus capucinus) como o de Leca et al. (2002), que mostrou tendências conciliatórias, podem ser usados para dar suporte a uma estrutura referencial de hierarquia de dominância, uma vez que discute a atividade conciliatória como um aspecto importante da estrutura social do grupo.
Como suporte as observações de interações agressivas para determinação de posições hierárquicas, pode-se levar em conta o trabalho de Sparks (1967), que mostrou a catação entre macacos do Velho Mundo sendo mais realizada no sentido subordinado - dominante, uma vez que as estratégias sociais envolvidas no ranqueamento tipo reverso de Cebus podem ser comparadas àquelas apresentadas também por chimpanzés durante o mesmo processo (Perry, 1998).
15
-OBJETIVOS
Objetivo Geral
Identificar e comparar a hierarquia apresentada por Cebus apella e Cebus
libidinosus durante as atividades alimentares.
Objetivos Específicos
1. Constatar através dos eventos de interação agressiva a posição hierárquica ocupada por cada membro do grupo;
2. Estabelecer a freqüência e a duração das interações de cada indivíduo com o objeto teste – T.O.R.A.;
3. Verificar se os padrões de hierarquia de dominância observados influenciam na obtenção de alimentos;
ARTIGO
HIERARQUIA DE DOMINÂNCIA DURANTE A OBTENÇÃO DE
ALIMENTO EM
CEBUS APELLA
E
CEBUS LIBIDINOSUS
EM
CATIVEIRO
COLLAÇO, B. J. R.¹ and ARAÚJO. A.¹
1 – Programa de Pós-Graduação em Psicobiologia Centro de Biociências – Departamento de Fisiologia Universidade Federal do Rio Grande do Norte – UFRN 59078-970 – Natal, RN, Brasil.
E-mail: brunocollaco@ufrnet.br, brunojrcollaco@gmail.com, arrilton@gmail.com
17 -HIERARQUIA DE DOMINÂNCIA DURANTE A OBTENÇÃO DE ALIMENTO EM
CEBUS APELLA E CEBUS LIBIDINOSUS EM CATIVEIRO Collaço B J R¹, and Araújo A¹
1 – Programa de Pós-Graduação em Psicobiologia Centro de Biociências – Departamento de Fisiologia Universidade Federal do Rio Grande do Norte – UFRN 59078-970 – Natal, RN, Brasil.
Resumo
A análise do índice de hierarquia e modelos estruturais de formação de grupos possibilitou estabelecer a posição hierárquica dos membros de dois grupos do gênero
Cebus. Através da análise das posições hierárquicas e também da aplicação de testes de obtenção de recurso alimentar (TORA), pudemos perceber a diferença existente entre estes grupos e grupos estudados em vida livre. Os resultados mostram linearidade tanto para Cebus apella, quanto para Cebus libidinosus. Os resultados nos permitiram estabelecer que a estrutura hierárquica em grupos de Cebus em cativeiro: a) pode ser rígida e fixa diferente da estrutura hierárquica altamente flexível estudada em grupos de vida livre; b) mesmo com índices similares de hierarquia, existem diferenças na estrutura hierárquica apresenta entre C. apella e C. libidinosus em cativeiro; c) hierarquia influencia diretamente os padrões comportamentais de obtenção de alimentos em Cebus.
19
-Abstract
The analysis of the index of hierarchy and structural models of the formation of groups allowed to establish the hierarchical position of members of two groups of the genus
Cebus. By the analyses of the hierarchical positions and the application of tests to obtain a food resource (TORA), we know the difference between these groups and groups in the wild. The results show a high ranking for both Cebus apella, as well as Cebus
libidinosus. The results have enabled us to establish that the hierarchical structure in groups of Cebus in captivity: a) can be fixed and rigid different from highly flexible hierarchical structure studied in groups of wild b) even which similar hierarchy indices, there are differences in the hierarchical structure presents between C. apella and C.
libidinosus in captivity c) hierarchy directly influence the behavioral patterns of obtaining food in Cebus.
Introdução
Na literatura sobre primatas a competição por alimento e parceiros é determinante para a diversidade das relações sociais observadas entre os membros dos grupos (Wrangham, 1980; van Schaick, 1986; Janson, 1986; Janson and van Schaik, 1988; Isbell, 1991; van Hoof and van Schaik, 1994). A formação de grupos estáveis permite que estudos sobre a influência da hierarquia de dominância sobre a aquisição de alimento sejam mais freqüentes (Wrangham, 1980; van Schaik e van Noordwijk, 1989; Silk et al., 2003; Vogel, 2005).
Modelos sociais mostram basicamente dois tipos de competição (Sterck, 1997; Boinsky, 2001). Direta, onde a base da relação é a agressão, ou indireta, onde a distribuição dos recursos é o que permite que alguns animais ascendam e outros sejam excluídos. Em vida livre existe uma combinação destes dois tipos de competição, porém é possível ser realizada uma estimativa de cada um separadamente (van Hoof and van Schaik, 1994; Izar et al. 2006).
Pesquisas mostram uma grande flexibilidade comportamental, baseada em altos índices de tolerância para Cebus, determinando uma hierarquia de dominância não tão rígida como para macacos Macaca ou Papio (Defler, 1982; de Waal, 2000). Mas, o uso do termo hierarquia, de modo pouco cuidadoso, ou mesmo de maneira inapropriada, em estudos de comportamento pode criar idéias contraditórias, não é totalmente verdade que uma relação de dominância forme uma hierarquia linear (Drews, 1993), e um baixo índice de linearidade não significa dizer que a hierarquia está ausente (Izar et al. 2006).
21 -muito mais fiel as condições naturais de dominância (Izar et al. 2006). A complexidade das relações de dominância está na existência de diversos caminhos independentes, possibilitando a formação de hierarquias parciais (Jameson et al., 1999).
Machos dominantes de Cebus apella caracteristicamente protetores, tradicionalmente ocupam o centro do grupo, fazendo com que tenham acesso incontestável ao alimento, e aliado a flexibilidade comportamental permite mais facilmente a formação de grupos multimachos (Byrne et al., 1996).
Janson (1985) trabalhando com C. apella dominantes percebeu que estes têm maiores ganhos sobre recursos alimentares, através de altos índices de agressão, e mesmo em estruturas com pouca ou nenhuma agressão, os índices de alimentação ainda assim são diferentes e vantajosos para os dominantes. Uma segunda teoria, também descrita por Janson (1985) diz que a agressão pode aumentar ainda mais o índice de ganho de energia, nos casos de competição alimentar em C. apella a agressão passa a ser um aspecto de incremento na dominância do indivíduo sobre outros.
A ação direta dos machos dominantes cria um forte vínculo destes com os subordinados, já que os subordinados por sua posição hierárquica, dificilmente criam um vínculo com outros machos também subordinados (Perry, 1998). Esta pode ser uma forma de confirmar os dados de Janson (1985), com machos dominantes monopolizando os recursos e direcionando altos índices de agressão sobre os machos subordinados.
obtenção de alimentos; 4. Analisar estes objetivos de forma comparativa entre Cebus
apella e Cebus libidinosus em cativeiro.
Materiais e Métodos
Sujeitos de estudo
As observações foram realizadas sobre duas espécies de macacos-prego, do gênero Cebus – Erxleben 1777, o Grupo Apella formado por indivíduos da espécie C.
apella, e o Grupo Libidinosus formado por C. libidinosus.
Todos os animais utilizados no estudo foram oriundos de apreensões do IBAMA – Alagoas contra o tráfico ou mesmo contra posse ilegal de espécimes da fauna silvestre. Em função disto, não foi possível determinar a origem geográfica, idade precisa dos indivíduos, nem experiência reprodutiva dos adultos. Os grupos estão formados há quatro anos, o que nos permite considerar que são estáveis.
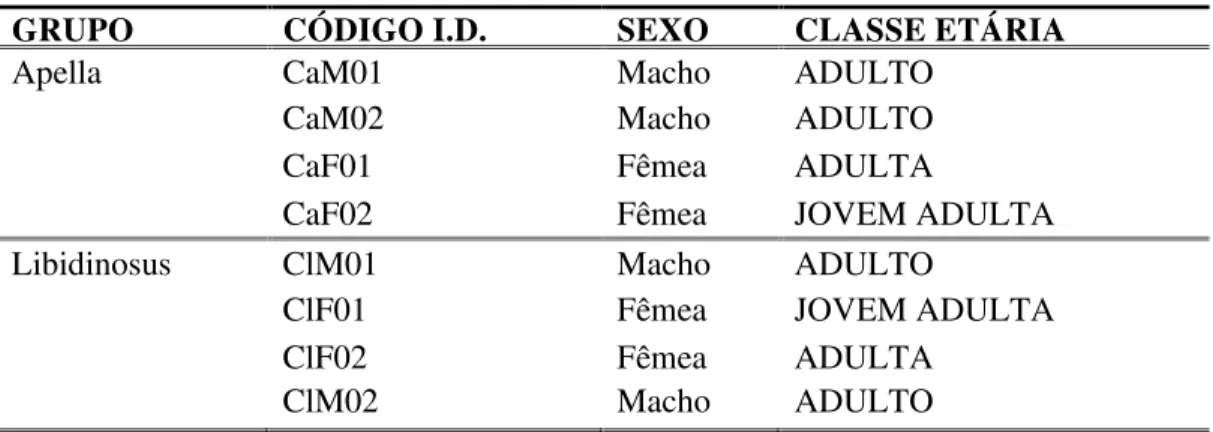
Para identificação correta durante as observações, foi estabelecido um código de identificação baseado nas características faciais e corporais próprias, cicatrizes e marcas específicas evidentes, naturais ou não, na intenção de se estabelecer um padrão lógico na anotação dos dados coletados. Este código foi gerado através da determinação de espécie, referência ao sexo do animal e seqüência de entrada no grupo (Tabela 1). Os indivíduos foram classificados em função da classe de idade baseado nos padrões de tamanho corporal descritos por Visalberghi (1988).
Local de estudo
23 -Os recintos do estudo formam um bloco de quatro gaiolões com uma entrada para um corredor comum e portas de acesso para cada um destes isoladamente, que ficam frente a frente, de maneira que os animais têm contato visual e vocal. Os gaiolões possuem todos, o mesmo tamanho 18 m³ cada um, totalizando 72 m³ de área, com muretas de 0,5 m de altura no perímetro de suas bases e uma parede inteiriça separando os recintos adjacentes, tudo isto cercado com grades envolvendo todo o restante da estrutura que é coberta com telhas, mantendo-se as laterais livres (Figura 1). Em todos os recintos são dispostos galhos e cordas, como forma de enriquecimento ambiental.
Tabela 1 – Composição e identificação dos grupos de C. apella e C. libidinosus.
GRUPO CÓDIGO I.D. SEXO CLASSE ETÁRIA
Apella CaM01 Macho ADULTO
CaM02 Macho ADULTO
CaF01 Fêmea ADULTA
CaF02 Fêmea JOVEM ADULTA
Libidinosus ClM01 Macho ADULTO
ClF01 Fêmea JOVEM ADULTA
ClF02 Fêmea ADULTA
ClM02 Macho ADULTO
Figura. 1 – Vista externa do recinto (a) e portas de acesso aos recintos de cada grupo (b).
25
-Métodos de Observação
Antes das observações efetivas, foi realizado um período de adaptação, a presença do pesquisador nos recintos, nos meses de fevereiro e março de 2008. As observações foram realizadas no período de abril a junho do mesmo ano, totalizando 156 horas efetivas. Cada sessão foi dividida em três etapas: pré-teste, teste e pós-teste
aplicados nesta ordem, aleatoriamente entre os grupos.
Pré-teste: Observação comportamental do grupo por um período de 30 minutos antes do teste de obtenção de recurso alimentar, utilizando como técnica, animal focal com registro contínuo (Altmann, 1974; Martin and Bateson, 1993), os dados foram registrados em planilha específica (Anexo I). Os comportamentos registrados nesta etapa estão listados no quadro I.
Quadro I – Etograma de identificação para tipos de interação física e não-física, e padrões comportamentais em Cebus. Adaptado dos etogramas de Visalberghi et al. (2006), Mendonça - Furtado (2006).
Tipo Padrão
Comportamental
FÍSICA NÃO-FÍSICA
AGRESSÃO
Ação física agressiva recíproca, ou não, por golpe
ou mordida. ---
VOCALIZAÇÃO ---
Vocalização agressiva, dirigida a um indivíduo que esteja iniciando ou em curso de uma ação.
PERSEGUIÇÃO --- Correr atrás ou afugentar indivíduos sem que haja contato físico.
BOTE
Salto ou investida repentina gerando contato dos corpos ou parte deles entre emissor-recebedor.
Salto ou investida repentina gerando fuga ou reação repentina do recebedor.
GROOMING
Inspeção objetiva do pêlo ou da pele de outro indivíduo seja com as mãos, dentes ou boca.
Teste ou Teste de Obtenção de Recurso Alimentar (TORA) - Para a obtenção de recurso alimentar foi introduzido no recinto de cada grupo um objeto de teste contendo uma recompensa alimentar, ração P-18 da marca MEGAZOO.
Este equipamento foi montado com as medidas de 12,5cm de comprimento de um tubo de PVC de 50 mm perfurado, com broca Nº. 8, para permitir a saída do cheiro do alimento, com uma corda de 6 mm fixada num tampão também de 50 mm em uma das extremidades, para resgate depois de encerrado o teste e uma tampa de borracha resistente de 2 ou 3 mm, que serviu como retentor de acesso ao alimento do interior do TORA, nessa tampa havia uma abertura em cruz que permitia aos animais a introdução de um de seus braços para buscar o recurso alimentar (Figura 2). O objeto de teste era introduzido na gaiola, pela portinhola de acesso frontal, possibilitando a avistagem de todos os membros do grupo, e permitindo seu acesso igualitariamente, contendo uma porção de recompensa, entre 20 a 30g.
27 -O T-ORA permaneceu pelo período de 30 minutos/sessão, uma única vez por dia de observação para cada grupo. Foram aplicados 104 testes no total sendo 52 para o Grupo Apella e 52 para o Grupo Libidinosus. Durante esta etapa foram registradas todas as atividades de interação com o TORA e entre manipulador do mesmo e os demais indivíduos do grupo. Os dados foram registrados em planilha específica (Anexo II), tendo como registros:
Tempo de posse: tempo de posse do objeto teste por um mesmo indivíduo, somando-se o tempo total por sessão/indivíduo;
Disputa: ação agressiva, física ou não-física com intenção de afastar outros indivíduos ou tomar posse do objeto teste;
Tolerância: comportamento permissivo da exploração do objeto teste por outro indivíduo, enquanto da posse deste;
Doação de recurso: entregar voluntariamente recurso alimentar obtido do objeto teste para outro indivíduo do grupo.
Pós-teste: Período de observação comportamental de 30 minutos, após a retirada do objeto teste do recinto, seguindo a mesma metodologia e forma de registro descrita para o pré-teste.
Análise de Dados
interações e quantidade/tipo de padrão comportamental, para determinar se estas apresentaram diferença significativa.
Os dados dos quadros de conflito foram plotados similarmente a analise realizada por Janson (1985) e Vogel (2005), que em seus estudos geraram um índice de linearidade de Landau (Landau, 1951; Martin and Bateson, 1993; Domingo-Balcells et al., 2003), que se reconhece através da aplicação da seguinte equação:
h = 12/(n³ - n) S[Si - ½ ( n – 1 )]²
Relevante ao processo de análise e construção do ranking hierárquico para cada grupo observado, onde: n é o número de indivíduos do grupo e Si é a soma dos valores de cada indivíduo nas tabelas de dominância. Também foram montadas matrizes de interação padrão com os dados dos quadros de conflito, e com estas duas informações, foi possível sugerir a construção das árvores de hierarquia segundo Izar et al. (2006).
Resultados
Estrutura hierárquica
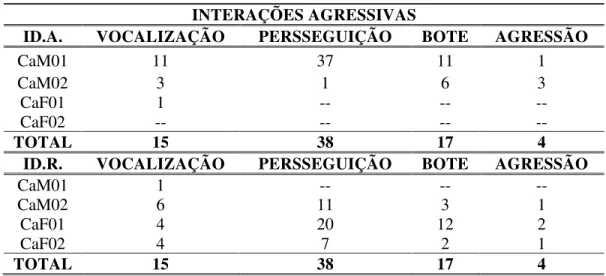
29 -Tabela 2 – Resultados quantitativos de cada evento comportamental apresentado pelos animais do Grupo de C. apella, separando membros agressores (ID.A. – Indivíduo Agressor) e membros agredidos (ID.R. – Indivíduo Receptor).
INTERAÇÕES AGRESSIVAS
ID.A. VOCALIZAÇÃO PERSSEGUIÇÃO BOTE AGRESSÃO
CaM01 11 37 11 1
CaM02 3 1 6 3
CaF01 1 -- -- --
CaF02 -- -- -- --
TOTAL 15 38 17 4
ID.R. VOCALIZAÇÃO PERSSEGUIÇÃO BOTE AGRESSÃO
CaM01 1 -- -- --
CaM02 6 11 3 1
CaF01 4 20 12 2
CaF02 4 7 2 1
TOTAL 15 38 17 4
Tabela 3 – Resultados quantitativos de cada evento comportamental apresentado pelos animais do Grupo de C. libidinosus, separando membros agressores (I.D.A.) e membros agredidos (I.D.R.).
INTERAÇÕES AGRESSIVAS
ID.A. VOCALIZAÇÃO PERSSEGUIÇÃO BOTE AGRESSÃO
ClM01 1 3 10 3
ClM02 -- -- -- --
ClF01 -- -- -- --
ClF02 -- -- -- --
TOTAL 1 3 10 3
ID.R. VOCALIZAÇÃO PERSSEGUIÇÃO BOTE AGRESSÃO
ClM01 -- -- -- --
ClM02 1 3 5 3
ClF01 -- -- 3 --
ClF02 -- -- 2 --
TOTAL 1 3 10 3
Para o grupo de C. apella, os comportamentos agonísticos foram quase que totalmente realizados pelos machos do grupo, sendo o macho CaM01 o indivíduo ativo da maioria dos eventos de vocalização, perseguição e bote, e o macho CaM02 o indivíduo que mais realizou agressões. Já as fêmeas deste grupo realizaram apenas o comportamento agonístico de vocalização, mesmo assim, este restrito a fêmea CaF01, não tendo à fêmea CaF02, participado com nenhum evento agonístico por todo período de observação (Figura 3).
Já no grupo de C. libidinosus, 100% das freqüências de todos os padrões comportamentais agressivos foram realizadas pelo mesmo membro, ClM01.
31 -0 10 20 30 40 50 60 70 80 90 100
CaM01 CaM02 CaF01 CaF02
F R E Q Ü Ê N C IA (% ) VOCALIZAÇÃO PERSEGUIÇÃO BOTE AGRESSÃO
Figura. 3 – Freqüência dos padrões comportamentais executados pelos membros agressores do Grupo de C. apella.
0 10 20 30 40 50 60 70 80 90 100
CaM01 CaM02 CaF01 CaF02
F R E Q Ü Ê N C IA (% ) VOCALIZAÇÃO PERSEGUIÇÃO BOTE AGRESSÃO
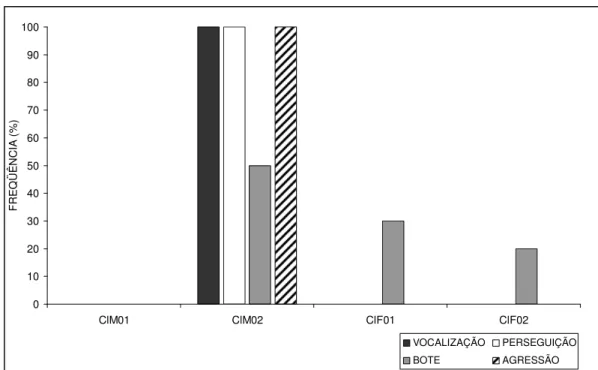
Em relação ao grupo de C. libidinosus, o macho ClM02 recebeu todas as interações agressivas de vocalização, perseguição e agressão, além de receber metade dos botes, já as fêmeas ClF01 e ClF02, que receberam o restante dos botes, não receberam mais nenhuma interação agressiva (Tabela 3 e Figura 5).
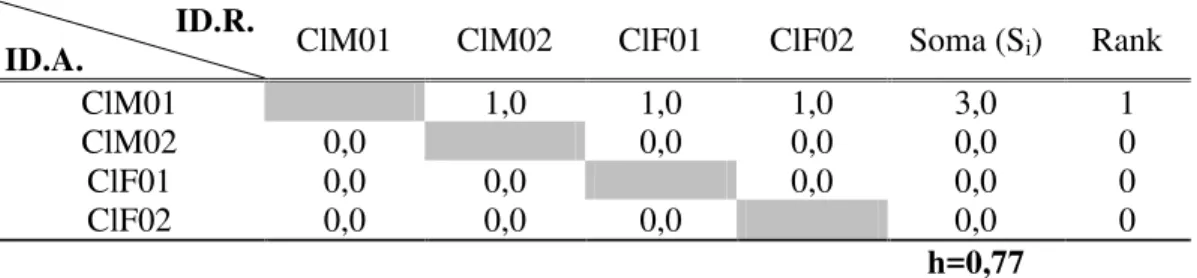
Na metodologia de análise das matrizes de interação, baseada em Domingo-Balcells et al. (2003), calculando-se o índice de Linearidade de Landau, os grupos apresentaram ambos, altos índices de linearidade para as tabelas de dominância (Tabelas 4 e 5). Segundo Izar et al. (2006), as árvores hierárquicas construídas para cada grupo podem então ser definidas como na figura 6.
Testes de Obtenção de Recurso Alimentar
Nos resultados do TORA, a interação individual de cada membro dos grupos foi assim estabelecida:
33 -0 10 20 30 40 50 60 70 80 90 100
ClM01 ClM02 ClF01 ClF02
F R E Q Ü Ê N C IA (% ) VOCALIZAÇÃO PERSEGUIÇÃO BOTE AGRESSÃO
Figura. 5 – Freqüência dos padrões comportamentais recebidos pelos membros agredidos do Grupo de C. libidinosus.
Tabela 4 – Matriz de direcionamento das interações agonísticas e índice de Landau (h) do Grupo de C. apella, com o somatório total das interações de cada membro e sua posição.
ID.R.
ID.A. CaM01 CaM02 CaF01 CaF02 Soma (Si) Rank
CaM01 1,0 0,5 1,0 2,5 1
CaM02 0,0 1,0 1,0 2,0 2
CaF01 0,5 0,0 1,0 1,5 3
CaF02 0,0 0,0 0,0 0,0 4
h=0,84
Tabela 5 – Matriz de direcionamento das interações agonísticas e índice de Landau (h) do Grupo de C. libidinosus, com o somatório total das interações de cada membro e sua posição.
ID.R.
ID.A. ClM01 ClM02 ClF01 ClF02 Soma (Si) Rank
ClM01 1,0 1,0 1,0 3,0 1
ClM02 0,0 0,0 0,0 0,0 0
ClF01 0,0 0,0 0,0 0,0 0
ClF02 0,0 0,0 0,0 0,0 0
h=0,77
Figura. 6 – Árvores hierárquicas dos Grupos de C. apella e C. libidinosus, onde, o membro hierarquicamente dominante, encontra-se na base da árvore.
CaM01 CaM02 CaF01 CaF02
ClM01
35 -0
100 200 300 400 500 600 700 800
CaM01 CaM02 CaF01 CaF02
TEMPO (min)
POSSE DISPUTA
TOLEROU TOLERADO
Figura. 7a – Tempo total de interação em minutos, com o objeto teste, de cada membro do grupo de C. apella nos padrões comportamentais descritos.
0 100 200 300 400 500 600 700 800
ClM01 ClM02 ClF01 ClF02
TEMPO (min)
POSSE DISPUTA
TOLEROU TOLERADO
No Grupo de C. libidinosus, os resultados mostram que a disputa foi uma interação unicamente existente entre os dois machos, por um período de tempo curtíssimo. O macho ClM02, praticamente não teve acesso ao objeto tendo sido tolerado por um período mínimo, já o macho ClM01, deteve a posse do objeto por quase todo o período de observação, tendo sido o indivíduo que mais tolerou os outros membros, principalmente as fêmeas e entre elas, mais a fêmea ClF02 (Figura 7b).
Do tempo acumulado de posse de cada membro do grupo obteve-se a freqüência de interação dos indivíduos com o objeto TORA que se definiu da seguinte forma: 53,31% do tempo de interação com o objeto foi de CaM01; 26,72% de CaM02; 15,52% de CaF01 e apenas 3,45% do tempo de CaF02 (Figura 8).
37 -0
10 20 30 40 50 60 70 80 90 100
CaM01 CaM02 CaF01 CaF02
FREQÜÊNCIA (%)
Figura. 8 – Freqüência de interação com o objeto teste, de cada membro do grupo de C. apella durante o período de testes.
0 10 20 30 40 50 60 70 80 90 100
ClM01 ClM02 ClF01 ClF02
FREQÜÊNCIA (%)
Discussão
Com a medição do índice de linearidade através da análise dos eventos agressivos, os dados analisados nas matrizes de agressão nos permitiram estabelecer cada posto hierárquico ocupado pelos indivíduos no estudo.
Percebe-se que os grupos estudados, apresentaram características hierárquicas, diferentes dos grupos observados em vida livre, principalmente no que se refere à flexibilidade da hierarquia, uma vez que a estrutura hierárquica nos grupos estudados apresentou-se fixa e rígida, podendo estar relacionado ao fato do animais estarem em cativeiro, com dominantes e subordinados muito bem definidos (Defler, 1982; McGonigle et al. 2003; Vogel, 2005; Vogel and Janson, 2007; Alfaro, 2007).
Fica claro neste trabalho que tanto no grupo de C. apella quanto em C.
libidinosus, houve uma grande diferença nas ações comportamentais, onde os machos executaram muito mais agressões do que as fêmeas, sendo que no grupo de C. apella os dois machos por várias vezes concentraram suas agressões sobre a fêmea CaF01, diferentemente do grupo de C. libidinosus onde o macho dominante ClM01, concentrou suas agressões sobre o macho ClM02.
O fato de existirem altos níveis de agonismo nos dois grupos contraria o proposto por Wolkenten et al. (2006), que comparando os seus resultados de macaco-prego aos resultados encontrados por Aurelli e de Waal (1997), com chimpanzés, determinou uma diminuição das interações sociais agressivas, resultantes do cativeiro em espaços reduzidos. Entretanto isto pode ser explicado pela formação dos grupos, apresentando-se pequenos e com dois machos e duas fêmeas, o que pode causar uma restrição das relações de dominância, aumentando níveis de pressão social.
39 -forma de afirmação das relações sociais, entre o macho alfa e seus subordinados. Os altos índices de agressão entre os machos também são relatados por Fedigan (1993), que mostra um nível de tolerância muito maior dos machos com as fêmeas.
Esta análise nos faz entender as estruturas apresentadas, uma hierarquia linear para o grupo de C. apella, e uma hierarquia parcial o grupo de C. libidinosus, apesar dos índices de linearidade h=0,84 para o C. apella e h=0,77 para C. libidinosus, onde os machos CaM01 e ClM01 ocupam indiscutivelmente, as posições de dominantes dos grupos. Utilizando os modelos propostos por Izar et al. (2006), para definir a árvore hierárquica dos grupos, mesmo os dois tendo apresentado matrizes de dominância similares, é possível estabelecer dinâmicas de relação diferentes, principalmente quando são analisadas as formas pelas quais os machos se estabelecem dominantes.
relação à posição espacial do macho dominante dentro do grupo, deixando clara a ligação entre a posição hierárquica e espacial para esta espécie. Eles também afirmam que, para grupos com uma organização social por hierarquia de dominância, a determinação da posição espacial é diretamente relacionada à posição de dominante, com a expulsão dos subordinados de forma agressiva das posições centrais (Janson, 1990; Hall and Fedigan, 1997), o que acaba gerando uma série de benefícios para o membro dominante.
Estudos com C. apella, realizados por Robinson (1981) e Janson (1990), mostraram também uma relação entre a posição hierárquica e a posição espacial com benefícios para os dominantes, sendo assim, podemos também supor um possível ganho de benefícios para o dominante dos grupos estudados, onde estes benefícios seriam diretamente ligados ao acesso ao recurso alimentar, neste caso a posse do TORA.
Para o grupo de C. apella, nota-se que o macho CaM01 manteve sua dominância, através de ações agressivas diretas, todos os membros foram de alguma forma agredidos pelo dominante que, no entanto, apresenta uma tolerância muito maior em relação à aproximação do membro imediatamente subordinado, o macho CaM02.
Já no grupo de C. libidinosus, o macho ClM01 tem uma interação muito menos agressiva com as fêmeas, restringindo estas ações somente a botes. Por outro lado foram presenciados diversos atos de grooming (catação) entre eles, sabendo-se que o grooming pode ser utilizado como um contraponto ao agonísmo (Schino, 2007).
41 -posições mais altas, correlacionando a quantidade de grooming muitas vezes aos benefícios adquiridos (Seyfarth, 1977; de Waal and Luttrell, 1986; de Waal, 1991; Parr, 1997). Esta parece ser a explicação para o maior número de acessos das fêmeas de C.
libidinosus ao TORA, em especial da fêmea ClF02, em detrimento dos outros dois indivíduos, pois o fato de existir para este grupo uma hierarquia parcial, destacaria a ação do membro dominante e distribuição igualitária entre os outros. Esta fêmea ClF02 foi a que apresentou a maior quantidade de eventos de grooming observados em relação ao macho dominante.
Ao mesmo tempo em que percebemos que os machos dominantes mantêm a posse do TORA por mais tempo, também percebemos que estes machos acumulam os maiores tempos de tolerância com outros indivíduos, tolerância esta que pode estar relacionada a aspectos de distribuição de alimento entre indivíduos, em situações de restrição de acesso ao alimento para algum dos membros, onde o dominante pode vir a executar o papel de “distribuidor” do recurso alimentares, como comentam de Waal (2000) em seu trabalho com C. apella e Fedigan (1990) com C. capucinus.
O tempo de posse do TORA esteve diretamente relacionado com a posição hierárquica do membro dominante, os resultados de acesso ao TORA, tanto para C.
apella como para C. libidinosus, foram iguais, reproduzindo exatamente a estrutura hierárquica linear apresentada para C. apella.
grooming, somente observado entre as fêmeas e o macho dominante no Grupo Libidinosus.
O fato de somente as fêmeas do Grupo Libidinosus apresentarem eventos freqüentes de grooming com o macho dominante, torna-se a principal diferença entre os indivíduos, podendo ter sido este o fator de influencia na diferença de acesso ao TORA.
Conclusão
Mesmo apresentando altos índices de hierarquia, a estrutura apresentada pelos grupos é diferente, o Grupo Apella apresenta uma hierarquia linear e o Grupo Libidinosus apresenta uma hierarquia parcial. Esta hierarquia influenciou diretamente no acesso dos dominantes e subordinados ao recurso alimentar, porém, dominantes apresentaram maiores índices de tolerância com os subordinados do que os subordinados entre si, possivelmente pela condição de maior tempo de posse do objeto teste.
O acesso ao TORA dos membros subordinados do Grupo Apella, seguiu exatamente a ordem hierárquica linear apresentada na estrutura de dominância, já para o Grupo Libidinosus, o acesso foi desigual entre os membros subordinados, mesmo estes estando num mesmo nível hierárquico, esta diferença deve-se possivelmente aos eventos freqüentes de grooming entre alguns membros do grupo.
43
-Agradecimentos
A todos que contribuíram para a execução deste trabalho, ressaltando o Programa de Pós-Graduação em Psicobiologia da UFRN e o apoio financeiro da CAPES, além da MEGAZOO pela doação da ração utilizada no experimento e a equipe do CETAS – IBAMA de Alagoas, pelo apoio ao desenvolvimento do trabalho. Licença de Autorização para Atividades com Finalidade Científica nº. 14370-1, emitida em: 08/02/2008 , pelo Ministério do Meio Ambiente – MMA, Instituto Brasileiro do Meio Ambiente e dos Recursos Naturais Renováveis – IBAMA, Sistema de Autorização e Informação em Biodiversidade – SISBIO.
Referências
Alfaro JWL (2007) Subgrouping patterns in a group of wild Cebus apella nigritus. Int J Primatol 28 (2): 271-289.
Altmann J, (1974) Observational study of behavior. Sampling methods. Behaviour 49: 227-267.
Archie EA, Morrison TA, Foley CAH, Moss CJ and Alberts SC (2006) Dominance rank relationships among wild female African elephants, Loxodonta Africana. Anim Behav 71: 117-127.
Aureli F and de Waal FBM (1997) Inhibition of social behavior in chimpanzee under high-density conditions. Am J Primatol 41: 213-228.
Byrne G, Abbott KM and Suomi SJ (1996) Reorganization of dominance rank among adult males in a captive group of tufted capuchins (Cebus apella). Lab Primatol News 35 (1): 1-4.
de Waal FBM (2000) Attitudinal reciprocity in food sharing among brown capuchin Monkeys. Anim Behav 60: 253-261.
de Waal FBM and Luttrell LM (1986) The similarity principle underlying social bonding among female rhesus monkeys Folia Primatol 46: 215-234.
Defler TR (1982) A comparison of intergroup behavior in Cebus albifrons and C.
apella. Primates 23 (3): 385-392.
Domingo-Balcells C, Rodriguez-Luna E, Escobar-Aliaga M, Morales-Mávil J (2003) Interaciones socials en un grupo de Monos Aulladores Alouatta palliate mexicana en
cautiverio. Neotrop Primates 11 (2): 114-121.
Drews C (1993) The concept and definition of dominance in animal behaviour. Behaviour 125: 283-313.
Fedigan L (1993) Sex Differences and intersexual relations in adult white-faced capuchins (Cebus capucinus). Int J Primatol 14(6).
Hall CL and Fedigan LM (1997) Spatial benefits afforded by high rank in white-faced capuchins. Anim Behav 53: 1069-1082.
Isbell L A (1991) Contest and scramble competition: patterns of female aggression and ranging behavior among primates. Behav Ecol 2: 143-155.
Izar P, Ferreira RG, Sato T (2006) Describing the organization of dominance relationships by dominance-directed tree method. Am J Primatol 68: 189-207.
Jameson KA, Appleby MC and Freeman LC (1999) Finding an appropriate order for a hierarchy based on probabilistic dominance. Anim Behav 57: 991-998.
45 -Janson C (1986) The mating system as a determinant of social evolution in capuchin monkeys (Cebus). In: Primate Ecology and Conservation, Else J G, Lee P C (eds.), Cambridge Univ. Press, Cambridge, pp. 169-179.
Janson CH (1990) Social correlates of individual spatial choice in foraging groups of brown capuchin monkeys, Cebus apella. Anim Behav 40: 922-934.
Janson CH and van Schaik CP (1988) Recognizing the many faces of primate food competition: methods. Behaviour 105: 165-186.
Landau HG (1951) On dominance relations and the structure of animal societies: I. Effect of inherent characteristics. Bull Math Bioph 13.
Martin P, and Bateson P (1993) Measuring Behaviour: an introductory guide. Cambridge, Cambridge University Press. 63-113.
McGonigle B, Chalmers M and Dickinson A (2003) Concurrent disjoint and reciprocal classification by Cebus apella in seriation tasks: evidence for hierarchical organization.
Anim Cogn 6 (3): 185-197.
Mendonça-Furtado O (2006) Uso de ferramentas como enriquecimento ambiental para macacos-prego (Cebus apella) cativos. Dissertação de Mestrado. Mestrado em Psicologia – Psicologia Experimental. Instituto de Psicologia da Universidade de São Paulo.
Parr LA, Matheson MD, Bernstein IS and de Waal FBM (1997) Grooming down the hierarchy: allogrooming in captive bron capuchin monkeys, Cebus apella. Anim Behav 54: 361-367.
Perry S (1998) A case report of a male rank reversal in a group of wild white-faced capuchins (Cebus capucinus). Primates 39 (1): 51-70.
Poisbleau M, Fritz H, Guillemain M, Lacroix A (2005) Testosterone and linear social dominance status in captive male dabbling ducks in winter. Ethology 111: 493-509. Reed C, O'Brien TG and Kinnaird MF (1997) Male social behavior and dominance hierarchy in the Sulawesi crested black macaque (Macaca nigra). Int J Primatol 18 (2).
Robinson JG (1981) Spatial structure in foraging groups of wedge-capped capuchin monkeys Cebus nigrivittatus. Anim Behav 29: 1036-1056.
Schino G (2007) Grooming and agonistic support: a meta-analysis of primate reciprocal altruism. Behav Ecol 18: 115-120.
Seyfarth RM (1977) A model of social grooming among adult female monkeys. J Theor Biol 65: 671-698.
Silk JB, Alberts SC, Altmann J (2003) Social bonds of female baboons enhance infant survival. Science 302: 1231-1234.
van Hooff, JARAM and van Schaik CP (1994) Male bonds – affiliative relationships among nonhuman primate males. Behaviour 130: 309-337.
van Schaik CP and van Noordwijk MA (1989) The special role of male Cebus monkeys in predation avoidance and its effect on group composition. Behav Ecol Sociobiol 24: 265-276.
van Wolkenten ML, Davis JM, Gong ML, de Waal FBM (2006) Coping with acute crowding by Cebus apella. Int J Primatol 27 (5).
Visalberghi E, (1988) Responsiveness to objects in two social groups of tufted capuchin monkeys (Cebus apella). Am J Primatol 15: 349-360.
Visalberghi E, Valenzano DR and Preuschoft S (2006) Facial displays in Cebus apella.
47 -Vogel ER (2005) Rank differences in energy intake rates in white-faced capuchin monkeys, Cebus capucinus: the effects of contest competition. Behav Ecol Sociobiol 58: 333-344.
Vogel ER, Janson CH (2007) Predicting the frequency of food-related agonism in white-faced capuchin monkeys (Cebus capucinus), using a novel focal-tree method. Am J Primatol 69 (5): 533-50.
REFERÊNCIAS BIBLIOGRAFICAS
Archie EA, Morrison TA, Foley CAH, Moss CJ and Alberts SC (2006) Dominance rank relationships among wild female African elephants, Loxodonta Africana. Anim Behav 71: 117-127.
Creel S, Creel NM and Monfort SL (1996) Social stress and dominance. Nature 379 (212).
Dewsbury DA (1982) Dominance rank, copulatory behavior, and differential reproduction. Q Rev Biol 57: 135-159.
Drews C (1993) The concept and definition of dominance in animal behaviour. Behaviour 125: 283-313.
FatjÓ J, Feddersen-Petersen D, Ruiz De La Torre JL, Amat M, Mets M, Braus B, Manteca X (2007) Ambivalent signals during agonistic interactions in a captive wolf pack. Appl Anim Behav Sci 105: 274-283.
Fedigan L (1993) Sex Differences and intersexual relations in adult white-faced capuchins (Cebus capucinus). Int J Primatol 14(6).
Fragaszy DM, Visalberghi E, and Robinson JG (1990) Variability and adaptability in the genus Cebus. Folia Primatol 54: 114-118.
Gomes DF (2006) Ecologia cognitiva e forrageio social em macacos-prego, Cebus
nigritus (Goldfuss, 1809) cativos. Pontifícia Universidade Católica do Rio Grande do Sul. Faculdade de Biociências. Programa de Pós-Graduacão em Zoologia.
Jean-Baptiste L, Fornasieri I, Petit O (2002) Aggression and reconciliation in Cebus
capucinus. Int J Primatol 23(5).
49 -Martin P and Bateson P (1993) Measuring Behaviour: an introductory guide. Cambridge, Cambridge University Press. 63-113.
Perry S (1996) Female-female social relationships in wild white-faced capuchin monkeys, Cebus capucinus. Am J Primatol 40: 167-182.
Perry S (1998) A case report of a male rank reversal in a group of wild white-faced capuchins (Cebus capucinus). Primates 39(1): 51-70.
Phillips KA (1995) Foraging-related agonism in capuchin monkeys (Cebus capucinus). Folia Primatol 65: 159-162.
Poisbleau M, Fritz H, Guillemain M, and Lacroix A (2005) Testosterone and linear social dominance status in captive male dabbling ducks in winter. Ethology 111: 493-509.
Reader SM, and Laland KN (2001) Primate Innovation: Sex, Age and Social Rank Differences. Int J Primatol 22(5).
Reed C, O'Brien TG, and Kinnaird MF (1997) Male social behavior and dominance hierarchy in the Sulawesi crested black macaque (Macaca nigra). Int J Primatol 18(2). Rose LM (1994) Sex-differences in diet and foraging behavior in white-faced capuchins (Cebus capucinus). Int J Primatol 15: 95-114.
Sapolsky RM, (2005) The Influence of Social Hierarchy on Primate Health. Science 308.
Sparks J (1967) Allogrooming in primates: a review. Primate Ethology. Ed. by D. Morris. London. Weidenfeld.
Vekovishcheva O, Yu, Sukhotina IA, and Zvartau E (2000) Co-housing in a stable hierarchical group is not aversive for dominant and subordinate individuals. Neuros Behav Physiol 30(2).
Visalberghi E, Valenzano DR, and Preuschoft S (2006) Facial displays in Cebus apella.
Int J Primatol 27(6).
Vogel ER (2005) Rank differences in energy intake rates in white-faced capuchin monkeys, Cebus capucinus: the effects of contest competition. Behav Ecol Sociobiol 58: 333-344.
51
Anexo I – Planilha para coleta de dados de amostragem comportamental de interação agressiva. Nome do pesquisador: ____________________________________________________ Grupo observado: _______________________________________________________ Data: __________________ Nº. da sessão: _______________________
Hora inicial: ____________ Hora final: __________________________
DATA I.D.A. I.D.R.
INTERAÇÃO AGRESSIVA
INTERAÇÃO NÃO-AGRESSIVA
PADRÃO OBSERVAÇÕES FÍSICA FÍSICA NÃO- FÍSICA FÍSICA
TORA
53
-Anexo II – Planilha para coleta de dados de teste com objeto para obtenção de recurso alimentar (TORA). Nome do pesquisador: ____________________________________________________
Grupo observado: _______________________________________________________ Data: __________________ Nº. do TORA: _______________________
Hora inicial: ____________________ Hora final: ____________________
DATA I.D.A. TEMPO DE POSSE (MIN) PADRÃO OBSERVAÇÕES
NORMAS PARA PUBLICAÇÃO NA ACTA ETHOLOGICA http://www.springer.com/life+sci/behavioural/journal/10211 Title Page
The title page should include: The name(s) of the author(s) A concise and informative title
The affiliation(s) and address(es) of the author(s)
The e-mail address, telephone and fax numbers of the corresponding author
Abstract
Please provide an abstract of 100 to 150 words. The abstract should not contain any undefined abbreviations or unspecified references.
Keywords
Please provide 4 to 6 keywords which can be used for indexing purposes.
Text Formatting
Manuscripts should be submitted in Word.
Use a normal, plain font (e.g., 10-point Times Roman) for text. Use italics for emphasis.
Use the automatic page numbering function to number the pages. Do not use field functions.
Use tab stops or other commands for indents, not the space bar. Use the table function, not spreadsheets, to make tables. Use the equation editor or MathType for equations.
Note: If you use Word 2007, do not create the equations with the default equation editor but use the Microsoft equation editor or MathType instead.
Save your file in doc format. Do not submit docx files.
Headings
Please use no more than three levels of displayed headings.
Abbreviations
Abbreviations should be defined at first mention and used consistently thereafter.
Footnotes
Footnotes on the title page are not given reference symbols. Footnotes to the text are numbered consecutively; those to tables should be indicated by superscript lower-case letters (or asterisks for significance values and other statistical data).
Acknowledgments
Acknowledgments of people, grants, funds, etc. should be placed in a separate section before the reference list. The names of funding organizations should be written in full.
Scientific style
Please always use internationally accepted signs and symbols for units, SI units. Genus and species names should be in italics.
55 -Citation
Cite references in the text by name and year in parentheses. Some examples: Negotiation research spans many disciplines (Thompson 1990).
This result was later contradicted (Becker and Seligman 1996).
This effect has been widely studied (Abbott 1991; Barakat et al. 1995; Kelso and Smith 1998; Medvec et al. 1993).
Reference list
The list of references should only include works that are cited in the text and that have been published or accepted for publication. Personal communications and unpublished works should only be mentioned in the text. Do not use footnotes or endnotes as a substitute for a reference list.
Reference list entries should be alphabetized by the last names of the first author of each work.
Journal article
Smith J, Jones M Jr, Houghton L et al (1999) Future of health insurance. N Engl J Med 965:325–329
Article by DOI
Slifka MK, Whitton JL (2000) Clinical implications of dysregulated cytokine production. J Mol Med. Doi:10.1007/s001090000086
Book
South J, Blass B (2001) The future of modern genomics. Blackwell, London Book chapter
Brown B, Aaron M (2001) The politics of nature. In: Smith J (ed) The rise of modern genomics, 3rd edn. Wiley, New York, pp 230-257
Online document
Doe J (1999) Title of subordinate document. In: The dictionary of substances and their effects. Royal Society of Chemistry. Available via DIALOG.
http://www.rsc.org/dose/title of subordinate document. Accessed 15 Jan 1999
Tables
All tables are to be numbered using Arabic numerals.
Tables should always be cited in text in consecutive numerical order.
For each table, please supply a table heading. The table title should explain clearly and concisely the components of the table.
Identify any previously published material by giving the original source in the form of a reference at the end of the table heading.
Footnotes to tables should be indicated by superscript lower-case letters (or asterisks for significance values and other statistical data) and included beneath the table body.
Electronic Figure Submission
Supply all figures electronically.
Indicate what graphics program was used to create the artwork.
For vector graphics, the preferred format is EPS; for halftones, please use TIFF format. MS Office files are also acceptable.
Permissions
If you include figures that have already been published elsewhere, you must obtain permission from the copyright owner(s) for both the print and online format. Please be aware that some publishers do not grant electronic rights for free and that Springer will not be able to refund any costs that may have occurred to receive these permissions. In such cases, material from other sources should be used.
Ethical standards
Manuscripts submitted for publication must contain a declaration that the experiments comply with the current laws of the country in which they were performed. Please include this note in a separate section before the reference list.
Conflict of interest
Authors must indicate whether or not they have a financial relationship with the organization that sponsored the research. This note should be added in a separate section before the reference list.
If no conflict exists, authors should state: The authors declare that they have no conflict of interest.
Copyright transfer
Authors will be asked to transfer copyright of the article to the Publisher (or grant the Publisher exclusive publication and dissemination rights). This will ensure the widest possible protection and dissemination of information under copyright laws. Open Choice articles do not require transfer of copyright as the copyright remains with the author. In opting for open access, they agree to the Springer Open Choice Licence.
Color illustrations
Online publication of color illustrations is free of charge. For color in the print version, authors will be expected to make a contribution towards the extra costs.
Proof reading
The purpose of the proof is to check for typesetting or conversion errors and the completeness and accuracy of the text, tables and figures. Substantial changes in content, e.g., new results, corrected values, title and authorship, are not allowed without the approval of the Editor.
After online publication, further changes can only be made in the form of an Erratum, which will be hyperlinked to the article.
Online First
The article will be published online after receipt of the corrected proofs. This is the official first publication citable with the DOI. After release of the printed version, the paper can also be cited by issue and page numbers.
Languages
57
-supplied in Unicode (see www.unicode.org for details), especially if they are using non-roman characters.
Such abstracts in other languages will carry a disclaimer: