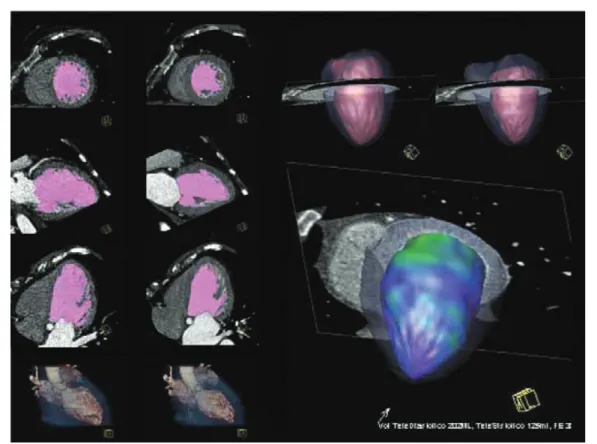
Avaliação por tomografia computadorizada da aurícula esquerda e veias pulmonares — contexto anátomo-‐clínico
Texto
Imagem


Documentos relacionados
a gene locus (or loci) that is instrumental in increasing blood pressure in this strain. Re- sults from both reciprocal crosses and consomic lines indicate that the Y chromo- some
O cartum é um gênero bastante conhecido por sua estrutura verbo-visual, assim como as tirinhas, as HQ e as charges. Diferencia-se dos demais por satirizar fatos universais
De acordo com a autora, esse panorama consolida-se nos níveis de educação formal mais elevada, de maneira que, ao longo dos últimos anos, a qualificação em nível de
Em relação à terceira questão de investigação, através da qual se procurou saber que existe relação entre as variáveis estilo/hábitos de vida e o grau de
Relationship between baseline white blood cell count and degree of coronary artery disease and mortality in patients with acute coronary syndromes: a TACTICS- TIMI 18 (Treat
Conclusion: A significant association was found between active periodontal disease and severe obstructive coronary artery in patients with acute coronary syndrome, underscoring
The most common secondary causes of resistant hypertension are hyperaldosteronism, chronic kidney disease, renal artery stenosis and obstructive sleep apnea (Table
The coronary angiographic findings in the patients with atrial septal defect and pulmonary hypertension (ASD + PH): compression of left main coronary artery by pulmonary