REVISTA
BRASILEIRA
DE
ANESTESIOLOGIA
PublicaçãoOficialdaSociedadeBrasileiradeAnestesiologiawww.sba.com.br
ARTIGO
CIENTÍFICO
Pré-condicionamento
com
dexmedetomidina
protege
contra
lesões
induzidas
por
lipopolissacarídeos
em
células
epiteliais
alveolares
humanas
Lei
Zhang
a,b,
Xian-Jin
Zhou
b,c,
Li-Ying
Zhan
a,b,
Xiao-Jing
Wu
a,b,
Wen-Lan
Li
a,b,
Bo
Zhao
a,b,
Qing-Tao
Meng
a,b,∗e
Zhong-Yuan
Xia
a,b,∗aWuhanUniversity,RenminHospital,DepartmentofAnesthesiology,Wuhan,Hubei,China
bWuhanUniversity,RenminHospital,LaboratoryofAnesthesiologyandCriticalCareMedicine,Wuhan,Hubei,China cTongjiUniversity,FirstMaternityandInfantHospital,DepartmentofAnesthesiology,Shanghai,China
Recebidoem17demarçode2016;aceitoem27defevereirode2017 DisponívelnaInternetem18deagostode2017
PALAVRAS-CHAVE
Dexmedetomidina; Lipopolissacarídeos;
Pré-condicionamento;
Lesãopulmonar
aguda;
Célulasepiteliais alveolares
Resumo
Justificativaeobjetivos: Dexmedetomidina(DEX)demonstrouterefeitopré-condicionantee tambémefeitosprotetorescontralesãoorganizada.Nesteestudo,comcélulasA549(células epiteliaisalveolareshumanas),investigamosseopré-condicionamentocomDEXproporcionaria protec¸ãocontralesãopulmonaraguda(LPA)invitro.
Métodos: CélulasA549foramaleatoriamentedistribuídasem quatrogrupos(n=5):controle, DEX, lipopolissacarídeos (LPS) e D-LPS (DEX+LPS). Administramos soluc¸ão de PBS (tampão fosfato-alcalino)ouDEX.Após2hdepré-condicionamento,omeiofoirenovadoeascélulas desafiadascomLPSpor24hnosgruposLPSeD-LPS.Emseguida,malondialdeído(MDA), supe-róxidodismutase(SOD),Bcl-2,Bax,caspase-3eemA549foramtestados.Apoptosetambémfoi avaliadanascélulas.
Resultados: Emcomparac¸ãocomogrupoLPS,opré-condicionamentocomDEXreduziua apop-tose(26,43%±1,05%vs.33,58%±1,16%,p<0,05)emcélulasA549,oqueestácorrelacionado coma diminuic¸ãode MDA (12,84±1,05vs. 19,16±1,89nmol.mg−1 de proteína,p<0,05) e aumentodaatividadedeSOD(30,28±2,38vs.20,86±2,19U.mg−1deproteína,p<0,05).O pré-condicionamentocomDEXtambémaumentouoníveldeBcl-2(0,53±0,03vs.0,32±0,04,
p<0,05)ediminuiuoníveldeBax(0,49±0,04vs.0,65±0,04,p<0,05),caspase-3(0,54±0,04
vs.0,76±0,04,p<0,05)ecitocromoc.
Conclusão:Opré-condicionamentocomDEXtemefeitoprotetorcontraLPAinvitro.Os poten-ciaismecanismosenvolvidossãoinibic¸ãodamortecelularemelhoriadaantioxidac¸ão. ©2017SociedadeBrasileiradeAnestesiologia.PublicadoporElsevierEditoraLtda.Este ´eum artigoOpen Accesssobumalicenc¸aCCBY-NC-ND(
http://creativecommons.org/licenses/by-nc-nd/4.0/).
∗Autorparacorrespondência.
E-mail:[email protected](Z.Y.Xia). http://dx.doi.org/10.1016/j.bjan.2017.07.003
KEYWORDS
Dexmedetomidine; Lipopolysaccharides; Preconditioning; Acutelunginjury; Alveolarepithelial cell
Dexmedetomidinepreconditioningprotectsagainstlipopolysaccharides-induced injuryinthehumanalveolarepithelialcells
Abstract
Backgroundandobjectives: Dexmedetomidine (DEX) has demonstrated the preconditioning effectandshownprotectiveeffectsagainstorganizeinjury.In thisstudy,usingA549(human alveolar epithelial cell) cell lines, we investigated whether DEX preconditioning protected againstacutelunginjury(ALI)invitro.
Methods:A549wererandomlydividedintofourgroups(n=5):controlgroup,DEXgroup, lipo-polysaccharides(LPS)group,andD-LPS(DEX+LPS)group.Phosphatebuffersaline(PBS)orDEX wereadministered.After2hpreconditioning,themediumwasrefreshedandthecellswere challengedwithLPSfor 24hontheLPSandD-LPSgroup.Thenthemalondialdehyde(MDA), superoxide dismutase(SOD), Bcl-2, Bax,caspase-3 andthe cytochromec intheA549 were tested.Theapoptosiswasalsoevaluatedinthecells.
Results:ComparewithLPSgroup,DEXpreconditioningreducedtheapoptosis(26.43%±1.05% vs.33.58%±1.16%,p<0.05)intheA549,whichiscorrelatedwithdecreasedMDA(12.84±1.05 vs. 19.16±1.89nmol.mg−1 protein, p<0.05) and increased SOD activity (30.28±2.38 vs. 20.86±2.19U.mg−1 protein, p<0.05). DEX preconditioning also increased the Bcl-2 level (0.53±0.03vs.0.32±0.04,p<0.05)anddecreasedthelevelofBax(0.49±0.04vs.0.65±0.04,
p<0.05),caspase-3(0.54±0.04vs.0.76±0.04,p<0.05)andcytochromec.
Conclusion: DEXpreconditioning has aprotective effectagainst ALI invitro. The potential mechanismsinvolvedaretheinhibitionofcelldeathandimprovementofantioxidation. ©2017SociedadeBrasileiradeAnestesiologia.Publishedby ElsevierEditoraLtda.Thisisan openaccessarticleundertheCCBY-NC-NDlicense(
http://creativecommons.org/licenses/by-nc-nd/4.0/).
Introduc
¸ão
A lesão pulmonar aguda (LPA) e sua forma mais grave, a síndromedo desconforto respiratório agudo(SARA), são umacondic¸ãorelativamentecomumempacientescríticos, associada a uma alta taxa de morbidade e mortalidade e caracterizada por edema pulmonar com alto teor de proteínae insuficiência respiratóriahipoxêmicagraveque podem ser o resultado de muitos insultos clínicos, inclu-sive sepse e pneumonia.1---3 Embora haja uma intensa
pesquisa e uma melhor compreensão dafisiopatologia de LPA/SARA, não há tratamentos farmacológicos específicos que comprovem seus benefícios. Portanto, as taxas de morbidade e mortalidade permanecem significativas em 35%---40%.3---5
Há relatos de que o pré-condicionamento oferece protec¸ãoefetivacontraLPApormeiodeestímuloprévio.6,7
Atualmente,opré-condicionamentotemsidoamplamente estudado na prática clínica por seu potencial de ofere-cerumaoportunidadeúnicadeexercerefeitosprotetores. Hojesabemosqueaprotec¸ãopodeserprovocadadeforma maissegurapormuitos fármacos,comodexmedetomidina (DEX).8,9
OusodeDEXcomosedativoécomumemcontextos clí-nicos. Recentemente, pesquisadoresdescobriram que DEX tempotencialparaimitaroefeitodopré-condicionamento emostrouefeitosprotetorescontralesõesorganizadas cau-sadasporlipopolissacarídeos(LPS).10,11Essaevidênciaindica
queDEXpodeterefeitoprotetorcontraLPA.Nesteestudo, usamosomodelodelesãoA549induzidaporLPSpara
simu-larLPAinvitro,investigamosseopré-condicionamentocom
DEXproduziriaprotec¸ãocontraLPA.Tambéminvestigamos osefeitosdopré-condicionamentocomDEXnamorte celu-lar e na func¸ão da antioxidac¸ão para obter uma melhor percepc¸ãodo(s)mecanismo(s).
Material
e
métodos
Culturacelularetratamentos
Célulashumanasdelinhagemepitelialalveolar(A549)foram obtidasdoChinaCenterforTypeCultureCollection(CCTCC, WuhanUniversity,Wuhan,China).AscélulasA549foram cul-tivadasemmeioRPMI-1640suplementadocomsorobovino fetal(10%),glutamina (2mmol.L), penicilina(100U.mL−1)
e estreptomicina (100mg.mL−1) e mantidas em ambiente
úmidoa37◦C eCO2a5%.
AsA549nafaselogarítmicadecrescimentoforam seme-adasem umaplaca de 96poc¸os(2×103). Apósa cultura
duranteanoite,essascélulasforamrandomicamente sepa-radasemquatrogruposdetratamentodiferentes:osgrupos DEX (Jiangsu Hengrui Medicine Co., Ltd., Jiangsu, China) eD-LPSreceberam DEX(10g.mL−1)e osgrupos controle
e LPS (Sigma-Aldrich, San Luis, MO, EUA) receberam o mesmovolumedesoluc¸ãotampão-fosfatosalina(PBS).Após duas horas de exposic¸ão ao agente farmacológico, cada placa de poc¸os foi lavada e as células foram desafiadas com LPS (50g.mL−1) por 24 horas nos grupos LPS e
Mensurac¸ãodaformac¸ãodemalondialdeído(MDA) edaatividadedesuperóxidodismutase(SOD)
Onível de formac¸ão de MDA e a atividadede SOD foram determinadoscomomarcadoresdeestresseoxidativocom kitscomercialmentedisponíveis(JianchengBiologicProject Co.,Nanjing,China).Aconcentrac¸ãodeproteínafoi deter-minadacomokitdeanálisedeproteínaBCA(BestBioCo., Shanghai,China),deacordocomoprotocolodofabricante.
Westernblotting
Ascélulasforamhomogeneizadaseaconcentrac¸ãode pro-teínadosobrenadantefoideterminadacomométodoBCA. O sobrenadante com 50g de proteína foi separado por SDS-PAGEe transferido paraumamembrana de nitrocelu-lose.Osanticorposprimáriosincluíramcaspase-3,Bcl-2,Bax (SantaCruzBiotechnology,SantaCruz,CA,EUA)e-actina (Abcam,Cambridge,MA,EUA).Amembranafoientão incu-bada com umanticorpo secundário anticoelho conjugado comHRP(1:20.000;Pierce)porumahoraeo‘‘borramento’’
(blotting)foidesenvolvidocomumkitdedetecc¸ãode
qui-mioluminescênciaSuperSignal(Pierce).Oimunoblottingfoi visualizadocomumprocessadorderaiosX Kodak102
(East-manKodak,Rochester,NY,EUA)eanalisadocomoprograma QuantityOne-4.2.3(Bio-Rad,Hercules,CA).
Ensaiodeliberac¸ãodocitocromo-c
Conformedescritoanteriormente,12 ascélulasA549 foram
fixadascomparaformaldeídoa4%por15minutos, permeabi-lizadascomTritonX-100a0,1%por10minutosebloqueadas
com3%desorodissolvidoem PBSpor30minutosem tem-peraturaambiente. As células foramentão sondadascom anticorpoanticitocromo-c(1:100;SantaCruzBiotechnology) duranteanoitea4◦C.AscélulasforamlavadascomPBSduas
vezeseincubadascomanticorposecundárioconjugadocom FITC(1:200; Biovision,China) por duas horas noescuro a 37◦C.Apósalavagem,asimagensdascélulascoradasforam
obtidascomummicroscópiodefluorescência.
Detecc¸ãodeapoptoseporcitometriadefluxo
Comumkitdedetecc¸ãodeapoptosedeanexina(AnnexinV
--PE/7-AADApoptosisDetectionKit---BioVision,MA,EUA),as célulasapoptóticasforamavaliadasviaanálisedacitometria de fluxo (FACScan, BD Biosciences, San Jose, CA, EUA).13
Osdadosforamanalisadoscom oprograma CellQuest(BD Biosciences).
Análiseestatística
Os dados de cinco experimentos independentes foram expressos em média±EPM. Anova e o teste de Student--Newman-Keuls (SNK) foram feitos para determinar a significância estatística. Diferenc¸as significativas foram estabelecidasemp<0,05.
A
60
50
40
30
20
25
20
15
10
5
0 10
0
Controle DEX
SOD (U.mg
–1 proteína)
MDA (mmol.mg
–1 proteína)
LPS D-LPS
Controle DEX D-LPS
∗ #
∗ #
∗
∗
B
LPS
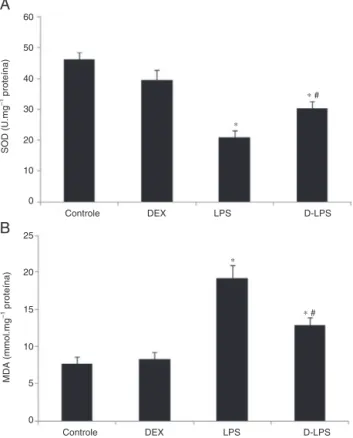
Figura1 (A)Atividadede SODem A549.(B)Níveisde MDA
em A549.Controle, semlesões;DEX, dexmedetomidina;LPS, lipopolissacarídeos; D-LPS, DEX+LPS. Valores expressos em média+EPM,n=5paracadagrupo.*p<0,05vs.grupocontrole e#p<0,05vs.grupoLPS.
Resultados
EfeitosdeDEXsobreoestresseoxidativoemA549
Em comparac¸ãocom o grupocontrole, osLPS diminuíram a atividadede SODem A549 (46,34±2,24U.mg−1 de
pro-teínavs.20,86±2,19U.mg−1deproteína,p<0,05)(fig.1A)
eaumentaramaformac¸ãodeMDA(7,68±0,92nmoL.mg−1
deproteínavs.19,16±1,8nmoL.mg−1deproteína,p<0,05)
(fig. 1B). Esse efeitofoi significativamente atenuado pelo pré-condicionamentocomDEX(30,28±2,38U.mg−1de
pro-teína e 12,84±1,05nmoL.mg−1 de proteína, p<0,05 vs.
grupoLPS).
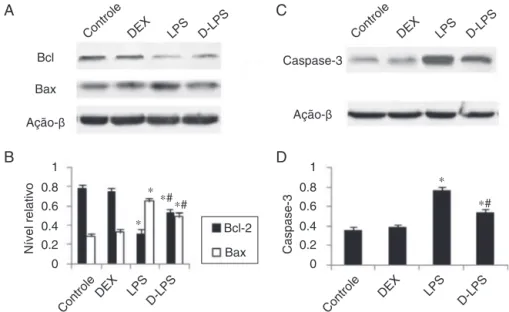
EfeitosdeDEXsobreaexpressãodeBcl-2, Baxecaspase-3
Em comparac¸ão com o grupo controle, os LPS dimi-nuíram o nível de Bcl-2 (0,79±0,03 vs. 0,32±0,04,
A
Bcl Caspase-3
Controle DEX LPS D-LPS Controle DEX LPS D-LPS
Bax
Bcl-2
∗
∗ ∗
∗# ∗#
∗#
Bax
Nível relativo Caspase-3
1 0.8 0.6 0.4 0.2 0
1 0.8 0.6 0.4 0.2 0
Controle Controle
DEX LPS DEX LPS
D-LPS D-LPS
Ação-β Ação-β
B
D
C
Figura2 (A)Imagemrepresentativade Bcl-2eBax.(B)Níveisde Bcl-2eBax.(C) Imagemrepresentativade caspase-3.(D)
Níveldecaspase-3.Controle,semlesões;DEX,dexmedetomidina;LPS,lipopolissacarídeos;D-LPS,DEX+LPS.Valoresexpressosem média+EPM,n=5paracadagrupo.*p<0,05vs.grupocontrolee#p<0,05vs.grupoLPS.
Controle
Citocromo-c
DAPI
DEX LPS D-LPS
Figura3 Sec¸õesrepresentativasdocitocromo-c.Controle,semlesões;DEX,dexmedetomidina;LPS,lipopolissacarídeos;D-LPS,
DEX+LPS.Afluorescênciaverdemostraocitocromo-ceafluorescênciaazul(DAPI)mostraoDNA.Ampliac¸ãooriginal400×.
significativamenteatenuadopelopré-condicionamentocom DEX(0,54±0,04,p<0,05vs.grupoLPS).
EfeitosdeDEXsobrealiberac¸ãodecitocromo-c
Ocitocromo-c doespac¸o intermembranarmitocondrial no citoplasmaéumpassocríticonaprogressãodavia apoptó-ticaintrínseca.Nogrupocontrole,ocitocromo-capresentou nível bem pouco detectável, enquanto LPS resultou em aumentos significativos. Esse efeito dos LPS foi atenuado pelopré-condicionamentocomDEX(fig.3).
EfeitosdeDEXsobreapoptose
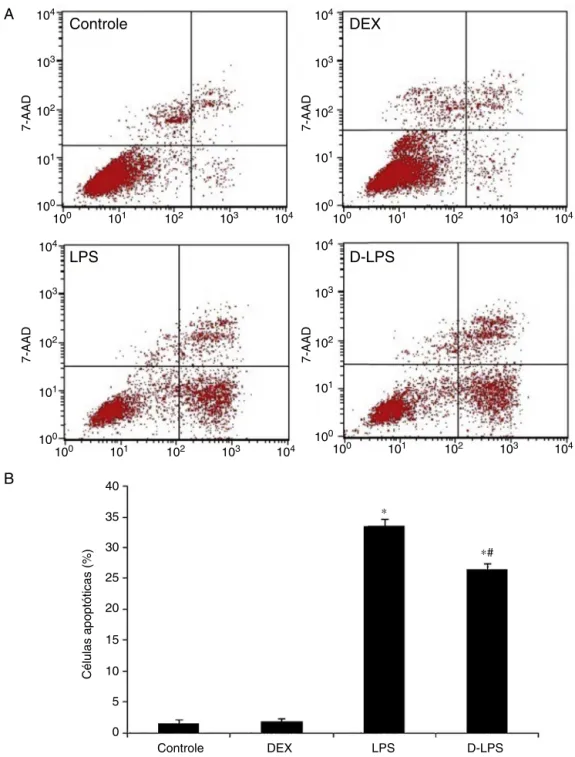
Emcomparac¸ãocomogrupocontrole,osLPSaumentarama porcentagemdecélulasapoptóticasemA549(1,57%±0,52%
vs.33,58%±1,16%,p<0,05)(fig. 4Ae4B).Esse efeitofoi significativamenteatenuadopelopré-condicionamentocom DEX(26,43%±1,05%,p<0,05vs.grupoLPS).
Discussão
Este estudo demonstrou que o pré-condicionamento com DEX diminuiu significativamente a lesão induzida por LPS em A549. Os principais achados são os seguintes: (1) o pré-condicionamentocomDEXreduziuaformac¸ãodeMDA e aumentou a atividade de SOD em A549; (2) o pré--condicionamentocomDEX aumentoua relac¸ãoBcl-2/Bax ediminuiuosníveisdecaspase-3ecitocromo-c;(3)o pré--condicionamentocom DEXatenuou a apoptoseem A549. Essesdadosfornecem a primeira evidência deque o pré--condicionamentocomDEXatenuaalesãoemcélulasA549 causadaporLPS.
Estudos relataram que o estresse oxidativo desempe-nha um papel importante na lesão induzida por LPS.14,15
A
B
Controle
LPS
D-LPS
DEX
100 101 100
101
7-AAD
7-AAD
7-AAD
7-AAD
102 103 104
100 101 102 103 104
100 101 102 103 104
102 103 104
100 101 102 103 104 100 101
40
∗
∗# 35
30
25
20
15
10
5
0
Controle DEX
Células apoptóticas (%)
LPS D-LPS 102 103 104
100 100 101 102 103 104
101 102 103 104
Figura4 (A)Imagemrepresentativadacitometriadefluxo.(B)Ograudeapoptosecelular.Controle,semlesões;DEX,
dexmede-tomidina;LPS,lipopolissacarídeos;D-LPS,DEX+LPS.Valoresexpressosemmédia+EPM,n=5paracadagrupo.*p<0,05vs.grupo controlee#p<0,05vs.grupoLPS.
comprometimentodaestruturanormaldamembranaelesão tecidualoxidativa.16 Emcontraste,SODéconsideradauma
importanteenzimaantioxidanteintracelularcommúltiplas func¸õesbiológicas.OaumentodaenzimaantioxidanteSOD podeindicaracapacidadecelulardeeliminac¸ãoeextinc¸ão de radicais livres.17,18 Estudos anteriores também
relata-ram que DEX impediu as reac¸ões de peroxidac¸ão com o aumentodeSOD,masdiminuiu oMDAnostecidos.19,20 No
experimento,nossosresultadosdemonstraramobviamente queopré-condicionamentocomDEXresultouemaumento daatividade deSODediminuic¸ão deMDAemA549. Essas descobertassugeremque opré-condicionamentocomDEX
poderiaexercerprotec¸ãocontraodanooxidativoinduzido porLPSemA549emodularassimalesãoedisfunc¸ãocelular. Váriasevidênciasindicaramoenvolvimentodoestresse oxidativonosmecanismospatológicossubjacentesda apop-toseinduzidaporLPSemA549.21,22Comosugeridoemnossos
eventoscelulares. Em estudosrecentes, descobriu-seque Bcl-2 fornece protec¸ão contra lesões induzidas por LPS em alguns órgãos, inclusive A549.23,24 Em contraste, Bax
exibeac¸õesproapoptóticas. Quandohá superexpressãode Bax, canais ouporospodemser formadospara permitir a liberac¸ãodefatorescomoocitocromo-c dasmitocôndrias parapropagaraapoptose.25Portanto,arelac¸ãodas
proteí-nasBcl-2/Baxéprovavelmentecríticaparaasobrevivência celular após a lesão.24 No presente estudo, os resultados
indicaramque DEXaumentouaexpressãodeBcl-2e dimi-nuiuaexpressãodeBaxe levouaumaumentodarelac¸ão Bcl-2/Bax.
Aliberac¸ãodecitocromo-ceaativac¸ãodacaspase-3são umpontocrucialnacascataapoptóticaepodemser regula-daspelarelac¸ãoBcl-2/Bax.26Estudosanterioresmostraram
queagerac¸ãoexcessivadeoxidac¸ãopodecausaraliberac¸ão de citocromo-c e a ativac¸ão de caspase-3. O processo podeserdeprimidopelaBcl-2.Ocitocromo-cliberadoe a caspase-3ativadaclivamajusanteosalvoscelulares críti-cosenvolvidosnacondensac¸ãodecromatina,fragmentac¸ão do DNA e destruic¸ão do citoesqueleto, expressam assim as dramáticas alterac¸ões morfológicas da apoptose.25-27
Demonstrou-se que os LPS são uma das formas de indu-zir a liberac¸ão de citocromo-c e a ativac¸ão de caspase-3 emA549.28Nopresenteestudo,osdadostambémmostram
quea liberac¸ãodecitocromo-c ea ativac¸ão decaspase-3 aumentaramsignificativamenteapósaadministrac¸ãodeLPS emA549,em linhacomosestudosanteriores.Alémdisso, observamosquealiberac¸ãodecitocromo-ceaativac¸ãode caspase-3foramdeprimidaspelopré-condicionamentocom DEX.
A apoptoseé umprocessofundamental damorte celu-larqueocorrepormeiodaativac¸ãodeviasdesinalizac¸ão distintaseenvolveumaregulac¸ãodeformadecrescenteda relac¸ãoBcl-2/Baxeliberac¸ãodecitocromo-ceativac¸ãode caspase-3invitro.28,29 Comoresultadofinal,ascélulassão
destruídaseformamórgãosapoptóticos.30LPSmostrou
ini-ciar essa cascata apoptóticaem A549.24 Com ummodelo
deLPAin vitro,nossosdadosdemonstramreduc¸ão
signifi-cativadaapoptoseapósopré-condicionamentocomDEX,o quecorrelacionoucomaregulac¸ãodeformacrescenteda relac¸ão Bcl-2/Baxedepressão daativac¸ãode caspase-3e liberac¸ãodecitocromo-c.
Contudo,nossoestudodescritivotemalgumaslimitac¸ões óbvias que precisam ser abordadas, tais como um único momento de coleta de amostra, o breve período de observac¸ãoeafaltadecorrelac¸ãocomasmensurac¸ões clíni-casdeLPA.Alémdisso,apenasinvestigamosaconcentrac¸ão de DEX, que é muito grande para a prática clínica. Em comparac¸ãocomaclínica,umagrandedose égeralmente usadaemlaboratório.31,32Emexperimentos,algunsestudos
relataramatéousodedosesmaisaltas.Essespodemestar relacionadosadiferentesespécimes.31,32 Arelac¸ãoentrea
doseeoefeitopermaneceobscura.Portanto,estudos rela-cionadosàrelac¸ãodose-efeitoprecisamdeumaexplorac¸ão maisabrangentedomodelo.
Sumário
Nossosdadosmostramqueopré-condicionamentocomDEX pode efetivamente atenuar a lesão induzida por LPS em
A549.Osefeitosprotetorespodemenvolverumareduc¸ãodo estresseoxidativoedamortecelularinduzidaporLPS.Esses resultadosexperimentaissugeriramDEXpodesereficazno tratamentodeLPAinduzidoporLPS.
Conflitos
de
interesse
Osautoresdeclaramnãohaverconflitosdeinteresse.
Referências
1.YangB,HuangW,HanJ,etal.Studyoftheroleofepidermal growthfactoronlungfluidtransportinrabbitswithacutelung injurycausedbyendotoxin.ExpTherMed.2012;4:611---4. 2.VincentJL,SakrY,RanieriVM.Epidemiologyandoutcomeof
acuterespiratoryfailure inintensive careunit patients.Crit CareMed.2003;31:S296---9.
3.Matthay MA, Zemans RL. The acute respiratory distress syndrome: pathogenesis and treatment. Annu Rev Pathol. 2011;6:147---63.
4.WareLB,MatthayMA.Theacuterespiratorydistresssyndrome. NewEnglJMed.2000;342:1334---49.
5.Rubenfeld GD, Herridge MS. Epidemiology and outcomes of acutelunginjury.Chest.2007;131:554---62.
6.Pang YL, Chen BS, Li SP, et al. The preconditioning pulmo-nary protective effect of volatile isoflurane in acute lung injuryismediatedbyactivationofendogenousiNOS.JAnesth. 2012;26:822---8.
7.LiQF,ZhuYS,JiangH,etal.Isofluranepreconditioning amelio-ratesendotoxin-inducedacutelunginjuryandmortalityinrats. AnesthAnalg.2009;109:1591---7.
8.Fang B, Li XQ, Bi B, et al. Dexmedetomidine attenuates blood---spinal cord barrier disruption induced by spinal cord ischemia reperfusion injury in rats. Cell Physiol Biochem. 2015;36:373---83.
9.Wang H, Chen H, Wang L, et al. Acute hyperglycemia pre-ventsdexmedetomidine-inducedpreconditioningagainstrenal ischemia-reperfusioninjury.ActaCirBras.2014;29:812---8. 10.TanF,ChenY,YuanD,etal.Dexmedetomidineprotectsagainst
acutekidneyinjurythroughdownregulatinginflammatory reac-tionsinendotoxemiarats.BiomedRep.2015;3:365---70. 11.BagcikE,OzkardeslerS,BoztasN,etal.Effectsof
dexmedeto-midineinconjunctionwithremoteischemicpreconditioningon renalischemia-reperfusioninjuryinrats.RevBrasAnestesiol. 2014;64:382---90.
12.Wang L, Huang H, Fan Y, et al. Effects of downregulation of microRNA-181a on H2O2-induced H9c2 cell apoptosis via themitochondrial apoptotic pathway. Oxid MedCellLongev. 2014;2014:960362.
13.DongS,QuX,LiW,etal.Thelongnon-codingRNA,GAS5, enhan-cesgefitinib-inducedcelldeathininnateEGFRtyrosinekinase inhibitor-resistantlung adenocarcinomacells withwide-type EGFRviadownregulationoftheIGF-1Rexpression.JHematol Oncol.2015;8:43.
14.Zhang XY, Cao JB, Zhang LM, et al. Deferoxamine attenua-teslipopolysaccharide-inducedneuroinflammationandmemory impairmentinmice.JNeuroinflamm.2015;12:20.
15.CuiK,KouJQ,GuJH,etal.Najanajaatravenom ameliora-tespulmonaryfibrosisbyinhibitinginflammatoryresponseand oxidativestress.BMCComplementAlternMed.2014;14:461. 16.LenazG.Roleofmitochondriainoxidativestressandageing.
BiochimBiophysActa.1998;1366:53---67.
18.Benov L, Batinic-Haberle I. A manganese porphyrin sup-presses oxidative stress and extends the life span of streptozotocin-diabetic rats. Free Radical Res. 2005;39: 81---8.
19.Shou-ShiW, Ting-TingS,Ji-ShunN,etal. Preclinicalefficacy ofdexmedetomidineonspinalcordinjuryprovokedoxidative renaldamage.RenFail.2015;37:1190---7.
20.LiS,YangY,YuC,etal.Dexmedetomidineanalgesiaeffectsin patientsundergoingdentalimplantsurgeryanditsimpacton postoperativeinflammatoryandoxidativestress.OxidMedCell Longev.2015;2015:186736.
21.LinWC,ChenCW,HuangYW,etal.Kallistatinprotectsagainst sepsis-relatedacutelunginjuryviainhibitinginflammationand apoptosis.SciRep.2015;5:12463.
22.KimW,YounH,KangC,etal.Inflammation-induced radiore-sistanceismediatedbyROS-dependentinactivationofprotein phosphatase 1innon-smallcelllungcancercells.Apoptosis. 2015;20:1242---52.
23.Wang Z, Wu Q, NieX, et al. Infusion of esmolol attenuates lipopolysaccharide-inducedmyocardialdysfunction.JSurgRes. 2016;200:283---9.
24.ZhaoJ,Li X,ZouM,etal.miR-135ainhibitionprotectsA549 cellsfrom LPS-inducedapoptosis bytargetingBcl-2.Biochem BiophysResCommun.2014;452:951---7.
25.Wolter KG, Hsu YT, Smith CL,et al. Movement of Baxfrom the cytosol to mitochondria during apoptosis. J Cell Biol. 1997;139:1281---92.
26.HaunstetterA,IzumoS.Apoptosis:basicmechanismsand impli-cationsforcardiovasculardisease.CircRes.1998;82:1111---29. 27.Hengartner MO. The biochemistry of apoptosis. Nature.
2000;407:770---6.
28.VeenaVK, PopavathRN,KennedyK, etal.In vitro antiproli-ferative,pro-apoptotic,antimetastaticandanti-inflammatory potentialof2,4-diacteylphloroglucinol(DAPG)byPseudomonas aeruginosastrainFP10.Apoptosis.2015;20:1281---95.
29.Lee US, Ban JO, Yeon ET, et al. Growth inhibitory effect of (E)-2,4-bis(p-hydroxyphenyl)-2-butenal diacetate through inductionofapoptoticcelldeathbyincreasingDR3expressionin humanlungcancercells.BiomolTher(Seoul).2012;20:538---43. 30.vanHeerdeWL,Robert-OffermanS,DumontE,etal.Markers ofapoptosisincardiovasculartissues:focusonAnnexinV. Car-diovascRes.2000;45:549---59.
31.ChenSL,ZhouW,HuaFZ,etal.Invitroeffectof dexmedeto-midineontherespiratoryburstofneutrophils.GenetMolRes. 2016:15.