www.jped.com.br
ARTIGO
ORIGINAL
Empirical
antimicrobial
therapy
for
late-onset
sepsis
in
a
neonatal
unit
with
high
prevalence
of
coagulase-negative
Staphylococcus
夽
,
夽夽
Roberta
Maia
de
Castro
Romanelli
a,b,∗,
Lêni
Márcia
Anchieta
a,c,
Ana
Carolina
Bueno
e
Silva
a,
Lenize
Adriana
de
Jesus
d,
Viviane
Rosado
d,ee
Wanessa
Trindade
Clemente
d,faUniversidadeFederaldeMinasGerais(UFMG),FaculdadedeMedicina,DepartamentodePediatria,BeloHorizonte,MG,Brasil bUniversidadeJosédoRosárioVellano,FaculdadedeCiênciasMédicas,BeloHorizonte,MG,Brasil
cUniversidadeFederaldeMinasGerais(UFMG),HospitaldasClínicas,UnidadeNeonataldeCuidadosProgressivos,Belo
Horizonte,MG,Brasil
dUniversidadeFederaldeMinasGerais(UFMG),HospitaldasClínicas,ComissãodeControledeInfecc¸ãoHospitalar,Belo
Horizonte,MG,Brasil
eUniversidadeFederaldeMinasGerais(UFMG),FaculdadedeMedicina,ProgramadePós-Graduac¸ãoemCiênciasdaSaúde,Belo
Horizonte,MG,Brasil
fUniversidadeFederaldeMinasGerais(UFMG),FaculdadedeMedicina,DepartamentodePropedêuticaComplementar,Belo
Horizonte,MG,Brasil
Recebidoem13deoutubrode2015;aceitoem18dejaneirode2016
KEYWORDS
Sepsis; Neonate; Staphylococcus; Oxacillin; Vancomycin
Abstract
Objective: Theaimofthisstudywastocomparetwodifferentempirictreatmentsfor late--onsetneonatalsepsis,vancomycinandoxacillin,inaneonatalintensivecareunitwithahigh prevalenceofcoagulase-negativeStaphylococcus.
Methods: Across-sectionalstudywasconductedinanneonatalintensivecareunitfrom2011 to2014.Data fromthemedicalrecordsofat-risk newbornswere collecteddaily. Infections weredefinedaccordingtotheNationalHealthSurveillanceAgencycriteria.Dataanalysiswas performedusinganinternalprogram.
Results: TherewasasignificantreductioninthenumberofStaphylococcusaureusinfections (p=0.008),withoutendocarditis,meningitis, orlowerrespiratory tractinfection,aswellas areductioninthefrequencyofdeathsrelatedtoS.aureusinfection.Therewereno signifi-cantchangesintheincidenceofGram-negativebacterialorfungalinfections.Anincreasein
DOIserefereaoartigo:
http://dx.doi.org/10.1016/j.jped.2016.01.008
夽 Comocitaresteartigo:RomanelliRM,AnchietaLM,SilvaAC,deJesusLA,RosadoV,ClementeWT.Empiricalantimicrobialtherapyfor
late-onsetsepsisinaneonatalunitwithhighprevalenceofcoagulase-negativeStaphylococcus.JPediatr(RioJ).2016;92:472---8.
夽夽EstudofeitonaFaculdadedeMedicina,UniversidadeFederaldeMinasGerais,BeloHorizonte,MG,Brasil.
∗Autorparacorrespondência.
E-mail:rmcromanelli@gmail.com(R.M.Romanelli).
coagulase-negativeStaphylococcusinfectionswasobserved(p=0.022).However,therewasno measured increaseinrelatedmorbidityandmortality.There wasareductioninthemedian numberofdaysoftreatmentwithoxacillinfrom11.5to6days(p<0.001)andanincreaseof onedayinthemediannumberofdaysoftreatmentwithvancomycin(p=0.046).
Conclusions: Modificationoftheempirictreatmentregimenforneonatallate-onsetsepsiswith useofoxacillinshowedasignificantreductioninS.aureusinfections,aswellasareductionin thefrequencyofinfectionswithmajororgansysteminvolvementandmortalityduetoinfection withthismicroorganism.Asaresult,oxacillincanbeconsideredasaneffectivetreatmentfor late-onsetsepsis,makingitpossibletoavoidbroad-spectrumantibiotics.
©2016PublishedbyElsevierEditoraLtda.onbehalfofSociedadeBrasileiradePediatria.Thisis anopenaccessarticleundertheCCBY-NC-NDlicense(http://creativecommons.org/licenses/ by-nc-nd/4.0/).
PALAVRAS-CHAVE
Sepse;
Recém-nascido; Staphylococcus; Oxacilina; Vancomicina
Terapiaantimicrobianaempíricaparasepsetardianaunidadeneonatalcomalta prevalênciadeStaphylococcuscoagulasenegativo
Resumo
Objetivo: Comparar dois períodos com diferentes esquemas empíricos para tratamentode sepseneonataltardia,incluindovancomicinaouoxacilinarespectivamente,emunidade neo-nataldereferênciacomaltaprevalênciadeStaphylococcuscoagulasenegativo.
Métodos: Estudotransversal,feito em unidade neonataldereferência,de 2011a2014. Os dadosforamcoletadosdiariamenteporvigilânciaativaem prontuárioderecém-nascidosde risco. As infecc¸ões foramnotificadasconforme critérios definidospela Agência Nacionalde VigilânciaSanitária.Obancodedadoseaanáliseforamfeitosemprogramainterno.
Resultados: Ocorreu reduc¸ão significativa da notificac¸ão de infecc¸ões por Staphylococcus aureus(p=0,008),semnotificac¸õesdeendocardite,meningiteeinfecc¸õesdeviasaéreas inferi-ores,alémdereduc¸ãonafrequênciadeóbitospelomicrorganismoesemalterac¸ãosignificativa nasincidênciasdeinfecc¸õesporbactériasGramnegativasefungos.Houveaumentodeinfecc¸ões S.aureuscoagulasenegativo(p=0,022),massemaumentodemorbidadeemortalidade. Ocor-reureduc¸ãonamediana dotempo deusodeoxacilina, de11,5para 6dias(p<0,001),com aumentodemedianadeumdiadeusodevancomicina(p=0,046).
Conclusões: Amodificac¸ãodoesquemaempíricocomusodeoxacilinareveloureduc¸ão signifi-cativadasinfecc¸õesporS.aureus,alémdareduc¸ãonafrequênciadeinfecc¸ãodefocoprofundo emortalidadepelomicrorganismo.Considera-sequeoxacilinapodeserusadacomoesquema detratamentodesepseneonataltardiaparaseevitarousodeantibióticosdelargoespectro. ©2016PublicadoporElsevierEditoraLtda.emnomedeSociedadeBrasileiradePediatria.Este ´
eumartigoOpenAccesssobumalicenc¸aCCBY-NC-ND(http://creativecommons.org/licenses/ by-nc-nd/4.0/).
Introduc
¸ão
Os microrganismos mais prevalentes na sepse neonatal tardia descritosna literaturainternacionalsão os Staphy-lococcus coagulase negativo (SCN).1---6 Embora astaxas de
sepseconfirmada emlaboratório devidoaesses microrga-nismosvariemde30%a60%,1tambémforamrelatadastaxas
maiselevadas.Essesmicrorganismosrepresentam77,9%da sepse neonatal tardia em países industrializados e 46,5% em regiões em desenvolvimento.2 Contudo, as infecc¸ões
causadasporessesmicrorganismoscomensaisnormalmente são questionadas devido a dificuldades na confirmac¸ão e diferenc¸asnoscritériosdenotificac¸ão.1,7
Também deve ser considerado que osSCN são micror-ganismos minimamente invasivos que colonizam neonatos após o nascimento e normalmente estão presentes nos microbiomas de diferentes partes do corpo. Eles têm o efeito benéfico de estimular a resposta imune inata e
melhorar a defesa contra outros patógenos.2 Contudo,
os mecanismos de defesa podem ser inadequados em recém-nascidos,aumentarsua susceptibilidade ainfecc¸ão poresses microrganismos.3 Por outro lado,embora sejam
considerados microrganismos responsáveis pela sepse em recém-nascidos,apresentamevoluc¸ãoinsidiosaebaixa mor-bidezemortalidade.2,5,8---11
Sabe-sequeoperfilderesistênciadosSCNpodeexceder 90%comrelac¸ãoàisoxazolilpenicilina.3 Comoresultado,a
vancomicinatemsidoconsideradaotratamentopadrão.1,12
Entretanto,a restric¸ãoàvancomicinacomo terapia empí-rica para sepse neonatal tardia tem sido indicada na literatura.9---11,13
Métodos
Este estudo prospectivo observacional foi feito no Hospi-tal das Clínicas da Universidade Federal de Minas Gerais (HC/UFMG), de janeiro de 2011 a dezembro de 2014. O HC/UFMG,hospitaluniversitário,éumrecursopara geren-ciamentodealtorisco obstétrico em Belo Horizontee no EstadodeMinasGerais.
Apopulac¸ão-alvoconsistiuem todososrecém-nascidos naUTINconsideradosemriscodesepsetardia.Osfatoresde riscoincluíampesoinferiora1.500g,presenc¸adeum cate-tervenosocentral(CVC),usodeventilac¸ãomecânica(VM), cirurgiae tratamento com agentesantimicrobianos.Esses neonatos em risco foramacompanhados diariamentepela equipeespecializadadaComissãodeControledeInfecc¸ão Hospitalar (CCIH). Os dados foram coletados por vigilân-ciaativa,análisedeprontuários médicose discussãocom aequipe médica. As infecc¸õesforamrelatadas deacordo comalegislac¸ãonacional,14comcritériosdeinfec¸ão
defini-dospelaAgênciaNacionaldeVigilânciaSanitária(Anvisa),15
combase naRede NacionaldeSeguranc¸a naAssistênciaà Saúde(NHSN).7,16
Os critérios de inclusão consideraram todos os recém--nascidos tratados com oxacilina ou vancomicina como tratamento empírico para sepse tardia, relatada após 48horasdevida,conformedefinidopelaAnvisa.15‘‘Sepse’’
e ‘‘infecc¸ão da corrente sanguínea’’ foram usados como sinônimos.
Um tamanho da amostra foi calculado considerando a prevalênciade infecc¸ões por SCN e S. aureus confirmada porlaboratórioaumataxadequase30%e15% respectiva-mente,combaseem umapopulac¸ãode300pacientesem riscoporano.
UmprogramainternodaCCIHfoiusadonaanálise esta-tística.Aanálisedescritivaincluiuafrequênciadepacientes em risco, a frequência de pacientes com infecc¸ão hospi-talar(IH),a frequênciadeIH, a incidência cumulativade IH(númerodeIHacada 100pacientesemrisco) ea den-sidade de incidência de IH (número de IH a cada 1.000 pacientes-dia).AdensidadedeincidênciadeIHtambémfoi estratificadadeacordocomafaixadepesoeatopografiada infecc¸ão.Adensidadedeinfecc¸ãodeinfecc¸õesrelacionadas aodispositivofoimedida,incluindoinfecc¸õesassociadasao CVC,àVMeàsondavesicaldedemora(SVD).
Afrequênciademicrorganismosfoidescrita em grupos (SCN,S. aureus, bactérias gram negativas e fungos) e de acordocom afrequênciade agentesantimicrobianos usa-dosnacoberturaempíricaouespecíficadasStaphylococcus
spp. (oxacilina e vancomicina). Em geral, esses agentes antimicrobianossãoempíricaouespecificamenteusadosno tratamento de infecc¸ões com Staphylococcus spp. Outros agentesantimicrobianosnãoforamdescritos,poisnãosão relevantesparaesteestudo.
Oisolamento microbiológicoem amostrasdepacientes foifeitopelo métodoautomatizado (VITEK®2,BioMérieux Inc,EUA)eo testedesusceptibilidade,peladisco-difusão emágar(KirbyBauer).Operfildesensibilidadede microrga-nismosfoidefinidodeacordocomaCCIHdohospitalecom basenoInstitutodePadrõesClínicoseLaboratoriais(CLSI). Paraaanálise comparativa,foramdefinidosdois perío-dos: janeiro de 2011 a dezembro de 2012 (Período 1) e
janeirode2013adezembrode2014(Período2).Duranteo Período1,avancomicinafoiusadanoregimedetratamento empírico de sepse tardia e a oxacilina foi usada durante oPeríodo2.
Amortalidade (mortesem relac¸ão ao númerototal de pacientes em risco)e a letalidade(mortesem relac¸ão ao númerototalde pacientescomIH) foramcomparadasem ambososperíodose selevou emconsiderac¸ãooSCNouo
S. aureus.Oóbitofoiconsideradoassociado àinfecc¸ãose ocorrido duranteou em até15dias dotratamento com o antibióticodoestudo.
Amorbidezfoidefinidacomoumainfecc¸ãocom envolvi-mentodosprincipaissistemasdeórgãos,comoendocardite, infecc¸ão do trato respiratório inferior (pneumonia, tra-queíteoubronquite)ouinfecc¸ãodosistemanervosocentral com isolamento desses microrganismos, bem como vários diasdetratamentoantimicrobianocomoxacilinaou vanco-micina.
Aanáliseestatísticafoifeitaporumestatísticopormeio doStatisticalPackageforSocialSciences®(SPSSInc.,versão 15.0,EUA)edoEpiInfo®v7.0(CDC,EUA).Aanálise descri-tivaincluiufrequência,percentual,média,desviopadrão, medianaefaixa.Aanálisecomparativafoifeitapormeiodo testequi-quadradooudotestedeFisherparaobter variá-veiscategóricasedotestetdeStudentoudeMann-Whitney paraobtervariáveisquantitativas,deacordocomaanálise devariânciapormeiodotestedeLevine.Arazãodechance foiusadaparacalcularamedidarelativadeeventosentreos doisperíodosdoestudoeumintervalodeconfianc¸ade95% (ICde95%)foi usadocomo medidadeprecisão doevento estimado. Arelevância estatísticafoi considerada quando p<0,05.
Outrasestratégiaspreventivasedereduc¸ãodeinfecc¸ões foramusadascontinuamentenaUTINpelaequipedaCCIH. EsteestudofoiaprovadopeloConselhodeRevisão Instituci-onaldoComitêdeÉticaemPesquisadaUFMG.
Resultados
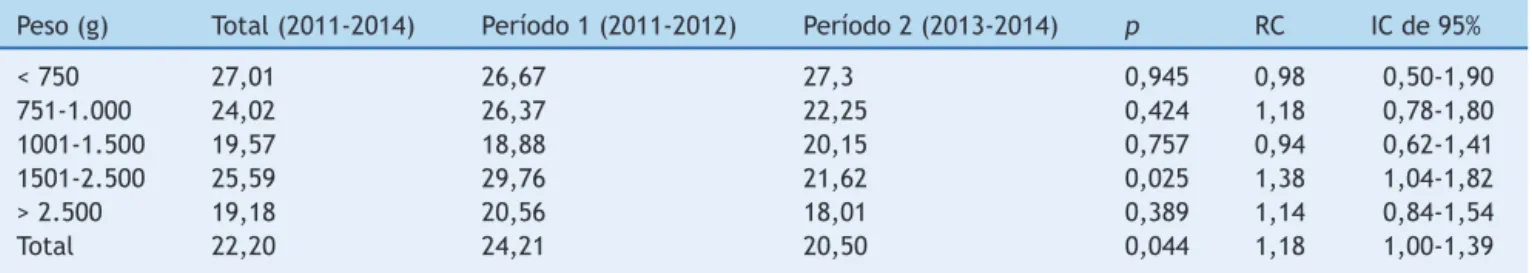
Ao longo doperíodo doestudo, 1.229 pacientes em risco foram acompanhados e totalizaram 26.260 pacientes-dia; 367 pacientes apresentaram 583 episódios de IH, com densidade de incidência de 22,20 episódios de IH em 1.000 pacientes-dia.A tabela1 apresentaa densidadede incidênciadeIHporfaixadepeso aonascer,comreduc¸ão significativa em infecc¸ões entre pacientes de 2.500g a 1.501gduranteo Período2.Houveumareduc¸ão significa-tivanonúmerototaldeinfecc¸õesrelatadas(p=0,044;RC: 1,18;ICde95%1-1,39)(tabela1).
DospacientesemriscoduranteoPeríodo 1e oPeríodo 2,296(54,81%)e355(52,98%)eramdosexomasculino, res-pectivamente.Não houvediferenc¸aestatística noquediz respeitoaosexo(p=0,564;RC:1,08;ICde95%0,85-1,36), porém19recém-nascidosnãotinhamsexodefinido.
AincidênciaacumuladadeIHfoide47,44%depacientes emrisco,comumareduc¸ãosignificativadoprimeiroparao segundoperíododoestudo:de53,8para42,4%(p<0,001).
Tabela1 Incidênciaadedensidadedeinfecc¸õeshospitalaresporfaixadepesoaonascer,UnidadedeTerapiaIntensivaNeonatal,
HC/UFMG,2011-2014
Peso(g) Total(2011-2014) Período1(2011-2012) Período2(2013-2014) p RC ICde95%
<750 27,01 26,67 27,3 0,945 0,98 0,50-1,90
751-1.000 24,02 26,37 22,25 0,424 1,18 0,78-1,80
1001-1.500 19,57 18,88 20,15 0,757 0,94 0,62-1,41
1501-2.500 25,59 29,76 21,62 0,025 1,38 1,04-1,82
>2.500 19,18 20,56 18,01 0,389 1,14 0,84-1,54
Total 22,20 24,21 20,50 0,044 1,18 1,00-1,39
a Númerodeinfecc¸õesem1.000pacientes-dia.
deestudo.Adensidadedeinfecc¸ãodacorrentesanguínea relacionada ao CVC foi de17,29 infecc¸ões por 1.000 dias deCVC e variou de15,39 a 19,09(p=0,117; RC:0,81; IC de95%0,62-1,06).Adensidadedepneumoniarelacionadaà ventilac¸ãomecânicafoide1,93infecc¸õespor1.000diasde VMe varioude2,09a1,79(p=0,789;RC:1,17;ICde95% 0,38-3,62).Adensidadedeinfecc¸ãodotratourinário rela-cionadaàSVDfoide6,05por1.000diasdeSVDevarioude 8,46a4,33(p=0,243;RC:1,96;ICde95%0,62-6,16).
A frequência dos episódios de IH tratada com ambos os antibióticos foi comparada entre os dois períodos e a implantac¸ãodonovoprotocolofoiconsideradaeficaz.Houve uma reduc¸ão significativano uso de vancomicina, de175 para97episódiosdeIHtratadacomvancomicina(p<0,001; RC:1,98;ICde95%1,52-2,60),ehouveumaumento signi-ficativode30para132episódiosdeIHtardiatratadacom oxacilina(p<0,001;RC:4,68;ICde95%3,07-7,17).
Considerando afrequênciadosmicrorganismosisolados em casos de IH em pacientes de alto risco, houve uma reduc¸ão significativa de IHdevido ao S. aureus quando a oxacilina era parte do regime empírico inicial (p=0,012) eumaumentonaIHdevidoaoSCN(p=0,028),porémnão foramobservadasalterac¸õessignificativasnaproporc¸ãode bactériasgram negativasoufungos(tabela2).Todas asS. aureusisoladasdeamostrasdepacientescomIHnoPeríodo 1eram sensíveisaoxacilina.Duranteo Período 2,apenas umaamostraapresentouumperfilresistenteaoxacilinano testedesensibilidade.IssorevelaqueaprevalênciadeS. aureus resistentea oxacilinanessaUTIN foicalculada em 2,4%(n=1/42).
A tabela 3 mostra IH por topografia, considerando infecc¸ões relacionadas a S. aureus e SCN. No Período 2, nãoobservamosinfecc¸ãocomoenvolvimentodosprincipais sistemas de órgãos, como endocardite, infecc¸ão dotrato respiratórioinferiorouinfecc¸ãodosistemanervosocentral comisolamentodeS.aureus;foramrelatadasapenas
con-juntivite,infecc¸ãodapeleeinfecc¸ãodacorrentesanguínea poressemicrorganismo.
A mortalidade e a letalidade foramcalculadas compa-rando casos de óbito devido a IH causada por S. aureus
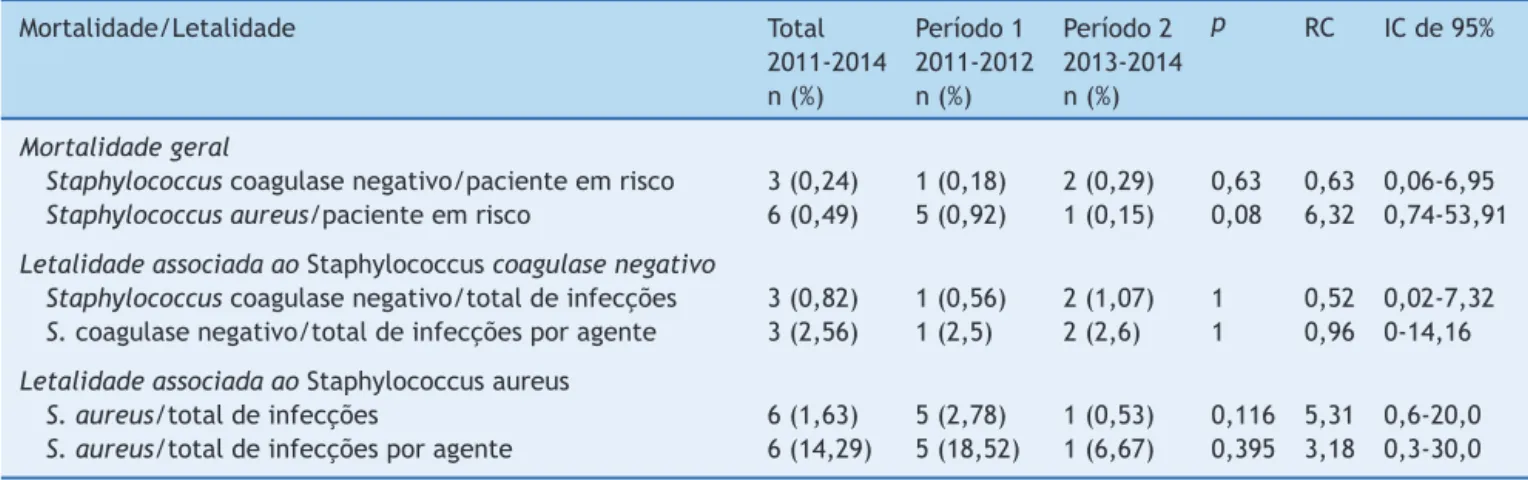
ou SCN entre os dois períodos (tabela 4). A mortalidade foi considerada o número de óbitos associados a essas infecc¸ões em relac¸ão ao número total de óbitos. A leta-lidade foi considerada o número de óbitos associados a essasinfecc¸õesemrelac¸ãoaonúmerototaldecasosdeIH porcadamicrorganismo.Nãohouvevariac¸õessignificativas, porémhouveapenasumóbitoassociadoaS.aureusdurante oPeríodo2(quandoaterapiaempíricaincluíaaoxacilina), em comparac¸ão com cinco óbitosnoPeríodo 1. Nenhuma diferenc¸aestatística foiobservada na mortalidade associ-adaà infecc¸ãoporSCN,com umnúmeromenor deóbitos associados.
Amorbideztambémfoiavaliadaconsiderandoadurac¸ão dotratamentoantimicrobiano.Houveumareduc¸ão signifi-cativanadurac¸ãodotratamentocomoxacilinanoPeríodo2, comreduc¸ãodotempomédiode11,5para6dias(p<0,001). Adurac¸ãodotratamentocomvancomicinaaumentou ape-nas1dia,varioude8diasnoPeríodo1para9diasnoPeríodo 2(p=0,046).
Discussão
Após a introduc¸ão do tratamento empírico com oxacilina noregimeterapêuticoparasepsetardia,observamos uma reduc¸ãosignificativanoscasosdeIHcausadosporS.aureus sensívelà oxacilina(p=0,012). Aincidência dadensidade dasinfecc¸ões tambémdiminuiu significativamentee ficou evidenteprincipalmenteempacientescompesoentre1.501 e2.500g.Umestudoanterior17jámostrouumnúmeromaior
de pacientes nessa faixade peso com risco de infecc¸ões nacorrentesanguíneaconfirmadasemlaboratório,devido,
Tabela2 Frequênciademicrorganismosisoladoseminfecc¸õeshospitalaresporpacienteemrisco,UnidadedeTerapiaIntensiva Neonatal,HC/UFMG,2011-2014
Microrganismo Total Período1 Período2 p RC ICde95%
2011-2014 2011-2012 2013-2014
n(%) n(%) n(%)
Staphylococcuscoagulasenegativo 117(9,52) 40(7,37) 77(11,22) 0,028 0,63 0,41-0,95
Staphylococcusaureus 42(3,42) 27(4,97) 15(2,19) 0,012 2,34 1,18-4,67
Bacilogramnegativo 91(7,40) 47(8,66) 44(6,41) 0,167 1,38 0,88-2,17
Tabela3 Infecc¸õeshospitalaresporS.aureuseStaphylococcuscoagulasenegativo(SCN)portopografia,UnidadedeTerapia IntensivaNeonatal,HC/UFMG,2011-2014
Topografia Microrganismo Período1 Período2 p RC ICde95%
n(%) n(%)
Conjuntivite SCN 5(38,5) 2(22,2) 0,648 2,19 0,23---20,0
S.aureus 3(23,1) 2(22,2) 1 1,05 0,10---12,44
Endocardite SCN - - - -
-S.aureus 3(100) 0 - -
-Enterocolitenecrosante SCN - 1(6,7) - -
-S.aureus - 0 - -
-Infecc¸ãointra-abdominal SCN - 1(50) - -
-S.aureus - 0 - -
-Infecc¸ãovascular SCN - 3(100) - -
-S.aureus - 0 - -
-Infecc¸ãodepeleoudo tecidomole
SCN 0 2(3,2) - -
-S.aureus 1(2,0) 1(1,6) 1 1,22 0,0---20,0
Bronquiteoutraqueíte SCN 0 - - -
-S.aureus 1(50,0) - - -
-Pneumonia SCN 0 - - -
-S.aureus 1(8,3) - - -
-Infecc¸ãodotrato urinário
SCN 1(7,1) 2(13,3) 1 0,5 0,02---8,61
S.aureus 0 0 - -
-Infecc¸ãodosistema nervosocentral
SCN 0 2(28,6) - -
-S.aureus 3(15,8) 0 - -
-Infecc¸ãodacorrente sanguínea(sepse)
SCN 34(21,38) 64(38,1) 0,001 0,44 0,26-0,74
S.aureus 15(9,4%) 12(7,1) 0,58 1,34 0,58-3,20
provavelmente,aoperfildessaUTIN,jáquesetratadeum CentrodeMedicinaFetal.Essespacientestêminternac¸ões prolongadas e estão em risco denecessidade decirurgia, CVCeVM,quepoderãoaumentaroriscodeinfecc¸ão.
Apesardoaumentonoscasosdeinfecc¸ãorelacionadaa SCN,nãoobservamosaumentonamortalidadeena morbi-dezavaliada.Issoindicaque essemicrorganismo podeser consideradomenospatogênicoeapresentaevoluc¸ão insidi-osaemcomparac¸ãocomoS.aureus,conformerelatadona literatura.1,2,12
Tambémdeveserindicadoqueainfecc¸ãoporSCNpoderá ser questionada e os critérios de diagnóstico exigem no mínimoduashemoculturascomomesmomicrorganismo.7,15
Alémdisso,outrosestudosdemonstramqueépossível acom-panhar os resultados clínicos, aguardar por resultados da cultura e tambémadiar a administrac¸ão de agentes anti-microbianos em pacientes com suspeita de infecc¸ão por SCN.9---11,18
Após a modificac¸ão do regime de tratamento empí-rico para incluir o uso de oxacilina, houve um aumento nas infecc¸ões relacionadas ao SCN. Entretanto, não foi detectadadiferenc¸aestatísticaempercentuaisdeinfecc¸ão associada a bactérias gram negativase fungos. Foi consi-derado que nãohouve interferêncianegativa no perfilda florae,consequentemente,noperfildeexposic¸ãodo paci-ente.Adicionalmente,foiatingidaumareduc¸ãoestatística
Tabela 4 Mortalidadee letalidade de pacientescomIH porStaphylococcus spp.,Unidade deTerapia IntensivaNeonatal, HC/UFMG,2011-2014
Mortalidade/Letalidade Total Período1 Período2 p RC ICde95%
2011-2014 2011-2012 2013-2014
n(%) n(%) n(%)
Mortalidadegeral
Staphylococcuscoagulasenegativo/pacienteemrisco 3(0,24) 1(0,18) 2(0,29) 0,63 0,63 0,06-6,95 Staphylococcusaureus/pacienteemrisco 6(0,49) 5(0,92) 1(0,15) 0,08 6,32 0,74-53,91
LetalidadeassociadaaoStaphylococcuscoagulasenegativo
Staphylococcuscoagulasenegativo/totaldeinfecc¸ões 3(0,82) 1(0,56) 2(1,07) 1 0,52 0,02-7,32 S.coagulasenegativo/totaldeinfecc¸õesporagente 3(2,56) 1(2,5) 2(2,6) 1 0,96 0-14,16
LetalidadeassociadaaoStaphylococcusaureus
S.aureus/totaldeinfecc¸ões 6(1,63) 5(2,78) 1(0,53) 0,116 5,31 0,6-20,0
geral de IH. Deve ser enfatizado que um número menor de infecc¸ões está diretamente relacionado ao uso menor de agentes antimicrobianos. Conformerelatado por Pinto etal.,6oscritériosparareduzirasepseincluemreduzir,de
formasignificativa,o usodevancomicinaecarbapenema, bemcomoaquantidadedeagentesantimicrobianosusada, apesardeessesautoresnãoapresentaremumperfildaflora. Conforme publicado em outros relatórios,9,11 este
estudo revelou que o tratamento empírico com oxacilina aindareduziu significativamentea durac¸ão dotratamento (p<0,001)em maisde50% dosdias,com aumentodeum único dia com a vancomicina noPeríodo 2. A reduc¸ão no númerodediasdeusodeoxacilinapode, provavelmente, serassociadaaousoempíricoouespecíficoadequado,pois aoxacilinatemmelhoratividadeantimicrobianaeeficácia terapêuticaeminfecc¸õessensíveisporS.aureus.É impor-tante ressaltar que o S. aureus tem um perfil sensível à oxacilinanessaUTIN,oquejustificaaalterac¸ãodaterapia empírica.
Em umestudonacional deBentlinetal.,19 que
investi-goupráticasrelacionadasàprevalênciadasepsetardiaem neonatos prematuros, os autores observaram que centros que usam terapia empírica com oxacilina e aminoglicosí-deosapresentammenorincidênciadesepsetardia,devido, provavelmente,aumtratamentomaiseficaz.
Considerando a recomendac¸ão de isoxazolilpenicilinas associadas à gentamicina como tratamento empírico de sepseneonataltardia, umestudodeChiuetal.9 também
mostrou umareduc¸ão significativano usode vancomicina e um aumento no uso de oxacilina sem diferenc¸a signifi-cativana morbidez e na mortalidade neonataisconforme avaliadopelaincidênciadasepsetardia,meningiteeóbito. Contudo,essesautoresnãocompararampacientescomIH relacionadaa S.aureus eSCNconfirmadas em laboratório comonesteestudo,oquemostraumareduc¸ãosignificativa nosepisódiosdeinfecc¸õesrelacionadasaS.aureus,comum númeromenordecasosdeinfecc¸õescomenvolvimentodos principaissistemasdeórgãos,comoendocardite, infecc¸ão dotratorespiratórioinferioreinfecc¸ãodosistemanervoso central.
Além de uma reduc¸ão estatística no número geral de IH, bem como IH devido a S. aureus suscetível, também foi observadoumnúmero menor deinfecc¸ões com envol-vimentodosprincipaissistemasdeórgãos,foiobservadaa reduc¸ãodamortalidadeassociadaaessemicrorganismoefoi demonstradaumareduc¸ãosignificativanosdiasdedurac¸ão dotratamentoeinternac¸ão.Essesachadospodemser consi-deradosadequadosparaevitaramorbidezassociadaàsepse eaexposic¸ãoaoutroseventosadversos.Conformerelatado porKaufman,20aprecisãonodiagnósticoeareduc¸ãodouso
deagentesantimicrobianossão importantesnaprevenc¸ão deinfecc¸õesemgeral e,especificamente,damortalidade neonatalrelacionadaàsepse.
Umestudomulticêntricocom348UTINs11 avaliououso
imediato de vancomicina (< 1 dia) e o uso postergado (1 a 3 dias) no primeiro episódio de sepse tardia associ-adaaSCN.Osautoresrelataramque nãohouvediferenc¸a nastaxasdemortalidadeem 7ou30diasapósoiníciodo tratamentoounaalta.Adicionalmente,pacientesque ini-ciaramousodevancomicinaapresentaramimediatamente umadurac¸ãosignificativamentemaiordetratamento,com medianade2diasadicionais.Emoutroestudomulticêntrico
conduzidopelomesmogrupo,18nãohouvediferenc¸ana
mor-talidadeaosecompararemosrecém-nascidoscominfecc¸ão porSCN possível, provável ou confirmada. Além disso, os autoresrelataram que ospacientes cominfecc¸ões associ-adasao SCN apresentarammortalidade significativamente menor do que os pacientes com hemoculturas negativas, considerandoquea mortalidade maiselevadapoderiaser atribuídaaoutrosmicrorganismosnãoisoladosem hemocul-turas.Deveserconsideradoqueumagenteantimicrobiano poderáserusadodesnecessariamente,conformeaspossíveis ouprováveisinfecc¸õesporSCNforemsuperestimadas.
Cottenetal.,21 emumestudodecoortemulticêntrico,
constataram em umaanálise multivariada que a durac¸ão prolongadadaterapia inicialem dias estavaassociada ao óbitodeneonatos deextremobaixo peso, principalmente seotratamentocomagentesantimicrobianosultrapassasse cinco dias, com aumento das chances por dia de uso de antimicrobianos.Tambémdeveserconsideradoquea mor-talidadeaumentaquandoaterapiaempíricaéinadequada, umfatorquepodeaumentaradurac¸ãodotratamento.
Um estudo anterior na mesma UTIN revelou alta mor-talidadedepacientescomsepseporS. aureusconfirmada porlaboratório.5Nesteestudo,observamosumareduc¸ãona
frequênciade óbitos devidoa IHrelacionada a S. aureus
noPeríodo2(1óbito)emcomparac¸ãoaoPeríodo1(5 óbi-tos). Essa reduc¸ão tendia a ser significativa (p=0,08). O único óbitoassociado aS. aureus no Período 2foi de um pacientecom váriasmalformac¸õese possível trissomiado cromossomo13. Devido à gravidade clínica dadoenc¸ado paciente, foram feitos testes para triagem da infecc¸ão. Contudo,o tratamento com oxacilina foi iniciado quando osresultados da hemocultura foramdivulgados, dois dias após o teste. O óbito poderá estar associado à doenc¸a debase e à demora nouso de umagente antimicrobiano adequado.
Esteestudoidentificouapenasumedoiscasosdeóbito devidoaIHrelacionadaaSCN nosPeríodos1e 2, respec-tivamente,semrelevânciaestatística.Aliteraturatambém informaqueamortalidadeassociadaainfecc¸ãoporSCNestá relacionadaa1%doscasos.5,10Karlowiczetal.10
investiga-ramcausas desepsetardiafulminantee observaramque, mesmoquandooscasosdeinfecc¸ãoporSCNforam associa-dosaóbito,ospacientesapresentavamoutrascomorbidades ouasculturasproduzirammaisdeummicrorganismo,oque sugerecontaminac¸ão.Mackhouletal.8avaliaramfatoresde
riscodemortalidadeprecoceapóssepseneonataltardiae relataramqueospacientescominfecc¸õescausadasporSCN apresentavamumriscomenordeóbitoemcomparac¸ãocom pacientescominfecc¸ões causadasporoutros microrganis-mos.
EmumestudofeitoporHemelsetal.13 usou-se
Considerando o uso racional de antibióticos, o uso da vancomicinadeveriaserrestritoemunidadescomalta pre-valênciade S. aureus resistentea vancomicina,em casos sem resposta clínica ou laboratorial em até 48-72 horas, apesar do uso de um betalactâmico como a oxacilina, e em casosdefinidosdeSCN resistentea oxacilinasem res-postaclínicaequenãosejaconsideradocomensal.1,22Essas
recomendac¸õesseguemasdiretrizesdoCentrodeControle ePrevenc¸ãodeDoenc¸asafimdeevitaraumento significa-tivo de cepas de Enterococcus spp e de outras bactérias resistentes a vancomicina.23 A restric¸ão do uso de
agen-tesantimicrobianoscombasenagestãoéimportantepara reduzirainterferêncianomicrobioma,naselec¸ãode micror-ganismosresistenteseemmanifestac¸õesatópicaseoutras complicac¸õesem neonatosprematuros,comoenterocolite eóbito.24
Concluindo, este estudo mostrou que nãohouve pioria dos resultados em recém-nascidos ao se usarem beta-lactâmicos antiestafilocócicos para tratar sepse tardia, considerandoqueastaxasdemortalidadeemorbidez relaci-onadasainfecc¸õesporSCNnãoaumentaramequetambém houveumamelhorianastaxasdeinfecc¸õesrelacionadasà
S.aureus.Assim,agestãodeantimicrobianoscomousoda oxacilinapodeser recomendada na sepse neonataltardia deacordocom operfilepidemiológico decada UTIN,que deveestar relacionada aoutras práticasde prevenc¸ãode infecc¸õeseficazesafimdeevitarousodeagentes antimi-crobianosdeamploespectro.
Conflitos
de
interesse
Osautoresdeclaramnãohaverconflitosdeinteresse.
Referências
1.BlanchardAC,QuachC,AutmizguineJ.Staphylococcal infecti-onsininfants:updatesandcurrentchallenges.ClinPerinatol. 2015;42:119---32,ix.
2.Dong Y, Speer CP.The roleof Staphylococcusepidermidisin neonatalsepsis:guardingangelorpathogenicdevil?IntJMed Microbiol.2014;304:513---20.
3.Venkatesh MP, Placencia F, Weisman LE. Coagulase-negative staphylococcalinfectionsintheneonateandchild:anupdate. SeminPediatrInfectDis.2006;17:120---7.
4.Stoll BJ, Hansen N. Infections in VLBW infants: studies fromtheNICHDNeonatalResearchNetwork.SeminPerinatol. 2003;27:293---301.
5.RomanelliRM,AnchietaLM,MourãoMV,CamposFA,LoyolaFC, JesusLA,etal.Notificationofhealthcareassociatedinfections basedoninternationalcriteriaperformedinareference neo-natal progressivecare unityinBelo Horizonte,MG. RevBras Epidemiol.2013;16:77---86.
6.PintoMC,BuenoAC,VieiraAA.Implementationofaprotocol proposedbytheBrazilianNationalHealthSurveillanceAgency forantibioticuseinverylowbirthweightinfants.JPediatr(Rio J).2013;89:450---5.
7.CenterforDiseasesControlandPrevention(CDC).Bloodstream
infectionevent(centralline-associatedbloodstreaminfection
andnon-centralline-associatedbloodstreaminfection).[citado
em 5 de setembro de 2015]. Disponível em: http://www.
cdc.gov/nhsn/PDFs/pscManual/4PSCCLABScurrent.pdf. 8.MakhoulIR,SujovP,SmolkinT,LuskyA,ReichmanB,Israel
Neo-natal Network. Pathogen-specificearlymortalityin verylow
birthweightinfantswithlate-onsetsepsis:anationalsurvey. ClinInfectDis.2005;40:218---24.
9.ChiuCH, MichelowIC, Cronin J, Ringer SA, Ferris TG, Puo-polo KM.Effectiveness of a guideline to reducevancomycin useintheneonatalintensivecare unit.PediatrInfect DisJ. 2011;30:273---8.
10.Karlowicz MG, Buescher ES,Surka AE. Fulminant late-onset sepsisin a neonatalintensive care unit,1988-1997,and the impact of avoiding empiric vancomycin therapy. Pediatrics. 2000;106:1387---90.
11.Ericson JE, Thaden J, Cross HR, Clark RH, Fowler VG Jr, Benjamin DK Jr, et al. No survival benefit with empirical vancomycintherapyforcoagulase-negativestaphylococcal blo-odstreaminfectionsininfants.Pediatr InfectDisJ.2015;34: 371---5.
12.MarchantEA,BoyceGK, SadaranganiM,LavoiePM.Neonatal sepsisduetocoagulase-negativestaphylococci.ClinDev Immu-nol.2013;2013:586076.
13.HemelsMA,vandenHoogenA,Verboon-MaciolekMA,FleerA, KredietTG.Aseven-yearsurveyofmanagementof coagulase--negativestaphylococcalsepsisintheneonatalintensivecare unit:vancomycinmaynotbenecessaryasempirictherapy. Neo-natology.2011;100:180---5.
14.Brasil.MinistériodaSaúde.Portaria2616/98,de12demaiode 1998.Regulamentaasac¸õesdecontroledeinfecc¸ãohospitalar nopaís.Brasília:MinistériodaSaúde;1998.
15.Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Critérios diagnósticos de infecc¸ão relacionados à assistência a saúde --- Neonatologia. Brasília: Ministério da Saúde;2013.
16.Center for DiseasesControl and Prevention.CDC/NHSN sur-veillancedefinitionsforspecifictypesofinfections.[cited08 Dec 2015]. Available from: http://www.cdc.gov/nhsn/PDFs/ pscManual/17pscNosInfDefcurrent.pdf.
17.Romanelli RM, Anchieta LM, Mourão MV, Campos FA, Loyola FC, Mourão PH, et al. Risk factors and lethality of laboratory-confirmed bloodstream infection caused by non--skin contaminant pathogens inneonates. J Pediatr (Rio J). 2013;89:189---96.
18.Jean-BaptisteN,BenjaminDKJr,Cohen-WolkowiezM,Fowler VGJr,LaughonM,ClarkRH,etal.Coagulase-negative staphy-lococcalinfectionsintheneonatalintensivecareunit.Infect ControlHospEpidemiol.2011;32:679---86.
19.BentlinMR,RugoloLM,FerrariLS,BrazilianNeonatalResearch Network (Rede Brasileira de Pesquisas Neonatais). Practices relatedtolate-onsetsepsisinverylow-birthweightpreterm infants.JPediatr(RioJ).2015;91:168---74.
20.KaufmanDA.Less is more:decreasing antibiotic daysinthe NICU.JPediatr(RioJ).2013;89:424---5.
21.Cotten CM, Taylor S, Stoll B, GoldbergRN, Hansen NI, Sán-chezPJ,etal.Prolongeddurationofinitialempiricalantibiotic treatment is associated with increased rates of necrotizing enterocolitisanddeathforextremelylowbirthweightinfants. Pediatrics.2009;123:58---66.
22.LiuC,BayerA,CosgroveSE,DaumRS,FridkinSK,GorwitzRJ, et al. Clinicalpractice guidelines bythe InfectiousDiseases SocietyofAmericaforthetreatmentofmethicillin-resistant
Staphylococcusaureusinfectionsinadultsand children.Clin InfectDis.2011;52:e18---55.
23.Center for Diseases Control and Prevention (CDC). Recom-mendations for preventing the spread of vancomycin resis-tance recommendations of the Hospital Infection Con-trol Practices Advisory Committee (HICPAC). [citado em 2 de setembro de 2015]. Disponível em: http://www.cdc. gov/mmwr/preview/mmwrhtml/00039349.htm.