UNIVERSIDADE FEDERAL DO RIO GRANDE DO NORTE CENTRO DE CIÊNCIAS DA SAÚDE
PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS DA SAÚDE
COMPARAÇÃO DE EFEITOS DOS EXTRATOS DE
HYPERICUM PERFORATUM (HIPÉRICO) E DE MENTHA CRISPA (HORTELÃ)
EM DIFERENTES MODELOS EXPERIMENTAIS.
SEBASTIÃO DAVID DOS SANTOS FILHO
Natal, RN
COMPARAÇÃO DE EFEITOS DOS EXTRATOS DE
HYPERICUM PERFORATUM (HIPÉRICO) E DE MENTHA CRISPA (HORTELÃ) EM DIFERENTES MODELOS EXPERIMENTAIS.
SEBASTIÃO DAVID DOS SANTOS FILHO
Tese apresentada à Universidade Federal do Rio
Grande do Norte, para a obtenção do título de
Doutor em Ciências da Saúde pelo Programa de
Pós-Graduação em Ciências da Saúde.
Orientador: Prof. Dr. Mário Bernardo Filho
Co-orientador: Prof. Dr. Aldo da Cunha Medeiros
Natal, RN
2007
CATALOGAÇÃO NA FONTE
S237 Santos Filho, Sebastião David dos.
Comparação de efeitos dos extratos de Hypericum perforatum (Hipérico) e de Mentha crispa (Hortelã) em diferentes modelos experiemtais. / Sebastião David dos Santos Filho. – 2007.
x, 81f. : il.
Orientador : Mario Bernardo-Filho. Co-orientador : Aldo da Cunha Medeiros.
Tese (doutorado) – Universidade Federal do Rio Grande do Norte, Centro de Ciências da Saúde.
1. Plantas medicinais - Teses. 2. Radiobiologia - Teses .3. Tecnécio - Teses. 4. Eritrócitos - Teses. 5. Plasma sangüíneo - Teses. 6. Proteínas - Teses. I. Bernardo-Filho, Mario. II. Medeiros, Aldo da Cunha. III. Universidade Federal do Rio Grande do Norte.Centro de Ciências da Saúde. IV. Título.
UNIVERSIDADE FEDERAL DO RIO GRANDE DO NORTE
CENTRO DE CIÊNCIAS DA SAÚDE
PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS DA SAÚDE
Prof.Dr. Aldo da Cunha Medeiros
Coordenador do Programa de Pós-graduação em Ciências da Saúde
Natal, RN
2007
SEBASTIÃO DAVID DOS SANTOS FILHO
COMPARAÇÃO DE EFEITOS DOS EXTRATOS DE
HYPERICUM PERFORATUM (HIPÉRICO) E DE MENTHA CRISPA (HORTELÃ) EM
DIFERENTES MODELOS EXPERIMENTAIS.
PRESIDENTE DA BANCA: Prof. Dr. Mario Bernardo Filho (UERJ)
BANCA EXAMINADORA
Prof. Dr. Mario Bernardo Filho (UERJ)
Prof. Dr. José Brandão Neto (UFRN)
Prof. Dr. Maria Teresa Jansem de Almeida Catanho (UFPE)
Prof. Dr. Eryvaldo Sócrates Tabosa do Egito (UFRN)
Prof. Dr. Adriana Augusto de Resende (UFRN)
Prof. Dr. Eveline Pipolo Milan (UFRN – suplente)
2007
DEDICATÓRIA
In memoriam, dedico este título ao meu pai Sebastião David dos Santos que me
agraciou com seu amor, paciência e determinação, para que seu filho pudesse
alcançar objetivos que ele não alcançou.
À minha mãe Thereza Girão dos Santos, meus filhos Fabiana, Mariana, Luiz
Eduardo e Elisa que foram fonte de energia quando precisei para poder atingir este
sonho.
À minha esposa e companheira de todas as horas, alegres e tristes, Maristela
Mascarenhas Nascimento, todo o meu amor.
DEUS reconhece a dignidade de teu servo.
AGRADECIMENTOS
Obrigado Senhor por ter me concedido a oportunidade de colaborar com mais um
conhecimento para a humanidade.
Ao Professor Mario Bernardo Filho, que como orientador e amigo, soube indicar
caminhos e sugerir soluções para que esta caminhada pudesse ter êxito, minha
amizade, respeito e admiração.
Ao Professor Aldo da Cunha Medeiros por todo incentivo e acompanhamento dos
trabalhos realizados.
Ao Professor José Brandão Neto pela acolhida no programa de Pós-Graduação em
Ciências da Saúde e por todo incentivo a que o doutorado fosse concluído.
Ao Programa de Pós-graduação em Ciências da Saúde. Ao auxílio dado pelo CNPq.
Aos amigos Adalgisa Ieda Maiworm, Giuseppe Antonio Presta, Severo de Paoli e
Tânia Santos Giani, meus irmãos na ciência, em todos os momentos difíceis e nos
momentos de alegria, muito obrigado.
Ao serviço de Medicina Nuclear, ao Laboratório de Endocrinologia e ao Laboratório
Central do Hospital Universitário Pedro Ernesto pelo suporte aos resultados obtidos.
A todos que direta ou indiretamente possibilitaram a realização deste trabalho.
LISTA DE ABREVIAÇÕES, SIGLAS E SÍMBOLOS.
DNA ácido desoxirribonucléico
LB Luria Broth
O-2x radical superóxido
OHx radical hidroxila
H2O2x peróxido de hidrogênio
O2 oxigênio
ANOVA análise de variância
ATP adenosina trifosfato
Bq Bequerel (unidade de atividade de amostra radioativa no Sistema
Internacional, sendo que 1 Bq equivale a uma desintegração por segundo)
BC Blood Cell (célula sanguínea)
Ca++ íon cálcio
Cl- íon cloreto
FI-C fração insolúvel da célula
FS-P fração solúvel da célula
FI-P fração insolúvel do plasma
FS-P fração solúvel do plasma
J radiação gama
Hb hemoglobina
HCO3- íon bicarbonato
MBq megabequerel
Pg micrograma
Pl microlitro
Mo molibdênio
NaCl cloreto de sódio
P plasma
PP proteína plasmática
% ATI porcentagem de radioatividade
rpm rotações por minuto
Sn+2 íon estanoso
SnCl2 cloreto estanoso
99mTc tecnécio-99m
TCA ácido tricloroacético
TcO4- íon pertecnetato
Na99mTcO4 pertecnetato de sódio
UI Unidade internaciomal
IPEN Instituto de Pesquisas Energéticas e Nucleares de São Paulo
CNEN Comissão Nacional de Energia Nuclear
RBC Célula Vermelha do Sangue
SUMÁRIO
Lista de abreviações………...………vii
Sumário...………....ix
Resumo………....x
1 Introdução...01
2 Revisão de literatura...03
3 Artigos anexados...08
3.1 Artigo publicado...10
3.2 Manuscritos no prelo...11
3.3 Manuscritos submetidos...47
4 Comentários, críticas e conclusões...64
5 Anexos...68
6 Referências...71
7 Abstract...76
RESUMO
Avaliações clínicas têm sido possíveis com radiobiocomplexos marcados com
tecnécio-99mTc (99mTc). Drogas naturais ou sintéticas são capazes de interferir na
marcação de estruturas sanguíneas com 99mTc, assim como na biodistribuição de
radiobiocomplexos. Também tem sido descrita a toxicidade de vários produtos
naturais. O objetivo deste estudo foi comparar o efeito dos extratos de Mentha
crispa (hortelã) e de Hypericum perfloratum (hipérico) em diferentes modelos experimentais. Na marcação de estruturas sangüíneas com 99mTc verificou-se que
ambos os extratos foram capazes de diminuir a radioatividade no compartimento
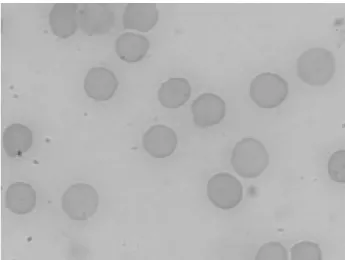
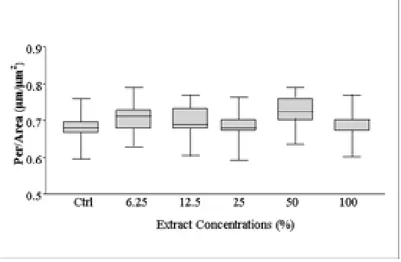
celular, nas proteínas plasmáticas e celulares. Na morfometria das hemácias,
apenas a hortelã foi capaz de alterar a forma e a relação perímetro/áreas das
hemácias. Na biodistribuição do radiobiocomplexo pertecnetato de sódio
(Na99mTcO4) a hortelã aumentou a captação do Na99mTcO4 no rim, no baço, no
fígado e na tireóide, enquanto que o hipérico diminuiu a captação do Na99mTcO4 no
osso, no estômago, no pulmão e na tireóide, e aumentou no pâncreas. Na
sobrevivência de culturas bacterianas o hipérico foi capaz de proteger a bactéria do
efeito danoso do cloreto estanoso (SnCl2). O hipérico não alterou a topologia nem
protegeu o DNA plasmidial da ação do SnCl2. Provavelmente os efeitos
apresentados por ambos os extratos poderiam ser explicados por substâncias
presentes nos extratos que poderiam alterar a morfologia das hemácias, o
transporte de íons pela membrana e/ou formar fitocomplexos. O estudo teve caráter
multidisciplinar com a participação das seguintes áreas do conhecimento:
Radiobiologia, Botânica, Endocrinologia, Fitoterapia e Hematologia.
Palavras-chave: hemácias; plasma; proteínas, tecnécio-99m; radiobiocomplexos;
ratos;Hypericum perforatum;Mentha crispa.
1
1 INTRODUÇÃO
O uso de produtos naturais é uma prática generalizada na
medicina popular. A pesquisa acadêmica trouxe novos conhecimentos sobre as
plantas e suas propriedades terapêuticas. O crescente aumento do interesse
da comunidade acadêmica em estudar os medicamentos naturais tem
contribuído para o uso cada vez mais freqüente de produtos naturais. Existem
alguns estudos sobre o efeito de plantas medicinais na marcação de hemácias
com tecnécio-99m (99mTc) (1, 2).
Nos procedimentos em medicina nuclear, o cloreto estanoso
(SnCl2) é freqüentemente usado como um agente redutor na marcação de
moléculas e células com 99mTc para obtenção de imagens cintilográficas.
Estudos com culturas bacterianas com diferentes capacidades do reparo de
lesões no DNA revelaram que essas lesões causadas pelo SnCl2 acarretavam
um efeito letal que parece ser mediado pela geração de radicais livres (3). Foi
relatado que o efeito do SnCl2 também dependeria da presença de mecanismo
de restauração (4, 5) e que o SnCl2 também é capaz de promover a quebra de
DNA plasmidial (3, 6, 7).
O mecanismo de ação do Hypericum perforatum (erva de
São João) e da Mentha crispa (hortelã) ainda não estão bem esclarecidos, e
até hoje não há descrição na literatura de sua influência na biodistribuição dos
radiofármacos empregados na Medicina Nuclear, nem os seus efeitos na
radiomarcação de elementos sangüíneos e em nível morfológico nos diversos
2
Este estudo teve como objetivo teórico e prático comparar
efeitos dos extratos de Hypericum perforatum (Hipérico) e de Mentha crispa
(Hortelã) em diferentes modelos experimentais.
Os modelos experimentais utilizados na presente pesquisa
avaliaram os efeitos biológicos da hortelã e do hipérico na marcação de
elementos sangüíneos com o tecnécio-99m, na biodistribuição do radiofármaco
(radiobiocomplexo) pertecnetato de sódio (Na99mTcO
4) e na morfologia de
hemácias e em culturas bacterianas tratadas com SnCl2.
A pesquisa foi realizada no Laboratório de Radiofarmácia
Experimental do Departamento de Biofísica e Biometria, e no Departamento de
Histologia do Instituto de Biologia Roberto Alcantara Gomes da Universidade
do Estado do Rio de Janeiro. Os experimentos foram possíveis através de
convênio firmado entre a Universidade do Estado do Rio de Janeiro e a
Universidade Federal do Rio Grande do Norte, sob a orientação do Professor
Doutor Mario Bernardo Filho, e na vigência dos auxílios concedidos pela
3
2 REVISÃO DE LITERATURA
A descoberta das radiações ionizantes e de elementos
radioativos despertou de imediato o interesse de suas aplicações na Biologia e
nas Ciências Médicas. Como a origem do fenômeno radioativo é nuclear, os
nuclídeos que emitem radiação são chamados mais apropriadamente de
radionuclídeos (8). Alguns nuclídeos existentes na natureza já são radioativos
(naturais) enquanto outros podem ser produzidos pelo homem (artificiais) (8,9).
Em medicina nuclear os radionuclídeos podem ser utilizados como fonte de
radiação ou como traçador. No primeiro caso, o material biológico recebe
apenas as radiações emitidas pelo radionuclídeo usado. No segundo, o próprio
radioisótopo é incorporado no meio biológico que se deseja estudar (10, 11,
12).
Os radionuclídeos quando utilizados na área biomédica têm
possibilitado a elucidação de inúmeros fenômenos que ocorrem nos seres
vivos, inclusive no homem, onde os mesmos são administrados como
radiofármacos (radiobiocomplexos), que são células ou moléculas marcadas
com o radionuclídeo, amplamente utilizadas em medicina nuclear, para
diagnóstico e para terapia (10, 13, 14). A utilização em medicina nuclear é
interessante pelo fato das doses administradas em diagnóstico acarretarem
uma baixa exposição do paciente e produzirem imagens de excelentes
qualidades (15).
O processo de marcação de células e moléculas com o
radionuclídeo tecnécio-99m (99mTc) normalmente necessita da utilização de
4
diferentes agentes químicos, sendo que o cloreto estanoso (SnCl2) é o agente
redutor mais freqüentemente utilizado para esta finalidade. O SnCl2 possui uma
eficiência de marcação do traçador radioativo superior a de outros agentes
redutores, justificando sua preferência, não só na medicina nuclear, mas
também na marcação de diversas estruturas de interesse biomédico (14, 16).
Estudos clínicos de diagnóstico em procedimentos estáticos
e avaliações dinâmicas têm sido possíveis com os radiofármacos marcados
com o 99mTc (8, 17, 18, 19) que é obtido como pertecnetato de sódio
(Na99mTcO4) por meio de um gerador 99Mo/99mTc.
A marcação de hemácias com 99mTc representa uma das
técnicas de relevância na medicina nuclear, e é aperfeiçoada em resposta ao
grande número de exames clínicos em que é utilizada (20,21). Hemácias
marcadas com 99mTc são utilizadas em medicina nuclear para a obtenção de
imagens do pool sangüíneo, avaliação do sistema cardiovascular, volemia e
hemorragias gastrintestinais (14,22). Além disso, novas aplicações têm sido
realizadas com este radiofármaco incluindo a determinação do fluxo sangüíneo
no miocárdio e no cérebro, de imagens do osso e para o diagnóstico da função
excretora do fígado e dos rins (21).
Estudos realizados demonstraram que na marcação de
hemácias com 99mTc, o ânion pertecnetato atravessa o espaço intracelular por
troca com os íons cloreto e/ou bicarbonato (23,24). Estes fatos indicam que o
processo de marcação ocorre em nível intracelular. Somando-se a isso, o
agente redutor, SnCl2, também parece ser transportado para o interior da
hemácia por um sistema de transporte específico, o canal de cálcio (5,25). Na
5
se ligar com as proteínas plasmáticas dependendo da concentração do agente
redutor, do radiobiocomplexo utilizado e do tempo de incubação considerado,
como pode ser observado pela técnica de precipitação com ácido
tricloroacético (2). Ao administrar-se um radiofármaco a um paciente sempre
uma fração do mesmo é encontrada ligada às proteínas plasmáticas (14, 26).
Quando um radiofármaco é administrado a um paciente,
ocorre o processo de biodistribuição. Este processo consiste de: (i) absorção,
(ii) distribuição, (iii) metabolismo e (iv) excreção da substância (27). Os
radiobiocomplexos são designados a ter uma biodistribuição específica e/ou
um padrão de eliminação quando administrados a indivíduos normais. Na
presença de alterações fisiopatológicas e/ou bioquímicas este padrão normal
de biodistribuição e eliminação são alterados. A biodistribuição ou
farmacocinética dos radiobiocomplexos pode ser alterada por uma variedade
de drogas administradas aos pacientes (28) e por procedimentos cirúrgicos (12,
29).
Com administração intravenosa, o Na99mTcO4é distribuído
no compartimento vascular, 70 a 80% dos íons pertecnetato se ligam
inicialmente às proteínas plasmáticas. A eliminação plasmática é muito rápida e
o equilíbrio entre o compartimento vascular e o fluido intersticial é completado
em um curto tempo, entre 2 a 3 minutos. A meia-vida de eliminação do plasma
é de aproximadamente 30 minutos (29). Íons pertecnetato livres difundem
através das membranas dos capilares para o líquido intersticial, de onde são
captados por diferentes órgãos como o estômago (30), intestino (31), glândulas
salivares (32), tireóide (33), plexo coróide e rins (29). A captação pela tireóide é
6
os íons pertecnetato são filtrados nos glomérulos, mas 86% são reabsorvidos
nos tubos proximais. Apenas 30% da dose injetada são excretados na urina em
24h. O íon pertecnetato é facilmente absorvido pelo sistema digestório após
administração oral ou após injeção intramuscular por processo de difusão
simples (8, 9).
O uso de drogas sintéticas e naturais é fundamental na
obtenção de um resultado terapêutico desejado no tratamento de doenças.
Neste caso existe a possibilidade de que uma droga possa alterar a
intensidade dos efeitos farmacológicos de outra droga administrada
concomitantemente. O resultado final pode ser o aumento ou diminuição dos
efeitos de uma droga ou ainda aparecimento de um novo efeito não observável
durante a administração dos fármacos isoladamente (27). O mecanismo
sinergístico, ou não, entre drogas pode alterar todo o comportamento
farmacocinético (absorção, metabolismo e excreção) e farmacodinâmicos
(afinidade pelo mesmo sítio de ligação) da droga, por meio de diversas
possibilidades que acabam por modificar a resposta farmacológica esperada
(12,27). Os mecanismos de ação envolvendo os produtos sintéticos têm sido
de modo geral, bem estabelecidos (27). Entretanto não é o que acontece com
muitos dos produtos naturais usados na clínica médica (34).
A interação medicamentosa com radiobiocomplexos pode
ser devido à possibilidade do medicamento: (i) modificar a natureza química do
radiobiocomplexo, (ii) alterar o meio bioquímico do alvo no qual o
radiobiocomplexo se concentra, (iii) alterar o meio bioquímico do não alvo para
o radiobiocomplexo, (iv) favorecer ou dificultar a ligação do radiobiocomplexo
7
ainda, exercer seu efeito terapêutico mimetizando sintomas de doenças (35).
Alterando a distribuição normal dos radiotraçadores, podem-se obter
diagnósticos imprecisos podendo haver a necessidade da repetição de
exames, expondo o paciente a doses de radiação desnecessárias (12).
A hortelã (Mentha crispa) é uma planta medicinal muito
utilizada por possuir propriedades carminática, eupéptica, estimulante,
colagoga, estomáquica, anti-séptica, antiemética, antiespasmódica e
analgésica (36). Como fitoterápico, é indicado para fadiga geral, para atonia
digestiva, cólicas, flatulência, vômitos durante a gravidez, intoxicações de
origem gastrintestinal, afecções hepáticas, palpitações, enxaquecas, tremores,
asma, bronquite crônica (favorece a expectoração), sinusite, dores dentárias
(bochechos) e nevralgias faciais provocadas pelo frio (36).
A erva de São João ou hipérico (Hypericum perforatum) tem
suas ações descritas como sedativa, diurética, útil para afecções nervosas com
depressão, hemorragias, diarréia e problemas urinários crônicos. De particular
interesse para cientistas é o uso potencial para diminuir a depressão com
poucos efeitos colaterais melhorando a terapia de drogas antidepressivas (37).
Extraída da erva de São João a hipericina é o principal composto responsável
pelo efeito antidepressivo (38).
Estudos com culturas bacterianas com diferentes
capacidades de reparo de lesões no DNA, revelaram que essas lesões
causadas pelo SnCl2 acarretavam um efeito letal que parece ser mediado pela
geração de radicais livres (3,9). Foi relatado que o efeito do SnCl2 também
dependeria da presença de mecanismo de restauração (4,7). O SnCl2 também
8
3 INDEXAÇÃO DE ARTIGOS
3.1 ARTIGO PUBLICADO
a- Efeito de um extrato de Hipérico (Hypericum perforatum) na marcação
in vitro de elementos sanguíneos com tecnécio-99m e na
biodisponibilidade do radiofármaco pertecnetato de sódio em ratos
Wistar, publicado em 2005, no periódico “Acta Cirúrgica Brasileira”, Qualis
Internacional C.
3.2 MANUSCRITOS NO PRELO
a- Aqueous extract of the medicinal plant Mentha crispa alters the
biodistribution of the radiopharmaceutical sodium pertechnetate in Wistar
rats. Aceito para publicação em 2007, no periódico “Medicinal Chemistry
Research”, Qualis Internacional C.
b- Influence of an aqueous extract of Hypericum perforatum (Hypericin)
on the survival of Escherichia coli AB1157 and on the electrophoretic
mobility of pBSK plasmid DNA.Aceito para publicação em 2007, no periódico
“Revista Brasileira de Farmacognosia”, Qualis Nacional A.
c- The male reproductive system and the effect of an extract of a
medicinal plant (Hypericum perforatum) on the labeling process of blood
constituents with technetium-99m. Aceito para publicação em 2007, no
periódico “Brazilian Archives of Biology and Technology”, Qualis Internacional
9
3.3 MANUSCRITOS SUBMETIDOS
a- Morphologic and morphometric in vitro evaluation of red blood cell
labeled with technetium-99m: effects of the Hypericum perforatum and
Mentha crispa extracts. Submetido ao periódico “Biological Research”, Qualis
10
3.1 ARTIGO PUBLICADO
Separata
Acta Cirúrgica Brasileira
v. 20, suplemento 1, pp. 76-80, 2005.
Efeito de um extrato de Hipérico (Hypericum perforatum) na marcação in
vitro de elementos sanguíneos com tecnécio-99m e na biodisponibilidade
do radiofármaco pertecnetato de sódio em ratos Wistar,
76- Acta Cirúrgica Brasileira - Vol 20 - Supl no 1 2005
Efeito de um extrato de Hipérico (Hypericum perforatum) na marcação
in vitro de elementos sangüíneos com tecnécio-99m e na biodisponibilidade
do radiofármaco pertecnetato de sódio em ratos Wistar
1Sebastião David Santos-Filho2, Mario Bernardo-Filho3
Santos-Filho SD, Bernardo-Filho M. Efeito de um extrato de Hipérico (Hypericum perforatum) na marcação in vitro de elementos sangüíneos com tecnécio-99m e na biodisponibilidade do radiofármaco pertecnetato de sódio em ratos Wistar. Acta Cir Bras [serial on line] Available from: URL: htt://www.scielo.br/acb.
RESUMO - Objetivo: Avaliar o efeito de um extrato de hipérico (Hypericum perforatum) na marcação de elementos sanguíneos com
tecnécio-99m (99mTc) e na biodisponibilidade do radiofármaco pertecnetato de sódio em ratos Wistar. Métodos: Sangue (heparinizado) de ratos Wistar é incubado com um extrato de hipérico, com cloreto estanoso e a seguir com Tc-99m, como pertecnetato de sódio (99mTcO
4
Na). Plasma (P) e células (CS) são isolados por centrifugação. Amostras de P e CS também são precipitadas com ácido tricloroacético 5%, e separadas as frações solúveis (FS-P e FS-CS) e insolúveis (FI-P e FI-CS). Para a análise da biodistribuição, 0,3 mL do radiofármaco 99mTcO
4
Na foi administrada em ratos Wistar que receberam por gavagem extrato ou salina (NaCl 0,9%) por 15 dias. Após 10 minutos os animais foram sacrificados e os órgãos isolados para contagem da atividade radioativa. Resultados: O extrato de hipérico reduziu de forma significativa (P<0,05) a %ATI ligada às células, à fração insolúvel celular e à fração insolúvel do plasma. A biodistribuição foi diminuída significativamente (P<0,01) no osso, no músculo e na tireóide. No pâncreas o percentual de radioatividade aumentou significativamente (P<0,05). Conclusão: No extrato vegetal estudado podem existir substâncias que oxidariam o íon estanoso, reduzindo a fixação do 99mTc às hemácias e proteínas plasmáticas e celulares. Da mesma forma poderiam produzir alterações metabólicas com conseqüente influência na captação do radiofármaco pertecnetato de sódio no osso, músculo, pâncreas e tireóide.
DESCRITORES: Hipérico. Tecnécio-99m. Biodisponibilidade. Cirurgia.
Introdução
1. Laboratório de Radiofarmácia Experimental, Departamento de Biofísica e Biometria, Instituto de Biologia Roberto Alcantara Gomes, Univer-sidade do Estado do Rio de Janeiro.
2. Doutorando do Programa de Pós-Graduação em Ciências da Saúde da Universidade Federal do Rio Grande do Norte.
3. Professor Titular, Laboratório de Radiofarmácia Experimental, Departamento de Biofísica e Biometria, Instituto de Biologia Roberto Alcantara Gomes, Universidade do Estado do Rio de Janeiro.
Hemácias podem ser marcadas com tecnécio-99m (99mTc) e empregadas em diagnóstico por imagem de sangramentos in-ternos, localização de hemangiomas e de obstruções no sistema circulatório que necessitariam de intervenção cirúrgica1,2,3. Es-sas hemácias marcadas também têm sido de importância em vários estudos clínicos e também experimentais de possível interesse para a pesquisa na medicina nuclear4-11. Essa marca-ção é baseada na capacidade de redumarca-ção do cloreto estanoso (SnCl
2
) que atua sobre o 99mTc, na forma de pertecnetato de sódio. Tem sido descrito que vários fatores interferem na mar-cação de hemácias e proteínas plasmáticas com 99mTc, e dentre eles estão os produtos naturais8,10,12,13.
O radiofármaco pertecnetato de sódio é distribuído através dos líquidos vasculares e intersticiais e apresenta normal-mente uma captação preferencial na tiróide, o estômago, trato intestinal, e glândulas salivares14. Vários fatores, como a tera-pia com drogas, a teratera-pia com radiação, processos cirúrgicos, condições de dieta, além de doenças podem afetar a biodistribuição dos diferentes radiofármacos9,16-19. Esses fa-tores levam a uma repetição do exame, resultando numa irradiação desnecessária ao paciente.
Plantas medicinais têm sido utilizadas largamente no mundo no tratamento de doenças, ou mesmo visando potencializar as ações terapêuticas, diminuindo doses e efeitos adversos. Muitos dos efeitos adversos e interações potenciais destas plantas são pouco estudados, assim como grande parte das aplicações médicas e populares é difícil de ser interpretada cientificamente19.
A erva de São João (hipérico; Hypericum perforatum) tem suas ações descritas como sedativa, adstringente e diurética, sendo também útil para afecções nervosas com depressão, hemorragias, diarréia e problemas urinários crônicos20. Tam-bém tem sido sugerida para tratar danos espinhais e é usada para contusões, feridas, tumores e ulcerações. Hypericum
perforatum parece ter uma significante atividade
antidepressiva tendo sido proposto ser o melhor indicador de estresse clínico do que estresse agudo, e pode indicar atividade adaptogênica21.
Acta Cirúrgica Brasileira - Vol 20 - Supl no 1 2005 - 77 Métodos
Sangue foi colhido de ratos Wistar (17 animais) machos, com peso de 336±11g, após injeção intraperitoneal com pentobarbital PA na dose de 50 mg/kg de peso. Amostras de 3 mL de sangue foram retiradas por punção cardíaca, em se-ringas com anticoagulante (0,2 mL de heparina). Após a coleta de sangue os ratos foram separados para serem novamente manipulados passados 15 a 20 dias. Isto é importante para prevenir infecções e reduzir o estresse e sofrimento dos ani-mais.
Para preparar o extrato, hipérico em pó (Herbarium, Brasil, lote 954661, validade: 08/2006, data de fabricação: 23/04/2002) foi misturado com salina (NaCl 0,9%) na concentração final de 50 mg/mL e homogeneizado em agitador tipo vortex por 30 segundos. Após filtração, essa solução do extrato foi deno-minada 100%, sendo diluído para as concentrações de: 6,25; 12,5; 25, 50 e 100% (estudos de marcação de constituintes sanguíneos) que foram usadas nos estudos in vitro e 100% no estudo in vivo (biodisponibilidade).
Os experimentos (total de 3) de marcação dos constituintes sanguíneos foram realizados em triplicata, havendo a neces-sidade de um total de 9mL de sangue que foram obtidos de um pool de sangue coletado de 3 animais. Amostras de 0,5 ml de sangue foram incubadas, a temperatura ambiente, com o extrato vegetal (100 ìL) em diferentes concentrações (6,25; 12,5; 25; 50 e 100%), por uma hora. Após, foi adicionado 0,5 mL de solução de cloreto estanoso (SnCl
2
; 1,2 mg/mL; Reagen S.A., Brasil) e realizou-se a incubação por mais uma hora. Após, foram adicionadas 0,1 mL de 99mTc (3,7 MBq) na for-ma de pertecnetato de sódio (99mTcO
4
Na), em todos os tubos, continuando a incubação por mais 10 minutos. As amostras foram centrifugadas (1500 rpm, 5 minutos) em centrífuga clí-nica Alpha ICA (Instrumentos Científicos Alpha Ltda.). Alíquotas de plasma (P) e células (C) foram então separadas e a porcentagem de atividades (% ATI) calculada. Para avaliar o efeito na ligação do Tc-99m às proteínas plasmáticas e celu-lares, alíquotas de P e C (20 mL) foram também precipitadas
em 1ml de ácido tricloroacético (TCA 5%), sendo então, centrifugadas e isoladas a fração solúvel (FS) e insolúvel (FI) de P e C. No controle foi adicionada solução salina no lugar do extrato vegetal. A porcentagem de radioatividade incorpo-rada aos elementos sanguíneos foi calculada.
Nos experimentos de biodisponibilidade (in vivo), um extrato de hipérico 100% (50mg/mL) foi administrado por gavagem em ratos Wistar (5 ratos), com intervalos de 24 horas, entre cada dose por 15 dias. Nos animais controle (3 ratos), foi administra-da salina. Uma hora após a última dose (15º. dia), 0,3ml do radiofármaco pertecnetato de sódio (7,4 MBq) é injetado atra-vés do plexo venoso orbital. Após 10 minutos os animais foram sacrificados e os órgãos isolados para contagem da atividade radioativa em cintilador sólido de NaI(Tl) (Automatic Gamma Counter, modelo C 5002, Packard, Canadá). A seguir foram cal-culadas: (i) as percentagens de radioatividade total (%ATI) nos órgãos e (ii) as percentagens de radioatividade por grama de tecido (%ATI/g) em cada órgão. As %ATI/g foram determi-nadas dividindo-se as percentagens de radioatividade por grama de tecido pela massa de cada órgão.
Os valores experimentais obtidos foram comparados com os resultados do grupo controle usando o teste ANOVA segui-do pelo teste de comparações múltiplas de Dunnett.
Resultados
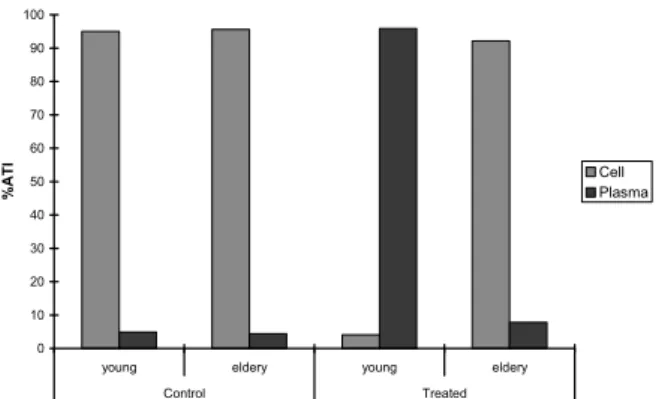
Na Figura 1 é mostrada a distribuição de radioatividade nos compartimentos celular (C) e plasmático (P) e nas frações insolúvel e solúvel celular e plasmática de amostras de san-gue tratadas com diferentes concentrações de extrato aquoso de hipérico (6,25, 12,5, 25, 50 e 100%). Os resultados mostram que o extrato de hipérico reduziu de forma significativa (P<0,05) a %ATI ligada às células de 95,03 ± 0,51 (controle) para 4,16 ± 0,92 (100% do extrato), à fração insolúvel celular de 87,46 ± 5,07 (controle) para 14,82 ± 0,61 (100% do extrato) e à fração insolúvel do plasma de 76,24 ± 6,15 (controle) para 26,67 ± 1,70 (100% do extrato).
FIGURA 1 – Distribuição de radioatividade nas frações sangüíneas de amostras de sangue tratadas
78- Acta Cirúrgica Brasileira - Vol 20 - Supl no 1 2005
Amostras de sangue foram obtidas de ratos Wistar através de punção cardíaca e incubadas in vitro durante uma hora com diferentes concentrações do extrato de hortelã (macerado - folhas e caule) (100; 50; 25; 12,5; 6,25 %). No controle foi utilizada solução salina 0,9%. A seguir foi adicionado cloreto estanoso e Tc-99m. Após centrifugação, amostras de célula (C) e Plasma (P) foram isoladas e também precipitadas com TCA 5 %. As amostras foram contadas em cintilador sólido e as %ATI calculadas.
FIGURA 2 – Distribuição da radioatividade do radiofármaco pertecnetato de sódio
Na Figura 2 são mostrados os percentuais de radioatividade por grama dos órgãos retirados de animais tratados com hipérico ou com solução salina (controle). Como pode ser observado alguns órgãos tiveram a biodistribuição diminuí-da significativamente (P<0,01): (a) no osso de 0,45 ± 0,01 para 0,16 ± 0,06; (b) no músculo de 0,18 ± 0,004 para 0,10 ± 0,02; (c) na tireóide de 6,09 ± 1,66 para 1,54 ± 1,07. No pâncreas o percentual de radioatividade aumentou significativamente (P<0,05) de 0,16 ± 0,04 para 0,24 ± 0,03.
Extrato de hipérico 100% (50mg/mL) foi administrado por gavagem em ratos Wistar (n=5), com intervalos de 24 horas, entre cada dose por 15 dias. Uma hora após a última dose (15º. dia), 0,3ml do radiofármaco (7,4 MBq) foi injetado atra-vés do plexo venoso orbital. Após 30 minutos os animais foram sacrificados, a contagem da atividade radioativa em cada órgão isolado obtida e foram calculadas as percenta-gens de radioatividade (%ATI) nos órgãos.
Discussão
A marcação de constituintes sanguíneos com 99mTc tem muitas aplicações. Tem sido descrito que extratos obtidos de plantas medicinais podem alterar a marcação de elementos sanguíneos com 99mTc e também a morfologia dos eritrócitos6,7,10,13.
A distribuição, a fixação e a eliminação de radiofármacos em um organismo dependem de vários fatores, tais como o fluxo sanguíneo, o metabolismo tecidual e a ligação aos elementos
sanguíneos4,15. Vários autores têm demonstrado que a biodisponibilidade de radiofármacos pode ser modificado por produtos naturais e sintéticos6-13,22.
Nos resultados apresentados na figura 1, o extrato de hipérico foi capaz de diminuir a marcação de constituintes celulares com 99mTc e nesse processo de marcação tanto os íons estanoso e pertecnetato parecem atravessar a membrana eritrocitária23. Seria altamente sugestivo que os produtos exis-tentes no extrato de hipérico poderiam comprometer o trânsito desses íons através da membrana através de proposta apre-sentada por Krishtal em outro tipo celular24. Esses autores descreveram que a hiperforina e outros constituintes do hipérico têm a capacidade de modular canais iônicos da mem-brana celular. Em relação aos canais de cálcio esse efeito seria devido a interação com a calmodulina ou através das vias de ativação da calmodulina. à ação da hiperforina.s e plasmáticos do sangue.
O extrato de hipérico usado (ver figura 2) diminuiu a captação do 99mTcO
4
Acta Cirúrgica Brasileira - Vol 20 - Supl no 1 2005 - 79
resultados poderiam, em parte, serem atribuídos à capacida-de capacida-de interação dos produtos presentes no hipérico à membranas lipídicas como descrito por Neagoe25. Esses au-tores têm demonstrado que os componentes de um extrato etanólico de hipérico seriam capaz de interagir com membra-nas lipídicas acarretando alterações na absorção e biodisponibilidade, assim como efeitos farmacodinâmicos na excitabilidade neuronal.
Na técnica de marcação dos constituintes sanguíneos com 99mTc é necessário um agente redutor. Uma vez que ocor-reu redução da marcação dos constituintes sanguíneos com 99mTc, poderia ser especulado que os produtos exis-tentes no extrato de hipérico estariam oxidando o íon estanoso impedindo sua ação. Os compostos químicos presentes nesse extrato também poderiam atuar com agen-tes quelanagen-tes levando à formação de complexos com o 99mTcO
4
Na e SnCl
2
, sendo que esse fato também poderia justificar a diminuição na fixação de radioatividade nos elementos sanguíneos. Possíveis alterações morfológicas promovidas pelo extrato do hipérico, à semelhança às ob-servadas nos estudos com a hortelã13 poderiam também justificar a não captação pelas células vermelhas do san-gue.
A evidência que um extrato de hipérico pode alterar a marca-ção de células vermelhas do sangue, assim como a biodisponibilidade de radiofármaco pode ser de grande rele-vância no momento da interpretação de imagens cintilográficas. Por outro lado, deve-se considerar que os achados experimentais obtidos nesse trabalho foram em con-dições experimentais controladas e realizadas com ratos.
Conclusão
De acordo com os resultados obtidos nesse estudo pode-se especular que o extrato de hipérico seria capaz de alterar in
vitro a marcação de elementos sanguíneos com 99mTc, assim
como também a biodistribuição do radiofármaco 99mTcO
4
Na. A ação biológica desse extrato poderia estar relacionada a (i) propriedades redox do extrato, (ii) efeitos quelantes, (iii) alte-rações na morfologia das hemácias, (iii) modificação no transporte de íons através da membrana eritrocitária, (iv) metabolização no organismo e (v) atuação em órgãos especí-ficos. Embora os resultados tenham sido obtidos com animais, sugere-se precaução com os exames em medicina nuclear em pacientes que utilizem Hypericum perforatum como medica-mento.
Referências
1- Shih WJ, Bognar B. Early appearance of the inferior vena cava in a Tc-99m red blood cell first-pass study: a sign of superior vena cava obstruction. Clin Nucl Méd 2000; 25:679-81.
2- Milhara Y, Kubota K, Nagata N, Takagi K, Morie T, Oda N, Ogura R, Watanabe Y, Terano A, Honma K. Total intraoperative
enteroscopy using a colonoscope for detecting the bleeding point. Hepatogastroenterology, 2004; 51:1401-3.
3- Tsai CC, Yen TC, Tzen KY. The value of Tc-99m red blood cell SPECT in differentiating giant cavernous hemangioma of the liver from other liver solid masses. Clin Nucl Med 2002; 27: 578-81.
4- Sampson CB. Complications and difficulties in radiolabelling blood cells: a review. Nucl Med Commun, 1996; 17:648-58.
5- Reineger IW, Oliveira JF, Caldeira-De-Araújo A, Bernardo-Filho M. Effect of Peumus boldus on the labeling of red blood cells and plasma proteins with technetium-99m. Appl Radiat Isot, 1999; 51:145-9.
6- Oliveira JF, Braga ACS, Ávila ASR, Araújo AC, Cardoso VN, Bezerra RJAC, Bernardo-Filho M. Assessment of the effect of Maytenus ilicifolia (espinheira santa) extract on the labeling of red blood cells and plasma proteins with technetium-99m. J Ethnopharmacol 2000; 72:179-84.
7- Oliveira JF, Avila AS, Braga ACS, Oliveira MBN, Boasquevisque EM, Jales RL, Cardoso VN, Bernardo-Filho M. Effect of extract of medicinal plants on the labeling of blood elements with techentium-99m and on the morphology of red bool cells: I – a study with Paullinia cupana. Fitoterapia 2002; 73:305-12.
8- Oliveira JF, Santos-Filho SD, Catanho MTJ, Srivastava SC, Lima-Filho GL Bernardo-Lima-Filho M. Effect of extract of medicinal plant on the labeling of blood elements with technetium-99m and on the morphology of red blood cells (RBC): Toxicological action of roast coffee beans (Coffea arabica). Indian J Nucl Med 2003; 18:52-6.
9- Diré G, Lima E, Mattos D, Oliveira MB, Pereira MJ, Moreno S, Freitas R, Gomes ML, Bernardo-Filho M. Effect of chayotte (Sechium edule) extract on the biodistribution of technetium-99m and on the morphometry of red blood cells. J Labelled Comp Radiopharm 2001; 44:648-50.
10- Lima EA, Dire G, Mattos DM, Freitas RS, Gomes ML, Olivei-ra MB, Faria MV, Jales RL, Bernardo-Filho M. Effect of an extOlivei-ract of cauliflower (leaf) on the labeling of blood elements with technetium-99m and on the survival of Escherichia coli AB1157 submitted to the treatment with stannous chloride. Food Chem Toxicol 2002; 40: 9149-53.
11- Moreno SRF, Diré G, Freitas RS, Farah MB, Lima-Filho GL, Rocha EK, Jales RLC Bernardo-Filho M. Effect of Ginkgo biloba on the labeling of blood elements with technetium-99m: in vitro study. Rev Bras Farmacogn 2002; 12:62-3.
12- Moreno S, Rocha EK, Pereira M, Mandarim-Lacerda C, Freitas RS, Nascimento ALR, Carvalho JJ, Lima-Filho GL, Diré G, Lima EAC, Bernardo-Filho M. Ginkgo Biloba: Experimental model to evaluate it’s action on the labeling of blood elements with technetium-99m and on the morphometry of red blood cells. Pakistan J Nut 2004; 3:68-71.
13- Santos-Filho SD, Diré GL, Lima E, Oliveira MN, Bernardo-Filho M. Effect of Mentha crispa (mint) extract on the labeling of blood elements with technetium-99m: A possible evaluation of free radicals. J Biol Sci 2004; 4: 266-70.
80- Acta Cirúrgica Brasileira - Vol 20 - Supl no 1 2005
15- Hladik III WB, Saha GB, Study KT. Essentials of Nuclear Medicine Science. Baltimore-London; Willians & Wilkings, 1987.
16- Britto DMM, Gomes ML, Rodrigues PC, Paula EF, Gutfilen B, Bernardo-Filho M. Effect of a chemotherapeutic drug on the biodistribution of 99mTc-DTPA in Balb/c mice. J Exp Clin Cancer Res 1998; 17:313-6.
17- Spicer JA, Hladick WB, Mulberry WE. The effects of selected antineoplastic agents on the labeling of erythrocytes with technetium-99m using the Ultra Tag RBC kit. J Nucl Med Technol 1999; 27:132-5.
18- Mattos DMM, Gomes ML, Freitas RS, Rodrigues PC, Nasci-mento VD, Boasquevisque EM, Paula EF, Bernardo-Filho M. Assessment of the vincristine on the biodistribution of 99mTc-labelled glucoheptonic acid in female Balb/c mice. Nucl Med Commun 2000; 21:117-21.
19- Gomes ML, Oliveira MBN, Bernardo-Filho M. Drug Interaction with radiopharmaceuticals: Effect on the labeling of red blood cells with technetium-99m and on the bioavailability of radiopharmaceuticals. Braz Arch Biol Technol 2002; 45:143-9.
20- Ferreira SH, Barata LES, Salles SLM, Queiróz SRR, Neto NEH, Corazza R, Farias, RC Medicamentos a partir de plantas medici-nais no Brasil. Rio de Janeiro: Academia Brasileira de Ciências, 1998.
21- Kumar V, Singh PN, Bhattacharya SK. Anti-stress activity of Indian Hypericum perforatum. Indian J Exp Biol 2001; 39:344-9.
22- Hesslewood S, Leung E. Drug interaction with radiopharmaceuticals. Eur J Nucl Med 1994; 21:348-56.
23- Gutfilen B, Boasquevisque EM, Bernardo-Filho M. Calcium channel blockers: interference on red blood cells and plasma proteins labeling with Tc-99m. Rev Esp Med Nucl 1992; 11:195-9.
24- Krishtal O, Lozovaya N, Fisunov A, Tsintsadze T, Pankratov Y, Kopanitsa M, Chatterjee SS. Modulation of ion channels in rat neurons by the constituents of Hypericum perforatum. Pharmacopsychiatry 2001;34:S74-82.
25- Neagoe I, Macri BM, Flonta ML. Hyperici herba extract interaction with artificial lipid bilayers. J Pharm Pharmacol 2004; 56:1283-9.
Santos-Filho SD, Bernardo-Filho M. Effect of Hypericum perforatum extract on in vitro labelling of blood elements with technetium-99m and on biodisponibility of sodium pertecnetate in Wistar rats. Acta Cir Bras [serial on line] Available from: URL: htt://www.scielo.br/acb.
ABSTRACT – Purpose: To evaluate the effect of a hiperico extract (Hypericum perforatum) on the labeling of blood elements with
technetium-99m (99mTc) and in the bioavailability of the radiopharmaceutical sodium pertechnetate in Wistar rats. Methods: Blood (heparinized) withdrawn from Wistar rats is incubated with a hiperico extract, with a stannous cloride and with 99mTc, as sodium pertechnetate (99mTcO
4
Na). Plasma (P) and cells (C) are isolated by centrifugation. Samples of P and C are also precipitated with trichloroacetic acid (TCA 5%) and soluble (FS-P; FS-C) and isoluble (FI-P; FI-C) fractions are separated. In the bioavailability analysis, the extract or NaCl 0.9% solution is administrated into Wistar rats (gavage) during 15 days. Sodium pertechnetate was administered and after 10 min, the animals are sacrificed, the organs were isolated, the radioactivity determined in a well counter, and the percentages of radioactivity per gram (%ATI/g) in the organs are calculated. Results: The hiperico extract decreased significantly (P<0.05) the %ATI in the cells, cellular insoluble fraction and plasma insoluble fraction. The biodistribution was significantly (P<0.01) decreased in bone, muscle and thyroid and significantly (P<0.05) increased in pancreas. Conclusion: The analysis of the results indicates that in studied extract should have substances that should oxidize the stannous ion, reducing the fixation of the 99mTc on the erythrocytes and plasma and cellular proteins. Moreover, it could produce metabolic alterations with influence in the uptake of the radiopharmaceutical 99mTcO4Na in bone, muscle, pancreas and thyroid.
KEYWORDS: Hiperico. Technetium-99m. Bioavailability. Surgery.
Correspondência:
Sebastião David Santos-Filho
Universidade do Estado do Rio de Janeiro Instituto de Biologia Roberto Alcantara Gomes Departamento de Biofísica e Biometria
Laboratório de Radiofarmácia Experimental Av. 28 de Setembro, 87
20551-030. Rio de Janeiro – RJ Tel.: 021-2587-6432
sdsfilho@terra.com.br Conflito de interesse: nenhum
11
3.2 MANUSCRITO NO PRELO
a-Medicinal Chemistry Research, Qualis Internacional C.
Aqueous extract of the medicinal plant Mentha crispa alters the biodistribution of
the radiopharmaceutical sodium pertechnetate in Wistar rats.
Sebastião David Santos-Filho1, 2, 3, Adalgisa Ieda Maiworm1, 3, Giuseppe Antonio Presta1,3, Severo de Paoli1,3, Tânia Santos Giani1,3, Mario Bernardo-Filho1,4.
1Departamento de Biofísica e Biometria, Instituto de Biologia Roberto Alcantara Gomes,
Universidade do Estado do Rio de Janeiro, 20551030, Rio de Janeiro, RJ, Brasil
2Ciências Biomédicas, Centro Universitário de Volta Redonda, 27251970, Volta
Redonda, RJ, Brasil
3Programa de Pós-Graduação em Ciências da Saúde, Universidade Federal do Rio
Grande do Norte, 59010180, Natal, RN, Brasil
4Coordenadoria de Pesquisa, Instituto Nacional do Câncer, 20230130, Rio de Janeiro,
RJ, Brasil.
Corresponding author:
Sebastião David Santos-Filho
Universidade do Estado do Rio de Janeiro
Instituto de Biologia Roberto Alcantara Gomes
Departamento de Biofísica e Biometria
Laboratório de Radiofarmácia Experimental
Av 28 de setembro, 87, 20551030
Vila Isabel, Rio de Janeiro, RJ, Brazil.
Phone/Fax: 55-021-21-2587-6432
12
Running Title: Mint and radiopharmaceutical biodistribution
Financial support: CAPES, CNPq and UERJ
Abstract
Mentha crispa extract or NaCl 0.9% were daily (15 days) administered by gavage into Wistar rats. After that, animals have received by ocular plexus via, the Na99mTcO4 and
they were sacrificed. Organs were isolated, the radioactivity determined, the
percentages of radioactivity in each organs calculated and statistical analysis
performed. Significant (p=0.0061) increase of the radioactivity was observed in kidney,
spleen, and thyroid, that could be justified by effects of the extract and/or by generation
of active metabolites.
Key-words:Mentha crispa, biodistribution, sodium pertechnetate, radiobiocomplex.
Introduction:
The relevance of the techniques used in the nuclear medicine is mainly related
with their ability to provide suitable information on physiology rather than on anatomy1. Several radiopharmaceutical or radiobiocomplex2 have been used to obtain single photon emission computed tomography (SPECT) and positron emission tomography
(PET) images3,4.
Sodium pertechnetate (Na99mTcO4) is a radiobiocomplex that has a long and
successful history of use in several clinical applications involving SPECT, such as, (i)
labeling of various 99mTc-radiobiocomplexes, (ii) imaging of the thyroid, (iii) imaging of the gastric mucosa to diagnose Meckel´s diverticulum, (iv) labeling (in vivo) of red blood
cells for blood pool imaging and first-pass cardiac angiography, (v) evaluating of the
nasolacrimal drainage, (vi) studying of the parathyroid adenoma in conjunction with
13
gland and (ix) imaging of the brain to investigate possible damage to the blood-brain
barrier4-7.
Some physiological and/or pharmacological properties related with the
radiobiocomplex Na99mTcO4have been reported. After intravenous injection, it is weakly
bound to serum proteins (70-80%). Unbound pertechnetate ion (99mTcO4-) diffuses
slowly through the capillary membranes to the interstitial fluids, from where it is cleared
by various organs such as stomach wall, intestines, salivary glands, thyroid, choroid
plexus, sweat glands, kidneys and mucous membrane. The thyroid uptake of 99mTcO4
-is by active transport, as a sodium-iodide symporter, and its uptake -is 2-4%. In the
kidneys, 99mTcO4- is filtered in the glomeruli, but 86% are reabsorved in the proximal
tubes. Only 30% of the injected dose is excreted in urine in 24 h. Lactating women
secrete 10% of 99mTcO4- in milk. 99mTcO4- is easily absorbed by the digestive system
after oral administration or after intramuscular injection by simple diffusion1,6,8.
Many factors, as drug therapy, radiation therapy, dietary conditions, besides
pathological process could affect the biodistribution of the different
radiobiocomplexes2,9-14 or the labeling of blood constituents15-18. These factors may lead to (i) a poor visualization of the organs and to induce inadequate interpretation of the
examination and misdiagnosis or (ii) the repetition of the examination procedure
resulting in unnecessary irradiation to the patient and the staff1,2,19.
It is well established that medicinal plants contain mixtures of various
pharmacologically active compounds, and thus they may have the potentiality to
14
Mentha crispa (mint; M.crispa) is utilized in herbal medicine due to various pharmacological actions. Mint is part of a genus of the Labiatae family, which
comprises a wide number of species, varieties and hybrids. Mint flowers and leaves are
used for tea infusions, which have digestive, calming, antiseptic and anti-asthmatic
properties30. The extract and leaves of the Mentha species are described as biological additives31. Rosmarinic acid, a natural phenolic compound contained in many Lamiaceae herbs such as mint, inhibits complement-dependent inflammatory processes
and may have therapeutic potential32. Mint was also capable of iron(III) reduction, 1,1-diphenyl-2-picrylhydrazyl radical scavenging, and to inhibit iron(III)-ascorbate-catalyzed
hydroxyl radical-mediated brain phospholipid peroxidation33. Santos-Filho28 have described that an extract of mint was capable to interfere on the labeling of blood cells
with the Tc-99m, as well as, the fixation of this radionuclide on the plasma and blood
cells proteins. The main pharmacodynamic effect of mint oil is a dose-related
antispasmodic effect on the smooth musculature due to the interference of menthol with
the movement of calcium across the cell membrane, relevant to the gastrointestinal
tract34.
As the extract of mint is commonly used in the world, the aim of this work
was to evaluate the effects of a mint extract on the biodistribution of the
radiobiocomplex sodium pertechnetate in Wistar rats.
Materials and methods:
All the experimental procedures have followed the Ethical Guidelines of the
Instituto de Biologia Roberto Alcantara Gomes, Universidade do Estado do Rio de
15
The experiments were performed without sacrificing the animals. The animals
were maintained under controlled conditions (22±5°C, 12h of light/dark cycle). Food and
water were availablead libitum.
Wistar rats (male, 3 months, 11 animals, 293±13g) were separated in 2 groups: mint group (n=5) and control group (n=6).
The mint group was treated with an extract of mint prepared with 4g of crushed
leaves of Mentha crispa (Mãe Terra Produtos Naturais – http://www.maeterra.com.br -,
Brazil, lot 05FEV2002) in 100mL of 0.9% NaCl solution (saline). The preparation was
centrifuged (clinical centrifuge, 3000 rpm, 10 min), filtered through paper (quality filter
paper) and the filtered solution was considered to be 40mg/mL. The control group
received only saline.
The extracts and saline were daily administered by intragastric via during 15 days
with 24 hours intervals. After that, the animals received by ocular plexus via 0.3mL of
the Na99mTcO4 (3.7MBq) and were rapidly sacrificed after 10 min following the criteria of
the Ethical Committee of the Institution.
The organs (pancreas, testis, stomach, kidney, spleen, duodenum, heart, lung,
liver, thyroid, bone, muscle and brain) were isolated and the mass of each organ was
determined in an analytical balance. The radioactivity in each organ was determined in
a well counter (mod C5002, Packard, USA).
The activity in each organ was divided by the total activity administered to
determine the percentage of radioactivity (%ATI) in each organ. The %ATI was divided
by the mass of each tissue to determine the percentage of radioactivity per gram
16
Statistical analysis was performed by Wilcoxon test. P< 0.05 was considered
significant. All data are expressed as mean r standard deviation (SD).
Results:
The results of the biodistribution of the radiobiocomplex sodium pertechnetate in
different organs isolated from male rats are shown in the Table 1. The comparison of
the %ATI/g of these tissues isolated from the control group and from the mint group has
revealed that the mint extract increased the fixation of this radiobiocomplex in the
pancreas, kidney, spleen, liver and thyroid (P = 0.0061). The results also show that the
mint extract did not modify the fixation of the radiobiocomplex sodium pertechnetate in
other organs.
Discussion:
In nuclear medicine the clinical procedures to obtain image, normally, are
associated with a low radiation dose level to the patient and to the staff when compared
with other similar procedures using X rays. Moreover, the environmental impact is
negligible due to the half-life and the energy of the radiation emitted in the decay of the
main radionuclides used in the nuclear medicine procedures. In addition, the high
quality of the scintigraphic images in the SPECT and in the positron emission
tomography (PET) has helped in a rapid and efficient elucidation of the diagnosis of
various diseases35-38.
The radiobiocomplexes can be utilized to study the blood flow, the metabolism,
the morphology of an organ3,36, and to evaluate the drug formulation and drug delivery systems37.
Unexpected patterns of the biodistribution of a radiobiocomplex have normally
17
some authors have reported that many factors, besides the disease, can interfere in the
bioavailibility of a radiobiocomplex. When these factors are unknown, it is undesirable
and the consequences are (i) the possibility of misdiagnosis (misleading information that
can either mask or mimic certain disease symptoms) and/or (ii) the repetition of the
examination with an increase of radiation dose to the patient and staff1,39.
The drug therapy, radiation therapy besides and surgical interventions could also
affect the biodistribution of the radiobiocomplexes1,12,40. The drug interaction with radiobiocomplexes has been studied and it can be know or unknown6. Passos41 and Passos42 have also demonstrated that the dietary conditions can also interfere with the biodistribution of radiobiocomplex. Several authors have also reported that some
chemical compounds due to their pharmacological properties can alter the
biodistribution of various radiobiocomplexes9,11,12,29,34,40,46,47,48,49.
Some authors have described that synthetic or natural products in the blood, as
well as, the labeling conditions can have an effect on the labeling of red blood cells with
technetium-99m (99mTc)11,25-28,43-45.
The mint extract (Table 1) increased the fixation of the studied radiobiocomplex
in the pancreas, kidney, spleen, liver and thyroid, and did not modify the fixation in the
other organs. Szentmihalyi and collaborators50 have reported that some components of the mint extracts could interfere with the movement of calcium ions across the cell
membrane51. It is possible to speculate that, as the radiobiocomplex studied is an ion, the effect of the components of the mint extract would act also in the transport6,8 of the pertechnetate ion through the cellular membrane of determined organs. Moreover, the
extract of mint seems to produce damage on the red blood cell membrane with
18
modifications in determined organs and could interfere in the uptake of ions, as the
pertechnetate.
In conclusion, these results can be justified by the presence of determined
chemical compounds in the extract and/or by the generation of active metabolites
capable to interfere with the biodistribution of the studied radiobiocomplex. As the use of
extracts is increasing in the world, the knowledge about the drugs and the other factors
capable to interfere on the biodistribution of the radiobiocomplexes is highly worthwhile
to permit secure diagnosis of diseases. In addition, the development of biological
models to study this phenomenon is relevant and desired. Although results described in
this work have been obtained with rats, it is suggested to consider the possibility of an
unexpected effect of the mint in the uptake of the radiobiocomplex sodium
pertechnetate in several organs in the examinations in nuclear medicine.
References:
1. Hladik III, W.B.; Saha, G.B.; Study, K.T. Essentials of Nuclear Medicine Science.
William and Wilkins, London, 1987.
2. Bernardo-Filho, M.; Santos-Filho, S.D.; Moura, E.G.; Maiworm, A.I.; Orlando, M.M.C.;
Penas, M.E.; Cardoso, V.N.; Bernardo, L.C.; Brito, L.C. Drug Interaction with
Radiopharmaceuticals: a Review. Braz. Arch. Biol. Technol.2005,48, 13-28.
3. Chandra R. Nuclear Medicine Physics the Basics, 5th ed. Williams & Wilkins: New
York, 1998.
4. Harbert, J.C.; Eckelman, W.C.; Neumann, R.D. Nuclear Medicine Diagnosis and
19
5. Malpica, O.; Eblen-Zajjur, A. Autoradiography of experimental blood brain barrier
breakdown areas in the rat using pertechnetate as radiotracer. Rev Neurol. 2001, 33,
7-16.
6. Owunwanne, A.; Patel, M.; Sadek, S. Preparation of radiopharmaceuticals. The
handbook of radiopharmaceuticals. Chapman & Hall: London, 1995.
7. Staudenherz, A.; Fazeny, B.; Marosi, C.; Nasel, C.; Hoffmann, M.; Puig, S.; Killer, M.;
Leitha, T. Does (99m)Tc-Sestamibi in high-grade malignant brain tumors reflect
blood-brain barrier damage only? Neuroimage, 2000,12, 109-111.
8. Zuckier, L.S.; Dohan, O.; Li, Y.; Chang, C.J.; Carrasco, N.; Dadachova, E. Kinetics of
perrhenate uptake and comparative biodistribution of perrhenate, pertechnetate, and
iodide by NaI symporter-expressing tissues in vivo. J. Nucl. Med.2004,45, 500-507.
9. Brito, D.M.M.; Gomes, M.L.; Rodrigues, P.C.; Paula, E.F.; Gutfilen, B.;
Bernardo-Filho, M. Effect of the chemotherapeutic drugs on the biodistribution of 99mTc-DTPA in Balb/c mice. J. Exp. Clin. Cancer Res.1998,17, 313-316.
10. Capriles, P.V.; Dias, A.P.; Costa, T.E.; Oliveira, M.B.; Faria, M.V.; Moura, E.G.;
Abreu B.A.; Bernardo-Filho, M. Effect of eggplant (Solanum melongena) extract on the
in vitro labeling of blood elements with technetium-99m and on the biodistribution of
sodium pertechnetate in rats. Cell Mol Biol. 2000,48, 771-776.
11. Diré, G.; Lima, E; Gomes, M; Bernardo-Filho, M. The effect of a chayotte (Sechium
edule) extracts (decoct and macerated) on the labeling of blood elements with Technetium-99m and on the biodistribution of the radiopharmaceutical sodium
pertechnetate in mice: an in vitro and in vivo analysis. Pakistan J Nutr. 2003, 2,
20
12. Gomes, M. L.; Braga, A. C.; Mattos, D. M.; Freitas, R. S.; Paula, E. F.; Bezerra, R.
J. A. C.; Bernardo-Filho, M. Effect of the mitomycin-C on the biodistribution of the
radiopharmaceutical 99mTechnetium-phytic acid in mice: a model to evaluate the toxic
effect of a chemical drug. J. Appl. Toxicol.2002,22, 85-87.
13. Mattos, D.M.M.; Gomes, M.L.; Freitas, R.S.; Rodrigues, P.C.; Nascimento, V.D.;
Boasquevisque, E.M.; Paula, E.F.; Bernardo-Filho, M. Assessment of the vincristine on
the biodistribution of 99mTc-labelled glucoheptonic acid in female Balb/c mice. Nucl.
Med. Commun.2000,21, 117-121.
14. Valença, S.S.; Lima, E.A.; Dire, G.F.; Bernardo-Filho, M.; Porto, L.C. Sodium
pertechnetate (Na99mTcO4) biodistribution in mice exposed to cigarette smoke. BMC
Nucl. Med.2005,5, 1.
15. Fonseca, A.S.; Frydman, J.N.; Santos, R.; Bernardo-Filho, M. Influence of
antipyretic drugs on the labeling of blood elements with technetium-99m. Acta Biol.
Hung.2005,56, 275-282
16. Holanda, C.M.C.X.; Leite, R.C.H.; Catanho, M.T.J.; Souza, G.M.; Bernardo-Filho, M.
The effect of glucantime™ on the labeling of blood constituents with technetium-99m.
Acta Cir. Bras.2005,20, 81-85.
17. Lima-Filho, G.L.; Lima, G.M.; Freitas, R.S.; Aleixo, L.C.; Moreno, S.R.; Catanho,
M.T.; Bernardo-Filho, M. Evaluation of the phytic acid effect on the labeling of blood
elements with technetium-99m and on the survival of a strain of Escherichia coli treated
with stannous fluoride. Mol Cell Biochem.2003, 247, 121-126.
18. Nigri, F.; Oliveira, .M.B.; Bernardo-Filho, M. Assessment of the effect of antiseizure
drugs on the labeling process of red blood cells and plasma proteins with
21
19. Hart, D.; Wall, B.F. UK nuclear medicine survey 2003-2004. Nucl Med Commun.
2005,26, 937-946.
20. Amorim, L.F.; Catanho, M.T.; Terra, D.A.; Brandão, K.C.; Holanda, C.M.;
Jales-Junior, L.H.; Brito, L.M.; Gomes, M.L.; De Melo, V.G.; Bernardo-Filho, M.; Cavalcanti
Jales, R.L. Assessment of the effect of Punica granatum (pomegranata) on the
biodistribution of the radiopharmaceutical sodium pertechnetate (99mTc) in Wistar rats.
Cell Mol Biol.2003,49, 501-507.
21. Diré, G.; Gomes, M.L.; Lima, E.A.C.; Jales, R.L.; Faria, M.C.; Bernardo-Filho, M.
Assessment of a fruit extract (Sechium edule) on the labeling of blood elements with
technetium-99m.Afr. J. Biotechnol.2004, 3, 484-488.
22. Lima, E.A.C.; Diré, G.; Mattos, D.M.M.; Freiras, R.S.; Gomes, M.L.; Oliveira, M.B.N.;
Faria, M.V.C.; Jales, R.L.; Bernardo-Filho, M. Effect of an extract of cauliflower (leaf) on
the labeling of blood elements with technetium-99m and on the survival of Escherichia
coli AB1157 submitted to the treatment with stannous chloride. Food Chem Toxicol. 2002,40, 919-923.
23. Moreno, S.R.F.; Diré, G.; Freitas, R.S.; Farah, M.B.; Lima-Filho, G.L.; Rocha, E.K.;
Jales, R.L.C.; Bernardo-Filho, M. Effect of Ginkgo biloba on the labeling of blood
elements with technetium-99m: in vitro study. Rev. Bras. Farmacogn.2002,12, 62-63.
24. Moreno, S.R.F.; Carvalho, J.J.; Nascimento, A.L.; Pereira, M.; Rocha, E.K.; Diré, G.;
Arnobio, A.; Caldas, L.Q.A.; Bernardo-Filho, M. (2005). Biodistribution of the sodium
pertechnetate and morphometry of organs isolated from Wistar rats: study of possible
pharmacokinetic interactions of a Ginkgo biloba extract.Braz. Arch. Biol. Technol.2005,
22
25. Oliveira, J. F.; Avila, A. S.; Braga, A. C. S.; Oliveira, M. B. N.; Boasquevisque, E. M.;
Jales, R. L.; Cardoso, V. N.; Bernardo-Filho, M. Effect of extract of medicinal plants on
the labeling of blood elements with technetium-99m and on the morphology of red blood
cells: I – a study with Paullinia cupana. Fitoterapia 2002, 73, 305-312.
26. Oliveira, J.F.; Oliveira, M.B.; Ávila, A.S.; Braga, A.C.S.; Catanho, M.T.J.A.; Jales,
R.L.C.; Cardoso, V.N.; Bernardo-Filho, M. Assessment of the effects of Fucus
Vesiculosos extract on the labeling of blood constituents with technetium-99m and the histological modifications on the shape of the red blood cells. Food Chem toxicol2003,
41, 15-20.
27. Santos-Filho, S.D.; Ribeiro, C.K.; Diré, G.F.; Lima, E.; Pereira, M.; Bernardo-Filho,
M. Morphological alterations on red blood cells labeled with technetium-99m: the effect
of Mentha crispa (hortelã) and Piper mthysticum (Kava Kava) extracts. Technetium,
Rhenium and Other Metals in Chemistry and Nuclear Medicine. SGEditoriali, Padova,
6:503-505, 2002.
28. Santos-Filho, S.D.; Diré, G.L.; Lima, E.; Oliveira, M.N.; Bernardo-Filho M. Effect of
Mentha crispa (mint) extract on the labeling of blood elements with technetium-99m: A possible evaluation of free radicals. J. Biol. Sci.,2004, 4, 266-270.
29. Diré, G.; Lima, E.; Mattos, D.; Oliveira, M.B.; Pereira, M.J.; Moreno, S.; Freitas, R.;
Gomes, M.L.; Bernardo-Filho, M. Effect of chayotte (Sechium edule) extract on the
biodistribution of technetium-99m and on the morphometry of red blood cells. J Labelled
Comp Radiopharm.2001, 44, 648-650.
30. Park, K.J.; Vohnikova, Z.; Brod, F.P.R. Evaluation of drying parameters and
desorption Isotherms of garden mint leaves (Mentha crispa L.). J. Food. Eng. 2002,51,
23
31. Davis, E.M.; Ringer, K.L; McConkey, M.E.; Croteau, R. Monoterpene metabolism.
Cloning, expression, and characterization of menthone reductases from peppermint.
Plant Physiol.2005,137, 873-881.
32. Renzulli, C; Galvano, F; Pierdomenico, L; Speroni, E; Guerra, M.C. Effects of
rosmarinic acid against aflatoxin B1 and ochratoxin-A-induced cell damage in a human
hepatoma cell line (Hep G2). J. Appl. Toxicol. 2004, 24, 289-296.
33. Dorman, H.J.; Kosar, M.; Kahlos, K.; Holm, Y.; Hiltunen, R. Antioxidant properties
and composition of aqueous extracts from Mentha species, hybrids, varieties, and
cultivars.J Agric Food Chem.2003,51, 4563-4569
34. Grigoleit, H.G.; Grigoleit, P. Pharmacology and preclinical pharmacokinetics of
peppermint oil. Phytomedicine.2005,12, 612-616.
35. Bacher, K.; Thierens, H.M. Accurate dosimetry: an essential step towards good
clinical practice in nuclear medicine. Nucl Med Commun.2005,26, 581-586.
36. Carlsson, S. A glance at the history of nuclear medicine. Acta. Oncol. 1995, 34,
1095-1102.
37. Perkins, A.; Frier, M. Nuclear Medicine in Pharmaceutical Research. Taylor &
Francis, London, 1999.
38. Saha, G.B. Fundamentals in Nuclear Pharmacy. Springer-Verlag, New York, 2004.
39. Sampson, C.B. Textbook of radiopharmacy theory and practice. Gordon and
Breach , Amsterdam, 1999.
40. Hesslewood, S.; Leung, E. Drug interactions with radiopharmaceuticals. Eur. J.
24
41. Passos, M.CF.; Ramos, C.F.; Bernardo-Filho, M.; Mattos, D.M.; Moura, E.G. The
effect of protein or energy restriction on the biodistribution of Na99mTcO4in Wistar rats.
Nucl. Med. Comm. 2000,21, 1059-1062.
42. Passos, M.C.F.; Ramos, C.F.; Dutra, S.C.P.; Bernardo-Filho, M.; Moura, E.G.
Biodistribution of Na99mTcO4changes in adult rats whose mothers were malnourished
during lactation.J. Nucl. Med.2002,43, 89-91.
43. Braga, A. C. S.; Oliveira, M. B. N.; Feliciano, G. D.; Reiniger, I. W.; Oliveira, J. F.;
Silva, C. R.; Bernardo-Filho, M. The effect of drugs on the labeling of blood elements
with technetium-99m. Curr. Pharm. Design.2000,6, 1179-1191.
44. Sampson, C.B. Adverse reactions and drug interactions with radiopharmaceuticals.
Drug Saf.2003,8, 280-294.
45. Sampson, C.B. Complications and difficulties in radiolabelling blood cells: A review.
Nucl. Med. Comm. 1996,17, 648-658.
46. Aguiar, R.O.; Kwee, J.K.; De Paula, E.F.; Gomes, M.L.; Bernardo-Filho M. The
effect of murine B16F10 melanoma on the biodistribution of 99mTc-MDP in male
C57BL/6J mice. Cell. Mol. Biol.2002,48, 747-750.
47. Gomes, M.L.; Mattos, D.M.M.; Freitas, R.S.; Bezerra, J.R.A.C.; Bernardo-Filho, M.
Study of the toxicological effect of mitomycin C in mice: alteration on the biodistribution
of radiopharmaceuticals used for renal evaluations. Hum. Exp. Toxicol. 2001, 20,
193-197.
48. Mattos, D.M.M.; Gomes, M.L.; Freitas, R.S.; Bernardo-Filho, M. Effect of the
chemotherapeutic drugs on the biodistribution of the radiopharmaceutical 99mTc-phytate
25
in Chemistry and Nuclear Medicine. Podova: Servizi Grafici Editoriali. pp. 465-472.
1999.
49. Mattos, D.M.M.; Gomes, M.L.; Freitas, R.S.; Cardoso, V.N.; Bernardo-Filho, M. Drug
interaction with radiopharmaceuticals and the importance for the radiation dose to the
patient. In: IAEA (eds.) Radiological protection of patients in diagnostic and interventional radiology, nuclear medicine and radiotherapy. Vienna, Áustria, 2001.
50. Szentmihalyi, K.; Forgacs, E.; Hajdu, M.; Then, M. In vitro study on the transfer of
volatile oil components.J. Pharm. Biomed. Anal.2001,24, 1073-1080.
51. Newall, C.A.; Anderson, L.A.; Phillipson, J.D. Herbal medicines: a guide for
26
TABLE
Table 1: The effect of a Mentha crispa extract on the biodistribution of sodium
pertechnetate in Wistar rats.
Percentage of radioactivity per gram of tissue
(%ATI/g) (MEAN±SD) Organs
Control Treated
Pancreas (*) 0.15±0.03 0.28±0.07
Testis 0.14±0.02 0.23±0.10
Stomach 3.51±0.03 3.17±0.23
Kidney (*) 0.55±0.01 0.90±0.08
Spleen (*) 0.42±0.05 0.69±0.09
Duodenum 0.88±0.18 1.06±0.21
Heart 0.31±0.02 0.33±0.09
Lung 0.84±0.05 0.92±0.17
Liver (*) 0.61±0.03 0.72±0.02
Thyroid (*) 6.09±0.09 12.83±0.82
Bone 0.45±0.01 0.41±0.11
Muscle 0.18±0.01 0.19±0.08
Brain 0.09±0.04 0.06±0.01
(*) P=0.0061. An extract of mint (40g/L) was administered (ig) in rats for 15
days. Na99mTcO4 (0.3mL, 3.7Mbq) was administered for ocular plexus way.
After 10 min the animals were sacrificed and the organs were isolated. The
radioactivity in each organ (%ATI/g) was determined in a well counter and the