REVISTA
BRASILEIRA
DE
ANESTESIOLOGIA
PublicaçãoOficialdaSociedadeBrasileiradeAnestesiologiawww.sba.com.br
ARTIGO
CIENTÍFICO
Controle
da
hipnose
na
administrac
¸ão
de
propofol
com
base
na
estratégia
de
controle
não
linear
Muhammad
Ilyas
a,
Ali
Khaqan
a,
Jamshed
Iqbal
b,∗e
Raja
Ali
Riaz
aaCOMSATSInstituteofInformationTechnology,DepartmentofElectricalEngineering,ChakShahzad,Paquistão
bNationalUniversityofComputerandEmergingSciences(FAST-NU),DepartmentofElectricalEngineering,Islamabad,Paquistão
Recebidoem28demaiode2015;aceitoem17deagostode2015 DisponívelnaInternetem28dedezembrode2016
PALAVRAS-CHAVE Anestesiadecircuito fechado;
Controlemoderno; Biocontrole; Farmacodinâmica; Farmacocinética
Resumo Oajustecontínuodepropofolnaadministrac¸ãomanualdeanestesiaparaum
pro-cedimentocirúrgico oneraacargade trabalhodeanestesistas quetrabalham emambiente multitarefa.Indoalémdaadministrac¸ãomanualedainfusãoalvo-controlada(IAC),ocontrole decircuitofechadodainfusãodepropofoltemopotencialdeoferecerváriosbenefíciosem ter-mosdemanejodasperturbac¸õesereduziroefeitodavariabilidadeinterpaciente.Esteartigo propõeumaabordagemparaaadministrac¸ãoautomatizadadedrogasemcircuitofechadopara controlaraprofundidadedahipnose(PDH)emanestesia.Emcontrastecomamaioriadas pes-quisasexistentessobreocontroledaanestesiaqueusamestratégiasdecontrolelinearoude suasvariantesmelhoradas,anovidadedapresentepesquisaresidenaaplicac¸ãodeuma estra-tégiadecontroleconsistente; istoé,oControleporModosDeslizantes(CMD)paracontrolar comprecisãoainfusãodadroga.Combasenomodeloderivado dopaciente,ocontrolador projetadousaasmedic¸õesdoEEGpararegularaPDHnoBispectralIndex(BIS),controlaataxa deinfusãodepropofol.Odesempenhodocontroladoréinvestigadoecaracterizadocomum conjuntodedadosreaisdeoitopacientessubmetidosàcirurgia.Osresultadosdesteestudoin silicoindicamque,paratodosospacientes,com0%deexcessoobservado,oerrodeestado estacionário ficaentre±5.Clinicamente, issoimplicaqueem todososcasos,semqualquer sobredosagem,ocontroladormantémoníveldesejadodePDHparaaconduc¸ãotranquilados procedimentoscirúrgicos.
©2016SociedadeBrasileiradeAnestesiologia.PublicadoporElsevierEditoraLtda.Este ´eum artigoOpen Accesssobumalicenc¸aCCBY-NC-ND (http://creativecommons.org/licenses/by-nc-nd/4.0/).
∗Autorparacorrespondência.
E-mail:jamshed.iqbal@nu.edu.pk(J.Iqbal).
http://dx.doi.org/10.1016/j.bjan.2016.12.005
KEYWORDS Closed-loop anesthesia; Moderncontrol; Biocontrol;
Pharmacodynamics; Pharmacokinetics
RegulationofhypnosisinPropofolanesthesiaadministrationbasedonnon-linear controlstrategy
Abstract Continuous adjustmentof Propofol inmanual deliveryofanesthesia for
conduc-ting a surgical procedure overburdens the workload ofan anesthetist who isworking in a multi-taskingscenario. Going beyondmanual administrationandTargetControlledInfusion, closed-loopcontrolofPropofolinfusionhasthepotentialtoofferseveralbenefitsintermsof handlingperturbationsandreducingtheeffectofinter-patientvariability.Thispaperproposesa closed-loopautomateddrugadministrationapproachtocontrolDepthOfHypnosisinanesthesia. Incontrastwithmostoftheexistingresearchonanesthesiacontrolwhichmakesuseoflinear controlstrategiesortheirimprovedvariants,thenoveltyofthepresentresearchliesinapplying robustcontrolstrategyi.e.SlidingModeControltoaccuratelycontroldruginfusion.Basedon thederivedpatient’smodel,thedesignedcontrollerusesmeasurementsfromEEGtoregulate DOHonBispectralIndexbycontrollinginfusionrateofPropofol.Theperformanceofthe control-lerisinvestigatedandcharacterizedwithrealdatasetof8patientsundergoingsurgery.Results ofthisinsilicostudyindicatethatforallthepatients,with0%overshootobserved,thesteady stateerrorliesinbetween±5.Clinically,thisimpliesthatinallthecases,withoutanyoverdose, thecontrollermaintainsthedesiredDOHlevelforsmoothconductionofsurgicalprocedures. ©2016SociedadeBrasileiradeAnestesiologia.Publishedby ElsevierEditoraLtda.Thisisan openaccessarticleundertheCCBY-NC-NDlicense (http://creativecommons.org/licenses/by-nc-nd/4.0/).
Introduc
¸ão
Grac¸as aos avanc¸os tecnológicos, os benefícios
ofereci-dos pela medicina moderna transformaram totalmente o
conceito de cirurgia clínica. Atualmente, os
procedimen-toscirúrgicospodemserfeitoscommuitomaisfacilidadee
conforto.Essemarcoincrívelfoialcanc¸adoapenasatravés
dos resultadosde pesquisasem anestesia moderna.Antes
dadescobertadaanestesia,ascirurgiasprecisavamser
fei-tascomextremarapidez.Historicamente,técnicastriviais
como aplicac¸ão de frio, compressão donervo oureduc¸ão
daperfusãocerebralforamusadasparamanteropaciente
inconsciente.1 Sem dúvida, a invenc¸ão de gases
inalató-riosem1840porHickmanfoiumpassofundamental rumo
à descobertadaanestesia para finalmentepermitir
cirur-giasinvasivas. Oprimeiro procedimentodeanestesia com
base em éter dietílico foi feito em 1842 por C.W. Long.
Essenovoconceitorevolucionáriofoiposteriormente
deno-minado‘‘anestesia’’,quesignificaausênciadeestesia,isto
é,deconsciência.
Aanestesiaéamplamenteusadaemmuitasaplicac¸ões,
especialmente na esfera médica para procedimentos
cirúrgicos com incisão, cirurgia dentária e tratamentos
intensivos.2 O principal objetivo da anestesia é oferecer
dessensibilizac¸ãoaospacientescirúrgicosao conduzi-losa
umestadodeinconsciênciasemmemória.Ocenário
funcio-nalglobaldaanestesiapodesercategorizadoemtrêsfases
temporais sequenciais: induc¸ão, manutenc¸ão e despertar.
Duranteaprimeirafase,oobjetivoélevaropacienteauma
determinada profundidade de hipnose (PDH). Para tanto,
é necessário administrar o anestésico para manter uma
PDHadequada.Paraainduc¸ãoemanutenc¸ãodaanestesia,
o agente anestésico comumente administrado por via
intravenosa é o propofol.3 Durante a fase de emergência
em procedimentos pós-cirurgia,os vaporizadorese outros
dispositivosdeinfusãosãodesligadosparapermitirorápido
despertardospacientes.
Durante a anestesia geral, propofol é geralmente
usado em conjunto com opioides de ac¸ão rápida (p.
ex., remifentanil), que têm efeito sinérgico.4 A
subdosa-gemdemedicamentosanestésicospodelevaràinsuficiência
deanalgesiaouàconsciência.Poroutrolado,oexcessode
medicamentoéperigosoparaospacientes.Logo,omanejo
cuidadosodosmedicamentos intravenososé ofator-chave
paraosucessodapráticaanestésica.Odesejáveléacessara
profundidadedaanestesiaemconjuntocomaadministrac¸ão
automática e interativa do medicamento, com pouca
intervenc¸ãohumana,paraoajusteadequadodadosagemdo
medicamentoparaequilibraroestadoanestésico,afunc¸ão
autonômicaearespostaaosestímulosnocivos.
Os procedimentos de administrac¸ão de medicamentos
intravenosos evoluíram da simples administrac¸ão manual
paraaautomatizadavia‘‘infusãoalvo-controlada’’(Target
Controlled Infusion ---TCI) e para a administrac¸ão mais
sofisticada de anestesia com circuito fechado (
Closed--LoopANesthesia --- CLAN). Tradicionalmente, astaxasde
administrac¸ão de agenteshipnóticos em anestesia venosa
sãocontroladas manualmente porumanestesiologista. As
doses são decididas principalmente com base nos dados
demográficosdopacienteenossinaismedidos
qualitativa-mente(p. ex.,presenc¸adecertosreflexos, movimento)e
quantitativamente(p.ex., saturac¸ãodeoxigênio, pressão
arterial, frequência cardíaca). O regime de dosagem é
então equilibrado por tentativa e êxito para aprimorar a
anestesiaeevitar atoxicidade. ATCI,tambémconhecida
por ‘‘infusão contínua assistida por computador’’ (
Com-puter Assisted Continuous Infusion --- CACI),5 depende de
modelos farmacodinâmicos e farmacocinéticos com base
populacional6 paracalcularumperfildeinfusão adequado
paraatingiraconcentrac¸ão domedicamentoestabelecida
pelo anestesiologista. De acordo com as taxas de
infu-são passadas e presentes, esses modelos podem prever
a evoluc¸ão temporal da concentrac¸ão plasmática. Essa
Estado de vigília (100-90)
Estado hipnótico
leve
Estado hipnótico moderado
Início do estado
hipnótico
profundo Linha plana do EEG Aumento do padrão de
alternância (burst suppression)
0 20
40 60
Faixa de procedimento cirúrgico
80 100
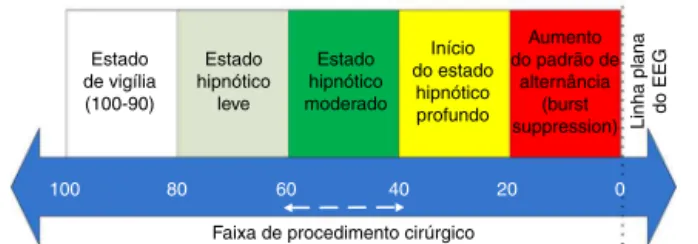
Figura1 FaixadaescaladoBISparaindicaroníveldePDH.
referência,forneceassimumparadigmadecontrolede
cir-cuito aberto. Em vez de ajustar a taxa de infusão, o
anestesiologista manipula a concentrac¸ão de referência,
de forma tanto reativa quanto proativa, usa bombas de
infusão comercialmente disponíveis. Os sistemas de TCI
têmasdesvantagensdesensibilidadeparamodelarasnão
linearidadeseperturbac¸õesporquenãoháfeedbacksobre
a mensurac¸ão do efeito do fármaco. Essas desvantagens
podemsertratadaspormeiodofechamentodocircuitode
controleatravésdamensurac¸ãodaPDH,queéfornecidapor
monitoresdeEEG;porexemplo,oíndice bispectral(BIS).7
OvalordoBISémapeadoparaoníveldaPDHdopaciente
combasenafaixaescalonadamostrada(fig.1).Ovalorde
100-90correspondeao estadodetotalvigíliaenquanto os
valoresde90-60e 60-40indicam níveisdehipnoseleve e
moderada,respectivamente.8Onívelmoderadorepresenta
afaixadeprocedimentocirúrgiconaquala cirurgiageral
éfeitaporprofissionaisclínicos.Umnívelacimadoestado
hipnóticoprofundo(40-20)émuitoperigoso.9
EmumsistemaCLAN,oefeitodofármacoémedidoem
tempo real e comparado com a PDH de referência para
obterumsinaldeerro.Embasadonesse,osistema
posterior-menteajustaataxadeinfusãodomedicamento.Umsistema
CLANofereceváriosbenefíciosemcomparac¸ãocomum
sis-temaTCI,inclusiveocontroleautomáticodeperturbac¸ões
eocontroleprecisodataxadeinfusão,minimizaoefeito
da variabilidade do paciente e reduz a necessidade de
intervenc¸ãopeloanestesiologista.
AtendênciaparaconceberumsistemaCLANfoibaseada
emabordagensdecontroletrivialoulinear.10Dong2propôs
um sistema CLAN para anestesia venosa total com base
em um ‘‘controlador proporcional, integral, derivativo’’
(Proportional, Integral, Derivative --- PID). Com BIS como feedbacksensorialeumsistemadesupervisãocombaseem
‘‘processamentodesinaldigital’’(DigitalSignalProcessing
---DSP),osistemaconcebidofoitestadoem 21voluntários
saudáveise15pacientessubmetidosàcirurgia.Excetopor
doispacientes,resultadosclínicossatisfatóriosforam
obti-dos.Outroestudo11combasenocontroladorPIDinvestigou
odesempenho docontrole em 10 pacientessubmetidos à
cirurgia eletiva de quadril e joelho. A mediana do
abso-luto de desempenho foi de 8%. A estratégia de controle
foi capaz de fornecer anestesia adequada em nove
paci-entes,com respostaoscilatória registrada em valoresBIS
paratrêspacientes.Outrosestudosimportantesrelataramo
controlePIDdaanestesia.12,13Acomparac¸ãodoPID
conven-cionalcomo‘‘modelolineardecontrolepreditivo’’(Linear
ModelPredictiveControl---LMPC)foifeita14erelatou-seque
oLMPCfoisuperioremtermosderobustezparaadinâmica
intraeinterpacienteenocontroledosdistúrbios,limitac¸ões
e mensurac¸ão de ruído. Estudos recentes15-18 objetivam
melhorarasabordagenslineareseajustarcorretamenteos
controladoresparaobtermargensdeconsistência
suficien-tesparaasincertezasidentificáveis.Contudo,paraasleis
decontrolebaseadasemabordagenslineares,omodelode
umpacientequeapresentaumcomportamentonãolinear
élinearizado.Talaproximac¸ãoobtémumbomdesempenho
do controle somente se a diferenc¸a prevista e realentre
ossistemasdecircuitofechadoforpequenaparao
contro-lador projetado.19 Ocontrolador PID tradicionalnãopode
controlar perturbac¸ões como alterac¸ões da pressão
arte-rial,bloqueioneuromuscularevariabilidadedafrequência
cardíaca10 e pode resultar em comportamento
oscilató-rio durante ensaios clínicos. Além disso, para a ampla
aceitac¸ão deumsistema CLANpor profissionais clínicose
órgãosreguladores, garantias consistentesdeestabilidade
e desempenhosãorequisitos. Aadoc¸ãodeumaestratégia
decontrolenãolineareconsistenteé,portanto,orequisito
domomentoemanestesiaclínica.
Estapesquisatemcomoobjetivorevelaropotencialde
uma estratégia de controle sofisticada, o ‘‘controle por
modos deslizantes’’ (Sliding Mode Control --- SMC), para
controlar a taxa de infusão de propofol. O trabalho está
organizadoda seguinteforma:a Sec¸ãoII trata domodelo
derivadodopaciente;aSec¸ãoIIIexplicaosdetalhesdo
pro-jetodeSMC;aSec¸ãoIVapresentaosresultadoscombasenos
parâmetrosclínicosdepacientesreaiseaSec¸ãoVapresenta
comentáriossobreasconclusões.
Modelo
derivado
do
paciente
Adinâmicadofármacohipnóticoécategorizadadeacordo
com seus parâmetros farmacocinético (PK) e
farmacodi-nâmico (PD). O parâmetro PK é usado para controlar
o comportamento do fármaco infundido no corpo ao
longo do tempo, inclusive distribuic¸ão, metabolismo,
absorc¸ão e depurac¸ão,20 enquanto o parâmetro PD
repre-senta a concentrac¸ão sanguínea do fármaco e o impacto
correspondentecausadonolocaldeefeito.21
Combasenofluxosanguíneoemdiferentesórgãos,a
lite-raturamédicadivideocorpohumanoemcompartimentos.22
Omodelocompartimentalrepresentaumaabordagem
ciné-tica básica para descrever a absorc¸ão, distribuic¸ão e
eliminac¸ão do fármaco.23 Por relacionaros níveis
plasmá-ticos do medicamento aos parâmetros PD, esse modelo
é intensamente usado em várias aplicac¸ões biomédicase
biotecnológicas devido a suainerente flexibilidade e
sim-plicidade.Aestruturaintegrada PKPDsegueamodelagem
compartimental. No presente estudo, um modelo PK de
três compartimentos foi adotado com umcompartimento
de efeitoadicional devido a suaprecisão adequada e
efi-ciênciacomputacional.24 Centradoem umcompartimento
primário(sangueintravascular)comvolumeV1,um
compar-timento periférico rápido (músculo) e umcompartimento
periféricolento (gordura),comvolumesV2e V3,
respecti-vamente,estãoligadosaocompartimentoprimário.Assim,
a distribuic¸ão e eliminac¸ão da droga entre os
comparti-mentosprimárioeperiféricoacontecemcomconstantesde
velocidadeponderadask12,k21,k13,k31,comoilustradona
figura2.Aqualquermomento,aalterac¸ãonaconcentrac¸ão
do fármaco no compartimento primário está relacionada
2
Compartimento periférico rápido
(V2) X2
Músculo
Gordura
Sangue intravascular Cérebro
Compartimento periférico lento
(V3) X3
Compartimento primário
(V1) X1
Compartimento local de efeito
Ce k1e
k10
T
axa
de infusão u(t)
k
21
k
12
k31
k13
ke0
3
1
Figura2 DiagramadeblocosdosmodelosPKePD.
periféricos rápido e lento. A induc¸ão e depurac¸ão do
fármacoacontecematravésdocompartimentoprimário.A
eliminac¸ão dofármaco desse compartimento acontece de
formaexponencial.17Nolocaldeatuac¸ãodofármaco
(cére-bro), aconcentrac¸ão é medida pelaatividade cortical no
cérebroqueémedidaatravésdaformamodificadadosinal
doEEG.25 Ainformac¸ãoextraídapode,então,sermapeada
para a profundidade de hipnose (PDH) para a análise da
adequac¸ãodopacienteparaosprocedimentoscirúrgicos.
Atabela1mostraanomenclaturaparaomodeloderivado
dopaciente.
ParaomodeloderivadodaPK,asequac¸õesdoestadoque
correspondemaostrêscompartimentospodemserescritas
como(1)---(3)
˙
x1(t)= −k10x1(t)− k12x1(t)− k13x1(t)+ k21x2(t)
+ k31x3(t)+ u(t) (1)
˙
x2(t)= −k12x1(t)− k21x2(t) (2)
˙
x3(t)= −k13x1(t)− k31x3(t) (3)
AstransformadasdeLaplacedasfunc¸ões(1)---(3)resultam
nasfunc¸ões(4)---(6)
sX1(s)= −(k10+ K12+ K13)X1(s)+ k21X2(s)+ k31X13(s)+ (t)
(4)
sX2(s)= k12X1(s)− k21X2(s) (5)
sX23(s)= k13X1(s)− k31X3(s) (6)
Resolvendo (4)---(6), a relac¸ão entrada-saída pode ser
escritacomo(7)
Dp(s)= X1(s)
U(s) =
(s2+ s(k
21+ k31)+ k21k31)
(s3+ s2(k
10+ k12+ k21+ k13+ k31)+ s(k10k21+ k10k31+ k13k21+ k31k21)+ (k10k21k31))
(7)
onde Dp(s)é ataxa deabsorc¸ão/metabolismo dofármaco
dentrodocorpo,definidacomoataxadedisposic¸ão.
Rees-crevendo(7),aformageraldomodeloPKéobtidacomo:
Dp(s)= X1(s)
U(s) =
b2s2+ b1s+ b0
a3s3+ a2s2+ a1s+ a0
(8)
onde b2=1, b1=21+31, b0=2131, a3=1,
a2=(10+12+13+31), a1=1021+1031+1231+1321+
3121,a0=102131
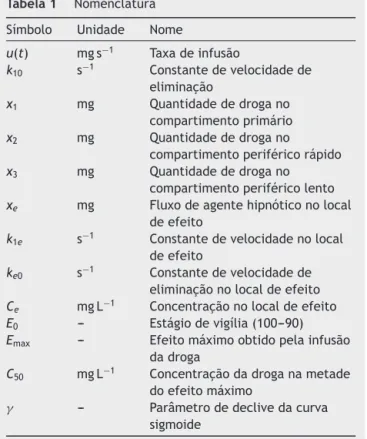
Tabela1 Nomenclatura
Símbolo Unidade Nome
u(t) mgs−1 Taxadeinfusão
k10 s−1 Constantedevelocidadede
eliminac¸ão
x1 mg Quantidadededrogano
compartimentoprimário x2 mg Quantidadededrogano
compartimentoperiféricorápido x3 mg Quantidadededrogano
compartimentoperiféricolento xe mg Fluxodeagentehipnóticonolocal
deefeito
k1e s−1 Constantedevelocidadenolocal
deefeito
ke0 s−1 Constantedevelocidadede
eliminac¸ãonolocaldeefeito Ce mgL−1 Concentrac¸ãonolocaldeefeito
E0 --- Estágiodevigília(100---90) Emax --- Efeitomáximoobtidopelainfusão
dadroga
C50 mgL−1 Concentrac¸ãodadroganametade
doefeitomáximo
--- Parâmetrodedeclivedacurva sigmoide
OmodeloPDindicaoníveldeconsciênciaerelacionaa concentrac¸ãodofármaconoplasmaàconcentrac¸ãonolocal deefeitoepodeserderivadocombasenoestadoEq.(9)
˙
xe(t)= k1ex1(t)− ke0xe(t) (9)
AplicandoastransformadasdeLaplace(9)
sXe(s)= k1eX1(s)− ke0Xe(s) (10)
Considerando que k1e e ke0 são iguais devido ao seu
volumedesprezível nocompartimento dolocal deefeito,
ataxadedisposic¸ãonolocaldeefeitoédadapor(11)
De(s)= Xe(s)
X1(s)
= ke0
(s+ ke0)
(11)
CombasenanaturezaemcascatadosmodelosPKePD,
o modelo global do paciente pode ser finalmente escrito
como:
Hp(s)= ke0
(s+ Xe0)
∗ b2s 2+ b
1s+ b0
a3s3+ a2s2+ a1s+ a0
(12)
OBISestárelacionado comaconcentrac¸ão nolocalde
efeitodoanestésicoCe(t)yatravésdeummodelosigmoide
nãolinear,ouseja
BIS(t)= E0− Emax∗
Ce(t)
Ce(t)+ C50 (13)
ondeCe(t)podesercalculadopelaintegrac¸ão(14)
˙
Modelo do paciente
Sigmoide PD
PK
BIS
S M C
b2s2 + b
1s + b0 ke0 Xe(s) s + ke0
a3s3 + a2s2 + a1s+a0 R(s)
Figura3 Diagramadeblocosdosistemaglobaldeciclofechado.
Concepc
¸ão
do
controle
Osistemadecircuitofechadoglobalnopresenteestudo
con-sisteprincipalmentedoSMCedomodeloPK-PDemcascata.
Asaídadessemodeloéalimentadaparaafunc¸ãosigmoide,
tambémconhecidacomofunc¸ãodeHill,quemapeiaasaída
em escaladoBIS. O valor doBISé usadocomo um
feed-backparaocontrolador.Afigura3apresentaodiagramade
blocosdosistemadecontroledofeedbackglobalusadopara
atingiraPDHdesejadaduranteosprocedimentoscirúrgicos.
Oobjetivoglobaldoprojetodecontroleéminimizaroerro
emestadoestacionárioparamanteroníveldaPDHdentro
davariac¸ãoaceitávelparaacirurgia.
A leide controle é baseada noSMC, umadas técnicas
decontrole maisconsistentes e eficazes para ossistemas
altamente não linearesque operam em ambientes
incer-tossujeitosaperturbac¸ões.O SMCenvolvea definic¸ãode
umasuperfíciedeslizante,tipicamenteumasuperfície
alta-mentelinear.Oconceitofundamental26 doSMC édirigira
dinâmicadosistemaapartirdequalquerestadoinicialpara
asuperfície deslizante(i.é,fasedealcance).Osistemaé
entãomantidonessasuperfícieparatodososvaloresfuturos
detempo(fasededeslizamento).Aprincipalvantagem
ofe-recidapeloSMCéasuabaixasensibilidadeparaimplantar
distúrbioseincertezas.27
ParaconceberoSMC,considera-seasuperfíciedeslizante
dadapor(15)
= a1x1+ a2x2+ a3x3+ a4xe (15)
Ou
˙
= a1˙x1+ a2˙x2+ a3x˙3+ a4˙xe (16)
ondea1,a2,a3,a4sãoparâmetrosdeajustedocontrolador.
Coma1=1,osvaloresdeoutrosparâmetrossãoescolhidos
demaneiraque0setorneopolinômiomônicodeHurwitz.
Essacondic¸ãogaranteareduc¸ãonaordemdosistema,que
pode ser representada com os estados n− 1. Tal sistema
demonstra insensibilidade às incertezas correspondentes.
Substituindoasequac¸õesdeestado,afunc¸ão(16)podeser
reescritacomo:
˙
= a1[(−k10− k12− k13)x1(t)+ k21x2(t)+ k31x3(t)+ u(t)]
+ a2[k12x1(t)− k21x2(t)]+ a3[k13x1(t)− k31x3(t)]
+ a4[k1ex1(t)− ke0xe(t)] (17)
Aleidecontroleglobal(u)consistenocontrole
equiva-lente(ueq)econtroledescontínuo(udisc),ouseja
u= ueq+ udisc (18)
Ocontroleequivalenteobrigaadinâmicadosistemaase
moverparaasuperfície deslizanteedependedosestados
tantodosistemaquantodosparâmetros.Tornaoderivado
dosmúltiplosdeslizamentosigualazeroepodeser
calcu-ladocolocando=0juntocomadinâmicadosistema(17).
Logo,
ueq= −[(−k10− k12− k13)x1(t)+ k21x2(t)+ k31x3(t)]
− a2[k12x1(t)− k21x2(t)]− a3[k13x1(t)− k31x3(t)]
− a4[k1e1(t)− ke0xe(t)] (19)
A presenc¸a de perturbac¸ões ouincertezas pode
resul-tar em = / 0. O controle descontínuo lida com tais
perturbac¸õesedependedoganhodafunc¸ãosinal,queexibe
mudanc¸adecomportamento.Logo,
udisc= −ksign() (20)
ondek∈ Rn×néamatrizdoganhodedescontinuidade.
Mate-maticamente,
sign()=
1for>0
−1for<0
(21)
Para investigar e caracterizar o desempenho do
con-troladorproposto,osdadosclínicos,inclusive asvariáveis
características dos oito pacientes, são apresentados na
tabela2.8
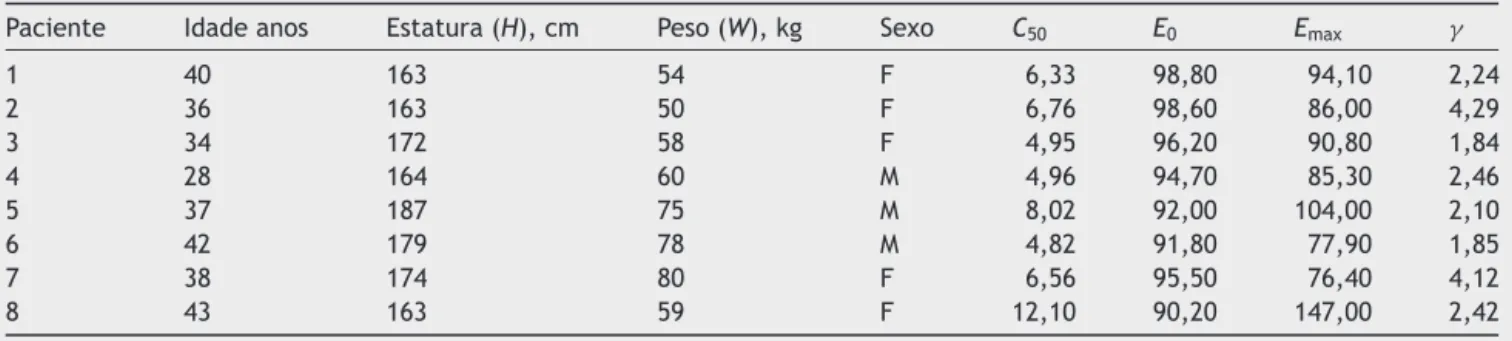
Tabela2 Conjuntodedadosclínicosquemostraascaracterísticasdospacientes
Paciente Idadeanos Estatura(H),cm Peso(W),kg Sexo C50 E0 Emax
1 40 163 54 F 6,33 98,80 94,10 2,24
2 36 163 50 F 6,76 98,60 86,00 4,29
3 34 172 58 F 4,95 96,20 90,80 1,84
4 28 164 60 M 4,96 94,70 85,30 2,46
5 37 187 75 M 8,02 92,00 104,00 2,10
6 42 179 78 M 4,82 91,80 77,90 1,85
7 38 174 80 F 6,56 95,50 76,40 4,12
a
b
0 50 100 150 200 250
–0,5 0 0,5 1
Tempo (s) Conc. plasmática da droga (mg/L)
Compartimento primário Compartimento periférico rápido Compartimento periférico lento Compartimento local de efeito
0 50 100 150 200 250
85 90 95 100
Tempo (s)
BIS
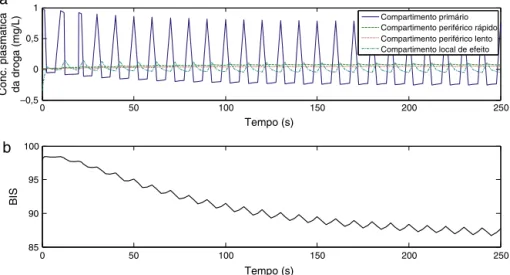
Figura4 Administrac¸ãosemcontroladordeagenteanestésiconopaciente6:(a)concentrac¸ãodofármacoemvários
comparti-mentose(b)perfildesaída.
Combasenosatributosdopaciente,osparâmetros clíni-coscalculadoscomousodomodelodetrêscompartimentos deSchniderparapropofolsãoapresentadosabaixo:
V1=4.27[l]
AV2=18.9−0.391(Age−53)[l]
AV3=238[l]
Cl1=1.89+0.0456(W−77)−0.0681(LBM−59)
+0.0264(H−177)
Cl2=1.29−0.24(Age−53)
Cl3=0.836
ondeamassacorporalmagra(LBM)éumafunc¸ãodesexo, pesoeestaturadopaciente.Parahomensemulheres,aLBM érespectivamentedescritacomo:
LBM=1.1∗W−128∗W 2
H2
LBM=1.07∗W−148∗W 2
H2r 2
Asconstantesdevelocidadek10,k12,k13,k21,k31 depen-demdepeso, estatura, idadee gênero dopaciente esão descritascomo:
k10= Cl1
V1
k12= Cl2
V1
b
a
c
0 50 100 150 200 250
1,4 1,6 1,8 2
Tempo (s) Taxa de infusão da droga (mg/s)
0 50 100 150 200 250
–0,5 0 0,5 1 1,5 2
Tempo (s) Conc. plasmática da droga (mg/L)
Compartimento primário Compartimento periférico rápido Compartimento periférico lento Compartimento local de efeito
0 50 100 150 200 250
40 50 60 70 80 90 100
Tempo (s)
BI
S
Figura 5 Controle de circuito fechado baseado em SMC do agente anestésico no paciente 6: (a) controle de entrada,
a
b
c
d
0 50 100 150 200 250
–0,5 0 0,5 1 1,5 2
Tempo (s) Conc. plasmática da droga (mg/L)
Compartimento primário Compartimento periférico rápido Compartimento periférico lento Compartimento local de efeito
0 50 100 150 200 250
–0,5 0 0,5 1 1,5 2
Tempo (s) Conc. plasmática da droga (mg/L)
Compartimento primário Compartimento periférico rápido Compartimento periférico lento Compartimento local de efeito
0 50 100 150 200 250
–0,5 0 0,5 1 1,5 2
Tempo (s) Conc. plasmática da droga (mg/L)
Compartimento primário Compartimento periférico rápido Compartimento periférico lento Compartimento local de efeito
0 50 100 150 200 250
–1 0 1 2
Tempo (s) Conc. plasmática da droga (mg/L)
Compartimento primário Compartimento periférico rápido Compartimento periférico lento Compartimento local de efeito
Figura6 Concentrac¸ãoplasmáticadadroganopaciente4(a),paciente8(b),paciente2(c),paciente7(d).
0 50 100 150 200 250
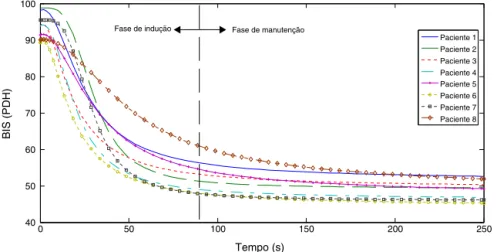
40 50 60 70 80 90 100
Tempo (s)
BIS (PDH)
Paciente 1 Paciente 2 Paciente 3 Paciente 4 Paciente 5 Paciente 6 Paciente 7 Paciente 8 Fase de manutenção
Fase de indução
k13= Cl3 V1
k21= Cl2 V2
k31= Cl3 V3
Resultados
e
discussão
Oesquemahabitualdeadministrac¸ãodoagenteanestésico
simplesmenteconsisteemumparadigmasemcontrolador.
Comtalesquema,afigura4Amostraaconcentrac¸ão
plas-máticadofármacoem várioscompartimentos,enquanto a
figura4BmostraoperfildesaídanaformadesinaldoBIS.
OsvaloresdoBISaindaestãolongedoníveldesejadodePDH
necessárioparaacirurgiageral.Observa-seapartirdesses
resultadosqueomanejodaanestesiasemumcontrolador
dedicadonocircuitopodeserbastantearriscadoe,em
mui-tassituac¸õescirúrgicas,podenãoseradequado.Comouso
desseesquema,aprecisãodaadministrac¸ãode
medicamen-tosa umpaciente durantea cirurgiadependetotalmente
daexperiênciadoanestesiologista.Arespostacríticadesse
controladortorna-semaisproblemáticaecrucial,
especial-mentenoscasosdecrianc¸asepacientescardíacos.
Ousodeumcontroladorconsistenteemformadecircuito
fechado muda totalmente a resposta. A figura 5A mostra
onívelcontroladodeinfusãodemedicamentoscomo uso
datécnicadeSMCparaopaciente6.Aconcentrac¸ão
plas-máticadofármaconoscompartimentosdaestruturaPKPD
é ilustrada na figura 5B, na qual a taxa de variac¸ão da
concentrac¸ãodofármacoemrelac¸ãoaotempoemtodosos
quatrocompartimentosdocorpoapósainfusãoé
apresen-tada. Inicialmente,a concentrac¸ão dofármaco é máxima
nocompartimentoprimário, masà medidaque ofármaco
semoveentreoscompartimentosprimárioeperiférico,seu
níveldiminuiexponencialmentenocompartimentoprimário
eaumentanoperiférico.Essefluxodofármaconos
compar-timentos é representadoatravés douso de constantesde
velocidade.Asaídadoindicador doBISestárepresentada
na figura5C.O gráficomostraclaramente quea presenc¸a
do controlador com umsistema de realimentac¸ão de
cir-cuito fechado melhora dramaticamente o desempenho do
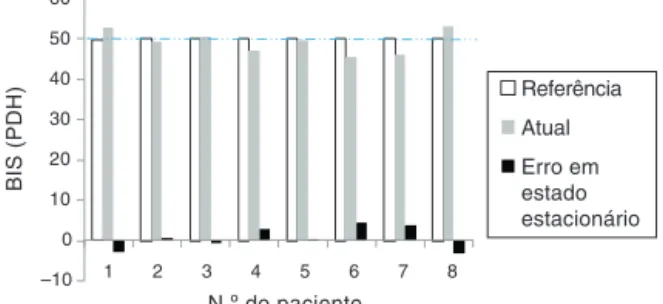
–10 0 10 20 30 40 50 60
8 7 6 5 4 3 2 1
BIS (PDH)
N.º do paciente
Referência
Atual
Erro em estado estacionário
Figura8 ErroemestadoestacionáriomostraqueaPDHestá navariac¸ãodesejada.
processodeanestesia.Dentrodesegundos,asaídaconverge
para o nível do BIS necessário para cirurgia. O
controla-dorentão mantém essenível dePDH, de modoa auxiliar
oanestesiologistaagarantirumaregiãomaisseguraparaa
operac¸ão.
Aconcentrac¸ão plasmáticado fármacoem vários
com-partimentoséumafunc¸ãodosfatoresqueincluemaidade
do paciente. Quanto menor for a idade de um paciente,
maisrápidoseráometabolismo/eliminac¸ãodadroga.Como
exemplo,compareaconcentrac¸ãodofármaconos
pacien-tes 4 e 8 ilustrada na figuras 6A e 6B, respectivamente.
É evidente que o paciente 4, por ser comparativamente
mais jovem, tem um metabolismo mais rápido do
medi-camentonocompartimento primáriodoque opaciente8.
Acomparac¸ão de pacientes jovens e velhos revela que a
concentrac¸ãonocompartimentoperiféricorápidoaumenta
substancialmentedevidoaofluxorápidodepropofola
par-tirdocompartimentoprimário.Omesmoefeitoérefletido
nocompartimentoperiféricolentoenocompartimentodo
localdeefeito.
Em contrastecomaidade, opeso deumpaciente não
interfere demodo significativo noperfil de concentrac¸ão
plasmática do fármaco. Para investigar esse efeito,
as concentrac¸ões nos pacientes 2 e 7 (peso=30kg)
foramcomparadas (figs. 6C e 6D). Podemos notar que a
concentrac¸ão de propofol no compartimento primário do
paciente2diminuia umataxa relativamenteigualàquela
dopaciente 7.Apequenadiferenc¸anasrespostasdeve-se
à diferenc¸a entre as idades dos pacientes. O mesmo é
observadoemrelac¸ãoaofluxodomedicamentoparaoutros
compartimentos.
0 50 100 150 200 250
1,2 1,3 1,4 1,5 1,6 1,7 1,8 1,9
Tempo (s)
Taxa de infusão da droga (mg/s)
Paciente 1 Paciente 2 Paciente 3 Paciente 4 Paciente 5 Paciente 6 Paciente 7 Paciente 8
Ocontroladorprojetadocomomodeloderivadodo
paci-enteéentãosimuladodeacordocomoconjuntodedados
(tabela 2). Os resultados da simulac¸ão apresentados na
figura 7 apresentamo nívelde hipnose de oitopacientes
apósainfusãodofármaco paraa cirurgia.Essasrespostas
indicamasfasestantodeinduc¸ãoquantodemanutenc¸ãoda
anestesia.Inicialmente,duranteafasedeinduc¸ão,o
paci-enteestáemestadodevigília(níveldePDHpróximoa100)
e,emseguida,opacienteentraemestadohipnótico
mode-rado(níveldePDHde40-60).Essenívelé mantidoparaa
execuc¸ãoseguradeprocedimentoscirúrgicos.Nesteestudo,
todosospacientes atingiramo nívelideal dehipnose.No
entanto,por razõesdequantificac¸ão, afigura 8 mostra o
erroem estadoestacionário considerandoo nível de PDH
de50comoreferência.Odelimitadoentre± 5aindaestá
dentrodavariac¸ãoaceitávelparaoperac¸õescirúrgicas.
O SMC projetado fornece diferentes taxas de infusão
depropofolcorrespondentesadiferentespacientes(fig.9)
devidoàsdiferenc¸as nosparâmetros dos pacientes,como
idade,peso,estatura,sexoeLBMparamanteronível
dese-jadodePDH.Ocontroladorinicialmentepermiteainjec¸ão
degrandesquantidadesdadrogaparalevaro pacienteao
estadode inconsciênciana fasede induc¸ão daanestesia.
Quandooníveldesejadodehipnoseéobtido,ocontrolador
entãomantém rigorosamente ataxa específicadeinfusão
duranteafasedemanutenc¸ãodaanestesiaparacada
paci-ente.
Conclusão
Este artigo propõe uma lei baseada em SMC para a
administrac¸ãoadequadaeseguradaanestesiacompropofol
paraaobtenc¸ãodeníveisideaisdehipnose.Osresultadosda
simulac¸ãocombasenoconjuntodedadosrespectivosaoito
pacientesreais,comdiferentesparâmetrosclínicos,
com-provamclaramentea eficáciadaabordagemapresentada.
ComaajudadosprofissionaismédicosdoNationalInstitute
ofHealth(NIH)doPaquistão,vamostestaroCLANproposto
emcenáriocirúrgicorealapósocumprimento dasnormas
deseguranc¸amédica.Éimperativodemonstrarosbenefícios
práticosdoCLANparaconvencerosprofissionaismédicos.
Atécnica deanestesiacom circuitofechado (Closed-Loop
ANesthesia ---CLAN), embora sejapotencialmente o
obje-tivofinaldainfusãodeagentesanestésicos,aindaestános
estágiosiniciaisde pesquisa.Aprevisão é quetal sistema
deCLANcom baseem umcontrole consistentenãolinear
substituiráaadministrac¸ãomanual,bemcomoosistemade
TCIemumfuturomuitopróximo.
Conflitos
de
interesse
Osautoresdeclaramnãohaverconflitosdeinteresse.
Referências
1.BibianS.Automationinclinicalanesthesia.Canada:Universityof BritishColumbia;2006[PhDThesis].
2.DongC.Closedloopcontrolledtotalintravenousanaesthesia.UK: UniversityofPlymouth;2003[PhDThesis].
3.WarpechowskiP,SantosATL,PereiraPJI,etal.Effectsofpropofolon thecardiacconductionsystem.RevBrasAnestesiol.2010;60:441---4.
4.AbsalomAR,SutcliffeN,KennyGNC.Closed-loopcontrolof anesthe-sia using bispectral index: performance assessment in patients undergoingmajororthopedicsurgeryundercombinedgeneraland regionalanesthesia.Anesthesiology.2002;96:67---73.
5.LiuN,ChazotT,GentyA,etal.Titrationofpropofolfor anesthe-tic induction and maintenance guided by the bispectral index: closed-loopversusmanualcontrol:aprospective,randomized, mul-ticenterstudy.Anesthesiology.2006;104:686---95.
6.Simoni RF,Miziara LEDPG, Esteves LO, et al. Pharmacodynamic evaluationandphysical/chemicalanalysisoftwoformulations of propofol usedin target-controlled infusion.RevBras Anestesiol. 2013;63:66---72.
7.NunesRR,ChaveIMM,AlencarJCGD,etal. Bispectralindex and otherprocessedparametersofelectroencephalogram:anupdate. RevBrasAnestesiol.2012;62:111---7.
8.IonescuCM,DeKeyserR,TorricoBC,etal.Robustpredictivecontrol strategyappliedforpropofoldosingusingBISasacontrolledvariable duringanesthesia.IEEETransBiomedEng.2008;55:2161---70.
9.StruysM,DesmetT,GreenwaldS,etal.Performanceevaluation oftwopublishedclosed-loopcontrolsystemsusingbispectralindex monitoring:asimulationstudy.Anesthesiology.2004;100:640---7.
10.LanJY,AbbodMF,YehRG,etal.Review:intelligentmodelingand controlinanesthesia.JMedBiolEng.2012;32:293---307.
11.AbsalomAR,StruysMMRF.Anoverviewoftargetcontrolledinfusions andtotalintravenousanaesthesia.SanDiego,CA,USA:Academia Press;2007.
12.SolteszK,HeusdenK,DumontGA,etal.Closed-loopanesthesiain childrenusingaPIDcontroller:apilotstudy.In:IFACconferenceon advancesinPIDcontrol.2012.
13.SakaiT,MatsukiA,WhitePF,etal.UseofanEEG-bispectral closed--loopdeliverysystemforadministeringpropofol.ActaAnaesthesiol Scand.2000;44:1007---10.
14.IngoleDD,SonawaneDN,NaikVV,etal.Linearmodelpredictive controllerforclosed-loop controlofintravenous anesthesiawith timedelay.ACEEEIntJControlSystInstrum.2013;4:8---15.
15.ZhusubaliyevTZ,MedvedevA,SilvaMM.Bifurcationanalysisof PID--controlledneuromuscularblockade in closed-loop anesthesia.J ProcessControl.2015;25:152---63.
16.HeusdenKV,DumontGA,SolteszK,etal.Designandclinical evalu-ationofrobustPIDcontrolofpropofolanesthesiainchildren.IEEE TransControlSystTechnol.2014;22:491---501.
17.SolteszK,DumontGA,AnserminoJM.Assessingcontrolperformance inclosed-loop anesthesia. In: 21stMediterraneanconference on controlandautomation.2013.p.191---6.
18.WestN,DumontGA,HeusdenKV,etal.Robustclosed-loopcontrol ofinductionandmaintenanceofpropofolanesthesiainchildren. PediatrAnesth.2013;23:712---9.
19.AjwadSA,IqbalJ,UllahMI,etal.Asystematicreviewofcurrent andemergent manipulator controlapproaches.Front MechEng. 2015;10:198---210.
20.ShargelL,Wu-PongS,YuAB.Appliedbiopharmaceuticsand phar-macokinetics.NY,USA:McGraw-Hill;2007.
21.HeusdenKV,SolteszK,KhosraviS,etal.Quantificationofthe varia-bilityinresponsetopropofoladministrationinchildren.IEEETrans BiomedEng.2013;60:2521---9.
22.CoppensMJ, EleveldDJ,ProostJH,etal.Anevaluationofusing populationpharmacokineticmodelstoestimatepharmacodynamic parametersforpropofolandbispectralindexinchildren. Anesthe-siology.2011;115:83---93.
23.BibianS,RiesCR,HuzmezanM,etal.Introductiontoautomated drugdeliveryinclinicalanesthesia.EurJControl.2005;11:535---57.
24.SchniderTW,MintoCF,CambusP,etal.Theinfluenceofmethodof administrationandcovariatesonthepharmacokineticsofpropofol inadultvolunteers.Anesthesiology.1998;88:1170---82.
25.HendrickxJF.Thepharmacokineticsofinhaledanestheticsand car-riergases.Belgium:GhentUniversity;2004[PhDThesis].
26.IslamRU,IqbalJ,KhanQ.Designandcomparisonoftwocontrol stra-tegiesformulti-DOFarticulatedroboticarmmanipulator.Control EngApplInform.2014;16:28---39.