Instituto de Ciˆencias Exatas e Biol´ogicas
Curso de P´os-graduac¸˜ao em Mestrado em F´ısica de Materiais
Ad´elia Moreira Marques dos Santos
Estudo da Resistˆencia `a Corros˜ao de Filmes de Carbono
Amorfo Hidrogenado GLCH (Graphite-like) Depositados
sobre a liga Ti6Al4V.
Estudo da Resistˆencia `a Corros˜ao de Filmes de Carbono
Amorfo Hidrogenado GLCH (Graphite-like) Depositados
sobre a liga Ti6Al4V.
Disserta¸c˜ao apresentada ao Curso de Mestrado em F´ısica de Materiais da UFOP, como requisito para a obten¸c˜ao do grau de MESTRE em Mestrado em F´ısica de Materiais.
Orientador: Prof(a). Dr(a). Ta´ıse Matte Manhabosco
Doutorado em Engenharia de Minas, Metal´urgica e de Materiais pela Universidade
Federal do Rio Grande do Sul, Brasil.
Coorientador: Prof. Dr. Ronaldo J´unio Batista Campos
Doutorado em F´ısica pela Universidade Federal de Minas Gerais, Brasil.
Catalogação: sisbin@sisbin.ufop.br
S237e Santos, Adélia Moreira Marques dos.
Estudo da resistência à corrosão de filmes de carbono amorfo hidrogenado GLCH (Graphite-like) depositados sobre a liga Ti6Al4V. – 2013.
66f.: il. color., grafs., tabs.
Orientador: Profa. Dra.Taíse Matte Manhabosco.
Dissertação (Mestrado) - Universidade Federal de Ouro Preto. Instituto de Ciências Exatas e Biológicas. Departamento de Física. Programa de Pós-Graduação em Ciências.
Área de concentração:Física de materiais
1. Carbono - Teses. 2. Nanoestrutura - Teses. 3. Corrosão - Teses. 4. Filmes finos - Teses. I. Manhabosco, Taíse Matte. II. Universidade Federal de Ouro Preto. III. Título.
No presente trabalho foram estudadas amostras de Ti6Al4V, Ti6Al4V nitretada e fil-mes de carbono amorfo graphite-like a-C:H (GLCH) depositados na liga de Ti6Al4V nua e nitretada. Os filmes GLCH, depositados por deposi¸c˜ao qu´ımica por vapor assistida por plasma (PACVD), foram caracterizados por microscopia eletrˆonica de varredura, micros-copia de for¸ca atˆomica e espectrosmicros-copia de Raman.
Um estudo da resistˆencia `a corros˜ao foi realizado por espectroscopia de impedˆancia eletroqu´ımica e curvas de polariza¸c˜ao potenciodinˆamica em solu¸c˜ao fisiol´ogica simulada.
Segundo as an´alises de espectroscopia de impedˆancia eletroqu´ımica, a liga nua e a liga nitretada puderam ser simuladas com o mesmo circuito equivalente, mas a resistˆencia `a polariza¸c˜ao da liga nitretada ´e bem maior em rela¸c˜ao `a liga nua, indicando um aumento da resistˆencia `a corros˜ao. J´a os filmes depositados em ambos os substratos apresentam elevada resistˆencia `a corros˜ao, contudo eles contˆem poros que permitem um processo difusivo e a corros˜ao do substrato. Ap´os 16 dias de imers˜ao, os filmes depositados sobre a liga nitretada apresentaram mudan¸cas no comportamento das curvas de impedˆancia, o que resultou em um circuito equivalente diferente. O novo circuito indica uma degrada¸c˜ao da interface substrato/filme GLCH, com delamina¸c˜ao e craqueamento do filme. Segundo ensaios de curva de for¸ca, esta ocorrˆencia poderia estar ligada `a baixa ades˜ao dos filmes ao substrato ou `a baixa afinidade qu´ımica entre o revestimento e o substrato.
In the present work samples of Ti6Al4V, nitrided Ti6Al4V and graphite-like hydrogena-ted amorphous carbon (GLCH) films deposihydrogena-ted onto bare and nitrided Ti6Al4V alloy were studied. GLCH films deposited by plasma assisted chemical vapor deposition (PACVD) were characterized by scanning electron microscopy, atomic force microscopy and Raman spectroscopy.
The corrosion resistance was verified by electrochemical impedance spectroscopy and potentiodynamic polarization curves in a simulated physiological solution.
According to electrochemical impedance spectroscopy analysis, the bare and the nitride alloy were simulated with the same equivalent circuit. However, the polarization resistance of the nitride alloy is greater than that of the bare alloy which indicates an increase in the corrosion resistance. Films deposited onto both substrates show high corrosion resistance, however they contain pores that allow a diffusive process and the substrate corrosion. The films deposited onto nitrided alloy show variations in the behavior of impedance curves after sixteen days of immersion, which result in a different equivalent circuit. The new equivalent circuit indicates the degradation of substrate/GLCH film interface with delamination and cracking of the film. Force curve tests indicates that the film degradation can be related to the low adhesion force of films to substrate or the low chemical affinity between the coating and the substrate.
Agrade¸co a DEUS, que me proporcionou a possiblidade de concluir mais essa etapa, o que seria de mim sem a f´e que tenho Nele. `A minha orientadora, Professora Dra. Ta´ıse Matte Manhabosco, pelos ensinamentos, por toda dedica¸c˜ao, paciˆencia e competˆencia com que me orientou neste trabalho, me transferindo uma parte valiosa do seu conhecimento. Ao meu co-orientador Ronaldo J´unio Campos Batista que tamb´em contribuiu com sua sabedoria e dedica¸c˜ao para conclus˜ao deste trabalho.
Aos laborat´orios Lacor da UFRGS e de Microscopia de Varredura por sonda da UFMG pela disponibilidade nas realiza¸c˜oes das medidas.
A UFOP e ao Programa de P´os-Gradua¸c˜ao em F´ısica de Materiais pela possibilidade de realiza¸c˜ao do mestrado e apoio financeiro. Aos professores do programa que participaram desta minha caminhada, `a secret´aria Mariana e aos meus colegas pela paciˆencia e o apoio que foram fundamentais para o t´ermino da disserta¸c˜ao.
Aos meus pais, ˆAngelo e Arlinda, aos meus irm˜aos Davi, Laurentina, ˆAngela, Isaac e Fernanda, meus cunhados J´ulio, Stefan, Gustavo e meu noivo Rafael pelo apoio, incentivo e paciˆencia durante os momentos em que estive ausente, para a conclus˜ao deste curso.
A todos que colaboraram direta ou indiretamente na elabora¸c˜ao e conclus˜ao deste tra-balho, o meu sincero reconhecimento.
j´a mais voltar´a ao seu tamanho origi-nal”.
Lista de Figuras 8
Lista de Tabelas 10
1 Introdu¸c˜ao 11
2 Materiais 12
2.1 Ti6Al4V e Ti6Al4V Nitretado . . . 12
2.2 Filmes de Carbono Amorfo . . . 14
2.3 Aplica¸c˜ao de Filmes de Carbono Amorfo . . . 16
2.4 Resvestimentos de Carbono Amorfo sobre o Titˆanio e suas Ligas . . . 16
2.5 Corros˜ao dos Metais . . . 17
3 T´ecnicas de Modifica¸c˜ao Superficial 20 3.1 T´ecnica de Obten¸c˜ao de Filmes de Carbono Amorfo Hidrogenado . . . 20
3.2 T´ecnica de Nitreta¸c˜ao . . . 23
4 T´ecnicas de Caracteriza¸c˜ao 26 4.1 Microscopia Eletrˆonica de Varredura . . . 26
4.2 Microscopia de For¸ca Atˆomica . . . 27
4.3 Espectroscopia Raman . . . 29
4.4 Espectroscopia de Impedˆancia Eletroqu´ımica . . . 32
4.4.1 Elementos de Circuito Comumente Encontrados em Sistemas Ele-troqu´ımicos . . . 34
5.1.1 Prepara¸c˜ao Superficial . . . 37
5.1.2 Nitreta¸c˜ao . . . 38
5.1.3 Deposi¸c˜ao de Filmes de Carbono Amorfo Hidrogenado do Tipo Gra-fite (GLCH) . . . 38
5.2 T´ecnicas Eletroqu´ımicas . . . 38
5.2.1 Polariza¸c˜ao Potenciodinˆamica . . . 38
5.2.2 Espectroscopia de Impedˆancia Eletroqu´ımica(EIS) . . . 39
5.3 Microscopia Eletrˆonica de Varredura . . . 40
5.4 Microspoia de For¸ca Atˆomica . . . 41
5.5 Espectroscopia Raman . . . 41
6 Resultados e Discuss˜oes 43 6.1 Caracteriza¸c˜ao dos Filmes GLCH . . . 43
6.2 T´ecnicas Eletroqu´ımicas . . . 47
6.2.1 Curva de Polariza¸c˜ao Potenciodinˆamica . . . 47
6.2.2 Espectroscopia de Impedˆancia Eletroqu´ımica (EIE) . . . 48
6.3 Curva de For¸ca . . . 58
7 Conclus˜ao 60
2.1 V´alvula artificial do cora¸c˜ao [3]. . . 13
2.2 Parafuso e placas ´osseas [3]. . . 13
2.3 Diagrama de fase tern´ario para filmes de carbono amorfo com rela¸c˜ao `a quantidade de liga¸c˜ao sp2
, sp3
e hidrogˆenio [6]. . . 15
3.1 Esquema de um diagrama para sistema de deposi¸c˜ao de filmes de DLC [31]. 22
3.2 Esquema b´asico de um equipamento de nitreta¸c˜ao por plasma [37]. . . 25
4.1 Esquema do princ´ıpio de funcionamento da coluna MEV [39]. . . 27
4.2 Diagrama representativo de funcionamento do microsc´opio de for¸ca atˆomica [40]. . . 28
4.3 Origem dos espalhamentos Rayleigh e Raman [42]. . . 31
4.4 Espectro Raman de um filme de a-C:H obtido pela t´ecnica de PACVD para um plasma de metano [43]. . . 31
4.5 Diagrama Nyquist, no eixo x a impedˆancia real e no eixo y a impedˆancia imagin´aria com vetor impedˆancia [44]. . . 33
4.6 Gr´afico de Bode em fun¸c˜ao da constante de tempo [44]. . . 34
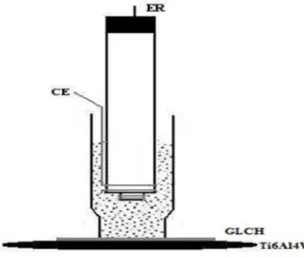
5.1 Desenho esquem´atico da c´elula eletroqu´ımica em ensaios de impedˆancia eletroqu´ımica. . . 40
6.1 Imagem ao MEV para o filme GLCH depositado sobre substrato de Ti6Al4V por PACVD. . . 43
6.2 Imagens de Microscopia de For¸ca Atˆomica para filmes depositados na (A) liga de Ti6Al4V e (B) liga Ti6Al4V nitretada. . . 44
6.5 Gr´afico da posi¸c˜ao de picos G em fun¸c˜ao do percentual de liga¸c˜oessp3
para filmes a-C:H [52]. . . 46
6.6 Diagrama tern´ario para filmes de carbono amorfo [6]. . . 46
6.7 Curva de polariza¸c˜ao potenciodinˆamica para substrato de Ti6Al4V, Ti6Al4V nitretado e filme GLCH depositado por PACVD sobre liga de Ti6Al4V nua e nitretada. Curva realizada a uma velocidade de varredura de 0,167mV/s. 48
6.8 Gr´afico de Bode da liga Ti6Al4V, imerso em solu¸c˜ao PBS para 1hora, 48 horas 7 dias, 16 dias, 23 dias, e 30 dias. . . 49
6.9 Modelo de circuito equivalente para a liga de Ti6Al4V. . . 49
6.10 Gr´afico de Bode da liga de Ti6Al4V nitretado, imerso em solu¸c˜ao PBS para 1hora, 48 horas, 7 dias, 16 dias, 23 dias, e 30 dias. . . 51
6.11 Modelo de circuito equivalente para o Ti6Al4V nitretado. . . 51
6.12 Gr´afico de Bode do filme GLCH depositado na liga Ti6Al4V, imerso em solu¸c˜ao PBS para 1hora, 48 horas, 7 dias, 16 dias, 23 dias, 30 dias e 37 dias. 53
6.13 Modelo de circuito equivalente para o filme GLCH depositado sobre a liga de Ti6Al4V. . . 53
6.14 Gr´afico de Bode do filme GLCH depositado na liga Ti6Al4V nitretada, imerso em solu¸c˜ao PBS para 1hora, 48 horas, 7dias, 16 dias, 23 dias, 30 dias e 37 dias . . . 55
6.15 Modelo de circuito equivalente para o filme GLCH depositado sobre o Ti6Al4V nitretado. . . 57
6.16 Curva de for¸ca experimental para a liga nua e nitretada, usando uma ponta de diamante ap´os um aquecimento a 120o
C por 30 min. . . 58
5.1 Composi¸c˜ao da barra de Ti6Al4V conforme fornecedor (Gustoc-Alemanha) 37
5.2 Tempo de imers˜ao das amostras . . . 40
6.1 Parˆametros de ajuste do espectro de impedˆancia realizados ao longo dos tempos de imers˜ao para Ti6Al4V. . . 50
6.2 Parˆametros de ajuste do espectro de impedˆancia realizados ao longo dos tempos de imers˜ao para Ti6Al4V nitretado. . . 52
6.3 Parˆametros de ajuste do espectro de impedˆancia realizados ao longo dos tempos de imers˜ao para o filme GLCH depositado sobre a Ti6Al4V. . . 54
1 Introdu¸c˜
ao
A liga de Ti6Al4V ´e um material muito empregado na biomedicina e na ind´ustria em geral devido `as suas propriedades como a alta resistˆencia `a corros˜ao, boa resistˆencia `a fadiga, baixa densidade, boa biocompatibilidade, entre outras. No entanto, em algumas aplica¸c˜oes tais como implantes de joelho e quadril, esta liga apresenta algumas limita¸c˜oes pois ´e requerida uma maior resistˆencia ao desgaste.
Para contornar este tipo de problema pode-se utilizar tratamentos termoqu´ımicos como, por exemplo, o processo de nitreta¸c˜ao que possibilita a forma¸c˜ao de uma camada de difus˜ao e uma camada de nitretos. O processo, melhora a resistˆencia ao desgaste, dureza e a resistˆencia `a corros˜ao da liga [1].
Outro m´etodo que pode ser aplicado para aumentar a resistˆencia ao desgaste do subs-trato de titˆanio e suas ligas ´e a utiliza¸c˜ao de revestimentos duros, tal como os filmes de carbono amorfo. A produ¸c˜ao desses filmes come¸cou no fim da d´ecada de 60 e desde ent˜ao estes filmes vem sendo obtidos por diferentes t´ecnicas de deposi¸c˜ao [2] para as mais vari-adas aplica¸c˜oes. Esses filmes s˜ao muito utilizados devido `as suas excelentes propriedades como in´ercia qu´ımica, excelente resistˆencia `a corros˜ao e ao desgaste, elevada dureza, bio e hemocompatibilidade. Al´em disso, estes revestimentos atuam como uma barreira de prote¸c˜ao que impedem a libera¸c˜ao de ´ıons da liga de Ti6Al4V ou de outros substratos em meio aquoso.
2 Materiais
2.1
Ti6Al4V e Ti6Al4V Nitretado
Nas ´ultimas d´ecadas a utiliza¸c˜ao de biomateriais para as mais diversas aplica¸c˜oes, tais como pr´oteses para o corpo humano e fabrica¸c˜ao de dispositivos m´edicos, vem sendo es-tudada devido `a necessidade das diversas ´areas de aplica¸c˜ao tais como: patologias ´osseas, repara¸c˜ao de traumatismo, est´etica bucal, entre outros. Devido `a grande utiliza¸c˜ao dos biomateriais e a importante fun¸c˜ao que desempenham, existe a necessidade de desenvolvi-mento e aprimoradesenvolvi-mento dos biomateriais e dispositivos que possam melhorar a qualidade de vida dos pacientes.
O titˆanio e suas ligas s˜ao amplamente usados na biomedicina, especialmente na subs-titui¸c˜ao de ossos, implantes dent´arios e cardiovasculares. A aplica¸c˜ao do titˆanio para tais finalidades se deve `as suas excelentes propriedades tais como: resistˆencia `a corros˜ao, formabilidade, boa resistˆencia `a fadiga, m´odulo el´astico relativamente baixo e boa bio-compatibilidade.
As aplica¸c˜oes mais comuns de titˆanio e suas ligas s˜ao em substitui¸c˜ao de articula¸c˜ao do quadril e joelho, que consistem em componentes do fˆemur, t´ıbia e patela. Tamb´em s˜ao usados em implantes dent´arios, que podem ser classificados como tais: subperiosteal, transosteal e end´ossea de acordo com sua posi¸c˜ao e forma, al´em de ser utilizado em quase todas as situa¸c˜oes, como implantes individuais para substitui¸c˜ao de um dente perdido, assim como em casos de edentulismo parcial e total.
Outra grande aplica¸c˜ao do titˆanio e suas ligas na medicina s˜ao em pr´otese de v´alvula de cora¸c˜ao, capas de prote¸c˜ao de marcapasso, cora¸c˜oes artificiais e dispositivos circulat´orios.
Os cora¸c˜oes artificiais feitos inteiramente de titˆanio n˜ao s˜ao bem sucedidos devido a problemas de coagula¸c˜ao sangu´ınea. Nesse caso, outros tipos de pr´oteses de v´alvulas card´ıacas s˜ao usadas na medicina. Um exemplo de pr´otese ´e apresentada na (Figura 2.1), na qual as v´alvulas card´ıacas s˜ao revestidas com um filme fino de carbono para melhorar a compatibilidade com o sangue [3].
Figura 2.1: V´alvula artificial do cora¸c˜ao [3].
O titˆanio e suas ligas s˜ao tamb´em materiais atrativos para implantes de osteoss´ıntese. Estes tem a fun¸c˜ao de reunir mecanicamente os fragmentos ´osseos de uma fratura, por interm´edio de uma pe¸ca met´alica, que permite a consolida¸c˜ao pela forma¸c˜ao do calo. O t´ıpico implante para osteoss´ıntese inclui parafusos e placas ´osseos e maxilofaciais (Figura 2.2). Al´em disso, um revestimento para melhorar as propriedades s˜ao os fosfatos de c´alcio bioativas (hidroxiapatite) que ajudam na fixa¸c˜ao ´ossea, reduz a libera¸c˜ao de ´ıons met´alicos e melhora o processo de cicatriza¸c˜ao.
O titˆanio e suas ligas tamb´em possuem uma s´erie de aplica¸c˜oes em tecnologia de ponta na ind´ustria, entre muitas aplica¸c˜oes pode-se citar tais como: componentes de turbinas a g´as; vasos de press˜ao aeroespaciais; materiais estruturais nas ind´ustrias aeron´autica, au-tomobil´ıstica e marinha; em carca¸cas de submarinos; containers de lixo nuclear; m´ısseis e pe¸cas de artilharia; estruturas de suporte para sistemas ´oticos; bens de consumo (pulseiras de rel´ogio, tacos de golfe, etc.), entre outras [4].
O titˆanio e suas ligas s˜ao excelentes materiais para aplica¸c˜ao na biomedicina, entre-tanto eles apresentam algumas limita¸c˜oes, o que reduz o seu espectro de aplica¸c˜ao especi-almente quando se faz necess´ario boas propriedades tribol´ogicas. As principais limita¸c˜oes s˜ao a baixa dureza comparado com as ligas de cobalto-cromo e a¸co inoxid´avel, e baixa resistˆencia ao desgaste [5]. Al´em disto, quando o material est´a sujeito ao desgaste e cor-ros˜ao simultˆaneos, como no caso de juntas de quadril e joelho, a corcor-ros˜ao ´e acelerada pelo desgaste e o desgaste ´e afetado pela corros˜ao gerando um mecanismo de degrada¸c˜ao complexo.
Estes problemas podem ser contornados utilizando-se tecnologias de melhoramento su-perficial ou recobrimento. Dentre eles podemos citar a nitreta¸c˜ao, revestimento de car-bono amorfo sobre a superf´ıcie do titˆanio, filme de nitreto de titˆanio sobre o titˆanio entre outras. Estes procedimentos s˜ao normalmente usados para o tratamento e modifica¸c˜ao de superf´ıcies, aumentando assim sua dureza, resistˆencia ao desgaste e a resistˆencia `a corros˜ao.
2.2
Filmes de Carbono Amorfo
Os filmes de carbono amorfo constituem uma ampla gama de revestimentos, os quais cont´em diferentes propor¸c˜oes de carbono sp2
e sp3
Dentre os filmes de carbono amorfo temos diferentes classes de revestimentos como o carbono amorfo tetra´edrico (ta-C), que tem um conte´udo elevado de liga¸c˜ao sp3
, e os carbonos amorfos hidrogenados, que s˜ao classificados em quatro tipos [6].
1 -a-C:H com a maior quantidade de H incorporado (40−60 %at). Estes filmes podem ter at´e 70 % de liga¸c˜oes sp3
. Entretanto a maioria das liga¸c˜oes sp3
s˜ao terminadas por hidrogˆenio e este material ´e macio e de baixa densidade. Este material ´e chamado de “polymer-like”a-C:H (PLCH).
2 - a-C:H com concentra¸c˜ao intermedi´aria de H (20−40 %at). Mesmo que estes filmes tenham um conte´udo total menor de sp3
, eles possuem mais liga¸c˜oes C-C sp3
que os PLCH. Logo, eles possuem melhores propriedades mecˆanicas. Estes filmes s˜ao chamados de “diamond-like carbon”a-C:H (DLCH).
3 - ta-C:H s˜ao filmes de carbono amorfo tetra´edrico hidrogenado. S˜ao uma classe de DLCH na qual a quantidade de sp3
mantˆem-se a concentra¸c˜ao de H fixa.
4 - a-C:H com baixa concentra¸c˜ao de H, menor que 20 %at. Estes possuem alta quan-tidade de sp2
. S˜ao filmes chamados de “graphite-like”a-C:H (GLCH).
O diagrama de fase tern´ario apresentado na (Figura 2.3) mostra a forma¸c˜ao de filmes de carbono amorfo com rela¸c˜ao `a quantidade de liga¸c˜ao sp2
,sp3
e o hidrogˆenio.
Figura 2.3: Diagrama de fase tern´ario para filmes de carbono amorfo com rela¸c˜ao `a quantidade de liga¸c˜ao sp2
, sp3
2.3
Aplica¸c˜
ao de Filmes de Carbono Amorfo
Um revestimento muito promissor no setor biol´ogico e na ind´ustria ´e o DLC (diamond-like carbon). Ele ´e um hidrocarboneto inerte, imperme´avel, com propriedades adequadas para aplica¸c˜ao de revestimento em v´arias ligas met´alicas. Al´em disso, possui uma mi-croestrutura que permite a incorpora¸c˜ao de outros elementos qu´ımicos tais como titˆanio, nitrogˆenio, sil´ıcio, tungstˆenio, prata entre outros, o que melhora a qualidade do reves-timento, como por exemplo, a prote¸c˜ao qu´ımica, o desgaste, fric¸c˜ao do revestimento e aderˆencia [7, 8].
Os filmes de carbono amorfos do tipo a-C:H tem sido aplicados na tecnologia de arma-zenamento magn´etico para prote¸c˜ao contra corros˜ao da m´ıdia magn´etica gravada [9]. Este filme tamb´em ´e utilizado como camada de revestimento interno em dutos de transporte de petr´oleo, o que proporciona uma vida ´util maior para a tubula¸c˜ao [10].
Em 1998 foi lan¸cado no mercado as lˆaminas de barbear da marca Gillete, na qual as bordas s˜ao revestidas com 150 nm de filme de carbono do tipo ta-C. Al´em dessas aplica¸c˜oes o uso de revestimentos com filmes DLC ´e utilizados em v´arias ferramentas de corte, incluindo instrumentos cir´urgicos, tais como agulhas cir´urgicas para transplantes de c´ornea e opera¸c˜oes de cataratas. Esses filmes tamb´em tˆem grande aplica¸c˜ao na ind´ustria automobil´ıstica, tˆextil, biom´edicas, entre outras aplica¸c˜oes [11, 12].
2.4
Resvestimentos de Carbono Amorfo sobre o Titˆ
anio
e suas Ligas
Segundo Love et al.[7] um dos maiores obst´aculos na utiliza¸c˜ao de revestimentos de filmes de carbono amorfo ´e que estes apresentam um elevado n´ıvel de tens˜ao interna, as quais s˜ao desenvolvidas durante o processamento de revestimento, especialmente aqueles com altos ´ındices sp3
ou sp2
. Revestimentos com 90 % de sp3
tem sido relatado ter uma tens˜ao interna perto de 10 GPa, enquanto revestimentos de (a-C:H) com elevadas quantidades de hidrogˆenio e liga¸c˜ao sp2
na estrutura do carbono com pouco ou nenhuma estruturas sp3
normalmente tˆem a menor tens˜ao interna, ou seja menor que um GPa. Revestimentos com tens˜oes internas elevadas, ou seja maior que um GPa s˜ao propensos a uma delamina¸c˜ao levando a uma falha catastr´ofica do filme.
Park et al.[14] mostram que a porosidade ou defeitos no filme s˜ao as principais vias de acesso do meio aquoso `a interface filme/substrato, a qual acaba sendo degradada e o filme delaminado.
Ainda pesquisas comprovam que os filmes de carbono amorfo em titˆanio e suas ligas tˆem ampla aplicabilidade, mas eles podem sofrer falhas que devem ser analisadas cui-dadosamente. Manhabosco et al. [1] mostaram a ocorrˆencia de falha catastr´ofica em filmes GLCH depositados sobre a liga Ti6AL4V e a liga nitretada quando testados em ensaios de tribocorros˜ao. Essas falhas est˜ao relacionadas com a penetra¸c˜ao de ´agua e ´ıons atrav´es dos poros que podem levar `a perda de ades˜ao entre o substrato e o filme GLCH e/ou `a degrada¸c˜ao da interface do filme GLCH/substrato devido `a a¸c˜ao da carga aplicada no ensaio e do meio corrosivo. Park et al. [14] mostraram que a falha catastr´ofica de filmes de carbono amorfo do tipo DLC em meio aquoso pode ser minimizada utilizando-se a deposi¸c˜ao PACVD em passos. Este tipo de procedimento proporciona a forma¸c˜ao de filmes com poros n˜ao passantes, o que impede a penetra¸c˜ao da ´agua at´e a interface revestimento/substrato e consequentemente sua degrada¸c˜ao.
2.5
Corros˜
ao dos Metais
n˜ao met´alicos. Por exemplo, a deteriora¸c˜ao da tinta e da borracha sob exposi¸c˜ao `a luz solar ou produtos qu´ımicos, o ataque de um metal s´olido por outro metal fundido s˜ao todos considerados corros˜ao. Em geral, a corros˜ao se d´a do ponto de vista qu´ımico e eletroqu´ımico.
A corross˜ao pode ocorrer de forma r´apida ou lenta, dependendo das condi¸c˜oes ambien-tais e do tipo de material que est´a sob o efeito corrosivo . Por exemplo, o a¸co inoxid´avel em meio `acido ´e danificado em horas, j´a os trilhos de trem geralmente apresentam ferru-gem, mas n˜ao ´e suficiente para afetar o seu desempenho ao longo de muitos anos. Ainda a corross˜ao dos metais pode ser considerado com processo inverso da metalurgia extrativa, em que o metal retorna ao seu estado original [15].
O titˆanio ´e um metal extremamente reativo e possui uma alta afinidade por oxigˆenio, quando este ´e exposto ao ar ou ´agua sofre corros˜ao levando ao crescimento espontˆaneo do filme ´oxido sobre a superf´ıcie do substrato que pode estar relacionado nas seguintes estruturas: TiO, T i2O3 ouT iO2, sendo que o filme de di´oxido de titˆanio (T iO2) ´e o mais
comum [16].
A compatibilidade que o titˆanio e suas ligas tem com oxigˆenio, limitam suas aplica¸c˜oes como materiais estruturais `a altas temperaturas. A solubilidade s´olida do oxigˆenio no titˆanio resulta em perda de material e na forma¸c˜ao de uma fr´agil camada de ´oxido durante a exposi¸c˜ao ao ar em elevadas temperaturas. A reatividade do titˆanio com o nitrogˆenio ´e parecida com a do oxigˆenio, onde uma camada de nitreto ´e formada na superf´ıcie do substrato [17].
´
E v´alido ressaltar que o titˆanio e suas ligas tamb´em podem sofrer com diferentes tipos de corros˜ao, como por exemplo, a corros˜ao por fresta e pites, principalmente em implantes biom´edicos [18, 19].
Em temperatura ambiente forma-se sobre o titˆanio e suas ligas um filmeT i02, filme este
3 T´
ecnicas de Modifica¸c˜
ao Superficial
3.1
T´
ecnica de Obten¸c˜
ao de Filmes de Carbono Amorfo
Hidrogenado
Para a obten¸c˜ao dos filmes de carbono amorfo hidrogenado pode-se recorrer a uma diversidade de t´ecnicas de deposi¸c˜ao, das quais podemos citar: Deposi¸c˜ao Qu´ımica por Vapor (CVD), Deposi¸c˜ao F´ısica por Vapor (PVD), Deposi¸c˜ao Qu´ımica por Vapor Assis-tida por Plasma (PACVD), Deposi¸c˜ao Eletroqu´ımica, entre outras.
A t´ecnica CVD ´e um processo vers´atil para obten¸c˜ao de revestimentos. Com essa t´ecnica ´e poss´ıvel fazer deposi¸c˜ao em metais, elementos n˜ao met´alicos e tamb´em em compostos como cabonetos, nitretos, ´oxidos, compostos intermet´alicos e muitos outros.
Atrav´es da t´ecnica de deposi¸c˜ao CVD ´e poss´ıvel obter filmes finos de carbono amorfo ao longo de todo material. A t´ecnica CVD geralmente utiliza elevadas temperaturas em seu processo, entretanto com a utiliza¸c˜ao de plasma ´e poss´ıvel a redu¸c˜ao da temperatura do processo, o que possibilita melhorar as caracter´ısticas espec´ıficas do revestimento e permite que metais que sofreriam transi¸c˜oes de fase no CVD convencional possam rece-ber filmes sem altera¸c˜ao de suas propriedades. Essa t´ecnica consiste, basicamente, na introdu¸c˜ao de reagentes gasosos no interior de um reator (cˆamara de deposi¸c˜ao) que le-vam `a ocorrˆencia de rea¸c˜oes qu´ımicas na superf´ıcie do material a ser revestido, ocorrendo assim “crescimento”do revestimento sobre o substrato [24, 25].
neste ´e aplicado a r´adio-frequˆencia (RF), e o outro eletrodo ´e a carca¸ca da cˆamara, a qual ´e mantida aterrada. O plasma ´e gerado por colis˜oes dos el´etrons acelerados pelo campo de RF com ´atomos e/ou mol´eculas da atmosfera precursora e acarreta na polariza¸c˜ao negativa do eletrodo. Uma bainha de plasma com excesso de ´ıons ´e criada pr´oxima dos eletrodos, sendo observada uma diferen¸ca de potencial entre o plasma e o eletrodo, onde a bainha ter´a polariza¸c˜ao positiva com rela¸c˜ao ao eletrodo. Com isso, os ´ıons positivos s˜ao transportados na dire¸c˜ao do substrato durante a deposi¸c˜ao, propiciando uma adsor¸c˜ao e bombardeio por ´ıons como, por exemplo, os ´ıons CH+
3 respons´aveis pelas propriedades e
crescimento dos filmes [25, 26, 27].
A t´ecnica PVD consiste num grupo de t´ecnicas de deposi¸c˜ao, as quais tem em comum o fato de permitirem o transporte de material, na fase vapor, entre o material do alvo e o substrato a ser revestido. Este processo ocorre numa cˆamara rarefeita [28]. Dentre as principais t´ecnicas PVD temos a evapora¸c˜ao e o “sputtering”[25, 29].
O processo de evapora¸c˜ao consiste no aquecimento do material que se deseja evaporar at´e alcan¸car a fase vapor e em seguida condensa na superf´ıcie do substrato. Algumas das t´ecnicas de revestimento por evapora¸c˜ao s˜ao: evapora¸c˜ao por feixe de el´etrons, evapora¸c˜ao por arco el´etrico, evapora¸c˜ao por efeito Joule, entre outras.
O processo de revestimento por “sputtering” consiste no bombardeamento do material do alvo com part´ıculas energ´eticas. Atrav´es deste bombardeamento ocorre o transporte do material para fase vapor que depositar˜ao no substrato formando o revestimento.
No grupo da t´ecnica de “sputtering”destacam-se a pulveriza¸c˜ao com magnetron, pul-veriza¸c˜ao com feixes de ´ıons, pulpul-veriza¸c˜ao por r´adio frequˆencia, pulpul-veriza¸c˜ao cat´odica, dentre outras.
As t´ecnicas de “sputtering”permitem obter filmes uniformes, com superf´ıcies suaves e os revestimentos apresentam boa ades˜ao [27].
feito a temperatura ambiente, n˜ao necessita de sistema a v´acuo, ´e bastante vers´atil para a produ¸c˜ao de uma infinidade de revestimentos. Nesta t´ecnica, a deposi¸c˜ao do revestimento ocorre por meio de rea¸c˜oes qu´ımicas que s˜ao produzidas pela passagem de uma corrente el´etrica. A eletrodeposi¸c˜ao de materiais pode ser realizada a partir de diferentes eletr´olitos, tais como solventes orgˆanicos, solu¸c˜ao iˆonica, meio de sais fundidos e l´ıquidos i´onicos [30].
A eletrodeposi¸c˜ao com solu¸c˜ao orgˆanica possibilita um processo bastante prop´ıcio para a obten¸c˜ao de filmes de DLC, j´a que pode ser aplicada a diferentes substratos condutores ou semincondutores sem a utiliza¸c˜ao de sistema a v´acuo e aplica¸c˜ao de altas tempera-turas. Na pesquisa de Namba [31], os mesmos relatam que os filmes de DLC podem ser obtidos/separados por eletr´olise em uma solu¸c˜ao orgˆanica de etanol e recentemente, segundo Wang et al. [32] os l´ıquidos orgˆanicos como acetonitrila e N-N dimetilformamida s˜ao utilizados tamb´em para obter filmes de carbono.
Um exemplo esquem´atico de diagrama para sistema de deposi¸c˜ao de filmes de DLC ´e mostrado na (Figura 3.1).
Figura 3.1: Esquema de um diagrama para sistema de deposi¸c˜ao de filmes de DLC [31].
espessura da pel´ıcula atrav´es de carga transferida durante de eletr´olise [33].
3.2
T´
ecnica de Nitreta¸c˜
ao
A nitreta¸c˜ao ´e um procedimento usado normalmente para o incremento das proprie-dades superficiais de superf´ıcies met´alicas. Esse processo consiste da difus˜ao de ´atomos de nitrogˆenio da superf´ıcie do metal para seu interior, ocorrendo o enriquecimento super-ficial com hidrogˆenio e podendo ocorrer a forma¸c˜ao de nitretos. Ap´os o tratamento de nitreta¸c˜ao ocorrem altera¸c˜oes na liga met´alica como, por exemplo: aumento da dureza superficial, aumento da resistˆencia ao desgaste, aumento da resistˆencia `a corros˜ao e uma vida ´util maior, o que proporciona uma melhor qualidade nos metais e suas ligas [34, 35].
Atualmente na literatura existem diversas t´ecnicas de nitreta¸c˜ao que envolve os m´etodos f´ısicos e qu´ımicos. Dentre os mais conhecidos est˜ao a nitreta¸c˜ao em meio l´ıquido (banho de sal) e em meio gasoso, esses relacionam ao m´etodo qu´ımico; a nitreta¸c˜ao a plasma ´e por m´etodo f´ısico.
A nitreta¸c˜ao em banho de sal ´e ainda uma das mais utilizadas por ser um processo, a princ´ıpio, simples e que pode obter camadas mais espessas. A pe¸ca ´e mergulhada em um banho de sais fundidos com temperatura na faixa de 530 a 6500
C, constitu´ıdo principalmente de cianetos e cianatos (N aCN, KCN, N aCN O, KCN O, N a2CO3, etc).
Ap´os o tempo de permanˆencia, que pode variar de 2 h at´e 20 h, o material ´e retirado e resfriado com um jato de ´agua para auxiliar na remo¸c˜ao dos sais da superf´ıcie, j´a que este se adere principalmente a cantos, quinas e furos. A camada formada raramente ultrapassa 600µm. Em aplica¸c˜oes industriais, a espessura tipicamente encontra-se entre 100µm e300µm [36].
O processo de nitreta¸c˜ao em meio gasoso ocorre quando as pe¸cas s˜ao colocadas em uma grande cˆamara sob v´acuo, onde ´e adicionado g´as amˆonia (N H3) que ´e mantido a
temperaturas na faixa de 5000
C e 5700
dissocia¸c˜ao para 65% a 85%, em geral alternando entre esse valor e a dissocia¸c˜ao comum para um melhor resultado. Mesmo assim, o tempo de tratamento chega aproximadamente a 30 h [36].
O processo conhecido por nitreta¸c˜ao iˆonica, nitreta¸c˜ao por descarga luminosa ou ni-treta¸c˜ao por plasma, representa uma nova alternativa aos processos convencionais que usam g´as ou banho de sais fundidos, geralmente t´oxicos. Essa t´ecnica de plasma ´e limpa, segura e relativamente simples de usar, sendo cada vez mais comum em aplica¸c˜oes indus-triais.
A utiliza¸c˜ao da nitreta¸c˜ao a plasma tem algumas vantagens como:
• Incremento de vida ´util das pe¸cas tratadas;
• Boa penetra¸c˜ao do plasma em complicadas geometrias permitindo nitreta¸c˜ao uni-forme;
• Bom controle da uniformidade da espessura e qualidade da camada nitretada;
• Redu¸c˜ao de uso de gases;
• Redu¸c˜ao do custo de manufatura, eliminando opera¸c˜oes de ret´ıfica e usinagem para corre¸c˜ao de deforma¸c˜oes estruturais;
• Elimina¸c˜ao da agress˜ao ambiental uma vez que o processo de nitreta¸c˜ao com plasma trabalha com g´asH2 e N2, eliminando o uso de gases corrosivos, poluentes e de dif´ıcil
manuseio;
• Economia de energia el´etrica.
O equipamento t´ıpico de nitreta¸c˜ao por plasma ´e constitu´ıdo basicamente por um sis-tema de v´acuo, uma fonte de potˆencia e um reator, como mostra a Figura 3.2.
O sistema a v´acuo possui uma v´alvula para controlar a vaz˜ao dos gases introduzidos no tratamento. J´a a fonte de tens˜ao possui uma sa´ıda de corrente continua (DC) com uma voltagem m´axima de aproximadamente 1500 V e uma corrente capaz de fornecer energia a pe¸ca para que ela seja aquecida a uma temperatura de 300 a 6000
dois eletrodos onde o catodo ´e tamb´em o porta amostra. Ainda no reator devem existir sa´ıdas para medida da press˜ao, temperatura e outras vari´aveis desejadas para o melhor controle do processo. ´E tamb´em necess´ario a entrada de atmosfera nitretante, bomba de v´acuo e outros acess´orios que sejam necess´arios para a nitreta¸c˜ao da amostra. Aplica-se uma diferen¸ca de potencial entre os eletrodos de 400 e 1200 V e ent˜ao Aplica-se introduz o g´as nitretante (tipicamente uma mistura de (N2 e H2) no reator at´e atingir a press˜ao
de trabalho (1-20 torr)) [37]. `A medida que a press˜ao aumenta, os ´ıons de nitrogˆenio s˜ao acelerados e bombardeiam a superf´ıcie da amostra, provocando assim, a difus˜ao de nitrogˆenio na superf´ıcie da amostra, e consequentemente o processo de nitreta¸c˜ao.
4 T´
ecnicas de Caracteriza¸c˜
ao
4.1
Microscopia Eletrˆ
onica de Varredura
A Microscopia Eletrˆonica de Varredura (MEV) ´e uma t´ecnica de caracteriza¸c˜ao pode-rosa, que permite a an´alise microestrutural de materiais s´olidos. A superf´ıcie da amostra pode ou n˜ao estar polida e atacada quimicamente, por´em a amostra deve ser condutora de eletricidade. No caso de materiais n˜ao condutores deve ser aplicado um revestimento condutor muito fino para a an´alise, geralmente usa-se um filme fino de ouro ou carbono.
Esta t´ecnica alcan¸ca aumentos muito superiores ao de um microsc´opio ´optico, s˜ao poss´ıveis amplia¸c˜oes que variam entre 10e mais de50.000 vezes. Esse aumento da re-solu¸c˜ao de imagem ´e devido `a amostra ser analisada por um fino feixe de el´etrons ao inv´es da radia¸c˜ao da luz [38].
Ap´os a intera¸c˜ao do feixe de el´etrons com a superf´ıcie da amostra pode ocorrer a emiss˜ao de uma s´erie de radia¸c˜oes tais como: el´etrons secund´arios, el´etrons retroespalhados, raios X caracter´ısticos, el´etrons Auger, f´otons, entre outros.
Na microscopia eletrˆonica de varredura os sinais de maior interesse para a forma¸c˜ao da imagem s˜ao os el´etrons secund´arios e os retroespalhados. `A medida que o feixe de el´etrons prim´arios vai varrendo a amostra estes sinais v˜ao sofrendo modifica¸c˜oes de acordo com as varia¸c˜oes da superf´ıcie. Os el´etrons secund´arios fornecem imagem de topografia da superf´ıcie da amostra e s˜ao os respons´aveis pela obten¸c˜ao das imagens de alta resolu¸c˜ao, j´a os retroespalhados fornecem imagem caracter´ıstica de varia¸c˜ao de composi¸c˜ao.
a amostra. Logo acima da lente objetiva existem dois est´agios de bobinas eletromagn´eticas respons´aveis pela varredura do feixe sobre a amostra.
Figura 4.1: Esquema do princ´ıpio de funcionamento da coluna MEV [39].
O feixe emitido interage com a amostra e a intera¸c˜ao pode chegar a uma profundidade que pode variar de 1µm a 6µm, dependendo da natureza da amostra e condi¸c˜oes de opera¸c˜ao do equipamento. Esta regi˜ao de intera¸c˜ao, conhecida por volume de intera¸c˜ao, ´e a regi˜ao a partir da qual s˜ao gerados os sinais que s˜ao detectados e utilizados para a forma¸c˜ao de imagem e para microan´alise.
A t´ecnica de microscopia eletrˆonica de varredura possibilita caracterizar a morfologia do material e a composi¸c˜ao qu´ımica tanto de materiais macios como tamb´em de filmes [27].
4.2
Microscopia de For¸ca Atˆ
omica
O principio b´asico de funcionamento desta t´ecnica ´e mostrado na Figura 4.2. Uma pequena ponta, com raio de aproximadamente 2 a 40 nm, presa a um cantilever flex´ıvel varre a superf´ıcie da amostra. As irregularidades da superf´ıcie promovem deflex˜oes no cantilever que s˜ao captadas por um sistema de laser que est´a focado na parte de tr´as do cantilever. O laser ´e refletido, atrav´es de espelhos, at´e um fotodector que capta as varia¸c˜oes do laser causadas pelas irregularidades da amostra, as quais s˜ao interpretadas por um sistema computacional e transformadas em imagem.
Figura 4.2: Diagrama representativo de funcionamento do microsc´opio de for¸ca atˆomica [40].
A t´ecnica de AFM pode ser efetuada em trˆes modos distintos: contato, n˜ao contato e intermitente.
No modo contato, a sonda que varre a superf´ıcie ´e mantida a uma distˆancia de poucos ˆangstrons da superf´ıcie da amostra, havendo ent˜ao uma repuls˜ao eletrˆonica. Nesse modo a ponta arrasta sobre a superf´ıcie da amostra e as irregularidades da superf´ıcie provocam a deflex˜ao no cantilever.
A an´alise por modo contato possibilita uma melhor topografia da amostra, mas existe a possibilidade de danificar a ponta e/ou a amostra.
Como n˜ao existe contato da sonda com a amostra evita-se danificar a amostra ou a sonda. Entretanto a resolu¸c˜ao ´e geralmente menor do que no modo de contato.
O modo intermitente ´e utilizado para amostras que podem ser facilmente danificadas ou para amostras que tem dificuldade de serem analisadas pelos outros dois m´etodos. Neste processo a ponta constantemente toca a superf´ıcie ocorrendo for¸cas de atra¸c˜ao e repuls˜ao. O cantilever chega a uma frequˆencia de ressonˆancia da ordem de 50.000 a 5000.000 Hz. Com este modo de opera¸c˜ao pode-se chegar a uma alta resolu¸c˜ao a ainda prevenir a danifica¸c˜ao da amostra e da ponta [41].
Al´em das aplica¸c˜oes citadas, a microscopia de for¸ca atˆomica permite a obten¸c˜ao de curvas de for¸ca em fun¸c˜ao da distˆancia entre a ponta e a amostra. As curvas de for¸ca s˜ao a representa¸c˜ao gr´afica da for¸ca aplicada `a ponta enquanto a amostra ´e aproximada e afastada. O sistema, na verdade, n˜ao mede for¸cas e sim as deflex˜oes do cantilever. Medidas das deflex˜oes em fun¸c˜ao da posi¸c˜ao da amostra ao longo do eixo z s˜ao obtidas durante o movimento vertical de aproxima¸c˜ao e afastamento do piezoel´etrico em rela¸c˜ao `a ponta.
`
A medida que a separa¸c˜ao entre a ponta e amostra torna-se pequena o suficiente para que for¸cas atrativas de van der Waals atuem, a ponta mergulha em dire¸c˜ao `a superf´ıcie, flexionando o cantilever para baixo. Uma vez estabelecido o contato, o cantilever sofre deflex˜ao idˆentica `a expans˜ao do piezoel´etrico. Depois de atingir o deslocamento m´aximo, o scanner inicia o caminho inverso, puxando a ponta aderida `a superf´ıcie da amostra at´e soltar. As for¸cas s˜ao calculadas a partir da deflex˜ao do cantilever (∆Z), o qual possui uma constante de mola k, usando a lei de Hooke F =k.∆Z.
4.3
Espectroscopia Raman
como `a presen¸ca de ´agua.
Do feixe de luz monocrom´atica que incide na amosta, uma parte da luz ´e transmitida, uma parte absorvida e a outra espalhada. A maior parte da luz espalhada tem o mesmo comprimento de onda da luz incidente. Uma pequena fra¸c˜ao da luz espalhada interage com a mol´ecula do material, no estado vibracional fundamental, levando-a a um estado energ´etico intermedi´ario. Temos ent˜ao dois tipos de intera¸c˜ao. O primeiro tipo n˜ao envolve troca de energia entre o f´oton incidente e as mol´eculas ou ´atomos da mat´eria, fazendo com que o f´oton espalhado tenha a mesma energia da luz incidente. Este tipo de espalhamento ´e de natureza el´astica e conhecida como espalhamento Rayleigh. O segundo tipo de intera¸c˜ao envolve transferˆencia de energia entre o f´oton incidente e as mol´eculas do material investigado. Isso faz com que o f´oton espalhado apresente uma frequˆencia diferente daquela presente no f´oton incidente, sendo que esta energia pode ser equivalente `a soma ou `a diferen¸ca entre as frequˆencias do f´oton incidente e a frequˆencia natural das esp´ecies termicamente excitadas no material. Este tipo de espalhamento ´e inel´astico e conhecido como Espalhamento Raman [42].
Ap´os a luz monocrom´atica interagir com a amostra pode ocorrer dois tipos de espalha-mento Raman: Stokes e anti- Stokes.
Quando, ap´os a intera¸c˜ao do f´oton incidente com a mol´ecula, a mol´ecula volta para um n´ıvel mais elevado de vibra¸c˜ao, o f´oton emitido tem menos energia e, por conseguinte, um comprimento de onda maior do que o f´oton inicial. A energia vibracional da mol´ecula ´e aumentada, esse evento ´e chamado de espalhamento Raman Stokes.
Quando a mol´ecula retorna para um n´ıvel vibracional mais baixo, o f´oton emitido tem mais energia, entretanto, um comprimento de onda menor do que o f´oton inicial. Nesse caso a energia vibracional da mol´ecula diminui e o comportamento ´e chamado de espalhamento Raman anti-Stokes. [43].
Figura 4.3: Origem dos espalhamentos Rayleigh e Raman [42].
A aplica¸c˜ao dessa t´ecnica ´e essencialmente para analise qualitativa e quantitativa dos materiais, al´em de permitir a descri¸c˜ao de materiais similares como, por exemplo, o car-bono que exibe diferentes arranjos estruturais tais como a estrutura da grafite e do dia-mante, e a mais recente a estrutura do fulereno e nanotubos de carbono.
A (Figura 4.4) ilustra um espectro Raman de um filme amorfo de carbono do tipo a-C:H obtido pela t´ecnica de PACVD para um plasma de metano. Nestes espectros pode-se observar duas bandas caracter´ısticas denominadas bandas G e D, localizadas em comprimento de onda de aproximadamente 1560cm−1
e 1350cm−1
[43].
4.4
Espectroscopia de Impedˆ
ancia Eletroqu´ımica
A t´ecnica de espectroscopia de impedˆancia eletroqu´ımica (EIE) ´e uma ferramenta em-pregada na caracteriza¸c˜ao de materiais no qual a condu¸c˜ao iˆonica predomina. A t´ecnica pode ser utilizada para estudo de materiais s´olidos e eletr´olitos l´ıquidos, pol´ımeros, vidros ionicamente condutores, c´elulas combust´ıveis, baterias recarreg´aveis e corros˜ao.
A impedˆancia ´e geralmente medida atrav´es da aplica¸c˜ao de uma diferen¸ca de potencial alternada (AC) na c´elula eletroqu´ımica e ent˜ao capta-se a corrente que flui atrav´es dos eletrodos. Assumindo-se que uma excita¸c˜ao de potencial senoidal ´e aplicada, a resposta ser´a um sinal de corrente alternado. Este sinal de corrente alternado pode ser analisado como a soma de fun¸c˜oes senoidais (uma s´erie de Fourrier).
A espectroscopia de impedˆancia eletroqu´ımica normalmente ´e medida utilizando-se uma pequena excita¸c˜ao para garantir uma resposta pseudo-linear. Na resposta pseudo-linear, a corrente de resposta a um potencial senoidal ser´a uma sen´oide de mesma frequˆencia, mas defasado de uma fase (ˆangulo). O sinal de excita¸c˜ao senoidal pode ser expresso como:
Et =E0sin(ωt) (4.1)
Onde, Et ´e o potencial em um tempo t, E0 ´e a amplitude do sinal e ω ´e a frequˆencia
angular. A rela¸c˜ao entre frequˆencia angular ω (rad/s) e frequˆencia f (Hz) ´e
ω= 2πf (4.2)
Em um sistema linear ou pseudo-linear, o sinal de resposta, It, est´a deslocado de uma
fase (φ) e tem uma amplitude diferente (I0).
It =I0sin(ωt+φ) (4.3)
A impedˆancia (Z) do sistema ser´a dada por
Z = Et It
= E0sin(ωt) I0sin(ωt+φ)
=Z0
sin(ωt)
sin(ωt+φ) (4.4)
Pode-se expressar a impedˆancia como uma fun¸c˜ao complexa atrav´es da rela¸c˜ao de Euler:
Exp(jφ) = cosφ+jsenφ (4.5)
Assim o potencial pode ser escrito como:
Et=E0exp(jωt) (4.6)
A corrente pode ser escrita como:
It=I0exp(jωt−φ) (4.7)
Assim, a impedˆancia em termos de n´umeros complexos ´e representada como:
Z(ω) = E
I =Z0exp(jφ) = Z0(cosφ+jsinφ) (4.8)
Se a parte real da impedˆancia for plotada no eixo X de um gr´afico e a parte imagin´aria for plotada no eixo Y, obteremos a representa¸c˜ao gr´afica denominada diagrama de Nyquist (Figura 4.5). Neste diagrama a impedˆancia pode ser representada como um vetor de comprimento |Z|. O ˆangulo entre este vetor e o eixo x ´e comumente chamado de ˆangulo de fase (φ=arg Z). Note que neste gr´afico o eixo y ´e negativo e que em cada ponto do diagrama Nyquist temos impedˆancia a uma determinada frequˆencia. Pode-se observar que no lado direito do gr´afico temos baixa frequˆencia e no lado esquerdo do gr´afico temos frequˆencias mais elevadas. O semic´ırculo ´e caracter´ıstica de uma ´unica constante de tempo [44].
Outra representa¸c˜ao poss´ıvel ´e o diagrama de Bode no qual a impedˆancia total (|Z|=Z0)
e a fase s˜ao plotadas em fun¸c˜ao do logar´ıtimo da frequˆencia. O diagrama de Bode, di-ferentemente do diagrama de Nyquist, mostra informa¸c˜oes a respeito da frequˆencia. Na Figura 4.6 temos a representa¸c˜ao t´ıpica de um diagrama de Bode.
Figura 4.6: Gr´afico de Bode em fun¸c˜ao da constante de tempo [44].
4.4.1
Elementos de Circuito Comumente Encontrados em
Sis-temas Eletroqu´ımicos
Resistˆencia Eletr´olito
A resistˆencia da solu¸c˜ao utilizada em uma c´elula eletroqu´ımica ´e um fator que deve ser levado em considera¸c˜ao para a simula¸c˜ao do modelo equivalente da c´elula. A resistˆencia da solu¸c˜ao iˆonica depende da concentra¸c˜ao iˆonica, do tipo de ´ıons, temperatura e geometria da ´area na qual a corrente passa. Para uma ´area de eletrodo A, de comprimento L, com passagem de corrente uniforme, a resistˆencia ´e definida como:
R=ρL
A (4.9)
Onde ρ ´e a resistividade da solu¸c˜ao.
Capacitˆancia de Dupla Camada
capacitˆancia que ´e denominada capacitˆancia de dupla camada. O valor da capacitˆancia depende de diferentes vari´aveis como o potencial de eletrodo, temperatura, concentra¸c˜ao dos ´ıons, tipo de ´ıons, rugosidade superficial, etc. Para metais imersos em um eletr´olito esperam-se capacitˆancias da ordem de 20a60µF para cada cm2
de ´area [44].
Resistˆencia `a Polariza¸c˜ao
Em c´elulas em que ocorre corros˜ao uniforme o potencial de circuito aberto, o potencial ´e controlado pelo equil´ıbrio entre duas diferentes rea¸c˜oes eletroqu´ımicas: a rea¸c˜ao an´odica e a rea¸c˜ao cat´odica. No equil´ıbrio a taxa que a rea¸c˜ao an´odica ocorre ´e a mesma que a rea¸c˜ao cat´odica ocorre e o valor de corrente para cada uma das rea¸c˜oes ´e conhecido como corrente de corros˜ao. O potencial em que isto ocorre ´e chamado de potencial de corros˜ao ou potencial misto.
Quando existem somente duas rea¸c˜oes simples, a an´odica e a cat´odica, a corrente que flui ´e associada a potencial atrav´es da f´ormula:
I =Icorr(e
2,303(E−Eoc)
βa −e
−2,303(E−Eoc)
βc ) (4.10)
Onde I ´e a corrente medida na c´elula em amp´eres; Icor ´e a corrente de corros˜ao em
amp´eres; Eoc ´e o potencial de circuito aberto em volts; βa ´e o coeficiente an´odico Beta
em volts/d´ecada; βc ´e o coeficiente cat´odico Beta em volts/d´ecada. Aplicando-se uma
aproxima¸c˜ao para pequeno sinal, obtem-se a seguinte express˜ao:
Icor =
βaβc
2,303(βa+βc)
. 1 (Rp)
(4.11)
A equa¸c˜ao 4.11 introduz um novo parˆametro, a resistˆencia `a polariza¸c˜ao (Rp) que se
comporta como um resistor.
Resistˆencia `a Transferˆencia de Carga
Uma resistˆencia similar ´e formada por uma ´unica rea¸c˜ao eletroqu´ımica cineticamente controlada. Este ´e o exemplo de um metal dissolvendo em uma solu¸c˜ao de acordo com a equa¸c˜ao:
No caso citado cargas s˜ao transferidas; os el´etrons entram no metal enquanto que ´ıons met´alicos difundem para o eletr´olito. A transferˆencia de cargas ocorre a uma certa velo-cidade que depende do tipo de rea¸c˜ao, temperatura, concentra¸c˜ao dos produtos de rea¸c˜ao e potencial [44]. A rela¸c˜ao geral entre potencial e corrente, para concentra¸c˜ao de ´ıons no seio da solu¸c˜ao igual `a da superf´ıcie do eletrodo, ´e dada pela equa¸c˜ao de Butler-Volmer.
i=i0(exp(α
nF
RTη)−exp(−(1−α) nF
RTη) (4.13)
Onde i0 ´e a corrente de troca;α ´e a ordem da rea¸c˜ao;n, o n´umero de el´etrons envolvido;
F a constante de Faraday; η, sobrepotencial. Quando o sobrepotencial ´e muito pequeno e o sistema eletroqu´ımico est´a em equil´ıbrio, a express˜ao para a resistˆencia `a transferˆencia de carga ´e:
Rct =
RT nF i0
(4.14)
Capacitˆancia do Revestimento
Um capacitor ´e formado quando temos duas placas condutoras separadas por um meio diel´etrico. A capacitˆancia do mesmo pode ser dada pela express˜ao abaixo:
C = ε0εrA
d (4.15)
Onde ε0 ´e a permissividade eletrost´atica do v´acuo ou espa¸co livre; εr ´e a constante
diel´etrica ou permissividade relativa do isolante utilizado; A ´e a ´area da placa; d a distˆancia entre as placas [44].
Elemento de Fase Constante
Geralmente, em experimentos de espectroscopia de impedˆancia eletroqu´ımica, os ca-pacitores n˜ao se comportam idealmente. Ao inv´es disto, eles se comportam como um elemento de fase constante no qual a impedˆancia pode ser descrita como:
ZCP E =
1 (jω)αY
0
(4.16)
No qual, Y0 = C = capacitˆancia e α ´e uma constante emp´ırica que expressa o fato de
5 Materiais e M´
etodos
5.1
Confec¸c˜
ao dos Corpos de Prova
5.1.1
Prepara¸c˜
ao Superficial
Neste trabalhou utilizou- se como material substrato a liga Ti6Al4V(Gr.V-ASTM F136) com composi¸c˜ao especificada na Tabela 5.1. Amostras cil´ındricas da liga, com diˆametro de 38mm e altura de 17mm, foram obtidas a partir de um tarugo do material.
Tabela 5.1: Composi¸c˜ao da barra de Ti6Al4V conforme fornecedor (Gustoc-Alemanha) Elemento Composi¸c˜ao (%) p/p
N 0,004
C 0,004
H 0,0022
Fe 0,04
o 0,117
Al 5,97
V 4,03
Ti balan¸co
remo¸c˜ao do metanol.
5.1.2
Nitreta¸c˜
ao
Parte das amostras preparadas no processo anterior foram nitretadas a plasma pela empresa PLATEG (Siegen- Alemanha). Segundo informado a press˜ao na cˆamara foi de 300 P a, durante 10 horas com tens˜ao el´etrica pulsada. A temperatura foi de 1073K, abaixo da temperatura de transi¸c˜ao de fase α−β para a liga (1228K). A atmosfera gasosa para o processo era composta de: 10%Ar, 50%H2 e 40%N2.
5.1.3
Deposi¸c˜
ao de Filmes de Carbono Amorfo Hidrogenado do
Tipo Grafite (GLCH)
Os filmes GLCH foram depositados comercialmente pelo Instituto Fraunhofer (Braunschweig-Alemanha) utilizando a t´ecnica RF (13,56Hz) PACVD (deposi¸c˜ao qu´ımica por vapor assistido por plasma). Os filmes foram depositados tanto sobre a superf´ıcie da liga nua (GLCH/Ti6Al4V) como sobre a superf´ıcie da liga nitretada (GLCH/Ti6Al4Vnitretada).
Anteriormente `a deposi¸c˜ao, as amostras foram limpas fisicamente por sputtering, com argˆonio, a fim de remover contamina¸c˜oes e ´oxidos superficiais. A deposi¸c˜ao foi realizada a uma press˜ao de 1,5P a, a partir de g´as acetileno (C2H2) injetado a um fluxo de 50 sccm
(standard centimeter cubic per minute) por 2 horas. A voltagem negativa aplicada foi de 1000 V.
5.2
T´
ecnicas Eletroqu´ımicas
5.2.1
Polariza¸c˜
ao Potenciodinˆ
amica
Curvas de polariza¸c˜ao potenciodinˆamica foram obtidas para todos os tipos de amos-tras em solu¸c˜ao salina tamponada com fosfato (solu¸c˜ao PBS), a fim de simular o fluido corp´oreo. A solu¸c˜ao PBS ´e composta de 8 g/l NaCl; 0,2 g/l KCl; 0,594 g/l N a2HP O4, e
0,2 g/l KH2P O4, com pH = 7,1. Ensaios de polariza¸c˜ao potenciodinˆamica foram
reali-zados a uma taxa de varredura de 0,167 mV/s.
Os testes foram realizados em uma c´elula eletroqu´ımica composta por trˆes eletrodos: um eletrodo de calomelano saturado (ECS) que foi usado como eletrodo de referˆencia, o fio de platina como contra eletrodo e a amostra com uma ´area de contato de 3,14cm2
.
A prote¸c˜ao dos revestimentos foi determinada a partir das curvas de polariza¸c˜ao utilizando-se a equa¸c˜ao emp´ırica abaixo descrita [46]:
Pi = 100
(1−icorr)
i0
corr
(5.1)
Onde icorr e i0corr s˜ao as densidades de corrente de corros˜ao na presen¸ca e ausˆencia do
revestimento.
5.2.2
Espectroscopia de Impedˆ
ancia Eletroqu´ımica(EIS)
Os espectro de impedˆancia reflete o comportamento diel´etrico, rea¸c˜oes de oxida¸c˜ao-redu¸c˜ao e controle de massa por migra¸c˜ao atrav´es da interface criada entre o eletrodo (amostra) e o meio corrosivo. O modelamento do espectro eletroqu´ımico, o qual forma uma parte essencial do estudo de impedˆancia eletroqu´ımica, utiliza-se de um circuito equivalente para descrever a interface eletroqu´ımica. Ajustando-se as vari´aveis pode-se chegar a uma correspondˆencia te´orica dos dados obtidos experimentalmente no dom´ınio de frequˆencia experimentado (analisado). Assim, informa¸c˜oes a respeito da corros˜ao ele-troqu´ımica podem ser extra´ıdas de uma apropriada interpreta¸c˜ao das vari´aveis.
Neste trabalho foi utilizado um equipamento Autolab para medidas de impedˆancias em amostras de Ti6Al4V e Ti6Al4V nitretado, amostras com filmes GLCH depositados sobre a superf´ıcie de Ti6Al4V nua e nitretada.
imersos em solu¸c˜ao salina tamponada com fosfato (solu¸c˜ao PBS), conforme esquematizado na Figura 5.1. A liga¸c˜ao entre a c´elula e a amostra era realizada com resina ep´oxi.
Figura 5.1: Desenho esquem´atico da c´elula eletroqu´ımica em ensaios de impedˆancia ele-troqu´ımica.
Medidas de impedˆancia foram realizadas a temperatura ambiente devido a dura¸c˜ao dos experimentos, na faixa de frequˆencia 100 kHz a 3 mHz e com uma perturba¸c˜ao de 10 mV. A aquisi¸c˜ao do espectro de impedˆancia foi realizada ao potencial de circuito aberto com os tempos de imers˜ao mostrados na Tabela 5.2.
Tabela 5.2: Tempo de imers˜ao das amostras
AMOSTRAS TEMPO DE IMERS ˜AO
Horas Dias
Ti6Al4V 1 48 7 16 23 30
-GLCH sobre Ti6Al4V 1 48 7 16 23 30 37
Ti6Al4V nitretada 1 48 7 16 23 30
-GLCH sobre Ti6Al4V nitretado 1 48 7 16 23 30 37
5.3
Microscopia Eletrˆ
onica de Varredura
5.4
Microspoia de For¸ca Atˆ
omica
A t´ecnica AFM foi utilizada para a observa¸c˜ao tanto da morfologia dos substratos quanto dos filmes depositados pela t´ecnica PACVD. As imagens foram obtidas com o microsc´opio de for¸ca atˆomica (SHIMADZU, modelo SPM-9500J3), operando no modo contato, com sondas de nitretos de sil´ıcio (NANOSENSORS) e scanner de 125µm . A fim de evitar o desgaste das sondas, uma baixa for¸ca de intera¸c˜ao teve que ser utilizada na aquisi¸c˜ao de imagens dos filmes GLCH, devido sua alta dureza.
An´alises de espectroscopia de for¸ca foram realizadas atrav´es de um microsc´opio SPM (Scanning Probe Microscope) da empresa Veeco Instruments. Foram adquiridas medidas sobre a liga nua e a liga nitretada. A aquisi¸c˜ao das medidas foi realizada ao ar ou sob atmosfera de hidrogˆenio, com a ajuda de uma cˆamara de controle ambiental. Os cantilevers utilizados para as medidas eram de sil´ıcio recobertos por um filme fino de diamante dopado com as seguintes especifica¸c˜oes: k∼ 2,5−10N/m , R ∼30−50nm e ω0 ∼115−190 KHz. Estimativas mais precisas de k e R foram obtidas utilizando-se
o m´etodo de Sader [49, 50] fazendo imagem de amostras de referˆencia. Experimentos foram realizados com aquecimento, atrav´es de um setup comercial do microsc´opio, para a remo¸c˜ao da maior parte da ´agua sobre a superf´ıcie da amostra. Esta camada de ´agua ´e respons´avel por for¸cas capilares e forma¸c˜ao de um menisco que interfere nas medidas. Assim, utilizando o aquecimento, as for¸cas de ades˜ao entre a ponta de diamante e a superf´ıcie da amostra podem ser medidas com a influˆencia reduzida da camada de ´agua.
5.5
Espectroscopia Raman
Os revestimentos obtidos pela t´ecnica de deposi¸c˜ao PACVD sobre a liga de Ti6Al4V nua e nitretada, foram caracterizadas por espectroscopia de Raman com um NTEGRA Spectra Nanofinder (NT-MDT), o qual foi operado com feixe de comprimento de onda de 514,5nm.
Atrav´es de espectro obtido pela t´ecnica de Raman ´e poss´ıvel estimar a porcentagem de hidrogˆenio no filme, atrav´es da equa¸c˜ao 5.2 como mostra Casiraghi et al [48].
H[at.%] = 21,7 + 16,6log[ m
6 Resultados e Discuss˜
oes
6.1
Caracteriza¸c˜
ao dos Filmes GLCH
A Figura 6.1 apresenta imagem ao MEV para filme GLCH depositado em substrato de TI6Al4V atrav´es da t´ecnica PACVD. Nesta amostra foi feito um corte transversal para a determina¸c˜ao da espessura aproximada de 4 µmdo filme.
Figura 6.1: Imagem ao MEV para o filme GLCH depositado sobre substrato de Ti6Al4V por PACVD.
As amostras de filmes depositados em Ti6Al4V e Ti6Al4V nitretado tamb´em foram avaliadas morfologicamente pela t´ecnica de microscopia de for¸ca atˆomica (AFM) conforme apresentado na Figura 6.2. Os filmes depositados sobre a liga nua de Ti6Al4V apresentam baixa rugosidade Ra = 8,9nm e s˜ao compostos por pequenos gr˜aos compactos com o
tamanho m´edio de 0,2µm. J´a as amostras de filmes depositados na liga nitretada s˜ao compostas por aglomerados n˜ao homogˆeneos de pequenos gr˜aos. A rugosidade ficou mais elevada, em torno de (Ra = 70,4nm), para a imagem apresentada. Este aumento na
superficial afeta a morfologia do revestimento mas tamb´em podemos ter a influˆencia da composi¸c˜ao qu´ımica da amostra e a emiss˜ao de el´etrons secund´arios. A emiss˜ao de el´etrons secun´arios de diferentes substratos aumenta diferentemente a intensidade do plasma, o que pode resultar em diferentes propriedades e morfologia do revestimento [51].
Figura 6.2: Imagens de Microscopia de For¸ca Atˆomica para filmes depositados na (A) liga de Ti6Al4V e (B) liga Ti6Al4V nitretada.
Foram realizadas varreduras na superf´ıcie das amostras para verificar a presen¸ca de falhas e/ou poros. Alguns poucos poros, como o apresentado na Figura 6.3, puderam ser identificados.
As amostras dos filmes depositados por PACVD tanto na liga de titˆanio nua quanto sobre titˆanio nitretado foram caracterizados por espectroscopia de Raman e o espectro obtido da an´alise encontra-se na Figura 6.4. Este espectro revela duas bandas com picos localizados aproximadamente entre 1385cm−1 e 1569cm−1, os quais est˜ao relacionados
`as bandas D e G, respectivamente, t´ıpicas dos filmes de carbono amorfo hidrogenados.
Figura 6.4: Espectro Raman de um revestimento depositado por PACVD (13,56Hz).
A banda D ´e atribu´ıda `a desordem do carbono induzida pelas liga¸c˜oes sp3
de ´atomos de carbono e pelo tamanho finito dos microcristalitos de liga¸c˜oes do tipo sp2
. J´a a banda G refere-se a liga¸c˜oes trigonais do tipo sp2
que ´e encontrada para fase grafite.
A quantidade de hidrogˆenio nos filmes pˆode ser estimada a partir da equa¸c˜ao 5.2 [48], no qual obtemos uma porcentagem de hidrogˆenio no filme de 16%.
Segundo Ferrari et al. [52], a espectroscopia Raman ´e uma poderosa ferramenta para caracterizar filmes de carbono amorfo. Em seu artigo [52], os autores apresentam um gr´afico da posi¸c˜ao de picos G em fun¸c˜ao do percentual de liga¸c˜oes sp3
para filmes a-C:H. O gr´afico tamb´em ´e apresentado na Figura 6.5.
Pode-se verificar que filmes com pico G em torno de 1569cm−1 apresentam um
percen-tual aproximado de 33 % de liga¸c˜oes sp3
. O percentual de liga¸c˜oes sp3
combinado com a quantidade de hidrogˆenio contida no filme permite a determina¸c˜ao da quantidade de liga¸c˜oes sp2
Figura 6.5: Gr´afico da posi¸c˜ao de picos G em fun¸c˜ao do percentual de liga¸c˜oes sp3
para filmes a-C:H [52].
Figura 6.6: Diagrama tern´ario para filmes de carbono amorfo [6].
Do diagrama tern´ario pode-se extrair uma porcentagem de aproximadamente 52% de liga¸c˜oes do tipo sp2
, resultando em uma raz˜ao sp3
/sp2
de 0.65.
6.2
T´
ecnicas Eletroqu´ımicas
6.2.1
Curva de Polariza¸c˜
ao Potenciodinˆ
amica
A Figura 6.7 mostra as curvas de polariza¸c˜ao potenciodinˆamica para a liga de Ti6Al4V, a liga de Ti6Al4V nitretada e para os filmes GLCH depositados em liga nua e nitretada. Todas curvas foram realizadas em solu¸c˜ao tamponada com fosfato (PBS).
A liga de Ti6Al4V apresenta um comportamento passivo em um meio simulado de um fluido corporal, que ´e caracterizado por uma baixa densidade de corrente an´odica da ordem de 8.10−7
A/cm2
em uma ampla faixa de potencial an´odicos (de 0 a 1,5 V). A liga, ap´os o tratamento superficial de nitreta¸c˜ao, adquire um comportamento mais nobre (maior potencial de corros˜ao) e com baixa densidade de corrente an´odica, inferior da liga n˜ao nitretada, at´e um potencial em torno de 0,75 V, indicando que o processo de nitreta¸c˜ao melhorou a resistˆencia `a corros˜ao da liga. Al´em disso, a liga nitretada apresenta uma pequena regi˜ao de passividade se comparada `a liga n˜ao tratada, a qual apresenta uma ampla regi˜ao passiva. Ainda na liga nitretada verifica-se o inicio de um pico an´odico em torno de 1,2 V correspondente `a acentua¸c˜ao do processo de oxida¸c˜ao do TiN para oT iO2,
segundo o diagrama de Pourbaix proposto por Heide e Schultze [22]. Os filmes GLCH depositados sobre a liga de titˆanio nua e nitretada apresentam nobreza semelhante `a liga nitretada, por´em as densidades de corrente an´odica, para um mesmo potencial, s˜ao pelo menos uma ordem de grandeza menor, indicando uma superior prote¸c˜ao `a corros˜ao.
Atrav´es da aplica¸c˜ao da f´ormula para determinar a eficiˆencia de prote¸c˜ao (Pi) para
as amostras recobertas e n˜ao recobertas com filmes GLCH, nas mesmas condi¸c˜oes das curvas de polariza¸c˜ao apresentadas anteriormente, verificou-se que a eficiˆencia de prote¸c˜ao dos filmes GLCH gira em torno de 95 a 97%. Como as curvas de polariza¸c˜ao para os filmes GLCH depositados sobre a liga nua e liga nitretada n˜ao apresentaram diferen¸cas significativas, isto poderia levar `a suposi¸c˜ao de que o substrato tem pouca influˆencia no comportamento apresentado nas curvas de polariza¸c˜ao. Somente a elevados potenciais, os filmes de GLCH depositados em ligas nitretadas apresentam algumas quebras que poderiam estar associados com a oxida¸c˜ao de TiN paraT iO2 que ocorre atrav´es dos poros
Figura 6.7: Curva de polariza¸c˜ao potenciodinˆamica para substrato de Ti6Al4V, Ti6Al4V nitretado e filme GLCH depositado por PACVD sobre liga de Ti6Al4V nua e nitretada. Curva realizada a uma velocidade de varredura de 0,167mV/s.
6.2.2
Espectroscopia de Impedˆ
ancia Eletroqu´ımica (EIE)
Neste trabalho, medidas de impedˆancia eletroqu´ımica foram realizadas com o intuito de estudar a resistˆencia `a corros˜ao das ligas Ti6Al4V, Ti6Al4V nitretada e dos filmes GLCH depositados sobre a liga nua e nitretada. Essas medidas foram realizadas em solu¸c˜ao tamponada com fosfato (PBS), com os tempos de imers˜ao mostrados anteriormente na Tabela 5.2.
Na Figura 6.8 temos o espectro de impedˆancia eletroqu´ımica para Ti6Al4V em dife-rentes tempos de imers˜ao. Verifica-se altos valores de impedˆancia e ˆangulo de fase de aproximadamente 800
Com o tempo de imers˜ao de 30 dias, o valor da impedˆancia diminui, indicando redu¸c˜ao da resistˆencia `a corros˜ao. Este fato pode estar ligado ao surgimento da corros˜ao por fresta. De fato, alguns autores tem verificado a possibilidade de corros˜ao por fresta em titˆanio [55, 56, 57].
Figura 6.8: Gr´afico de Bode da liga Ti6Al4V, imerso em solu¸c˜ao PBS para 1hora, 48 horas 7 dias, 16 dias, 23 dias, e 30 dias.
Atrav´es dos dados obtidos experimentalmente foi poss´ıvel simular um circuito el´etrico equivalente representativo dos processos f´ısicos que ocorrem no sistema sob investiga¸c˜ao. Os dados foram melhor simulados usando o circuito el´etrico equivalente apresentado na Figura 6.9. O circuito ´e constitu´ıdo por uma resistˆencia da solu¸c˜ao do eletr´olito utilizado no teste (RS), a resistˆencia do filme associada `a resistˆencia da barreira de ´oxido formada
sobre a liga do titˆanio (Rp), e uma capacitˆancia do filme de ´oxido (Qc), sendo que Qc
representa um elemento de constante de fase (CPE) e descreve um capacitor n˜ao ideal.
A Tabela 6.1 mostra os valores de elementos de circuito obtidos atrav´es da simula¸c˜ao ao longo do tempo de imers˜ao. ´E poss´ıvel observar que a resistˆencia da solu¸c˜ao decresce com o passar do tempo de imers˜ao, indicando uma libera¸c˜ao de ´ıons do substrato para a solu¸c˜ao. J´a a resistˆencia `a polariza¸c˜ao do titˆanio aumenta com o tempo de imers˜ao at´e dezesseis dias, o que indica um aumento na espessura do ´oxido protetor. Ap´os vinte e trˆes dias de imers˜ao ocorre um pequeno decr´escimo da resistˆencia, o qual se torna mais evidente aos trinta dias, indicando uma poss´ıvel corros˜ao por fresta, como j´a discutido anteriormente.
A capacitˆancia do revestimento (Qc) apresenta uma tendˆencia de queda ao longo do
tempo, o que est´a associado ao crescimento do ´oxido, j´a que capacitˆancia ´e dada pela seguinte f´ormula:
C = ε0εrA
d (6.1)
Onde, ε0 ´e a permissividade do v´acuo, εr ´e a constante diel´etrica, A ´e a ´area e d a
distˆancia entre duas placas (espessura do filme).
Aos 23 dias a capacitˆancia torna aumentar o que indica um ac´umulo de carga no sistema que pode estar ligado `a presen¸ca de ´ıons oriundos da corros˜ao por fresta.
Tabela 6.1: Parˆametros de ajuste do espectro de impedˆancia realizados ao longo dos tempos de imers˜ao para Ti6Al4V.
1hora 48 horas 7 dias 16 dias 23 dias 30 dias Rs(Ω.cm2) 45,40 38,60 29,65 31,08 31,90 24,88
Rp(kΩ.cm2) 148,1 253,8 382,0 1788,0 1654,0 330,0
Qc(F.cm−2) 0,481e−4 0,466e−4 0,446e−4 0,428e−4 0,435e−4 0,515e−4
nc 0,910 0,896 0,896 0,899 0,898 0,893
A Figura 6.10 mostra o gr´afico de Bode para a liga de titˆanio nitretado nos seguintes tempos de imers˜ao: 1 hora, 48 horas, 7 dias, 16 dias, 23 dias e 30 dias.
devido ao processo de nitreta¸c˜ao, o qual forma uma camada de nitretos [58]. Verifica-se que a liga nitretada apresenta um comportamento capacitivo indicado por um ˆangulo de fase de aproximadamente 800
em regi˜oes de baixa-m´edia frequˆencias.
Figura 6.10: Gr´afico de Bode da liga de Ti6Al4V nitretado, imerso em solu¸c˜ao PBS para 1hora, 48 horas, 7 dias, 16 dias, 23 dias, e 30 dias.
O modelo de circuito el´etrico equivalente que representa o processo f´ısico em estudo da liga de titˆanio nitretado ´e idˆentico ao da liga nua de titˆanio como mostra a Figura 6.11. O circuito el´etrico ´e constitu´ıdo por uma resistˆencia da solu¸c˜ao (RS), uma resistˆencia
representada pela camada nitretada (Rp) e uma capacitˆancia (Qc) da camada nitretada.
Figura 6.11: Modelo de circuito equivalente para o Ti6Al4V nitretado.
Na Tabela 6.2 temos os elementos de circuito para a amostra de Ti6Al4V nitretado. A resistˆencia da solu¸c˜ao (Rs) diminui com o tempo de imers˜ao possilvemente devido `a
nitretada (Rp) tem uma queda devido `a ocorrˆencia de processo corrosivo. Aos vinte e trˆes
dias houve um aumento na resistˆencia a polariza¸c˜ao que n˜ao pˆode ser explicado. Pode-se verificar que o Ti6Al4V nitretado apresenta uma maior resistˆencia (Rp) em rela¸c˜ao a liga
de titˆanio, o que indica que a camada nitretada confere uma melhor resistˆencia `a corros˜ao.
No caso da capacitˆancia da camada nitretada (Qc), verificou-se um aumento do valor
com o passar do tempo devido ao acumulo de carga na superf´ıcie oriundo do processo corrosivo.
Tabela 6.2: Parˆametros de ajuste do espectro de impedˆancia realizados ao longo dos tempos de imers˜ao para Ti6Al4V nitretado.
1hora 48 horas 7 dias 16 dias 23 dias 30 dias
Rs(Ω.cm2) 19,5 17,7 13,8 12,0 9,04 5,88
Rp(Ω.cm2) 8,900e+6 3,890e+6 3,130e+6 2,860e+6 4,400e+6 3,048e+6
Qc(F.cm−2) 0,786e−4 0,962e−4 0,997e−4 0,986e−4 0,107e−3 0,118e−3
nc 0,901 0,887 0,885 0,885 0,877 0,870
A Figura 6.12 mostra os gr´aficos de Bode obtidos para filme de GLCH depositado na liga de Ti6Al4V (GLCH/Ti6Al4V) para diferentes tempos de imers˜ao. Verifica-se que os valores de impedˆancia s˜ao superiores ao da liga nua e nitretada. Al´em disto o comporta-mento das curvas praticamente n˜ao muda com o passar do tempo de imers˜ao. Estes dois fatos indicam que o filme apresenta um excelente car´ater protetor e que este car´ater se mant´em ao longo dos dias, indicando uma excelente resistˆencia `a corros˜ao e estabilidade do filme. Devido a alta resistividade dos filmes, os diagramas de Bode s˜ao dominados pelo comportamento capacitivo. No espectro da Figura 6.12 existem duas regi˜oes capaci-tivas, uma com ˆangulo de fase pr´oximo a 900
, na regi˜ao de alta frequˆencia e o outra entre ˆangulos 650
−750
em uma regi˜ao de baixa frequˆencia. A regi˜ao de alta frequˆencia cont´em informa¸c˜oes do revestimento, enquanto a regi˜ao de baixa frequˆencia cont´em informa¸c˜oes sobre os processos relacionados a rea¸c˜oes na interface eletr´olito/substrato.
![Figura 2.1: V´alvula artificial do cora¸c˜ao [3].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15748725.637632/17.892.320.617.273.600/figura-v-alvula-artificial-do-cora-c-ao.webp)
![Figura 2.3: Diagrama de fase tern´ario para filmes de carbono amorfo com rela¸c˜ao `a quantidade de liga¸c˜ao sp 2 , sp 3 e hidrogˆenio [6].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15748725.637632/19.892.320.626.865.1071/figura-diagrama-fase-filmes-carbono-amorfo-quantidade-hidrogˆenio.webp)
![Figura 3.1: Esquema de um diagrama para sistema de deposi¸c˜ao de filmes de DLC [31].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15748725.637632/26.892.259.679.642.965/figura-esquema-diagrama-para-sistema-deposi-filmes-dlc.webp)
![Figura 3.2: Esquema b´asico de um equipamento de nitreta¸c˜ao por plasma [37].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15748725.637632/29.892.290.647.403.668/figura-esquema-asico-de-equipamento-nitreta-por-plasma.webp)
![Figura 4.1: Esquema do princ´ıpio de funcionamento da coluna MEV [39].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15748725.637632/31.892.301.656.178.431/figura-esquema-do-princ-ıpio-funcionamento-coluna-mev.webp)
![Figura 4.2: Diagrama representativo de funcionamento do microsc´opio de for¸ca atˆomica [40].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15748725.637632/32.892.302.634.336.593/figura-diagrama-representativo-funcionamento-microsc-opio-for-atˆomica.webp)
![Figura 4.4: Espectro Raman de um filme de a-C:H obtido pela t´ecnica de PACVD para um plasma de metano [43].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15748725.637632/35.892.286.649.731.970/figura-espectro-raman-obtido-ecnica-pacvd-plasma-metano.webp)
![Figura 4.5: Diagrama Nyquist, no eixo x a impedˆancia real e no eixo y a impedˆancia imagin´aria com vetor impedˆancia [44].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15748725.637632/37.892.300.638.841.1025/figura-diagrama-nyquist-impedˆancia-impedˆancia-imagin-vetor-impedˆancia.webp)
![Figura 4.6: Gr´afico de Bode em fun¸c˜ao da constante de tempo [44].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15748725.637632/38.892.363.574.242.434/figura-gr-afico-de-bode-fun-constante-tempo.webp)