Clínica Universitária de Cardiologia
Disfunção Microvascular Coronária em
Doentes Diabéticos
Rui Carlos Gregório Antunes Coelho
1
Clínica Universitária de Cardiologia
Disfunção Microvascular Coronária em
Doentes Diabéticos
Rui Carlos Gregório Antunes Coelho
Orientado por:
Professora Doutora Conceição Azevedo Coutinho
2
Resumo
A disfunção microvascular coronária (DCMV) está bem estabelecida como causa de isquémia miocárdica em indivíduos nos quais foi excluída doença coronária epicárdica obstrutiva (1). Esta entidade é particularmente relevante nos subgrupos de doentes diabéticos, do sexo feminino ou idosos (2–4).
Existem dados experimentais e clínicos suficientes para incluir a disfunção microvascular coronária no conjunto das complicações microvasculares da diabetes mellitus (5–8). A resistência periférica à insulina e a hiperglicemia levam à desregulação de vias de sinalização intra-celular, activação inflamatória e geração de
stress oxidativo. Promovem, desta forma, a disfunção endotelial e o «remodeling»
microvascular, que têm como consequência a redução da capacidade vasomotora (dependente e independente do endotélio) da microcirculação coronária (9).
A miocardiopatia diabética corresponde a disfunção diastólica (ou, mais raramente, sistólica), na ausência de doença coronária obstrutiva, hipertensão arterial ou doença valvular. Esta patologia, cuja principal causa é a disfunção microvascular coronária, é caracterizada por fibrose perivascular e hipertrofia ventricular esquerda (10).
A disfunção microvascular coronária é um determinante importante no prognóstico dos doentes diabéticos e é fundamental compreender a sua fisiopatologia para estabelecer um plano terapêutico eficaz (11).
Palavras-chave
Disfunção microvascular coronária. Diabetes mellitus. Complicações microvasculares. Disfunção endotelial. Miocardiopatia diabética.
3
Abstract
Coronary microvascular dysfunction is well established as a cause of myocardial ischemia in patients without obstructive epicardial coronary disease (1). This entity is particularly relevant in the subgroups of diabetic, female or elderly patients (2-4).
There are sufficient experimental and clinical data to include coronary microvascular dysfunction in all microvascular complications of diabetes mellitus (5-8). Peripheral insulin resistance and hyperglycemia lead to dysregulation of intra-cellular signaling pathways, inflammatory activation and oxidative stress generation. They promote endothelial dysfunction and microvascular remodeling, which results in the reduction of the vasomotor capacity (dependent and independent of the endothelium) of the coronary microcirculation (9).
Diabetic cardiomyopathy corresponds to diastolic (or, more rarely, systolic) dysfunction, in the absence of obstructive coronary disease, arterial hypertension or valvular disease. This pathology, mainly caused by coronary microvascular dysfunction, is characterized by perivascular fibrosis and left ventricular hypertrophy (10).
Coronary microvascular dysfunction is an important determinant in the prognosis of diabetic patients and it is critical to understand its pathophysiology to establish an effective therapeutic plan (11).
Key words
Coronary microvascular dysfunction. Diabetes mellitus. Microvascular complications. Endothelial dysfuncion. Diabetic cardiomyopathy.
4
Índice
Página Resumo/Abstract. . . 2 Índice. . . . 4 Introdução. . . 5Anatomia funcional da circulação arterial coronária . . . 9
Apresentação clínica da disfunção microvascular coronária. . . . 11
Classificação e fisiopatologia da disfunção microvascular coronária . . 14
Documentação de isquémia miocárdica por disfunção microvascular coronária. . 20
Avaliação da função microvascular coronária. . . 22
Disfunção microvascular coronária em doentes diabéticos. . . . . 24
Miocardiopatia diabética. . . 26
Mecanismos de disfunção microvascular coronária induzida pela hiperglicemia. . 28
Terapêutica da disfunção microvascular coronária em doentes diabéticos . . 34
Conclusão. . . 37
5
Introdução
A diabetes mellitus (DM) é uma doença metabólica multifactorial, caracterizada por hiperglicemia. Actualmente, o diagnóstico de diabetes, baseado nas recomendações da World Health Organization e da American Diabetes Association, é feito através de glicemia em jejum igual ou superior a 126 mg/dL, hemoglobina A1c igual ou superior a 6,5% ou glicemia maior ou igual a 200 mg/dL, duas horas após sobrecarga de glicose, em duas medições consecutivas. Estes critérios baseiam-se no nível de glicemia a partir do qual ocorre retinopatia (12).
A diabetes mellitus está dividida em quatro categorias etiológicas: 1) tipo 1, causada por produção deficiente de insulina; 2) tipo 2, estado de resistência à insulina de longa duração, com hiperinsulinemia compensatória e hiperglicemia; 3) gestacional; 4) grupo denominado «outros tipos específicos» (12).
Estima-se que, em 2035, a diabetes mellitus afecte 10% da população mundial. Esta elevada prevalência constitui um enorme problema de saúde pública, devido às complicações microvasculares (retinopatia e nefropatia), macrovasculares (doença coronária, doença cerebrovascular e doença arterial periférica) e não vasculares (neuropatia) (12–15).
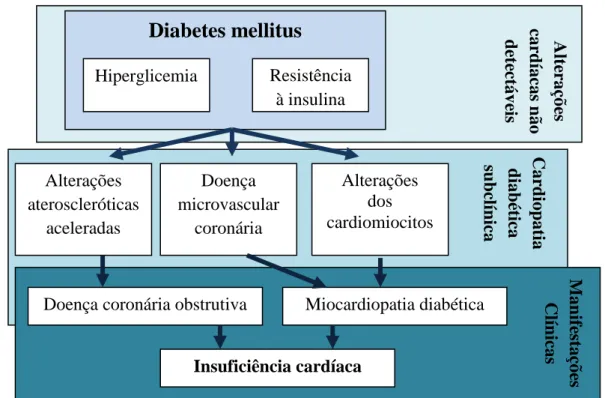
Figura 1 – Progressão clínica da cardiopatia diabética. (adaptado de Kibel et al. Journal of International Medical Research. 2017; 45(6): 1901–1929).
Alte raç õ es car d íacas n ão d ete ctáv eis Car d iop at ia d iab étic a su b clí n ica M an ife staç õe s Clín icas
Diabetes mellitus
Hiperglicemia Resistência à insulina Alterações ateroscleróticas aceleradas Doença microvascular coronária Alterações dos cardiomiocitosDoença coronária obstrutiva Miocardiopatia diabética
6
A cardiopatia diabética pode manifestar-se como doença coronária obstrutiva (a manifestação mais frequente), disautonomia cardíaca ou miocardiopatia diabética, causada essencialmente por disfunção microvascular coronária [figura 1] (16).
A disfunção endotelial, o stress oxidativo, a hipercoagulabilidade e a disautonomia são tidos como factores de risco no estabelecimento da causalidade entre a diabetes mellitus e os eventos cardiovasculares (17).
A disfunção microvascular coronária consiste na incapacidade da microcirculação coronária em ajustar o tónus vascular às necessidades de perfusão miocárdica, ou seja, na diminuição da reserva do fluxo coronário (18).
Em indivíduos com manifestações clínicas de isquémia miocárdica submetidos a coronariografia, observa-se ausência de doença coronária obstrutiva significativa em 20-50% dos casos (1,19,20). Estes doentes podem referir angina de peito ou equivalentes anginosos (cansaço, dispneia, náuseas ou lipotimia) e apresentar testes de sobrecarga farmacológica com evidência de isquémia miocárdica, condição conhecida como síndrome X (21).
A disfunção microvascular coronária é um preditor de aumento considerável do risco de doença coronária obstrutiva, enfarte agudo do miocárdio, insuficiência cardíaca e morte súbita, assim como de admissões no serviço de urgência por angina instável e cateterismos cardíacos repetidos [figura 2] (22–26).
Figura 2 – A) Curvas de sobrevivência de Kaplan-Meier por morte de causa cardiovascular e B) ausência de eventos cardiovasculares (enfarte agudo do miocárdio, insuficiência cardíaca, admissão no serviço de urgência por angina instável e revascularização coronária) em 124 doentes com e sem disfunção microvascular coronária, durante o follow-up (até 101 meses) após enfarte agudo do miocárdio e reperfusão (adaptado de Bolognese et al. Circulation. 2004; 109(9): 1121–6).
Sem disfunção microvascular
Com disfunção microvascular
Sem disfunção microvascular
Com disfunção microvascular P < 0,0001 P < 0,0001 S o b re v iv ên ci a ( %) S o b re v iv ên ci a l iv re d e ev en to s (%)
7
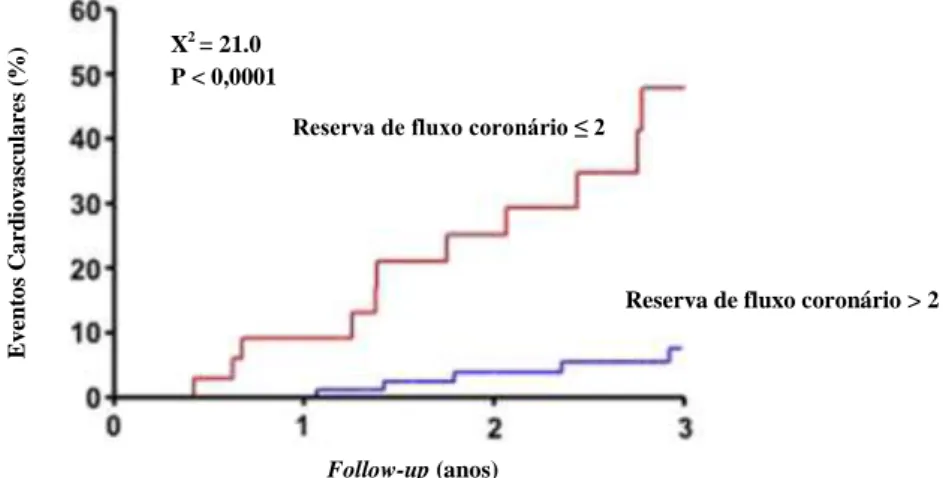
Em doentes diabéticos sem doença coronária obstrutiva, a presença de reserva de fluxo coronário igual ou inferior a 2,0 prevê um risco de eventos cardiovasculares sete vezes superior [figura 3] (27–29). Por outro lado, a prevalência da isquémia silenciosa em populações diabéticas oscila entre 12 e 57%(30).
Figura 3 – Percentagem de doentes que sofrem enfarte agudo do miocárdio e/ou morte de causa cardíaca, num follow-up de 3 anos, num grupo de doentes diabéticos, com reserva de fluxo coronário menor ou igual a 2 (vermelho) ou superior a 2 (azul) (adaptado de Cortigiani et al. J Am Soc Echocardiogr. 2014; 27(7): 742–8).
No estudo “Improve Diagnosis and Treatment of Women with Angina Pectoris
and Microvessel Disease” (iPOWER study), que incluiu 963 mulheres com angina de
peito sem estenose coronária epicárdica significativa, detectou-se uma redução significativa da reserva do fluxo coronário – valor mediano de 2,33 (31). Neste estudo, a disfunção microvascular coronária associou-se à idade, hipertensão arterial, tabagismo activo, taquicardia e redução do colesterol HDL [quadro 1] (31).
O estudo recente de Taqueti et al mostrou que a mortalidade cardiovascular é superior nas mulheres pós-menopáusicas (grupo com maior prevalência de disfunção microvascular coronária) relativamente aos homens (grupo com maior prevalência de doença coronária obstrutiva) (32).
À luz do conhecimento actual, o diagnóstico clínico de disfunção microvascular coronária não pode ser estabelecido em definitivo (33), até porque a disfunção microvascular pode instalar-se em sobreposição com doença das artérias coronárias epicárdicas (34,35). A avaliação da função microvascular coronária é complexa, dada a impossibilidade de estudar directamente a microcirculação pelos métodos invasivos e
X2 = 21.0 P < 0,0001 E v en to s C a rd io v a scu la re s ( %) Follow-up (anos)
Reserva de fluxo coronário ≤ 2
8
não invasivos tradicionais (36). No entanto, justifica-se a investigação, dado que cerca de 55% dos doentes com angina de peito de causa microvascular tem episódios recorrentes após o diagnóstico (37).
Quadro 1 – Variação esperada (em percentagem) da reserva de fluxo coronário em função da presença de factores de risco cardiovasculares, numa análise de regressão multivariada, numa população de 885 mulheres.
(Adaptado de Mygind et al. J Am Heart Assoc. 2016; 5(3): e003064).
Neste trabalho, procedeu-se à revisão da literatura médica relativa à associação clínica e experimental entre diabetes mellitus e disfunção microvascular coronária, assim como às hipóteses de explicação dos respectivos mecanismos fisiopatológicos.
Variação da reserva do fluxo coronário (%)
IC 95% p value
Idade (por cada 10 anos) -6,2 -8,0 a -4,4 <0.001
Hipertensão arterial -4,0 -7,2 a -0,8 0,016
Tabagismo (no passado) -1,9 -5,2 a + 1,6 0,29
Tabagismo (no presente) -8,6 -12,7 a -4,0 <0,001
Frequência Cardíaca (por cada 10 bpm aumentados)
-2,3 -3,8 a -0,8 0,002
Colesterol HDL (por cada 1mmol/L aumentado)
9
Anatomia funcional da circulação arterial coronária
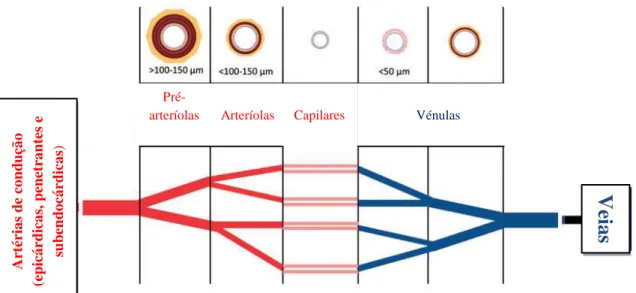
A circulação arterial coronária está dividida em três compartimentos funcionais, com base no diâmetro, estrutura e função fisiológica [figuras 4 e 5] (18):Figura 4 – Circulação coronária (adaptado de Kibel et al. Journal of International Medical Research.
2017; 45(6): 1901–1929).
1) Artérias coronárias epicárdicas, conhecidos como vasos capacitantes, com diâmetro entre 500 µm e 5 mm, respondem às variações do fluxo sanguíneo por mecanismos dependentes do endotélio, contribuindo apenas em 10% para a resistência coronária total.
2) Pré-arteríolas, vasos de diâmetro compreendido entre 100 e 500 µm, respondem ao fluxo, na sua porção proximal, e à pressão, na porção distal. Não respondem directamente à difusão de metabolitos miocárdicos, pois apresentam localização extramiocárdica e a sua parede têm uma espessura incompatível com processos de difusão. A sua principal função biológica é a manutenção da pressão da circulação coronária, independentemente das variações de pressão de perfusão, sendo responsáveis por 30% da resistência coronária total.
3) Arteríolas, vasos de calibre inferior a 100 µm de diâmetro e localização intramiocárdica. São o compartimento mais distal do território arterial coronário e responsáveis por 50% da resistência coronária total (18).
Art ér ia s de co nd uçã o (epicá rdica s, penet ra nte s e sub en do cá rdica s)
Pré-arteríolas Arteríolas Capilares Vénulas
V
ei
a
10
Os restantes 10% da resistência coronária total são provenientes dos capilares. É no território arteríolar que ocorre a regulação metabólica do fluxo arterial coronário, através de mecanismos dependentes e independentes do endotélio (36).
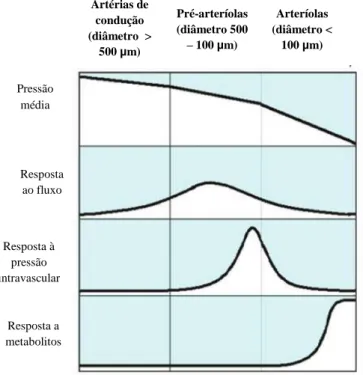
Figura 5 – Anatomia funcional da circulação coronária – os diferentes compartimentos do território arterial coronário respondem de forma diferente ao fluxo, à pressão e à difusão de metabolitos (adaptado de Camici et al. N Engl J Med. 2007; 356(8): 830-40).
As arteríolas têm elevada tonicidade basal, sendo que a sua principal função é a vasodilatação em resposta aos estímulos metabólicos, com diminuição da resistência arteríolar e pré-arteríolar (38). É o ajuste de resistência nos três compartimentos da circulação arterial coronária que permite adequar o fluxo coronário às necessidades de oxigénio e nutricionais do miocárdio (17).
Artérias de condução (diâmetro > 500 µm) Pré-arteríolas (diâmetro 500 – 100 µm) Arteríolas (diâmetro < 100 µm) Pressão média Resposta ao fluxo Resposta à pressão intravascular Resposta a metabolitos
11
Apresentação clínica da disfunção microvascular
coronária
A suspeita de disfunção microvascular coronária ocorre em doentes com angina de peito após a realização de coronariografia, onde é excluída lesão obstrutiva significativa ou espasmo coronário após teste de provocação com acetilcolina intra-arterial (33).
O diagnóstico diferencial da dor pré-cordial sem evidência de doença coronária obstrutiva não se limita à disfunção microvascular coronária, mas também a outras causas isquémicas (angina de Prinzmetal), causas não isquémicas cardíacas (dor de origem pericárdica, perturbações da nocicepção) ou não cardíacas (doença de refluxo gastro-esofágico, patologia pulmonar, dor de origem músculo-esquelética, perturbações psiquiátricas) (39).
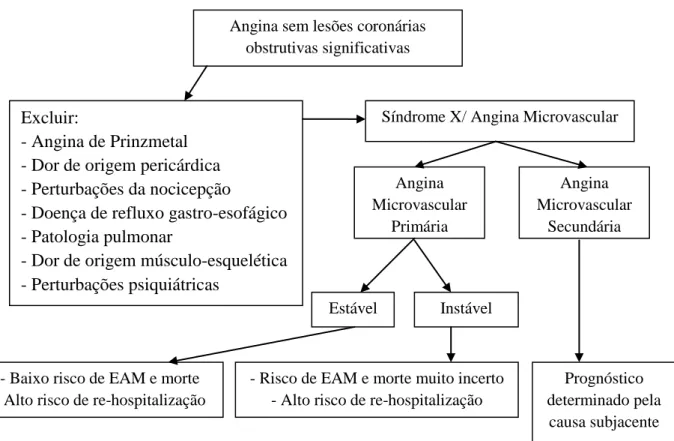
Figura 6 - Diagnóstico diferencial, classificação e prognóstico da angina microvascular (adaptado de
Crea et al. (2014). Coronary Microvascular Dysfunction. eBook. Fist edition, Springer. Milan).
Angina sem lesões coronárias obstrutivas significativas
Excluir:
- Angina de Prinzmetal - Dor de origem pericárdica - Perturbações da nocicepção
- Doença de refluxo gastro-esofágico - Patologia pulmonar
- Dor de origem músculo-esquelética - Perturbações psiquiátricas
Síndrome X/ Angina Microvascular
Angina Microvascular Secundária Prognóstico determinado pela causa subjacente Angina Microvascular Primária Instável Estável
- Baixo risco de EAM e morte - Alto risco de re-hospitalização
- Risco de EAM e morte muito incerto - Alto risco de re-hospitalização
12
Síndrome X cardíaca:
A apresentação clínica da disfunção microvascular coronária é chamada de síndrome X cardíaca (ou angina microvascular), entidade, presente sobretudo em mulheres, que designa angina de peito e evidência de isquémia miocárdica (prova de esforço e/ou testes de perfusão miocárdica de stress positivos), na ausência de doença coronária obstrutiva (40).
A angina microvascular pode ser classificada como primária (em que a disfunção microvascular coronária do tipo 1 é considerada a única causa dos sintomas) ou secundária (causada por disfunção microvascular coronária dos tipos 2, 3 e 4, no contexto de outras doenças cardíacas). Na angina microvascular secundária, é difícil determinar qual a contribuição da doença microvascular na angina de peito [quadro 2] (34).
A angina microvascular primária pode ser classificada em estável (relacionada com o esforço) ou instável (precipitada por pequenos esforços ou em repouso), com diferentes mecanismos fisiopatológicos, apresentação clínica, abordagem terapêutica e prognóstico [figura 6] (18).
Em doentes com angina microvascular estável, a dor pré-cordial persiste frequentemente após a interrupção do esforço e não responde (ou responde de forma lenta e insuficiente) à administração de nitratos. Em 20 a 30% dos doentes, ocorrem episódios de dor pré-cordial para esforços progressivamente menores (18).
A disfunção microvascular coronária é responsável por 5 a 10% dos casos de angina instável sem supra-desnivelamento do segmento ST, percentagem que sobe para 30% na população de mulheres pós-menopáusicas (18).
Angina microvascular variante e miocardiopatia de takotsubo:
Em situações raras, ocorre espasmo microvascular intenso que causa isquémia transmural, com duas formas de apresentação (34). Uma delas é a angina microvascular variante, que foi observada na população japonesa. Ocorre angina de repouso e/ou de esforço, com evidência de isquémia transmural transitória, reproduzida pela administração intra-coronária de acetilcolina, na ausência de lesão obstrutiva ou espasmo das artérias coronárias epicárdicas (18).
A outra entidade é a miocardiopatia de takotsubo, ou miocardiopatia relacionada com o stress, que se caracteriza por dor anginosa típica, desencadeada pelo esforço
13
físico ou stress emocional, acompanhada por alterações electrocardiográficas, como supra-desnivelamento do segmento ST ou inversão da onda T, e elevações mínimas da troponina, em doentes sem doença coronária obstrutiva. Ocorre diminuição transitória da função ventricular esquerda, com hipo/acinesia/discinesia apical e médio-ventricular e preservação da contractilidade nos segmentos basais. Estão documentados casos de insuficiência cardíaca aguda e choque cardiogénico (41).
Cerca de 80 a 90% dos casos envolve mulheres pós-menopáusicas. O prognóstico é bastante favorável, com recuperação das alterações em 1 a 3 meses, sendo a recorrência anual de aproximadamente 1,5% e a mortalidade entre 1,0 a 3,2% (41,42).
Vários mecanismos, como trombose coronária, espasmo epicárdico de múltiplos vasos ou miocardite, foram estudados e considerados pouco prováveis como causa da miocardiopatia de takotsubo (18).
A miocardiopatia de takotsubo parece ser mediada pelo sistema adrenérgico, estando associada a episódios de stress e verificando-se um aumento da concentração local de catecolaminas e sinais de toxicidade das catecolaminas na biópsia endomiocárdica. Além disso, a distribuição particular das alterações da contractilidade miocárdica parece reflectir a inervação adrenérgica. A hiperactivação adrenérgica causa vasoconstrição microvascular intensa e prolongada, o que aparenta estar na base da isquémia miocárdica (18,41).
14
Classificação e fisiopatologia da disfunção microvascular
coronária
A disfunção microvascular coronária é classificada em quatro tipos [quadro 2] (18) e está associada a alterações intravasculares (estruturais e funcionais) e extra-vasculares (hemodinâmicas), que variam em função das diferentes causas de disfunção microvascular mas coexistem frequentemente [figura 11 e quadro 3] (36).
Quadro 2 – Classificação clínica da disfunção microvascular coronária.
Classificação da disfunção microvascular coronária
Tipo 1 Ocorre na ausência de doença coronária obstrutiva ou outra doença miocárdica. Está associada a factores de risco para doença coronária (diabetes mellitus, hipertensão arterial, dislipidémia ou tabagismo) e é parcialmente reversível se estes forem tratados.
Tipo 2 Secundária a miocardiopatias primárias (miocardiopatia hipertrófica, miocardiopatia dilatada), cardiopatia hipertensiva ou valvulopatias (estenose aórtica).
Tipo 3 Instala-se no contexto de doença coronária obstrutiva estável ou síndrome coronária aguda, com ou sem supra-desnivelamento do segmento ST.
Tipo 4 Iatrogénica, ocorre após revascularização coronária epicárdica.
(Adaptado de Camici et al. N Engl J Med. 2007; 356(8): 830-40).
Tipo 1:
A disfunção microvascular coronária do tipo 1 pode ser causada por quatro mecanismos fisiopatológicos. Porém, o «remodeling» vascular é menos significativo do que na disfunção microvascular coronária do tipo 2. Os três principais mecanismos fisiopatológicos associados à disfunção microvascular coronária do tipo 1 são: 1) a diminuição da capacidade vasodilatadora dependente do endotélio; 2) a diminuição da capacidade vasodilatadora independente do endotélio e 3) o aumento da vasoconstrição [figuras 8 e 9] (18).
15
Figura 7 – Mecanismos fisiopatológicos da disfunção microvascular coronária (adaptado de Kibel et
al. Journal of International Medical Research. 2017; 45(6): 1901–1929).
Quadro 3 – Sistematização dos mecanismos fisiopatológicos da disfunção microvascular coronária.
Alterações Causas
Estruturais
Obstrução luminal Micro-embolização em contexto de síndrome coronária aguda ou desobstrução coronária percutânea Infiltração da parede
vascular
Miocardiopatias infiltrativas (ex.: miocardiopatia de Anderson-Fabry)
«Remodeling» vascular Miocardiopatia hipertrófica; hipertensão arterial Rarefacção vascular Estenose aórtica; hipertensão arterial Fibrose perivascular Estenose aórtica; hipertensão arterial Funcionais
Disfunção endotelial Tabagismo, hiperlipidemia, diabetes mellitus Disfunção do músculo
liso vascular
Miocardiopatia hipertrófica; hipertensão arterial
Disautonomia Desobstrução coronária percutânea
Extra-vasculares
Compressão extramural Estenose aórtica; miocardiopatia hipertrófica; hipertensão arterial
Redução do tempo de perfusão diastólico
Estenose aórtica
(Adaptado de Camici et al. N Engl J Med. 2007; 356(8): 830-40).
Alterações estruturais Remodeling Disfunção endotelial Disfunção do músculo liso Inflamação Infiltração da parede Resposta -adrenérgica aumentada Aumento da vasoconstrição
16
Figura 8 – Alterações funcionais associadas à disfunção microvascular coronária (adaptado de Crea
et al. (2014). Coronary Microvascular Dysfunction. eBook. Fist edition, Springer. Milan).
A) Diminuição da capacidade vasodilatadora dependente do endotélio. É consequência da disfunção endotelial provocada pelos factores de risco cardiovascular tradicionais (hipertensão arterial, dislipidémia, tabagismo e diabetes mellitus). Este fenómeno é uma alteração precoce no aparecimento de aterosclerose e um mecanismo patológico comprovado na disfunção microvascular coronária (43).
Em doentes sem doença coronária obstrutiva, os hábitos tabágicos (preditores de disfunção endotelial) estão associados a uma redução da reserva do fluxo coronário de 21% (44).
A lesão endotelial é evidenciada pela diminuição do monóxido de azoto (NO), causada pela diminuição da actividade da enzima monóxido de azoto sintetase endotelial (eNOS) e pelo aumento da degradação do NO. Em situações normais, o NO aumenta a produção de monofosfato de guanosina cíclico (cGMP) nas células de músculo liso, molécula que activa os canais de potássio dependentes de ATP (KATP), levando a hiperpolarização da membrana celular e encerramento dos canais de cálcio dependentes de voltagem. A consequente diminuição do cálcio intra-celular causa vasodilatação. Assim, a diminuição do NO é o principal mecanismo de redução da vasodilatação dependente do endotélio (18).
Disfunção microvascular coronária
Diminuição da vasodilatação Aumento da vasoconstrição Endotelina-1 Catecolaminas Acetilcolina, Serotonina, etc
Mediada pelo fluxo Acetilcolina, Serotonina, Histamina, Bradicinina, etc Adenosina Catecolaminas Independente do endotélio Dependente do endotélio
17
Também se verifica redução da produção endotelial de outras moléculas vasodilatadoras, como a prostaciclina (PGI) e o factor de hiperpolarização derivado do endotélio (EDHF) (45).
B) Diminuição da capacidade vasodilatadora independente do endotélio. É causada por disfunção do músculo liso vascular. Na ausência de disfunção, a activação dos receptores ß2-adrenérgicos, a ligação da adenosina aos receptores A2 e a acção de outras moléculas (H+, prostaciclina, dióxido de carbono, peróxido de hidrogénio) aumentam a produção de monofosfato de adenosina cíclico (cAMP) nos miócitos. O cAMP é uma via alternativa ao NO para activação dos canais de potássio dependentes de ATP, e consequente vasodilatação (18).
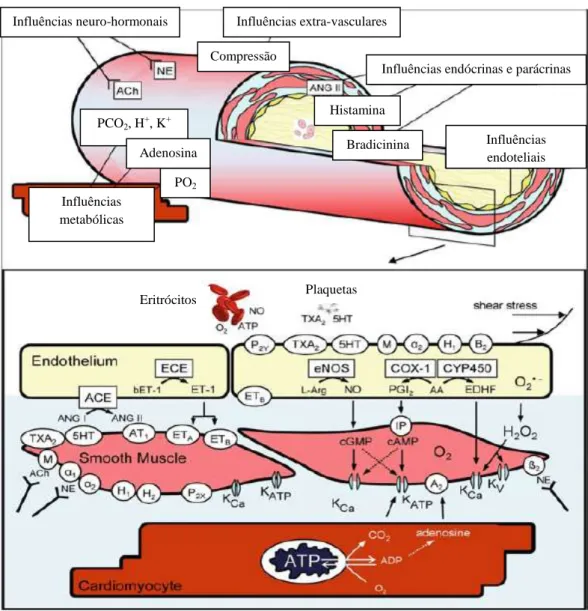
Figura 9 – Controlo vasomotor das arteríolas coronárias (adaptado de Crea et al. (2014). Coronary Microvascular Dysfunction. eBook. Fist edition, Springer. Milan).
Influências extra-vasculares Influências neuro-hormonais
Influências endócrinas e parácrinas
Influências endoteliais Influências metabólicas Compressão Histamina Bradicinina PO2 PCO2, H+, K+ Eritrócitos Plaquetas Adenosina
18
A disfunção nas vias intra-celulares do cGMP, do cAMP ou dos canais de K na membrana dos miócitos leva à perda de capacidade de relaxamento do músculo liso vascular, que permite a vasodilatação (36).
C) Aumento da vasoconstrição. Deve-se à produção, no endotélio lesado, de endotelina-1, o vasoconstritor mais potente do organismo humano, que se liga ao receptor ETA das células do músculo liso (46). Estão envolvidas outras moléculas
vasoconstritoras, como a angiotensina II (produzida pelo endotélio), a serotonina, o neuropéptido Y ou leucotrienos (18).
Tipo 2:
Mesmo na ausência de hipertrofia ventricular esquerda, a hipertensão arterial associa-se a redução da reserva coronária. Ocorre «remodeling» arteríolar (hipertrofia do músculo liso, aumento do colagénio da camada média e espessamento da camada íntima da parede vascular), redução do lúmen, fibrose perivascular, compressão extrínseca e rarefacção microvascular (devido à hipertrofia ventricular e ao aumento das pressões diastólicas) (18).
A disfunção microvascular coronária no contexto de estenose aórtica deve-se, não só à hipertrofia ventricular esquerda, mas também à redução do tempo e da pressão de perfusão diastólica (36).
Em miocardiopatias primárias (miocardiopatia hipertrófica, miocardiopatia dilatada, doença de Anderson-Fabry, amiloidose), observa-se redução da reserva do fluxo coronário em todo o território ventricular, com evidência de «remodeling» microvascular (36).
Tipo 3:
A presença de disfunção microvascular coronária no contexto de doença coronária obstrutiva associa-se a pior prognóstico desta (22,47). A doença coronária obstrutiva causa disfunção microvascular coronária através de diferentes mecanismos, em função do padrão de isquémia miocárdica:
1) Na angina estável, a doença arterial coronária pode causar disfunção microvascular através de falhas na redistribuição da perfusão miocárdica transmural. Na presença de uma estenose crítica, ocorre vasoconstrição paradoxal (mediada pelo sistema nervoso simpático e pela inibição dos receptores A1 da adenosina) das arteríolas
19
subepicárdicas durante o exercício, para favorecer a perfusão das arteríolas subendocárdica, mais sensíveis à isquémia. Este mecanismo compensatório é deletério, pois a redução da reserva do fluxo coronário leva à diminuição do limiar de esforço para isquémia miocárdica (36).
2) No enfarte agudo do miocárdio com supra-desnivelamento do segmento ST, a disfunção coronária está associada a fenómenos de «no-reflow», nos quais não ocorre restabelecimento eficaz do fluxo coronário após desobstrução coronária percutânea (48). A disfunção microvascular pode ser causada por embolização distal de placa de ateroma e/ou do trombo, lesão endotelial por produção de radicais livres (lesão de isquémia-reperfusão), assim como libertação de moléculas vasoconstritoras (sobretudo endotelina-1 e tromboxano) (49).
3) Nas síndromes coronários agudos sem supra-desnivelamento do segmento ST, as causas e as consequências da disfunção microvascular são semelhantes às apresentadas para as anteriores manifestações de doença coronária (36).
Tipo 4:
A disfunção microvascular coronária de causa iatrogénica ocorre por embolização distal de fragmentos da placa de ateroma ou do trombo e vasoconstrição do território microvascular (mediada por activação de receptores -adrenérgicos) na sequência de revascularização coronária epicárdica bem-sucedida (36).
20
Documentação de isquémia miocárdica por disfunção
microvascular coronária
Na angina microvascular, a prova de esforço mostra infra-desnivelamento do segmento ST e dor pré-cordial (50). A cintigrafia de perfusão miocárdica com rádio-isótopos tem baixa sensibilidade neste contexto, pois apenas detecta defeitos reversíveis da perfusão na doença grave (33). Estes exames são pouco relevantes no diagnóstico de disfunção microvascular (34). A figura 10 é um exemplo ilustrativo de demonstração de isquémia anterior num doente sem doença coronária significativa.
Figura 10 - Prova de Esforço (com infra-desnivelamento do segmento ST em V3-V6 em esforço) e Cintigrafia de perfusão miocárdica com 99mTc-MIBI (com defeito de perfusão na parede anterior do ventrículo esquerdo) em doente com angina de peito típica sem doença coronária obstrutiva. (Adaptado de Crea et al. (2014). Coronary Microvascular Dysfunction. eBook. Fist edition, Springer. Milan).
Em 20 a 30% dos pacientes com angina microvascular estável, há evidência metabólica de isquémia miocárdica em testes de sobrecarga farmacológica, com
Stress Stress Stress Repouso Repouso Repouso
21
dessaturação da hemoglobina, redução do pH, libertação de lactato e produtos de peroxidação lipídica no seio coronário (34,51).
A ecocardiografia convencional não apresenta alterações segmentares da contractilidade miocárdica em repouso (34). A ecocardiografia com sobrecarga farmacológica induzida por dobutamina ou dipiridamol não demonstra alterações da contractilidade, apesar da ocorrência de angina ou equivalentes anginosos [figura 11] (34,52,53).
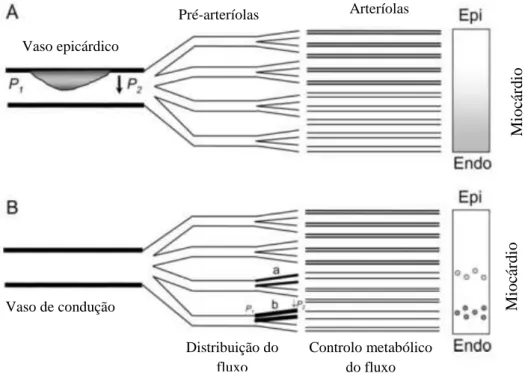
Figura 11 - Diferenças entre a isquémia miocárdica causada por estenose coronária significativa (A) e por disfunção microvascular coronária (B). No caso da estenose epicárdica (Epi), a isquémia atinge difusamente toda o miocárdio perfundido pelo vaso obstruído, sobretudo na sua região subendocárdica (a cinzento), o que resulta em disfunção contráctil regional. Na disfunção microvascular, pequenas áreas de isquémia (círculos pequenos) estão desigualmente distribuídas no miocárdio, com atingimento preferencial da região subendocárdica. Esta distribuição não resulta em alterações da contractilidade segmentar, dada a presença de miócitos com função contráctil preservada no mesmo território. (Adaptado de Lanza et al. Circulation. 2010. 121(21): 2317-25)
Vaso epicárdico Pré-arteríolas Arteríolas Vaso de condução Distribuição do fluxo Controlo metabólico do fluxo Mi oc ár d io Mi oc ár d io
22
Avaliação da função microvascular coronária
A microcirculação coronária não pode ser directamente visualizada in vivo, dado que o seu calibre (menor que 500 µm) é inferior à resolução espacial da coronariografia e não permite a introdução dos cateteres intravasculares (36). A função da microcirculação coronária é avaliada indirectamente, através do cálculo da reserva do fluxo coronário (CFR).
Esta corresponde ao aumento do fluxo entre a perfusão coronária basal e a hiperemia máxima, sendo calculada através da divisão do fluxo em hiperemia (induzida pela perfusão intra-coronária/endovenosa de adenosina ou endovenosa de dipiridamol) pelo fluxo coronário em repouso (36).
Na ausência de doença coronária obstrutiva, a disfunção microvascular coronária é considerada para valores de reserva de fluxo coronário inferiores a 2,0. No entanto, devemos ter em conta que, mesmo em indivíduos saudáveis, a reserva coronária varia em função do sexo e da idade, pelo que os seus valores devem ser ajustados para estas variáveis (34,36).
Ainda não são consensuais os intervalos de valores de reserva coronária que permitem a estratificação da disfunção microvascular coronária em função da gravidade (39,54).
Dado que a resistência coronária é maioritariamente determinada pela microcirculação, a reserva do fluxo coronário quantifica a capacidade vasodilatadora dos microvasos em resposta aos estímulos vasodilatadores. A destacar que, em doentes com doença coronária obstrutiva, a redução da reserva coronária é proporcional à gravidade da estenose e perde especificidade para a disfunção microvascular (18).
A avaliação da reserva coronária pode ser feita por técnicas invasivas e não invasivas [quadro 4].
As técnicas invasivas, realizadas por cateterismo, incluem o método de termodiluição intra-coronária (que determina o fluxo coronário através de uma curva de diluição térmica) e o Doppler intra-coronário (18). O estudo de Doppler intra-coronário permite avaliar directamente a velocidade do fluxo coronário e calcular a vasodilatação microvascular em resposta a adenosina (independente do endotélio) e a acetilcolina (dependente do endotélio) (55).
As técnicas não invasivas incluem a ecocardiografia com estudo de Doppler da artéria descendente anterior, a ecocardiografia de contraste miocárdico, a tomografia por
23
emissão de positrões (PET) com rubídio-82 e a ressonância magnética nuclear com captação de gadolínio (18,56,57).
Quadro 4 - Comparação entre diferentes métodos de investigação da função coronária microvascular. Dis p o n ib ilid ad e C u sto R is co Reprodutibilidade Dep en d ên cia d o o p er ad o r Acesso à função microvascular coronária total Avaliação quantitativa do fluxo coronário Ecocardiografia transtorácica com estudo de Doppler +++ +++ +++ +++ - - - Ecocardiografia de contraste miocárdico ++ ++ + ++ + + + PET - - ± + ++ ++ +++ Ressonância magnética cardíaca + - - ± ++ ++ ++ Doppler intra-coronário ± ± ± - + +++ ++
(-) = mau; (+) = suficiente; (++) = bom; (+++) = muito bom. (Adaptado de Crea et al. (2014). Coronary Microvascular Dysfunction. eBook. Fist edition, Springer.
Milan).
A ecocardiografia com estudo de Doppler da artéria descendente anterior é o método de screening inicial para detectar disfunção microvascular coronária (reserva de fluxo coronário inferior a 2,0). Neste método, a reserva do fluxo coronário é calculada através da divisão da velocidade do fluxo coronário em vasodilatação máxima (induzida por adenosina ou dipiridamol) pela velocidade do fluxo coronário em repouso (34).
A ecocardiografia de contraste miocárdico é útil quando a ecocardiografia com estudo de Doppler é negativa ou inconclusiva (15,18).
A tomografia por emissão de positrões (PET) com rubídio-82 determina o fluxo coronário por grama de miocárdio, em repouso e após hiperemia induzida por adenosina ou dipiridamol. Alguns autores consideram este método como o gold standard na determinação da reserva de fluxo miocárdico (15,58).
O estudo recente de Liu et al. atribuí à ressonância magnética nuclear com captação de gadolínio sensibilidade de 89% e especificidade de 95% na detecção de disfunção microvascular coronária confirmada por cateterismo (59).
24
Disfunção
microvascular
coronária
em
doentes
diabéticos
A disfunção microvascular coronária é uma complicação microvascular da diabetes mellitus, sendo que a hiperglicemia está associada à redução da reserva do fluxo coronário, mesmo em indivíduos sem evidência de doença cardiovascular (5,6,9,60).
Está também demonstrada, em doentes diabéticos sem manifestações de doença cardiovascular, a associação entre a redução da reserva coronária e a disautonomia cardíaca (nomeadamente redução do índice coração/mediastino tardio na cintigrafia miocárdica com 123-I-metaiodobenzilguanidina) (61).
Avaliação da reserva do fluxo coronário nos doentes diabéticos:
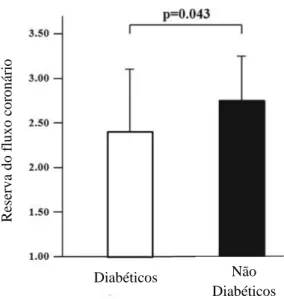
Marciano et al realizaram ecocardiografia com estudo de Doppler após
administração de dipiridamol em 59 indivíduos com dor anginosa mas sem doença coronária obstrutiva, dos quais 23 eram diabéticos tipo 2 e 26 não diabéticos. Verificaram que a reserva de fluxo coronário foi inferior nos diabéticos (2,38 ± 0,74
versus 2,75 ± 0,49, p=0,04) [figura 12] (7).
Figura 12 – Reserva do fluxo coronário em doentes diabéticos e não diabéticos (Adaptado de
Marciano et al. Eur J Med Mol Imaging. 2012; 39(7): 1199-206).
Diabéticos Não Diabéticos R eser v a d o f lu x o co ro n ár io
25 Scholten et al usaram a tomografia por emissão de positrões com rubídio-82,
para avaliar 60 doentes com diabetes mellitus tipo 2 e sem manifestações de doença cardiovascular e 30 indivíduos sem doença. Foi observada uma redução significativa da reserva do fluxo coronário em 83,3% dos diabéticos com albuminúria, 40,0% dos diabéticos sem albuminúria e 16,7% dos controlos [figura 13] (8).
Figura 13 – Valor médio da reserva do fluxo coronário em doentes não diabéticos e diabéticos com e sem albuminúria (Adaptado de Scholten et al. Diabetologia. 2016; 59(2): 371-8).
Em indivíduos com estenose aórtica grave sem doença coronária obstrutiva, a diabetes mellitus é um preditor independente de redução da reserva do fluxo coronário (IC 95%: - 0,916 a -0,368, p <0,001) (62).
Comprovou-se também redução da reserva coronária em doentes pré-diabéticos, ainda que menos acentuada do que nos indivíduos com critérios de diagnóstico de diabetes (63).
O controlo da diabetes mellitus aumenta a reserva coronária e reduz as manifestações anginosas e a evidência de isquémia nos testes de stress em doentes sem doença coronária obstrutiva (64,65).
Controlos Diabéticos sem albuminúria Diabéticos com albuminúria R eser v a d o f lu x o co ro n ár io
26
Miocardiopatia diabética
Vários estudos mostraram que, nos doentes diabéticos, a duração e a gravidade da hiperglicemia, assim como a presença de complicações microvasculares (redução da reserva de fluxo coronário, mas também retinopatia e/ou nefropatia diabética), estão associadas significativamente a disfunção diastólica do ventrículo esquerdo (aumento da pressão de enchimento do ventrículo esquerdo) (66–75).
Em doentes diabéticos, observa-se frequentemente a redução da função ventricular esquerda, na ausência de doença arterial coronária, hipertensão arterial ou valvulopatias. Esta entidade, descrita inicialmente por Rubler et al., é denominada miocardiopatia diabética (76).
A miocardiopatia diabética é uma doença multifactorial (77). Na práctica, as comorbilidades associadas à diabetes mellitus (obesidade, hiperlipidemia, hipertensão arterial) são factores de risco adicionais para disfunção diastólica do ventrículo esquerdo (15).
A hiperglicemia, a hiperinsulinemia e a resistência periférica à insulina têm efeitos directos nos cardiomiocitos, como sejam alterações no metabolismo dos lípidos (aumento do up-take de ácidos gordos livres) e lesão dos componentes sub-celulares (mitocôndrias e transportadores de Cálcio, entre outros). A resistência periférica à insulina causa diminuição do up-take de glicose nos receptores GLUT-1 e GLUT-4 dos cardiomiocitos, o que perturba a produção de energia e, consequentemente, a contractilidade. Ocorre ainda activação do sistema renina-angiotensina-aldosterona, disautonomia cardíaca e indução de respostas inflamatórias desadequadas. No entanto, o mecanismo principal da miocardiopatia diabética parece ser a disfunção microvascular [figura 14] (2,78).
O miocárdio apresenta maior susceptibilidade à lesão de isquémia-reperfusão (10), sendo que um mau controlo glicémico (hemoglobina A1c igual ou superior a 7.0) está associado a maior incidência de fenómenos de «no-reflow» (79). Os indivíduos diabéticos têm mais micro-embolização distal na intervenção percutânea primária (PCI), associada à disfunção microvascular coronária iatrogénica (80).
Na miocardiopatia diabética, ocorre inicialmente fibrose perivascular e intersticial e, progressivamente, hipertrofia miocárdica com «remodeling» ventricular concêntrico, observando-se disfunção diastólica do ventrículo esquerdo e insuficiência cardíaca com fracção de ejecção preservada (81).
27
A disfunção sistólica, associada a dilatação do ventrículo esquerdo, ocorre numa fase mais avançada da doença e é frequentemente subclínica (78).
Figura 14 – Mecanismos fisiopatológicos da miocardiopatia diabética (Adaptado de Lee et al. Korean J Intern Med. 2017; 32(3): 404-21) Hiperglicemia Hiperinsulinemia Resistência à insulina Disfunção microvascular Alteração do metabolismo dos lípidos Activação do SRAA Respostas imunitárias não adaptativas Lesão de componentes sub-celulares Disautonomia cardíaca
Lesões estruturais e funcionais - Lesão dos cardiomiocitos e apoptose - Fibrose e hipertrofia miocárdica - Citocinas inflamatórias - Disfunção mitocondrial - Diminuição do metabolismo do Cálcio - Espécies reactivas de oxigénio - Produção de AGE - Oxidação de ácidos gordos - Expressão deTGF-ß Disfunção diastólica Insuficiência Cardíaca Disfunção sistólica Miocardiopatia diabética
28
Mecanismos de disfunção microvascular induzida pela
hiperglicemia
Di Carli et al mostraram que, após ajuste para a duração da doença, índice de
massa corporal, insulinoterapia, perfil lipídico e disautonomia, a redução da reserva do fluxo coronário é semelhante na diabetes mellitus tipo 1 (deficiência de insulina) e tipo 2 (resistência periférica à insulina e hiperinsulinemia). Assim, a hiperglicemia (característica comum dos dois tipos de diabetes) é considerada a causa principal de disfunção microvascular coronária nos diabéticos (9).
A lesão microvascular induzida pela hiperglicemia deve-se a disfunção endotelial e «remodeling» microvascular (82,83).
Disfunção endotelial induzida pela hiperglicemia:
Em indivíduos diabéticos, a disfunção endotelial microvascular ocorre frequentemente na ausência de lesões anatómicas (84).
Figura 15 – Vias de lesão microvascular induzida pela hiperglicemia (Adaptado de Scheetz et al. JAMA. 2002; 288(20): 1579-88). Via das hexosaminas Hiperglicemia Via da Aldolase Reductase
Via dos produtos de glicação avançada
Via das espécies reactivas de
oxigénio
Via da proteína cinase C
Glicotoxinas (Metabolitos reactivos)
Alterações na expressão de genes e na função de proteínas Activação de moléculas de sinalização celular
Disfunção Endotelial
Alterações da angiogénese Aumento da permeabilidade Alterações do fluxo Aumento da contractilidade Alterações do crescimento e sinalização celular
Espessamento da membrana basal Aumento da Adesão leucocitária Trombose Miocardiopatia
29
Os mecanismos de lesão endotelial induzida pela hiperglicemia têm sido agrupados em cinco teorias [figura 15], que estão ligadas:
1) Via dos polióis/ aldolase reductase. A elevação da concentração de glicose intracelular activa a enzima aldolase reductase (AR), levando à redução de glicose a sorbitol com consumo de NADPH. Por sua vez, a enzima sorbitol desidrogenase reduz NAD+ a NADH na reacção de oxidação do sorbitol a frutose. O aumento das relações NADP+/NADPH e NADH/NAD+ gera stress oxidativo [figura 16] (82).
Figura 16 – Teoria da via dos polióis (à esquerda) e da via das espécies reactivas de oxigénio (à direita) (Adaptado de Scheetz et al. JAMA. 2002; 288(20): 1579-88).
2) Via das espécies reactivas de oxigénio (ROS). O metabolismo da glicose, através da via glicolítica ou do Ciclo de Krebs, assim como a auto-oxidação da glicose, produzem radicais livres como o anião superóxido. Estas moléculas quimicamente instáveis e muito reactivas induzem disfunção endotelial, pois lesam proteínas e o DNA mitocondrial, diminuem os níveis intra-celulares de NO e promovem a adesão leucocitária ao endotélio [figura 16] (85).
Fosforilação oxidativa Hiperglicemia
Glicose
Disfunção e lesão celular
Activação de moléculas de sinalização celular PKC MAPK NF-kB Espécies reactivas de Oxigénio Aldolase Reductase Sorbitol desidrogenase Stress Osmótico Espécies reactivas de Oxigénio Stress Oxidativo Stress Oxidativo Diminuição de defesas anti-oxidantes
Alterações na expressão de genes e na função de proteínas Desequilíbrio
30
3) Via dos produtos de glicação avançada (AGE). Os produtos de glicação avançada englobam um grupo de proteínas (ex: colagénio, proteínas intra-celulares) danificadas pela ligação covalente cruzada à glicose. Os AGEs ligam-se a receptores transmembranares da família das imunoglobulinas (RAGEs), iniciando uma cascata de sinalização intra-celular que activa a proteína activada por mitogénios cinase (MAPK), factor nuclear kB (NF-kB) e proteína cinase C (PKC), factores de transcrição que induzem a lesão endotelial [figura 17] (86,87).
Figura 17 – Teoria da via dos produtos de glicação avançada (à esquerda) e da proteína cinase C (à direita) (Adaptado de Scheetz et al. JAMA. 2002; 288(20): 1579-88).
4) Via das hexosaminas. A hiperglicemia e a produção de superóxido desviam glicose para a via das hexosaminas, levando à O-glicação de receptores de insulina e de outras proteínas da via do inositol-3-fosfato cinase (PI3-K), que activam a via da proteína cinase C (88).
Glicação não enzimática AGE intra e extra-celulares
Hiperglicemia Glucose Gliceraldeido -3- fosfato Diacilglicerol Activação da Proteína Cinase C Activação da Fosfolipase C ou D Glicólise Activação de outras moléculas de sinalização celular
Alterações na expressão de genes (citocinas, factores de crescimento) e na função de proteínas (NADPH oxidase)
Disfunção e lesão celular
Glu Proteínas intracelulares Proteínas
extracelulares
Ligação aos Recetores AGE Activação de moléculas de sinalização celular PKC MAPK NF-kB
31
5) Via da proteína cinase C (PKC). A isoforma ß da proteína cinase C, induzida pelo diacilglicerol (DAG) ou pela via AGE-RAGE, activa moléculas, como o NF-kB, o factor de crescimento do endotélio vascular (VEGF), o TGF-ß ou a endotelina-1, que aumentam a permeabilidade, vasomotricidade, activação endotelial, sinalização por factores de crescimento e de sinalização. A PKC inibe a produção de NO e prostaciclina [figura 17] (89,90).
A lesão das células endoteliais [figuras 15 e 18] leva a:
1) Redução da actividade da NO sintase e consumo directo de NO pelo superóxido (O2-) na formação de peroxinitrito (ONOO-). A redução do NO, assim como
da prostaciclina, causam redução da vasodilatação dependente do endotélio (91).
2) Produção aumentada de endotelina-1 e angiotensina-II, que vão actuar no músculo liso, levando a vasoconstrição e «remodeling» microvascular (92).
3) Perturbações da angiogénese (síntese deficiente de VEGF) (93).
4) Sobreprodução de factores pró-trombóticos (factor de von Willebrand, inibidor do activador do plasminogénio-1) e de moléculas de adesão leucocitária (molécula de adesão da célula vascular 1 (VCAM-1), molécula de adesão intercelular 1 (ICAM-1), E-selectina), o que facilita a agregação plaquetar e a inflamação local (94,95).
Figura 18 – Alterações associadas à disfunção endotelial (Adaptado de Crea et al. (2014). Coronary Microvascular Dysfunction. eBook. Fist edition, Springer. Milan).
Estímulo Anormal
Função endotelial normal: - Vasodilatação - Anti-agregação - Anti-inflamatório - Anti-proliferativo - Barreira biológica Disfunção endotelial: - Vasoconstrição - Agregação plaquetária - Pró-inflamatório - Proliferativo - Aumento da permeabilidade
32
«Remodeling» microvascular induzido pela hiperglicemia:
O «remodeling» microvascular ocorre com espessamento da membrana basal, hipertrofia do músculo liso e hialinização da camada média da parede vascular. Podem observar-se microaneurismas capilares (96,97). Estas alterações são induzidas por perturbações no metabolismo do músculo liso vascular (secundárias à hiperglicemia, resistência à acção da insulina e acumulação de ácidos gordos livres) e pela acção de moléculas produzidas no endotélio (angiotensina-II, endotelina-I) e citocinas inflamatórias (IL-6, TNF ) (98–100).
Uma das vias intracelulares mais importantes no «remodeling» microvascular é a do factor nuclear kB (NF-kB) [quadro 5], que activa a expressão de factores de crescimento e de sobrevivência celular, a diferenciação fenotípica fibroblasto-like (produção de TGF-ß e metaloproteinases, associados à fibrose da parede e perivascular) e a inflamação (101,102). O NF-kB é activado por:
1) Vias de lesão microvascular induzidas pela hiperglicemia, já abordadas no âmbito da disfunção endotelial.
2) Ligação da angiotensina II ao receptor de AngII tipo I (AT1R) (14).
3) Ligação da endotelina-1 ao receptor ETA (103).
Quadro 5 – Vias de sinalização do NF-kB
Indutores do NF-kB Interleucinas, factores de crescimento,
mitogénios
IL-1, TNF- , IFN-γ, PDGF, VEGF
Microrganismos, vírus e os seus componentes
LPS, Chlamydia pneumoniae, Borrelia burgdorferi,
Shigella dysenteriae, Plasmodium falciparum
Factores físicos Radiação UV, Radiação γ, Shear stress
Outros Stress oxidativo, trombina, homocisteína, lesão isquémia-reperfusão, leptina, metais pesados, complemento Genes regulados pelo NF-kB
Interleucinas, factores de crescimento IL-1, IL-6, IL-8, TNF- , G-CSF, M-CSF, GM-CSF, MCP-1 , RANTES
Citocinas e moléculas de adesão E-selectina, ICAM-1, VCAM-1, LOX-1, RAGE Indutores de apoptose A20, A1, XIAP, c-IAP1, c-IAP2
Imunomoduladores MHC-I, MHC-II, factor regulador do interferão Outros iNOS, COX-2, factor tecidual, PAI-1, MnSOD,
MMP-2, MMP-9
(Adaptado de Martin et al. Arterioscler Thromb Vasc Biol. 2000;20:e83-e88).
As consequências na função microvascular das alterações estruturais e funcionais associadas ao «remodeling» arteríolar já foram descritas anteriormente.
33
Em ratos com fenótipo diabético db/db, o bloqueio do receptor AT1R durante 4
semanas com losartan associou-se a regressão no «remodeling» microvascular e a aumento da reserva coronária (104).
O bloqueio selectivo dos receptores ETA em doentes diabéticos associou-se a
valores de reserva de fluxo coronário (3,33±0,5) superiores aos obtidos com placebo (2,3±1,2) e mais próximos dos valores obtidos nos indivíduos sem doença (4,9±2,3) (105).
A hiperglicemia está também associada à inactivação de canais de potássio dependentes de ATP (KATP) no músculo liso vascular, responsáveis pela vasodilatação arteríolar coronária em resposta à hipoxia e à isquémia, vulgo vasodilatação metabólica, que é independente do endotélio (106,107).
34
Terapêutica da disfunção microvascular coronária em
doentes diabéticos
Figura 19 – Proposta de algoritmo para diagnóstico e terapêutica da disfunção microvascular coronária (Adaptado de Kibel et al. Journal of International Medical Research. 2017; 45(6): 1901–1929).
Ecocardiografia com estudo de Doppler
PET
Ressonância magnética cardíaca
Coronariografia Doppler intra-coronário Doença Subclínica Angina Microvascular Miocardiopatia/ Insuficiência Cardíaca Se as técnicas não invasivas forem positivas Controlo glicémico Controlo dos factores de risco
Alterações do estilo de vida
Inibidores da enzima de conversão da angiotensina Antagonistas dos receptores
da Angiotensina II Prevenção das complicações da diabetes Ácido acetilsalicílico Estatinas
Todos os pacientes com Angina Microvascular
Beta-bloqueantes Bloqueadores dos Canais de Cálcio
Nitratos de longa acção Ivabradina Ranolazina Trimetazidina Sintomas de Insuficiência Cardíaca Diuréticos da ansa Antagonistas da aldosterona
35
Actualmente, as estratégias terapêuticas da angina microvascular são baseadas em evidência científica escassa, pois estão concluídos poucos ensaios clínicos nesta população (39).
O algoritmo elaborado por Kibel et al. [figura 19] é uma proposta para diagnóstico e tratamento da disfunção microvascular coronária em doentes diabéticos (15).
A minimização dos factores de risco de angina microvascular deve ser incentivada em todos os doentes (38). Pauly et al. estudaram o efeito do quinalapril (um inibidor da enzima de conversão da angiotensina) em 13 mulheres com angina microvascular e verificaram uma subida significativa na reserva de fluxo coronário (+0,55 ± 0,50) (108).
A prevenção secundária, com ácido acetilsalicílico e estatinas, está recomendada em todos os doentes diabéticos com angina microvascular. O efeito anti-inflamatório e anti-aterosclerótico das estatinas parece ser útil no tratamento da disfunção microvascular coronária (109).
Os beta-bloqueantes estão recomendados como terapêutica de primeira linha para controlo sintomático, pela redução das necessidades metabólicas do miocárdio e pelo aumento da perfusão diastólica. Os beta-bloqueantes de terceira geração (carvedilol e nebivolol) parecem ser os mais eficazes na recuperação da reserva do fluxo coronário (110).
Os bloqueadores dos canais de cálcio estão indicados se os beta-bloqueantes não permitirem um controlo eficaz dos sintomas ou não forem tolerados. Porém, um ensaio clínico com diltiazem não demonstrou correcção da diminuição da reserva coronária em doentes com angina microvascular (111).
As restantes opções terapêuticas estão suportadas por um menor nível de evidência científica. Estudos envolvendo fármacos como os moduladores do monóxido de azoto (sildenafil, L-arginina), alfa-bloqueantes ou anti-anginosos (ranolazina, ivabradina) têm tido resultados positivos, ainda que pouco significativos (39,70,112,113).
O tratamento com metformina está associado a recuperação da reserva do fluxo coronário e redução dos episódios de angina (64). Porém, não está provado que o controlo da glicémia contribua para a prevenção e reversão da disfunção microvascular coronária. Valenzuela-Garcia et al. analisaram 314 doentes com angina microvascular
36
(100 doentes com diabetes mellitus tipo 2 e 214 sem diabetes mellitus tipo 2) e concluíram que hemoglobina A1c inferior a 7,0 mg/dl não se associa a valores de reserva de fluxo coronário mais elevados (74).
37
Conclusão
Em doentes sem doença coronária obstrutiva, sobretudo se diabéticos, do sexo feminino ou idosos, a disfunção microvascular coronária pode manifestar-se clinicamente através de dor pré-cordial ou equivalentes anginosos (cansaço, dispneia, náuseas ou lipotimia) (21).
A angina microvascular tem, geralmente, um padrão estável. Porém, pode apresentar-se como síndrome coronária aguda sem supra-desnivelamento do segmento ST (18).
A angina microvascular não se associa a alterações segmentares da contractilidade miocárdica durante a ecocardiografia com teste de stress, dada a distribuição focal e predominantemente subendocárdica da isquémia provocada pela disfunção microvascular coronária (34).
Raramente, a disfunção microvascular coronária associa-se a síndrome coronária aguda com isquémia miocárdica transmural e alterações da contractilidade, em entidades com fisiopatologia muito específica e, em parte, desconhecida: a angina microvascular variante e a miocardiopatia de takotsubo (18).
O diagnóstico de disfunção microvascular coronária implica a realização de coronariografia (para excluir doença coronária obstrutiva) e teste de provocação intra-coronária com acetilcolina (para excluir angina de Prinzmetal) (33).
Porém, o diagnóstico é feito pela determinação de uma reserva de fluxo coronário igual ou inferior a 2,0, após ajuste para o sexo e idade. Este teste pode ser realizado por métodos invasivos (termodiluição ou Doppler intra-coronário durante cateterismo) (18) e não invasivos (ecocardiografia com Doppler da artéria descendente anterior, ecocardiografia de contraste miocárdico, tomografia por emissão de positrões com captação de rubídio-82 e ressonância magnética nuclear com captação de gadolínio) (18,56,57).
A disfunção microvascular coronária é uma complicação microvascular frequente da diabetes mellitus. A associação entre a hiperglicemia e a redução da reserva do fluxo coronário está bem demonstrada, mesmo em indivíduos sem evidência de doença cardiovascular (5,6,9,60).
A hiperglicemia induz disfunção endotelial e «remodeling» na microcirculação coronária, o que diminui a capacidade de ajustar o tónus vascular às necessidades metabólicas e de oxigénio do miocárdio (18).
38
A disfunção microvascular coronária é o principal mecanismo fisiopatológico da miocardiopatia diabética (66–75). Esta entidade corresponde a disfunção diastólica (e, mais raramente, sistólica) do ventrículo esquerdo, na ausência de doença arterial coronária, hipertensão arterial ou valvulopatias (76,81).
Em doentes diabéticos, a disfunção microvascular coronária prevê um aumento de risco de eventos cardiovasculares (doença coronária obstrutiva, enfarte agudo do miocárdio, insuficiência cardíaca ou morte súbita) sete vezes superior (27–29). Porém, ainda é escassa a evidência científica sobre o melhor algoritmo de diagnóstico e tratamento desta entidade.
39
Bibliografia
1. Cuculi F, Kharbanda R, Prendergast B. Low diagnostic yield of elective coronary angiography. N Engl J Med. 2010;363(1):93-94-95.
2. Adameova A, Dhalla NS. Role of microangiopathy in diabetic cardiomyopathy. Heart Fail Rev. 2014;19(1):25–33.
3. Swoboda PP, McDiarmid AK, Erhayiem B, Ripley DP, Dobson LE, Garg P, et al. Diabetes mellitus, microalbuminuria, and subclinical cardiac disease: Identification and monitoring of individuals at risk of heart failure. J Am Heart Assoc. 2017;6(7):1–11.
4. Factor, S. M., Minase, T., Cho, S., Fein, F., Capasso, J. M., Sonnenblick EH. Coronary Microvascular Abnormalities in the Hypertensive-Diabetic Rat - A Primary Cause of Cardiomyopathy? Am J Pathol. 1984;116:9–20.
5. Haffner, S. M., Lehto, S., Rönnemaa, T., Pyörälä K., Laakso M. Mortality from coronary heart disease in subjects with type 2 diabetes and nondiabetic subjects with and without prior myocardial infarction. N Engl J Med. 1998;339(4):229– 34.
6. Jenkins MJ, Edgley AJ, Sonobe T, Umetani K, Schwenke DO, Fujii Y, et al. Dynamic synchrotron imaging of diabetic rat coronary microcirculation in vivo. Arterioscler Thromb Vasc Biol. 2012;32(2):370–7.
7. Marciano C, Galderisi M, Gargiulo P, Acampa W, D’Amore C, Esposito R, et al. Effects of type 2 diabetes mellitus on coronary microvascular function and myocardial perfusion in patients without obstructive coronary artery disease. Eur J Nucl Med Mol Imaging. 2012;39(7):1199–206.
8. von Scholten BJ, Hasbak P, Christensen TE, Ghotbi AA, Kjaer A, Rossing P, et al. Cardiac 82Rb PET/CT for fast and non-invasive assessment of microvascular function and structure in asymptomatic patients with type 2 diabetes. Diabetologia. 2016;59(2):371–8.
9. Di Carli MF, Janisse J, Grunberger G, Ager J. Role of chronic hyperglycemia in the pathogenesis of coronary microvascular dysfunction in diabetes. J Am Coll Cardiol [Internet]. 2003;41(8):1387–93.
10. Lee WS, Kim J. Diabetic cardiomyopathy: Where we are and where we are going. Korean J Intern Med. 2017;32(3):404–21.
11. Sezer M, Kocaaga M, Aslanger E, Atici A, Demirkiran A, Bugra Z, et al. Bimodal pattern of coronary microvascular involvement in diabetes mellitus. J Am Heart Assoc. 2016;5(11):1–11.
12. Rydén L, Grant PJ, Anker SD, Berne C, Cosentino F, Danchin N, et al. ESC guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J. 2013;34(39):3035–87.
40
13. Leon BM. Diabetes and cardiovascular disease: Epidemiology, biological mechanisms, treatment recommendations and future research. World J Diabetes [Internet]. 2015;6(13):1246.
14. Labazi H, Trask AJ. Coronary microvascular disease as an early culprit in the pathophysiology of diabetes and metabolic syndrome. Pharmacol Res [Internet]. 2017;123:114–21.
15. Kibel A, Selthofer-Relatic K, Drenjancevic I, Bacun T, Bosnjak I, Kibel D, et al. Coronary microvascular dysfunction in diabetes mellitus. J Int Med Res [Internet]. 2017;30006051667550.
16. Pappachan JM, Varughese GI, Sriraman R, Arunagirinathan Joseph Pappachan GM. Diabetic cardiomyopathy: Pathophysiology, diagnostic evaluation and management. World J Diabetes [Internet]. 2013;4(45):177–89.
17. Matheus ASDM, Tannus LRM, Cobas RA, Palma CCS, Negrato CA, Gomes MDB. Impact of diabetes on cardiovascular disease: An update. Int J Hypertens [Internet]. 2013;2013(Cvd).
18. Crea F, Lanza GA, Camici PG (2014). Coronary Microvascular Dysfunction. eBook. First edition, Springer. Milan.
19. Radico F, Cicchitti V, Zimarino M, De Caterina R. Angina pectoris and myocardial ischemia in the absence of obstructive coronary artery disease: Practical considerations for diagnostic tests. JACC Cardiovasc Interv. 2014;7(5):453–63.
20. Jespersen L, Hvelplund A, Abildstrøm SZ, Pedersen F, Galatius S, Madsen JK, et al. Stable angina pectoris with no obstructive coronary artery disease is associated with increased risks of major adverse cardiovascular events. Eur Heart J. 2012;33(6):734–44.
21. Sara JD, Widmer RJ, Matsuzawa Y, Lennon RJ, Lerman LO, Lerman A. Prevalence of Coronary Microvascular Dysfunction Among Patients With Chest Pain and Nonobstructive Coronary Artery Disease. JACC Cardiovasc Interv. 2015;8(11):1445–53.
22. Bolognese L, Carrabba N, Parodi G, Santoro GM, Buonamici P, Cerisano G, et al. Impact of Microvascular Dysfunction on Left Ventricular Remodeling and Long-Term Clinical Outcome after Primary Coronary Angioplasty for Acute Myocardial Infarction. Circulation. 2004;109(9):1121–6.
23. Westergren H U, Michaëlsson E, Blomster, J I, Miliotis T, Svedlund S, Gan L. Determinants of coronary flow reserve in non-diabetic patients with chest pain without myocardial perfusion defects. PLoS One [Internet]. 2017;12(4):1–16. 24. Rubinshtein R, Yang EH, Rihal CS, Prasad A, Lennon RJ, Best PJ, et al.
Coronary microcirculatory vasodilator function in relation to risk factors among patients without obstructive coronary disease and low to intermediate Framingham score. Eur Heart J. 2010;31(8):936–42.