UNIVERSIDADE CATÓLICA DE BRASÍLIA
PROGRAMA DE PÓS-GRADUAÇÃO
STRICTO SENSU
EM EDUCAÇÃO FÍSICA
Massa livre de gordura e polimorfismos no gene Fator Neurotrófico
Ciliar (
CNTF
) em brasileiras pós-menopausadas
Autor: Luiz Humberto Rodrigues Souza Orientador: Prof. Dr. Rinaldo Wellerson Pereira Co-Orientador: Prof. Dr. Ricardo Jacó de Oliveira
LUIZ HUMBERTO RODRIGUES SOUZA
Massa livre de gordura e polimorfismos no gene Fator Neurotrófico
Ciliar (
CNTF
) em brasileiras pós-menopausadas
Dissertação apresentada ao Programa de Pós-Graduação Stricto Sensu em Educação Física da Universidade Católica de Brasília, como requisito para a obtenção do Título de Mestre em Educação Física.
Orientador: Prof. Dr. Rinaldo Wellerson Pereira
Co-Orientador: Prof. Dr. Ricardo Jacó de Oliveira
DEDICATÓRIA
Dedico este trabalho a três ilustres pessoas: Minha Mãe Sandra Cristina, um ser inigualável,
que me ensinou o melhor de todos os valores: “AMAR A VIDA COMO ELA É!”
Minha Vó Agripina, exemplo de amor, persistência e serenidade.
Minha Irmã Fernanda, pelo carinho, afeto, compreensão e confiança.
AGRADECIMENTOS
Talvez, aqui seja o momento mais oportuno para registrar minha gratidão pelas pessoas que convivi. Portanto, agradeço:
A Deus por ter me concedido o privilégio de concretizar esta meta, e ter colocado pessoas tão especiais na minha vida. Também agradeço à Santa Rita de Cássia por ter me iluminado durante esta árdua jornada de trabalho e estudos;
À minha mãe Sandra, meus avós Pedro e Agripina, minha irmã Fernanda e meu sobrinho Nélio Neto pela confiança, paciência e incentivo aos meus estudos. Gostaria de estender os sinceros agradecimentos aos demais familiares, que direta ou indiretamente, contribuíram nesta caminhada;
Ao orientador Prof. Rinaldo Wellerson pelas sábias orientações e pela imensurável paciência que teve comigo durante este tempo; valeu pelas informações e pela forma que conduziu nosso convívio, tentando me deixar o mais independente possível;
Ao co-orientador Prof. Ricardo Jacó pela incomparável acolhida no programa de pós-graduação. Gostaria de dizer que o nosso convívio pôde me tornar uma pessoa mais centrada com objetivos mais concretos e audaciosos. Seu espírito realista e de perspectivas contagia as pessoas que têm o privilégio de estar ao seu lado. Obrigado por tudo e principalmente pela amizade que pudemos construir;
À professora Geni de Araújo Costa pela sabedoria, experiência e oportunidade compartilhadas; também agradeço à professora Maria Helena Candelori pelas palavras de carinho e ensinamentos;
Às minhas grandes amigas Adriana Giavonni e Gislane Melo pelas palavras de carinho, atenção, oportunidades, confiança, ensinamentos. Vocês me fazem enxergar a vida sob uma óptica diferenciada. Aproveito a ocasião para dizer que meu amor por vocês NÃO SE DEVE AO ACASO, DEVE-SE À CONFIANÇA QUE SOLIDIFICAMOS AO LONGO DESTE TEMPO!
À minha irmã Luciana das Mercês pela paz e serenidade que carrega. Obrigado pela atenção, paciência e disposição. Lu, você foi um dos maiores achados da minha vida!
À minha grande amiga, irmã e companheira Vânia Lurdes (...). É muito difícil te agradecer!!! Apenas digo que te encontrar foi uma das maiores dádivas que DEUS pôde me conceder. Para mim, você é simplesmente demais!
À minha irmã mais crazy: Grassyara! Sua energia é contagiante. Saiba que acima de qualquer coisa, gosto e confio muito em você!
À amiga Mônica Miranda que sempre me ouviu e incentivou a crescer. Também te agradeço pelas inúmeras “idas e vindas” da asa norte. Obrigado pela confiança. Adoro-te!
Às amigas Maria Fátima Glaner e Nanci Maria França pelo companheirismo, aprendizado, atenção e momentos ímpares de descontração que me proporcionaram;
À minha esporádica família do mestrado: Lu Baiana, Kayte (sem base), Lourenzo e Juliano pelos momentos de descontração e aprendizado!
Às minhas grandes companheiras, Cíntia e Marilda, que jamais deixaram minha vida ficar monótona. Valeu pelo companheirismo, atenção e carinho. Vocês são 10! Também agradeço ao amigo João Cardeal pelos sábios ensinamentos, e ao pequeno Heitor pela alegria que transmite;
À ilustre amiga Dédima pela confiança e amizade compartilhada. Você mora no meu coração!
Às queridas colegas Graziela Cristina e Vanessa Cardoso, que também contribuíram para o meu aprendizado!
A todos aqueles que se hospedaram em minha casa e trouxeram paz, carinho e conhecimento para ser compartilhado, fazendo acima de tudo, que a minha vida nunca caísse em uma rotina!
Aos professores do Programa de Pós-Graduação em Educação Física que me ensinaram a trilhar este caminho com sabedoria;
Aos meus amigos de Tupaciguara, Uberlândia e da 53ª Turma de Educação Física/UFU que sempre me apoiaram; Agradeço, especialmente, à amiga Alana pelo incentivo, carinho e atenção;
Aos colegas Ricardo Moreno, Paulo Gentil e Breno Abreu que contribuíram de forma decisiva na realização deste estudo. Também agradeço à minha querida companheira de estudos, Lídia Mara, pelas dicas, informações e desabafos;
Aos alunos, funcionários e professores do Laboratório de Biotecnologia pela paciência e aprendizado. Agradeço especialmente a amiga Cena, que me deu carinho, atenção nos momentos mais tumultuados durante a elaboração deste trabalho. Não posso deixar de nomear e agradecer algumas pessoas que foram decisivas durante o construto deste estudo: Angélica, Tadeu, Érika, Túlio, Breno, Priscila Lasse, Rodrigo, Ana Cláudia, Kelly e Dione. Obrigado pela imensurável atenção!
Aos colegas do Projeto Geração de Ouro/UCB, especialmente à Thalyta Villar, que sempre se dispôs a me escutar nos momentos de angústia; Indubitavelmente, devo agradecer a todos os alunos do programa de Pós-graduação em Educação Física, pois o convívio com vocês contribuiu fortemente para o meu aprendizado;
Aos meus amigos de Uberlândia Bira, Vivi, Flávia e Marcelo que sempre me apoiaram a continuar os estudos; também devo agradecer a todos os alunos da Performance Academia/SESC-Uberlândia que me incentivaram a fazer o mestrado;
À Coordenação de Aperfeiçoamento Pessoal de Nível Superior (CAPES) pela bolsa de estudo concedida, sem a qual não haveria a concretização deste estudo;
EPÍGRAFE
TRÊS COISAS
SUMÁRIO
Lista de abreviaturas...09
Lista de tabelas...12
Lista de quadros...13
Lista de figuras...14
Resumo...15
Abstract...16
1. Introdução...17
2. Objetivos...21
3. Revisão de Literatura...22
3.1. Envelhecimento...22
3.2. Sistema Muscular...23
3.3. Envelhecimento e Massa Muscular...27
3.4. Sarcopenia...29
3.4.1. Fatores Relacionados à sarcopenia... 32
3.5. Genes que se associam com força e massa muscular...37
3.6. CNTF...…...41
4. Materiais e Métodos...47
4.1. Delineamento da Pesquisa...47
4.2. Amostra...47
4.3. Procedimentos Éticos...48
4.4. Procedimentos para a Coleta de Dados...48
4.4.1. Composição Corporal...48
4.4.2. Nível de Atividade Física...50
4.4.3. Análise do DNA...51
4.4.3.1. Extração do DNA...51
4.4.3.2. Quantificação do DNA...53
4.4.3.3. Polimorfismos no gene CNTF...54
4.4.3.4. Amplificação do DNA...54
4.4.3.5. Purificação e Seqüenciamento...56
4.5. Tratamento Estatístico...59
4.5.1. Freqüência alélica e genotípica...59
4.5.2. Equilíbrio de Hardy-Weinberg...59
4.5.3) Associação genotípica...59
4.5.4) Associação haplotípica...61
5. Resultados...62
5.1. Caracterização da amostra...62
5.2. Associação entre os genótipos do SNP rs1800169 no CNTF e MLG...64
5.3. Associação entre os genótipos do SNP rs2515363 no CNTF e MLG...66
5.4. Análise haplotípica...68
6. Discussão...69
6.1. Características da amostra...69
6.2. Freqüência alélica e genotípica dos SNPs rs1800169 e rs2515363...73
6.3. Paradoxo: manutenção de motoneurônios X efeitos caquéticos...77
6.4. O contexto dos estudos de associação...80
6.5. Implicações dos estudos genéticos para a sociedade...83
7. Conclusão...85
8. Referências Bibliográficas...87
9. Lista de definição de termos...105
10. Anexos...108
10.1. Anexo A: Termo de Consentimento Livre e Esclarecido...108
10.2. Anexo B: Questionário de Caracterização da Amostra...110
10.3. Anexo C: Seqüência Genômica do CNTF...111
LISTA DE ABREVIATURAS
A – adenina;
ACE - enzima conversora de angiotensina I (do inglês, Angiotensin I converting
enzime);
ANCOVA – análise de covariância (do inglês, analysis of covariance);
ANOVA – análise de variância (do inglês, analysis of variance); C – citosina;
CNTF - fator neurotrófico ciliar (do inglês, Ciliary neurotrophic factor);
CNTFR - receptor do fator neurotrófico ciliar (do inglês, Ciliary neurotrophic factor
receptor);
CNTFRα - receptor α do fator neurotrófico ciliar;
COL1A1 - colágeno alfa 1(do inglês, Collagen type I alpha 1);
CT-1 – cardiotrofina-1 (do inglês, cardiotrophin-1);
DMO – densidade mineral óssea;
DNA - ácido desoxirribonucléico (do inglês, deoxyribonucleic acid);
dNTP – deoxiribonucleotídeo trifosfato (do inglês, deoxyribonucleotide triphosphate);
DXA – absortometria por raios-X de dupla energia (do inglês, dual energy X-ray absorptiometry);
EDTA - ácido etilenodiaminotetracético (do inglês, ethylenediaminetetracetic acid); Exo I - enzima exonuclease I;
G – guanina;
GDF8 - fator de diferenciação do crescimento tipo 8/miostatina (do inglês, Growth
GH – hormônio do crescimento (do inglês, growth hormone);
gp130 - componente receptor glicoproteína-130; HCl – ácido clorídrico;
IBGE – Instituto Brasileiro de Geografia e Estatística;
IGF1 - fator de crescimento insulínico tipo 1 (do inglês, Insulin-like growth factor 1); IGF2 - fator de crescimento insulínico tipo 2 (do inglês, Insulin-like growth factor 2);
IL-1 - interleucina 1 (do inglês, interleukin 1);
IL-6 – interleucina-6 (do inglês, interleukin-6); IMC – índice de massa corporal;
IPAQ - questionário internacional de atividade física (do inglês, International Physical Activity Questionaire);
Jak – Janus quinase (do inglês, Janus Kinase);
kD – quilodalton;
LEEFS - Laboratório de estudos em educação física e saúde;
LIF - fator inibitório de leucemia (do inglês, leukemia inhibitory factor);
LIFRβ - receptor β do fator inibitório de leucemia (do inglês, leukemia inhibitory factor
receptor β);
MgCl2 – cloreto de magnésio;
MLG – massa livre de gordura;
MLGA – massa livre de gordura apendicular;
MLGAR – massa livre de gordura apendicular relativa;
MLGT – massa livre de gordura total;
MLGTR – massa livre de gordura total relativa;
NCBI - Centro Nacional para Informação em Biotecnologia (do inglês, National Center for Biotechnology Information);
NR3C1 - subfamília do receptor nuclear tipo 3, grupo C, membro 1/receptor de
glicocorticóide (do inglês, Nuclear receptor subfamily 3, group C, member
1/glucocorticoid receptor;
p – nível de significância;
pb – pares de base;
PCR – reação em cadeia da polimerase (do inglês, polymerase chain reaction); rpm - rotações por minuto;
SAP - enzima fosfatase alcalina (do inglês, Shrimp Alkaline Phosphatase); SDS – dodecil sulfato de sódio (do inglês, sodium dodecyl sulfate);
SNP - Polimorfismo de um único nucleotídeo (do inglês, Single Nucleotide
Polymorphism);
STAT – sinal de transdução ativador da transcrição (do inglês, signal transduction activator of transcription);
Taq – Thermus aquaticus; TE – tampão tris EDTA;
TNF- - fator de tumor necrose (do inglês, tumor necrosis factor alpha);
T.S - Tampão de seqüenciamento – 5x Sequencing Buffer (400 mM Tris-HCl, 10 mM
MgCl2, pH 9.0);
Tyk – tirosina quinase (do inglês, tyrosine kinase); UCB – Universidade Católica de Brasília;
LISTA DE TABELAS
TABELA 1: Características da amostra...62
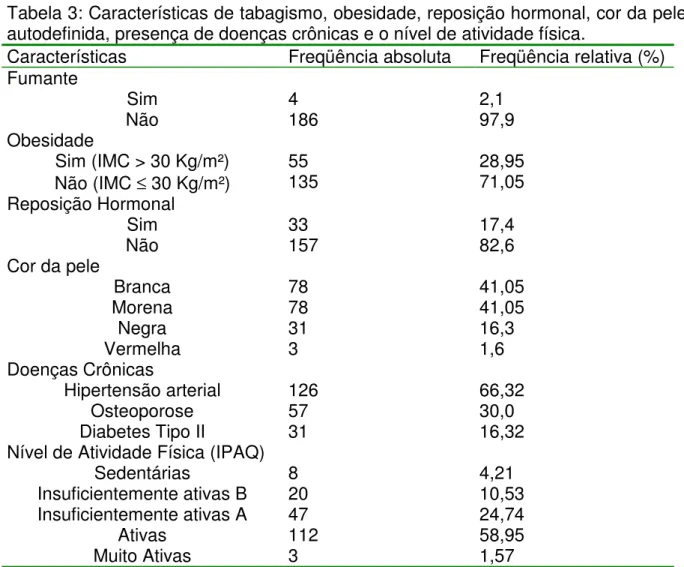
TABELA 2: Médias e desvios padrão dos fenótipos musculares de acordo com a faixa etária...62 TABELA 3: Características de tabagismo, obesidade, reposição hormonal, cor da
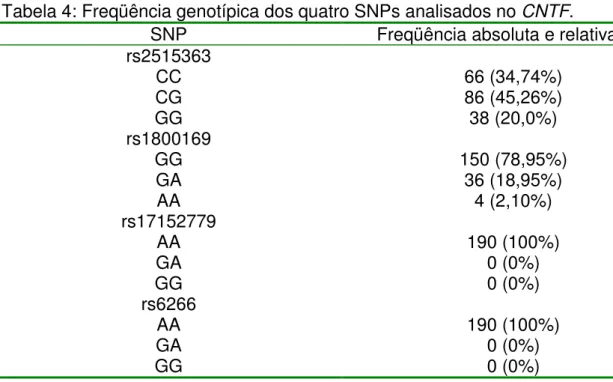
pele autodefinida, presença de doenças crônicas e o nível de atividade física...63 TABELA 4: Freqüência genotípica dos quatro SNPs analisados no CNTF...64
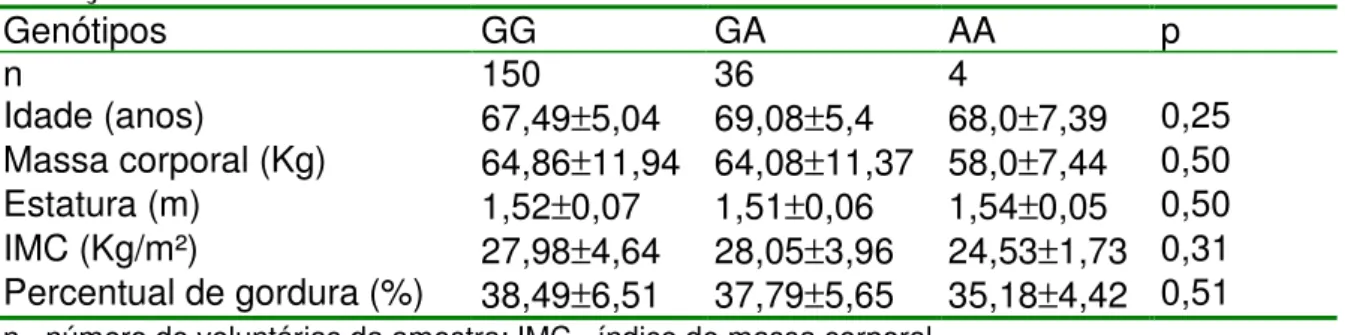
TABELA 5: Características físicas (média e desvio padrão) da amostra em relação à mutação nula do CNTF...65 Tabela 6: Características físicas das voluntárias homozigotas para o alelo G e das
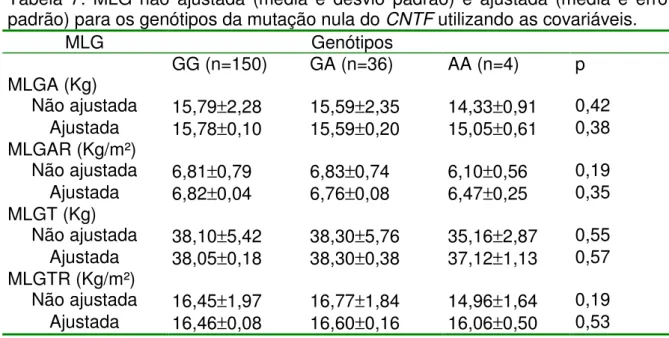
voluntárias que carregam o alelo A da mutação nula do CNTF...65 TABELA 7: MLG não ajustada (média e desvio padrão) e ajustada (média e erro
padrão) para os genótipos da mutação nula do CNTF utilizando as covariáveis...66 TABELA 8: Características físicas (média e desvio padrão) da amostra em relação aos genótipos do SNP rs2515363 do CNTF...67
Tabela 9: Características físicas das voluntárias homozigotas para o alelo C e das voluntárias que carregam o alelo G do SNP rs2515363 do CNTF...67
LISTA DE QUADROS
LISTA DE FIGURAS
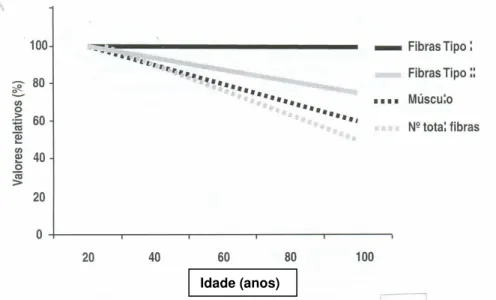
FIGURA 1: Redução do músculo devido à redução total do número de fibras e a atrofia das fibras tipo II ...26
FIGURA 2: Desenho esquemático ilustrando a perda progressiva de massa muscular...29 FIGURA 3: Mudança na massa muscular relacionada com a idade, em uma secção
transversa na coxa, de duas pessoas com IMC similar... 30 FIGURA 4: Influência de fatores que levam ao declínio da massa e força muscular
associada com a idade, bem como seu impacto na inabilidade e perda de independência...33 FIGURA 5: Desenho esquemático destacando que o CNTF encontra-se no braço
longo do cromossomo 11 (11q12.2)...41 FIGURA 6: Desenho esquemático do CNTF representando as regiões codificadoras
e não codificadoras...41
FIGURA 7: Apresentação do ponto de mutação (G→A) e a inserção dos 4
ribonucleotídeos no início do éxon...42 FIGURA 8: DXA modelo Lunar DPX-IQ (Lunar Corporation, Madison, WI, USA)...50
FIGURA 9: Quantificação do DNA...53
FIGURA 10: Termociclador da marca GeneAmp PCR System 9700, Applied
Biosystems, Foster City, CA, EUA...55
RESUMO
O envelhecimento provoca alterações no organismo que diminuem a capacidade das pessoas em realizar suas atividades cotidianas. Dentre essas modificações a perda de massa muscular, também conhecida como sarcopenia, tem se destacado, pois contribui na redução da autonomia e capacidade funcional dos idosos. A sarcopenia é influenciada por fatores ambientais e genéticos. Dentre os genes identificados até o momento, o CNTF por seu papel na formação das unidades neuromotoras e por conseqüência no estímulo das fibras musculares, é um candidato já investigado em alguns estudos. Este estudo verificou a associação entre SNPs do CNTF com os fenótipos da MLG, considerando-se a ancestralidade genômica, em 190 idosas brasileiras (67,81±5,16 anos). As voluntárias tiveram a MLG não óssea analisada através do DXA, e responderam um questionário para caracterização da amostra. O DNA genômico foi extraído de leucócitos do sangue e tiveram 806 pb do CNTF seqüenciados. Para verificar a associação entre os genótipos do CNTF com MLG, utilizou-se a análise de covariância. A estimativa e a análise de regressão dos haplótipos em função das covariáveis foram realizadas pela metodologia implementada no programa whap. A ancestralidade genômica individual foi estimada a partir das freqüências alélicas nas populações ancestrais pelo programa IAE3CI. Os SNPs rs17152779 e rs6266 não foram polimórficos na amostra estudada. A distribuição genotípica dos demais estava de acordo com o esperado para o equilíbrio de Hardy-Weinberg, porém não foi encontrada nenhuma associação genotípica com os fenótipos de MLG (p>0,05). Os resultados da análise de haplótipos também não mostraram associação (p>0,05). Dessa forma, para a amostra do presente estudo, não foi observada associação entre os polimorfismos do CNTF e os fenótipos musculares avaliados.
ABSTRACT
Aging evokes changes in the body that reduce people’s capacity of performing daily living activities. Among these alterations, the loss of muscle mass, also known as sarcopenia, has been stuck out, once it contributes for decreasing the autonomy and the functional capacity of the elders. Sarcopenia is influenced by environmental and genetic factors. Among the already identified genes, the CNTF is a candidate that has been investigated in some studies, due to its role in the formation of motor units and, consequently, in the stimulation of muscle fibers. This study verified the association between CNTF SNPs and the FFM phenotypes, considering genomic ancestry, in 190 Brazilian female elders (67,81±5,16 years). The volunteers had their nonosseous-FFM analyzed through the DXA and answered a questionnaire for sample characterization. The genomic DNA was extracted from blood leukocytes and had 806 base pairs sequenced along the CNTF. In order to verify the association between the CNTF SNPs genotypes and the FFM, covariance analysis was used. The haplotypes statistical inference and the regression analysis as a function of the covariants were performed using the methodology implemented in the software Whap. The individual genomic ancestry was estimated from the allelic frequencies in the ancestral populations, through the program IAE3CI. The SNP rs17152779 and rs6266 were not polymorphic in the sample studied. The genotypic distribution of the others was in agreement with the expected for the Hardy-Weinberg equilibrium, however no genotypic association was found with FFM phenotypes (p>0,05). The results of the haplotype analysis also showed no associations (p>0,05). This way, for the sample of this study, no associations were observed between the polymorphisms of CNTF and the muscular phenotypes assessed.
1.
INTRODUÇÃO
Parafraseando Beauvoir (1970) “o envelhecimento tem, sobretudo, uma dimensão existencial e, como todas as situações humanas, modifica a relação do
homem com o tempo, com o mundo e com a sua própria história, revestindo-se não
só de características biopsíquicas, como também sociais e culturais”. Sabe-se que
este processo está associado a uma maior disposição para receber influências
físicas e emocionais, e que a expressão dessas suscetibilidades encontra-se na dependência da complexa interação de fatores físicos, psicológicos, sociais,
econômicos e culturais, tornando o envelhecer um processo extremamente individualizado marcado pelos padrões socioculturais de uma época (GUERREIRO, RODRIGUES, 1999).
O envelhecimento acarreta modificações nos aparelhos locomotor, cardiovascular, respiratório e queda do metabolismo basal devido à diminuição da
massa muscular e aumento de tecido adiposo. A perda de massa muscular e a diminuição de massa óssea estão entre as alterações orgânicas mais importantes no processo de envelhecimento, sendo os grandes responsáveis pela redução na
autonomia e capacidade funcional do idoso (BARBOSA, 1999; BOOTH, CHAKRAVARTHY, SPANGENBURG, 2002). Estas alterações são respectivamente
denominadas de sarcopenia e osteoporose (ROSENBERG, 1989; SCHAPIRA, SCHAPIRA, 1992).
O entendimento dos fatores ambientais e genéticos, que tornam os idosos
mais propensos à perda muscular e óssea, está entre os grandes desafios em direção ao estabelecimento de medidas terapêuticas eficientes que possam retardar
entendimento torna-se ainda mais importante tendo em vista o notório aumento da
expectativa de vida nas populações em países desenvolvidos e em desenvolvimento (RAMOS, 1993).
Entre os fatores ambientais importantes no processo de perda muscular,
pode-se citar a prática irregular de exercícios físicos, uma dieta precária em nutrientes e o uso de álcool (BURCKHARDT, MICHEL, 1989; HUI, SLEMENDA,
JOHNSTON, 1990; KELLY, EISMAN, SAMBROOK, 1990; NEWITT, 1994; GOYER et al. 1994; BERGLUND et al. 2000; GÜR et al. 2003) que podem agravar as
alterações musculares, uma vez que deixa os idosos mais suscetíveis às quedas
e/ou outras fatalidades (TRAPPE et al. 2001; CARTER et al. 2002; STEL et al. 2004; ROBINE, MICHEL, 2004; CAPODAGLIO et al. 2005).
É do conhecimento científico o papel de fatores genéticos nas alterações musculares decorrentes do envelhecimento, muito embora a identificação destes fatores e o peso de cada um deles ainda esteja em sua infância (ARDEN, SPECTOR, 1997; TIAINEN et al. 2004). Apesar do estágio inicial em que se
encontram os estudos para identificação e caracterização dos genes envolvidos nos fenótipos musculares, há um esforço empreendido desde 2001 em catalogar genes
importantes à performance física e saúde em humanos, e alguns candidatos aparecem de maneira recorrente (RANKINEN et al. 2001; RANKINEN et al. 2002; PERUSSE et al. 2003; RANKINEN et al. 2004; WOLFARTH et al. 2005; RANKINEN
et al. 2006). Dentre eles, está o fator de diferenciação do crescimento tipo
8/miostatina (GDF8, do inglês Growth differentiation factor 8/myostatin), o receptor
inglês Angiotensin I converting enzime) e o fator neurotrófico ciliar (CNTF, do inglês Ciliary neurotrophic factor).
A Universidade Católica de Brasília vêm desde 2000 através do programa multidisciplinar de extensão “Geração de Ouro” contribuindo para o envelhecimento
saudável da população do Distrito Federal e entorno. A partir deste projeto de extensão, projetos de pesquisa também com enfoque multidisciplinar estão sendo
desenvolvidos. Dentre eles, pode-se destacar o projeto colaborativo entre o Programa de Pós-Graduação em Educação Física e o Programa de Pós-Graduação em Ciências Genômicas e Biotecnologia sob as coordenações do Prof. Dr. Ricardo
Jacó de Oliveira e o Prof. Dr. Rinaldo Wellerson Pereira, respectivamente. Este projeto visa identificar genes importantes para a variação dos fenótipos ósseos e
musculares, bem como a relação entre polimorfismos genéticos e resposta a atividade física em mulheres pós-menopausa. Duas dissertações de mestrado foram concluídas no âmbito desta proposta (GENTIL, 2006; LIMA, 2006b). O trabalho aqui
apresentado também é parte deste projeto e tem como foco polimorfismos no gene CNTF e variações no fenótipo de massa muscular em mulheres pós-menopausadas.
Ip et al. (1991) descreveram que as atividades biológicas do CNTF são
largamente restritas às células do sistema nervoso, entretanto Helgren et al. (1994) mostraram que este gene pode exercer função no músculo esquelético quando
submetido a lesões. Assim, essas informações além de comprovar a ação neurotrófica já conhecida do CNTF, mostram que ele exerce efeitos miotróficos por minimizar as mudanças morfológicas e funcionais associadas com desnervação do
Esta dissertação investigou a relação entre quatro polimorfismos no gene CNTF e suas possíveis implicações na massa muscular em brasileiras
pós-menopausadas, uma vez que não foram encontrados, nos grandes bancos de referências bibliográficas, trabalhos em que se tenha estudado o CNTF e fenótipos
musculares na população brasileira.
O reconhecido grau de miscigenação na população brasileira (PARRA et al. 2003; CALLEGARI-JACQUES et al. 2003; MARRERO et al. 2005) e o conhecimento
de que o fenótipo massa muscular possui heterogeneidade entre grupos populacionais (OBISESAN et al. 2005) traz o risco de obtenção de resultados
espúrios. A miscigenação pode levar a obtenção de resultados espúrios quando se tem uma doença/fenótipo com incidência diferenciada entre grupos populacionais (KNOWLER et al. 1988). Em situações como esta, tem-se uma maior representação
de indivíduos com ancestralidade para um determinado grupo entre os casos. Assim, alelos mais freqüentes neste grupo populacional aparecerão espuriamente associados à doença em questão (KNOWLER et al. 1988).
Dessa forma, vários métodos têm sido desenvolvidos no sentido de corrigir a estratificação gerada pela miscigenação (DEVLIN, ROEDER, 1999; PRITCHARD,
ROSENBERG, 1999; HOGGART et al. 2003). Apesar de controvérsias sobre o efetivo papel da estratificação como causa de resultados espúrios em estudos de
associação, resultados empíricos apontam para um impacto considerável da miscigenação em estudos de associação (MARCHINI et al. 2004; CHOUDHRY et al. 2006). Para análise dos resultados deste trabalho também foram utilizados dados de
2.
OBJETIVOS
2.1) Objetivo Geral
• Verificar a associação de polimorfismos no gene CNTF com o fenótipo de massa livre de gordura em brasileiras pós-menopausadas.
2.2) Objetivos Específicos
• Genotipar os SNPs rs2515363, rs1800169, rs17152779 e rs6266 em uma amostra de 190 mulheres pós-menopausa previamente avaliadas através da técnica de absortometria por raios-X de dupla energia (DXA do inglês, Dual Energy X-Ray Absorptiometry) e caracterizadas por meio de
questionários;
• Verificar se as distribuições genotípicas encontram-se de acordo com o Equilíbrio de Hardy-Weinberg;
• Analisar a associação entre os genótipos dos SNPs polimórficos e fenótipos musculares na população estudada, levando em consideração a ancestralidade genômica;
3.
REVISÃO DE LITERATURA
3.1) Envelhecimento
De acordo com o Instituto Brasileiro de Geografia e Estatística (IBGE, 2000), responsável pelo Censo Demográfico do país, em 1970 o Brasil contava com 4,7
milhões de pessoas com mais de 60 anos (o que representava 5,05% da população total); em 1980 já eram 7,2 milhões (6,06%); em 1991 a população de idosos
cresceu para 10,7 milhões (7,30%). No final do ano 2000, o número de idosos era 14,5 milhões (8,6%).A projeção para o ano de 2020, quando a expectativa de vida estiver alcançando 75,5 anos, mostra que a população será formada por 16,2
milhões de idosos - 1 em cada 13 brasileiros pertencerá à população idosa (CAMARGO, 1995; BERQUÓ, 1999; LITVOC, BRITO, 2004). A estimativa para o
ano de 2025 mostra que a população geral aumentará em cinco vezes e que a população idosa terá um aumento de 25 vezes. Por volta de 2080, a proporção de jovens e idosos deverá se estabilizar em 20% e 15% do total, respectivamente
(CAMARANO, 1989; LITVOC, BRITO, 2004).
O envelhecimento populacional traz mudanças nas principais causas de
morbidade e mortalidade, de tal modo que as doenças não-transmissíveis e as causas externas passam a predominar sobre as doenças transmissíveis, já que os idosos apresentam um maior risco de adquirirem doenças crônicas e desenvolverem
incapacidades (PORTO, 2001). De forma geral, as mudanças com a senescência podem englobar alterações de natureza sensória (visão, propriocepção), motora
envelhecimento resulta em um decréscimo progressivo de força e massa muscular que está associado com o declínio na capacidade funcional (ROTH et al. 1999).
Nesse processo, a musculatura esquelética perde uma quantidade significativa de fibras musculares glicolíticas tipo II, bem como sua habilidade contrátil
(GOODPASTER et al. 2001). Essas alterações contribuem para enfermidades, fadiga e lentidão do movimento, além de limitar as habilidades do idoso em
desempenhar suas atividades de vida diária (KIRKENDALL, GARRETT, 1998). Ainda, pode associar-se com o aumento do risco de quedas, fraturas de quadril e mudanças psicológicas adversas, o que pode trazer limitações para a realização das
tarefas cotidianas (LINDLE et al. 1997), resultando na perda de independência (PETRELLA, MILLER, CRESS, 2004).
3.2) Sistema Muscular
Segundo Junqueira e Carneiro (1999), o tecido muscular, responsável pelos movimentos corporais, é constituído por células alongadas que contêm grande quantidade de filamentos citoplasmáticos, responsáveis pela contração. As células
musculares têm origem mesodérmica e sua diferenciação ocorre principalmente devido a um alongamento gradativo, com simultânea síntese de proteínas
filamentosas. De acordo com suas características morfológicas e funcionais, podem se distinguir nos mamíferos em músculo liso, músculo estriado cardíaco e músculo estriado esquelético: o primeiro, cujo processo de contração é lento e não está
sujeito ao controle voluntário, é formado por aglomerados de células fusiformes e não possuem estrias transversais; o músculo estriado cardíaco que apresenta
por células alongadas e ramificadas, que se unem por intermédio dos discos
intercalares; já o músculo estriado esquelético que tem contração rápida, vigorosa e sujeita ao controle voluntário, é formado por feixes de células cilíndricas muito longas e multinucleadas, e também apresentam estrias transversais.
O músculo estriado esquelético possui três camadas de tecido conjuntivo: a mais externa que o envolve totalmente é chamada epimísio; à medida que se move
para o interior, um tecido conjuntivo denominado perimísio envolve feixes individuais de fibras musculares. Esses feixes são os fascículos, e cada fibra muscular que o constitui é revestida por um tecido nomeado endomísio (POWERS, HOWLEY,
2000). Estes tecidos conjuntivos mantêm as fibras musculares unidas, permitindo que a força de contração gerada individualmente atue sobre o músculo inteiro.
Sendo assim, o papel desse tecido tem grande significado funcional, porque na maioria das vezes as fibras não se estendem de uma extremidade do músculo até a outra (JUNQUEIRA, CARNEIRO, 1999).
Além de apresentar papel metabólico e de locomoção, o músculo é o maior depósito de proteínas no corpo, e sua capacidade funcional depende da qualidade e quantidade destas proteínas musculares, que são provavelmente mantidas através
de um processo de remodelagem contínuo envolvendo sua síntese e quebra. Sabe-se que um declínio na sínteSabe-se da proteína específica é uma indicação de queda no
processo de remodelagem, com possíveis conseqüências funcionais. Portanto, a perda de massa muscular pode ocorrer se a taxa de síntese de proteínas for menor que a taxa de quebra (BALAGOPAL et al. 1997).
Existem dois tipos de fibras musculares que apresentam características contráteis e metabólicas peculiares. As fibras vermelhas ou do tipo I (tônicas e de
presentes em músculos envolvidos na manutenção da postura, têm maior densidade
capilar, fluxo sangüíneo e atividade de enzimas oxidativas. Considerando que essas fibras utilizam predominantemente o metabolismo oxidativo para a produção de energia, a adaptação vascular e enzimática ocorre para atender à demanda
metabólica local. Por outro lado, as fibras brancas ou do tipo II (fásicas e de contração rápida) são subdivididas em grupos que variam de acordo com o seu
potencial oxidativo. As fibras tipo IIa apresentam contração rápida, mas também possuem uma capacidade oxidativa razoável. Já as fibras do tipo IIb são glicolíticas e apresentam maior capacidade anaeróbia que as do tipo IIa (KIRKENDALL,
GARRETT, 1998; AIRES, 1999).
A redução de massa muscular oriunda da desnervação das fibras musculares
relacionada com a idade, particularmente das fibras tipo II, pode conduzir à atrofia. Na tentativa de minimizar esta perda, motoneurônios colaterais das fibras tipo I expandem-se para algumas fibras musculares desnervadas tipo II. Desta forma, a
massa muscular dos idosos torna-se menor, apresenta uma proporção mais alta de fibras tipo I, e é mais fraca em função da perda de fibras glicolíticas (KIRKENDALL, GARRETT, 1998).
A figura 1 mostra que a diminuição do músculo deve-se a perda do número total de fibras e a atrofia de fibras tipo II. Devido a redução do tamanho destas fibras,
FIGURA 1: Redução do músculo devido à redução total do número de fibras e a atrofia das fibras tipo II. FONTE: adaptado de SOTO et al. 2003.
Em 1991, Charette et al. evidenciaram o decréscimo da força e massa muscular com a idade, de modo que as fibras musculares tipo II atrofiaram enquanto
as fibras tipo I não. De encontro com esta informação, Hagerman et al. (2000) encontraram que as fibras vermelhas são pouco afetadas com o envelhecimento,
enquanto as brancas podem sofrer uma redução de 26% no seu tamanho. Elliott, Sale e Cable (2002) mostraram que sujeitos sedentários apresentam uma redução de 50% nas fibras musculares tipo II, o que implica em perdas funcionais
significativas.
Segundo Frontera et al. (2000a), poucos estudos longitudinais de força têm
comparado mudanças na função do músculo com as devidas alterações no tamanho e tipo da fibra muscular. Afirmam ainda, que a força da musculatura extensora dos joelhos é uma preditora de dependência e sobrevivência. Portanto, compreender a
disfunção deste grupo muscular no envelhecimento pode contribuir com importantes implicações clínicas e sociais. Neste sentido, os autores buscaram avaliar, em um
grupo de homens idosos durante 12 anos, as mudanças longitudinais na força dos
músculos flexores e extensores de joelho e cotovelo e na área de secção transversa
do quadríceps. Os resultados mostraram que houve uma redução significativa na força muscular isocinética da musculatura analisada, bem como na área de secção transversa. Sendo assim, foi sugerido que estas alterações podem contribuir para
que os idosos tornem-se mais frágeis e debilitados.
3.3) Envelhecimento e Massa Muscular
Está bem estabelecido que o processo de envelhecimento, desde a
maturidade até a senescência, associa-se com um declínio significante na função neuromuscular (DOHERTY, 2003), na massa livre de gordura e no aumento do
conteúdo de gordura no corpo (BASU, BASU, NAIR, 2002). Segundo Klein, Rice e Marsh (2001), as alterações na força relacionadas com a idade estão diretamente correlacionadas com a perda de massa muscular esquelética. Foi demonstrada que
a área de secção transversa do músculo total diminui em 40% entre os 20 a 60 anos (VANDERVOOT, 2002). Sua mensuração tem sido determinada em vários grupos musculares através da ultrasonografia, tomografia computadorizada, ressonância
magnética, medidas diretas por dissecação de cadáveres (DOHERTY, 2003), bem como pela técnica DXA (BASU, BASU, NAIR, 2002).
Sabe-se que a perda de tecido muscular esquelético contribui significativamente para a redução de massa magra corporal (KENT-BRAUN, ALEXANDER, YOUNG, 2000), e isto se associa fortemente com mudanças nos
diversos sistemas do corpo humano, como no sistema cardiovascular, nervoso, músculo-esquelético, endócrino, bem como no desempenho das atividades
resultado da senescência, está relacionada com o prejuízo de várias habilidades
funcionais (AL-ABDULWAHAB, 1999).
Neste sentido, a relação entre envelhecimento e decréscimo progressivo de força e massa magra pode culminar com a redução da capacidade funcional,
diminuição do nível de atividade física (ROTH et al. 2000), associação às fraturas osteoporóticas (GALLAGHER et al. 1997), indução a inabilidades (FRONTERA et al.
2000b), provocar mudanças na composição corporal, contribuir para limitações funcionais, imobilidade e fragilidade (GALLAGHER et al. 2000), prejudicar o desempenho das tarefas da vida diária (REEVES, NARICI, MAGANARIS, 2004a),
desencadear alterações no sistema neuromuscular, levar a desordens no equilíbrio metabólico (HÄKKINEN et al. 2001), além de limitar a vida independente que pode
cooperar com as quedas e outras formas de morbidades (REEVES, NARICI, MAGANARIS, 2004b).
Um estudo realizado por Hughes et al. (2001) examinou as modificações na
força dos músculos flexores e extensores do cotovelo e joelho em idosos durante um período de 10 anos. Tanto para os homens quanto para as mulheres, o declínio na força isocinética foi em média de 14% e 16% por década para os músculos
extensores e flexores de joelho, respectivamente. Quanto aos extensores e flexores de cotovelo, as mulheres demonstraram taxa mais lenta de queda que os homens.
Segundo os dados encontrados na literatura, pode-se notar que a perda de massa e força muscular durante o envelhecimento tem sido identificada, decisivamente, como um importante fator que contribui para o declínio da
independência (FLYNN et al. 1999). Portanto, manter a autonomia é uma meta primária de cuidado à saúde pública para adultos velhos, pois a busca pela
cognitivas, que em conseqüência, otimizam o desempenho físico na função
cotidiana (PETRELLA, MILLER, CRESS, 2004).
3.4) Sarcopenia
Sarcopenia é uma palavra do idioma grego criada por Irwin Rosenberg em 1988, em que sarx significa carne e penia significa perda (ROSENBERG, 1989).
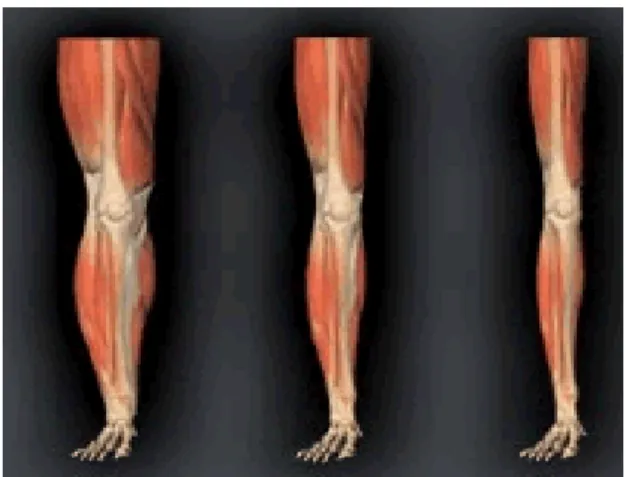
Sarcopenia refere-se à perda involuntária de força e massa muscular esquelética (BROSS, JAVANBAKHT, BHASIN, 1999; SKELTON, BEYER, 2003). As figuras 2 e 3
mostram, respectivamente, a perda progressiva de massa muscular e as alterações relacionadas com a idade.
FIGURA 2: Desenho esquemático ilustrando a perda progressiva de massa muscular.
FONTE: http://www.bioethics.gov/images/sarcopenia.gif
21 anos
63 anos
FIGURA 3: Mudança na massa muscular relacionada com a idade, em uma secção transversa na coxa, de duas pessoas com IMC similar.
FONTE: adaptado de http://www.gtxinc.com/graphics/ bmi.jpg
A etiologia deste fenômeno é multifatorial e envolve mudanças no metabolismo do músculo, desordens endócrinas, fatores nutricionais, mitocondriais e
genéticos (MISHRA, MISRA, 2003). Atualmente, a sarcopenia é usada para descrever modificações relacionadas com a idade que ocorrem dentro do músculo
esquelético, e desse modo inclui os efeitos da alteração central e inervação do sistema nervoso periférico, efeitos inflamatórios, mudanças hormonais e da ingestão de proteínas. Todos esses fatores contribuem com a sarcopenia, atrofia muscular
esquelética e a fragilidade, que são considerados os maiores pivôs da perda de mobilidade funcional e independência dos idosos (ROUBENOFF, 2001).
Em um trabalho realizado por Baumgartner et al. (1998), foi estimada a
prevalência da sarcopenia entre voluntários residentes no Novo México, participantes do estudo intitulado “New México Elder Health Survey”. A sarcopenia
foi definida como a musculatura esquelética apendicular relativa (Kg/m2) inferior a dois desvios padrão abaixo da média encontrada para jovens. A prevalência
acima de 80 anos de idade. A sarcopenia foi significativamente associada com a
inabilidade física auto relatada pelos homens e mulheres, independente da etnia, idade, renda e estado de saúde. Sendo assim, estes resultados apontam fortes evidências que sarcopenia é um importante problema de saúde pública entre os
idosos.
A revisão realizada por Roth, Ferrell e Hurley (2000) elucidou a magnitude da
perda de massa e força muscular, suas conseqüências funcionais e a eficácia do treinamento de força como uma intervenção para os efeitos do atraso, prevenção ou reversão da sarcopenia. Encontrou-se que o treinamento é uma intervenção efetiva
para melhorar força, massa e qualidade muscular, além de retardar a fragilidade física adjacente ao envelhecimento. Entretanto, as diferenças de sexo e fatores
genéticos podem desenvolver um papel importante na determinação da resposta muscular.
Jassen, Heymsfield e Ross (2002) buscaram estabelecer a prevalência da
sarcopenia e inabilidade física em 4504 norte-americanos com idade igual ou superior a 60 anos, e testar a hipótese de que a sarcopenia está relacionada com inabilidade funcional. Os sujeitos foram considerados normais quando apresentaram
índice de massa muscular maior que um desvio padrão acima do sexo específico para adultos jovens. A sarcopenia classe I foi considerada para sujeitos que
apresentaram o índice entre um e dois desvios padrão em relação aos valores de referência, enquanto a classe II foi presente em sujeitos que manifestaram índice abaixo de dois desvios padrão. A prevalência da primeira classe foi de 59% para as
mulheres e 45% para os homens. Quanto à segunda classe de sarcopenia, a prevalência foi de 10% e 7% para as mulheres e homens, respectivamente. A
maior em homens e três vezes maior em mulheres com sarcopenia classe II, quando
comparados aos homens e mulheres com índice normal. Dessa forma, uma redução relativa na massa muscular esquelética em idosos norte-americanos é uma ocorrência comum, que está significativamente associada com perda funcional e
inabilidade, particularmente em mulheres senis. Estas observações dão suporte à visão de que a prevalência da sarcopenia é um importante indicador da causa de
morbidade entre as pessoas idosas.
3.4.1) Fatores Relacionados à Sarcopenia
Sabe-se que a perda de massa muscular derivada da redução de fibras é
responsável pela sarcopenia. Entretanto, fatores hormonais, metabólicos, nutricionais, imunológicos, moleculares e o nível de atividade física também contribuem para este processo (WELLE, 2002; BASU, BASU, NAIR, 2002; SOTO et al. 2003). Ademais, Dirks e Leeuwenburgh (2002) mostraram que uma redução
significante de força e massa muscular pode ser devido à perda de motoneurônios, uma vez que no envelhecimento a carência de estímulos contribui com este prejuízo.
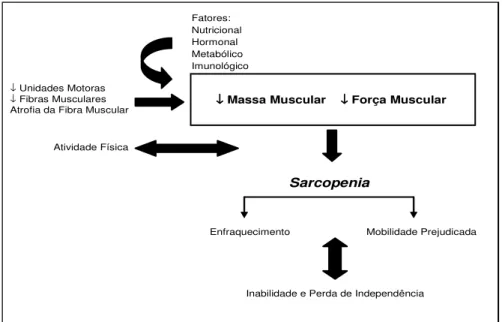
FIGURA 4: Influência de fatores que levam ao declínio da massa e força muscular associada com a idade, bem como seu impacto na inabilidade e perda de independência.
FONTE: adaptado de DOHERTY, 2003.
O estudo de Doherty e Brown (2002) demonstrou uma perda no funcionamento das unidades motoras na musculatura proximal e distal das
extremidades superiores e inferiores, o que pode conduzir a alterações orgânicas funcionais. McComas (1998) observou que o declínio importante das unidades
motoras começa a partir dos 70 anos, coincidindo com o aumento na prevalência da fragilidade. A partir desta mesma faixa etária, nota-se que a desnervação desempenha um papel relevante na queda de massa e qualidade muscular (SOTO
et al. 2003).
Diversos hormônios desempenham um papel no turnover da proteína
muscular, seja ele anabólico - como o hormônio do crescimento (GH, do inglês growth hormone) e testosterona que aumentam a síntese protéica, e a insulina que
inibe a sua quebra; do estresse - como o cortisol e glucagon que causam
catabolismo muscular; ou da tireóide, em que tanto o excesso quanto a deficiência podem aumentar a degradação muscular. O nível de GH diminui com a idade, e sua
Fatores: Nutricional Hormonal Metabólico Imunológico
↓ ↓ ↓
↓Massa Muscular ↓↓↓↓Força Muscular
Sarcopenia ↓Unidades Motoras
↓Fibras Musculares Atrofia da Fibra Muscular
Atividade Física
Enfraquecimento Mobilidade Prejudicada
administração para adultos mais velhos acarreta aumento do nível de fator de crescimento insulínico tipo I (IGF-I, do inglês insulin growth factor), aumentando a
massa muscular total e força. Entretanto, os resultados da reposição de GH não são universalmente positivos, pois aumentam a síntese protéica do corpo todo com um
reticente efeito na musculatura esquelética, levando a compreender que a síntese de proteína não muscular pode aumentar com reposição deste hormônio. Já a
testosterona, tem muitos efeitos no músculo, osso, próstata e medula óssea, e a partir da quarta década de vida seu nível sangüíneo apresenta um declínio gradual (BASU, BASU, NAIR, 2002). O estudo de Brodsky, Bolagopal e Nair (1996) mostrou
que homens submetidos a reposição de testosterona apresentaram um aumento na massa muscular e diminuição na massa gorda.
A redução dos níveis de IGF-I relacionada com o envelhecimento normal também pode ser afetada pela qualidade da nutrição, nível de atividade física, doenças coexistentes, ingestão de álcool e função renal. O IGF-I é um potente
mediador de alterações na massa muscular e força, e pela razão de sua importância clínica no envelhecimento, pode contribuir no desempenho das tarefas dependentes do músculo (O’CONNOR, TOBIN, HARMAN, 1998; KAKLAMANI et al. 1999). Na
pesquisa de Cappola et al. (2001), foi investigada a relação entre baixos níveis de IGF-I, pouca força muscular e mobilidade em mulheres idosas. Encontrou-se que
baixa concentração de IGF-I relaciona-se com dificuldade auto-relatada em tarefas de mobilidade, escassa força muscular dos extensores de joelho e caminhada lenta. Já a miostatina, é uma proteína secretada que funciona como um regulador
negativo de massa muscular (McNALLY, 2004). Durante a embriogênese, é expressa no desenvolvimento da musculatura esquelética e atua na regulação do
produzida pelo músculo esquelético, circula no sangue e tende a limitar o crescimento de fibras musculares (LEE, 2004). Em um estudo realizado por Zhu et
al. (2000) avaliou-se o papel da miostatina no estado degenerativo do músculo, e foi
evidenciado que sua inibição pode ser apropriada para o tratamento de doenças
degenerativas musculares como as distrofias ou degenerações musculares associadas ao envelhecimento.
Lalani et al. (2000) investigaram em ratos, se a perda muscular associada
com vôo espacial era acompanhada por aumento nos níveis de miostatina e redução nos níveis de IGF-I e II no músculo. Notaram que o nível intramuscular de IGF-I não
foi diferente entre os grupos experimental e controle. Por outro lado, a perda muscular esquelética que ocorre durante o vôo associa-se com o aumento de
miostatina e um decréscimo de IGF-II (fator de crescimento insulínico tipo II). Estes dados mostram que mudanças recíprocas na expressão da miostatina e IGF-II podem contribuir para fisiopatologias multifatoriais da atrofia muscular que ocorrem
durante o vôo espacial.
Um estudo feito por dE Martino et al. (2000) demonstrou que a interleucina-6 (IL-6, do inglês interleukin-6) inibe a secreção do IGF-I e sua atividade biológica,
sugerindo que o efeito negativo do IL-6 na função muscular pode ser mediada através do IGF-I. Barbieri et al. (2003) avaliaram o efeito do IGF-I e IL-6 na função
muscular em 526 pessoas. Após os ajustes realizados para idade, sexo e IMC notou-se que o IGF-I, IL-6, bem como sua interação foram significativamente preditores de força de punho e potência muscular. De encontro com esta
informação, Cappola et al. (2003) investigaram se mulheres idosas com baixo nível de IGF-I e alto nível de IL-6 estão mais propensos a incapacidades, e verificaram
progressivas. Portanto, a união de forma adequada, entre IGF-I e IL-6 pode ser uma
estratégia importante para prevenir ou imunimizar as alterações associadas com o envelhecimento.
Roth et al. (2006) recentemente descreveram a importância dos fatores
inflamatórios no desenvolvimento da sarcopenia. Estes autores mostraram que a perda de massa muscular e as limitações funcionais dos idosos podem ser devido aos altos níveis do fator de tumor necrose (TNF- , do inglês tumor necrosis factor
alpha), interleucina 1 (IL-1, do inglês interleukin 1) e IL-6, uma vez que estes fatores
estão envolvidos no processo de catabolismo muscular. Dessa forma, Schaap et al.
(2006) investigaram se os níveis séricos de marcadores inflamatórios como a IL-6, a proteína reativa C e a proteína antiquimotripsina-1 estavam associadas com perda
de massa e força muscular em 986 voluntários idosos. Os resultados sugeriram que altos níveis de IL-6 e proteína reativa C aumentam o risco de perda na força muscular, enquanto altos níveis de antiquimotripsina-1 diminuem o risco na perda
de força muscular em idosos.
Outro fator que afeta a sarcopenia é o status nutricional, pois com o avançar da idade tende-se a ocorrer uma ingestão cada vez mais pobre de alimentos (SOTO
et al. 2003), e a senescência induz a uma redução nas adaptações metabólicas. A
fragilidade nutricional é decorrente das inabilidades inerentes à velhice, devido à
acentuada perda involuntária de peso e de massa muscular. Este dano deve-se à redução da ingesta calórica, embora sua possível etiologia, ainda inclua causas fisiológicas e não fisiológicas (BALES, RITCHIE, 2002).
A atividade física também diminui com a idade, privando o músculo de um dos mais importantes estímulos ambientais para manter sua massa e função. Está bem
massa muscular e maior prevalência de incapacidades (SOTO et al. 2003). Neste
sentido, os exercícios apropriados podem estabelecer uma combinação de estímulos para manter a integridade do tecido durante o envelhecimento (EDSTRÖM, ULFHAKE, 2005).
Em um estudo realizado por Szulc et al. (2004) foram investigados, em 845 homens de 45-85 anos, os fatores de risco para a sarcopenia. O índice de massa
muscular esquelética apendicular diminuiu com a idade e aumentou com a intensidade da atividade física de trabalho. Os fumantes apresentaram menor índice de massa em relação aos sujeitos que nunca fumaram. Os homens que
participavam de exercícios regulares durante o tempo livre tiveram índice de massa 2.2% mais alto diante daqueles que não os faziam.
3.5) Genes que se associam com força e massa muscular
Segundo Wolfarth et al. (2005) existem alguns estudos que evidenciam a
associação de genes candidatos ao fenótipo de força e massa muscular. Dentre estes genes pode-se citar o GDF8, Subfamília do receptor nuclear tipo 3, grupo C,
membro 1/receptor de glicocorticóide (NR3C1, do inglês Nuclear receptor subfamily 3, group C, member 1/glucocorticoid receptor), Receptor do fator neurotrófico ciliar
(CNTFR, do inglês Ciliary neurotrophic factor receptor), Fator de crescimento
insulínico tipo 2 (IGF2, do inglês Insulin-like growth factor 2), VDR, COLIA1, ACE e CNTF.
polimórficas na miostatina, e a mais comum foi um polimorfismo de restrição para a enzima ApaI. Este polimorfismo leva a mudança K153R, ou seja, fazendo com que
uma arginina seja codificada no lugar da lisina. Os valores encontrados sugerem que as mulheres heterozigotas e homozigotas para o alelo que leva a codificação de
uma arginina apresentam menor força muscular, quando comparadas com aquelas homozigotas para o alelo que leva a codificação de uma lisina.
Koper et al. (1997) identificaram um polimorfismo no gene receptor de
glicocorticóide que consiste em duas mutações, sendo uma no códon 22 e outra no códon 23 (ER22/23EK). A primeira mutação não altera a codificação do aminoácido
glutamato, mas a segunda resulta na troca de uma arginina por uma lisina. Neste sentido, van Rossum et al. (2004) investigaram se há associação entre o polimorfismo ER22/23EK, composição corporal e força muscular em 350 pessoas
com idade de 13 a 36 anos. Foi identificado que 8% eram portadores deste polimorfismo. Os homens de 36 anos que carregam ER22/23EK eram mais altos,
tinham maior massa corporal, maior circunferência de coxa e mais força muscular de braços e pernas. Observou-se também que não houve diferenças significantes no IMC. Nas mulheres de 36 anos, a relação cintura/quadril tendeu ser menor em
portadoras de ER22/23EK, e não foi encontrada diferença significativa no IMC.
Roth et al. (2003) identificaram três polimorfismos no gene CNTFR: C1703T, T1069A e C174T. Foi estudada a associação destas variações do CNTFR com
força, massa muscular e composição corporal em 465 homens e mulheres de 20 a 90 anos. Somente a variação C174T foi significativamente associada com fenótipos
Em um estudo realizado por Sayer et al. (2002) foi determinado se o polimorfismo ApaI no gene IGF-2 explica a ligação entre estatura e peso do
nascimento com a força de punho na vida adulta. Após a análise distinta do genótipo IGF-2 e do peso de nascimento, notou-se que ambos foram preditores significantes
da força de punho em homens adultos, porém as associações não foram encontradas entre as mulheres. Quando o genótipo IGF-2 e peso do nascimento em
homens foram estudados simultaneamente, observou-se que também contribuíram de forma significativa para a força de punho. Estes resultados mostraram que o polimorfismo do gene IGF-2 e peso do nascimento têm efeitos independentes na
força estudada, porém sugerem que o polimorfismo verificado não explica a associação entre estatura do nascimento e força de punho na vida adulta.
A concentração imprópria de vitamina D é facilmente encontrada nos idosos, sendo resultado de inúmeros fatores de risco que interagem nesta população. Esta condição também se associa com a fragilidade do músculo, que abaixo de certo
limiar afeta a mobilidade e habilidade funcional, colocando pessoas idosas em alto risco de quedas e fraturas (JANSSEN, SAMSON, VERHAAR, 2002). Desta forma, Endo et al. (2003) notaram que o VDR contribui para a manutenção da homeostase
nas células musculares esqueléticas, e neste sentido suportaram a idéia de que o músculo é um alvo fisiológico direto da ação deste gene.
No estudo de Roth et al. (2004) foi investigada a associação dos genótipos do
VDR com massa livre de gordura em 302 homens idosos caucasianos. Todos foram
genotipados para os polimorfismos FokI (FF; Ff; ff) e BsmI (BB; Bb; bb). O
polimorfismo BsmI não foi associado com MLG em nenhuma análise, enquanto o FokI foi associado com MLG total, MLG apendicular absoluta e relativa. O grupo FF
Já Lima (2006b) investigou a associação entre MLG e os polimorfismos ApaI, Cdx-2, BsmI, FokI e TaqI do gene VDR em 191 mulheres brasileiras pós-menopausadas.
Nenhuma das variações alélicas do VDR foi associada com o fenótipo de MLG. O colágeno tipo I, uma proteína abundante nos ossos, é composto de cadeias
alfa 1 e alfa 2 codificadas, respectivamente, pelos genes COLI1A1 e COL1A2. Uma substituição de guanina por timina no fator de transcrição Sp1 ligado ao sítio da região promotora do gene COL1A1 tem sido associada com densidade mineral
óssea - DMO (GRANT et al. 1996). Sendo assim, van Pottelbergh et al. (2001) examinaram se em homens acima de 70 anos, o polimorfismo Sp1 do gene COL1A1
estava associado com DMO e força muscular. A presença do alelo s foi significativamente associada com baixa DMO no antebraço distal e no quadril, menor
força de punho e bíceps no braço dominante. Portanto, este polimorfismo do gene COL1A1 associou-se com DMO no antebraço e com força muscular dos membros
em homens idosos.
Folland et al. (2000) estudaram em 33 homens jovens ativos, o efeito dos
genótipos da enzima conversora de angiotensina I (ACE) sobre as mudanças na força do quadríceps, em resposta a 9 semanas de um programa de treinamento. Foi
observado que os sujeitos com o alelo D mostraram maior ganho de força (II- 9,0 ±
1,7%; ID- 17,6 ± 2,2%; DD- 14,9 ± 1,3%) com o treinamento isométrico. Conforme
3.6) CNTF
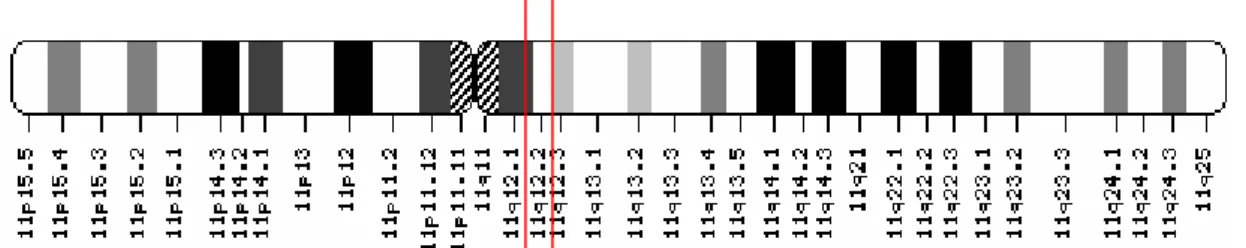
O gene CNTF promove a sobrevivência de várias células neuronais (IP et al. 1991), e está localizado no cromossomo 11q12.2 (GIOVANNINI, ROMO, EVANS,
1993), conforme figura abaixo.
FIGURA 5: Desenho esquemático destacando que o CNTF encontra-se no braço longo do cromossomo 11 (11q12.2).
FONTE: GIOVANNINI, ROMO, EVANS, 1993.
Em seguida, o gene CNTF está esquematicamente representado com as regiões codificadoras ou exons (compartimentos em negrito) e não codificadoras ou introns (linhas).
FIGURA 6: Desenho esquemático do CNTF representando as regiões codificadoras e não codificadoras.
FONTE: LAM et al. 1991.
A proteína codificada por este gene é um peptídeo de 200 aminoácidos com peso molecular de 22 kD, cuja ação, a princípio, parecia ser restrita ao sistema
nervoso, onde ela promove a sobrevivência e o crescimento demasiado - desencadeado pelo processo inflamatório - em certas populações neuronais. A
pode ser relevante na redução da destruição tecidual durante ataques inflamatórios (LAM et al. 1991; VERGARA, RAMIREZ, 2004). Em 1994, Takahashi et al.
identificaram um polimorfismo no gene CNTF, em que o alelo mutado é representado por uma transição de guanina para adenina na posição -6 do primeiro
íntron. Esta mutação promove a inserção de 4 ribonucleotídeos no início do éxon 2,
resultando na produção de uma proteína truncada com apenas 62 aminoácidos. Nos
391 japoneses avaliados, 61,9% foram homozigotos normais, 35,8% heterozigotos e 2,3% homozigotos mutantes. A ilustração a seguir mostra o ponto de mutação e a inserção de quatro ribonucleotídeos no início do éxon.
FIGURA 7: Apresentação do ponto de mutação (G→A) e a inserção dos 4 ribonucleotídeos no início do éxon. FONTE: Adaptado de TAKAHASHI et al. 1994.
O CNTF foi inicialmente identificado e descrito pela sua habilidade em promover o crescimento dos neurônios parassimpáticos dos gânglios embrionários de aves (BARBIN, MANTHORPE, VARON, 1984). Além disso, outros estudos
demonstraram a habilidade do CNTF em promover o crescimento de neurônios sensórios (SKAPER, VARON, 1986), simpáticos (BLOTTNER, BRUGGEMANN, UNSICKER, 1989), hipocampais (IP et al. 1991) e motoneurônios (ARAKAWA,
SENDTNER, THOENEN, 1990; SENDTNER et al. 1991). De acordo com Stöckli et al. (1991) esta citocina é encontrada principalmente no citoplasma das células de
Schwann mielinizadas e nos astrócitos, contudo, o mecanismo pelo qual ocorre sua liberação ainda permanece obscuro. Por outro lado, foi sugerido (SENDTNER et al.
Alelo normal
1997) que a danificação de um nervo pode causar a ruptura dessas células,
permitindo assim, sua liberação.
Além das funções desempenhadas pelo CNTF, descritas anteriormente, Masu et al. (1993) demonstraram que a anulação da expressão gênica do CNTF em ratos
resultou em uma atrofia progressiva e perda de motoneurônios, que culminou em uma pequena, mas significante redução na força muscular. Em 1993, no estudo realizado por Forger et al. foi examinada a habilidade do CNTF em prevenir a
degeneração do sistema neuromuscular em ratas em desenvolvimento, e se constatou que o CNTF pôde preservar os motoneurônios, além de resultar em um
aumento de 17% na área das fibras musculares. Diante das evidências encontradas nestes estudos, nota-se que o CNTF, além do papel neurotrófico já estabelecido,
também desempenha função miotrófica (VERGARA, RAMIREZ, 2004).
Em 1997, Marques e Neto também notaram que o CNTF reduz a atrofia observada com a desnervação, sugerindo seu papel como um fator trófico para as
células musculares. Neste sentido, os autores estudaram os efeitos da administração do CNTF in vivo na capacidade de regenerar fibras musculares esqueléticas. Os resultados mostraram que o CNTF aumentou o número de
miofibras em regeneração, porém os valores vistos nos grupos controle e tratamento não foram significativamente diferentes. Posteriormente, Guillet et al. (1999)
verificaram que o CNTF participa na sobrevivência de motoneurônios, reduz a desnervação induzida por atrofia do músculo esquelético e aumenta força muscular. O estudo realizado por Wang e Forsberg (2000) mostrou que os efeitos do CNTF no
metabolismo da proteína foram dependentes do tempo e da dose. O CNTF, quando administrado em concentrações que variam de 1 a 10 ng/ml, aumentou a síntese de
síntese de proteínas não-miofibrilares. Exposições longas ao CNTF (24h) reduzem a
síntese de proteínas não-miofibrilares e não tem efeito na síntese de proteínas miofibrilares. Altas concentrações de CNTF (10 a 20 ng/ml) reduziram a degradação de proteínas miofibrilares, mas não tem efeito na degradação de proteínas
não-miofibrilares.
Fraysse et al. (2000) relataram que a administração subcutânea de CNTF
preveniu a redução de força e a atrofia do músculo solear de ratos, sugerindo, portanto, que o CNTF desempenha efeitos tróficos no tecido muscular. Peroulakis e Forger (2000) observaram se o volume do músculo do assoalho pélvico é
aumentado em ratas tratadas com CNTF durante o período de nascimento. Constataram que o tratamento com CNTF aumentou o número de fibras musculares
em mais de 300%, porém não apresentou efeitos no tamanho das fibras.
Roth et al. (2001) examinaram a relação entre o CNTF e força muscular em 494 homens e mulheres saudáveis. A idade, sexo e massa corporal foram usados como covariáveis. Os indivíduos heterozigotos (G/A) para a mutação nula do CNTF
exibiram maior pico de torque concêntrico dos músculos extensores e flexores do joelho que homozigotos G/G. Quando a MLG dominante foi usada no lugar de
massa corporal, o pico de torque concêntrico de extensores de joelho também foi significativamente melhor nos indivíduos G/A. O mesmo foi observado para a
qualidade muscular nos extensores de joelho dos voluntários G/A. Estes dados indicam que indivíduos exibindo o genótipo G/A possuem melhor força e qualidade muscular, bem como contração relativamente mais rápida que indivíduos G/G.
Ramirez, Retamal e Vergara (2003) estudaram os efeitos de baixas doses de CNTF liberado sistematicamente por uma bomba osmótica, através das
desnervados. O CNTF induziu descargas elétricas espontâneas e mostrou forças de
contração nos músculos inervados, mas não preveniu as mudanças induzidas por desnervação. Em baixas doses, o CNTF não exerceu seu papel miotrófico sobre os músculos desnervados, mas afeta claramente as propriedades excitáveis e
contráteis dos músculos inervados. Desta forma, estes estudos contribuem fortemente na confirmação de que o CNTF pode desempenhar um importante papel
em nível muscular.
Na perspectiva de compreender o mecanismo de ação do CNTF, Ip e Yancopoulos (1996) mostraram que seus efeitos são mediados através de um
complexo tripartido composto pelos receptores gp130, LIFRβ e CNTFRα. Enquanto
gp130 e LIFRβ são expressos em diversos tecidos, particularmente no fígado,
medula óssea, sistema nervoso central, tecido adiposo e músculo esquelético, a
expressão do componente α é mais restrita às células nervosas (DAVIS et al. 1991;
IP et al. 1993), embora altos níveis CNTFRα estejam presente no músculo
esquelético (DAVIS et al. 1993; HELGREN et al. 1994). Estes três componentes,
inicialmente, não estão associados à superfície da célula, mas formam um complexo na resposta para o CNTF.
A primeira etapa na formação do complexo envolve a ligação do CNTF ao seu
componente α, que recruta os receptores gp 130 e LIFRβ para formar o complexo
(DAVIS et al. 1993; STHAL, YANCOPOULOS, 1994). A heterodimerização dos
componentes β, induzida pela ligação do CNTF ao CNTFRα, inicia a sinalização do
processo por ativar as tirosinas quinases Jak/Tyk que permitem a fosforilação destes
componentes β gerando um local de entrada para moléculas sinalizadoras como o
STAT3. O STAT3 também é fosforilado pelas quinases Jak, e nesta condição, ele
seqüência específica do DNA e ativar a transcrição do gene alvo (IP,
4.
MATERIAIS E MÉTODOS
4.1) Delineamento da Pesquisa
Trata-se de um estudo transversal, em que a variável dependente é o fenótipo de massa livre de gordura e as variáveis independentes são os genótipos do CNTF
(THOMAS, NELSON, 2002).
4.2) Amostra
Foram selecionadas 190 voluntárias em fase pós-menopausa, fisicamente
independentes (SPIRDUSO, 1995), com idade média de 67,81±5,16 anos,
residentes no Distrito Federal e inscritas no Projeto Geração de Ouro. Nenhuma mulher apresentou significativos problemas de saúde e/ou incapacidade que
pudesse ser agravada com o protocolo dos testes. Todas as participantes assinaram o Termo de Consentimento Livre e Esclarecido, no qual foram explicados os
objetivos, os procedimentos adotados, os possíveis desconfortos, bem como os riscos e benefícios decorrentes da realização deste estudo (ANEXO A). Adotou-se neste delineamento os seguintes critérios de exclusão:
• Não ter nacionalidade brasileira;
• Incapacidade de caminhar sem a assistência de outra pessoa;
• Não autorizar a coleta de uma amostra de sangue venoso;