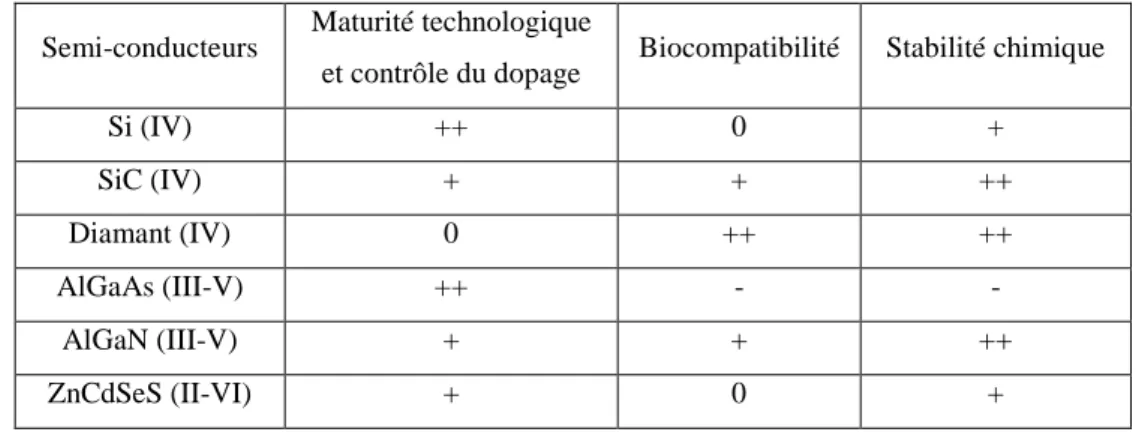
Je ne les remercierai jamais assez, notamment lors de la relecture et de la fameuse aide à la traduction anglaise du manuscrit. 3 De nombreux travaux portent actuellement sur l'étude du comportement de la surface d'un matériau en interaction avec son microenvironnement. Voici quelques exemples de ces semi-conducteurs en fonction de leur maturité technologique, de leur contrôle du dopage, de leur biocompatibilité et de leur stabilité chimique de surface (Tableau 1).
L'objectif de cette thèse est d'utiliser ce matériau, le diamant, comme support pour la réalisation de biocapteurs. Dans un chapitre d'introduction, je présenterai l'état de l'art concernant les aspects biologiques et chimiques de la surface du diamant. Ensuite, j'étudierai en détail les différentes méthodes de fonctionnalisation de la surface du diamant et tenterai de comparer leur stabilité chimique.
On peut noter que ce manuscrit ne mentionne pas la création d'un biocapteur. D’autre part, un biocapteur enzymatique ampérométrique a été produit à l’aide d’une méthode de fonctionnalisation de surface en diamant, actuellement en instance de brevet.
GENERALITES – ETAT DE L’ART
L A BIOCOMPATIBILITE DU DIAMANT
- Introduction
- L’hémocompatibilité du diamant
- Les cellules adhérentes
- a. Les ostéoblastes et les fibroblastes
- b. Les neurones
L A FONCTIONNALISATION DU DIAMANT
- Le diamant hydrogéné
- Oxydation et fonctionnalisation
- a. Les différentes voies d’oxydation de la surface du diamant
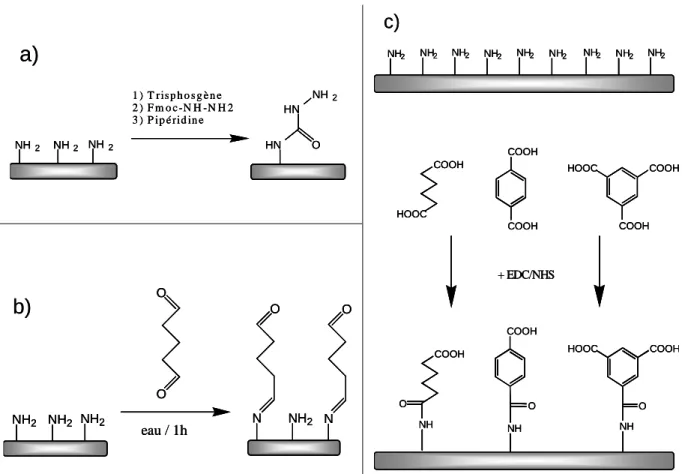
- b. La fonctionnalisation via les groupements oxydés (C-O par voie chimique)
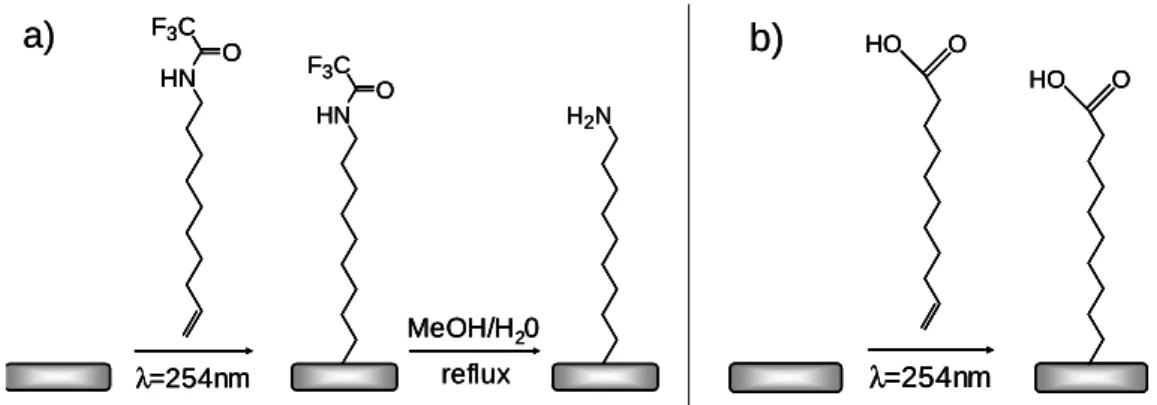
- La fonctionnalisation des surfaces hydrogénées avec formation de liaisons C-C
- La fonctionnalisation des surfaces hydrogénées avec formation d’autres liaisons
- Bilan
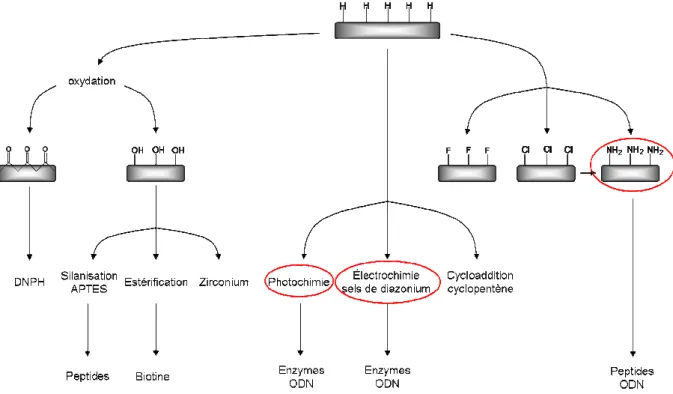
Ces modifications de surface ont été utilisées dans le cadre de l'étude de la biocompatibilité du diamant. Le schéma de la figure I-22 résume l'ensemble des travaux dédiés à la fonctionnalisation de la surface du diamant. Cette fonctionnalisation de la surface du diamant par la biotine démontre alors l'aspect générique du greffage.
Ainsi, le film proche de la surface du diamant a été réduit aux fonctions amino et hydroxylamine. Pour confirmer la présence de biotine à la surface du diamant, tous les échantillons ont été caractérisés par microscopie à fluorescence. L'image de fluorescence (Figure IV-A-22fluo) confirme la présence de biotine localement immobilisée en surface.
171 Sur la figure IV-B-12 on peut observer le spectre caractéristique de la surface du diamant avec la présence des trois composants résumés dans le tableau IV-B-2. La figure IV-B-15 montre le spectre de la zone N1s obtenue après greffage d'un complexe de ruthénium sur une surface de diamant.
A PPLICATIONS : DIAGNOSTIQUE ET BIO - DETECTION
- Les biopuces
- Les biocapteurs
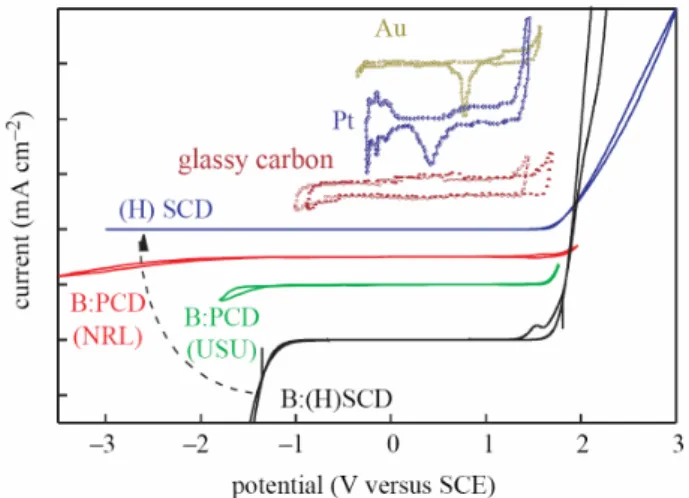
- a. Les biocapteurs ampérométriques
- b. Les transistors à effet de champ (FET)
LE DIAMANT – SYNTHESE ET CARACTERISATIONS
S TRUCTURE ET PROPRIETES DU DIAMANT
L A SYNTHESE DU DIAMANT
- La technique HPHT
- La technique CVD
- Les bâtis de synthèse de l’Institut Néel et du LIST
- a. Institut Néel
- b. LIST
- Préparations et conditions de croissance du diamant monocristallin
- a. Préparation des substrats de diamant
- b. Conditions de croissance des couches homoépitaxiées selon l’orientation (100)
- c. Conditions de croissance des couches homoépitaxiées selon l’orientation (111)
- Préparations et conditions de croissance du diamant polycristallin
- a. Institut Néel
- b. LIST
C ARACTERISATIONS DES COUCHES DE DIAMANT
- La cathodoluminescence (CL)
- La microscopie électronique à balayage (MEB)
- La spectroscopie à effet Raman
LA BIOCOMPATIBILITE DES ELECTRODES DE DIAMANT
L E DIAMANT POLYCRISTALLIN
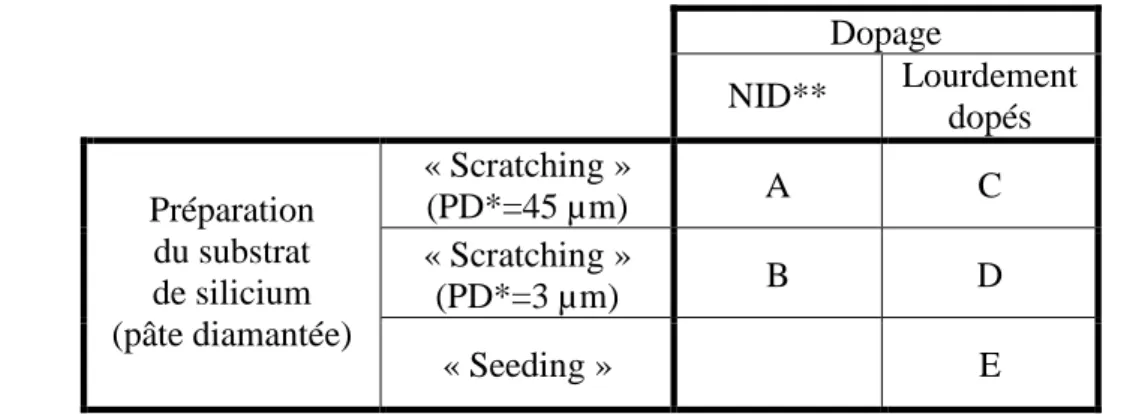
- Les différents paramètres d’étude : dopage et rugosité
- a. La rugosité de surface
- b. Le dopage
- Les angles de contact
- Adhésion, prolifération et morphologie des cellules
- a. L’adhésion cellulaire
- b. La prolifération des pré-ostéoblastes
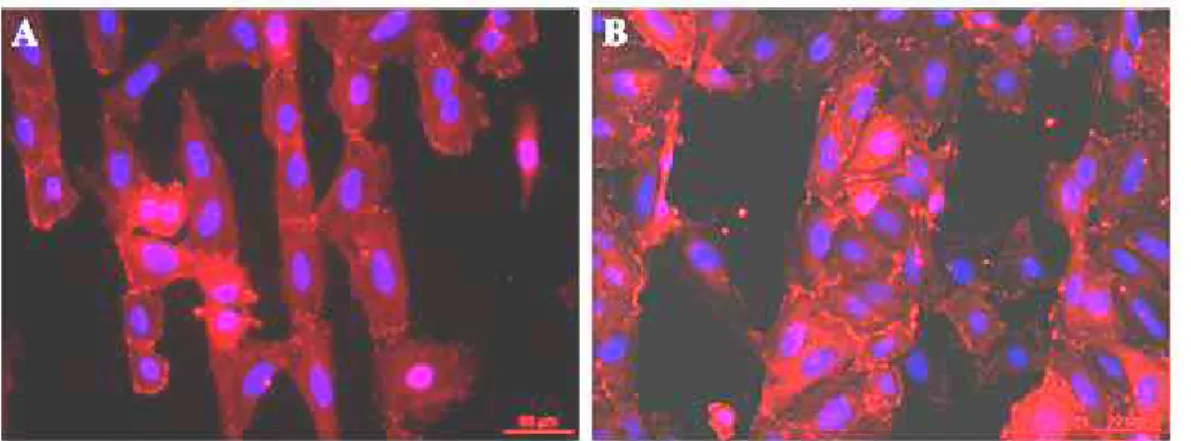
- c. Etude morphologique des cellules sur nos échantillons
Toutes les zones explorées mesuraient 20x20 µm², ce qui correspond à la surface caractéristique des cellules que nous avons utilisées. Cependant, la rugosité rms ne représente qu'une valeur caractéristique de la direction perpendiculaire à la surface : elle ne donne finalement aucune information sur le diamètre des motifs. Le dopage constitue un paramètre important de biocompatibilité puisque les dopages importants à la surface des échantillons provoquent une quantité de bore dont on pourrait penser à première vue qu'elle pourrait être toxique pour les cellules.
Les échantillons A et B contiennent moins de 1 ppm (parties par million) de bore par rapport à tous les atomes de carbone qui composent la surface. Le caractère hydrophile/hydrophobe d'une surface est mesuré en déposant une goutte calibrée de solvant sur la surface d'un échantillon. Lorsque les échantillons quittent le cadre de croissance après un plasma d’hydrogène, la surface est très hydrophobe car composée uniquement de liaisons CH.
La surface n'est alors plus constituée uniquement de liaisons CH, mais également de liaisons hydroxyles. Ce changement de composition doit donc affecter la valeur de l'angle de contact, et la surface doit devenir plus hydrophile. Les mesures d'angle de contact sur tous les échantillons sont résumées dans le tableau III-3.
Dans notre cas, la surface spécifique augmente lorsque la rugosité diminue (figures III-1b, III-1d, III-1f), ce que nous avons pour les échantillons fortement dopés. Nous venons de démontrer que le dopage ainsi que la rugosité étaient des paramètres importants liés au caractère hydrophile/hydrophobe de la surface des échantillons. Grâce à une courbe d'étalonnage, développée pour chaque expérience, nous pouvons extraire colorimétriquement la densité de cellules vivantes attachées à la surface des échantillons.
Enfin, lorsque la rugosité est moindre (50 nm rms), la surface présente plusieurs sites d'adhésion des cellules (Figures III-1). En revanche, un paramètre est important : la rugosité : il semble exister une limite, située entre 50 et 200 nm rms, en dessous de laquelle les cellules adhèrent plus facilement à la surface. 109 Lorsque le diamant est nanocristallin (Figure III-7a, échantillon E : B-NCD), on peut observer que les cellules s'étendent et s'ajustent parfaitement à la surface.
L E DIAMANT MONOCRISTALLIN
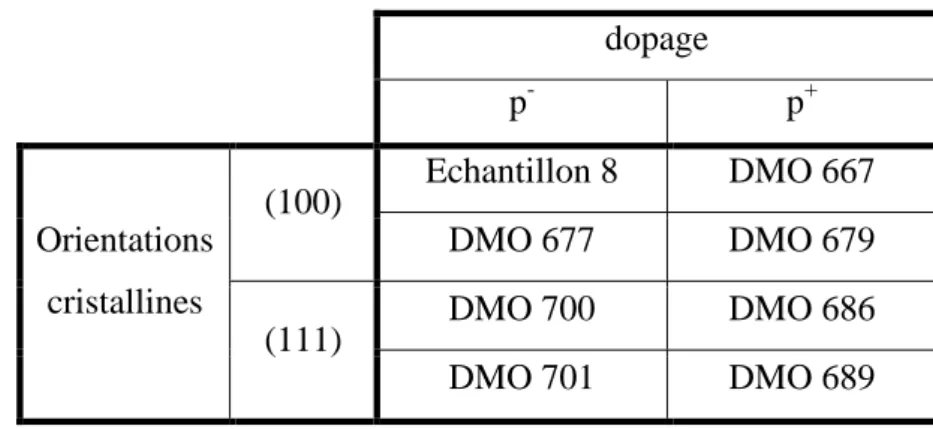
- Les différents paramètres d’études : orientations cristallines, dopage et angles de contact
- a. Le dopage
- b. Les angles de contact
- Adhésion et prolifération des cellules
- a. L’adhésion cellulaire
- b. La prolifération des pré-ostéoblastes
Cette différence vient probablement de la surface spécifique plus grande de l’échantillon NCD par rapport à celle de l’échantillon µCD (figure III-1). La figure IV-A-16 montre le voltamogramme du premier et du deuxième cycle de réduction. La réduction des fonctions nitro situées à l'extérieur de la couche a été réalisée chimiquement (figure IV-A-18).
Nous avons comparé l'efficacité de la réduction chimique avec la réduction électrochimique en utilisant la spectroscopie XPS. Ainsi, toutes les étapes permettant le clivage de la biotine après réduction chimique étaient efficaces. Ainsi, ces résultats permettent de confirmer que l'étape de réduction des sels de diazonium par électrophotographie représente l'étape clé du clivage et de la localisation des amorces d'amarrage à la surface du diamant.
On remarque que la fluorescence reste homogène sur toute la parcelle, indiquant une bonne répartition macroscopique de la biotine en surface. L'histogramme de la figure IV-A-24 montre l'intensité relative de fluorescence en fonction de ces deux paramètres. Ce comportement diffère significativement de celui observé lors de l'évolution de la concentration en sels de diazonium.
La réduction des espèces n'est plus possible du fait de la limitation du transfert électronique à travers le film généré en surface. En revanche, le comportement capacitif est sans doute lié à une diminution de la réactivité de la surface du diamant. Avec ces deux spectres XPS de référence de la zone C1s que nous venons de compiler (complexe immobilisé sur or (partie IV.B.c.) et surface nue du diamant (partie IV.B.d.)), nous pouvons identifier le complexe immobilisé à la surface du diamant immobilisé , étudié.
Une oxydation de surface semble s'être produite lors des étapes électrochimiques (synthèse et caractérisation) et/ou lors du stockage des échantillons. En conclusion, nous avons pu nous rendre compte de la complexité de la caractérisation par film XPS du complexe métallique immobilisé à la surface du diamant, notamment dans la région C1s-Ru3d. Dans le cas présenté ici, le potentiel diminue légèrement, cela est dû à la modification de la surface de l'électrode par des complexes de greffage.
FONCTIONNALISATION DE LA SURFACE DU DIAMANT VIA L’UTILISATION
L E GREFFAGE DE LA BIOTINE
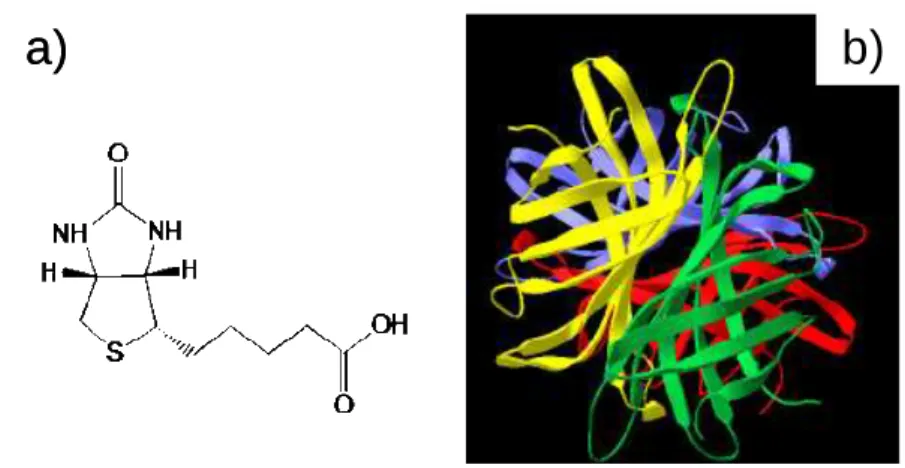
- Un modèle biologique : le couple biotine/avidine
- Un greffage multi-étape
- L’electrospotting
- Greffage et caractérisations des groupements nitrophényles
- a. Le greffage
- b. Caractérisation XPS
- c. Caractérisations structurales (MEB, AFM)
- Réductions chimique et électrochimique des nitrophényles – arrimage de la biotine
- a. Le carbone vitreux
- b. Le diamant
- Caractérisation par microscopie de fluorescence
La réduction chimique est très efficace et permet le greffage de biotine après les deux étapes 3 et 4. A partir de l'image obtenue par microscopie à fluorescence sur la figure IV-A-22fluo, nous avons tracé une image tridimensionnelle avec l'axe z étant le intensité de fluorescence (figure IV-A-23). Cela indique que le greffage de biotine est directement lié à l’efficacité du processus électrochimique.
Enfin, nous sommes aujourd'hui les seuls à avoir localement immobilisé par électrochimie, une molécule biologique à la surface du diamant sans prétraitement de la surface. Enfin, avec les résultats obtenus lors de la caractérisation électrochimique et par spectroscopie XPS du complexe immobilisé à la surface du diamant, nous avons tenté de corréler les résultats de la caractérisation élémentaire avec ceux de la caractérisation électrochimique. La figure IV-B-6 montre le voltamogramme du complexe de ruthénium immobilisé sur la surface du diamant.
Cependant, toutes ces mesures ne permettent pas de conclure sur l’état de la liaison entre la première couche déposée et la surface de l’or. Cette dernière composante à 285,1 eV est située à une énergie inférieure à la résolution dispositif du composant principal du complexe de ruthénium (285,3 eV pour Cb). La figure IV-B-13 montre le spectre global du complexe de ruthénium immobilisé sur la surface du diamant.
L E GREFFAGE D ’ UN COMPLEXE DE RUTHENIUM
- Position du problème
- Greffage et caractérisation électrochimiques sur or et diamant
- Etude XPS du complexe immobilisé sur or
- Etude XPS sur diamant nu
- Etude XPS du complexe immobilisé sur diamant
- Vers le contrôle de l’épaisseur sur diamant
MATERIAUX COMPOSITES ET NANOSTRUCTURES
S YNTHESE DES NANOTUBES DE CARBONE (NTC)
C ARACTERISATION ET FONCTIONNALISATION DES NTC SUR SUBSTRATS
- Nanotubes de carbone sur silicium (NTC/Si)
- Nanotubes de carbone sur diamant (NTC/BDD)
![Figure I-5 : Etude XPS de la zone spectrale C1s d’électrodes de diamant NCD après traitement électrochimique [5]](https://thumb-eu.123doks.com/thumbv2/1bibliocom/465395.70624/39.892.270.628.238.506/figure-etude-xps-spectrale-électrodes-diamant-traitement-électrochimique.webp)