Il a été détecté dans le système nerveux central (SNC) des mammifères il y a une quarantaine d'années. Dans le chapitre 3 de cette thèse, nous présenterons les résultats des études QSAR réalisées sur les différentes familles de composés 5-HT1A (indole, tétraline, chroman, thiochromane et un ensemble de 382 ligands) et au chapitre 4 les études mécaniques et dynamiques. . molécule de complexes ligand/récepteur 5-HT1A avec des ligands potentiels.
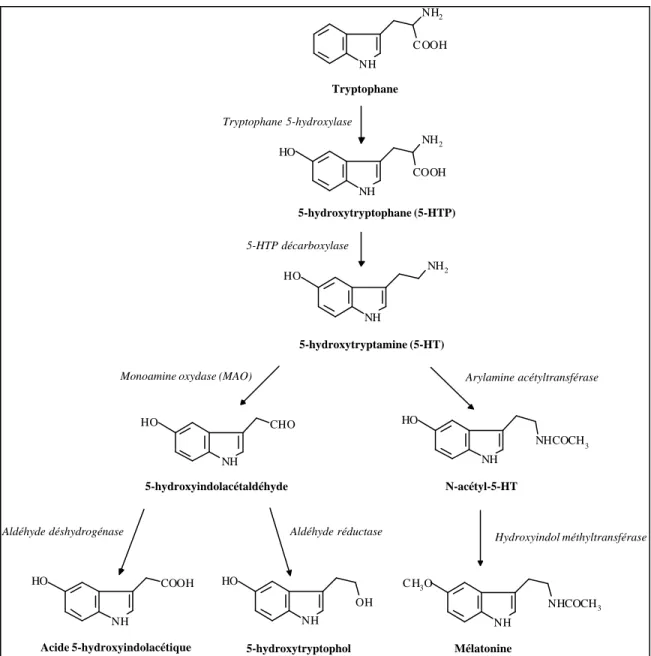
2 - Biosynthèse et catabolisme de la sérotonine
La biosynthèse de la sérotonine peut être bloquée par des composés tels que la p-chlorophénylalanine, un inhibiteur de la tryptophane hydroxylase. La dégradation de la sérotonine peut être bloquée par les inhibiteurs de la monoamine oxydase (MAO), qui peuvent doubler.
LES RECEPTEURS TRANSMEMBRANAIRES DU SYSTEME NERVEUX CENTRAL
1 - La famille 5-HT 1
- A - Le récepteur 5-HT 1A
- B - Les récepteurs 5-HT 1B et 5-HT 1Dβ
- C - Le récepteur 5-HT 1Dα
- D - Le récepteur 5-HT 1E
- E - Le récepteur 5-HT 1F
Le récepteur 5-HT1A est caractérisé par une affinité nanomolaire pour le [3H]-5-HT et une affinité micromolaire pour les antagonistes de la sérotonine. Les études pharmacologiques ont montré une faible activité du 5-CT par rapport à celle du 5-HT1E.
2 - La famille 5-HT 2
A - Le récepteur 5-HT 2A
Le récepteur 5-HT2a a été cloné pour la première fois chez le rat69 avec une homologie avec le récepteur 5-HT2C70 du rat, anciennement appelé 5-HT1C. L'analyse des gènes des récepteurs 5-HT2A révèle la présence de deux introns74 conservés dans trois récepteurs 5-HT2.
B - Le récepteur 5-HT 2B
C - Le récepteur 5-HT 2C
3 - Famille des activateurs de l’adénylate cyclase
A - Le récepteur 5-HT 4
B - Le récepteur 5-HT 6
C - Le récepteur 5-HT 7
4 - La famille 5-HT 5
A - Le récepteur 5-HT 5A
B - Le récepteur 5-HT 5B
5 - Le récepteur à canal ionique 5-HT 3
6 - Les récepteurs sérotoninergiques chez les invertébrés
POTENTIALITES THERAPEUTIQUES DES LIGANDS DES RECEPTEURS 5-HT
De plus, le temps d'action antidépresseur des inhibiteurs de la recapture de la 5-HT (plus de 2 semaines) correspond au temps nécessaire à la désensibilisation des autorécepteurs25. Cependant, un tel ligand existe déjà ; Il s’agit du sumatriptan, efficace pour traiter les crises de migraine.
LES LIGANDS 5-HT1A ET LEURS APPLICATIONS PHARMACOLOGIQUES
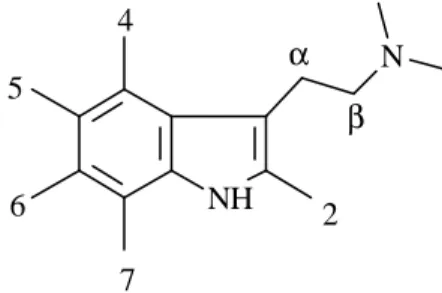
1 - Les dérivés indoliques
2 - Les arylpipérazines
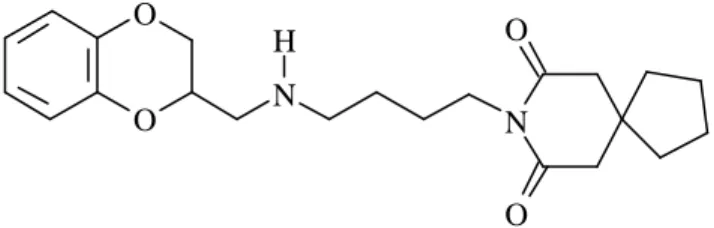
3 - Les dérivés benzodioxanes
4 - Les tétralines
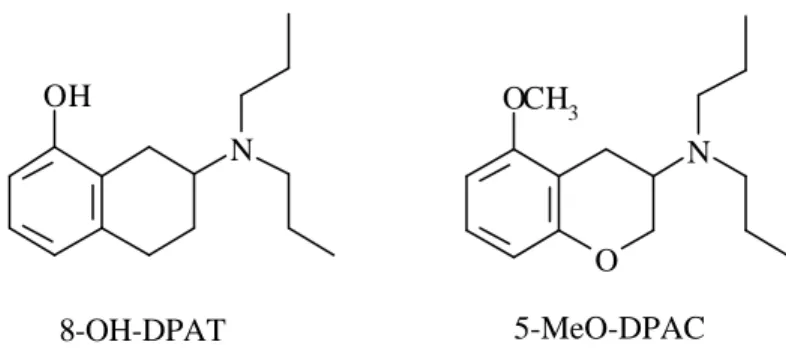
Plus récemment109, une étude sur l'effet des substituants aryle et hétéroaryle en position 8 a montré une faible activité in vitro de ces composés par rapport au 8-OH-DPAT.
5 - Les dérivés à structure benzopyranique
Une cyclisation entre l'azote et la position 1 ou 3 semble rigidifier la structure et fournit des activités intéressantes selon la stéréochimie des carbones 1, 2 et 3110,113.
![Figure 9. Représentation du composé « spiro » rigidifié ; N-[4-(8-azaspiro[4,5]décane-7,9- N-[4-(8-azaspiro[4,5]décane-7,9-dione)butyl]-spiro[5-méthoxy-2H-1-benzopyran-3,2’-pyrrolidine)](https://thumb-eu.123doks.com/thumbv2/1bibliocom/465616.70738/35.894.302.590.344.471/représentation-composé-rigidifié-azaspiro-azaspiro-méthoxy-benzopyran-pyrrolidine.webp)
LES DONNEES PHARMACOLOGIQUES
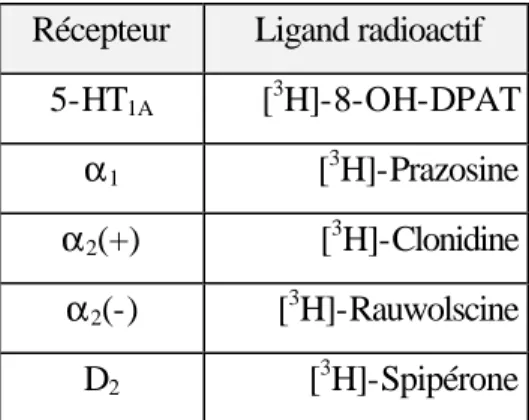
1 - La méthode de l’étude de liaison « binding » in vitro
Deuxièmement, le ligand radioactif est déplacé de son site de liaison en raison des concentrations croissantes de la substance à étudier, L1. Une nouvelle mesure de radioactivité et la connaissance de la concentration C de L1, nécessaire au déplacement total du ligand radioactif, permettent d'évaluer l'affinité de la nouvelle substance pour le site étudié.
2 - Quantification
Concentration de ligand qui provoque 50% du déplacement de la liaison spécifique du radioligand
3 - Interprétation des résultats
Tous les composés ayant une affinité inférieure à 7,5 unités pIC50 et vice versa pour les composés actifs seront considérés comme des ligands inactifs. Dans les sous-types de récepteurs de la sérotonine : aspects fondamentaux et cliniques ; Peroutka, S. ; Éd.; John Wiley et fils ltée.
LES TECHNIQUES DE MODELISATION MOLECULAIRE
LES OUTILS POUR OBTENIR OU DECRIRE UNE STRUCTURE MOLECULAIRE
1 - Les méthodes statiques
- A - Les méthodes quantiques
- B - La mécanique moléculaire
- B.1 - Les champs de forces
- B.2 - Les charges atomiques
- B.3 - La minimisation d’énergie
- B.4 - L’analyse conformationnelle
La charge partielle atomique totale de la molécule est donc la somme des charges σ et π. On obtient généralement une meilleure convergence que dans le cadre de la méthode de la plus grande pente.
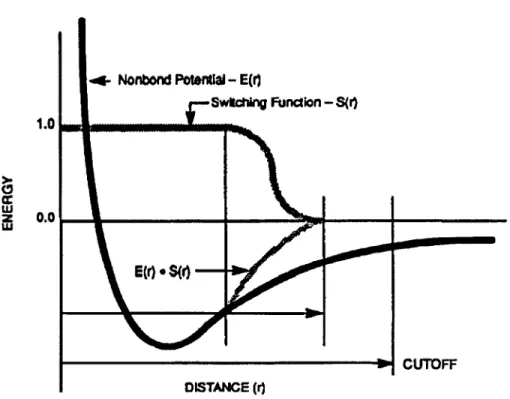
2 - La dynamique moléculaire
C'est le cas des vibrations de longueur de liaison en relation avec les mouvements atomiques de la molécule. On sait que la température est calculée à partir de la valeur de l'énergie cinétique selon le théorème d'équipartition d'énergie.
3 - Les données expérimentales de cristallographie et de RMN
APPLICATION AUX ETUDES STRUCTURE-ACTIVITE
1 - L’approche par pharmacophores
- A - Présentation de la méthode
- B - Les modèles de pharmacophores
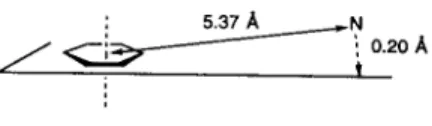
Un autre modèle (Figure 15) a ensuite été proposé par Mellin et al.49 en 1991.49 Ce pharmacopore 5-HT1A basé sur une étude conformationnelle d'analogues de 8-OH-DPAT prend toujours en compte le cycle aromatique mais a cette fois le noyau aromatique. localisation théorique de l'ion carboxylate du récepteur qui devrait avoir une interaction électrostatique avec la paire électronique d'azote. La distance entre un atome fictif passant par le milieu de la distance aromatique de 2,1 à 2,5 Å et la position fictive de l'ion carboxylate du récepteur est comprise entre 5,2 et 5,7 Å. Cette valeur ne prend donc plus en compte la position de l'atome d'azote et de son doublet électronique mais la position fictive de l'ion carboxylate du récepteur.
On voit donc que la fonction OH ou OR doit être opposée à un résidu du récepteur capable d'accepter les électrons de l'oxygène. Et une information très intéressante montre que les substituants azotés sont soumis à des tolérances stériques.

2 - Les méthodes QSAR
- A - Historique et développement du QSAR 53
- B - Les descripteurs moléculaires
- B.1 - Les indices de connectivité
- B.2 - Les indices de forme et de flexibilité
- B.3 - Les propriétés moléculaires
- B.4 - Les vecteurs d'autocorrélation
- B.5 - Les indices de topologie
- C - Les outils statistiques
- C.1 - L’analyse en composantes principales
- C.2 - L’analyse discriminante 104,105,106
- C.3 - L’analyse de régression linéaire multiple
- C.4 - L’analyse Partial Least Square 110,111,112
- D - Les outils 3D
- D.1 - L’analyse des similarités moléculaires
- D.2 - L’analyse CoMFA
QSAR, qui sera plus tard appelée analyse Hansch62 et analyse Free Wilson63. Ces méthodes sont l'analyse en composantes principales (ACP), l'analyse discriminante (DA), la régression linéaire multiple (MR) et les moindres carrés partiels (PLS). L'une des particularités de l'analyse discriminante est la possibilité de prédictions qualitatives basées sur le modèle statistique.
Dans la méthode CoMFA, l’alignement des molécules est très important et a une grande influence sur le résultat de l’analyse. Un champ qui prend en compte les interactions hydrophobes125 (interaction hydrophobe TIP) est également disponible pour l'analyse CoMFA.
3 - Dynamique des complexes ligand/récepteur
- A - La construction des complexes ligand/récepteur
- B - Nature des interactions drogue/récepteur
- B.1 - Les liaisons covalentes
- B.2 - Les interactions électrostatiques
- B.3 - Les liaisons hydrogènes
- B.4 - Les transferts de charges
- B.5 - Les interactions de van der Waals
- B.6 - Les interactions hydrophobes
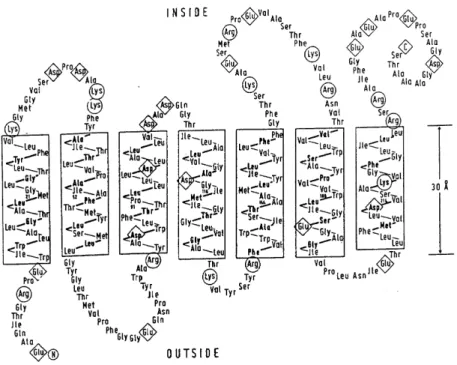
Pour l'étude hydrophobe de la Bacteriorhodopsine par Kyte et Doolittle, on note très clairement les sept domaines représentant les sept hélices α. Cette énergie potentielle est définie empiriquement et dépend de la composition des molécules ainsi que de leur distance. L'un des objectifs de la modélisation est de déterminer l'importance relative de ces interactions dans la stabilisation du complexe ligand/récepteur.
Une liaison hydrogène résulte de l’attraction de deux ou plusieurs atomes électronégatifs voisins et du partage d’un atome d’hydrogène lié de manière covalente à l’un de ces atomes (Figure 20). Les interactions Van der Waals-Londen ou interactions dispersives résultent de la polarisation instantanée induite lorsque deux atomes non liés se réunissent.
ETUDES QSAR
FAMILLE DES INDOLES -
FAMILLE DES TETRALINES -
FAMILLE DES CHROMANES -
FAMILLE DES THIOCHROMANES -
ENSEMBLE DES 382 LIGANDS -
CONCLUSION ; BILAN DES PREDICTIONS
FAMILLE DES INDOLES
Cet échantillon, non totalement représentatif de la famille des indole, a fait l'objet d'une étude de descripteurs moléculaires classiques et d'indices de similarité moléculaire. Pour l'étude des indices de similarité moléculaire, les composés ont été alignés selon les critères du pharmacophore 5-HT1A. Les indices Carbo ont été calculés par optimisation (rotation, translation et déformation des angles dièdres) des molécules.
Différentes méthodes d'analyse statistique ont été testées telles que l'analyse en composantes principales (ACP), l'analyse discriminante (DA), la régression multiple (MR) et les moindres carrés partiels (PLS). Cet échantillon offre une large gamme d’activités avec une bonne différence entre les composés inactifs et actifs.
Etude des descripteurs classiques
Concernant les deux ligands (I56 et I57) dont la prédiction est mauvaise, on peut préciser que leur valeur de liaison expérimentale (7,8 et 7,85) est très proche du seuil de 7,5 choisi pour distinguer les composés actifs et inactifs. Pour l’analyse discriminante, nous avons dû déterminer un seuil séparant les composés inactifs des composés actifs. Pour répondre à la première question, nous dirons que cette valeur correspond à la valeur moyenne des activités extrêmes de tous les composés de notre échantillon.
Ce graphique 4, comme le graphique 3, montre que les composés à forte activité sont plus proches de l'axe de régression que les composés à faible activité. En résumé, les composés actifs sont mieux prédits dans nos modèles que les composés inactifs.
Etude des indices de similarité moléculaire Potentiel de charge électrostatique
La régression multiple a donné les résultats suivants : un coefficient de régression r2 est de 0,46 avec sept variables. Pour l'analyse utilisant 13 variables, tous les ligands inactifs sont classés comme inactifs sauf I29 qui a une activité expérimentale de 7,4. Le premier constat qui ressort de cette analyse des prédictions est que l’analyse à 8 variables donne de meilleures prédictions.
Dans ce scénario, l'analyse à 8 variables offre une plus grande puissance prédictive que l'analyse z. L'analyse de régression multiple et l'analyse des moindres carrés partiels donnent des résultats de faible linéarité (r2 = 0,25 et 0,42) avec de faibles pouvoirs descriptifs (r(CV)2 = 0,17 et 0,32) et des prédictions très éloignées des valeurs expérimentales.
Conclusions
FAMILLE DES TETRALINES
Ces méthodes sont l'analyse en composantes principales, l'analyse discriminante, la régression multiple et les moindres carrés partiels. Une étude d'analyse discriminante réalisée sur tous ces descripteurs classiques donne les résultats suivants, présentés dans le tableau 21. L'analyse de régression multiple et l'analyse des moindres carrés partiels donnent des résultats avec une faible linéarité (r2 = 0,25 et 0,32) et des prédictions très éloignées des valeur expérimentale.
Les résultats de l’analyse en composantes principales sont les suivants : les trois premiers axes factoriels contiennent 25% de l'information des descripteurs et l'analyse des combinaisons axiales 2D et 3D ne renseigne pas sur la répartition des connexions selon ces repères 2D et 3D. L'analyse de régression multiple et l'analyse des moindres carrés partiels donnent des résultats avec une faible linéarité (r2 = 0,28 et 0,47) et des prédictions éloignées de la valeur expérimentale.
FAMILLE DES CHROMANES
Etude 3D avec le pharmacophore de Mellin
En termes de composés non spiraniques, le premier conformère pouvant être superposé au pharmacophore 5-HT1A est rarement un conformère présentant l'une des valeurs énergétiques les plus faibles.
Analyses QSAR
Pour choisir les modèles, nous avons sélectionné le nombre de vecteurs en fonction de la valeur PRESS la plus basse. Les méthodes d'évaluation du potentiel lipophile et des indices de forme ont été exclues en raison de leur coefficient de régression plus faible, et la méthode du champ lipophile en raison de la valeur relativement faible de la « validation croisée ». Le graphique 16 montre la corrélation entre les valeurs expérimentales et les valeurs prédites pour le modèle utilisant les indices Carbo du potentiel électrostatique.
Le graphique 17 montre la corrélation entre les valeurs expérimentales et les valeurs prédites pour le modèle utilisant les indices de champ électrostatique Carbo. Le graphique 18 montre la corrélation entre les valeurs expérimentales et la moyenne des valeurs prédites par les modèles utilisant les indices de potentiel Carbo et de champ électrostatique.
Discussion
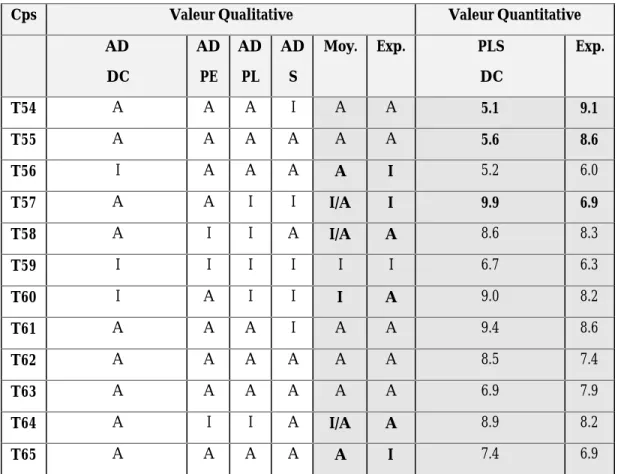
- FAMILLE DES THIOCHROMANES
En ce qui concerne les composés C54 à C57, la présence de deux atomes d'azote interagissant potentiellement avec un résidu aspartate du récepteur perturbe clairement les interactions ligand/récepteur, car ces composés en possèdent tous un. Cet échantillon est séparé en trois sous-ensembles de 19 composés inactifs (TH1 à TH19) avec une pIC50 <. Diverses méthodes d'analyse statistique ont été testées ; il s'agit de l'analyse discriminante (DA), de la régression multiple (MR) et des moindres carrés partiels (PLS).
Dans cette étude, nous avons testé et comparé les différents descripteurs et les différentes méthodes d'analyse statistique. Tous les composés pris en compte dans cette étude QSAR sont issus des travaux de synthèse du laboratoire41,42.
Analyses QSAR pour l’affinité 5-HT 1A
Pour le récepteur α2, la distinction entre composés est due à deux vecteurs d'autocorrélation 3D pondérés par la charge électrostatique. Le récepteur dopaminergique D2 possède une affinité proportionnelle à quatre variables composées d'un indice de Randic, d'un indice de Balaban et de deux vecteurs d'autocorrélation 3D pondérés par la charge électrostatique. Pour le récepteur 5-HT1A, l'affinité est liée à deux vecteurs qui expriment principalement des indices d'autocorrélogramme 3D pondérés par la charge électrostatique et la lipophilie.
Pour le récepteur α2, les principales variables vectorielles sont des vecteurs d'autocorrélation 3D pondérés par la charge électrostatique. Le récepteur dopaminergique D2 possède une affinité proportionnelle à deux vecteurs qui expriment principalement des variables composées de vecteurs d'autocorrélation 3D pondérés par une charge électrostatique.