Alexandre Naime Barbosa
Avaliação das citocinas (ELISA e RT-PCR) e da fibrose hepática na
coinfecção pelo HIV e vírus da hepatite C
Botucatu - SP
2010
Tese apresentada ao Programa de Pós-Graduação em Doenças
Tropicais da Faculdade de Medicina de Botucatu -
Universidade Estadual Paulista - UNESP para a obtenção do
Título de Doutor em Doenças Tropicais.
FICHA CATALOGRÁFICA ELABORADA PELA SEÇÃO DE AQUIS. E TRAT. DA INFORMAÇÃO DIVISÃO TÉCNICA DE BIBLIOTECA E DOCUMENTAÇÃO - CAMPUS DE BOTUCATU - UNESP
BIBLIOTECÁRIA RESPONSÁVEL: ROSEMEIRE APARECIDA VICENTE
Barbosa, Alexandre Naime.
Avaliação das citocinas séricas e dosadas por RT-PCR, e da fibrose hepática na coinfecção pelo HIV e vírus da hepatite C / Alexandre Naime Barbosa. – Botucatu, 2010
Tese (doutorado) – Faculdade de Medicina de Botucatu, Universidade Estadual Paulista, 2010
Orientador: Domingos Alves Meira Assunto CAPES: 40100006
1. Medicina tropical. 2. Hepatite C. 3. HIV (Vírus).
Epígrafe
“A tarefa não é tanto ver o que ninguém viu ainda,
mas pensar o que ninguém pensou sobre algo que todos vêem”
Agradecimentos
Ao Prof. Titular Emérito Dr. Domingos Alves Meira,
pelo modelo de conduta na prática médica, no ensino e na pesquisa,
pelo convívio e ensinamentos científicos, éticos e culturais,
pela energia que contagia, pela capacidade de sonhar.
À minha família:
meu pai, pela dedicação e condução desde cedo, ao mundo dos livros;
minha mãe, pelo carinho e apoio à toda prova;
meu irmão, pelo incentivo e companheirismo;
meus avós, referência pessoal de moral e de bondade.
Aos colegas da Disciplina:
Lenice do Rosário de Souza, Ricardo Augusto Monteiro de Barros Almeida e
Carlos Magno Fortaleza Castelo Branco, pelo companheirismo e amizade.
Ao Dr. Lucas Marques da Costa Alves pela ajuda no recrutamento.
Aos Funcionários do Hospital Dia e Residentes da MIP pela ajuda na
identificação dos pacientes e coleta das amostras.
À Equipe do Laboratório de Doenças Tropicais:
Sueli Aparecida Calvi, Eliana Peresi e Vanessa Cristina Nicoleti pelo
processamento das amostras.
Aos funcionários do Departamento de Doenças Tropicais e da Seção de
Agradecimentos
Aos funcionários da Biblioteca do Campus de Rubião Jr. e do Grupo de
Apoio à Pesquisa da Faculdade de Medicina de Botucatu - Unesp pelo apoio
técnico.
Aos meus queridos amigos, minha família em Botucatu (e fora dela
também): Abigail, Jú, Zumira, Saci, Faiado, Stella, Maligno, Secrê, Jeba,
Kesan, Ritchie, Pardal, Dalva, Marila, Anabele, Amanda, Vidal e tantos
outros que não cabem aqui.
E principalmente aos pacientes e voluntários que aceitaram em participar
dessa pesquisa. Espero que os resultados possam contribuir de alguma
forma para aprimorar o conhecimento sobre a infecção pelo HIV/aids e a
Sumário
Sumário
I. Resumo... x
II. Abstract... xii
III. Introdução... 01
1. Fundamentação Científica... 02
2. Objetivos... 08
II. Casuística e Métodos... 09
1. Casuística... 10
2. Métodos... 10
III. Resultados... 24
1. Homogeneidade entre os grupos... 25
2. Linfócitos T CD4, carga viral do HIV, genótipo do VHC e fibrose hepática... 26
3. Valores de referência de normalidade para as citocinas... 30
4. Comparação entre as citocinas nos grupos de estudo e o grupo controle... 31
IV. Discussão... 40
V. Considerações Finais... 49
VI. Referências Bibliográficas... 51
VII. Apêndice... 60
1. Manuscrito submetido à AIDS (Journal of International AIDS Society)…….…. 61
2. Manuscript submitted to AIDS (Journal of International AIDS Society)…... 80
Resumo
Resumo
A aids e a hepatite C crônica são infecções caracterizadas por importante processo
inflamatório contínuo, regulado por uma complexa interação entre citocinas. A
persistência da atividade inflamatória crônica está intimamente relacionada com a
progressão da patogênese da aids, bem como na indução de fibrose na hepatite C. Com o
objetivo de avaliar o padrão de citocinas na infecção pelo HIV e na hepatite C crônica, as
citocinas IL-2, IL-4, IL-10, TNF-α, INF-γ, TGF-β foram dosadas por Elisa e RT-PCR em cinco
grupos: pacientes coinfectados pelo HIV/VHC (n=22), monoinfectados pelo HIV com
supressão virológica pelo tratamento, e sem supressão virológica (n=17), monoinfectados
pelo VHC (n=22) e um grupo controle composto por indivíduos doadores de sangue
(n=10). IL-4 e IL-10 estiveram aumentadas consistentemente nos quatro grupos de
estudo, determinando predomínio do perfil Th-2. INF-γ, TNF-α e TGF-β estiveram
aumentados apenas nos grupos com infecção pelo VHC, com ou sem coinfecção pelo HIV.
No grupo de monoinfectados pelo HIV com supressão virológica, a IL-2 dosada por RT-RCR
esteve aumentada, porém os níveis séricos dosados por Elisa estavam normais. A alta
produção de citocinas pró-inflamatórias INF-γ, TNF-α e TGF-β nos dois grupos de
pacientes com infecção pelo VHC refletem o processo progressivo de acúmulo de
inflamação e fibrose hepática. Já o predomínio de IL-4 e IL-10 em todos os grupos,
citocinas ligadas ao perfil Th-2, demonstram a incapacidade de produção de uma resposta
citotóxica Th-1, perpetuando a infecção e a inflamação crônica, mesmo naqueles
indivíduos com supressão virológica pelo tratamento. Além de drogas antivirais, novos
tratamentos imunomoduladores têm sido propostos para a erradicação viral, ou a
interrupção das lesões causadas pelo estado inflamatório crônico. A avaliação das
citocinas tem papel principal verificar a eficácia de intervenções, e também se constituir
Abstract
Abstract
Both AIDS and chronic hepatitis C (HCV) are characterized by continuous
inflammatory process, regulated by a complex interaction between cytokines. The
persistence of chronic inflammatory activity is closely related to the progression of the
pathogenesis of AIDS, as well as the induction of fibrosis in HCV. In order to analyze the
role of cytokines in HIV/HCV coinfection and the fibrosis progression, IL-2, IL-4, IL-10,
TNF-α, INF-γ, TGF-β were measured by ELISA and RT -PCR in five groups: HIV/HCV coinfected
patients (n = 22), HCV monoinfected patients (n = 22), HIV monoinfected patients with
and without virological suppression (n = 17) and a control group composed by blood
donors (n = 10). Hepatic biopsy and METAVIR classification were performed in all HCV
patients (n=44). The baseline characteristics (sex, age and race) of all groups were similar.
No correlations were found between cytokines and hepatic fibrosis. IL-4 and IL-10 were
consistently increased in the four study groups, findings associated to a Th-2 profile.
INF-γ, TNF-α and TGF-β were increased only in groups with HCV infection. In the group of HIV
monoinfected patients with virological suppression, IL-2 measured by RT-RCR was
increased, but serum levels measured by ELISA were normal. The high production of
pro-inflammatory cytokines INF-γ, TNF-α and TGF-β in two groups of patients with HCV
infection reflect the gradual process of inflammation and liver fibrosis. The predominance
of IL-4 and IL-10 in all study groups demonstrates an inability to promote a cytotoxic Th-1
response. Even in HIV monoinfected patients with virological suppression with increased
IL-2 expression, Th-2 cytokines were the predominant, perpetuating the chronic
inflammation. In addition to antiviral drugs, new immunomodulatory treatments have
been proposed to treat HIV or HCV, and cytokines may be an important marker of efficacy
Introdução
I - Introdução
1. Fundamentação Científica
Apesar de conhecidas relativamente há pouco tempo, a aids e a infecção pelo
vírus da hepatite C (VHC) têm se destacado como duas das mais importantes e
prevalentes doenças em todo o mundo, por gerar alta morbi-mortalidade e grande
impacto social e financeiro, mesmo em países mais desenvolvidos (1,2).
Desde os primeiros relatos em 1981, estima-se que aproximadamente 65 milhões
de pessoas se infectaram pelo vírus da imunodeficiência humana (HIV), sendo que dessas,
cerca de 25 milhões já morreram (1). Os países mais pobres, como muitos da África,
Sudeste Asiático e América Latina, concentram o maior percentual dessas mortes por
falta de recursos para estabelecer políticas de saúde pública adequadas para o
enfrentamento dessa epidemia, em especial, por não poderem sustentar programas de
acesso gratuito ao tratamento da aids (1).
Fato é que, após 1995, o surgimento da terapia antirretroviral combinada e
potente, denominada na língua inglesa de highly active antiretroviral therapy (HAART),
trouxe rápida diminuição na incidência das infecções oportunísticas, levando a uma
conseqüente redução da mortalidade relacionada à aids, nos países onde essa terapia foi
disponibilizada (3,4,5). Porém, com o aumento da sobrevida, muitas doenças crônicas
passaram a ter maior importância para as pessoas vivendo com HIV/aids (PVHA), com
destaque para as complicações da hepatite crônica pelo vírus C (HVC), condição bastante
prevalente nessa população.
Estima-se que cerca de 180 milhões de pessoas, ou cerca de 3% da população
mundial esteja infectada pelo VHC, sendo que 130 milhões com alto risco de desenvolver
cirrose e/ou carcinoma hepatocelular (2). A HVC é responsável por 50% a 76% de todos os casos novos de câncer de fígado e por dois terços dos transplantes hepáticos nos países
desenvolvidos (2).
Se a infecção isolada pelo HIV ou pelo VHC pressupõe alto risco à saúde do
Introdução
tratamento, a situação específica de coinfecção HIV/VHC traz particularidades ainda mais
complexas.
A prevalência da HVC em PVHA varia muito, dependendo, principalmente, do
modo de aquisição do HIV, mas em via de regra, é bem maior do que na população em
geral. Pelo fato dos dois vírus compartilharem os mesmos mecanismos de transmissão,
essa relação pode ser muito alta, como verificado em usuários de drogas ilícitas (91%) ou
em hemotransfundidos (71%), ou mesmo ser mais baixa (7%), como naqueles que tem
apenas fator de risco sexual, via não muito efetiva para transmissão do VHC (6).
Há, também, muitas variações regionais. No Brasil, estudos dessa prevalência
apontam índices de 14,3% em Belo Horizonte, MG (7), 17,7% em São Paulo, SP (8) e Vitória, ES (9), 37,0% em Santos, SP (10), 53,8% em Campinas, SP (11) e 58,3% em Florianópolis, SC
(12). Nos Estados Unidos da América (EUA), diferentes centros de pesquisa têm taxas que
variam de 16,1% até 74,2% (13,14,15,16). O EuroSIDA, importante estudo de coorte
observacional prospectivo, com mais de 9800 PVHA de países da Europa mais a
Argentina, revelou prevalência de 34,0%, porém, encontrando novamente grandes
diversidades nacionais (17).
Além de mais freqüente, a HVC pode ser considerada uma doença oportunista nas
PHVA, pois há aceleração de sua história natural, representada por elevação da carga viral
plasmática do VHC, fibrose hepática precoce e maior ocorrência de esteatose, cirrose e de
carcinoma hepatocelular (18,19,20,21,22). Como conseqüência, a morbi-mortalidade por
doença hepática terminal é maior nos indivíduos coinfectados pelo HIV/VHC em
comparação com monoinfectados pelo VHC (23).
A patogênese da infecção pelo VHC difere dos modelos clássicos de infecção por
vírus, reflexo da alta adaptação ao ser humano. Logo após o contágio, durante a fase
aguda, alguns mecanismos de escape do sistema imunológico do hospedeiro foram
descritos, como o efeito supressivo de antígenos virais sobre a resposta inata e
adaptativa, a influência de altas cargas virais já no início da infecção contrapondo a uma
resposta celular mais tardia, queda nas contagens de linfócitos TCD4, baixa efetividade
dos linfócitos TCD8, mutação em quasispecies, impedindo o reconhecimento pelos
Introdução
A soma desses fatores, a outros ainda não totalmente conhecidos, determina baixas taxas
de eliminação viral espontânea, o que ocorre em apenas 14% a 26% dos indivíduos
infectados (26).
Não havendo a cura espontânea na fase aguda, a maioria dos casos, cerca de 80%,
evolui para hepatite crônica, definida pela persistência do VHC após seis meses do
contágio. Como a infecção aguda geralmente é assintomática e as lesões causadas
durante a fase crônica são de instalação lenta, progressiva e silenciosa, o diagnóstico de
HVC torna-se difícil até que surja descompensação hepática ou hepatocarcinoma. Por
vezes a descoberta é mais precoce, mas de forma acidental, através de investigação
sorológica em doações de sangue ou exames de check-up.
Em cerca de um terço dos indivíduos com HVC, conhecidos como progressores
lentos, seguidos por 30 anos ou mais, a infecção parece não evoluir, cursando com
transaminases normais e lesões histológicas leves. Nos dois terços restantes, conhecidos
como progressores rápidos, a inflamação e a fibrose estão ativas, e em menos de 20 anos
pode haver evolução para cirrose e hepatocarcinoma (26,27).
A interação entre diversos fatores virais e imunológicos explica a persistência da
infecção, já que não há evidências de integração de material genético do VHC no
hospedeiro, pois nunca foi encontrado um DNA intermediário (28).
Os mecanismos que determinam as lesões encontradas na HVC não são
totalmente conhecidos. Inicialmente, existe controvérsia sobre a existência do efeito
citopático direto pelo VHC. Indivíduos com imunodepressão, como
hipogamaglobulinemia, coinfecção pelo HIV, transplante de medula, rins e fígado
apresentam maior taxa de hepatite crônica em atividade, além de maior viremia e
velocidade de evolução da lesão, fatores favoráveis à teoria de lesão direta pelo VHC.
Porém, em indivíduos imunocompententes a viremia não se relaciona com a gravidade
das lesões hepáticas (29).
Fatores intrínsecos do hospedeiro têm relação mais estreita com a progressão da
HVC, como gênero masculino, a idade acima de 40 anos, a raça negra e alguns
determinantes genéticos, assim como fatores extrínsecos como o uso abusivo de álcool, o
Introdução
A suscetibilidade genética está intimamente ligada ao desenvolvimento da
doença, desde o reconhecimento e apresentação do antígeno até o tipo de resposta T
helper à infecção pelo VHC (33). A resposta celular a polipeptídeos do core NS4 e NS5 parecem ser mais acentuada em indivíduos que eliminaram o VHC espontaneamente e
em respondedores ao tratamento com interferon. Já a resposta específica contra os
peptídeos da região NS3 promove a eliminação espontânea do VHC(34). Alguns alelos do
complexo principal de histocompatibilidade tipo II (MHC-II), como o DR5, têm sido
relacionados com menor incidência de cirrose em indivíduos cronicamente infectados
pelo VHC (33). A proteína viral core parece ter efeito imunomodulador, se ligando a um receptor de TNF-α e, conseqüentemente, inibindo a apoptose da célula infectada (35). Outro mecanismo antiapoptótico seria a inibição de um fator nuclear Kappa (NF-κβ) (36). Por outro lado, citocinas pró-inflamatórias estão associadas à resposta e à progressão das
lesões, e têm diferentes padrões de expressão individual.
Assim, a reposta imune tem papel principal no entendimento da patogênese dessa
infecção. Na HVC, já na primeira linha de defesa, a resposta inespecífica, alguns modelos
de estudo apontam que células natural killer (NK) são menos ativadas por células
dendríticas e também são inibidas em sua função pela ligação do vírus ao receptor CD81
(37,38)
. A ação do interferon tipo I (IFN I) α e β também se mostra prejudicada em outros
modelos, seja por diminuição da sensibilidade a essa citocina, ou por uma apresentação
de antígenos pelo MHC-II anômala, decorrente da inibição da indução do IFN I por
proteínas virais (39).
Em relação à resposta imune humoral, após a evasão da imunidade inata, há
produção de altos títulos de anticorpos contra vários epítopos virais, porém sem
capacidade de eliminação viral (39). A pressão seletiva exercida pelos anticorpos
neutralizantes estimula alta taxa de mutações nucleotídeas, e a conseqüente coexistência
de múltiplas quasispecies impedem a ação humoral específica, estratégia essa que ajuda a
perpetuar a infecção (40).
A resposta imune celular específica está relacionada tanto com a eliminação viral
Introdução
que estimulam a síntese de colágeno pelos fibroblastos e formação de fibrose (42). Há também indução de apoptose, e os restos celulares fagocitados por células estreladas
amplificam a produção de colágeno por TGF-β, aumentando a fibrose hepática (43).
Contudo, não há consenso entre os diversos estudos que objetivam determinar
qual é o perfil de citocinas relacionado com melhor ou pior prognóstico na HVC (44). Alguns trabalhos, utilizando determinação de citocinas no sangue periférico, apontam
que a resposta Th-1, definida principalmente pela produção de IL-2 e IFN-γ, se relaciona
com melhor controle da infecção e evolução mais benigna, e que o perfil Th-2,
determinado principalmente pela expressão de IL-4 e IL-10, é responsável pela
cronificação da infecção e progressão das lesões hepáticas (44, 45, 46, 47, 48). Outros estudos, com dosagem de citocinas no ambiente intra-hepático apontam resultados
absolutamente inversos, relacionando o perfil Th-1 com pior prognóstico (49, 50, 51). Uma hipótese para explicar essa disparidade seria a “compartimentalização” da resposta
imune, com perfil Th2 nos tecidos linfóides periféricos, e perfil Th1 no fígado, nos
pacientes com tendência de progressão da doença (44, 52).
Se a dinâmica imunopatogênica já é complexa em indivíduos monoinfectados pelo
VHC, na situação de coinfecção HIV/VHC poucos estudos abordam especificamente o
tema, sem, contudo, avaliar a correlação dos entre a resposta T específica e o
estadiamento da lesão hepática. Em indivíduos monoinfectados pelo HIV, sem
tratamento antirretroviral e com progressão da doença, observa-se predomínio do perfil
Th-0/Th-2, principalmente influenciados pelo aumento de IL-10 (53). Mesmo em indivíduos tratados com HAART, com carga viral plasmática do HIV (CV-HIV) indetectável ou não,
estudo realizado em nosso meio demonstrou não haver recuperação da capacidade de
expressão de perfil Th-1, sendo que esses pacientes exibiram em sua maioria perfil Th-0
maduro e baixos níveis de IL-2, sugerindo que a apoptose de linfócitos durante a evolução
da doença seja a responsável por esse fenômeno (54).
A progressão da HVC em PVHA é mais rápida e o prognóstico pior, como já
colocado anteriormente (18, 19, 20, 21, 22, 23). A carga viral do VHC em PVHA é maior, tanto no plasma, quanto em tecido hepático, sendo demonstrada, inclusive, replicação do VHC em
Introdução
Estudos recentes apontam que o TGF-β está especialmente alto nessa coinfecção,
justificando, portanto a instalação mais rápida de fibrose, já que essa citocina está
envolvida em processos pró-fibróticos (60,61). Adicionalmente, o TGF-β reduz a resposta de linfócitos T CD8 ao IFN-γ, favorecendo a persistência da infecção e impedindo a resposta T
específica (61, 62, 63). Em relação ao tratamento antirretroviral, há evidências que os pacientes coinfectados virgens de HAART apresentem tendência a exibir perfil Th-2 mais
freqüentemente do que os indivíduos tratados, sem, contudo diferenças significativas nos
níveis de TGF-β (61, 64).
Devido à escassez de estudos que correlacionem a expressão e secreção de
citocinas, tanto pró-inflamatórias, quanto indutoras de fibrogênese, na população
co-infectada pelo HIV/VHC, com os achados histopatológicos da biópsia hepática,
investigações nesse sentido se fazem necessárias a fim de estabelecer parâmetros que
possam predizer melhor ou pior prognóstico, ou mesmo, indicar de forma mais precisa a
Introdução
2 - Objetivos
- Comparar o perfil de citocinas por ELISA e por RT-PCR de coinfectados HIV/VHC,
com grupos de pacientes monoinfectados pelo HIV ou pelo VHC, bem como, com
um grupo de indivíduos normais.
- Comparar os perfis de citocinas por ELISA e por RT-PCR com a graduação de
fibrose observada na biópsia hepática em pacientes com coinfecção HIV/VHC e
monoinfectados pelo VHC.
- Comparar os achados histológicos entre biópsias hepáticas de coinfectados
HIV/VHC e indivíduos monoinfectados pelo VHC.
- Comparar os perfis de citocinas por ELISA com os valores obtidos por RT-PCR nos
pacientes coinfectados HIV/VHC e estabelecer a correlação e concordância entre
Casuística e Métodos
II. Casuística e Métodos
1 - Casuística
Foram estudados 61 pacientes, de ambos os sexos, atendidos no Serviço de
Ambulatórios Especializados e Hospital Dia Domingos Alves Meira (SAE/HD), unidade do
complexo médico-hospitalar da Faculdade de Medicina de Botucatu – Unesp
(FMB-Unesp), no período entre outubro de 2008 e agosto de 2009. Além dos pacientes,
também foram estudados 10 doadores de sangue do Hemocentro do Hospital das Clínicas
da FMB-Unesp (HC Unesp).
2 - Métodos
Foi realizado estudo prospectivo de corte transverso não randomizado em
pacientes com coinfecção HIV/VHC, monoinfecção pelo HIV ou pelo VHC, além de
indivíduos normais, doadores de sangue.
2.A - Caracterização das Populações Estudadas
2.A.1 - Indivíduos com coinfecção HIV/VHC
Do total de indivíduos com infecção pelo HIV, foram selecionados 22 pacientes
que, inicialmente triados por sorologia reagente para o VHC, apresentaram também
detecção do ácido ribonucléico (RNA) desse vírus, por técnica de amplificação pela reação
em cadeia da polimerase qualitativa (RT-PCR).
Critérios de Inclusão
- ambos os sexos, idade maior que 18 anos completos;
- diagnóstico de infecção pelo HIV;
- estabilidade clínica e função hepática preservada;
- diagnóstico de infecção pelo VHC, confirmado por PCR;
- concordância e assinatura do Termo de Consentimento Livre e Esclarecido (TCLE - anexo
Casuística e Métodos
Critérios de Exclusão
- idade menor que 18 anos completos;
- diagnóstico de infecção pelo HIV ou pelo VHC não confirmados;
- instabilidade clínica
- insuficiência hepática (Child-Pugh B ou C);
- presença de infecção inativa ou ativa pelo vírus da hepatite B (VHB);
- outras causas de imunossupressão;
- gestantes;
- não concordância com o TCLE.
2.A.2 Indivíduos Monoinfectados pelo HIV
Do total de indivíduos com infecção pelo HIV foram selecionados 17 pacientes, em
uso ou não de terapia antirretroviral. Esses indivíduos, necessariamente, tiveram
posterior exclusão, sorológica e por PCR qualitativo, de infecção pelo VHC.
Critérios de Inclusão
- idade maior que 18 anos completos;
- diagnóstico de infecção pelo HIV;
- estabilidade clínica
- função hepática preservada;
- concordância e assinatura do TCLE.
Critérios de Exclusão
- idade menor que 18 anos completos;
- diagnóstico de infecção pelo HIV não confirmado;
- instabilidade clínica
- infecção pelo VHC ou presença de infecção inativa ou ativa pelo VHB;
- insuficiência hepática (Child-Pugh B ou C);
- outras causas de imunossupressão ou gestantes;
Casuística e Métodos
2.A.3 - Indivíduos Monoinfectados pelo VHC
Do total de indivíduos com infecção pelo VHC foram selecionados 22 pacientes,
com confirmação do diagnóstico por PCR qualitativo, porém, sem tratamento específico
prévio. Esses indivíduos, necessariamente, tiveram posterior exclusão sorológica de
infecção pelo HIV.
Critérios de Inclusão
- idade maior que 18 anos completos;
- diagnóstico de infecção pelo VHC, confirmado por PCR;
- função hepática preservada;
- concordância e assinatura do TCLE.
Critérios de Exclusão
- idade menor que 18 anos completos;
- diagnóstico de infecção pelo VHC não confirmado;
- infecção pelo HIV;
- insuficiência hepática (Child-Pugh B ou C);
- presença de infecção inativa ou ativa pelo VHB;
- outras causas de imunossupressão;
- gestantes;
- não concordância com o TCLE.
2.A.4 Indivíduos Normais
Foram selecionados ao acaso 10 indivíduos normais, sem queixas espontâneas ou
sinais evidentes de doenças, doadores de sangue do Hemocentro de Botucatu - HC
Casuística e Métodos
2.B - Caracterização dos Grupos de Estudo
Grupo 1 (G1): 22 pacientes com coinfecção HIV/VHC;
Grupo 2 (G2): 22 pacientes monoinfectados pelo VHC;
Grupo 3 (G3): 06 pacientes com monoinfecção pelo HIV, com carga viral detectável;
Grupo 4 (G4): 11 pacientes com monoinfecção pelo HIV, com carga viral indetectável;
Grupo 5 (Grupo Controle): 10 indivíduos normais doadores de sangue.
2.C - Coleta de Parâmetros Clínicos e Laboratoriais da Rotina
Para a composição dos grupos de estudo, foram revisados todos os prontuários
médicos dos pacientes atendidos no SAE/HD para verificação do status sorológico para o
HIV-1 e para o VHC, bem como para coleta de parâmetros clínicos e laboratoriais da
rotina desse serviço, que permitiram a inclusão ou exclusão no presente estudo.
2.C.1 - Grupos 1: População com coinfecção HIV/VHC
Nos pacientes com diagnóstico sorológico confirmado de infecção pelo HIV-1, e
que também tiveram sorologia reagente para o VHC, foi verificado a confirmação dessa
coinfecção por PCR qualitativo, bem como a subseqüente genotipagem e subtipagem do
VHC. Foram, então, selecionados 22 pacientes com estabilidade clínica, preservação da
função hepática e exclusão de infecção ativa ou inativa pelo VHB.
Foi, então, observado o score relativo às alterações anátomo-patológicas da
biópsia hepática, o uso ou não de terapia antirretroviral, a contagem de linfócitos T CD4,
além da CV-HIV, em um mesmo momento. Nesse grupo de pacientes também foram
coletadas informações sobre sexo, idade, cor da pele, além dos valores de
Casuística e Métodos
2.C.2 - Grupo 2 – População com Monoinfecção pelo VHC
Nos pacientes com diagnóstico sorológico de infecção pelo VHC, foi verificada a
confirmação dessa infecção por PCR qualitativo, bem como a subseqüente genotipagem e
subtipagem do VHC. Foram, então, selecionados 22 pacientes sem tratamento específico
prévio e sem evidências de insuficiência hepática demonstrada clínica e/ou
laboratorialmente relacionados ou não à infecção pelo VHC, bem como, ausência de
marcadores sorológicos para HIV ou VHB.
Foi, então, observado o score relativo às alterações anátomo-patológicas da
biópsia hepática, e, também foram coletadas informações sobre sexo, idade, cor da pele,
além dos valores de aminotransferases.
2.C.3 - Grupo 3 e 4: População com Monoinfecção pelo HIV-1
Nos pacientes com diagnóstico sorológico confirmado de infecção pelo HIV-1, com
sorologia não reagente para o VHC, foi confirmada a exclusão desta coinfecção por PCR
qualitativo. Foram selecionados 17 pacientes com estabilidade clínica em relação à
infecção pelo HIV-1, em uso ou não de terapia antirretroviral, preservação da função
hepática e com exclusão de infecção ativa ou inativa pelo VHB.
Foram, também, observado a contagem de linfócitos T CD4, além da CV-HIV, em
um mesmo momento. Nesse grupo de pacientes também foram coletadas informações
sobre sexo, idade, cor da pele, além dos valores de aminotransferases.
2.D - Diagnóstico Laboratorial de Infecção pelo HIV-1
O diagnóstico de infecção pelo HIV-1 foi determinado de acordo com o fluxograma
estabelecido pelo Ministério da Saúde do Brasil, utilizando testes sorológicos (65). Esses testes fazem parte da rotina de acompanhamento de pacientes seguidos nos
ambulatórios do SAE/HD, sendo realizados pelo Hemocentro de Botucatu - HC
Casuística e Métodos
2.E - Diagnóstico Laboratorial de Infecção e Genotipagem do VHC
A investigação de infecção pelo VHC foi inicialmente realizada por testes
sorológicos. Em caso de reação não reagente, o paciente foi classificado como não
infectado pelo VHC, salvo em condições que permitam supor janela sorológica. Nos casos
de sorologia reagente ou inconclusivo, foi indicada a pesquisa de RNA do VHC por PCR
qualitativo (limite de detecção mínimo: 50 cópias/ml), sendo considerado como não
infectados pelo VHC aqueles indivíduos com dois testes com resultado não detectado
com intervalo mínimo de um ano. Nos casos de PCR qualitativo detectado, foi realizado
também a genotipagem do VHC.
Esses testes fazem parte da rotina de acompanhamento de pacientes seguidos nos
ambulatórios do SAE/HD, sendo que os testes sorológicos foi realizado pelo Laboratório
Clínico do HC FMB-Unesp, e o PCR qualitativo e a genotipagem do VHC, realizados pelo
Hemocentro de Botucatu - HC FMB-Unesp.
2.F - Caracterização de Estabilidade Clínica relacionada à infecção pelo HIV-1
Para inclusão no presente estudo, o indivíduo infectado pelo HIV-1 teve que
apresentar estabilidade clínica no momento da observação, caracterizada pela ausência
de infecções oportunistas decorrentes da imunossupressão causada pelo HIV-1, a saber:
pneumocistose, neurotoxoplasmose, candidíase esofágica, neurocriptococose,
criptosporidiose, histoplasmose disseminada, citomegalovirose disseminada, tuberculose
disseminada e micobacteriose atípica, entre outras.
A justificativa para os limites acima descritos é que a biópsia hepática tem como
principal função, indicar ou não o tratamento específico para a HVC, sendo que esse
tratamento tem sérios efeitos adversos, e conseqüentes contra-indicações,
principalmente na população infectada pelo HIV-1 com falha clínica.
2.G - Contagem de linfócitos T CD4
Foi observada a contagem de linfócitos T CD4, realizado pelo Hemocentro do HC
FMB-Unesp, utilizada na rotina do acompanhamento de pacientes infectados pelo HIV-1.
Casuística e Métodos
com marcador CD4+ foi a técnica de citometria de fluxo, com emprego do Coulter
Monoclonal, Antibodies, Reagents.
2.H - Determinação da Carga Viral Plasmática do HIV-1
A quantificação da CV-HIV foi determinada por técnica de bDNA, pelo kit HIV 3.0
RNA, tendo limites mínimos e máximos de detecção de 50 e 500.000 cópias/ml (log10 1,69
e 5,69), respectivamente. Esse exame é realizado na rotina dos indivíduos infectados pelo
HIV-1, pelo Hemocentro de Botucatu - HC FMB-Unesp.
2.I - Caracterização de Insuficiência Hepática
Os critérios utilizados para graduar insuficiência hepática foi a classificação de
Child-Pugh(66), representada nos quadros abaixo. Não foram incluídos no presente estudo aqueles indivíduos com estadiamento B ou C.
Classificação de Child-Pugh:
Pontuação 1 2 3 Unidade
Bilirrubina total < 2 2 - 3 > 3 mg/dL
Albumina Sérica > 3,5 2,8 – 3,5 < 2,8 mg/dL
RNI < 1,7 1,71 - 2,20 > 2,20 -
Ascite ausente Resolvida com medicação Refratária -
Encefalopatia
Hepática ausente Resolvida com medicação Refratária -
RNI: razão internacional de normalidade
Classe Pontuação
Sobrevida (anos)
1 2
A 5 - 6 100% 85%
B 7 - 9 81% 57%
Casuística e Métodos
As determinações de bilirrubina total e albumina no soro foram realizadas pelo
Laboratório Clínico do HC FMB-Unesp, e a RNI pelo Hemocentro desse HC. Esses exames
fazem parte da rotina de acompanhamento dos pacientes infectados pelo VHC no
SAE/HD.
2.J - Infecção pelo Vírus da Hepatite B
Não foram incluídos no presente estudo indivíduos com infecção ativa ou inativa
pelo VHB, sendo, portanto, desconsiderados aqueles com marcador sorológico AgHBs
reagente. Foram incluídos aqueles indivíduos que, eventualmente, sejam portadores
ocultos do VHB (AgHBs não reagente, anti-HBc reagente, anti-HBs reagente ou não), pois
além da baixa freqüência da detecção do DNA viral nessa situação, a replicação viral no
caso se faz em baixíssima velocidade, levando a pouca ou nenhuma agressão tecidual.
Os marcadores sorológicos para diagnóstico de VHB são solicitados na rotina do
SAE/HD para os pacientes infectados pelo HIV-1 e/ou pelo VHC, e realizados pelo
Laboratório Clínico do HC FMB – Unesp.
2.K - Biópsia Hepática e Classificação Anátomo-Patológica
2.K.1 - Critérios para indicação de biópsia hepática
A biópsia hepática é indicada na rotina do SAE/HD para todo indivíduo com
infecção pelo VHC confirmada por PCR qualitativo detectado, independente dos valores
das aminotransferases, e que não tenham contra-indicações ao procedimento e/ou ao
tratamento específico com interferon e ribavirina.
- Contra-indicações ao procedimento: hemoglobina sérica inferior a 10 g/dL,
contagem de plaquetas inferior a 75.000/mm3 e qualquer alteração no coagulograma. - Contra-indicações ao tratamento: consumo abusivo de álcool nos últimos seis
meses, consumo regular de drogas ilícitas, hepatopatia descompensada (Child-Pugh B ou
C), cardiopatia grave, doença tireoidiana descompensada, neoplasias, diabete melittus
tipo 1 de difícil controle ou descompensada, convulsões não controladas,
Casuística e Métodos
indivíduos infectados pelo HIV-1, também é necessário atingir estabilidade clínica, como
descrito no item 2.F deste capítulo.
2.K.2 - Procedimento da Biópsia
A biópsia hepática foi realizada por profissional médico da Seção de
Radiodiagnóstico do HC FMB - Unesp, no momento do exame ultrassonográfico de fígado.
Para tanto, o paciente foi colocado em divã clínico, em posição de decúbito dorsal
horizontal. Durante o exame, foi marcado o ponto para introdução da agulha de biópsia
entre os arcos costais, à direita, realizando-se, aí, antissepsia com Povidine® tópico. Foi utilizada anestesia local, com cerca de 10 ml de lidocaína a 2% sem vasoconstritor, no
ponto marcado para a biópsia. A seguir, a agulha de Trucut 16G para biópsia hepática foi
introduzida até atravessar a musculatura intercostal, extraindo o fragmento de fígado.
Retirada a agulha, o material da biópsia foi recuperado de sua luz, após lavagem com
água destilada, e imediatamente colocado em frasco contendo formol.
As amostras de tecido hepático foram processadas na rotina do Laboratório de
Anatomia Patológica do HC FMB - Unesp, sendo utilizadas as técnicas de
hematoxilina-eosina (HE), retículo e Masson, para o estadiamento histológico . É importante ressaltar
que a supervisão da equipe que realizou as leituras histopatológicas do material da
biópsia foram feitas, em todos os doentes, pela mesma profissional, médica patologista,
responsável pela Seção de Hepatologia do Departamento de Patologia da FMB - Unesp.
As amostras foram classificadas e estadiadas de acordo com a classificação METAVIR (67). Os pacientes submetidos à biópsia hepática foram internados e mantidos em
observação por período de seis horas, na Enfermaria de Moléstias Infecciosas e
Parasitárias do HC FMB - Unesp. Durante a internação, foram realizadas medidas de pulso
periférico, pressão arterial e exame físico de abdome, a cada hora. Os pacientes
receberam alta quando, após todos esses cuidados, não fossem verificados sinais ou
Casuística e Métodos
2.K.3 - Classificação das Alterações Histológicas Hepáticas (METAVIR)
A classificação das alterações histológicas das hepatites crônicas, utilizada no
presente estudo, foram propostas pelo grupo METAVIR em 1996, e observa os seguintes
parâmetros (67):
Alterações Estruturais (Fibrose)
0: ausência de fibrose;
1: expansão fibrosa portal, sem septos porta-porta;
2: expansão fibrosa portal, com poucos septos;
3: muitos septos, sem cirrose;
4: cirrose.
2.L - Determinação sérica de alanina-aminotransferase (ALT)
A determinação sérica de ALT foi realizada através do Método Química Seca, pelo
Laboratório de Análises Clínicas do HC FMB - Unesp, como parte da rotina de
atendimento ambulatorial dos pacientes infectados pelo HIV e/ou VHC no SAE/HD. A
coleta foi realizada no mesmo dia da biópsia hepática.
2.M - Determinação de citocinas séricas
Nos cinco grupos de estudo foi realizada a determinação das seguintes citocinas
séricas: IL-2, IL-4, IL-10, TNF-α, INF-γ, TGF-β
Foram colhidos em tubo seco oito ml de sangue. Os soros obtidos foram
estocados em alíquotas sob refrigeração a - 80°C. Os níveis séricos das citocinas foram
determinados pelo método de ELISA, por meio de kits comerciais (R&D Systems).
Inicialmente, microplacas de 96 orifícios foram sensibilizadas com anticorpo
monoclonal anticitocina a ser dosada (IL-2, IL-4, IL-10, TNF-α, IFN-γ e TGF-β). A seguir,
foram adicionados os soros testes (diluição 1:2) e dos controles positivo e negativo, que
foram então incubados à temperatura ambiente por duas horas. Após esse
procedimento, foram realizadas quatro lavagens com solução detergente contendo
Casuística e Métodos
substrato. Posteriormente, as placas foram incubadas à temperatura ambiente com
anticorpo policlonal anticitocina a ser dosada, conjugado com peroxidase. Após o período
de incubação, o substrato formado por peróxido de hidrogênio (0,02%) e
tetrametilbenzina (2%) foi adicionado aos orifícios das placas. A interrupção da reação foi
realizada à temperatura ambiente, utilizando-se ácido sulfúrico 2M. Os resultados foram
avaliados pela leitura da densidade óptica (DO) em leitor automático de ELISA (Titertek
Multiskan), em comprimento de onda de 450 nm. As concentrações das citocinas, em
pg/ml, foram calculadas a partir dos resultados em DO aplicados em curva padrão de
citocina recombinante utilizada como controle.
2.N - Quantificação relativa de mRNA por PCR em tempo real para citocinas
Nos cinco grupos de estudos foi realizada a quantificação relativa de mRNA por
PCR em tempo real das seguintes citocinas: INF-γ, IL-2, IL-4, IL-10, TNF-α e TGF-β.
2.N.1 - Isolamento e cultura de células mononucleares totais
Foram coletados 20 ml de sangue periférico por punção venosa, e colocados em
tubo estéril, contendo 200 μL de heparina (Liquemine, Roche®). As células mononucleares
foram obtidas por meio de separação em gradiente de Ficoll-Hypaque. O anel rico em
linfócitos e monócitos foi lavado por duas vezes com meio de cultura RPMI 1640 (Gibco
Laboratories, Grand Island, N. Y.) por 10 minutos a 200 g, cada lavagem. Após este
período, a suspensão celular foi ressuspensa em meio de cultura RPMI 1640
suplementado com 2 mM de L-glutinina (Sigma Chemical Co., ST Louis, MO, USA), 40
μg/ml de gentamicina e 10% de soro sendo a identificação, a verificação de viabilidade e a
contagem realizadas utilizando corante Turk (alíquotas de 50 μl da suspensão celular
acrescidas de 50 μl da solução corante a 5%). A concentração celular foi ajustada para
2x106 células viáveis/ml após contagem em câmara hemocitométrica.
2.N.2 - Extração de RNA
Casuística e Métodos
extraído foi tratado com DNAse (RQ1 RNAse Free-DNAse, M6,101, Promega) para a
purificação do RNA, de acordo com as instruções do fabricante. O RNA obtido foi
quantificado com o auxílio de espectofotômetro NanoDrop (NP-1000) a 260 nm e 280 nm.
2.N.3 - Obtenção do cDNA
O cDNA foi sintetizado a partir de 1Pg de RNA total. Para cada 1 Pg de amostra de
RNA foram adicionados 4 μl de Tampão da reação, 1 μl da mistura de nucleotídeos
(dNTP-mix) 10 mM, 1 μl de Random Primers, 1 μl Superscript, 1 μl de inibidor de RNAse
(GeneAmp- Applied Biosystems), 1 μl DTT, 1ul RNAse H e H2O deionizada tratada com
0,1% de DEPC (dietilpirocarbonato).
Para a obtenção do cDNA, foi programado o aparelho Temociclador Mastercycler
(Eppendorf) por 25°C por cinco minutos, 50°C por 50 minutos, 70°C por 15 minutos e 37°C
por 20 minutos.
2.N.4 - RT-PCR
Para a detecção da produção de mRNA para as citocinas foram utilizados primers
específicos:
Forward Reverse
β-actina CTGGAACGGTGAAGGTGACA AAGGGACTTCCTGTAACAATGCA
TNF-α CACGCTCTTCTGCCTGCTG GATGATCTGACTGCCTGGGC
TGF-β GGACACCAACTATTGCTTCAG TCCAGGCTCCAAATGTAGG
IFN-γ AGCTCTGCATCGTTTTGGGTT GTTCCATTATCCGCTACATCTGAA
IL-2 GAATGGAATTAATAATTACAAGAATCCC GACACTGAAGATGTTTCAGTTCTGT
IL-4 AACAGCCTCACAGAGCAGAAGACT GCCCTGCAGAAGGTTTCCTT
Casuística e Métodos
Os primers foram desenhados utilizando o software IDSciTools (www.idtdna,com)
a partir de seqüência publicada no Genebank.
A reação de PCR em tempo real para a quantificação relativa de mRNA das
citocinas, foi desenvolvida no aparelho de PCR em tempo real modelo 7300 ( Applied
Biosystems, EUA) com o uso do kit Power Syber Green PCR Master Mix (Applied
Biosystems, EUA) conforme as instruções do fabricante, em um volume final de 20 μl,
com adição de 4 μl da amostra de cDNA (obtido conforme item 2.N.3) por reação e 300
nM de cada primer. As condições da reação foram: 95°C por 10 minutos, seguidos de 40
ciclos de 95°C por 15 segundos e 60°C por um minuto, sendo os sinais de fluorescência
adquiridos nos passos de anelamento e extensão do ciclo de amplificação (60°C por um
minuto). Em todas as placas foi adicionado o cDNA de uma mesma amostra utilizada para
construção da curva padrão. Paralelamente, foi realizada a amplificação do gene da E
-actina, visto que o valor real de expressão gênica foi realizado através da comparação do
resultado da amplificação dos genes de interesses, e desse gene constitutivo. Os valores
de expressão relativa para cada amostra testada foi fornecida diretamente pelo programa
SDS versão 1.23, (Sequence Detection Systems 1.2.3 – 7300 Real Time PCR Systems-
Applied Biosystems, EUA), e posteriormente normalizados pelos valores de expressão
relativa da β-actina.
2.O - Análise Estatística
Para comparar as variáveis sexo, idade e cor da pele foi utilizado o teste χ2 e o teste exato de Fisher, com um nível de significância de p < 0,05.
Na análise das citocinas, foi calculado para o grupo controle (G5) média ( ) e
desvio padrão (σ). Os valores inferiores e superiores de normalidade das citocinas séricas
e por RT-PCR foram então calculados subtraindo e somando respectivamente dois desvios
padrão ( -/+ 2σ) dos valores de G5. A comparação entre os grupos também foi obtida
pelo teste não paramétrico de Kruskal-Wallis, ajustado pelo teste de Dunn, com o cálculo
das estatísticas H e p (com distribuição de χ2) e contrastes entre postos médios dos
Casuística e Métodos
Os perfis de citocinas séricas e por RT-PCR foram definidos por alteração de dois
desvios padrão em relação às médias normais de G5. Então, o perfil Th-1 foi definido
quando as médias de IL-2 e INF-γ foram maiores que dois desvios padrão do G5, e as
médias de IL-4 e IL-10 foram comparáveis ao G5. O perfil maduro Th-0 foi considerado
quando as médias de INF-γ e a IL-4 foram maiores que dois desvios padrão de G5,
independente da elevação de outras citocinas (IL-2 e/ou IL-10). O perfil Th-2 foi definido
quando as médias de IL-4 e a IL-10 foram maiores que dois desvios padrão do G5, e as
médias de IL-2 e o IFN-γ foram comparáveis ao G5. A mesma interpretação foi refeita com
os resultados obtidos pelo teste não paramétrico de Kruskal-Wallis, ajustados pelo teste
de Dunn. Essa linha de análise de perfil de citocinas foi também utilizada em outro
trabalho realizado em nosso meio (54).
3. Apreciação pelo Comitê de Ética em Pesquisa
O presente estudo foi submetido e aprovado pelo do Comitê de Ética em Pesquisa
da Faculdade de Medicina de Botucatu – Unesp, sob o protocolo Of. 243/2007-CEP
FMB/Unesp (anexos 2 e 3).
4. Registro de Ensaio Clínico
O presente estudo foi registrado no ClinicalTrials.gov sob o protocolo NCT
00499434 (anexo 4).
5. Financiamento e Apoio Institucional
O presente estudo recebeu financiamento da Fundação de Amparo à Pesquisa do
Estado de São Paulo (FAPESP), modalidade auxílio à pesquisa, processo nº 2007/56695-6
(anexo 5). Houve por contrapartida da Faculdade de Medicina de Botucatu - Unesp, o
fornecimento de insumos para a coleta das amostras, a retirada de prontuários médicos,
a análise estatística, a tradução para o inglês, a revisão da referência bibliográfica e a
Resultados
III - Resultados
1 - Homogeneidade entre os grupos
A distribuição dos 71 indivíduos estudados em relação ao gênero, idade e cor da
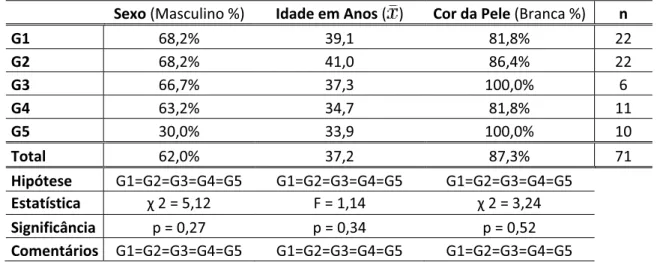
pele está apresentada na tabela 1.
Tabela 1: Distribuição dos 71 indivíduos estudados em relação ao sexo, idade e cor da pele. Porcentagem de ocorrências e médias. Estatísticas calculadas e comentários.
Sexo (Masculino %) Idade em Anos ( ) Cor da Pele (Branca %) n
G1 68,2% 39,1 81,8% 22
G2 68,2% 41,0 86,4% 22
G3 66,7% 37,3 100,0% 6
G4 63,2% 34,7 81,8% 11
G5 30,0% 33,9 100,0% 10
Total 62,0% 37,2 87,3% 71
Hipótese G1=G2=G3=G4=G5 G1=G2=G3=G4=G5 G1=G2=G3=G4=G5
Estatística χ 2 = 5,12 F = 1,14 χ 2 = 3,24
Significância p = 0,27 p = 0,34 p = 0,52
Comentários G1=G2=G3=G4=G5 G1=G2=G3=G4=G5 G1=G2=G3=G4=G5
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados com o VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável; G5: indivíduos doadores de sangue.
Em relação ao sexo, no total 62% dos indivíduos eram do sexo masculino e 38% do
feminino; no G1 e G2, 68,2% dos pacientes eram do sexo masculino e 31,8% do sexo
feminino; no G3, 66,7% dos pacientes eram do sexo masculino e 33,3% do sexo feminino;
no G4, 63,2% dos pacientes eram do sexo masculino e 36,8% do sexo feminino e, no G5,
30% dos indivíduos eram do sexo masculino e 70% do sexo feminino.
Em relação à idade, no total a média encontrada foi de 37,2 anos, no G1 a média
foi de 39,1 anos, no G2 a média foi de 41,0 anos, no G3 a média foi de 37,3 anos, no G4 a
média foi de 34,7 anos e, no G5, a média foi de 33,9 anos.
Em relação à cor da pele, no total 87,3% dos indivíduos se declararam brancos e
12,2% negros; no G1, 81,8% dos pacientes se declararam brancos e 18,2% negros; no G2,
Resultados
se declararam brancos; no G4, 81,8% dos pacientes se declararam brancos e 18,2%
negros; e no G5, 100,0% dos pacientes se declararam brancos.
2 - Linfócitos T CD4, carga viral plasmática do HIV, genótipo do VHC e fibrose hepática
2.A - Contagem de Linfócitos T CD4+
O gráfico 1 ilustra a distribuição dos valores de linfócitos T CD4 entre os grupos de
indivíduos portadores de infecção pelo HIV (Grupos 1, 3 e 4).
Gráfico 1: Distribuição dos valores de linfócitos T CD4+ entre os grupos de indivíduos
portadores de infecção pelo HIV (Grupos 1, 3 e 4).
0%
25%
50% 75% 100%
Grupo 1 Grupo 3 Grupo 4 Total
50% 33,3% 81,2% 56,5% 27,3% 33,3% 18,2% 25,6% 22,7% 33,3% 17,9%
> 351 201-350 < 200
CD4
G1: pacientes portadores da coinfecção HIV/VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável;
G4: pacientes monoinfectados pelo HIV com carga viral indetectável. CD4: contagem de linfócitos T CD4+ em células/mm3.
Em G1, a distribuição dos valores de linfócitos T CD4 mostrou que na faixa menor
que 200 células/mm3 se concentraram cinco indivíduos (22,7%), na faixa entre 201 a 350 células/mm3, seis indivíduos (27,3%) e na faixa acima de 350 células/mm3, 11 indivíduos
(50%). Já no grupo 3, a distribuição dos valores de linfócitos T CD4 mostrou uma
concentração de dois indivíduos por faixa de variação de linfócitos T CD4 (33,3%). No
Resultados
valores de linfócitos T CD4 mostrou que na faixa menor que 200 células/mm3 se
concentraram sete indivíduos (17,9%), na faixa entre 201 a 350 células/mm3, 10
indivíduos (25,6%) e na faixa acima de 350 células/mm3, 22 indivíduos (56,5%).
2.B - Carga Viral Plasmática do HIV-1
O gráfico 2 ilustra a distribuição dos valores de carga viral plasmática do HIV-1
entre os grupos de indivíduos portadores de infecção pelo HIV-1 (Grupos 1, 3 e 4).
Gráfico 2: Distribuição dos valores de carga viral plasmática do HIV-1 entre os grupos de indivíduos portadores de infecção pelo HIV (Grupos 1, 3 e 4).
0% 25% 50% 75% 100%
Grupo 1 Grupo 3 Grupo 4 Total
68,2%
100%
63,9%
31,8%
100%
36,1%
CV Indetectável CV Detectável
G1: pacientes portadores da coinfecção HIV/VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável. Cv: carga viral plasmática do HIV.
No grupo 1, sete indivíduos (31,8%) tiveram CV-HIV detectável, e 15 (68,2%)
indetectável. Os grupos 3 e 4 por definição tiveram 100% dos indivíduos com CV-HIV
detectável e indetectável, respectivamente. No total, 13 indivíduos (36,1%) tiveram
Resultados
2.C - Genótipos do VHC
O gráfico 3 ilustra a distribuição genotípica do VHC entre os grupos de indivíduos
portadores de infecção pelo VHC (Grupos 1 e 2).
Gráfico 3: Distribuição genotípica do VHC entre os grupos de indivíduos portadores de infecção pelo VHC (Grupos 1 e 2).
0% 25% 50% 75% 100%
Grupo 1 Grupo 2 Total
91%
63,7% 77,3%
9%
4,5% 9%
27,3% 18,2%
Genótipo 1 Genótipo 2 Genótipo 3
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados pelo VHC.
No grupo 1, 20 indivíduos (91%) eram do genótipo 1 do VHC, enquanto 2 (9%)
eram do genótipo 3. Já no grupo 2, 14 indivíduos (63,7%) pertenciam ao genótipo 1, dois
indivíduos (9%) ao genótipo 2 e seis (27,3%) ao genótipo 3. No total, 34 indivíduos
Resultados
2.D - Fibrose Hepática
O gráfico 4 ilustra a distribuição de fibrose hepática (classificação METAVIR) entre
os grupos de indivíduos portadores de infecção pelo VHC (Grupos 1 e 2).
Gráfico 4: Distribuição da fibrose hepática (classificação METAVIR) entre os grupos de indivíduos portadores de infecção pelo VHC (Grupos 1 e 2).
0% 25% 50% 75% 100%
Grupo 1 Grupo 2 Total
4,5% 9% 6,8%
54,5% 59% 56,9%
32% 23% 27,3%
9% 9% 9%
Grau 1 Grau 2 Grau 3 Grau 4
Fibrose
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados pelo VHC.
No grupo 1, um paciente (4,5%) exibiu grau 1 de fibrose hepática, 12 (54,5%)
tinham grau 2, sete (32%) grau 3 e dois pacientes (9%) grau 4. No grupo 2, dois pacientes
(9%) tinham grau 1 de fibrose hepática, 13 (59%) grau 2, cinco grau 3 (27,3%) e dois (9%)
Resultados
3 - Valores de referência de normalidade para as citocinas
A tabela 2 ilustra os valores de referência de normalidade das citocinas, que foram
calculadas a partir dos resultados do G5 (doadores de sangue).
Tabela 2: Valores estipulados como de referência de normalidade, com limites inferiores e superiores ( -/+ 2σ), baseados nos resultados encontrados no Grupo 5 (G5).
Média Desvio Padrão Limite Inferior Limite Superior RT PCR (mRNA)
TNF-α 22,40 5,36 11,68 33,12
IFN-γ 25,40 5,42 14,56 36,24
IL-2 23,80 4,29 15,22 32,38
IL-4 19,60 4,48 10,65 28,55
TGF-β 43,30 9,24 24,82 61,78
IL-10 19,80 4,87 10,06 29,54
ELISA (pg/ml)
TNF-α 109,30 14,61 80,09 138,51
IFN-γ 180,20 63,96 52,28 308,12
IL-2 130,30 40,86 48,57 212,03
IL-4 7,20 4,87 0,00 16,94
TGF-β 139,50 24,75 90,00 189,00
IL-10 11,70 5,77 0,15 23,25
G5: indivíduos doadores de sangue
Houve tendência de distribuição simétrica, permitindo o cálculo dos valores
inferiores e superiores de normalidade pelo desvio padrão, seguindo descrição contida no
Resultados
4 - Comparação entre as citocinas nos grupos de estudo e o grupo controle
4.A - Comparação pelos valores Limite Inferior e Superior e pelo teste estatístico de Kruskal-Wallis, seguido pelo teste de Dunn
O quadro 01 mostra quais grupos diferiram do controle de acordo com cada
citocina estudada, quando se utilizou os valores Limite Inferior e Superior ou o teste
estatístico de Kruskal-Wallis, seguido pelo teste de Dunn.
Quadro 1: Comparação dos valores de citocinas por RT-PCR e ELISA entre os grupos de estudo (G1, G2, G3 e G4) e o grupo controle (G5), utilizando o desvio padrão da
normalidade e pelo teste estatístico de Kruskal-Wallis, seguido pelo teste de Dunn.
Desvio Padrão Kruskal-Wallis Dunn Citocina G1 G2 G3 G4 G1 G2 G3 G4
IFN-γ RT-PCR
ELISA
IL-2 RT-PCR Valores Superiores ao G5
ELISA Valores Equivalentes ao G5
IL-4 RT-PCR
ELISA
IL-10 RT-PCR
ELISA
TNF-α RT-PCR
ELISA
TGF-β RT-PCR
ELISA
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados com o VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável; G5: indivíduos doadores de sangue.
Quando as citocinas dos grupos de estudo foram comparadas ao grupo controle
utilizando os limites inferiores e superiores, o perfil das citocinas dosadas por RT-PCR
ficou do seguinte modo: INF-γ superior em G1, G2, G3 e G4; IL-2 superior em G4; IL-4
superior em G2, G3 e G4; IL-10 superior em G1, G2, G3 e G4; TNF superior em G1, G2, G3
e G4 e TGF-β superior em G1 e G2. Já o perfil de comparação dessas citocinas dosadas por
ELISA teve o seguinte resultado: INF-γ superior em G2; IL-4 superior em G1; G2, G3 e G4;
Resultados
Quando a comparação foi realizada se utilizando o teste estatístico de
Kruskal-Wallis, seguido pelo teste de Dunn, o perfil das citocinas dosadas por RT-PCR ficou do
seguinte modo: INF-γ superior em G1, G2; IL-2 superior em G4; IL-4 superior em G2, G3 e
G4; IL-10 superior em G1, G3 e G4; TNF superior em G1, G2 e TGF-β superior em G1 e G2.
Já o perfil de comparação dessas citocinas dosadas por ELISA teve o seguinte resultado:
INF-γ superior em G2; IL-4 superior em G2, G3 e G4; IL-10 superior em G1, G2, G3 e G4;
TNF superior em G1, G2 e TGF-β superior em G1 e G2.
4.B - Comparação entre IFN-γ, IL-2, IL-4 e IL-10 e interpretação do perfil imune
O quadro 2 ilustra especificamente o comportamento das citocinas mais
intimamente ligadas à caracterização dos perfis de resposta imune Th-1, Th-2 e Th-0
maduro, e sua interpretação.
Quadro 2: Comparação dos valores de IFN-γ, IL-2, IL-4 e IL-10 por RT-PCR e ELISA entre os grupos de estudo (G1, G2, G3 e G4) e o grupo controle (G5), utilizando o desvio padrão da
normalidade e pelo teste estatístico de Kruskal-Wallis, seguido pelo teste de Dunn.
Interpretação do perfil de resposta imune Th-1/Th-2.
IFN-γ IL-2 IL-4 IL-10
Grupo DP KD DP KD DP KD DP KD DP KD DP KD DP KD DP KD RT-PCR ELISA RT-PCR ELISA RT-PCR ELISA RT-PCR ELISA Perfil
G1 Th-2
G2 Th-0/Th-2
G3 Th-2
G4 Th-2
Valores Superiores ao G5 Valores Equivalentes ao G5
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados com o VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável; G5: indivíduos doadores de sangue; DP: cálculo pelo desvio padrão da normalidade; KD: teste estatístico de Kruskal-Wallis, seguido pelo teste de Dunn.
O G1 teve IFN-γ superior ao G5 apenas quando dosado pelo RT-PCR, e a IL-2 se
mostrou equivalente pelos dois métodos, enquanto a IL-4 estava aumentada pelo ELISA
quando utilizado a análise pelo desvio padrão da normalidade, e a IL-10 se mostrou
aumentado por todos os meios. Tal comportamento foi interpretado como mais
Resultados
No G2 o IFN-γ foi superior por todas as análises, e a Il-2 se mostrou equivalente
pelos dois métodos, enquanto a IL-4 foi superior por todas as análises, o mesmo
acontecendo com a IL-10, com exceção da dosagem pelo RT-PCR utilizando o teste
estatístico de Kruskal-Wallis, seguido pelo teste de Dunn. Tal comportamento foi
interpretado como intermediário entre Th-0 e Th-2.
Já no G3 o IFN-γ foi superior ao G5 apenas quando dosado pelo RT-PCR na análise
pelo desvio padrão da normalidade, enquanto a IL-4 foi superior por todas as análises, o
mesmo acontecendo com a IL-10. Tal comportamento foi interpretado como mais
compatível com o perfil Th-2.
Finalmente no G4, o IFN-γ foi superior ao G5 apenas quando dosado pelo RT-PCR
na análise pelo desvio padrão da normalidade, e a IL-2 se mostrou superior quando
dosada por RT-PCR, enquanto a IL-4 foi superior por todas as análises, o mesmo
acontecendo com a IL-10, com exceção da dosagem pelo RT-PCR utilizando o teste
estatístico de Kruskal-Wallis, seguido pelo teste de Dunn. Tal comportamento foi
Resultados
4.C - Comparação individual entre as citocinas nos grupos de estudos e no grupo controle
4.C.1 - IFN-γ
Os gráficos 5 e 6 mostram a distribuição dos valores de IFN-γ dosados por RT-PCR
e ELISA respectivamente nos grupos estudados.
Gráficos 5 e 6: Distribuição dos valores de IFN-γ dosado por RT-PCR e ELISA respectivamente, nos grupos estudados.
pg/
m
l
G1 > G3/G4/G5 G2 > G5
*p < 0,05
G2 > G1/G3/G4/G5 *p < 0,05
RT-PCR ELISA
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados com o VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável; G5: indivíduos doadores de sangue. Estatística: Kruskal-Wallis, seguido pelo teste de Dunn.
Analisando a distribuição dos valores de IFN-γ dosados por RT-PCR, o resultado é
que G1 tem valores significativamente maiores que G3, G4 e G5, e que G2 tem valores
maiores que G5. Já pela dosagem sérica do IFN-γ por ELISA, os valores de G2 foram
Resultados
4.C.2 - IL-2
Os gráficos 7 e 8 mostram a distribuição dos valores de IL-2 dosados por RT-PCR e
ELISA respectivamente nos grupos estudados.
Gráficos 7 e 8: Distribuição dos valores de IL-2 dosado por RT-PCR e ELISA respectivamente, nos grupos estudados.
pg/
m
l
G4 > G1/G2/G5 *p < 0,05
G4 > G1 *p < 0,05
RT-PCR ELISA
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados com o VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável; G5: indivíduos doadores de sangue. Estatística: Kruskal-Wallis, seguido pelo teste de Dunn.
Analisando a distribuição dos valores de IL-2 dosados por RT-PCR, o resultado é
que G4 tem valores significativamente maiores que G1, G2 e G5. Já pela dosagem sérica
Resultados
4.C.3 - IL-4
Os gráficos 9 e 10 mostram a distribuição dos valores de IL-4 dosados por RT-PCR e
ELISA respectivamente nos grupos estudados.
Gráficos 9 e 10: Distribuição dos valores de IL-4 dosado por RT-PCR e ELISA respectivamente, nos grupos estudados.
pg/
m
l
G2/G3 > G1/G5 G4 > G5
*p < 0,05
G2/G3/G4 > G1/G5 *p < 0,05
RT-PCR ELISA
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados com o VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável; G5: indivíduos doadores de sangue. Estatística: Kruskal-Wallis, seguido pelo teste de Dunn.
Analisando a distribuição dos valores de IL-4 dosados por RT-PCR, o resultado é
que G2 e G3 têm valores significativamente maiores que G1 e G5, e que G4 tem valores
maiores que G5. Já pela dosagem sérica do IL-4 por ELISA, os valores de G2, G3 e G4
Resultados
4.C.4 - IL-10
Os gráficos 11 e 12 mostram a distribuição dos valores de IL-10 dosados por
RT-PCR e ELISA respectivamente nos grupos estudados.
Gráficos 11 e 12: Distribuição dos valores de IL-10 dosado por RT-PCR e ELISA respectivamente, nos grupos estudados.
pg/
m
l
G1/G3 > G5 *p < 0,05
G1 > G2/G4/G5 G2/G3 > G5
*p < 0,05
RT-PCR ELISA
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados com o VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável; G5: indivíduos doadores de sangue. Estatística: Kruskal-Wallis, seguido pelo teste de Dunn.
Analisando a distribuição dos valores de IL-10 dosados por RT-PCR, o resultado é
que G1 e G3 têm valores significativamente maiores que G5. Já pela dosagem sérica da
IL-10 por ELISA, os valores de G1 foram superiores ao G2, G4 e G5 e os de G2 e G3
Resultados
4.C.5 - TNF-α
Os gráficos 13 e 14 mostram a distribuição dos valores de TNF-α dosados por
RT-PCR e ELISA respectivamente nos grupos estudados.
Gráficos 13 e 14: Distribuição dos valores de TNF-α dosado por RT-PCR e ELISA respectivamente, nos grupos estudados.
pg/
m
l
G1 > G4/G5 G2 > G5
*p < 0,05
G1 > G2/G4/G5 G2 > G5
*p < 0,05
RT-PCR ELISA
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados com o VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável; G5: indivíduos doadores de sangue. Estatística: Kruskal-Wallis, seguido pelo teste de Dunn.
Analisando a distribuição dos valores de TNF-α dosados por RT-PCR, o resultado é
que G1 tem valores significativamente maiores que G4 e G5, e que G2 tem valores
maiores que G5. Já pela dosagem sérica do TNF-α por ELISA, os valores de G1 foram
Resultados
4.C.6 - TGF-β
Os gráficos 15 e 16 mostram a distribuição dos valores de TGF-β dosados por
RT-PCR e ELISA respectivamente nos grupos estudados.
Gráficos 15 e 16: Distribuição dos valores de TGF-β dosado por RT-PCR e ELISA respectivamente, nos grupos estudados.
pg/
m
l
G1/G2 > G3/G4/G5 *p < 0,05
RT-PCR ELISA
G1/G2 > G3/G4/G5 *p < 0,05
G1: pacientes portadores da coinfecção HIV/VHC; G2: pacientes monoinfectados com o VHC; G3: pacientes monoinfectados pelo HIV com carga viral detectável; G4: pacientes monoinfectados pelo HIV com carga viral indetectável; G5: indivíduos doadores de sangue. Estatística: Kruskal-Wallis, seguido pelo teste de Dunn.
Analisando a distribuição dos valores de TGF-β dosados por RT-PCR, o resultado é
que G1 e G2 têm valores significativamente maiores que G3, G4 e G5. Os mesmo