DETERMINAÇÃO DE ÁCIDO BENZÓICO Ε ÁCIDO SÓRBICO EM IOGURTES COMERCIAIS.
Caio Cesar T o r r e s ( * ) Sebastião C. C. Brandão ( * * )
RESUMO
Quinze amoòtAOó
de
iogu
/uteò
comexciait,
fohAm analiòadaè,
quanto ao teoh. de
ácido
benzóico
e
òohhico, ροκ.
meio do, cn.omatogn.afia liquida de alta pefifonmance do. acondo com
Ito
tt ai. ! ? 9 £ 3 ) .
0 teoK de. ácido òõnhico em todaò aò amoòtjun, encontAava-òe den£&o do&
UmiteA e&tabelecidoò pon. lei.. 0 n,otulo de. t/ièA amoòttwA não continham a especificação
(P.
0 ácido benzóico foi enconüuxdo
em
todaò
OÓ
amoòtnxu,. devido a fermentação
lática nenhuma amoòtna. declamava a adição do ácido benzóico no n.ò~tulo.
INTRODUÇÃO
A determinação dos teores de conservantes em a l i m e n t o s é importante, porque seu uso é l i m i t a d o pela l e g i s l a ç ã o bromatológica b r a s i l e i r a . Os ácidos benzóico e s ó r b i c o são muito empregados na i n d ú s t r i a a l i m e n t í c i a , em polpas e sucos de f r u t a s , bases de f r u tas para i o g u r t e s , r e f r i g e r a n t e s , m a r g a r i n a s , revestimento de q u e i j o s , e t c . 0 M i n i s t é -r i o da Saúde adota o l i m i t e máximo de 0 , 2 ¾ ( 2 . 0 0 0 ppm) pa-ra polpa de f -r u t a s (mo-rango, pêssego e , a b a c a x i ) a d i c i o n a d a em i o g u r t e s , e e x i g e que o á c i d o s ó r b i c o ( P . IV) seja de-clarado no r ó t u l o do p r o d u t o .
Apesar da l e g i s l a ç ã o c i t a r d i v e r s o s a l i m e n t o s que possam ser a d i c i o n a d o s de ácido benzóico ( P . 1 ) , e e x i g i r que também seja d e c l a r a d o no r ó t u l o , ela não c i t a a adição de_s te conservante em polpas de f r u t a s para i o g u r t e s ( D e c r e t o - L e i n ° 5 5 . 8 7 1 de 2 6 . 0 3 . 6 5 ) .
Os ácidos s ó r b i c o e b e n z ó i c o , normalmente na forma de sorbato e benzoato de potá_s sio, são empregados como substâncias f u n g i s t á t i c a s . 0 ácido s ó r b i c o atua como i n i b i d o r no metabolismo de ácidos graxos α e β insaturados em fungos e leveduras (Melnick e t a l . ,
195
*0.
Diversos métodos podem ser u t i l i z a d o s na determinação dos ácidos s ó r b i c o e benzó_^ co, a exemplo do c o l o r i m é t r i c o , do e s p e c t r o f o t o m é t r i c o e c r o m a t o g r ã f i c o . Wahbi e t a l .
1 9 7 7 determinaram o á c i d o s ó r b i c o no l e i t e por e s p e c t r o f o t o m e t r i a u t i l i z a n d o a Ia
d e r i -vada da curva do seu e s p e c t r o de absorção. No P a í s , os métodos o f i c i a l m e n t e
recomenda-(*) Instituto Nacional de Pesquisas da Amazônia, Manaus-AM.
(**) Universidade Federal de Viçosa, Viçosa-MG.
dos são complexos e demandam muito tempo, desestimulando como conseq٧ência, o c o n t r o l e destes ácidos nos a l i m e n t o s . Um método mais e f i c a z para sua detecção (Coelho e t a l . , 1 9 8 3 ) , se torna n e c e s s á r i o .
Entre os métodos c r o m a t o g r á f i c o s , citam-se a cromatografia de camada f i n a , gasosa e l í q u i d a . D i v e r s o s t r a b a l h o s tem s i d o executados baseando-se nesta técnica para deteç ção dos ácidos s ó r b i c o e benzóico em produtos l á c t e o s . Coelho e t a l . (1983) analisaram a presença destes d o i s conservantes por cromatografia gasosa em d i v e r s o s a l i m e n t o s .
A cromatografia l í q u i d a de a l t o desempenho é uma das técnicas mais recentes para Ia q u a n t i f i c a ç ã o destes conservantes. Ela permite a n á l i s e rápida e a l t a s e n s i b i l i d a d e
para pequenas concentraçυes dos ácidos s ó r b i c o e b e n z ó i c o . Puttemans et a l . ( 1 9 8 5 ) ex-t r a í r a m esex-tes d o i s ácidos de i o g u r ex-t e s , u ex-t i l i z a n d o ex-t r i - n - o c ex-t i l a m i n a . S ex-t i j v e & Ηischenube r (198*0 detectaram baixos n í v e i s destes d o i s agentes conservantes em i o g u r t e s por meio de cromatografia l í q u i d a de a l t o desempenho por fase r e v e r s a ,
MATERIAIS Ε MÉTODOS
U t i l i z o u - s e um sistema i s o c r ã t i c o para o bombeamento da sol ução tampão-f osf a t o (pH **>5): metanol através de uma coluna de grupamentos s i l a n o s quimicamente ligados ã s i l i -ca. A q u a n t i f i c a ç ã o f o i efetuada por monitoramento da v a r i a ç ã o do í n d i c e de absorbãncia da f a s e móvel com padrυes e amostras.
Equipamentos
Foi u t i l i z a d o um sistema de bombeamento CG-*»80C da Instrumentos C i e n t í f i c o s CG equipado com um i n j e t o r Rheodyne 7 1 2 5 e um " l o o p " de l O O u l . Foram i n j e t a d o s volumes de 5 e 2 0 μ 1 das amostras preparadas com uma seringa Hamilton de 5 0 u l .
Empregou-se como detector o espectrofotômetro de ccmprimento de onda v a r i á v e l UV-50 da Varian Assoc. Para o ácido s ó r b i c o adotou-se o comprimento de onda de 2 5 0 n m , enquan_ to a atenuação f o i mantida em 0 , 2 X . A v a r i a ç ã o do í n d i c e de absorbância f o i mantida com um r e g i s t r a d o r Linear (20 c m / h ) . 0 preparo das amostras e degasagem da fase móvel f o -ram f e i t o s com um s o n i f i c a d o r modelo B-220 (Branson C o . ) com f r e q ٧ ê n c i a v a r i a n d o de 5 0 60 Hz.
Na c e n t r i f u g a ç ã o e a j u s t e do pH das amostras empregou-se, respecti vãmente, uma cen_ t r í f u g a modelo Κ I n t e r n a t i o n a l Equipment Co. e um pHmetro d i g i t a l modelo E500(Metrohm He r i s o n ) .
Condiçυes cromatograficas
1,5pm (Merck S . A . ) , enquanto a solução tampão-fosfato f o i preparada a p a r t i r de 1.000ml de água d e s t i l a d a , a c i d i f i c a d a com 1,2*» ml de ácido o r t o - f o s f ó r i c o ( m i n . 85%) P.A. (MercW S.A.) a t é pH 2,0 e b a s i d í f i ç a d a com 1 3 , 7 ml de h i d r ó x i d o de sódio 2,ON a t é pH k,S.
No preparo da solução padrão 0,001ľ (lOppm) f o i empregado sorbato e b e n z o a t o d e p c tássio grau P.A.
Preparo das amostras
Amostras de 15 d i f e r e n t e s marcas de i o g u r t e foram coletadas nos supermercados de Belo H o r i z o n t e (MG).
De duas marcas de i o g u r t e t i p o " s u n d a e " , a polpa de f r u t a f o i removida para o i o -gurte ser a n a l i s a d o separadamente. Uma amostra de i o g u r t e n a t u r a l f o i usada para se ve^ r i f i c a r a presença de p o s s í v e i s compostos i n t e r f e r e n t e s .
A extração do á c i d o s ó r b i c o e benzóico do i o g u r t e e da polpa de f r u t a f o i f e i t a de acordo com I to e t a l . ( 1 9 8 3 ) . A 20g da amostra a d i c i o n o u - s e 2 5 ml de h i d r ó x i d o de s ó d i o 0,1N. 0 pH da solução r e s u l t a n t e f o i a j u s t a d o para pH 8 , 0 , para e v i t a r s o l u b i 1 i z a ç ã o da s i l i c a da coluna cromatografica e , em s e g u i d a , s o n i f i ç a d a por 15 min. Após s o n i f i c a ção, a d i c i o n o u s e 1 ml de f e r r o c i a n e t o de p o t á s s i o 15ľ ( p / v ) e 1 ml de s u l f a t o de z i n -co 30¾ ( p / v ) para p r e c i p i t a ç ã o das p r o t e í n a s do i o g u r t e (reagentes de C a r r e z ) . A amos-tra amos-tratada f o i mantida em repouso por 15 m i n . e logo t r a n s f e r i d a para um tubo de c e n t r í fuga (capacidade 100 ml) e os resíduos a r r a s t a d o s com 2 5 ml de metanol P.A. (Grupo Quí-mica Ltda) e c e n t r i f u g a d a a 3 . 0 0 0 rpm por 10 min. 0 sobrenadante f o i t r a n s f e r i d o para, um balão volumétrico (100 ml) e o p r e c i p i t a d o lavado com 2 5 ml de metanol. 0 volume f i -nal do balão f o i completado com água.
As amostras foram f i l t r a d a s em f i l t r o M i l l i p o r e t i p o HA de 0 .'•Su m da Waters Assoc. para e l i m i n a r p a r t í c u l a s que poderiam e n t u p i r o f i l t r o da coluna a n a l í t i c a .
RESULTADO Ε DISCUSSÃO
As F i g u r a s 1 e 2 mostram o cromatograma das soluçυes padrυes dos ácidos sórbico e benzóico, respectivamente. A regressão l i n e a r da resposta do detector (mm) com o peso padrão, apresenta um c o e f i c i e n t e de c o r r e l a ç ã o de 0 , 9 8 6 e 0 , 9 9 2 , para os ácidos s ó r b i c o e b e n z ó i c o , respectivamente. As Figuras lb e 2 b mostram o cromatograma de iogurte na tu r a l , demonstrando resolução completa dos ácidos s ó r b i c o e b e n z ó i c o .
O Quadro I I ! mostra uma recuperação média de 3 6 , 3 8 ± 8 , 7 * * ¾ do ácido s ó r b i c o adi-cionado ao i o g u r t e , conforme F i g u r a s lc e I d .
0 Quadro IV mostra os n í v e i s de ácido benzóico em d i f e r e n t e s amostras de iogurte.
Nenhuma das amostras deixou de conter ácido b e n z ó i c o , e o Quadro V mostra que as amostras das polpas de f r u t a s a n a l i s a d a s continham n í v e i s r e l a t i v a m e n t e baixos do mesmo. Em ne-nhum dos r ó t u l o s das amostras constava a e s p e c i f i c a ç ã o deste conservante ( P . l ) . A le-g i s l a ç ã o ainda é omissa quanto a adição deste conservante em polpas de f r u t a s para io-g u r t e s .
0 Quadro VI mostra recuperação de 9 7 , 3 ± 2 5 , 0 ¾ do á c i d o b e n z ó i c o , conforme Figuras
2 c e 2 d , considerada s a t i s f a t ó r i a para os dois c o n s e r v a n t e s .
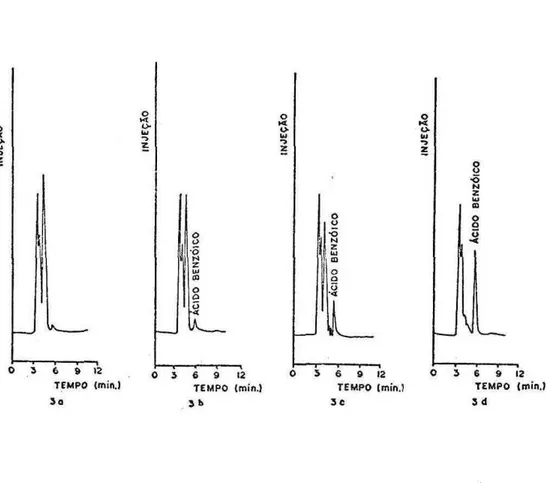
A Figura 3 mostra o r e s u l t a d o de um experimento r e a l i z a d o com l e i t e durante a ela boração de i o g u r t e na usina de l a t i c í n i o s da UFV. Uma amostra f o i coletada do l e i t e pa^ t e u r i z a d o , instantes antes da adição de 1¾ da c u l t u r a ( L . b u l g a r i c u s e S . thermophilus) e incubada a A 0 ° C / 3 h , e as 3 amostras seguintes de hora em h o r a . Foi observada a forma çao crescente de á c i d o benzóico até o f i n a l da incubação.
Os r e s u l t a d o s concordam com B e r t l i n g ( 1 9 8 6 ) e Schmidt-Hebbel (198*0 que observaram produção de ácido benzóico durante a fermentação do i o g u r t e , a p a r t i r do ácido h i p ú r i -co. 0 ácido benzóico e p r o d u z i d o por b a c t é r i a s da fermentação l a t i c a , alcançando níveis de 5 3 0 ppm. Segundo B e r t l i n g ( 1 9 8 6 ) , o ácido benzóico pode também r e s u l t a r de sua adi ção a f l a v o r i z a n t e s e/ou em polpa de f r u t a s conforme o Quadro V. Esta observação indi-ca a necessidade dos f a b r i c a n t e s de i o g u r t e s a n a l i s a r e m o produto f i n a l , antes de decla rarem que seus produtos são isentos deste c o n s e r v a n t e .
Pig. 1. Cromatograma de diferentes amostras de Iogurte. Fase móvel: metanol/ tampão
fosfato, pH 4,5 (50/50, v/v); fluxo = 0,7 ml/min.; atenuação: 0,5X; Detector:
ÜV - 250 nm.
Ia - Solução padrão,
lb - Iogurte natural,
lc - Iogurte sabor morango
Fig.
2 .
Cromatograma de diferentes amostras de Iogurte. Fase móvel: metanol / tampão
fosfato, pH 4,5 (50/50, v / v ) ; fluxo = 0,7 ml/min.; atenuação: 0,2X; Detector:
UV - 227 nm.
2a - Solução padrão.
2b - Iogurte natural.
2c - Iogurte sabor morango
2d - iogurte sabor morango adicionado de benzoato de potássio
6 9 12
T E M P O ( m i n . ) S o
O > 6 9 12 T E M P O ( m i n . ) 5 b
5 6 9 12 T E M P O ( m i n . s e
1 6 9 12 T E M P O ( m i n . ) 3 d
Fig. 3. Cromatograma de Amostras coletadas durante a elaboração de Iogurte Natural.
Fa-se móvel: metanol/tampão fosfato, pH 4,5 (50/50, v / v ) ; fluxo = 0,7 ml/min.; ate
nuação: 0,2X; Detector: UV - 227 nm.
3a - Leite pasteurizado.
Quadro I. Teor médio de á c i d o s ó r b i c o em d i f e r e n t e s i o g u r t e s c o m e r c i a i s .
Amostra R ó t u l o Concentração
(ppm ± d pa
)
1 P. IV 3 8 , 2 ± 0 , 5
2 P. IV 3 6 , 9 ± 0 , 5
3 P. IV ^ 9 , 9 ± 1 , 5
4 P. IV 7 2 , 7 ± 2 , 6
5 b 6 6 , 3 ± 0 , 8
6 9 6 , 7 ± 2 , 8
7 5 7 , 2 ± 1 , 3
8 P. IV 1 2 , 1 ± 0 , 3
9 P. IV 4 9 , 6 ± 0 , 6
10 P. IV 1 ^ , 2 ± 0 , 3
1 1 P. IV 1 9 , 2 ± 0 , 2
1 2 P. IV 1 7 , 3 ± 0 , 9
1 3 P. IV 2 3 , 0 ± 0 , 6
a
d p = d e s v i o padrão de t r ê s r e p e t i ç υ e s .
'"" = a e s p e c i f i c a ç ã o do conservante ( P . I V ) não consta no r ó t u l o do p r o d u t o .
Quadro I I . Teor médio de á c i d o s ó r b i c o na base de morango.
Amostra Concentração (ppm ± d pa
)
1 4 6 , 5 + 0,8
2 7 4 , 9 + 1,2
dp = desvio padrão de t r ê s r e p e t i ç υ e s .
Quadro I I I . Percentual médio de recuperação do á c i d o s ó r b i c o a d i c i o n a d o ao i o g u r t e .
Quantidade Adicionada (ppm) Recuperação ( ľ )3
1 9 4 , 8
2 77,4
5 87,0
a
Média de t r ê s r e p e t i ç υ e s .
Quadro IV. Teor médio de ácido benzóico em d i f e r e n t e s i o g u r t e s c o m e r c i a i s .
Amostra R ó t u l o Concentração
(ppm ± d pa
)
continuação (Quadro I V ) .
Amostra R ó t u l o Concentração
(ppm ± d pa
)
5 6 7 8 9
10
1 11 2
13
7 , 1 7 ± 0,02 7 . 0 7 ± 0 , 0 8 7 , 3 2 ± 0,03 6 , 9 0 ± 0,04 6,86 ± 0 , 1 3 7 , 0 3 ± 0,04 7 . 0 8 ± 0 , 1 1 6,90 ± 0,02 7 , 1 3 ± 0,21
'dp t* d e s v i o padrão de t r ê s r e p e t i ç υ e s .
) = a e s p e c i f i c a ç ã o do conservante P . I . não consta no r ó t u l o do p r o d u t o .
Quadro V. Teor médio de ácido benzóico na base de morango.
Amostra Concentração (ppm ± d p * )
1 4,56 ± 0 , 2 7
2 3,49 ± 0,05
dp = d e s v i o padrão de t r ê s r e p e t i ç υ e s .
Quadro V I . Percentual médio de recuperação do ácido benzóico a d i c i o n a d o ao i o g u r t e .
Quantidade adicionada (ppm) Recuperação [%) a
1 0 115,0
2 0 7 9 , 6
SUMMARY