NATALIA MEDINA RAMÍREZ
MODULAÇÃO DOS FATORES DE RISCO METABÓLICO ASSOCIADOS À OBESIDADE, POR CHÁ DE FOLHAS DE MANGUEIRA (Mangifera indica L. variedade Ubá), EM RATOS ALIMENTADOS COM DIETA HIPERLIPÍDICA
Dissertação apresentada à Universidade Federal de Viçosa, como parte das exigências do Programa de Pós-Graduação em Ciência da Nutrição, para obtenção do título de Magister Scientiae.
VIÇOSA
NATALIA MEDINA RAMÍREZ
MODULAÇÃO DOS FATORES DE RISCO METABÓLICO ASSOCIADOS À OBESIDADE, POR CHÁ DE FOLHAS DE MANGUEIRA (Mangifera indica L. variedade Ubá), EM RATOS ALIMENTADOS COM DIETA HIPERLIPÍDICA
Dissertação apresentada à Universidade Federal de Viçosa, como parte das exigências do Programa de Pós-Graduação em Ciência da Nutrição, para obtenção do título de Magister Scientiae.
APROVADA: 24 de fevereiro de 2015
_______________________________ _______________________________
Maria Eliza de Castro Moreira João Paulo Viana Leite
_______________________________ _______________________________
Maria Inês de Souza Dantas José Humberto de Queiroz (Coorientador)
Aos familiares, amigos e cada pessoa que
“Cuando se abre nuestra visión interior, se
AGRADECIMENTOS
Aos meus pais, José Marino e Maria Eunice, pelo apoio incondicional em cada
etapa da minha vida, pelo amor e por serem uns excelentes guias.
Aos meus irmãos, Lorena e Camilo, por serem um exemplo de luta e por contribuir
para realizar meus projetos de vida.
Aos meus sobrinhos, Tomás e Mateo, por serem minha força e por me ensinar a
sorrir cada dia.
Ao meu namorado David, pelo amor, apoio incondicional e por tantos momentos
de felicidade.
Aos meus grandes amigos por me incentivarem e me acompanharam neste
caminho.
À professora Sônia Machado Rocha por sua maravilhosa orientação e disposição
para me ajudar, me guiar e me compartilhar seus conhecimentos. Muito obrigada por
fazer desta experiência, algo inesquecível.
Aos professores: Hércia Stampini, João P. Viana, José H. de Queiroz, Maria I.
Dantas, Andréia Q. Ribeiro e Laércio A. Benjamin pelo auxílio neste trabalho e seu olhar
científico.
Aos colegas de trabalho dos Laboratórios de Nutrição Experimental do
Departamento de Nutrição e Saúde, Metabolismo e Fermentação e Biodiversidade do
Departamento de Bioquímica Agrícola, da Universidade Federal de Viçosa.
Especialmente agradeço a Renata Lopes, a Maria Eliza Castro e a Letícia Monteiro pela
constante ajuda, amizade, paciência e carinho.
Aos professores e funcionários do Departamento de Nutrição e Saúde, pela
À PPGCN e a Universidade Federal de Viçosa, pela oportunidade do mestrado.
À CAPES pela concessão da bolsa de mestrado e à FAPEMIG pelo apoio
financeiro ao projeto.
Agradeço a todos os que contribuíram direta ou indiretamente para a realização
deste trabalho.
SUMARIO
RESUMO...xvii
ABSTRACT...xix
LISTA DE FIGURAS...x
LISTA DE TABELAS...xii
LISTA DE ABREVIATURAS, SIGLAS E SÍMBOLOS...xiv
INTRODUÇÃO GERAL...1
CAPITULO 1. REVISÃO BIBLIOGRÁFICA 1. Síndrome metabólica: mecanismos e alterações 1.1.Componentes da SM...4
1.1.1. Obesidade abdominal...4
1.1.2. Dislipidemia aterogênica...5
1.1.3. Elevada pressão arterial...5
1.1.4. Resistência insulínica...5
1.2.Patogênese e mecanismos fisiopatológicos da síndrome metabólica...5
1.3.Metabolismo dos adipócitos na síndrome metabólica...8
1.4.Hiperplasia e Hipertrofia do tecido adiposo...10
1.5.Mecanismos de inflamação e de estresse oxidativo...11
1.5.1. Inflamação...11
1.5.2. Estresse oxidativo (EO) ...12
1.5.3. Genes envolvidos em mecanismos inflamatórios e na homeostase redox...13
2. Compostos bioativos da Mangifera indica. 2.1.Mangiferina...14
3. Consumo de chás e seu uso no controle das alterações metabólicas associadas à
obesidade... 15
Conclusão...17
Referências bibliográficas ...18
CAPITULO 2. AVALIAÇÃO DA EFICÁCIA DE EXTRAÇÃO DE MANGIFERINA E ANÁLISES QUÍMICA, ANTIOXIDANTE E SENSORIAL DO CHÁ DE FOLHAS DE Mangifera indica L., VARIEDADE UBÁ Resumo ...31
Abstract...32
1. Introdução...32
2. Materiais e métodos...35
2.1.Reagentes...35
2.2.Material vegetal...35
2.3.Desenvolvimento do chá avaliando três técnicas de preparo...35
2.3.1. Preparo dos chás...35
2.3.2. Quantificação da Mangiferina...36
2.4.Caracterização físico-química do chá obtido por decocção...37
2.4.1. Quantificação de fenólicos totais (FT) ...37
2.4.2. Avaliação da atividade antioxidante (AA) ...37
2.5.Avaliação da estabilidade oxidativa do chá...38
2.6.Análise sensorial...38
2.6.1. Preparo dos chás...38
2.6.2. Teste...38
2.7.Análise estatística...38
3. Resultados e discussão...39
3.1.Concentração de mangiferina nos chás preparados por três diferentes técnicas...39
3.2.Caracterização físico-química do chá...41
3.3.Estabilidade...43
CAPITULO 3. EFEITO ANTI-OBESIDADE DO CHÁ DE FOLHAS DE Mangifera
indica L. var. UBÁ EM RATOS ALIMENTADOS COM DIETA HIPERLIPÍDICA.
Resumo...51
Abstract...52
1. Introdução...53
2. Materiais e métodos...54
2.1.Preparo do chá ...54
2.2.Experimento, animais e dietas...55
2.3.Parâmetros avaliados...55
2.3.1. Consumo da dieta, chá e parâmetros biométricos...55
2.3.2. Constituintes bioquímicos do sangue...56
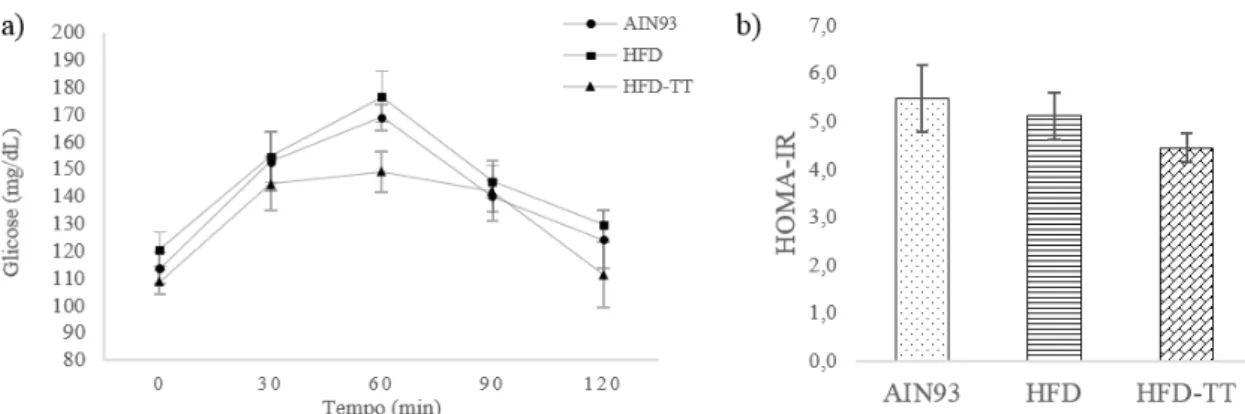
2.3.3. Teste de tolerância oral à glicose e HOMA-IR...56
2.3.4. Concentrações de TNF-α e IL-10 no plasma...56
2.3.5. Análise histológica de hepatócitos e adipócitos...56
2.3.6. Nível de expressão de genes no tecido adiposo epididimal...58
2.4. Análise estatística...57
3. Resultados...58
3.1.Consumo da dieta, chá e parâmetros biométricos...58
3.2.Efeito do chá sobre os parâmetros bioquímicos séricos...59
3.3.Efeito do consumo do chá no metabolismo da glicose...59
3.4.Efeito anti-inflamatório e pro-inflamatório do chá...60
3.5.Efeito do chá nos tecidos hepático e epididimal ...60
3.5.1. Hepatócitos...60
3.5.2. Adipócitos...61
3.6.Efeito do chá no metabolismo de lipídios...63
4. Discussão...63
5. Conclusão...66
6. Referências...67
ANEXOS Anexo 1...73
Anexo 2...76
Anexo 4...78
Anexo 5...79
LISTA DE FIGURAS
CAPITULO 1. REVISÃO BIBLIOGRÁFICA
Figura 1. Interações de componentes moleculares e o tecido adiposo na síndrome
metabólica...6
Figura 2. Biomarcadores e mecanismos fisiopatológicos na síndrome metabólica...8
Figura 3. Regulação da lipólise e lipogênese nos adipócitos...11
Figura 4. Hiperplasia e Hipertrofia adipócitos na obesidade...12
CAPITULO 2. AVALIAÇÃO DA EFICÁCIA DE EXTRAÇÃO DE MANGIFERINA E ANÁLISES QUÍMICA, ANTIOXIDANTE E SENSORIAL DO CHÁ DE FOLHAS DE Mangifera indica L., VARIEDADE UBÁ. Figura 1. Estrutura da mangiferina...33
Figura 2. Conteúdo de mangiferina nos chás utilizando as três técnicas de preparo e três relações da droga vegetal/ solvente a partir de (a) folhas novas e (b) folhas maduras de M. indica ………...39
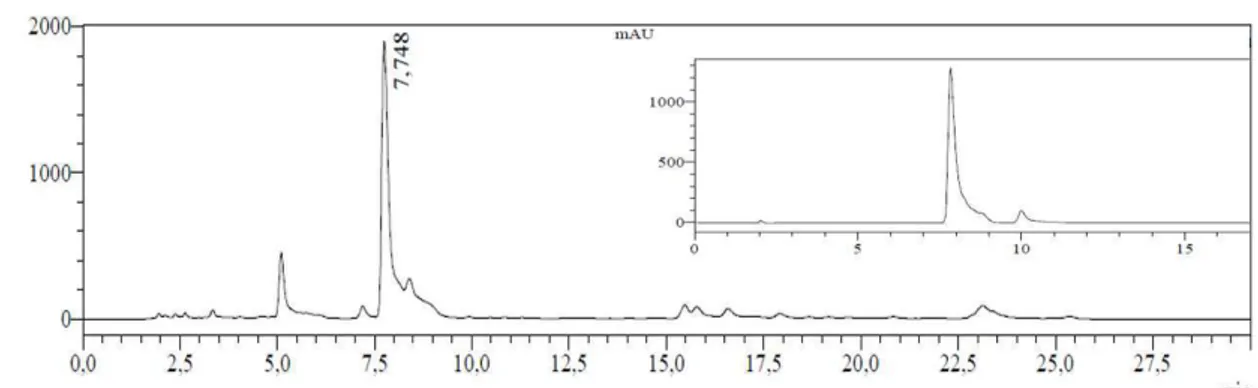
Figura 3. Cromatograma do chá de folhas de M. indica e padrão de mangiferina. ...41
Figura 4. Estabilidade do conteúdo de (a) Mangiferina, (b) Fenólicos Totais e (c) Atividade de retirada de Radical dos chás, nos dois métodos de conservação (Refrigeração 4± 2 ºC e Temperatura ambiente 20 ± 2 ºC) e nos tempos (0, 24 e 48 horas). ……...43
Figura 2. Concentrações plasmáticas (pg.µm-1) de IL-10 e TNF-α em ratos alimentados com dieta controle (AIN93), hiperlipídica (HFD) e hiperlipídica suplementada com chá
(HFD-TT)...……...62
Figura 3. Histologia do tecido hepático de ratos alimentados com a) AIN93, dieta
controle; b) HFD, dieta hiperlipídica; c) HFD-TT; dieta hiperlipídica suplementada com
chá; d) Relação núcleo-plasmática dos hepatócitos………...……62
Figura 4. Histologia do tecido adiposo epididimal de ratos alimentados com a) AIN93,
dieta controle; b) HFD, dieta hiperlipídica; c) HFD-TT; dieta hiperlipídica suplementada
com chá. Medições do d) tamanho do adipócito, e) diâmetro equivalente, f) número de
adipócitos...63
LISTA DE TABELAS
CAPITULO 1. REVISÃO BIBLIOGRÁFICA
Tabela 1. Critérios para diagnóstico da síndrome metabólica em adultos...4
Tabela 2. Biomarcadores associados à síndrome metabólica...7
Tabela 3. Genes envolvidos em mecanismos da inflamação e do estresse oxidativo....14
Tabela 4. Principais Compostos Bioativos da Mangifera indica L...16
CAPITULO 2. AVALIAÇÃO DA EFICÁCIA DE EXTRAÇÃO DE MANGIFERINA
E ANÁLISES QUÍMICA, ANTIOXIDANTE E SENSORIAL DE CHÁ COM FOLHAS
DE Mangifera indica L., VARIEDADE UBÁ.
Tabela 1. Condições de preparo dos chás com folhas de M. indica...36
Tabela 2. Conteúdo de mangiferina nos chás de folhas de M. indica preparados por três
técnicas, usando dois tipos de folha e três relações da droga vegetal/ solvente...40
Tabela 3. Valores médios de pH, conteúdo de fenólicos totais e atividade antioxidante do
chá de folhas de M. indica ao 5% (relação da droga vegetal / solvente)...42
Tabela 4. Valores médios das pontuações da escala hedônica, dos diferentes chás de
folhas de M. indica...45
CAPITULO 3. EFEITO ANTI-OBESIDADE DO CHÁ DE FOLHAS DE Mangifera
indica L. var. UBÁ EM RATOS ALIMENTADOS COM DIETA HIPERLIPÍDICA.
Tabela 2. Influência do chá de folhas M. indica no consumo de dieta, energia consumida,
ganho de peso, peso dos órgãos e nos parâmetros biométricos. ...58
Tabela 3. Efeito do chá de folhas de M. indica nos parâmetros bioquímicos em ratos
alimentados com dieta hiperlipídica, após 8 semanas de tratamento s...59
Tabela 4. Efeito do chá de folhas de M. indica sobre o parâmetros morfométricos do
fígado de ratos Wistar machos adultos alimentados com dieta hiperlipídica, após 8
LISTA DE ABREVIATURA E SIGLAS
AA Atividade antioxidante
AAR Atividade de retirada de radical
AGL Ácidos graxos livres
AGS Ácidos graxos saturados
AP-1 Proteína ativadora 1
AQP Aquaporina
ALT Alanina aminotransferase
AST Aspartato aminotransferase
AUR Ácido úrico
CAT Capacidade antioxidante total
CBA Composto bioativo
Cd Cluster de diferenciação
CLAE Cromatografia líquida de alta eficiência
CRE Creatinina
CT Colesterol total
DP Desvio padrão
EAQ Equivalentes de ácido gálico
EP Erro padrão
EO Estresse oxidativo
ERO Espécies reativas de oxigênio
DPPH 2,2-difenil-1-picrilhidrazil
FABP Proteína de ligação de ácidos graxos
FAS Ácido graxo sintase
FAT Transportador de ácidos graxos
FFA Ácidos graxos livres
FT Fenólicos totais
GAPDH Gliceraldeído-3-fosfato-desidrogenase
GLU Glicose
GLUT 4 Transportador 4 de glicose
HDL Lipoproteína de alta densidade
HGF-1 Fator de crescimento do hepatócito
IMC Índice de massa corporal
IL-1,6,10 Interleucinas 1,6 e 10
IRF-3 Fator regulatório do interferon tipo 3
IRS Substrato do receptor de insulina
JNK Quinasses c-Jun N-terminal
LDL Lipoproteína de baixa densidade
LHS Lípase hormônio sensível
LIF Fator inibidor de leucemia
LP Leptina
LPL Lipoproteína lipase
MCP1 Proteína quimiostática de monócitos
MIMF Fator inibitório da migração de macrófagos
PAI1 Inibidor ativador plasminógeno
NF-ĸB Fator nuclear kappa B
NPY Neuropeptídeo Y
PC Perímetro de cintura
PCR Proteína C reativa
PPAR-γ Receptor ativado do peroxissoma gama
QM Quilomicrons
RI Resistência insulínica
SAA3 Polipoproteína A3
SM Síndrome metabólica
SRT Sirtuina
TAK 1 Quinasse ativada 1
TG Triacilgliceróis
TLR Receptores tipo Toll
TNF-α Fator alfa de necrose tumoral
TTOG Teste de tolerancia oral à glicose
UCP Proteína de desacople mitocondrial
UNIDADES
pg - µg - mg - g - Kg Picogramas – Microgramas – Miligramas – Gramas – Quilogramas
µm – mm – cm Micrometros – Milímetros – Centímetros
mmol Milimol
RESUMO
MEDINA RAMÍREZ, Natalia, M.Sc, Universidade Federal de Viçosa, fevereiro de 2015.
Modulação dos fatores de risco metabólico associados à obesidade, por chá de folhas de mangueira (Mangifera indica L. variedade ubá), em ratos alimentados com dieta hiperlipídica. Orientadora: Sônia Machado Rocha Ribeiro. Coorientadores: Hércia
Stampini Duarte Martino e José Humberto de Queiroz.
A obesidade é uma alteração metabólica caraterizada pelo acúmulo de gordura corporal,
sendo causada por fatores genéticos e ambientais (comportamento alimentar inadequado,
sedentarismo). Está associada aos processos de inflamação, estresse oxidativo, doenças
cardiovasculares, diabetes tipo 2, hipertensão arterial e dislipidemia. O presente estudo
teve como objetivo desenvolver um chá de folhas de Mangifera indica L. da variedade
Ubá, e avaliar seus efeitos na modulação de fatores de risco associados à obesidade, em
ratos alimentados com dieta hiperlipídica. Este trabalho foi realizado nos Laboratórios de
Nutrição Experimental, Desenvolvimento de Novos Produtos, Biodiversidade e
Metabolismo e Fermentação da Universidade Federal de Viçosa, Minas Gerais (Brasil).
Foram preparados chás com folhas jovens e maduras da M. indica, processadas (secas e
trituradas) em concentrações de 1,25; 2,5 e 5% (g.mL-1) utilizando as técnicas de infusão,
decocção e ultrassom. Foi determinada a concentração de mangiferina (por CLAE),
sendo selecionado o chá com maior eficácia na obtenção desta xantona para o estudo de
efeitos biológicos. O chá com teor elevado de mangiferina foi caracterizado
determinando-se pH, fenólicos totais (utilizando o reagente de Folin-Ciocalteau) e
atividade antioxidante (teste de retirada do radical DPPH). Também foi analisada a
estabilidade oxidativa do chá por meio da quantificação de mangiferina, fenólicos totais
e atividade antioxidante, utilizando dois tratamentos de conservação (refrigeração 4 ± 2°C
e temperatura ambiente 20 ± 2°C) nos tempos 0, 24 e 48 horas. Finalmente, uma análise
sensorial foi realizada para avaliar a aceitação do chá pelos consumidores. Para o ensaio
biológico, ratos machos Wistar adultos foram alimentados com dieta hiperlipídica (n=16)
durante sete semanas para induzir a obesidade. Finalizado este período, os ratos foram
divididos considerando a homogeneidade dos fatores de risco metabólico (peso corporal,
glicemia de jejum e Índice Lee) em dois grupos (n=8): dieta hiperlipídica (HFD) e dieta
Foram avaliados parâmetros biométricos, bioquímicos e histomorfométricos. Além disso,
foi realizado o teste de tolerância à glicose, controle de consumo de dieta e do chá, e foi
determinado o nível de expressão de PPAR-γ, FAS e LPL no tecido adiposo epididimal.
Os resultados foram analisados por meio de análise de variância (ANOVA) seguida dos
testes Tukey ou Dunnett (paramétricos) e Dunn’s (não paramétricos). Os dados foram
expressos como média ± desvio padrão ou média ± erro padrão. O nível de significância
utilizado em todas as análises foi P<0,05. Houve diferenças significantes na concentração
de mangiferina entre os tipos de folha para as três concentrações nas três técnicas
(P<0,05). O chá preparado por decocção utilizando folhas novas na concentração 5%
(m/v), apresentou o maior valor de mangiferina (0,72 ± 0,08 mg.mL-1). O chá apresentou
estabilidade durante 48 horas após seu preparo em ambos os tratamentos avaliados e
houve aceitação da bebida pelo consumidor. Alterações como tecido adiposo total
aumentado, adipócitos com maior tamanho e acúmulo de lipídeos no tecido hepático,
foram observadas nos animais alimentados com a dieta hiperlipídica. Foi observado que
a dieta hiperlipídica, elevou os níveis da citocina pro-inflamatória TNF-α e reduziu a
expressão de PPAR-γ. O chá teve efeitos anti-inflamatórios por meio da elevação dos
níveis da citocina IL-10 e expressão de mRNA de LPL e PPAR-γ. Análises
histomorfométricas evidenciaram os efeitos modulatórios do chá na redução do acúmulo
de lipídeos e gotículas de gordura no tecido hepático e epididimal. Concluiu-se que o chá
de folhas de M. indica é viável para ser consumido como bebida fonte de compostos
bioativos, tendo efeitos anti-obesidade por meio da regulação da expressão de genes que
ABSTRACT
MEDINA RAMÍREZ, Natalia, M.Sc, Universidade Federal de Viçosa, February of 2015.
Modulation of metabolic risk associated to obesity, by Mangifera indica L. leaves tea in rats fed by high fat diet. Adviser: Sônia Machado Rocha Ribeiro. Co-advisers: Hércia
Stampini Duarte Martino and José Humberto de Queiroz.
Obesity is a metabolic disorder characterized by the body fat accumulation, caused by
genetic and environmental factors (inadequate eating habits, sedentary lifestyle, and
smoking). It is associated with inflammatory processes, oxidative stress, cardiovascular
diseases, type II diabetes, hypertension and dyslipidemia. This study aimed to develop a
Mangifera indica L. leaves tea, Ubá variety and the effects in the modulation of risk
factors associated with obesity in rats fed by high-fat diet. This work was performed at
the Experimental Nutrition and New Product Development Laboratories, Federal
University of Viçosa, Minas Gerais (Brazil). Teas were prepared from young and mature
leaves of Mangifera indica L., processed (crushed and dried) at the concentrations of 1.25,
2.5 and 5% (g.mL-1) using infusion, decoction and ultrasound techniques. It was
determined the concentration of mangiferin by HPLC, being selected the tea with greater
efficiency in obtaining this xanthone for the biological effects study. Tea with high
mangiferin content was characterized determining pH, density, total phenolics (using the
Folin-Ciocalteau) and antioxidant activity (DPPH test). The oxidative stability of tea was
analyzed by quantification of mangiferin, total phenolics and antioxidant activity, using
two preservation treatments (cooling 4 ± 2 ° C and room temperature 20 ± 2 ° C) at the
times 0, 24 and 48 hours. Sensorial analysis was performed to evaluate the acceptance of
tea by consumers. For the assay, Wistar adult male rats were fed by high fat diet for seven
weeks to induce obesity. After, they were divided, considering the homogeneity of
metabolic risk factors (body weight, fasting glucose and Lee Index), in two groups (n =
8): fat diet (HFD) and high-fat diet supplemented with 50 ml of tea, replacing the water
(HFD-TT). A control group (n = 8) received the AIN-93 diet M. The experiment lasted 8
weeks. We evaluated biometric, biochemical and morphometric variables. In addition, it
was tested the glucose tolerance, control of food intake and energy, and it was determined
the level of gene expression in epididymis adipose tissue. The results were analyzed by
standard error. The significance level for all analyses was P<0.05. There were significant
differences in mangiferin concentration between the types of sheet for the three
techniques in three concentrations (P <0.05). The tea decoction prepared by using new
leaves in the concentration 5% (w / v), had the highest value of mangiferin (0.72 ± 0.08
mg.mL-1). The tea was stable for 48 hours after its preparation in both treatments and was
well accepted by the consumer. Changes such as increased overall adipose tissue,
adipocytes with larger size and lipid accumulation in the liver tissue were attributed to
high-fat diet. In addition it was observed that the high fat diet, raised levels of
pro-inflammatory cytokine TNF-α and reduce the PPAR-γ expression. The tea demostrated
anti-inflammatory effects by elevating the cytokine IL-10 levels and LPL and PPAR-γ
mRNA expression. Histomorphometric analyzes showed the modulatory effects of tea on
reducing the lipids accumulation and fat droplets in liver and epididymal tissue. It is
concluded that the M. indica leaves tea is feasible to be consumed as a beverage source
of bioactive compounds having anti-obesity effects through the genes expression
INTRODUÇÃO GERAL
A Síndrome Metabólica (SM) engloba uma série de alterações metabólicas
desencadeadas pelo estresse oxidativo, inflamação e excesso de adiposidade corporal,
sendo que estas constituem alvos de ações terapêuticas no controle da síndrome
(DEVALARAJA et al., 2011). A SM também pode ser precursora no desenvolvimento
de doenças cardiovasculares, diabetes mellitus tipo 2, hipertensão e dislipidemia, uma vez
que a resistência insulínica parece ser um mecanismo que sustenta a fisiopatologia de tais
enfermidades (SIRDAH et al., 2012). O estresse oxidativo e a inflamação são dois
importantes mecanismos envolvidos nas alterações metabólicas da obesidade,
relacionadas com as doenças cardiovasculares e o diabetes (OTANI, 2011).
A manga (Mangifera indica L.) é uma das frutas comestíveis mais conhecidas e
cultivadas no mundo. Na atualidade ocupa o quarto lugar na produção mundial de frutas
sendo cultivada em mais de 100 países tanto tropicais como subtropicais (FAOSTAT,
2011). Dentre as variedades cita-se a manga Ubá, presente na zona da Mata Mineira, no
estado de Minas Gerais (Brasil). Esta variedade de manga, possui excelentes qualidades
de sabor e aroma, sendo aceita pelo consumidor para consumo in natura, e também muito
utilizada na agroindústria, principalmente na fabricação de sucos. A manga Ubá é
reconhecida por seu teor de compostos bioativos, com grande potencial funcional
(BENEVIDES et al., 2008). Estudos com mangas identificaram diversos compostos,
incluindo flavonoides, xantonas (mangiferina), galotaninos e benzofenonas (DORTA et
al., 2014). Yakubu et al. (2015), reportaram que o extrato aquoso de folhas de M. indica
apresentou atividade antidiarreica em ratos. Por outro lado, Brito (2013) avaliou o efeito
de um extrato etanólico com folhas de M. indica na modulação da expressão dos
receptores CB1, PPARγ e adipocinas em ratos alimentados com dieta de cafeteria, encontrando efeitos benéficos auxiliando o tratamento dos fatores de risco da síndrome
metabólica, como é a obesidade.
A mangiferina pertence ao grupo das xantonas sendo, um composto fenólico
característico da família Anacardiaceae. Estudos evidenciaram as atividades
farmacológicas desta xantona, incluindo as anti-inflamatórias, antioxidantes,
antidiabetes, imunomodulatórias e antitumorais (DUANGA et al., 2011).
parâmetros de risco metabólico na obesidade e diminuindo a ingestão alimentar (ALVES
N.G et al., 2012).
A compreensão sobre os efeitos de compostos bioativos em alvos moleculares no
tecido adiposo humano para uso terapêutico na obesidade é ainda difícil, devido às
limitações para realização de estudos in vivo. O uso de ratos alimentados com dieta de
cafeteria foi apontado como um modelo adequado para estudar a síndrome metabólica
humana, pois há presença de inflamação no tecido adiposo e alterações hepáticas que
simulam a esteatose presente na obesidade humana (SAMPEY et al., 2011). Na atualidade
tem sido estudado o efeito de chás na obesidade induzida com dieta hiperlipídica
denominada HFD (High Fat Diet) em ratos. Foram demonstradas atividades inibitórias,
supressoras e anti-inflamatórias de alguns compostos bioativos de chás Goishi, Verde e
Preto (LI SHEN et al., 2012; JOBU et al., 2013; YAJIMA, 2014). O potencial de
compostos bioativos para modular a expressão gênica na síndrome metabólica tem sido
investigado por meio de modelos animais. A obesidade induzida em ratos por dieta
hiperlipídica (HFD) e dieta de cafeteria é considerada um modelo robusto para estudar a
síndrome metabólica (IDF, 2005).
O excesso de adiposidade corporal é um dos componentes da síndrome metabólica, a
qual apresenta crescente prevalência na população atual. O interesse em buscar estratégias
terapêuticas para o controle desta doença é devido aos seus efeitos negativos sobre a
saúde, qualidade de vida e custo do tratamento de suas comorbidades. Dentro deste
contexto, existe um grande interesse nos alimentos com propriedades funcionais, ricos
em compostos fenólicos e com potencial antioxidante. Dentre eles, destacam-se as
bebidas naturais, incluindo sucos e infusões contendo frutas e variedade de plantas, as
quais podem ser utilizadas como fonte de fitoquímicos antioxidantes e anti-inflamatórios,
que possam ser coadjuvantes no controle do risco metabólico da obesidade.
A ideia de buscar um produto alimentício que possa ser utilizado como coadjuvante
no tratamento da obesidade, surge da necessidade de controlar as alterações metabólicas
presentes nestes indivíduos, os quais muitas vezes dificultam tanto a redução de peso
corporal, quanto o controle do risco de comorbidades. Estudar uma bebida feita com as
folhas da mangueira (M. indica, variedade Ubá), é uma alternativa tanto para conhecer
seu potencial funcional e para modular os fatores de risco da síndrome metabólica, como
para propor inovações no setor da agroindústria de bebidas naturais no Brasil e agregar
CAPITULO 1
REVISÃO BIBLIOGRÁFICA
1. Síndrome metabólica: mecanismos e alterações
A síndrome metabólica (SM) foi aventada na década de 80, apontando a associação
de fatores de risco metabólico presentes na obesidade com as doenças cardiovasculares.
Atualmente, denomina-se síndrome metabólica a um conjunto de fatores presentes na
obesidade e que aumentam o risco de desenvolver doenças cardiovasculares ou diabetes
tipo 2 (GRUNDY et al., 2004).
Não há um critério unânime acerca da definição da SM, a qual inclui um conjunto de
alterações metabólicas, constituídas por vários componentes: obesidade abdominal,
dislipidemia aterogênica, elevação de pressão arterial, resistência insulínica e intolerância
à glicose, estados pro-inflamatório e protrombótico (SIRDAH et al., 2012; BREMER;
JIALAL, 2013). A SM e a obesidade são entidades clínicas complexas e heterogêneas,
associadas ao componente genético, cuja expressão é influenciada pelos fatores
ambientais, sociais, culturais, econômicos e outros (GARCIA et al., 2008). Fatores
genéticos (genes reguladores de lipólise, termogênese, metabolismo da glicose) e
ambientais (sedentarismo, obesidade central e abdominal, dieta rica em gorduras e
carboidratos) são os principais fatores associados à presença da SM, sendo responsáveis
pelo aumento da sua prevalência na população atual (ALBORNOZ; PÉREZ, 2012).
Ainda não há consenso quanto aos critérios para definir ou identificar clinicamente a
SM, embora haja concordância quanto aos seus componentes, mas há diferenças na
proposição dos valores de pontos de corte para alguns parâmetros. A Associação
Americana de Saúde propôs no ATP III (Adult Treatment Panel III) que se pelo menos
três dos cinco componentes associados à SM estiverem presentes, seu diagnóstico poderia
ser estabelecido (AMERICAN DIABETES ASSOCIATION, 2014). A Tabela 1
apresenta os critérios para diagnóstico clínico da SM em adultos, segundo três organismos
Tabela 1
Critérios para diagnóstico da síndrome metabólica em adultos.
ENTIDADE PARÂMETROS Obesidade Abdominal Triacilgliceróis (mg/dL) Pressão arterial (mmHg)
Glicose de jejum
(mg/dL) HDL (mg/dL)
Associação Americana de Saúde (ADA, 2014)
PC:
Homens: >102 Mulheres: >88
Homens: ≥150 Mulheres: ≥150
Homens: ≥130/ ≥85 Mulheres: ≥130/ ≥85
Homens: ≥100 Mulheres: ≥100
Homens: <40 Mulheres: <50 Organização Mundial
de Saúde (WHO, 1998)
IMC > 30,0 Adultos: >150 Adultos: ≥ 140/90 Adultos: ≥100 Homens: <35 Mulheres: <40 Federação internacional de diabetes (IDF, 2005) PC: Homens: ≥ 94 Mulheres: ≥ 84
≥ 150
[1.7 mmol/L] Adultos: ≥130/ ≥85
≥ 100 [5.6 mmol/L]
PC: Perímetro de cintura (cm); IMC: índice de massa corporal (kg/m2); HDL: lipoproteína de alta
densidade.
1.1.Componentes da SM
1.1.1. Obesidade abdominal
Há evidências de que a deposição da gordura na região abdominal, referida como
visceral, epididimal, omental ou intra-abdominal, é um fator mais importante na
associação entre obesidade e síndrome metabólica do que o excesso de gordura corporal
isoladamente, medido como índice de massa corporal (VAZQUEZ et al., 2007;
FABBRINI et al., 2010; KAWAI; ROSEN, 2010; DESPRÉS, 2012;
GUEBRE-EGZIABHER, 2013; TCHERNOF; DESPRÉS et al., 2013). A Organização Mundial de
Saúde (2015) estabeleceu que um indivíduo apresenta obesidade se tiver o índice de
massa corporal superior a 30.
O aumento da adiposidade abdominal está associada também ao aumento das
citocinas pro-inflamatórias (REYES, 2010) tais como fator alfa de necrose tumoral (TNF- α), interleucina 6 (IL-6) e proteína quimiostática de monócitos (MCP-1), levando a um
estado de inflamação de baixo grau (KONRAD, 2012; TCHERNOF; DESPRÉS et al.,
2013).
1.1.2. Dislipidemia aterogênica
A dislipidemia associada com o risco cardiometabólico é caracterizada por
1.1.3. Elevada pressão arterial
Por causa de sua associação com a obesidade, a hipertensão foi incluída na lista
de componentes da SM, embora alguns investigadores acreditem que a mesma apresenta
menos envolvimento com os mecanismos de risco metabólico, em comparação com os
demais componentes. A elevação de níveis pressóricos ocorre comumente em indivíduos
portadores de resistência insulínica, condição na qual há elevação da concentração de
ácidos graxos livres (AGL) no plasma, com a presença de esteatose hepática e
dislipidemia aterogênica (GRUNDY, 2004).
1.1.4. Resistência insulínica
Resistência insulínica (RI) é uma condição em que existe uma captação
inadequada da glicose dependente da insulina, sendo que o pâncreas continua produzindo
a insulina, mas a sua ação está prejudicada e a concentração de glicose no sangue
permanece elevada, caracterizando a intolerância à glicose, o que favorece o
desenvolvimento de doenças tais como as cardiovasculares e o diabetes
(BLOOMGARDEN, 2005).
A concentração de insulina no sangue é resultante do equilíbrio entre a sua
produção pelo pâncreas e a sua captação ou degradação pelo fígado e outros tecidos,
incluindo o renal e os periféricos (músculo e tecido adiposo) (HOME, 2008; ARDER et
al., 2013)
O aumento de AGL no sangue inibe a captação da insulina e altera os dois
mecanismos anteriores que controlam sua concentração no sangue. Um estado
hiperinsulinêmico causa diminuição dos receptores de insulina por meio de regulação
gênica, o que contribui para a diminuição da remoção de insulina do meio circulante e
manutenção do estado hiperinsulinêmico (STEARS, 2012).
1.2.Patogênese e mecanismos fisiopatológicos da síndrome metabólica
Na síndrome metabólica há a interação multifatorial que envolve principalmente
alterações do metabolismo dos adipócitos, resistência insulínica e vários outros fatores
tais como disfunção hepática, vascular e imunológica, os quais são mediadores do
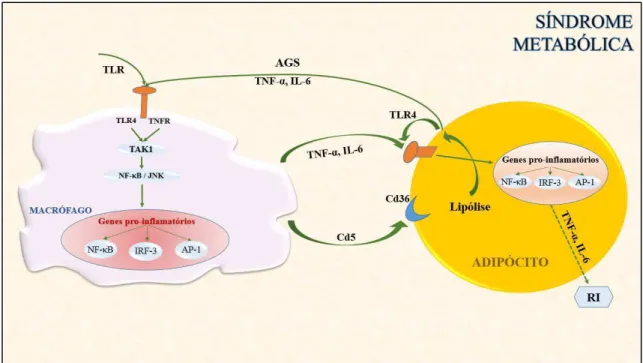
Figura 1. Interações de componentes moleculares e o tecido adiposo na síndrome
metabólica.
Abreviações: AGS: ácidos graxos saturados; AP-1: proteína ativadora 1; Cd: cluster de diferenciação;
IL-6: interleucina 6; IRF-3:Fator regulatório do interferon tipo 3; JNK: Quinasses c-Jun N-terminal; NF-κβ:
fator nuclear kappa B; TAK1: Quinasse ativada 1; TNF-α: fator alfa de necrose tumoral; TLR: receptores
tipo Toll.
Fonte: Adaptado (Nature Medicine, 2013).
Ácidos graxos saturados da dieta (AGS) ativam os receptores de tipo Toll (Toll like
receptor TLR 2/4) nos macrófagos do tecido adiposo, levando a uma ativação da cascata
dos sinalizadores inflamatórios IRF-3/AP-1/NF-κβ. Isto induz a produção de citocinas inflamatórias tais como IL-1β e TNF-α que inibem a ação da insulina nos adipócitos. Os macrófagos liberam Cd5 induzindo à expressão de quimiocinas numa forma dependente
de TLR4, favorecendo a formação de monócitos inflamatórios e macrófagos do tecido
adiposo. A inflamação de baixo grau ou subclínica se estabelece no tecido adiposo e em
nível sistêmico afetando outros órgãos como o fígado e músculo, produzindo a resistência
insulínica (RI).
Com a RI são desencadeados problemas cardiovasculares, diabetes, arteriosclerose, e
outras (NATURE MEDICINE, 2013). Alguns biomarcadores envolvidos na homeostase
energética, inflamação e resistência insulínica na síndrome metabólica são descritos na
Tabela 2 e os mecanismos de interação dos mesmos com a síndrome metabólica são
Tabela 2
Biomarcadores associados à síndrome metabólica.
Marcador Efeitos e mecanismos de ação
Adiponectina
Proteína com efeito antiaterogênico. À medida que aumenta a obesidade os
níveis de adiponectina no plasma diminuem e aumenta a resistência insulínica.
Melhora a sensibilidade à insulina, efeito anti-inflamatório e antiapoptótico.
Portanto, melhora a resistência insulínica e a tolerância à glicose.
Resistina Proteína especifica do adipócito associada à resistência insulínica. Pode contribuir para a inflamação sistemática.
Interleucina 6 (IL-6)
Citocina pro-inflamatória e diminui a sensibilidade insulínica. Contribui para o
aumento do colágeno na parede celular e aumenta a síntese de fibrinogênio,
favorecendo a hipertensão. Participa da lipólise de triacilgliceróis aumentando a
liberação de AGL, que está fortemente relacionado à resistência insulínica.
Leptina (LP)
Efeito anorexigênico, com efeito na diminuição do apetite. Favorece ativação do
sistema nervoso simpático que leva à retenção de sódio, vasoconstrição elevando
a pressão arterial.
Fator alfa de
necrose tumoral
(TNF-α)
Citocina pro-inflamatória. Favorece a resistência insulínica ao alterar a
capacidade de fosforização de resíduos de tirosina no receptor (IRS-1),
necessário para a produção do sinal intracelular do hormônio.
Receptor ativado do
peroxissoma
(PPARγ)
Induz a diferenciação de adipócitos e acúmulo de lipídios mediante a regulação
de genes da adipogênese e a absorção e metabolismo de lipídios. Diminui a
lipólise e regula a expressão de proteínas relacionadas à resistência insulínica.
Favorece a termogênese estabilizando o sistema nervoso simpático.
Sirtuina (SRT)
Aumenta a biogênese mitocondrial, o metabolismo no músculo e a
gliconeogênese no fígado. Atua em conjunto com o outros genes, favorecendo a
secreção de insulina e melhoram o metabolismo.
Proteína C reativa Proteína de fase aguda, sintetizada pelo fígado e participa da cascata de inflamação. Favorece os eventos agudos coronários.
Fonte (MORENO, 1997; NATALI; FERRANNINI, 2005; PEREZ; MEDINA, 2011; ZAFRIRA et al.,
2013)
síndrome metabólica, desencadeando várias alterações no metabolismo, o que leva ao
rompimento da homeostase metabólica. A elevação crônica dos ácidos graxos livres
(AGL) circulantes causa a lipotoxicidade e a glicotoxicidade e favorecendo o aumento
das citocinas inflamatórias (TNF-α e IL-6) com a diminuição da adiponectina,
Figura 2 - Biomarcadores e mecanismos fisiopatológicos na síndrome metabólica. Abreviações: AGL: ácidos graxos livres; HDL: lipoproteína de alta densidade; IL-6: interleucina 6; LPL:
lipase lipoproteica; PCR: proteína C reativa; TNF-α: fator alfa de necrose tumoral.
Fonte: Adaptado (LÓPEZ et al., 2004; RENDON; LURBE, 2007; BASTIDAS et al.,2011)
1.3.Metabolismo dos adipócitos na síndrome metabólica
O adipócito tem como função principal o armazenamento de lipídios, como reserva
energética, especificamente triacilgliceróis e colesterol esterificado. Entretanto, participa
da regulação do equilíbrio energético do organismo, por meio da secreção de peptídeos
ou hormônios com ação endócrina, e autócrina. Existem dos tipos de adipócitos, o branco
e o marrom. O primeiro é especializado em armazenar lipídios como reserva energética a
longo prazo e se caracteriza por ter uma vesícula única de gordura, ocupando todo o
volume celular e deixando o citosol, organelas e o núcleo numa pequena área periférica.
O segundo, tem menor quantidade de gordura armazenada em maior número de vesículas
de menor tamanho, apresentando maior quantidade de mitocôndrias; sua função principal
é gerar calor e regular a homeostase energética do organismo (TARIQ et al., 2013).
Os adipócitos interagem com outros tecidos metabolicamente ativos por meio da
liberação de fatores de secreção (adipocinas) que são expressas em níveis baixos nos
adipócitos saudáveis. Estes fatores regulam respostas metabólicas relacionadas ao
e o músculo (melhoram a sensibilidade à insulina), células do pâncreas e miócitos
(garantem sobrevivência e função) e o epitélio (NATURE MEDICINE, 2013).
A homeostase dos adipócitos é mantida por vias metabólicas: lipólise e lipogênese. A
lipólise é a via de mobilização do lipídio por meio da hidrólise das ligações ésteres nos
triacilgliceróis (TG), resultando na formação de ácidos graxos livres (AGL) e glicerol. É
uma via metabólica estimulada por diferentes hormônios catabólicos como, glucagon,
epinefrina, norepinefrina, hormônio do crescimento e cortisol, por meio de um sistema de
tradução de sinais. A lipólise desempenha um papel fundamental na obtenção de energia
e na oxidação de triacilgliceróis e ocorre mediante a ativação da enzima lipase hormônio
sensível (LHS), pela adrenalina. Os produtos da lipólise, ácidos graxos e glicerol, são
liberados na circulação sanguínea para serem utilizados por outros tecidos; os ácidos
graxos são oxidados liberando energia e o glicerol é conduzido ao fígado para participar
na síntese de glicose (VERNON, 1992; FRÜHBECK et al., 2014; SCHWEIGER et al.,
2014).
A lipogênese é uma reação bioquímica na qual os carboidratos e proteínas em excesso,
são convertidos em ácidos graxos e esterificados para formar triacilgliceróis e gordura de
reserva. Este processo ocorre principalmente no período pós-prandial e sua função
principal é armazenar o excesso de energia consumido. O principal órgão lipogênico é o
fígado e a principal enzima envolvida na lipogênese é a acetil CoA carboxilase. A
lipogênese ocorre no citoplasma das células e necessita de um excesso de carboidratos
para ocorrer (SCHUTZ, 2004; LAFONTAN, 2014). Estes dois processos constituem vias
metabólicas diferenciadas porque a lipogênese está relacionada com a síntese de
triacilgliceróis e a lipólise com o catabolismo dos triacilgliceróis. Basicamente, a
lipogênese favorece um aumento do tecido adiposo e a lipólise o reduz (Figura 3). Na
lipogênese, a insulina se une ao seu receptor situado na superfície dos adipócitos e
estimula o deslocamento de GLUT4 para a membrana celular, possibilitando a captação
de glicose pela célula. A glicose intracelular é convertida em glicerol-3-fosfato. A
insulina ativa a LPL situada na superfície do endotélio vascular, liberando os ácidos
graxos, a partir dos quilomicrons e VLDL. Os ácidos graxos são transferidos aos
adipócitos por meio de transportadores de ácidos graxos (FAT), proteína transportadora
de ácidos graxos (FATP) e proteína de ligação de ácidos graxos (FABP). Finalmente os
Figura 3. Regulação da lipólise e lipogênese nos adipócitos.
Abreviações: AQP7: aquaporina 7; FABP: proteína de ligação de ácidos graxos; FFA: ácidos graxos livres;
FAT: transportador de ácidos graxos; FATP: proteína transportadora de ácidos graxos; Glicerol-3-P:
glicerol-3-fosfato; GLUT4: transportador 4 de glicose; LHS: lípase hormônio sensível; LPL: lipase
lipoproteica; QM: quilomicrons; TG: triacilgliceróis; VLDL: Lipoproteínas de muito baixa densidade.
Fonte: Adaptado (MAEDA et al., 2008).
(LHS) para as partículas de lipídios, e os estímulos relacionados a este evento conduzem
a inserção da aquaporina (AQP7) na membrana celular. Os níveis de mRNA de AQP7 se
elevam em resposta à diminuição da atividade da cascada de sinalização da insulina. Estas
duas vias de regulação diferentes asseguram a liberação eficiente de glicerol dos
adipócitos, em condições de jejum (MAEDA et al., 2008).
1.4.Hiperplasia e Hipertrofia do tecido adiposo
O desequilíbrio crônico entre o alto consumo e baixo gasto energético pelo organismo
dos mamíferos causa uma alteração no armazenamento de energia na forma de depósitos
intracelulares de triacilgliceróis nos adipócitos. O incremento da gordura corporal é
manifestado pelo acúmulo de lipídios intracelulares no adipócito, aumentando seu
tamanho; este fenômeno é conhecido como hipertrofia e causa uma diminuição de
adiponectina e um aumento de adipocinas inflamatórias, com redução no fluxo sanguíneo,
Na Hiperplasia, o acúmulo de lipídios intracelulares no tecido adiposo ocorre em duas
etapas: um aumento do número de preadipócitos e a diferenciação deste em adipócitos
maduros (por meio da secreção de adiponectina), levando ao aumento do número de
adipócitos. Ao contrário da hipertrofia, na hiperplasia há aumento de adiponectina e
redução de adipocinas inflamatórias (Figura 4) (FERRANTI; MOZAFFARIAN, 2009;
FLORES et al., 2011).
Um estudo mostrou que adipócitos hipertróficos e hiperplásicos apresentam uma
menor densidade dos receptores de insulina e maior número de receptores adrenérgico
3β, o que facilita a infiltração dos monócitos no estroma adiposo, iniciando o processo
inflamatório entre os adipócitos (DENG; SCHERER, 2010). Outros estudos sugerem que
os fatores TNF-α, HGF-1 e PPAR-γ, estimulam a hiperplasia, já que têm efeitos na
transcrição de genes de proteínas envolvidas neste mecanismo (AVRAM et al., 2007;
BAHCECI et al., 2007).
1.5.Mecanismos de inflamação e de estresse oxidativo
1.5.1. Inflamação
A inflamação é um processo que ocorre em resposta a uma elevada secreção de
citocinas e substâncias inflamatórias. Inicia-se com o reconhecimento dos sinais, que
podem ser de origem infecciosos ou inflamatórios, ocasionando a ativação celular e
adipocinas e são desencadeados vários processos fisiopatológicos relacionados com a
inflamação. Neste processo ocorre um aumento de adipocinas, quimiocinas e outros.
Vários fatores reguladores da inflamação expressos nos adipócitos são TNF-α, IL-6,
inibidor ativador plasminógeno (PAI-1), proteína quimioatática de monócitos-1 (MCP1),
IL-1β, IL-8, 10, 15, fator inibidor de leucemia (LIF), fator de crescimento do hepatócito (HGF), a polipoproteína A3 (SAA3), fator inibitório da migração de macrófagos (MIMF),
moduladores inflamatórios como leptina, adiponectina e resistina, assim como a proteína
C reativa (HOTAMISLIGIL et al., 1995; BLANCAS et al., 2010).
Um estudo realizado em adolescentes com obesidade central, mostrou que este tipo
de obesidade, reduz o nível de adiponectina no plasma por meio do aumento de adipocinas
pro-inflamatórias como o TNF-α, IL- 1β e leptina, sugerindo a existência do equilíbrio entre a adiponectina e a leptina para controlar os processos inflamatórios
(EL-WAKKADA et al., 2013). Estudos demonstraram que a leptina, IL-6 e TNF-α, aumentam
na obesidade e os efeitos inflamatórios alteram a sinalização celular (STELZERA et al.,
2012; ARNOLDUSSEN et al., 2014). Outros estudos sugerem que a sirtuina e a
adiponectina têm efeito anti-inflamatório, antioxidante e regulam a secreção de citocinas
pro-inflamatórias (FANTUZZI, 2008; FERNANDES et al., 2012; CHENG et al., 2014).
1.5.2. Estresse oxidativo (EO)
O estresse oxidativo é um estado da célula no qual a homeostase de óxido-redução
intracelular (equilíbrio entre pro-oxidantes e antioxidantes) se encontra alterada em favor
do estado oxidante. Este desequilíbrio ocorre quando há uma excessiva produção de
espécies reativas de oxigênio (ERO) e/ou deficiência nos mecanismos antioxidantes,
conduzindo ao dano celular. O estresse oxidativo está presente em processos patológicos
como a obesidade, diabetes, doença cardiovascular, dislipidemia, câncer e processos
aterogênicos (MATSUDA; SHIMOMURA, 2013). Está caracterizado pela grande
diminuição da capacidade redutora dos pares redox como a glutationa, podendo causar
morte celular e uma oxidação moderada (apoptose) ou intensa (necrose). Há
comprovações de que o promotor da hemoxigenase (HO-1) tem pontos de união aos
fatores de transcrição AP-1, AP-2 e NF-kB que também são ativados pelo EO, resultando
na síntese de várias proteínas conhecidas como enzimas de resposta ao estresse. É
importante considerar a participação de enzimas como defesas antioxidantes na regulação
tiorredoxinas, peroxirredoxinas, quinonas, redutase e oxigenase podem prevenir o
estresse oxidativo (RÍOS, 2003; FERNANDÉZ et al., 2011).
Há evidências que o estresse oxidativo está presente nos seguintes mecanismos
celulares: disfunção mitocondrial, alterações em proteínas críticas para manter a
homeostase e a função muscular, retículo endoplasmático, apoptose celular, senescência
celular e sinalização celular anormal (WU et al., 2014).
Fatores dietéticos alteram o equilíbrio entre lipogênese e lipólise, influenciam o
estado inflamatório e interferem na homeostase redox do organismo. Um estudo
demonstrou que uma dieta alta em gorduras afeta a tolerância à glicose, a sinalização da
insulina hepática, atividade de transcrição e tradução que favorecem a lipogênese, a
produção de citocinas, a sinalização pro-inflamatória e o estresse oxidativo, por meio da
ação de TNF-α, SRT-1, NF-ĸβ, proteína kinase e outros (PENG et al., 2012). Outros estudos apresentaram uma forte relação entre a dieta consumida e o desenvolvimento do
estresse oxidativo. Eles sugerem que uma dieta rica em compostos antioxidantes pode
melhorar o estado oxidativo e uma dieta alta em gorduras favorece a sua presença
(CARRILLON et al., 2003; SUWANNAPHET et al., 2010; COLACINO et al., 2014;
NEWSOME et al., 2014).
1.5.3. Genes envolvidos em mecanismos inflamatórios e na homeostase redox
A síndrome metabólica é considerada uma entidade poligênica multifatorial, na qual
participam interações metabólicas, hormonais, genéticas e o estilo de vida. Inúmeros
genes são considerados de importância nos mecanismos moleculares envolvidos na
patogênese e fisiopatologia da SM (GONZALES, 2003). São citados:
∗ Resistência insulínica: TNF-α, IRS-1, adiponectina, interleucinas (IL-6,10),
PPAR-γ-1,2, resistina.
∗ Obesidade: NPY (potente estimulador do apetite), UCP-1,2, TNF-α, NF-ĸβ. ∗ Inflamação e estresse oxidativo: TNF-α, leptina, IL-6, visfatina, resistina, NF-ĸβ.
∗ Dislipidemia: LPL, FAS.
Na Tabela 3 são apresentados alguns genes que participam dos processos de
Tabela 3
Genes envolvidos em mecanismos da inflamação e do estresse oxidativo.
Fonte (ADEGHATE, 2008; MIRANDA; REZA, 2008; COSTA et al., 2013).
2. Compostos bioativos da Mangifera indica.
A manga, da família Anarcadiaceae, gênero Mangifera e espécie indica, é uma das
frutas tropicais mais produzidas e comercializadas no mundo. É uma fruta nativa da Ásia,
tem sido cultivada na Índia por mais de 4000 anos e atualmente é cultivada e naturalizada
na maioria dos países tropicais, incluído Brasil. Várias partes da planta tem sido usadas
como adstringente, anticéptico, anti-inflamatório, e para tratar anemia, hipertensão,
reumatoide e asma (OJEWOLE, 2005; MOHAN et al., 2013). Estudos avaliaram extratos
etanólicos e aquosos a partir das folhas de M. indica, reportando efeitos antidiabéticos e
antidiarreicos em ratos (BHOWMIK et al., 2009; YACUBU; SALIMON, 2015). A seguir
são relacionados os principais compostos da M. indica.
2.1.Mangiferina
A Mangiferina é uma glicosilxantona presente em várias plantas medicinais e
frutíferas da família Anacardiaceae como a manga. Este composto bioativo tem mostrado
atividade biológica benéfica incluindo a antioxidante, anti-obesidade, anti-inflamatória,
neuroprotetora, inmunomodulatoria e hepatoprotetora (GARCÍA et al., 2011; DAS et al.,
2012). Este composto, está sendo amplamente estudado devido ao seu potencial no
Gene Atividade
Adiponectina Antioxidante, anti-inflamatória
Leptina Pro-inflamatória, oxidativa
Fator α de necrose tumoral Inflamatória, oxidativa
Interleucina 6 Pro-inflamatória, oxidativa
Visfatina Inflamatória
Resistina Pro-inflamatório,
Superóxido dismutase Antioxidante, anti-inflamatória
Catalase Antioxidante
Glutationa Antioxidante
tratamento e redução de risco de doenças, principalmente as relacionadas às alterações
metabólicas. Foi demonstrado em modelo animal de obesidade induzida por dieta
hiperlípidica que a mangiferina regulou 87 das 865 proteínas quantificadas, sendo muitas
delas envolvidas em vias metabólicas do metabolismo energético, incluindo a biogênese
mitocondrial, lipogênese e melhora de função hepática (LIM et al., 2014). Também foi
comprovado que a mangiferina regula a glioxilase impedindo a nefropatia diabética (LIU
et al., 2013), tem efeito anti-inflamatório na lesão pulmonar aguda por meio da regulação
da heme oxigenasse-1 (GONG et al., 2013), modula a expressão de genes envolvidos em
vias de inflamação e proteção antioxidante relacionados com a dor neuropática
(GARRIDO et al.,2010) e exerce atividade antitumoral nas células do câncer de mama
regulando catequinas e metaloproteinases (LI et al., 2013).
Cuba produz um extrato aquoso a partir dos galhos do tronco da mangueira e casca
da M. indica, denominado de Vimang®, sendo este caracterizado por ter propriedades
anti-inflamatórias, antioxidantes e imunomodulatórias evidenciadas em estudos clínicos
(GARRIDO et al., 2004; RODEIRO et al., 2006; PARDO et al., 2006-2008; MOHAN et
al., 2013). Análises químicas identificaram compostos fenólicos, flavonoides, ésteres,
galotaninos e mangiferina, no extrato do Vimang® (CAPOTE et al., 1998; SINGH et al.,
2015). Guerra et al. (2010) reportaram que o extrato do Vimang®, não induz efeitos
tóxicos em ratos, nas doses de mangiferina de aproximadamente 20-2000 mg.kg-1,
sugerindo que poderia ser utilizado em seres humanos.
2.2.Outros compostos
Polpa, folhas, galhos, flores, casca e sementes de M. indica são utilizadas para a
elaboração de produtos fitoterapêuticos, sendo administrados com fins medicinais
(RIBEIRO; SCHIEBER, 2010). Na Tabela 4 são apresentados alguns compostos
bioativos e fitoconstituentes encontrados na M. indica.
3. Consumo de chás: e seu uso no controle das alterações metabólicas associadas à obesidade.
Desde a antiguidade, o chá tem sido utilizado para manter e melhorar a saúde humana.
Tabela 4
Principais compostos bioativos da Mangifera indica L.
Compostos Parte da Mangifera indica L.
Fenólicos: antocianinas Casca, polpa, folhas, sementes, galhos
Flavonoides: quercetina, Galhos
Xantonas: mangiferina Casca, polpa, folhas
Catequinas e galotaninos Polpa
Ácidos: gálico, cumárico, caféico, ferúlico,
ascórbico.
Polpa, casca, folhas
Terpenoides: limoneno, sesquiterpenos, terpineno. Flores, folhas, casca, galhos
Fonte (RIBEIRO; SCHIEBER, 2010; LUO et al., 2014).
de matérias-primas alimentares provenientes de fontes naturais como flores, folhas e
frutos. A medicina Chinesa, por exemplo, recomenda o uso das plantas para tratar dores,
melhorar a digestão, depressão, desintoxicação, sugerindo ser energizante, capaz de atuar
no aumento da longevidade (SALEH et al., 2013).
As propriedades farmacológicas mais importantes dos chás mate, goishi, verde e preto
são: antioxidantes, anti-inflamatório, antimutagênico, anti-obesidade (ARÇARI et al.,
2009), ação hipoglicemiante, efeitos redutores da hipercolesterolemia e aterosclerose
(HONGLI et al., 2012; JOBU et al., 2013).
O desenvolvimento de terápicos para o tratamento da obesidade e de suas
comorbidades tem sido lento, comparado com a velocidade de aumento da ocorrência
dessas desordens metabólicas (LIM et al., 2014).
O uso de chás e infusões como coadjuvante no tratamento da obesidade tem se
popularizado, ultimamente. Atualmente, o mercado oferece chás, sendo os mesmos
amplamente disponibilizados para o consumo e são classificados de acordo com seus
métodos de preparação. Chás não fermentados, semi-fermentados, fermentados e
post-fermentados tem sido estudados, como fonte substâncias tais como polifenóis, catequinas,
xantonas e outros compostos bioativos (MORIYAMA; TAKEDA, 2008; JOBU et al.,
2013).
Estudos em extratos ricos em polifenóis e taninos provenientes dos chás verde, preto,
de ervas ou de frutas como a uva, tem reportado que estes compostos são inibidores da
lipase pancreática, principal responsável pela digestão de triacilgliceróis,
2010; SERGENT et al., 2012). Também foi demonstrado que as antocianinas têm
importantes atividades biológicas incluindo as antioxidantes, anticancerígenas,
anti-inflamatórias, além de ter a capacidade de controlar macrófagos e proteger do estresse
oxidativo e a apoptose (BADSHAH et al., 2013; WUA et al., 2013; LEE et al., 2014).
Compostos fenólicos, incluindo as xantonas, têm efeitos inibidores na síntese de
ácidos graxos (ZHONG et al., 2010), antioxidantes, anticancerígenos, antimicrobianos,
anti-inflamatórios, antialérgicos, analgésicos (KERIO et al., 2013; IBRAHIM et al.,
2014) e antipiréticos (SINGH et al., 2011).
Conclusão
A síndrome metabólica gera um conjunto de alterações no metabolismo levando ao
desenvolvimento de múltiplas doenças, que representam um problema de saúde pública
atual e cuja prevalência está aumentando. Tais doenças compreendem a obesidade, as
cardiovasculares, dislipidemia, diabetes tipo II, resistência insulínica e outras.
A obesidade está caraterizada pelo aumento de peso e acumulo de gordura corporal,
produtos de uma alimentação inadequada, sedentarismo ou fatores genéticos. Nesta
doença são observadas alterações metabólicas influenciadas por diferentes mecanismos e
vias celulares. Atrofias nos adipócitos, apoptose, estresse oxidativo e inflamação são as
principais alterações da obesidade.
A M. indica tem potencial como fonte de compostos bioativos com atividades
funcionais. Seu principal constituinte, a mangiferina, pode ser utilizado como fitoterápico
REFERÊNCIAS BIBLIOGRÁFICAS
ADA. American Diabetes Association. Diabetes Type II; 2014 [Citado 2014]; Disponível
em: http://www.diabetes.org/?loc=util-header-es.
ALBORNOZ, R. e PÉREZ, I. Nutrición y Sindrome Metabólico. Nutrición Clinica y
Hospitalaria, v.32, n.3, p.92-97. 2012.
ALVES N.G, SAMANTA T. VALDÉS S.T., SILVEIRA C.M., et al. Studies on
Mechanistic Role of Natural Bioactive Compounds in the Management of Obesity An
Overview. The Open Nutraceuticals Journal, v.5, p.193-206. 2012.
ADEGHATE, E. Visfatin: structure, function and relation to diabetes mellitus and other
dysfunctions. Current Medicinal Chemistry, v.15, n.18, p.1851-1862. 2008.
ADER, M., STEFANOVSKI, D., KIM, S. P., et al. Variable hepatic insulin clearance
with attendant insulinemia is the primary determinant of insulin sensitivity in the normal
dog. Obesity (Silver Spring). PubMed, v. PubMed PMID: 24123967. Epub 2013/10/15.
Eng. 2013.
ARÇARI D.P., BARTCHEWSKY W., DOS SANTOS T.W., et al. Antiobesity effects of
yerba mate extract (Ilex paraguariensis) in high-fat diet-induced obese mice. Obesity,
v.17, p.2127–2133. 2009.
ARNOLDUSSEN, I., KILIAAN, A. J. e GUSTAFSON, D. R. Obesity and dementia:
Adipokines interact with the brain. European Neuropsychopharmacology: Elsevier
2014.
AVRAM, M. M., SHARPE, A. e JAMES, W. D. Subcutaneous fat in normal and diseased
states: 3. Adipogenesis: From stem cell to fat cell. Journal of the American Academy
BADSHAH, H., ULLAH, I., EUN, S. E., et al. Anthocyanins attenuate body weight gain
via modulating neuropeptide Y and GABAB1 receptor in rats hypothalamus.
Neuropeptides, Elsevier, v.47, n.5, p.347-353. 2013.
BAHCECI, M., GOKALP, D., BAHCECI, S., et al. The correlation between adiposity
and adiponectin, tumor necrosis factor alpha, interleukin-6 and high sensitivity C-reactive
protein levels. Is adipocyte size associated with inflammation in adults? Journal of
Endocrinological Investigation, v.30, n.3, p.210-214. 2007.
BASTIDAS, R., CASTAÑO, J., ENRIQUEZ, M., et al. Relación entre Hipertensión
arterial y obesidad en pacientes hepertensos atendidos en ASSBASALUD E.S.E,
Manizales (Colombia). Archivos de Medicina, v.11, n.2, p.150-158. 2011.
BENEVIDES, S., RAMOS, A. M., STRINGHETA, P. C., et al. Qualidade da manga e
polpa da manga Ubá. Ciência e Tecnologia de Alimentos, v.28, n.3, p.571-578. 2008.
BHOWMIK, A., ALI KHAN, L., AKHTER, M., et al. Studies on the antidiabetic effects
of Mangífera indica stem-barks and leaves on nondiabetic, type 1 and type 2 diabetic
model rats Journal of the Bangladesh Pharmacological Society, v.4, p.110-114. 2009.
BLANCAS, G., ALMANZA, J. C., LÓPEZ, R. I., et al. La obesidad como un proceso
inflamatorio. Boletin Médico, sciELO, v.67, n.2, p.88-97. 2010.
BLOOMGARDEN, Z. T. Insulin Resistance: Causes and Consequences. International
Review of Neurobiology. HARRIS RA, J. P.: Elsevier. 65: 1-24 p. 2005.
BREMER, A. A. e JIALAL, I. Adipose Tissue Dysfunction in Nascent Metabolic
Syndrome. Journal of Obesity, v.2013, p.1155. 2013.
BRITO, L. F. Efeito do extrato das folhas de manga ubá (Mangífera indica L.) e da
Post-Graduaçao em Bioquimica Agricola. Universidade Federal de Viçosa. Viçosa (MG).
2013.
CAPOTE, R., GUARDADO, I., NOVOA, H., et al. Chemical–analytical characterization
of aqueous extract of Mangífera indica L. Revista Cubana de Química, v.10, n.111–
120. 1998.
CARILLON, J., ROMAIN, C., BARDY, G., et al. Cafeteria diet induces obesity and
insulin resistance associated with oxidative stress but not with inflammation:
improvement by dietary supplementation with a melon superoxide dismutase. Free
Radical Biology and Medicine, v.65, p. 254–261. 2013.
CHAKRABARTI R. Pharmacotherapy of obesity: Emerging drugs and targets. Expert
Opinion on Therapeuyic Targets, v.13, p.195-207. 2009.
CHENG, Y., TAKEUCH, H., SONOBE, Y., et al. Sirtuin 1 attenuates oxidative stress
via upregulation of superoxide dismutase 2 and catalase in astrocytes. Journal of
Neuroimmunology, v.269, n.1-2, p.38-43. 2014.
COLACINO, J. A., ARTHUR, A., FERGUSON, K., et al. Dietary antioxidant and
anti-inflammatory intake modifies the effect of cadmium exposure on markers of systemic
inflammation and oxidative stress. Environmental Research, v.131, p.6-12. 2014.
COSTA, L. A., BADAWI, A. e EL-SOHEMY, A. Nutrigenética y modulación del estrés
oxidativo. Annales Nestlé, v.60, n.3, p.27-36. 2012.
DAS J., GHOSH J., ROY A., et al. Mangiferin exerts hepatoprotective activity against
D-galactosamine induced acute toxicity and oxidative/nitrosative stress via Nrf2–NFκB pathways. Toxicology and Applied Pharmacology, v.260, p.35-47. 2012.
DENG, Y. e SCHERER, P. E. Adipokines as novel biomarkers and regulators of the
metabolic syndrome. Annals of the New York Academy of Sciences, v.1212, p.E1-E19.
DESPRÉS, J. Body fat distribution and risk of cardiovascular disease: an update.
Circulation, v.126, n.10, p.1301-13. 2012.
DEVALARAJA S., JAIN S. e YADAV H. Exotic fruits as therapeutic complements for
diabetes, obesity and metabolic syndrome. Food Research International, Elsevier.
2011.
DORTA E., GONZÁLEZ M., LOBO M., et al. Screening of phenolic compounds in
by-product extracts from mangoes (Mangifera indica L.) by HPLC-ESI-QTOF-MS and
multivariate analysis for use as a food ingredient. Food Research International,
Elsevier, v.57, p.51-60. 2014.
DUANGA X., WANGA Q., ZHOUB X., et al. Mangiferin: A possible strategy for
periodontal disease to therapy. Medical Hypotheses, v.76, n.4, p.486-488. 2011.
EL-WAKKADA, A., EL-MORSI, N., SIBAIIA, H., et al. Proinflammatory,
anti-inflammatory cytokines and adiponkines in students with central obesity. Cytokine, v.61,
n.2, p.682-687. 2013.
FABBRINI, E., SULLIVAN, S. e KLEIN, S. Obesity and nonalcoholic fatty liver disease:
biochemical, metabolic, and clinical implications. Hepatology. v.51, n.2, p.679-89. 2010.
FANTUZZI, G. Adiponectin and inflammation: Consensus and controversy Journal of
Allergy and Clinical Immunology, v.121, n.2, p.326–330. 2008.
FAOSTAT. Food and Agriculture Organization of the United Nations FAO Agriculture
Statistics 2011. [Citado 2014]; Disponível em: http://www.fao.org/corp/statistics/en/
FERNANDES, C. A., FIEVEZ, L., NEYRINCK, A. M., et al. Sirtuin inhibition attenuates
the production of inflammatory cytokines in lipopolysaccharide-stimulated macrophages.