CARLA POLESELLI BRUNIERA
Sistemática e taxonomia de Rudgea Salisb.
(Palicoureeae, Rubiaceae)
SÃO PAULO
CARLA POLESELLI BRUNIERA
Sistemática e taxonomia de Rudgea Salisb.
(Palicoureeae, Rubiaceae)
Tese apresentada ao Instituto de Biociências
da Universidade de São Paulo, para a
obtenção de Título de Doutor em Ciências, na
Área de Botânica.
Orientador: Prof. Dr. Milton Groppo Jr
Co-orientadora: Dra. Daniela Cristina Zappi
SÃO PAULO
Bruniera, Carla Poleselli
Sistemática e taxonomia de
Rudgea
Salisb.
(Palicoureeae, Rubiaceae)
273 páginas
Tese (Doutorado) - Instituto de Biociências da
Universidade de São Paulo. Departamento de Botânica.
2015.
1.
Rudgea
2.Rubiaceae 3.Palicoureeae 4.Filogenia
I.Universidade de São Paulo. Instituto de Biociências.
Departamento de Botânica.
Comissão Julgadora:
Prof(a). Dr(a)
.
Prof(a). Dr(a).Prof(a). Dr(a). Prof(a). Dr(a).
Ao Mateus e à Lara, que chegaram no meio do
caminho e viraram minha vida de ponta cabeça,
obrigada por bagunçarem tudo e fazerem dessa nossa
bagunça o melhor lugar para viver. Hoje vivo para
“O sucesso nasce do querer, da
determinação e persistência em se chegar
a um objetivo. Mesmo não atingindo o
alvo, quem busca e vence obstáculos, no
mínimo fará coisas admiráveis”
José de Alencar
Agradecimentos
A presente tese é produto de muito empenho e esforço individual e conjunto. Por isso, gostaria de agradecer a todos que contribuíram de alguma forma para que este trabalho pudesse ser realizado, em especial:
Ao Programa de Pós‐Graduação em Botânica, do Departamento de Botânica, Instituto de Biociências da Universidade de São Paulo pelo Curso de Pós‐Graduação e aos membros da Secretaria dos respectivos Departamento e Instituto, por estarem sempre dispostos a auxiliar quando necessário;
Ao Departamento de Biologia da Faculdade de Filosofia, Ciências e Letras de Ribeirão Preto, por disponibilizar as instalações, equipamentos, materiais e técnicos de seus laboratórios para o desenvolvimento deste estudo;
À Fundação de Amparo à Pesquisa no Estado de São Paulo (FAPESP), pela concessão da bolsa de doutorado (Processo 2010/18172‐4) e do Auxílio à Pesquisa (Processo 2011/10446‐0), sem o qual não teria sido possível desenvolver este trabalho;
À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES) e ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) pela concessão das bolsas de doutorado através do Programa de Pós‐Graduação em Botânica (IB‐USP) no primeiro ano do doutorado;
Ao Prof. Dr. Milton Groppo, por aceitar a orientação dos meus projetos desde a graduação, pela confiança no desenvolvimento deste trabalho, pelas oportunidades concedidas que têm contribuído para minha formação profissional e pela amizade;
À Dra. Daniela Cristina Zappi, co‐orientadora deste trabalho, por ter confiado na minha capacidade de desenvolver este projeto e por ter aceitado compartilhar seu grupo de estudo, seus conhecimentos, materiais, literaturas de difícil acesso e ilustrações, por ter sido uma orientadora e colaboradora essencial para o desenvolvimento deste trabalho, e pela amizade durante estes anos;
discutir e auxiliar nas questões taxonômicas e pelas oportunidades concedidas durante estes anos;
Ao Missouri Botanical Garden, pela concessão da Bolsa “Elizabeth E. Bascom”, concedida anualmente à latinas‐americanas, propiciando a visita e permanência por um período de ca. 40 dias no herbário do Missouri Botanical Garden, no qual grande parte dos dados deste trabalho foram coletados, propiciando também uma grande experiência em trabalhar em uma Instituição Estrangeira de Excelência em Pesquisa com Sistemática e Taxonomia de Plantas;
Às pessoas que foram essenciais durante minha estadia no Missouri Botanical Garden: a Dra. Charlotte Taylor, que me supervisionou e orientou durante este período, e também pelo passeio na cidade de Saint‐Louis, idas às hamburguerias, e pelo jantar de Thanksgiving; à Kathy Hurlbert, por ter auxiliado no planejamento da viagem; à Alba Arbelaez, pela amizade e pela auxílio sempre que necessário; às funcionárias da Biblioteca Peter Raven, que estavam sempre disponíveis para auxiliar; aos demais pesquisadores e funcionários, principalmente à Rosa Ortiz‐Gentry, Carmen Ulloa e John Pruski pela amizade e assistência durante o período; e também à Sarah Souza e à Nállarett Dávilla, pelo companheirismo durante o período, que construiu uma boa amizade entre nós;
Ao Laboratório de Sistemática de Plantas, do Departamento de Biologia da FFCLRP; à sua técnica Maria Helena Pires, pela disponibilidade e auxílio em todos os momentos necessários; aos estagiários e pós‐graduandos deste laboratório pelo apoio, sugestões, discussões e amizade: Anelize Barbosa, Camila Dias, Carimi Cortez, Carolina Ferreira, Luciano Margalho, Luisa Lemos, Paola de Lima Ferreira e Milton Henrique Ferreira, especialmente à Camila Dias e Paola de Lima Ferreira, pela ajuda na obtenção de dados moleculares, como bolsistas de treinamento técnico vinculadas a este trabalho;
Aos membros da banca de qualificação, Prof. Dr. José Rubens Pirani, Dr. Pedro Fiaschi e Dra. Maria Fernanda Calió, pelas valiosas opiniões e sugestões a este trabalho durante seu andamento. E também à Profa. Dra. Lúcia Garcez Lohmann, pelas sugestões na banca de ingresso, que foram muito importantes na delimitação do projeto inicial;
Aos queridos amigos botânicos que me acompanharam em campo, ou que coletaram amostras de Rudgea contribuindo com o trabalho, especialmente à Adriana Lobão, Juliana El Ottra, Mariana Saavedra, Mateus Fortes dos Santos, Pablo Viany e Pedro Fiaschi. E aos guias e auxiliares de campo que foram essenciais nas coletas, principalmente nas expedições na Amazônia e no Peru;
Aos herbários e seus respectivos curadores, pelos empréstimos e doações de exsicatas concedidas ao herbário SPFR, indispensáveis para este estudo: BHCB, ESA, GB, HRCB, HUEFS, INPA, K, MBML, MO, OUPR, P, RB, SP, SPF, UEC and UPCB. Em especial à Dra. Rafaela Forzza, curadora do herbário RB e ao Dr. André Amorim, curador do herbário CEPEC, por incentivarem e possibilitarem o uso das dependências dos respectivos herbários para coletas de campo;
Ao Laboratório de Biologia Molecular de Plantas (Dep. de Biologia, FFLCRP – USP) e ao Laboratório de Bioquímica e Biologia Molecular (Dep. de Tecnologia, UNESP Jaboticabal) pelas centenas de sequências geradas para este trabalho e às respectivas técnicas destes laboratórios, Dra. Andréa Quiapim e Dra. Agda Paula Facincani;
Aos botânicos que disponibilizaram e autorizaram o uso de fotos de suas autorias nesta tese: Alex Popovkin, Ana Magalhães C. Teixeira, Denise Sasaki, Eliana Gressler, Felipe Amorim, Henrique R. Magalhães, Júlio L. Campbell, Luiz Funez e Milton Groppo;
Ao grupo de discussão em Sistemática, coordenado pelo Prof. Dr. Eduardo Almeida (FFCLRP, USP), pelas discussões sempre proveitosas e enriquecedoras a respeito dos Conceitos e Metodologias em Sistemática;
Às minhas amigas Sarah Leandrini, Carolina Laurini e Juliana Rando, e à minha prima Fernanda Poliselli, por concederem hospedagem em São Paulo sempre que foi preciso;
Às irmãs que a vida me deu, Graziele Ferreira, Giovana da Silva Leandro e Priscilla de Campos, que são peças fundamentais na minha história e nunca me negaram apoio, mesmo nos momentos mais complicados. À “Terra do Nunca” e a todas às amigas que passaram por ela, pois se existia um lugar onde me sentia em casa, desde os tempos de agregada até virar moradora, era ali.
À minha família, que além de todo o amor e carinho, me concedem apoio total e constante na minha vida acadêmica. Em especial aos meus pais por me lembrarem sempre dos meus objetivos e de nunca desviar o olhar daquilo que realmente queremos no futuro.
À minha mãe Maria Aparecida Bruniera, à minha sogra Vera Lúcia Lopes e à minha irmã Carina Bruniera Duarte, por não medirem esforços para cuidarem da Lara enquanto eu trabalhava nesta tese, não tenho como mensurar minha gratidão à vocês.
Ao meu companheiro Mateus Lopes, por ter ajudado e colaborado em diversos aspectos da tese, e por ter sido tão parceiro nos plantões de finais de semana e feriados no Herbário e na USP. Obrigada também por todo o amor e carinho que me fazem ser tão feliz e por ter me dado o melhor presente de todos, nossa pequena Lara.
A todas às pessoas que não foram citadas, mas que ajudaram em viagens de coleta, nas visitas aos herbários, durante os processos experimentais, na discussão de metodologias e de resultados, nas questões burocráticas, ou em qualquer outro aspecto deste trabalho. Muito obrigada!
ÍNDICE
LISTA DE TABELAS, FIGURAS E APÊNDICES ... 1
RESUMO ... 6
ABSTRACT ... 7
INTRODUÇÃO GERAL ... 9
1. RUBIACEAE ... 9
2. RUDGEA ... 12
3. OBJETIVOS ... 14
4. ORGANIZAÇÃO DA TESE ... 15
REFERÊNCIAS ... 15
CAPÍTULO 1 ‐ DELIMITATION OF RUDGEA SALISB. (PALICOUREEAE, RUBIACEAE) BASED IN PHYLOGENETIC INFERENCE FROM MOLECULAR DATA AND IN MORPHOLOGICAL EVOLUTION ANALYSES. ... 23
ABSTRACT ... 23
RESUMO ... 24
INTRODUCTION ... 25
MATERIALS AND METHODS ... 30
RESULTS ... 42
DISCUSSION ... 62
CONCLUSION ... 75
LITERATURE CITED ... 76
CAPÍTULO 2 ‐ SYNOPSIS OF RUDGEA SALISB. (PALICOUREEAE, RUBIACEAE) FOR BRAZIL ... 94
ABSTRACT ... 94
RESUMO ... 94
INTRODUCTION ... 95
MATERIAL AND METHODS ... 97
RESULTS AND DISCUSSION ... 98
CONCLUSION ... 198
REFERENCES ... 198
CAPÍTULO 3 ‐ RUDGEA AGRESTEOPHILA AND R. HILEIABAIANA (PALICOUREEAE, RUBIACEAE): TWO NEW SPECIES FROM EASTERN BAHIA, BRAZIL ... 244
CAPÍTULO 4 ‐ TAXONOMIC TRANSFERS IN NEOTROPICAL PALICOUREEAE: NEW COMBINATIONS IN RUDGEA AND PALICOUREA ... 258
CONCLUSÃO GERAL E CONSIDERAÇÕES FINAIS ... 272
Lista de Tabelas, Figuras e Apêndices
Capítulo 1
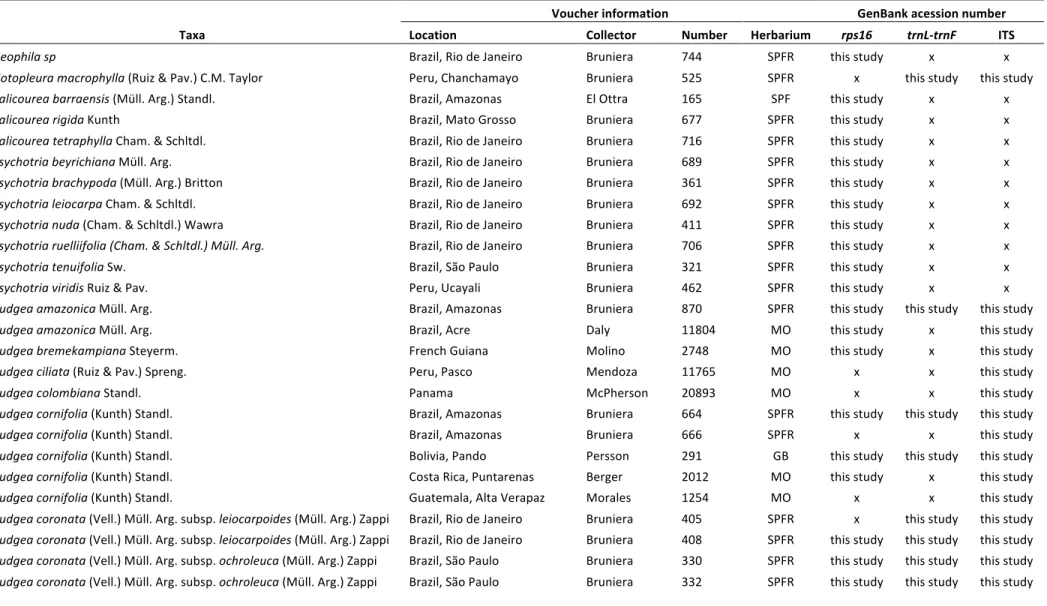
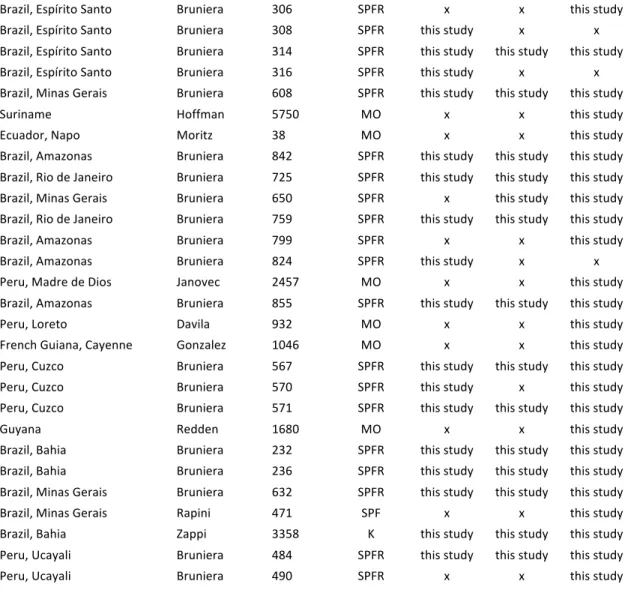
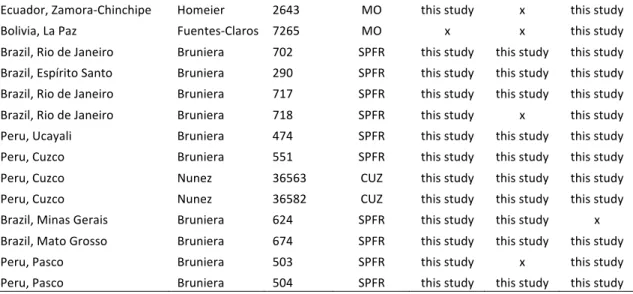
Table 1. Voucher information about sequences produced in the present work………..………..34 Table 2. GenBank acession numbers of sequences used in molecular analyses……….40 Table 3. Characteristics of the markers/data sets used, including statistics of alignments and evolutionary models suggested by jModelTest v.0.1.1 (Posada, 2008)……….………...43 Table 4. Summary of the distribution of the four morphological characters analysed in the five minor groups of Rudgea………..……….….……69
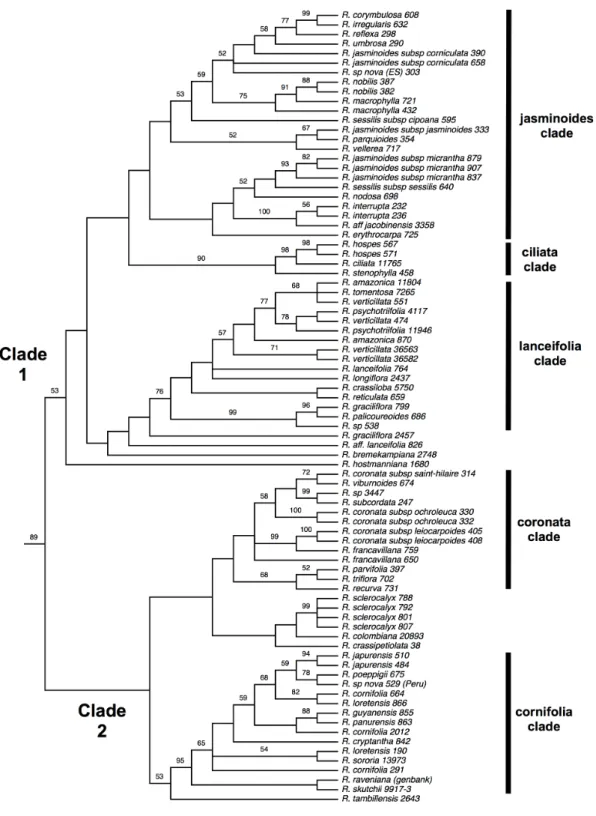
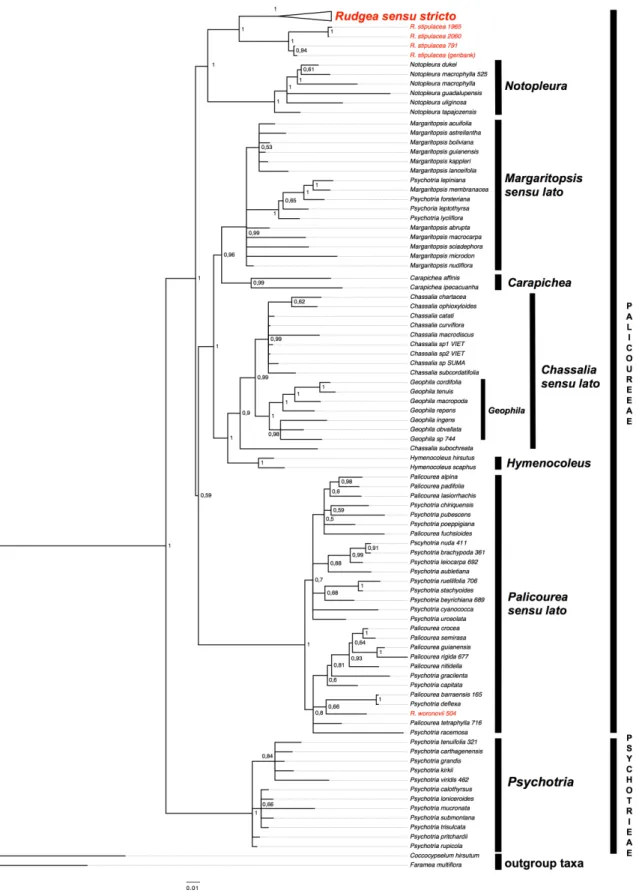
Figure. 1. Majority‐rule consensus tree from the 106 most parsimonious trees (CI=0.45, RI=0.77) from combined datasets of rps16, trnL‐trnF and ITS. The numbers above branches refers to bootstrap values. Taxa in red correspond to species of Rudgea. The clade Rudgea sensu stricto is detailed in Fig. 2……….………46 Figure. 2. Clade Rudgea sensu stricto from majority‐rule consensus tree from the 106 most parsimonious trees (CI=0.45, RI=0.77) from combined datasets of rps16, trnL‐trnF and ITS. (Fig. 1). The numbers above branches refers to bootstrap values………...47 Figure. 3. Majority‐rule consensus tree from the Bayesian analysis of the combined datasets of rps16, trnL‐trnF and ITS. The numbers above or on the side of the nodes refers to posterior probabilities. Taxa in red correspond to species of Rudgea. The clade Rudgea sensu stricto is detailed in Fig. 4………48 Figure. 4. Clade Rudgea sensu stricto from majority‐rule consensus tree from the Bayesian analysis of the combined datasets of rps16, trnL‐trnF and ITS (Fig. 3). The numbers above or on the side of the nodes refers to
posterior probabilities.………..…49
Figure. 5. Maximum Likelihood ancestral state reconstruction of morphological characters on the clade Rudgea sensu lato of the parsimony majority‐rule consensus tree of combined data, with reduced taxa. Pie diagrams indicate ancestral state probabilities for each state of character at a given node……….53 Figure. 6. Maximum Likelihood ancestral state reconstruction of morphological characters traced on the clade
Rudgea sensu lato of the parsimony majority‐rule consensus tree of combined data, with reduced taxa. The color of the branches indicates the most probable ancestral state for a given character……….54 Figure. 7. Maximum Likelihood ancestral state reconstruction of morphological characters on the clade Rudgea sensu lato of the parsimony majority‐rule consensus tree of combined data, with reduced taxa. Pie diagrams indicate ancestral state probabilities for each state of character at a given node……….56 Figure. 8. Maximum Likelihood ancestral state reconstruction of morphological characters traced on the clade
Rudgea sensu lato of the parsimony majority‐rule consensus tree of combined data, with reduced taxa. The color of the branches indicates the most probable ancestral state for a given character……….57 Figure. 9. Maximum Likelihood ancestral state reconstruction of morphological characters on the clade Rudgea sensu lato of the parsimony majority‐rule consensus tree of combined data, with reduced taxa. Pie diagrams indicate ancestral state probabilities for each state of character at a given node……….58 Figure. 10. Maximum Likelihood ancestral state reconstruction of morphological characters traced on the clade
Rudgea sensu lato of the parsimony majority‐rule consensus tree of combined data, with reduced taxa. The color of the branches indicates the most probable ancestral state for a given character……….59 Figure. 11. Maximum Likelihood ancestral state reconstruction of morphological characters on the clade
Rudgea sensu lato of the parsimony majority‐rule consensus tree of combined data, with reduced taxa. Pie diagrams indicate ancestral state probabilities for each state of character at a given node………..60 Figure. 12. Maximum Likelihood ancestral state reconstruction of morphological characters traced on the clade
Figure. 13. Examples of stipules found in Rudgea. A. Bilobed‐fimbriate stipule of R. woronovii. B. Entire stipule of R. stipulacea. C. Fimbriate stipule of R. sessilis subsp. sessilis. D. Dorsally keeled stipule of R. macrophylla. E. Dorsally keeled stipule of R. nobilis. Photos by C.P. Bruniera………...66
Appendix 1. Characters and the respective states used in the evolution analyses of morphological characters………84 Appendix 2. Matrix of morphological data………..………..85 Appendix 3. Majority‐rule consensus tree from the parsimony analysis of rps16. The numbers above branches refers to bootstrap values.……….………….…..87 Appendix 4. Majority‐rule consensus tree from the Bayesian analysis of rps16. The numbers above or on the side of the nodes refers to posterior probabilities. ………..………..………88 Appendix 5. Majority‐rule consensus tree from the parsimony analysis of trnL‐trnF. The numbers above branches refers to bootstrap values.………..………...89 Appendix 6. Majority‐rule consensus tree from the Bayesian analysis of trnL‐trnF. The numbers above or on the side of the nodes refers to posterior probabilities.………..……….…..90 Appendix 7. Majority‐rule consensus tree from the parsimony analysis of ITS. The numbers above branches refers to bootstrap values.………..………..91 Appendix 8. Majority‐rule consensus tree from the Bayesian analysis of ITS. The numbers above or on the side of the nodes refers to posterior probabilities.………..………..92 Capítulo 2
of inflorescence. [A: Noblick 1738 (HUEFS); B, C: Jardim 4635 (HUEFS); D: Grogan 558 (INPA); E: Grogan 397 (INPA); F: Grogan 583 (INPA); G, H: Pohl 805 (K, type)]. Drawn by Maíra Clasen Massarani...228 Figure 27. A‐B. Rudgea francavillana. A. Inflorescence. B. Detail of inflorescence. C‐G. Rudgea gardenioides. C. Branch with inflorescence. D. Stipule. E. Flowerbud. F. Corolla and stamens. G. Calyx, longitudinal section. [A‐B: Taken from Zappi (2003: 558); C‐G: Taken from Zappi (2003: 581)]. Drawn by Daniela C. Zappi...229 Figure 28. A‐C. Rudgea graciliflora. A. Branch with infrutescence. B. Stipules. C. Flower. D‐J. Rudgea hileiabaiana. D. Branch with inflorescence. E. Stipule. F. Flowerbud. G. Flower. H. Fruit. I. Seed, dorsal view. J. Seed, ventral view. [A: Rodrigues 8302 (INPA); B: Jardim 4521 (HUEFS); C: Assunção & Pereira 393 (INPA); D, F, G: Santos 3882 (SP); E: Fiaschi 1880 (SPF); H: Thomas 11917 (SP); I, J: Fiaschi 2121 (SPF)]. Drawn by Maíra Clasen Massarani...230 Figure 29. A‐C. Rudgea hostmanniana. A. Branch with infrutescence. B. Stipule. C. Fruit. D‐F. Rudgea ilheotica. D. Branch with old inflorescence. E. Stipule. F. Fruit. [A‐C: Prévost & Sabatier 4154 (MO); D‐F: Sobral & Toscano 6800 (SP)]. Drawn by Maíra Clasen Massarani...231 Figure 30. A‐D. Rudgea insignis. A. Branch with solitary flower. B. Stipule. C. Flower. D. Calyx, longitudinal section. E‐I. Rudgea irregularis. E. Branch with infrutescence. F. Stipule. G. Corolla. H. Calyx. I. Fruit. [A, B:
Duarte 1500 (SPFR); C, D: Taken from Zappi (2003: 541); E, F: Lughadha & Queiroz 53337 (SPFR); G‐I: Taken from Zappi (2003: 581)]. Drawn by Maíra Clasen Massarani (A, B, E, F) and Daniela C. Zappi (C, D, G‐I)...232 Figure 31. A‐C. Rudgea jacobinensis. A. Branch with infrutescence. B. Stipule. C. Flower. D‐F. Rudgea japurensis. D. Stipule. E. Inflorescence. F. Fruit. G‐J. Rudgea jasminoides subsp. corniculata. G. Branch with inflorescence. H. Fragment of inflorescence. I. Flowerbud. J. Flower. [A: Amorim 3008 (SP); B: França 3181 (HUEFS); C: Mori 11167 (RB); D, F: Romaniuc Neto 495 (SPFR); E: Delprete 8016 (MO); G‐J: Taken from Zappi (2003: 522)]. Drawn by Maíra Clasen Massarani (A‐F) and Daniela C. Zappi (G‐J)...233 Figure 32. A. Rudgea lanceifolia. Flower. B‐E. Rudgea longiflora. B. Branch with inflorescence. C. Stipule. D. Flower. E. Fruit. F. Rudgea longipes. Branch with inflorescence. G‐I. Rudgea macrophylla. G. Calyx. H. Corolla. I. Fruit. [A: Van der Werff 10024 (MO); B‐D: Grogan 399 (INPA); E: Sasaki 1200 (INPA); F: Saint‐Hilaire s.n. (P, type); G‐I: Taken from Zappi (2003: 534)]. Drawn by Maíra Clasen Massarani (A‐F) and Daniela C. Zappi (G‐I)... ...234 Figure 33. A‐E. Rudgea minor subsp. minor. A. Branch with infrutescence. B. Detail of Inflorescence. C. Flower. D. Fruit. E. Pyrene, ventral view. F‐I. Rudgea minor subsp. calycina. F. Branch with infrutescence. G. Flowerbud. H. Flower. I. Fruit. [A‐E, G: Taken from Zappi (2003: 562); F, I: Fiaschi 3504 (SPFR); H: Brade 14983 (SPFR)]. Drawn by Daniela C. Zappi (A‐E, G) and Maíra Clasen Massarani (F, H, I)...235 Figure 34. A. Rudgea mucronata. Branch with infrutescence. B‐G. Rudgea nodosa. B. Branch with inflorescence. C. Inflorescence. D. Flower. E. Fruit. F. Pyrene, dorsal view. G. Pyrene, ventral view. H‐J. Rudgea obtusa. H. Branch with inflorescence. I. Stipule. J. Flower. [A: Assis & Cribari 2677 (K); B: Jardim & Lopes 3940 (HUEFS); C‐ G: Taken from Zappi (2003: 562); H: Sidney & Onishi 1334 (RB); I: Thomas 4532 (SPF); J. Prance & Silva 59489
(MO)]. Drawn by Maíra Clasen Massarani (A, B, H‐J) and Daniela C. Zappi (C‐G)...236 Figure 35. A‐C. Rudgea pachyphylla. A. Branch with inflorescence. B. Flowerbud. C. Corolla. D. Rudgea palmarum. Branch with inflorescence. E‐G. Rudgea panurensis. E. Branch with infrutescence. F. Stipule. G. Inflorescence. [A‐C: Costa 498 (RB); D: Krukoff 8561 (BR); E, F: Vásquez & Jaramillo 16124 (MO); G: Revilla 1447
Daniela C. Zappi...239 Figure 38. A‐E. Rudgea reticulata. A. Branch with infrutescence. B. Corolla. C. Calyx. D. Calyx, longitudinal section. E. Fruit. F‐H. Rudgea sessilis subsp. sessilis. F. Inflorescence. G. Corolla. H. Calyx. I. Rudgea sessilis
RESUMO
A sistemática da família Rubiaceae passou por grandes mudanças nas últimas duas décadas. O uso de dados moleculares levou a revisões significativas na classificação intra‐ familiar, principalmente a nível genérico. As relações entre alguns dos gêneros neotropicais mais diversos de Rubiaceae (e.g. Psychotria, Palicourea e Rudgea) estão sendo investigadas. O gênero neotropical Rudgea possui c. 130 espécies, distribuídas do México ao nordeste da Argentina, com dois centros de diversidade, um no noroeste da América do Sul, e outro no sudeste do Brasil. As espécies são caracterizadas pelas estípulas inteiras ou fimbriadas, com apêndices glandulares, presença de domácias nas folhas, inflorescência terminal, lobos da corola corniculados e sementes profundamente sulcadas na face adaxial. Trabalhos filogenéticos anteriores incluíram uma amostragem limitada de espécies do gênero Rudgea. Nossas análises moleculares mostram Rudgea como um gênero monofilético com a exclusão de R. woronovii, uma espécie mais próxima de Palicourea sensu lato. Por outro lado, R.
stipulacea emergiu como grupo‐irmão das demais espécies de Rudgea, sendo o grupo formado por estas espécies altamente sustentado e denominado “Rudgea sensu stricto”. Mudanças taxonômicas serão necessárias para acomodar Rudgea stipulacea, e uma classificação infragenérica de Rudgea será proposta, com suporte molecular e morfológico. Além da análises filogenéticas, também foi realizado um tratamento taxonômico para as espécies brasileiras de Rudgea, com 64 espécies aceitas e 26 sinônimos novos. Informações nomenclaturais completas foram fornecidas e 36 lectótipos foram designados. Chaves de identificação para as espécies e subespécies (quando apropriado) também foram apresentadas. Informações sobre distribuição geográfica, habitat, fenologia, discussões taxonômicas, material examinado e figuras também foram apresentadas. Este é o primeiro tratamento de Rudgea para o Brasil desde a monografia de Mueller Argoviensis em 1881 para a Flora Brasiliensis. Como parte dos estudos taxonômicos em Rudgea, o manuscrito que compreende as descrições de duas novas espécies da Bahia (Brasil) e o manuscrito com novas combinações em Rudgea e Palicourea sensu lato também foram incluídos nesta tese.
ABSTRACT
INTRODUÇÃO
GERAL
Rudgea insignis
INTRODUÇÃO GERAL
1. Rubiaceae
Rubiaceae Juss. é a quarta maior família entre as Angiospermas, com aproximadamente 611 gêneros e 13100 espécies (Govaerts et al. 2015), classificadas em mais de 40 tribos (Bremer & Eriksson 2009). A família possui distribuição cosmopolita e predominantemente pantropical, e estão presentes nos mais diversos habitats, dos “páramos” aos ambientes desérticos e áridos. Praticamente metade das espécies e um terço dos gêneros ocorrem no neotrópico (Delprete 2004, Delprete & Jardim 2012). No Brasil ocorrem 125 gêneros (17 endêmicos) e ca. 1400 espécies, das quais ca. 732 são endêmicas, sendo especialmente diversa nos biomas da Amazônia, Cerrado e na Mata Atlântica (Barbosa et al. 2015).
esquizocárpicos, bacáceos ou drupáceos. Os pirênios, compostos da semente e do endocarpo coriáceo ou lenhoso, são encontrados em diversos representantes com frutos drupáceos. As sementes são livres, imersas em tecido placentário, aladas ou excepcionalmente com um tufo de pêlos, 1‐muitas por cada lóculo, com endosperma presente, albúmen abundante, raramente escasso ou ausente; o embrião é reto ou curvo, com radícula superior ou inferior (Robbrecht 1988; Delprete 2004, 2010; Delprete et al. 2004; Jung‐Mendaçolli 2007).
Apesar dessa grande variação morfológica, a família é reconhecida pela associação de algumas características: folhas opostas (a verticiladas), com lâmina simples e inteira; presença de estípulas interpeciolares, raro intrapeciolares, inteiras, bífidas ou multifimbriadas; corola gamopétala; estames isostêmones e ovário ínfero (Delprete 2010). Apesar de algumas exceções, estas características diagnósticas estão presentes em praticamente todos os gêneros e espécies da família.
Alguns representantes da família são utilizados comercialmente, sendo de maior importância econômica o gênero Coffea, que atualmente envolve cultivares de Coffea
arabica L., C. canephora Pierre ex A. Froehner e C. liberica W. Bull ex Hiern, originários da África e cultivados em regiões tropicais do mundo inteiro. A família também possui espécies produtoras de alcalóides, sendo uma das principais fontes de remédios naturais (e.g. Cinchona, Ladenbergia, Pogonopus, Uncaria), alucinógenos (e.g. Psychotria viridis Ruiz & Pav.) e venenos (e.g. Palicourea e Psychotria). Muitos gêneros arbóreos (e.g. Simira, Chimarrhis, Calycophyllum, Parachimarrhis, Capirona) são utilizados como fonte de madeira para a construção de móveis, casas e barcos, enquanto outros produzem frutos comestíveis, como o “jenipapo” (Genipa americana L.) e o “puruí” (Borojoa sorbilis (Ducke) Cuatrec.). Muitas espécies de Mussaenda, Pentas, Ixora e Gardenia, nativas da Ásia tropical, e de gêneros neotropicais como Bouvardia, Hamelia, Ixora, Manettia, Pogonopus, Randia, Rondeletia e Warszewiczia são cultivadas como ornamentais na América tropical (mais informações em Delprete 2004).
Apesar da família ser atualmente considerada um grupo monofilético, a classificação intrafamiliar das Rubiaceae ainda está em discussão. Robbrecht (1988) propôs uma classificação com quatro subfamílias (Rubioideae, Antirrheoideae, Ixoroideae e Cinchonoideae) e 44 tribos. Estudos filogenéticos utilizando dados moleculares (e.g. Bremer & Jansen 1991; Bremer & Eriksson 1992, 2009; Bremer et al. 1995; Bremer 1996; Bremer & Manen 2000; Rova et al. 2002) contrastaram com a classificação proposta por Robbrecht (1988), indicando que a família deveria ser dividida preferencialmente em três subfamílias: Rubioideae, Ixoroideae e Cinchonoideae. Em todos os estudos filogenéticos Rubioideae aparece como grupo monofilético e irmão das outras duas subfamílias. Apesar de rearranjos consideráveis estarem sendo propostos nos níveis de subfamília e tribo, a classificação de Robbrecht ainda é utilizada nos tratamentos florísticos em todo o mundo (Delprete 2004). Além dos estudos de filogenia molecular já citados, outros estudos que contribuíram para a sistemática da família são: Bremer (1987), Manen et al. (1994), Natali et al. (1995, 1996), Delprete (1996), Andersson & Rova (1999), Andreasen et al. (1999), Nepokroeff et al. (1999), Persson (2000), Delprete & Motley (2001), Delprete & Cortés (2004), Andersson & Antonelli (2005), Motley et al. (2005), Davis et al. (2007), Barrabé et al. (2012), Razafimandimbison et
al. (2014) e muitos outros envolvendo diferentes níveis taxonômicos, e aumentando consideravelmente o conhecimento a respeito da sistemática da família.
continuamente atualizada, de espécies brasileiras de criptógamas e fanerógamas, na qual a família Rubiaceae é coordenada por Maria Regina Barbosa e Daniela Cristina Zappi (Barbosa
et al. 2015).
2. Rudgea
O gênero Rudgea é exclusivamente neotropical, com ca. 130 espécies (Govaerts et al. 2015), distribuídas do México até o nordeste da Argentina, com dois principais centros de diversidade, um no Oeste da América do Sul (Peru, Equador, Colômbia) e outro no Sudeste do Brasil (Espírito Santo, Rio de Janeiro) (Zappi 2003). Os principais ambientes ocupados pelas espécies deste gênero são as florestas úmidas da Amazônia e da Mata Atlântica, porém diversos representantes ocorrem também em ambientes florestais associados ao Cerrado e à Caatinga, como matas de galeria, matas nebulares e florestas semi‐deciduais (Zappi 2003, 2006, 2007; Delprete et al. 2005a).
As espécies de Rudgea são caracterizadas pelas estípulas inteiras a fimbriadas com apêndices glandulares, folhas geralmente com domácias, inflorescência terminal, flores brancas, cremes ou amareladas, usualmente com lobos corniculados e pirênios adaxialmente sulcados (Zappi 2003, Bruniera et al. in press, Taylor et al. submitted). Além disso, de acordo com Robbrecht (1989) e Piesschaert (1999), Rudgea pode ser definido por seu padrão de fendas na pré‐germinação encontrado nos pirênios. O trabalho de Zappi (2003) confirmou que a presença de duas fendas longas basais e marginais e uma a três (até cinco) fendas longas basais abaxiais é um padrão constante encontrado nos representantes do gênero. As espécies de Rudgea podem ser confundidas com espécies dos gêneros Coussarea, Margaritopsis, Palicourea ou Psychotria, no entanto além das estípulas apendiculadas, não divididas de Rudgea, que é a característica mais utilizada para distinguir o gênero, outras características podem ser úteis na diferenciação, como os ramos mais lenhosos e menos ramificados e as flores, que são maiores, enquanto em Margaritopsis e
Psychotria os ramos são menos lenhosos e mais ramificados. Os frutos de Rudgea são consideravelmente maiores do que os encontrados em Psychotria e Palicourea. Além disso, diferentemente de Faramea e Coussarea, onde apenas um óvulo se desenvolve, os frutos de
semente, e sua ocorrência é correlacionada com o aumento no tamanho do fruto (Zappi 2003).
Segundo Zappi (2003), com a fragmentação das florestas da Serra do Mar (nos estados do Rio de Janeiro, São Paulo e Espírito Santo), as coletas de espécies de Rudgea são cada vez mais escassas já que os distúrbios provocados pela ação humana não favorecem plantas como espécies de Rudgea, que são lenhosas e com crescimento mais lento e com populações menores e com indivíduos mais esparsos do que outros gêneros de Rubiaceae, como Psychotria e Palicourea. Ao contrário de Rudgea, estes dois últimos gêneros parecem tornar‐se mais comuns em ambientes degradados.
Em relação ao seu posicionamento filogenético, Rudgea está inserida na subfamília Rubioideae, tribo Palicoureeae (Robbrecht & Manen 2006, Barrabé et al. 2012, Razafimandimbison et al. 2014). Nestes dois últimos trabalhos foi constatado também que Rudgea é filogeneticamente mais próximo do gênero neotropical Notopleura (Benth.) Bremek. em relação aos demais gêneros de Palicoureeae (e.g. Chassalia Comm. ex Poir.,
Geophila D. Don, Margaritopsis C. Wright, Palicourea Aubl. sensu lato). Apesar de vários trabalhos envolvendo filogenias com a família Rubiaceae terem sido publicados nas últimas décadas, como os citados anteriormente, ainda não havia sido realizado um estudo filogenético com o gênero Rudgea que tivesse incluído uma amostragem adequada deste gênero para inferir as relações entre as espécies e até mesmo o monofiletismo do gênero. Como Rudgea é um gênero com ca. 130 espécies, sua divisão em subgêneros ou seções foi avaliada neste trabalho, pois a subdivisão pode auxiliar na identificação das espécies e direcionar estudos mais aprofundados e monografias de partes do gênero.
Em relação aos trabalhos taxonômicos, a única revisão compreensiva das espécies de Rudgea no Brasil foi publicada por Mueller Argoviensis (1881), incluída na primeira parte das rubiáceas para a Flora Brasiliensis. Entre os principais estudos taxonômicos mais atuais com o gênero destacam‐se os de: Zappi & Nunes (2000) para o norte do Brasil, Zappi (2003) para o Sul e Sudeste do Brasil, Zappi & Steyermark (2004) para a Guiana Venezuelana, Delprete et
preparar uma sinopse do gênero para o Brasil, integrando os dados presentes na literatura e os dados inéditos do presente trabalho.
Com a análise cladística e o estudo taxonômico foi possível identificar prováveis sinapomorfias morfológicas que sustentem grupos monofiléticos dentro do gênero (aliados ao estudo de evolução de caracteres). Assim, filogenias moleculares aliadas à identificação de possíveis sinapomorfias morfológicas é de suma importância na delimitação do gênero e de grupos infragenéricos. Os estudos filogenéticos são de grande importância aos estudos taxonômicos, pois grupos bem delimitados direcionam e otimizam estes trabalhos, além de proporcionar classificações teoricamente mais estáveis. Por outro lado, um estudo filogenético é dependente do conhecimento taxonômico de um grupo, evidenciando que a abordagem taxonômica e filogenética são complementares.
3. Objetivos
Dadas as considerações expostas acima, essa Tese de Doutorado teve os seguintes objetivos:
1. Reconstruir a filogenia de Rudgea a partir de seqüências de DNA para investigar as relações entre as espécies do gênero e com os gêneros próximos;
2. Investigar o padrão de evolução de características morfológicas selecionadas ao longo da diversificação de Rudgea, testando se haveria suporte morfológico para grupos infragenéricos;
3. Produzir uma sinopse do gênero para o Brasil, incluindo a delimitação do número de espécies, chave de identificação, lista de sinônimos, distribuição geográfica, notas taxonômicas e ilustrações;
4. Promover o intercâmbio entre a doutoranda e pesquisadoras de Instituições estrangeiras, uma vez que o trabalho contou com a participação das especialistas em Rubiaceae, Dra. Charlotte Taylor (Missouri Botanical Garden, Saint‐Louis/EUA) e Dra. Daniela Zappi (Royal Botanic Gardens, Kew/Inglaterra), co‐orientadora da doutoranda.
4. Organização da Tese
Além da Introdução Geral, a Tese foi organizada em 4 capítulos, sendo que os Capítulos 3 e 4 são manuscritos de artigos científicos, resultantes do desenvolvimento desta tese. O capítulo 3 compreende a descrição de duas espécies novas de Rudgea para a Bahia, e é um manuscrito já aceito e em vias de ser publicado (Bruniera et al. in press) pela Revista
Phytotaxa. O Capítulo 4 compreende um artigo sobre transferência de nomes em Rudgea e Palicourea sensu lato. Este trabalho resultou da viagem da doutoranda ao Missouri Botanical Garden, que propociou discussões com a especialista Dra. Charlotte Taylor sobre a delimitação de espécies originalmente descritas em Rudgea ou em Psychotria subgênero
Heteropsychotria (hoje inserido em Palicourea sensu lato). Essas discussões unidas à colaboração da Dra. Daniela Zappi, co‐orientadora da doutoranda, resultaram na produção e envio de um artigo à Revista Kew Bulletin em 2014 (Taylor et al. submitted).1
Os Capítulos 1 e 2 compreendem os maiores resultados da tese, sendo que o Capítulo 1 apresenta os resultados filogenéticos baseados em dados moleculares, e também as análises de evolução de caracteres morfológicos dando suporte molecular e morfológico na delimitação do gênero Rudgea e de grupos infragenéricos. Este capítulo está previamente formatado para ser enviado à Revista Táxon. O capítulo 2 compreende um tratamento taxonômico no formato de uma sinopse para as 64 espécies aceitas de Rudgea para o Brasil. O tratamento inclui chave de identificação para as espécies e subespécies quando necessário, citação de tipos e sinônimos, designação de sinônimos novos e lectotipificações, dados de distribuição, habitat e fenologia, lista de materiais examinados e figuras com fotos e ilustrações. Este capítulo está formatado para ser enviado à Revista Phytotaxa.
Referências
Andersson, L. & Antonelli, A. 2005. Phylogeny of the tribe Cinchoneae (Rubiaceae), its position in Cinchonoideae, and description of a new genus, Ciliosemina. Taxon 54: 17‐‐ 28.
Andersson, L. & Rova, J.H.E. 1999. The rps‐16 intron and the phylogeny of the Rubioideae. Plant Syst. Evol. 214: 161‐‐186.
1As espécies e combinações novas encontradas nesta tese não são validamente publicadas. Estes nomes serão
Andreasen, K., Baldwin, B.G. & Bremer, B. 1999. Phylogenetic utility of the nuclear rDNA ITS region in subfamily Ixoroideae (Rubiaceae): comparison with cpDNA rbcL sequence data. Plant Syst. Evol. 217: 119‐‐135.
Anunciação, E.A. 1998. A família Rubiaceae Juss. na Serra da Juréia, São Paulo, Brasil. Dissertação de Mestrado. Universidade de São Paulo.
Bacigalupo, N.M. 1974. Rubiaceae. Pp. 3‐‐50 in: Burkart, A. (ed.), Flora Ilustrada de Entre Rios (Argentina). Buenos Aires: Instituto Nacional de Tecnología Agropecuaria.
Bacigalupo, N.M. 1993. Rubiaceae. Pp. 375‐‐437 in: Cabrera, A.L. (ed.), Flora de la provincia del Jujuy. Buenos Aires: Instituto Nacional de Tecnología Agropecuaria.
Backlund, A., Oxelman, B. & Bremer, B. 2000. Phylogenetic relationships within the Gentianales based on ndhF and rbcL sequences, with particular reference to the Loganiaceae. Amer. J. Bot. 87: 1029‐‐1043.
Baillon, H.E. 1880. Rubiacées‐Dipsacacées. Histoire Naturelle des Plantes, Vol. 7, p. 257‐503. L. Hachette et Cie., Paris, França.
Barbosa, M.R., Taylor, C.M., Cabral, E., Jardim, J.G., Pereira, M.S., Calió, M.F., Pessoa, M.C.R., Salas, R., Souza, E.B., Di Maio, F.R., Macias, L., Anunciação, E.A. da, Germano Filho, P., Oliveira, J.A., Bruniera, C.P., Gomes, M., De Toni, K., Firens, M., Zappi, D.C. 2015 (continuously updated). Lista de Espécies da Flora do Brasil: Rubiaceae. Jardim Botânico do Rio de Janeiro. http://floradobrasil.jbrj.gov.br/jabot/floradobrasil/FB210 (accessed 30 Nov. 2014)
Barrabé, L., Buerki, S., Mouly, A., Davis, A.P., Munzinger, J. & Maggia, L. 2012. Delimitation of the genus Margaritopsis (Rubiaceae) in the Asian, Australasian and Pacific region, based on molecular phylogenetic inference and morphology. Taxon 61(6): 1251‐‐1268. Barroso, G.M., Peixoto, A.L., Ichaso, C.L.F., Costa, G.C. & Guimarães, E.F. 1991. Rubiaceae.
Sistemática de Angiospermas do Brasil, vol. 3, p. 189‐228, figs. 711‐840. Universidade Federal de Viçosa, Imprensa Universitária, Viçosa, MG.
Bentham, G. & Hooker, J.D. 1873. Ordo LXXXIV. Rubiaceae. Pp. 7‐‐151 in: Bentham, G. & Hooker, J.D. (eds.), Genera Plantarum, London: Reeve & Co..
Boom, B.M. & Delprete, P.G. 2002. Rubiaceae. Pp. 606‐‐649 in: Angell, B., Cremers, G.A., Gracie, C.A., Granville, J.J., Heald, S.V., Hoff, M. & Mitchell, J.D. (eds.), Guide to the vascular plants of central French Guiana: part 2. Dicotyledons. Mem. New York Bot. Gard. 76(2): 1‐‐776.
Bremekamp, C.E.B. 1934. Notes on the Rubiaceae of Surinam. Recueil Trav. Bot. Néerl. 31: 248‐‐308.
Bremer, B. 1987. The sister group of the Paleotropical tribe Argostemmateae: A redefined Neotropical tribe Hamalieae (Rubiaceae, Rubioideae). Cladistics 2: 55‐‐71.
Bremer, B. 1996. Phylogenetic studies within Rubiaceae and relationships to other families based on molecular data. Opera Bot. Belg. 7: 33‐‐50.
Bremer, B. & Jansen, R.K. 1991. Comparative restriction site mapping of chloroplast DNA implies new phylogenetic relationships within the Rubiaceae. Am. J. Bot. 78: 198‐‐213. Bremer, B. & Eriksson, O. 1992. Evolution of fruit characters and dispersal modes in the
Bremer, B. & Manen, J.F. 2000. Phylogeny and classification of the subfamily Rubioideae (Rubiaceae). Plant Syst. Evol. 225: 43‐‐72.
Bremer, B. & Eriksson, O. 2009. Time Tree of Rubiaceae. Phylogeny and dating the family, subfamilies, and tribes. Int. J. Plant Sci. 170(6): 766‐‐793.
Bremer, B., Andreasen, K. & Olsson, D. 1995. Subfamilial and tribal relationships in the Rubiaceae based on rbcL sequence data. Ann. MO. Bot. Gard. 82: 383‐‐397.
Bruniera, C.P., Zappi, D.C. & Groppo, M. In press. Rudgea agresteophila and Rudgea hileiabaiana (Palicoureeae, Rubiaceae), two new species from Eastern Bahia, Brazil. Phytotaxa volume.
Burger, W.C. & Taylor, C.M. 1993. Rubiaceae. Fieldiana Bot. n.s. 33: 1‐‐333.
Cronquist, A.J. 1981. An Integrated System of Classification of Flowering Plants. New York: Columbia University Press.
Davis, A.P., Chester, M., Maurin, O. & Fay, M.F. 2007. Searching for the relatives of Coffea (Rubiaceae, Ixoroideae): the circumscription and phylogeny of Coffeeae based on plastid sequence data and morphology. Am. J. Bot. 94: 313‐‐329.
De Candolle, A.P. 1830. Rubiaceae. Pp. 341‐‐622 in: De Candolle, A.P. (ed.), Prodromus Systematis Naturalis Regni Vegetabilis. Paris: Treuttel & Würtz.
Delprete, P.G. 1996. Evaluation of the tribes Chiococceae, Condamineeae and Catesbaeeae (Rubiaceae) based on morphological characters. Opera Bot. Belg. 7: 165‐‐192.
Delprete, P.G. 1999. The status of monographic and floristic studies of Neotropical Rubiaceae, with emphasis on the Flora of the Guianas. Flora of the Guianas Newsletter 12: 11‐‐13.
Delprete, P.G. 2004. Rubiaceae. Pp. 328‐‐333 in: Smith, N., Mori, S.A., Henderson, A., Stevenson, D.W. & Heald, S.V. (eds.), Flowering Plants of the Neotropics. Princeton: Princeton University Press.
Delprete, P.G. 2010. Rubiaceae. Fl. Estados Goiás e Tocantins 40(1‐3): 1‐‐1610.
Delprete, P.G. & Motley, T.J. 2001. Molecular systematics of the Chiococceae‐Catesbaeeae complex (Rubiaceae): Flower and fruit evolution and systematic implications. Botany 2001 Abstracts, "Plants and People", Systematics Section, BSA / ASPT / IOPB, pt. 2, 438, 109‐‐110. Botanical Society of America. http://www.botany2001.org/
Delprete, P.G. & Cortés, R. 2004. A phylogenetic study of the tribe Sipaneeae (Rubiaceae, Ixoroideae), using trnL‐F and ITS sequence data. Taxon 53(2): 347‐‐356.
Delprete, P.G. & Jardim, J.G. 2012. Systematics, taxonomy and floristics of Brazilian Rubiaceae: an overview about the current status and future challenges. Rodriguésia 63(1): 101‐‐128.
Delprete, P.G., Smith, L.B. & Klein, R.M. 2004. Rubiaceae. Pp. 1‐‐344 in: Reitz, R. (ed.), Flora Ilustrada Catarinense. Itajaí, Brasil: Herbário "Barbosa Rodrigues".
Delprete, P.G., Schuster, T. & Hiepko, P. 2005b. An annotated translation of Karl Schumann’s (1888) “Über einige Verkannte oder Wenig Gekannte Geschlechter der Rubiaceen Südamerikas”. Bot. Jahrb. Syst. Pflanzengesch. Pflanzengeogr. 126(1): 3‐69.
Dillenburg, C.R. & Porto, M.L. 1985. Tribo Psychotrieae. Rubiaceae. Pp. 1‐‐76 in: Baptista, L.R.M. (coord.), Flora Ilustrada do Rio Grande do Sul. Porto Alegre, Rio Grande do Sul: Boletim do Instituto Central de Biociências.
Dwyer, J.D. 1980. Flora of Panama, part IX. Family 179. Rubiaceae ‐ part 1 and part 2. Ann. Missouri Bot. Gard. 67(1‐2): 1‐‐522.
Gomes, M. 1996. Rubiaceae. Pp. 345‐‐426 in: Lima, M.P.M. & Guedes‐Bruni, R.R. (eds.) Reserva Ecológica de Macaé de Cima, Nova Friburgo, Rio de Janeiro: aspectos florísticos das espécies vasculares. Rio de Janeiro: Jardim Botânico do Rio de Janeiro. Govaerts, R., Ruhsam, M., Andersson, L., Robbrecht, E., Bridson, D., Davis, A., Schanzer, I. &
Sonké, B. Continuosly updated. World Checklist of Rubiaceae. The Board of Trustees of the Royal Botanic Gardens, Kew. http://www.kew.org/wcsp/rubiaceae/ (accessed 16 Jan. 2015).
Heywood, V.H. 1979. Flowering Plants of the World. London: Oxford University Press. Pp. 257‐‐259.
Jung‐Mendaçolli, S.L. 1994. Flora Fanerogâmica da Reserva do Parque Estadual das Fontes do Ipiranga (São Paulo, Brasil), 155‐Rubiaceae. Hoehnea 21(1/2): 97‐‐129.
Jung‐Mendaçolli, S.L. 1999. Rubiaceae. Pp. 45‐‐136 in: Melo, M.M.R.F., Barros, F., Chiea, S.A.C., Kirizawa, M., Jung‐Mendaçolli, S.L. & Wanderley, M.G.L. (eds.), Flora Fanerogâmica da Ilha do Cardoso (São Paulo, Brasil), São Paulo: Instituto de Botânica. Jung‐Mendaçolli, S.L. 2007. Rubiaceae. Pp. 256‐‐460 in: Wanderley, M.G.L., Shepherd, G.J. &
Giulietti, A.M. (eds.), Flora Fanerogâmica do Estado de São Paulo. São Paulo: Editora Hucitec.
Krause, K. & Hoehne, F.C. 1922. Contribuição ao conhecimento das Rubiáceas do Brasil Meridional. Mem. Inst. Butantan 1(3): 1‐‐32.
Manen, J.‐F., Natali, A. & Ehrendorfer, F. 1994. Phylogeny of Rubiaceae‐Rubiae inferred from the sequence of a cpDNA intergene region. Plant Syst. Evol. 190(3‐4): 195‐‐211.
Motley, T.J., Wurdack, K.J. & Delprete, P.G. 2005. Molecular systematic of the Chiococceae‐ Catesbaeeae complex (Rubiaceae): flower and fruit evolution and biogeographic implications. Am. J. Bot. 92(2): 316‐‐329.
Mueller Argoviensis, J. 1881. Rubiaceae, tribus I. Retiniphylleae, tribus II. Guettardeae, tribus III. Chiococceae, tribus IV. Ixoroideae, tribus V. Coussareae, tribus VI. Psychotrieae. Pp. 1‐‐470 in: Martius, C.P.F., Eichler, A.G. & Urban, I. (eds.), Flora Brasiliensis. Leipzig, Alemanha: Fleischer.
Mueller Argoviensis, J. 1888. Rubiaceae. Pp 472‐‐486 in: Martius, C.P.F., Eichler, A.G. & Urban, I. (eds.), Flora Brasiliensis. Leipzig, Alemanha: Fleischer.
Natali, A., Manen, J.‐F., Kiehn, M. & Ehrendorfer, F. 1996. Tribal, generic and specific relationships in the Rubioideae‐Rubieae (Rubiaceae) based on sequence data of cpDNA intergene region. Opera Bot. Belg. 7: 193‐203.
Nepokroeff, M., Bremer, B. & Systma, K.J. 1999. Reorganization of the genus Psychotria and the tribe Psychotrieae (Rubiaceae) inferred from ITS and rbcL sequence data. Syst. Bot. 24(1): 5‐‐27.
Olmstead, R.G., Kim, K.‐J., Jansen, R.K. & Wagstaff, S.J. 2000. The phylogeny of the Asteridae sensu lato based on chloroplast ndhF gene sequences. Mol. Phylogenet. Evol. 16: 96‐‐ 112.
Persson, C.H. 2000. Phylogeny of Gardenieae (Rubiaceae) based on chloroplast DNA sequences from the rps16 intron and trnL(UAA)‐F(GAA) intergenic spacer. Nord. J. Bot. 20(3): 257‐‐270.
Piesschaert, F., Jansen, S., Huysmans, S., Smets, E. & Robbrecht, E. 1999. Chassalia petitiana (Rubiaceae ‐ Psychotrieae), an Overlooked Epiphytic Species Hidden in the African Canopy. Syst. Bot. 24(3): 315‐‐322.
Porto, M.L., Callegari Jacques, S.M., Sfoggia Miotto, S.T., Waechter, J.L. & Detoni, M.L. 1977. Tribo Spermacoceae. Rubiaceae I. Pp. 1‐‐114 in: Holmrich, M.H. (ed.), Flora Ilustrada do Rio Grande do Sul. Posto Alegre, RS: Série Botânica.
Razafimandimbison, S.G., Taylor, C.M., Wikström, N., Pailler, T., Khodabandeh, A. & Bremer, B. 2014. Phylogeny and generic limits in the sister tribes Psychotrieae and Palicoureeae (Rubiaceae): evolution of schizocarps in Psychotria and origins of bacterial leaf nodules of the Malagasy species. Am. J. Bot. 107(1): 1102‐‐1126.
Richard, A. 1830. Mémoire sur la famille des Rubiacées. Imprimerie de J. Tatsu. Paris 224 p. Robbrecht, E. 1988. Tropical woody Rubiaceae. Opera Bot. 1: 1‐‐271.
Robbrecht, E. 1989. Germination slits in Rubiaceae diaspores. Flora Males. Symp. [Leiden, August 1989], Progr. & Abstr.: 53.
Robbrecht, E. & Manen, J.‐F. 2006. The major evolutionary lineages of the coffee family (Rubiaceae, angiosperms). Combined analysis (nDNA and cpDNA) to infer the position of Coptosapelta and Luculia, and supertree construction based on rbcL, rps16, trnL‐ trnF and atpB‐rbcL data. A new classification in two subfamilies, Cinchonoideae and Rubioideae. Syst. Geogr. Plants 76: 85‐‐146.
Rova, J.H.E., Delprete, P.G., Andersson, L. & Albert, V.A. 2002. A trnL‐F cpDNA sequence study of the Condamineeae‐Rondoletieae‐Sipaneeae complex with implications on the phylogeny of the Rubiaceae. Am. J. Bot. 89: 145‐159.
Schumann, K.M. 1888a. Rubiaceae. Pp. 1‐‐124 in: Martius, C.F.P. (ed.), Flora Brasiliensis. Monachii & Lipsiae: F. Fleischer.
Schumann, K. 1888b. Über einige verkannte oder wening gekannte Geschlechter der Rubiaceen Südamerikas. Bot. Jahrb. Syst. Pflanzengesch. Pflanzengeogr. 10: 302‐‐363. Schumann, K. 1889. Rubiaceae [III]. Pp. 125‐‐442 in: Martius, C.F.P. von (ed.), Flora
Schumann, K.M. 1891. Rubiaceae. Pp. 1‐‐194 in: Engler, A. & Prantl, K. (eds.), Die Natürlichen Pflanzenfamilien. Leipzig: Engelmann.
Smith, L.B. & Downs, R.J. 1956. Resumo preliminar das Rubiáceas de Santa Catarina. Sellowia 7: 13‐‐86.
Soltis, D.E., Soltis, P.S., Chase, M.W., Mort, M.E., Albach, D.C., Zanis, M., Savolainen, V., Hahn, W.H., Hoot, S.B., Fay, M.F., Axtell, M., Swensen, S.M., Prince, L.M., Kress, W.J., Nixon, K.C. & Farris, J.S. 2000. Angiosperm phylogeny inferred from 18S rDNA, rbcL and atpB sequences. Bot. J. Linn. Soc. 133: 381‐‐461.
Standley, P.C. 1931a. The Rubiaceae of Bolivia. Publ. Field Mus. Nat. Hist., Bot. Ser. 7(3): 255‐ ‐339.
Standley, P.C. 1931b. Studies of American Plants‐V. Publ. Field Mus. Nat. Hist., Bot. Ser. 8(5): 295‐‐398.
Steyermark, J.A. 1965. Rubiaceae. Pp. 178‐‐285 in: Maguire, B. & Collaborators (eds.), The Botany of the Guayana Highland‐Part VI. Memoirs of the New York Botanical Garden. New York: NYBG Press.
Steyermark, J.A. 1967. Rubiaceae. In: B. Maguire & collaborators, The botany of the Guayana Highland—Part VII. Mem. New York Bot. Gard. 17(1): 230‐‐439.
Steyermark, J.A. 1972. Rubiaceae. Pp. 227‐‐832 in: Maguire, B. & Collaborators (eds.), The Botany of the Guayana Highland—Part IX. Memoirs of the New York Botanical Garden. Bronx: New York Botanical Garden Press.
Steyermark, J.A. 1974. Rubiaceae. Pp. 7‐‐2070 in: Lasser, T. (ed.), Flora de Venezuela. Caracas: Fondo Editorial Acta Científica Venezolana.
Sucre, B.D. 1959. Rubiaceae da cidade do Rio de Janeiro I: tribo Spermacoceae. Rodriguésia 33‐34: 241‐‐280.
Sucre, B.D. 1961. Flora do Estado da Guanabara, Rubiaceae II: tribo II – Cinchoneae – Arq. Jard. Bot. Rio J. 17: 25‐‐41.
Taylor, C.M. 1996. Overview of the Psychotrieae (Rubiaceae) in the Neotropics. Opera Bot. Belg. 7: 261‐‐270.
Taylor, C.M., Campos, M.T.V.A. & Zappi, D.C. 2007. Flora da Reserva Ducke, Amazonas, Brasil: Rubiaceae. Rodriguésia 58(1): 549‐‐616.
Taylor, C.M., Bruniera, C.P. & Zappi, D.C. (submitted). Taxonomic transfers in Neotropical Palicoureeae: new combinations in Rudgea and Palicourea. Kew Bull.
Vellozo, J.M.C. 1825 (1829). Florae fluminensis. Flumine Januario, Typographia Nationali. Vellozo, J.M.C. 1827 (1831). Florae fluminensis Icones. Parisiis, Lithog. Senefelder. Verdcourt, B. 1976. Rubiaceae (part 1). Pp. 1‐‐414 in: Polhill, R.M. (ed.), Flora of Tropical East
Africa, Rotterdam: A. A. Balkema.
Zappi, D.C. 2003. Revision of Rudgea (Rubiaceae) in Southeastern and Southern Brazil. Kew Bull. 58(3): 513‐‐596.
Zappi, D.C. 2006. Rudgea Salisb. Flora Ecuador 79: 74‐‐109.
Zappi, D.C. 2007. Rudgea Salisb. (Rubiaceae). Pp. 419‐‐429 in: Wanderley, M.G.L., Shepherd, G.J., Melhem, T.S. & Giulietti, A.M. (eds.), Flora Fanerogâmica do Estado São Paulo. São Paulo: Instituto de Botânica.
Zappi, D.C. & Stannard, B.L. 1995. Rubiaceae. in: Stannard, B.L. (ed.), Flora of the Pico das Almas – Chapada Diamantina, Bahia, Brazil. Royal Botanical Gardens, Kew.
Zappi, D.C. & Nunes, T.S. 2000. Notes on the Rubiaceae of Northeastern Brazil I. Erithalis, Psychotria and Rudgea. Kew Bull. 55(4): 655‐668.
Zappi, D.C. & Nunes, T.S. 2002. Lista preliminar da Família Rubiaceae na Região Nordeste do Brasil. Royal Botanic Gardens, Kew: Richmond.
Zappi, D.C. & Steyermark, J.A. 2004. Rudgea. Pp. 805‐‐816 in: Berry, P.E., Yatskievych, K. & Holst, B.K. (eds.), Flora of the Venezuelan Guayana 8 (Poaceae‐Rubiaceae). Saint Louis, Missouri, USA: Missouri Botanical Garden Press.
Zappi, D.C., Barbosa, M.R.V., Calió, M.F., Jardim, J.G., Pereira, M.S. & Souza, E.B. 2009. Rubiaceae. Pp. 449‐‐461 in: Stehmann, J.R., Forzza, R.C., Salino, A., Sobral, M., Costa, D.P. & Kamino, L.H.Y. (eds.), Plantas da Floresta Atlântica. Rio de Janeiro: Jardim Botânico do Rio de Janeiro.
Zappi, D.C., Calió, M.F. & Pirani, J.R. 2014. Flora da Serra do Cipó: Rubiaceae. Bol. Bot. Universidade de São Paulo 32(1): 71‐‐140.
CAPÍTULO 1
Rudgea coriacea
Delimitação de
Rudgea
Salisb. (Palicoureeae, Rubiaceae)
baseada em inferência filogenética a partir de dados
moleculares e em análises de evolução morfológica.
CAPÍTULO 1
Delimitation of Rudgea Salisb. (Palicoureeae, Rubiaceae) based in phylogenetic inference from molecular data and in morphological evolution analyses2.
Abstract
Systematics of Rubiaceae has undergone major changes during the last two decades. The use of molecular data has lead to a profound revision in the intra‐familiar classification, mainly at generic level. It has become clear that the relationships between some of the largest genera of Neotropical Rubiaceae (e.g. Psychotria, Palicourea and Rudgea) had to be investigated. The neotropical genus Rudgea encompasses c. 130 species distributed from Mexico to northeastern Argentina with two main centers of diversity, one in the western portion of South America and another in southeastern Brazil. Previous Rubiaceae phylogenies have included a limited sample of Rudgea species. The present study used sequences of plastidial rps16 intron, trnL‐trnF region and the nuclear ITS region to verify the monophyly of the genus and check for possible internal groupings. A total of 57 species of Rudgea and 85 species of other genera of Rubiaceae were analysed, with 268 new sequences produced. Individual and combined analyses were performed using PAUP 4.0b10 under the parsimony criterion and MrBayes 3.1.2 for Bayesian analysis. Results corroborate the circumscription of Psychotriae as a monogeneric tribe besides a Palicoureeae tribe comprising nine genera and also the recent generic classifications within Palicoureeae. The analyses have shown Rudgea as a monophyletic genus with the exclusion of R. woronovii Standl., a species more closely related to Palicourea sensu lato. On the other hand, R.
“ciliata” and “lanceifolia”, and two in clade 2, named as “coronata” and “cornifolia” groups. An infrageneric classification of Rudgea will be further proposed, aiming to facilitate the production of future monographs for this large and complex genus.
Keywords: Bayesian analysis, ITS, Notopleura, Palicourea, parsimony, Psychotria, Psychotrieae, rps16, Rubioideae, trnL‐trnF.
Resumo
A sistemática da família Rubiaceae passou por grandes mudanças nas últimas duas décadas. O uso de dados moleculares levou a revisões significantes na classificação intra‐familiar, principalmente em nível genérico. As relações entre alguns dos gêneros neotropicais mais diversos de Rubiaceae (e.g. Psychotria, Palicourea e Rudgea) devem ser investigadas. O gênero neotropical Rudgea possui ca. 130 espécies, distribuídas do México ao nordeste da Argentina, com dois centros de diversidade, um no noroeste da América do Sul, e outro no sudeste do Brasil. Trabalhos filogenéticos anteriores incluíram uma amostragem limitada de espécies do gênero Rudgea. O presente estudo utilizou sequências do íntron rps16, da
região trnL‐trnF e da região nuclear ITS para verificar a monofilia do gênero e a possibilidade da formação de grupos internos. No total, 57 espécies de Rudgea e 85 espécies de outros gêneros de Rubiaceae foram analisadas, com a produção de 268 novas sequências. Análises individuais e combinadas foram realizadas, utilizando PAUP 4.0b10 sob critério da parsimônia e MrBayes 3.1.2 para as análises bayesianas. Os resultados corroboram a circunscrição de Psychotrieae como uma tribo monogenérica, assim como a de Palicoureeae compreendendo nove gêneros, além das recentes classificações genéricas em Palicoureeae. As análises mostraram Rudgea como um gênero monofilético com a exclusão de R. woronovii Standl., uma espécie mais próxima de Palicourea sensu lato. Por outro lado, R. stipulacea (DC.) Steyerm. emergiu como grupo‐irmão das demais espécies de Rudgea, sendo o grupo formado por estas espécies altamente sustentado e denominado “Rudgea sensu