Bol Of Sanit Panam 96(Z). 1984
EVALUACION
DE POSIBLES METODOS INTERNACIONALES
DE REFERENCIA
PARA LA PRUEBA DE INHIBICION
DE LA
HEMAGLUTINACION
PARA LA RUBEOLA:
INFORME DE UN ESTUDIO EN COLABORACION’
M. Suggs,’ P. Brès,3 L. Huoang4 y 0. Sobeslavsky5
Existen varios procedimientos en todo el mundo para efec- tuar la prueba de la inhibición de la hemaglutinación (IH) para detectar anticuerpos de la rubéola en sueros humanos. En este artÉculo se presenta un proyecto internacional de in- vestigación patrocinado por la OMS para seleccionar uno de dichos procedimientos como método internacional de refe- rencia.
Introducción
La infección por el virus de la rubéola produce en los niños y adultos una enfer- medad benigna y autolimitada, caracteri- zada por leves síntomas en las vías respira- torias superiores, una erupción eritemato- sa y linfadenopatía suboccipital. En las mujeres jóvenes son muy frecuentes las complicaciones de artralgia y artritis, que
’ Se publica en inglés en el Bulletin of the Pan Ameticatr Health Organuatron, Vol. 17. No 3, 198S!Del documento del mismo título LAB182.1. Organización Mundial de la Salud, Ginebra. Suiza. 1982. Participaron en este estudio. además de lm autores indicados los siguientes investigadores: M. Badillet. Centro Nacional de Transfusión Sanguínea (Paris. Francia): C.M.P. Bradstreet, Centro Colaborador de Virus de la OMS (Londres. Inglaterra): W. K. Chang. Queen Mary Haspital (Hong Kong): N. E. Cremcr. Labora- torio de Enfermedades Víricas y Ricketsias. Departamento de Salud deCalifornia (Berkeley. California. EUA): 1. D. Gust. Faifield Hos- pital (Fairfield, Victoria, Asutralia): K. Henmann. Centros para el Control de Enfermedades (Atlanta, Georgia, EUA): Lam Sai Kit. Universidad de Malasia (Kurda Lumpur, Malasia): Reisaku Kono. Instituto Nacional de Salud (Toldo. Japón). y J. Strauss. Centro de Epidemiología y Microbiología (Praga. Checoslovaquia).
’ Centros para el Control de Enfermedades. Centro de Enfer- medades Infecciosas. Programa de Productos Biológicos. Atlanta. Georgia. EUA
’ Organización Mundial de la Salud. Servicio de Virosis. Gi- nebra. Suiza. Dirección actual, Instituto Pasteur. París. Francia.
’ Organización Mundial de la Salud. Senicio de Tecnolo@ de los Laboratorios de Salud. Ginebra.
5 Organización Mundial de la Salud. Enfermedades Vnles. Dirección actual: Instituto de Sueros y Vacunas. Praga. Chrcoslo- vaquia.
pueden presentarse después de desapare- cer la erupción. Son raras las complica- ciones graves. La infección del feto duran- te el primer trimestre del embarazo y, en menor medida, en el segundo y el tercero puede dar lugar a rubéola congénita, causa frecuente de malformaciones e inca- pacidades (1, 2).
Entre los diversos métodos serológicos para detectar o medir anticuerpos de la ru- beola, el que se ha usado y evaluado con mayor frecuencia ha sido la prueba de inhibición de la hemaglutinación (IH). Cuando se practica bien la prueba, la pre- sencia de anticuerpos observada guarda mucha correlación con la resistencia a la rubéola. Se puede utilizar la prueba para determinar qué individuos necesitan vacu- narse y qué mujeres embarazadas están ex- puestas a dar a luz a niños con rubéola congénita. Sin embargo, la prueba no dis- tingue entre el anticuerpo IgM y el IgG, por lo que para determinar si una prueba positiva responde a una infección reciente es necesaria una prueba del anticuerpo IgM.
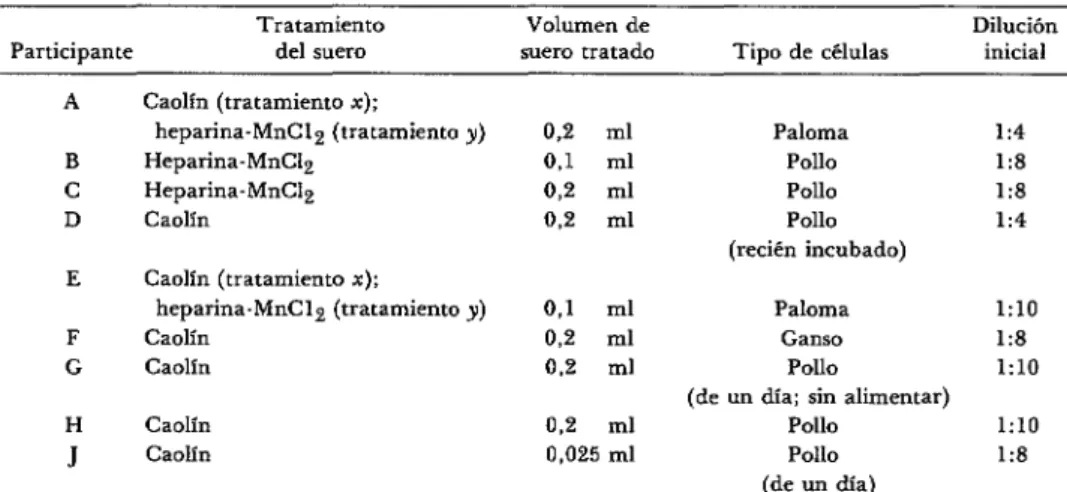
el procedimiento de IH. En EUA, han publicado procedimientos estandarizados de IH los Centros para el Control de Enfer- medades (CDC en la sigla inglesa) y el Co- mité Nacional de Normas para Laborato- rios Clínicos (4, 5). Sin embargo, la Orga- nización Mundial de la Salud (OMS) y va- rios grupos consultivos reconocieron en 1976 la necesidad de un método interna- cional de referencia de IH para la rubéola. Se diseñó un estudio en colaboración en el cual nueve participantes analizaron un grupo preseleccionado6 de especímenes co- dificados de suero humano con la técnica de IH empleada normalmente en sus res- pectivos laboratorios. Los participantes presentaron protocolos de las nueve técni- cas utilizadas, los cuales están archivados en los Servicios de Virosis y de Tecnología de los Laboratorios de Salud de la OMS.7 En el cuadro 1 se presentan las diferencias fundamentales entre estas nueve técnicas.
6 Un conjunto de sueros con diferentes grados de reactividad o diferentes títulos.
‘I Pueden solicitarse copias de estos pmtocolos. Una descripción detallada de la técnica seleccionada como método de referencia de la OMS se encuentra en el documento mimeografiado LAB/82.1 de la OMS, la cual puede obtenerse de la Organización Mundial de la Salud, 1211 Ginebra 27, Suiza.
Objetivos
El propósito del estudio fue seleccionar una prueba de inhibición de la hemagluti- nación para la rubéola que pudiera ser adoptada como método de referencia de la OMS. El método seleccionado debería ser el que diera los mejores resultados en las si- guientes mediciones practicadas en el estu- dio: a) precisión global (reproducibilidad global), b) precisión en el día (reproduci- bilidad en el día), c) especificidad y d) sen- sibilidad. Para los propósitos del estudio, estos términos y el término “reactividad” se definen de la manera siguiente:
1) Preczkión global del método es la des- viación estándar (DE) compuesta de todas las variaciones en los resultados menos la variación correspondiente al espécimen de que se trate.
2) Precz%n en el dúz del método es la DE compuesta de todas las variaciones en los resultados menos la variación cor-respon- diente al día y al espécimen de que se trate.
3) Reproducibilidad global es la propor- ción de especímenes distintos en los que un par de títulos, obtenidos en dos días dife- rentes, diferida como máximo por un fac- tor de dos. Esta reproducibilidad refleja el
CUADRO l-Los nueve procedimientos de IH para la rubéola según tratamiento del suero,
volumen del suero, tipo de células y diluch inicial.
Participante
Tratamiento del suero
Volumen de
suero tratado Tipo de células
Dilución inicial A
B C D E F G H
J
Caolín (tratamiento x):
heparina-MnC12 (tratamiento y) Heparina-MnC12
Heparina-MnC12 Caolín
Caolín (tratamiento x);
heparina-MnC12 (tratamiento y) Caolín
Caolín Caolín Caolín
0,2 ml Paloma 0,l ml Pollo
0,2 ml Pollo
0,2 ml Pollo (recién incubado) 0,l ml Paloma
0,2 ml Ganso
0,2 ml Pollo (de un día; sin alimentar)
0,2 ml Pollo
0,025 ml Pollo
(de un día)
1:4 1:8 1:8 1:4
Suggs et al. RUBEOLA 97
componente de la variación observable en un mismo día y el observable entre días di- ferentes.
4) Re@-oducibilidad en el día es la pro- porción de especímenes distintos en los que un par de títulos, obtenidos en la misma serie diaria de titulaciones, diferiría como máximo por un factor de dos. Esta repro- ducibilidad refleja solo el componente de la variación observable en un mismo día.
5) fipecz@dud es la proporción de es- pecímenes negativos que el método clasifi- ca correctamente como tales (índice de ne- gativos correctos).
6) Sensibilidad es la proporción de espe- címenes positivos que el método clasifica correctamente como tales (índice de positi- vos correctos).
7) Reactividad del método es la que está indicada por el factor de dilución del
antígeno. Por ejemplo, un método que re- quiera una dilución del antígeno de 1:8 (es decir, un factor de dilución de ocho) es menos reactivo que un método que re- quiera una dilución de 1:32 (es decir, un factor de dilución de 32).
Preparación y plan del estudio
Fase I
Cada uno de los nueve participantes uti- lizó el procedimiento de microtitulacion de IH para la rubéola empleado normalmen- te en su laboratorio respectivo para anali- zar de 80 a 100 especímenes (40-50 pares) de suero humano codificado al azar. Los análisis tenían que hacerse en tres días di- ferentes, con una semana de intervalo co- mo mínimo, con conjuntos diferentes de muestras de suero codificadas al azar y su- ministradas por los Centros para el Control de Enfermedades para cada uno de esos días. Además, se proporcionó a cada parti- cipante tres sueros testigo: uno de reacción negativa (<8), otro de reacción positiva y baja titulación (16-32) y otro de reacción
positiva y alta titulación ( 1128) y se le pi- dió que los incluyera con sus sueros testigo normales en cada serie de pruebas.
Se proporcionó a cada participante el mismo lote de antígeno CDC. Los 40-50 pares de especímenes de suero humano
codificados con doble anonimato
incluían: a) 8-10 pares de sueros que dieron resultados negativos ( < 8) en los CDC cuando se probaron para rubéola por IH y radioinmunovaloración (RIV), y b) 30-40 sueros positivos diferentes: 8-10 con titulaciones bajas (IH S-16), 2-4 con titulaciones elevadas (1256) y los restan- tes con titulaciones entre 32 y 128.
Los sueros negativos y de baja titula- ción fueron analizados por la técnica nor- malizada de los CDC para la IH y tam- bién por la técnica RIV del Dr. Olli Meurman, Departamento de Virología, Universidad de Turku, Turku, Finlandia.
Fase II
Todos los participantes aplicaron en la fase II los dos procedimientos que en la fase 1 habían obtenido el primero y el se- gundo lugar en cuanto a reproducibili- dad, especificidad y sensibilidad (los de los laboratorios B y J). Los especímenes eran los mismos de la fase 1, pero en la fa- se II se prepararon y utilizaron seis nuevos conjuntos codificados al azar (tres para cada procedimiento de prueba). Primero, se hicieron las pruebas en tres días distin- tos, con intervalos mínimos de una sema- na, por el procedimiento del laboratorio J (adsorción del suero con caolín). A conti- nuación, se repitieron las pruebas de la misma manera empleando el procedi- miento del laboratorio B (adsorción con heparina-cloruro de manganeso).
Se suministraron a los participantes los materiales siguientes:
ferencia comprendía un suero humano negativo (CS), otro de baja titulación (16- 32) y otro de alta titulación (>128).
3) Caolín, Fisher Scientific Company, lote 771130.
4) Heparina sódica (USP: United Sta- tes Pharmacopeia), 5 000 unidades/ml, Upjohn Company, lote 787FX.
5) Gelatina, BBL, lote J 1 DIOK. 6) Albúmina bovina en polvo, fracción V, Reheis Chemical Company, número de control S 12506, número de almacén 2293-01.
7) HEPES,O ICN, lote 0697.
8) MnCl,.4H,O, Fisher Scientific Com- pany, lote 775323.
9) Cianmetahemoglobina, Hycel Re-
agents No 116, lote 6349A 1, patrón No 117, lote 6819A 1.
Los materiales 5 y 9 se suministraron a un solo laboratorio . . . . por problemas de ad- qumclon.
Fase III
Los nueve participantes aplicaron para la prueba de IH el procedimiento B (tra- tamiento del suero con heparina-cloruro de manganeso) empleado en la fase II a tres conjuntos de 49 pares de especímenes codificados de suero con intervalos mínimos de una semana. A continuación, los participantes aplicaron el procedi- miento J (tratamiento del suero con caolín) con las mismas modalidades que en la fase II. El único material suministra- do a los participantes fueron los seis con- juntos de muestras de suero codificadas y
los tres sueros testigo de referencia de los CDC.
Grupos de sueros
Las muestras de suero humano codifi- cados con doble anonimato, con las que
* HEPES= N-Z-hidroxietilpiparazina-N-2.ácido etanmulfónico.
se constituyó cada grupo, procedían de donantes únicos y no se mezclaron. Los donantes eran hombres y mujeres adultos de 19 a 55 años de edad. Se agregó al suero azida sódica (O,loJ,) como agente conservador y se almacenaron los sueros a
4 oc.
Se practicaron pruebas de esterilidad con el primero y el último tubo de ensayo colocando 0,5 ml del suero sobre dos pla- cas de agar sangre y en un tubo con caldo de tioglicolato. Una placa se incubó a 23 OC y la segunda placa, así como el cal- do de cultivo, a 37 OC, todo ello durante
72 horas. Todos los resultados fueron ne- gativos. En todos los especímenes se exa- minó la presencia del antígeno superficial de la hepatitis B mediante la técnica de RIV para HB,Ag en el Laboratorio de la Hepatitis de los CDC en Phoenix, Arizo- na. El único espécimen que resultó positi- vo fue retirado del estudio. En dos labora- torios de los CDC se hicieron pruebas pre- liminares de todas las muestras de suero utilizadas en las tres fases, para las que se empleó el método normalizado de inhibi- ción de la hemaglutinación de los CDC en el que se usa heparina-MnCl, para tratar el suero (4).
Los especímenes de suero usados en las fases II y III del estudio fueron también analizados en dos laboratorios de los CDC por los procedimientos J y B.
Después de determinar los títulos de los sueros, se analizaron de nuevo por el mé- todo de RIV del Dr. Meurman todos los especímenes negativos (<8) y los positivos de baja titulación (16-32). Todos los especímenes se distribuyeron en cantida- des de 0,5 ml en frascos estériles de vidrio de 2 ml, cerrados con tapones de caucho blanco y cubiertos con tapas de aluminio.
Suggs et al. RUBEOLA 99
En las fases 1 y II se usó el mismo grupo de sueros, pero codificado en forma dife- rente. En la fase III se utilizó un segundo grupo.
Resultados
Fase I
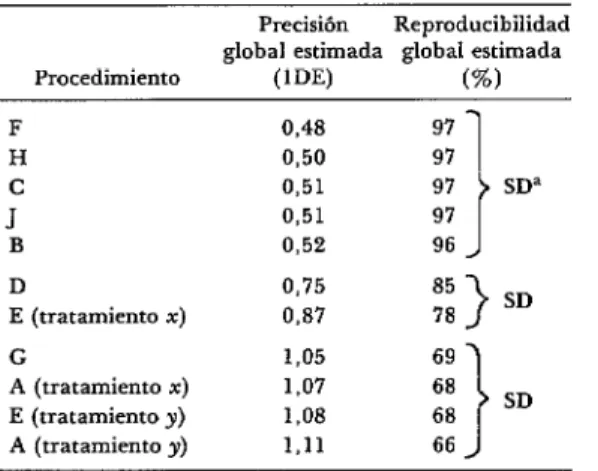
El cuadro 2 presenta un resumen de los resultados obtenidos en la fase 1. Los pro- cedimientos se clasificaron de acuerdo con su precisión global (cuadro 3) y su precisión en el día (cuadro 4), y se aplicó la prueba F para determinar si las dife- rencias observadas entre los diferentes va- lores de precisión y de reproducibilidad de los distintos procedimientos eran signi- ficativas al 5%. Como se señala en los cuadros, los procedimientos F, H, C, J y B tuvieron valores similares de precisión glo- bal (y, por lo tanto, de reproducibilidad global). Lo mismo fue válido para los pro- cedimientos D y E (tratamiento x) y para G, A y E (tratamiento y). Sin embargo, G, A y E (tratamiento y) tuvieron valores de precisión global significativamente infe- riores que F, H, C, J y B.
Los procedimientos F, H, E, B, J, C y G tuvieron valores similares de precisión en el día (y de reproducibilidad en el día). Lo mismo cabe decir de H, E, B, J, C, G y D. Sin embargo, el procedimiento D tuvo valores de precisión en el día significativa- mente menores que F.
Se facilitaron a los nueve participantes los resultados de los cuadros 2, 3 y 4 y se les pidió que ordenasen por rangos los procedimientos codificados. En cada ca- so, se asignó el número 1 al procedimien- to que obtuviera el primer lugar y así su- cesivamente por orden de posición, Si un participante consideraba equivalentes va- rios procedimientos, se asignaba a todos ellos el mismo rango. Cuando se sumaron los números correspondientes a los distin-
tos rangos asignados, se consideró el me- jor el procedimiento con menor puntaje, y así por orden descendente hasta el que tuviera el máximo puntaje.
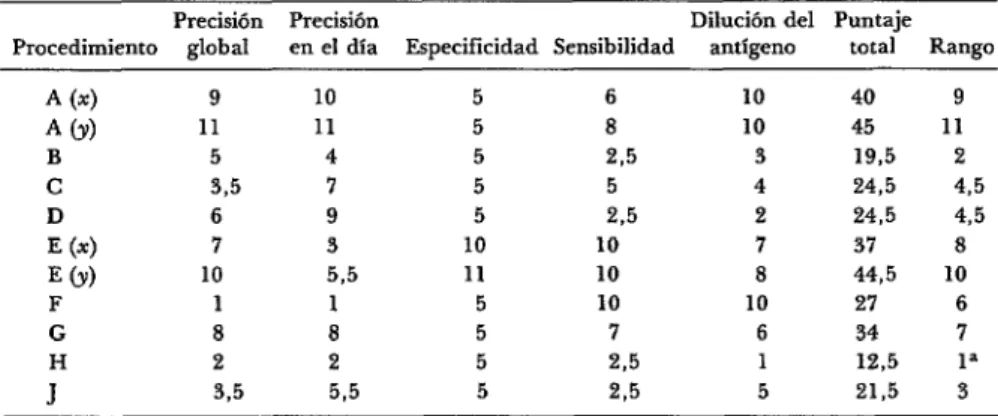
Los cuatro mejores procedimientos de IH para la rubéola seleccionados por los participantes fueron: B, H, J y C (cuadro 5). Cuando se ordenaron los procedimien- tos según los resultados de los análisis estadísticos (cuadro 6), los mismos cuatro procedimientos ocuparon los cuatro pri- meros lugares. En dos de las cuatro técni- cas se empleó caolín para el tratamiento del suero y en las otras dos se usó
heparina-MnClz. Basándose en estos
hallazgos, los participantes eligieron para las Fases II y III los procedimientos B y J.
Fase II
En la fase II del estudio, cada uno de los nueve laboratorios analizó seis conjun- tos de los mismos sueros, codificados con doble anonimato, tres por el procedi- miento B (heparina-MnCls) y tres por el procedimiento J (caolín). A los seis con- juntos se habían asignado códigos aleato- rios diferentes. Antes de iniciar las pruebas con el procedimiento J se termi- naron todas las pruebas hechas con el procedimiento B. La finalidad era selec- cionar el método mejor en las categon’as de precisión (reproducibilidad), especifici- dad, sensibilidad y dilución del antígeno.
El cuadro 7 presenta por laboratorios los resultados obtenidos para cada proce- dimiento en cuanto a precisión y reprodu- cibilidad. Los procedimientos de la heparina-MnClz y del caolín no presenta- ron diferencias significativas en sus valo- res de precisión y reproducibilidad global o en el día de acuerdo con la prueba de Wilcoxon, p> 0,05.
Suggs et al. RUBEOLA 101
CUADRO 3-Valores de precisión y reproducibi. CUADRO 4-Valores de precisión y reproducibi-
lidad globales. lidad en el día.
Precisión Reproducibilidad global estimada global estimada
Procedimiento (1W (%)
F 0,48 97
H 0,50 97
T 0,51 0,51 97 97
B 0,52 96
1 SDa
D 0,75 85
E (tratamiento x) 0.87 78 ) SD
G 1.05
A (tratamiento x) 1.07 E (tratamiento y) 1,08 A (tratamiento y) 1.11
’ SD: Sin diferencias significativas.
también por la prueba de Wilcoxon, (heparina-MnCls) resultó significativa- mente más específico que el del procedi- miento J utilizando caolín (p<O,O5). No se observaron diferencias significativas de sensibilidad.
El cuadro 9 presenta los factores de di- lución del antígeno utilizado por cada la- boratorio. No se observaron diferencias significativas de reactividad global entre los dos procedimientos asociadas con dichos factores de dilución.
Procedimiento
Precisión en Reproducibilidad el día estimada en el día WW estimada (%)
F 039 99
H 0.44 98
E (tratamiento x) 0,46 98
B 0,49 97
E (tratamiento y) 0,50 97
J 0,50 97
C 0,51 97
G 0,53 96
* SDa
D 0.57
A (tratamiento x) 0,85 A (tratamiento y) 0.96
’ SD: Sin diferencias significativas.
Fase III
La selección de un procedimiento de referencia de IH para la rubéola no debe depender de que cada laboratorio emplee los mismos reactivos. El propósito de la fa- se III del estudio era determinar qué pro- cedimiento, el J o el B, era el que daba re- sultados más uniformes entre los distintos laboratorios y en un mismo laboratorio cuando cada uno de estos utilizaba sus propios reactivos.
CUADRO 5-Puntajes asignados de los diferentes procedimientos por participantes basados en los
datos presentados en los cuadros 2,3 y 4 y en la ordenación por rango de los cinco procedimientos de mayor rango.
Procedi- EUA
dimiento Japón (Califomia)Francia
B 1
Y 1 1
C 1
F 1
D E (~1 G A (x) A 0 E Q
2 2
1 1
4 4
3 5
6 3
5 6
10 7
7 8
8 9
9 10
ll ll
EUA Checoslo- Hong Puntaje
WC) vaquia Malasia Kong Inglaterra Australia total Rango
2 2 4 1 1 3 18 1
3 1 5 5= 1 1 19 2
1 3 3 2 1 2 21 3
4 4 2 3 1 4 27 4
7 5 1 4 1 5 33 5
5 6 7 6
7 6 7
6 8 8 9
10 10 8
ll ll 10
9 9 ll
CUADRO 6-Puntajes numéricos y rango de los procedimientos de IH para la rubéola según los resultados de anhlisis estadísticos de los datos presentados en los cuadros 2,
3 y 4.
Precisión Precisión Dilución del Puntaje Procedimiento global en el día Especificidad Sensibilidad antígeno total Rango
A (4 A 0 B C D E (4 E 01) F G
J”
9 10 5 6 10 40 9
ll ll 5 8 10 45 ll
5 4 5 25 3 19,5 2
3,5 7 5 5 4 24,5 4.5
6 9 5 25 2 24,5 4,5
7 3 10 10 7 37 8
10 5,5 ll 10 8 44,5 10
1 1 5 10 10 27 6
8 8 5 7 6 34 7
2 2 5 2.5 1 12,5 1=
3,5 5,5 5 25 5 21,5 3
a No se siguió el protocolo para la fase 1.
Se empleó para el estudio un grupo de 12 especímenes de suero negativos y 37 positivos. Cada uno de los nueve laborato- rios analizó seis conjuntos, codificados con doble anonimato, de los mismos sueros: tres por el procedimiento B y otros tres por el procedimiento J (siempre un conjunto por día en tres días espaciados). Los seis conjuntos tenían códigos aleato- rios diferentes y no se iniciaron las pruebas con el procedimiento J hasta te-
ner terminadas y notificadas todas las pruebas con el procedimiento B.
Los datos sobre precisión y reproduci- bilidad de cada procedimiento obtenidos por los nueve laboratorios figuran en el cuadro 10. No hubo diferencias significa- tivas entre los dos procedimientos en los valores de precisión y reproducibilidad global o en el día, de acuerdo con la prueba de Wilcoxon.
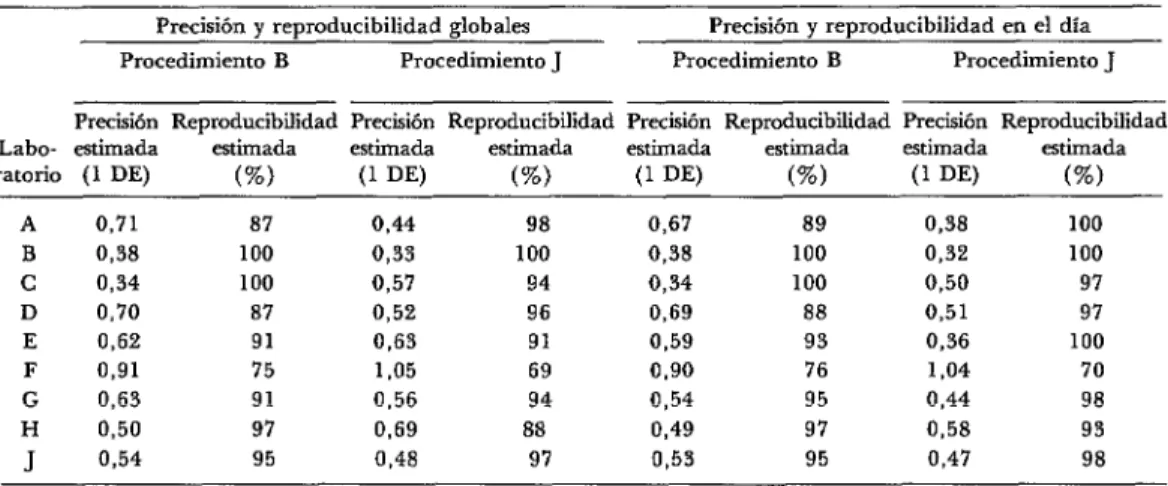
El cuadro ll presenta por laboratorios
CUADRO 7-Precisión y reproducibilidad obtenidas por los nueve laboratorios participantes median-
te los procedimientos B y J para la prueba de IH. Fase II.
Precisión y reproducibilidad globales Precisión y reproducibilidad en el día Procedimiento B Procedimiento J Procedimiento B Procedimiento J (heparina-MnCl& (caolín) (heparina-MnCle (caolín) Precisión Reproducibilidad Precisión Reproducibilidad Precisión Reproducibilidad Precisión Reproducibilidad Labe- estimada estimada estimada estimada estimada estimada estimada estimada
ratorio (1 DE) (%) (1 DE) (%) (1 DE) (%) (1 DE) (%)
C 0,44 98
F 0,46 98
D 0.52 96
J
0,56 94E 0,62 91
H 0,63 91
G 0,65 90
B 0,69 88
A 0,69 88
0,37 100
0,48 97
0,58 93
0,49 97
0,39 99
0,98 72
0,66 89
0,72 86
- -
0.43 99
0,39 99
0.46 98
0,52 96
0,56 94
0,59 93
0,60 92
0,61 92
0,59 93
OS5 100
0,45 98
0.54 95
0,41 99
0,38 100
0.98 72
0.64 90
0,64 90
Suggs et al. RUBEOLA 103
CUADRO 8-Especificidad y sensibilidad obtenidas por los nueve laboratorios
participantes mediante los procedimientos B y J para la prueba de IH. Fase ll.
Especificidad (%) Sensibilidad (%)b Procedimiento B Procedimiento J Procedimiento B Procedimiento J Laboratorio (heparina-MnQ) (caolín) (heparina-MnC&) (caolín)
C 100 98 100 100
F 100 98 100 99
D 100 36 100 100
J 100 98 100 100
E 100 98 100 100
H 77 77 100 98
G 100 89 99 95
B c c
A c c
a Basado en 11 especímenes negativos (comprobados por un laboratorio independiente). b Basado en 37 especímenes positivos.
’ No se pudo estimar porque apareció en los datos “16” (recíproca de la dilución del suero demasiado baja para el análisis estadístico).
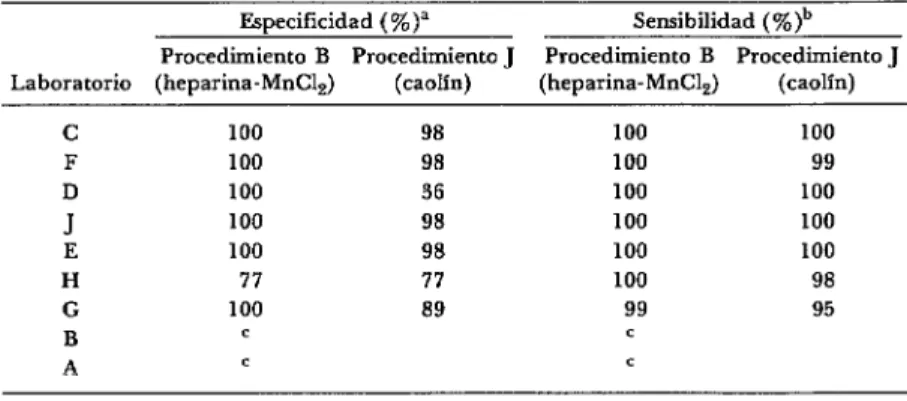
los resultados de sensibilidad y especifici- dad de cada procedimiento. Las diferen- cias observadas entre los dos procedimien- tos no fueron estadísticamente significati- vas.
El cuadro 12 presenta los factores de di- lución del antígeno empleados por cada laboratorio. Estos factores diferían en solo cuatro de los nueve laboratorios: sin em- bargo, en los cuatro se observó que el pro- cedimiento con caolín (procedimiento J) era más reactivo que el procedimiento con heparina-MnC& (procedimiento B).
CUADRO g-factores de dilucih del antígeno
utilizados por los nueve participantes durante la
fase ll del ensayo de los procedimientos B y J.
Procedimiento B Procedimiento J Laboratorio (heparina-kW&) (caolín)
40 32 64. 64,
128 64 64 32 256 128
64 32
128 64
256 16 64 32 256 -
Conclusiones
Se utilizaron cuatro medidas de rendi- miento en las pruebas para recomendar, un procedimiento de referencia de IH: sensibilidad, especificidad, reactividad y reproducibilidad.
Los datos sobre la sensibilidad observa- da en las fases II y III figuran en los cuadros 8 y ll. Para el procedimiento B (heparina-MnCl,), se registraron valores de la sensibilidad muy elevados; en las 15 series de resultados, el valor más bajo fue del 96,3% y en 10 de ellas la sensibilidad fue del 100%. Ello demuestra que este procedimiento dio lugar a muy pocos fal- sos negativos. Lo mismo cabe decir del procedimiento J (utilizando caolín), con el que el valor más bajo fue de 95,0% y en 12 de las 16 series de resultados la sensibi- lidad fue del 100%.
CUADRO IO-Precisión y reproducibilidad obtenidas utilizando los procedimientos B y J. Fase III.
Precisión y reproducibilidad globales Precisión y reproducibilidad en el día Procedimiento B Procedimiento J Procedimiento B Procedimiento J
Precisión Reproducibilidad Precisión Reproducibilidad Precisión Reproducibiidad Precisión Reproducibiiidad Labe- estimada estimada estimada estimada estimada estimada estimada estimada
ratorio (1 DE) (%) (1 DE) (%) (1 DE) (%) (1 DE) (%)
A 0,71 87 0,44 98 0,67 89 0,38 100
B 0,38 100 0,33 100 0,38 100 0,32 100
C 0,34 100 0,57 94 0,34 100 0.50 97
D 0.70 87 0,52 96 0,69 88 0,51 97
E 0,62 91 0,63 91 0,59 93 0,36 100
F 0,91 75 1.05 69 0.90 76 1,04 70
G 0,63 91 0.56 94 0,54 95 0,44 98
H 0,50 97 0,69 88 0,49 97 0,58 93
J 0,54 95 0,48 97 0,53 95 0,47 98
un numero excesivo de falsos positivos. Lo mismo es válido para el procedimiento H, ya que ocho de las 16 series indicaron una especificidad superior al 980J0, pero los va- lores más bajos fueron de 77, 46 y 36Q/,, lo que indica que de nuevo hubo un proble- ma con los falsos positivos.
Los cuadros 7 y 10 contienen los resul- tados de reproducibilidad global obteni- dos de las fases II y III. Con el procedi- miento B, aunque en siete de las 18 series de resultados la reproducibilidad fue de 95% o más, en cinco fue menor de 90%.
Eso quiere decir que este procedimiento es susceptible de variaciones importantes en los resultados de ciertos laboratorios. La misma conclusión es aplicable al proce- dimiento J. en el que ocho de las 17 series dieron una reproducibilidad de 95% o mas, y cinco no llegaron a 90%. Sin embar- go, debe señalarse que dos de los laborato- rios en los que el procedimiento J presentó poca reproducibilidad fueron distintos de aquellos en los que se registró escasa repro- ducibihdad en el procedimiento B.
Como la diferencia observada entre los
CUADRO ll-Especificidad y sensibilidad obtenidas utilizando los procedi-
mientos B y J. Fase III.
Especificidad (%) Sensibilidad ( %)b Laboratorio Procedimiento B Procedimiento J Procedimiento B Procedimiento J
A 98.6 98,6 99,5 100.0
B 100,o 100,o 100,o 100.0
C 100.0 98,6 100,o 100.0
D 90,3 100.0 100,o 100.0
E 98,6 100,o 99,5 100,o
F 41,8 45,8 99,5 100,o
G 98,6 100,o 96,3 100,o
H c 98,6 c 100.0
J 98.6 98,6 100,o 99,5
1 Basado en 12 espeámenes negativos (comprobados por un laboratorio independiente). Basado en 37 especímenes positivos.
Suggs et al. RUBEOLA 105
CUADRO 12-Factores de dilución del antígeno
utilizados durante la fase III del ensayo de los pro- cedimientos B y J.
Factores de dilución del antígeno
Laboratorio Procedimiento B Procedimiento J
A 64 64
B 32 32
C 64 64
D 16 16
E 16, 25, 32 32, 16, 32
F 32 64, 32, 45
G 8 64, 64, 128
H 80 80
J 32, 32, 64 64
dos procedimientos no fue significativa, pero era necesario designar tan solo un procedimiento de referencia, la OMS escribió a los participantes en este estudio pidiéndoles que seleccionaran uno de los dos para recomendarlo como el procedi- miento de referencia de IH para la rubéo- la de la OMS. Cinco de los nueve partici- pantes eligieron el procedimiento B (heparina-MnCl,), el cual es por consi- guiente el procedimiento recomendado.
Resumen
Son varios los procedimientos que se utilizan en el mundo para la prueba de la inhibición de la hemaglutinación (IH) pa- ra detectar anticuerpos de la rubéola en sueros humanos con objeto de determinar cuáles son las personas que necesitan va-
cunarse así como las mujeres embaraza- das con riesgo de dar a luz niños con rubé- ola congénita. Tomando en cuenta la ne- cesidad de contar con un solo método in- ternacional de referencia de IH para la rubéola, la Organización Mundial de la Salud patrocinó un estudio en colabora- ción en el cual nueve laboratorios de ocho países analizaron varios procedimientos.
Las pruebas preliminares indicaron que cuatro procedimientos eran mejores en términos de su sensibilidad, especifíci- dad, reactividad y reproducibilidad, y los participantes principales en los nueve la- boratorios seleccionaron dos de ellos para realizar pruebas ulteriores. Estos indica- ron que ambos métodos eran muy sen- sibles, dando lugar a pocos falsos negati- vos; que los dos eran altamente específicos (pocos falsos positivos), si bien en ciertos laboratorios participantes hubo un núme- ro excesivo de falsos positivos, y que en al- gunos laboratorios, pero no en otros, se registraron valores de precisión y repro- ducibilidad muy elevados.
En general, no se observaron diferen- cias significativas entre los dos procedi- mientos, por lo que se pidió a los nueve participantes en el estudio que selecciona- ran el método de su preferencia. Los par- ticipantes seleccionaron el procedimiento en el que se empleaba heparina-MnCl, para tratar los sueros. Una descripción detallada de este método de referencia puede solicitarse a la Organización Mun-
dial de la Salud. n
REFERENCIAS
1. Lennette, E. H., Spaulding, E. A. y Truant, J. P. A Procedural Guide to the Perfkmance of
eds. Manual of Clinical Microbiology. 2 ed. Rubella Hemagglutination-Inhibition Tests.
Washington, D.C., Ameritan Society for Atlanta, Georgia, Centers for Disease Control,
Microbiology, 1974. 1977. (Immunology Series ND 2, revised.)
2. Gregg, N. M. Congenital cataract following 5. Estados Unidos de América. National Committee
German measles in the mother. Trans for Cliical Laboratory Standards (NCCLS).
Ophthalmol Soc Aust 335-46, 1931. Approued Standard: ASM-5-Standard for
3. Stewart, G. L. et al. Rubella-virus hemag- Rubella Hemmagglutination (HAI) Reagent
glutination inhibition test. NEnglJMed 176:554- Speczfications and for a Rubella HAI Referente
557, 1967. Method.
Evaluation of candidate international referente methods for the rubella hemagglutination inhibition test:
Report of a collaboratíve study (Summary)
Various rubella hemagglutination-inhibition (HI) test procedures are used around the world to detect rubella antibodies in human sera-in order to determine which individuals need vaccination and which pregnant women are at risk of giving birth to an infant with congenital rubella. In view of the need to have a single intemational rubella HI referente method, the World Health Organization sponsored a collaborative study involving the testing of various procedures by nine laboratories in eight countries.
The initial tests singled out four procedures as being superior in terms of their sensitivity, specificity, reactivity, and reproducibility, and the chief participants at the nine laboratories selected two of these for further testing. This
subsequent testing indicated that both methods were very sensitive, yielding few false negative results; that both showed a high degree of specificity (few false positive results), though some of the participating laboratories did have problems with false positive readings; and that high levels of precision and reproducibility were attained in some laboratories but not in others.
Overall, the observed differences between the two procedures were not signilicant. The nine study participants were therefore asked to select which of the two methods they preferred, and they accordingly selected the one employing heparin-manganous chloride to treat the sera. A detailed description of this referente method is available from the World Health Organization upon request .
Avalia@io de métodos internacionais de referência projetados para o teste de inibi@o da hemaglutina#io nos casos de rubéola:
Relatório de um estudo feito em colabora@o (Resumo)
Há vários testes de inibicáo da hemaglutinacão (IH) nos casos de rubéola que são empregados no mundo inteiro para detectar anticorpos de rubéola nos soros dos seres humanos com o fim de determinar quais individuos necessitam da vacinacáo e quais as mulheres grávidas que correm o risco de dar à luz a um bebé que sofra de rubéola congênita. Levando em consideracáo a necessidade de ter um único método de referéncia internacional de IH nos casos de rubéola, a Organizacáo Mundial da Saúde patrocinou um estudo em colaboracão que incluiu os métodos de testes adotados por nove laboratórios em oito países diferentes.
Os testes iniciais particularizaram quatro métodos como sendo superiores no referente à sensitividade, especificidade, reatividade e reprodutibilidade. Os participantes principais nesses testes feitos nos nove laboratórios escolheram dois deles para serem testados
adicionalmente. Esse testado subseqüente indicou que os dois métodos eram muito sensíveis, que produziam poucos resultados negativos falsos; que ambos possuiam alto grau de especificidade (poucos resultados positivos falsos) embora alguns dos laboratórios participantes tivessem tido problemas com a leitura de positivos falsos; e que em alguns laboratórios, nao em todos, atingiram-se altos níveis de precisa0 e reprodutibilidade.
Suggs et al. RUBEOLA 107 Evaluation de méthodes internationales de référence pour I’épreuve
d’inhibition d’hémagglutination pour la rubéole: Rapport d’une étude faite en collaboration (Résumé)
Diverses méthodes sont utilisées dans le monde pour l’épreuve de l’inhibition d’hémagglutination (IH) pour détecter les anticorps de la rubéole dans les sérums humains. Il s’agit par 12 de déterminer quelles sont les personnes qu’il est indispensable de vacciner, comme te1 est le cas des femmes enceintes qui courent le risque de donner naissance 2 des enfants atteints de rubéola congénitale. En raison de la nécessité de disposer d’une seule méthode intemationale de référence de I’IH pour la rubéola, l’organisation mondiale de la Santé a chargé neuf laboratoires de huit pays différents d’effectuer en collaboration une étude ayant pour objet d’analyser les divers procédés employés.
D’apres les épreuves préliminaires, quatre des méthodes utilisées se sont révélées être les meilleures sous les aspects sensibilité, spécificité et reproductibilité, et les principaux chercheurs
des neuf laboratoires en ont retenu deux en vue des épreuves ultérieures. Ces dernières ont prouvé que les deux méthodes étaient également sensibles, ne donnant lieu qu’à tres peu de faux négatifs; qu’elles étaient hautement spécifiques (peu de faux positifs), bien que dans certains laboratoires se soit produit un nombre excessif de faux positifs et que dans quelques uns, mais non dans d’autres, des valeurs de précision et de reproductibilité tres élevées ont été relevées.