CALOR Y DE ENVOLTURA EXTERNA ’
J. A. Zeigler, R. H. Jones y K. Kubica *
Se evaluó la utilidad, como vacuna, de dos preparaciones an- tigénicas de leptospiras. Las suspensiones de células enteras sometidas a calentamiento demostraron ser muy eficaces para proteger a los cricetos contra la leptuspirosis experimental.
Introducción
Se considera que la leptospirosis es la zoonosis más importante en Barbados. Aproximadamente el 30% de los SS casos clínicos registrados en 1970 y 1971 fueron terminales (1) . Estudios serológicos pos- teriores revelaron niveles significativos de aglutinación sérica respecto a las leptospiras del serogrupo Autumnalis en un porcentaje muy elevado de los bovinos estudiados (2). Los cultivos de ,tejido renal extraído de roe- dores salvajes capturados produjeron cepas de Leptospira de los serogrupos Icterohae- morrhagiae, Ballum, Canicola y Autumnalis
(incluida en esta última una cepa que se clasificó serológicamente como fort-bragg
(I-3).
La investigación que se describe a con- tinuación 3 se emprendió respondiendo al problema de la leptospirosis en Barbados. Primeramente fue preciso elaborar un pro- totipo de vacuna eficaz utilizando cepas modelo conocidas, antes de evaluar cepas recién aisladas de Barbados.
Material y métodos
Se obtuvieron, mediante el método de Zeigler y Van Eseltine (4), preparaciones de envoltura externa de los serotipos cani-
cola Moulton, canicala Hond Utrecht IV,
pomona S-91 y pomona HCE de Leptospira
1 Publicado en inglés en el Bulletin of the Pan Ameritan Health Organization, VOI. X, No. 2, 1976.
a Todos los autores pertenecen al Instituto de Investiga- ciones Médicas, Instituto de Tecnología de Florida, Mel- bourne. Florida, E.U.A.
3 Esta investigación contó con el apoyo del Proyecto AMRO-3139 de la Organización Panamericana de la Salud y de la subvención No. 74346 de Ia Fundación John A. Hartford de Nueva York. Nueva York.
interrogans. La envoltura externa se separó
mediante shock ósmico, se purificó por centrifugación gradiente isopícnica y se liofi- lizó. Los serotipos canicola Moulton y po- monu HCE son patógenos para los cricetos, mientras que los canicoh Hond Utrecht IV
y pomona S-91 son avirulentos.
Todos los serotipos se mantuvieron en medio semisólido de polisorbato 80 a base de albúmina bovina (5) y se procedió al subcultivo a intervalos de 30 días. Los culti- vos líquidos se prepararon mediante la ino- culación de un medio semisólido fresco que luego se transferfa a un medio líquido des- pués de la proliferación a los 29°C durante un período de cinco a siete días.
Para obtener las diluciones en serie de las preparaciones de envoltura externa purifi- cadas se suspendieron de nuevo las prepara- ciones liofilizadas en una solución salina estéril al 0.85%. Las bacterinas muertas por calor se prepararon mediante la sedimenta- ción de células enteras (fase logarítmica) de cultivos de cinco días (recuento celular 1 Og/ ml) por centrifugación, resuspensión del sedimento celular en 50 ml de solución salina estéril al 0.85% y calentamiento a 56°C durante 30 minutos, seguido de la liofiliza- ’ ción. Para todos los serotipos mencionados se utilizó en las preparaciones de bacterinas muertas por calor y ,de envoltura externa, células cultivadas en el mismo lote del medio. Las diluciones en serie de bacterinas de células enteras muertas por calor se prepara- ron de la misma manera que el material de envoltura externa.
hembra que pesaban 40 g y que se distri- buyeron en cinco grupos de cinco animales. Cada animal de estos grupos fue inoculado por vía intraperitoneal con 1,000, 100, 10 ó 1 pg de la preparación de envoltura externa o de células enteras muertas por calor. Los testigos recibieron solución salina estéril al 0.85%.
Transcurridos 14 días después de la inocu- lación los cricetos inmunizados y los testigos fueron confrontados, también por vía intra- peritoneal, con 2 x 10G células/animal del serotipo respectivo. Los animales se man- tuvieron en observación durante 21 días, y los que sobrevivieron fueron sacrificados y se prepararon cultivos de sus riñones. En un mortero se molió tejido renal de los animales en una mezcla de arena estéril en solución amortiguadora de fosfato, también estéril. Luego se inocularon diluciones seriadas en
cuatro tubos de un medio semisólido de polisorbato 80 a base de albúmina bovina. Los cultivos se incubaron a 29°C y se exami- naron semanalmente durante 10 semanas. Se consideró que la presencia de un “anillo de Dinger” en el tubo de cultivo y las células de leptospiras, observada en la microscopia de campo oscuro, indicaba un cultivo posi- tivo.
Para confirmar el serotipo de leptospira se empleó la prueba de microaglutinación des- crita por Galton et aE. (6).
Los recuentos celulares se determinaron por microscopia de campo oscuro, utilizando una cámara de recuento Petroff-Hausser.
Resultados
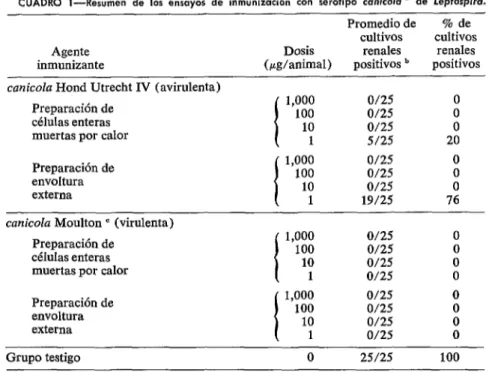
Los cricetos inmunizados con la prepara- ción de envoltura externa procedente de
CUADRO I-Resumen de los ensayos de inmunización con serotipo canicoh n de Lepfospira. Promedio de 9% de
cultivos cultivos
Agente Dosis renales renales
inmunizante (pg/animal) positivos ’ positivos
canicolu Hond Utrecht IV (avirulenta)
Preparación de 1,000 0/25 0
células enteras 100 0/25
muertas por calor 10 1 0/25 5/25 20 i
Preparación de envoltura externa
1,000
0/25 0100 0/25 0
10 0/25 0
1 19/25 76
cunicoZa Moulton ’ (virulenta) Preparación de
células enteras muertas por calor
Preparación de envoltura externa
1,000 0/25 0
100 0/25 0
10 0/25 0
1 0/25 0
1,000 0/25 0
100 0/2.5 0
10 0/25 0
1 0/25 0
Grupo testigo 0 25/25 100
a A los 14 días de la inoculación, los cricetos inmunizados y los testigos inoculados con diluente fueron confrontados por vía intraperitoneal con 2~ 10” células/animal del serotipo virulento.
’ Transcurridos 20 días los animales sobrevivientes fueron sacrificados y se prepara- ron cultivos de sus riñones.
canicola Hond Utrecht IV fueron confronta- dos con 2 x 10” células/animal de canicoZa Moulton virulenta (cuadro 1) . Las concen- traciones inmunógenas de 1,000, 100 y 10 pg/ml protegieron a los animales contra la muerte y la infección renal. Sin embargo, a la concentración de 1 pg/ml se observó in- fección renal (pero no la muerte); en esta concentración el 76% de los cultivos de tejido renal resultaron positivos ( 19/25), mientras que en las otras más fuertes no se detectó ninguno (0/25). La bacterina de células enteras muertas por calor preparadas de canicola avirulenta demostró ser un in- munógeno más activo que las preparaciones de envoltura externa con el mismo grado de dosificación; a la concentración de 1 rg/ml solo el 20% de los cultivos renales (5/25) resultaron positivos.
La inmunización con preparación de en-
voltura externa y células enteras muertas por calor de canicola Moulton fue muy eficaz, sin causar ninguna muerte ni cultivos renales positivos, al terminar el período de observa- ción.
Los resultados de los experimentos con pomona HCE virulento y pomona S-91 avi- rulento (cuadro 2) fueron análogos a los obtenidos con las cepas canicola avirulenta y virulenta. Ninguno de los animales inmuni- zados con la cepa pomona HCE virulenta (preparación de envoltura externa o de célu- las enteras muertas por calor) y confronta- dos con el organismo homólogo mostraron cultivos positivos. En cambio, los que reci- bieron bacterina de células enteras muertas por calor de pomona S-91 produjeron un 16% de cultivos renales positivos (4/25) cuando se empleó una concentración de
1 pg/ml, mientras que los que recibieron la
CUADRO P-Resumen de los ensayos de inmunización con serotipo pomonrr n de Lepfospira.
Agente inmunizante
pomona S-P 1 (avirulenta) Preparación de células enteras muertas por calor
Promedio de % de cultivos cultivos
Dosis renales renales
(pg/animal) positivos ’ positivos
1,000 0/25 0
100 0/25 0
10 0/25 0
1 4/25 16
Preparación de envoltura externa
1,000
0/25 0100 0/25 0
10 0/25 0
1 9/25 36
pomona HCE c (virulenta)
Preparación de células enteras muertas por calor
Preparación de envoltura externa
1
1,000 10010 1
0/25 0
0/25 0
0/25 0
0/25 0
1,000
0/25 0100 0/25 0
10 0/25 0
1 0/25 0
Grupo testigo 0 25125 100
n A los 14 días de la inoculación, los cricetos inmunizados y los testigos inoculados con diluente fueron confrontados por vía intraperitoneal con 2~ 10’ células/animal del serotipo virulento.
’ Transcurridos 20 días los animales sobrevivientes fueron sacrificados y se prepara- ron cultivos de sus riñones.
‘El promedio del tiempo de la muerte del animal en el caso del serotipo pumonn
preparación de envoltura externa de pomona S-9 1 en la misma concentración, presentaron un 36 % de cultivos positivos (9/25 > .
Discusión
En general, las preparaciones de envoltura externa y de células enteras muertas por calor de leptospiras avirulentas y virulentas demostraron ser poderosos inmunogénicos. Sin embargo, la comparación de bacterinas o preparaciones elaboradas a base de cepas homólogas virulentas y avimlentas de sero- tipos pomona y canicola revelaron varia- ciones en cuanto a la actividad.
Si bien todas las preparaciones confirieron protección contra la muerte, se observaron infecciones renales cuando se administró la dosis más débil de las que se elaboraron con organismos avirulentos. Es posible que la pérdida de virulencia vaya acompañada de una reducción correspondiente de la anti- genicidad. A las concentraciones más bajas ensayadas, las bacterinas de células enteras muertas por calor parecían ser más eficaces para prevenir la infección renal que las pre- paraciones de envoltura externa. Una expli- cación de este resultado podría ser que en las bacterinas de células enteras muer.tas por calor puede haber cantidades variables de diferentes antígenos, lo que no ocurriría con el antígeno que quizá sea específico de tipo, relativamente puro de las preparaciones de envoltura externa. Ciertos resultados re- cientes obtenidos por otros investigadores (7, 8) han indicado que el antígeno especí- fico de tipo reside en la envoltura externa.
Recientemente, Bey et al. (9), utilizando el análisis probit, hallaron que la dosis pro- tectora eficaz mínima de una bacterina de envoltura externa ensayada en cricetos y preparada con el método (de Auran et al. (IO), era menor que la ensayada en los estu- dios acabados de describir (0.72 rg/animal en comparación con 1 ~g/animal). Glosser et al. (II) observaron con el empleo de la preparación de envoltura externa, descrita por Auran et al. (IO), que una dosificación
de ll.5 pg/animal protegía a los cricetos contra la infección renal. Los antígenos des- critos por Bey et al. (9) eran envoltura externa y células enteras, el primero quími- camente separado y luego agregado de nuevo, mientras que la preparación de célu- las enteras consistía en células vivas liofiliza- das. El antígeno de envoltura externa de- mostró ser más eficaz que la preparación de células enteras. Por el contrario en los expe- rimentos descritos las bacterinas de células enteras muertas por calor fueron por lo menos tan eficaces como las preparaciones de envoltura externa obtenidas físicamente. El calentamiento de las células enteras es, con mucha diferencia, el procedimiento más sencillo y económico de preparación de bac- terinas. Además, los resultados muestran que esta es la preparación preferida. Estos resul- tados concuerdan con los obtenidos en fechas recientes por Ellinghausen y Painter (comunicación personal), es decir, los anti- genos de células enteras muertas por calor son inmunógenos protectores eficaces.
Los datos que se presentan proceden de los resultados de estudios de inmunización de bacterinas de células enteras o fracciones de células preparadas con serotipos de pato- genicidad conocida para el hombre y los animales. Actualmente se está investigando la dosis mínima requerida para conferir pro- tección contra la muerte y la infección renal, así como la duración de la protección. Tam- bién se están llevando a cabo estudios con bacterinas de células enteras muertas por calor, preparadas de aislados procedentes de Barbados.
Resumen
aún más, en lo que se refiere a protección son más económicas y fáciles de prepa- contra la muerte y la infección y, además, rar. q
REFERENCIAS
(1) Jones, C. J. Preliminary report on the isola- tion of 12 Leptospira serotypes in Barba- dos. West Indian Med J 65:65-68, 1974. (2) Myers, Donald. Leptospirosis Unit Sum- mary Report. Project LEP 3, Isolation of serotype fort bragg in Barbados and its possible association to leptospirosis of cat- tle and man. Centro Panamericano de Zoonosis. Informe del Comité Científico Asesor. Noviembre de 1974.
(3) Myers, D. M. y C. J. Jones. Aislamiento de
Leptospira f&t-bragg de una rata de Bar- bados. Bol Of Sanit Panam 80(3):254-
257, 1976. .
(4) ZeigIer, J. A. y W. P. Van Eseltine. Isolation and characterization of outer envelope of
Leptospira pomona. Can J Microbio1 21: 11021112,197s.
(5) Ellinghausen, H. C., Jr., y W. G. McCul- lough. Nutrition of Leptospira pomona
and growth of 13 other serotypes: A
serum-free medium employing oleic-albu- min complex. Am .l Vet Res 26z39-44,
1965.
(6) Galton, M. M., C. R. Suzler, C. A. Santa
Rosa y M. D. Fields. Applications of a
microtechnique to the agglutination test for leptospirosis antibodies. J. Appl Mi- crobiol 13:81-85, 1965.
(7) Kasai, 1. y R. Yanagawa. Studies on the
antigenic determinant group of the type- specific antigen of Leptospira canicola. Z Bakt Parasit Infekt Hvn ABT I Orin 228:
533-541,1974: - -
(8) Palit. A.. R. C. Hamilton v J. Gulasekharam. ~ I
Further studies on leptospira1 genus-spe- cific antigen: Its ultra-structure and im- munochemistry. .i Gen Microbio1 82:223- 236, 1974.
(9) Bey, R. F., N. E. Auran y R. C. Johnson. Immunogenicity of whole-cell and outer envelope leptospira1 vaccines in hamsters.
Infect Zmmun 10(5):1501-1506, 1974. (10) Auran, N. E., R. C. Johnson y D. M. Ritzi.
Isolation of the outer sheath of Leptospira
and its immunogenic properties in ham- sters. Infect Immun 51968-975, 1972.
(II) Glosser, J. W., R. C. Johnson, C. R. Sulzer y N. E. Auran. Immunogenic properties of a leptospira1 outer envelope bacterin in
hamsters and foxes. Am J Vet Res 35:
681-684, 1974.
Immunization against leptospirosis: Vaccine trials with heat-killed whole-cell and outer envelope antigens in hamsters (Summary)
Heat-killed whole-ce11 and outer envelope an- heat-killed bacterins proved at least as effective tigens prepared from homologous virulent and as the outer envelope antigens, or more so, in avirulent strains of Leptospira serotypes cani- providing protection against death and infec- cola and pomona were evaluated for protecting tion, and they are easier and more economical hamsters against experimental leptospirosis. The to prepare.
Imunizacão contra a leptospirose: Ensaios em cricetos com antígenos mortos por calor e preparados com células inteiras e cobertura externa (Resumo)
Avaliou-se a protecão contra a leptospirose tecáo contra a morte e a infeccáo, as bacterinas conferida a cricetos por antígenos de células mortas por calor revelaram-se pelo menos táo
inteiras mortas por calor e de cobertura ex- eficazes como os antígenos de cobertura ex-
terna, preparados com cepas homdlogas viru- terna, sendo também mais fáceis e econômicas lentas e náo virulentas de ser&ipos canicola e de preparar.
pomona de Leptospira. Em matéria de pro-
Immunisation centre la leptospirose: Essais de vaccins faits avec des cellules entières tuées à la chaleur et des antigènes 6 enveloppe extérieure, effectués sur des hamsters (Résumé)
Les cellules entières tuées à la chaleur et les bactérines tuées à la chaleur se sont avérées
antigènes à enveloppe extérieure, préparés à au moins aussi efficaces que les antigènes à base de variétés homologues virulentes et aviru- enveloppe extérieure, et même davantage, car lentes de sérotypes canicola et pomona de Lep- elles ont fourni une protection centre la mort tospira ont été expérimentés sur des hamsters et I’infection, et elles sont plus faciles et plus