624 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 10.26843/rencima.v11i6.2548 eISSN 2179-426X
Recebido em 07/10/2019 / Aceito em 15/08/2020 / Publicado em 01/10/2020
O Modelo Atômico de Thomson: um estudo sobre o livro didático,
estratégia docente e concepção dos alunos
Thomson's Atomic Model: a study on the textbook, teaching strategy and students’ conception
Danilo Lopes Santos
Universidade Federal dos Vales do Jequitinhonha e Mucuri/ Departamento de Química/
danilo.lopes@ufvjm.edu.br
http://orcid.org/0000-0003-2244-2267
Geraldo Wellington Rocha Fernandes
Universidade Federal dos Vales do Jequitinhonha e Mucuri/ Departamento de Ciências Biológicas/ PPGECMaT/ geraldo.fernandes@ufvjm.edu.br
http://orcid.org/0000-0002-1337-1236
Resumo
Esta pesquisa teve como objetivo analisar as concepções de 22 alunos do 1º ano do ensino médio, de uma escola pública, sobre o modelo atômico de Thomson, a partir das estratégias de ensino usadas por um(a) docente de Química e das informações do livro didático. Para a coleta de dados, foi analisado o livro didático utilizado pelos participantes, aplicado um questionário aos alunos e realizada uma entrevista semiestrutura com o(a) docente de Química. A partir da Análise Textual Discursiva, emergiram categorias e subcategorias que foram analisadas dentro de quatro eixos: 1) O conteúdo do livro didático, 2) As respostas do docente, 3) As respostas dos alunos, 4) Confronto do modelo atômico de Thomson (1904) com o encontrado no livro didático e as respostas dos alunos. Concluiu-se que o modelo atômico de Thomson é representado no ensino de Química pela analogia do “pudim de passas” e que este análogo está distante do modelo proposto por Thomson em 1904, dificultando a compreensão correta por parte dos discentes.
625 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020
Palavras-chave: Modelo Atômico de Thomson; ensino de Química; livro didático. Abstract:
This research aimed to analyze the conceptions of 22 students from the 1st year of high school, from a public school, about Thomson's Atomic Model, from the teaching strategies used by a Chemistry teacher and from the textbook information. For data collection, the textbook used by the participants was analyzed, a questionnaire was applied to the students and a semi-structured interview was conducted with the Chemistry teacher. From the Discursive Textual Analysis, categories and subcategories emerged that were analyzed within four axes: 1) The content of the textbook, 2) The answers of the teacher, 3) The answers of the students, 4) Confrontation of the Atomic Model of Thomson ( 1904) with the one found in the textbook and the students' answers. It was concluded that Thomson's Atomic Model is represented in the teaching of Chemistry by the analogy of “raisin pudding” and that this analogue is far from the model proposed by Thomson in 1904, making it difficult for students to understand correctly.
Keywords: Thomson's Atomic Model; chemistry teaching; textbook. 1 Introdução
Ao iniciar o conteúdo dos modelos atômicos e características dos átomos, os livros didáticos trazem os cientistas por ordem cronológica das suas contribuições: John Dalton (1766-1844) e seu modelo atômico conhecido como “bola de bilhar”, Joseph John Thomson (1856-1940) com o modelo conhecido como “pudim de passas”, Ernest Rutherford (1871-1937) com o modelo “planetário” e Niels Bohr (1885-1962). Thomson foi uma das figuras mais importantes no desenvolvimento das teorias atômicas no final do século XIX e início do século XX (LOPES, 2009), e seu modelo atômico é descrito na maioria dos livros didáticos utilizados nas turmas do 9º ano do ensino fundamental, 1º ano do ensino médio, e muitas vezes no ensino superior, de forma equivocada, não refletindo o grande trabalho realizado por este cientista (LOPES; MARTINS, 2000). O uso de analogias para o ensino dos modelos atômicos é uma das ferramentas empregadas por muitos docentes, no entanto, por diversos fatores (como o uso equivocado de analogias ou desconhecimento do modelo atômico), não acabam contribuindo adequadamente para que os discentes possam compreender o modelo proposto por Thomson (RAMOS; MOZZER, 2018) .
Visto que a analogia é um instrumento comumente utilizado na apresentação dos modelos atômicos nas aulas de Ciências e Química, este trabalho tem o objetivo de analisar as concepções dos alunos do 1º ano do ensino médio sobre o modelo atômico de Thomson, a partir das estratégias de ensino usadas por um docente de Química e das informações do livro didático utilizado por eles.
626 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 Visando aprofundar o objetivo geral apresentado anteriormente, esta pesquisa propõe alcançar alguns objetivos específicos: (i) analisar e comparar o modelo atômico apresentado pelo livro didático com o que foi proposto por Thomson em 1904; (ii) caracterizar as principais estratégias de ensino utilizadas pelo docente de Química para ensinar o modelo atômico de Thomson; e (iii) caracterizar as concepções dos estudantes sobre o modelo atômico de Thomson.
Compreender o ensino e a aprendizagem dos modelos atômicos possibilita que o discente tenha as ferramentas necessárias para discutir e entender os aspectos e conceitos mais complexos de Química. Neste sentido, esta pesquisa buscará apresentar o modelo original proposto por Thomson e colocar em perspectiva com o ensinado na sala de aula por um professor de Química, o encontrado no livro didático e o compreendido pelos estudantes do ensino médio.
2 Fundamentação teórica
J. J. Thomson, também conhecido por Sir Joseph John Thomson, nasceu em 18 de dezembro de 1856, em Cheetham Hill, Inglaterra, e morreu em 30 de agosto de 1940, Cambridge (Cambridgeshire). Thomson foi um físico que contribuiu para revolucionar o conhecimento da estrutura atômica por sua descoberta do elétron (1897) e ganhador do Prêmio Nobel de Física em 19061,2. Iniciou sua vida acadêmica em Manchester,
desenvolvendo interesse pela Física, pelas leis das combinações químicas e pelas teorias atômicas da matéria, principalmente pelas ideias de John Dalton (1766-1844) (LOPES; MARTINS, 2000). Segundo Melzer e Aires (2015), Thomson esteve à frente do laboratório de Cavendish, sendo cientista responsável pela fama mundial deste, bem como pela migração de jovens cientistas que sonhavam em trabalhar sob sua orientação. Dentre os alunos orientados por Thomson, tem-se Ernest Rutherford (1871-1937), que foi o primeiro pesquisador formado fora de Cambridge a atuar no Laboratório Cavendish. Rutherford tornou-se um dos cientistas mais importantes nas pesquisas em radioatividade e estrutura atômica e acabou sucedendo Thomson na condução do Laboratório (LOPES; MARTINS, 2000).
Segundo Melzer e Aires (2015), Thomson foi influenciado pelas leituras dos trabalhos de Michael Faraday, que o levou a elaborar um modelo atômico baseado em girostatos e que possibilitou o cálculo da razão de carga negativa. No entanto, foi em 1897, com a publicação de seu artigo sobre raios catódicos (On the cathode rays), que Thomson visualizou uma profunda mudança em sua proposta atômica. Em 1904, Thomson apresentou o modelo que era formado por anéis coplanares de corpúsculos dentro de uma esfera de carga positiva e uniforme (THOMSON, 1904).
1Disponível em: https://www.britannica.com/biography/J-J-Thomson. Acesso em: 22/12/2018.
627 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 Curiosamente, a analogia, como um meio facilitador para a aprendizagem, foi um instrumento utilizado por Thomson em sua adolescência. De acordo com Lopes (2009), em 1870, aos 14 anos, Thomson ingressou no curso de engenharia na Owens College (hoje Universidade de Manchester). Em sua formação em Owens, as analogias mecânicas e teorias especulativas foram componentes essenciais do pensamento físico apresentado a Thomson. Para Lopes (2009), a analogia foi uma ferramenta utilizada por Thomson, mesmo antes de propor o seu modelo atômico em 1904 e a experiência adquirida, ao fazer uso das analogias mecânicas e teorias especulativas, proporcionaram a ele aprendizagens que foram incorporadas à sua produção teórica como um valioso instrumental para compreender o “invisível”.
Junior (2009) relata que vários autores definem de forma diferente os conceitos comparados em uma analogia, no entanto o entendimento é o mesmo, assim, utiliza-se a denominação de conceito alvo para aquele conceito que se quer aprender (ensinar) e de
conceito análogo para aquele que servirá de subsídio no alcance ao primeiro. O uso de
analogias, como ferramenta na educação em Ciências, apresenta pontos positivos e negativos. Duarte (2005) diz que um dos grandes potenciais das analogias são que elas desenvolvem a capacidade cognitiva dos estudantes, como a criatividade e a tomada de decisões; tornam o conhecimento científico mais plausível e constituem um instrumento poderoso e eficaz no processo de facilitar a evolução ou mudança conceitual. No que diz respeito às dificuldades/problemas são que as analogias podem ser interpretadas como o conceito em estudo, ou seja, os alunos podem centrar-se nos aspectos positivos da analogia e desvalorizar as suas limitações (DUARTE, 2005). Esta discussão sobre a forma de abordar objetos alvo e análogo se faz cada vez mais necessária, pois a Química está baseada em modelos e analogias, não apenas nos atômicos, como também nos moleculares, nos de reações e muitas vezes, essa ideia não é contemplada pelo professor, pela maioria dos livros didáticos e, consequentemente, pelo aluno (MELO; NETO, 2013).
Na medida em que o ensino de Química, principalmente na educação básica, se ampara fortemente nas analogias, Monteiro e Justi (2000) nos chamam atenção sobre o perigo mais frequente apontado na utilização destas, nas quais os alunos podem estabelecer relações analógicas que não são corretas. Para essas autoras, é importante lembrar que apesar de possíveis relações analógicas incorretas, as analogias não têm o seu valor diminuído enquanto modelo de ensino, mas ressalta a necessidade de auxiliar os alunos a identificarem não só as similaridades, como também as diferenças entre o domínio (ou conceito) alvo e o domínio análogo.
Os livros didáticos ainda são um dos principais recursos usados por professores e alunos no processo educacional, seja na educação básica, com as obras avaliadas e disponibilizadas pelo Programa Nacional do Livro Didático (PNLD), ou, na educação superior, através da bibliografia básica das disciplinas curriculares (SANTOS; JÚNIOR; VALASQUE, 2018; LOPES; MARTINS, 2000).
628 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 Chaves, Santos e Carneiro (2014) analisaram seis livros didáticos da educação básica e concluíram que nenhum destes demostravam a dinamicidade do modelo atômico proposta por Thomson. Ainda, com o nome de corpúsculo (elétron), Thomson (1904, p. 254) dizia que “cada corpúsculo gira em alta velocidade na circunferência do anel em que se encontra”. Neste sentido, é fundamental que os professores, ao tratarem do estudo dos modelos atômicos em suas aulas, procurem apresentar aos discentes outras histórias que não estão nos livros. Segundo estes autores, existe uma falta de informações que permita ao discente entender os passos que levaram os cientistas à conclusão do modelo estudado e, portanto, compromete o entendimento do conteúdo.
3 Metodologia
3.1 Caracterização da abordagem da pesquisa
Para o desenvolvimento deste trabalho, buscou-se realizar um estudo exploratório com uma abordagem qualitativa. Esta abordagem busca aproximar a teoria e os fatos, através da descrição e interpretação de episódios isolados ou únicos, privilegiando o conhecimento das relações entre contexto e ação (LÜDKE; ANDRÉ, 1986).
3.2 Caracterização do ambiente de realização do estudo e dos sujeitos
O local utilizado para coletar os dados e desenvolver este estudo é um colégio público, localizada na cidade de Diamantina, Minas Gerais. A escolha do local se deu pelo fato de a escola ser assistida pelo Programa Institucional de Bolsa de Iniciação à Docência – PIBID, no subprojeto de Química. A instituição participante atende o ensino fundamental, ensino médio e a Educação de Jovens e Adultos. Atualmente, encontram-se matriculados cerca de 713 alunos, distribuídos nos três turnos.
A escola não tem laboratório de Ciências, mas tem laboratório de Informática que se encontra em funcionamento. As atividades experimentais são realizadas no interior da sala de aula com a utilização de materiais de baixo custo.
A coleta foi realizada no segundo semestre de 2018 e contou com a colaboração do docente, que atua como supervisor do PIBID, licenciado em Química e atuante a mais de 19 anos. Também contou com a colaboração de uma turma do 1º Ano do ensino médio, com 22 alunos presentes na sala de aula no momento da coleta de dados.
3.3 Caracterização dos instrumentos de coleta de dados
Para alcançar os objetivos propostos, foram utilizados, como instrumentos de coleta de dados, um questionário aplicado aos alunos participantes e uma entrevista semiestruturada ao docente, e que estão apresentados nas Figura 1(a) e Figura 1(b) respectivamente.
629 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 Figura 1: (a) Questionário aplicado aos alunos e (b) Roteiro de entrevista aplicado ao professor.
Os questionários foram aplicados durante a aula de Química em horário e data estabelecidos pelo docente. É válido destacar que todos os aspectos éticos da pesquisa foram preservados3. Foi solicitada a assinatura do Termo de Consentimento Livre e
Esclarecido (TCLE) aos participantes e o pesquisador esclareceu aos estudantes e ao docente o objetivo da aplicação do questionário e da realização da entrevista.
3Para preservar a ética da pesquisa com seres humanos, este trabalho foi aprovado pelo Comitê de Ética e
Pesquisa (CEP) sob o número CAAE 03347318.4.0000.5108.
Figura 1(a) - Fonte: Arquivo dos autores.
630 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 Também foi utilizado como fonte de dados, o livro “Ser Protagonista de Química do 1º Ano do Ensino Médio, Volume 1, 3ª edição São Paulo – 2016” (LISBOA et al., 2016). A escolha deste livro didático se justifica por fazer parte do PNLD e por ser utilizado pelo docente de Química e alunos participantes da pesquisa.
3.5 Caracterização do instrumento metodológico de análise de dados
Como metodologia de análise dos dados qualitativos, foi utilizada a Análise Textual Discursiva (ATD) (MORAES; GALIAZZI, 2016). A ATD foi utilizada para analisar o livro didático, as respostas do docente de Química e de seus discentes. A escolha da ATD se justifica por esta metodologia transitar entre duas formas consagradas de análise na pesquisa qualitativa que são a análise de conteúdo e a análise de discurso e por buscar compreender os fenômenos inerentes aos dados coletados (MORAES; GALIAZZI, 2016). Outra justificativa para a escolha da Análise Textual Discursiva, está no fato de que as unidades de significado e até mesmo as categorias são não excludentes, enquanto a Análise de Conteúdo assume a exclusividade das unidades a uma categoria.
Para este trabalho, o processo da ATD foi realizado em quatro etapas:
1) Construção do corpus: consistiu no texto do livro didático de Química
relacionado ao modelo do atômico de Thomson, utilizado pelos participantes (LISBOA et al., 2016), nas respostas do questionário e nas falas do professor provenientes da entrevista semiestruturada. Embora, geralmente, a ATD se ocupe de textos no sentido de produções escritas, para Moraes e Galiazzi (2006), o termo corpus deve ser entendido num sentido mais amplo, incluindo imagens, esquemas e outras expressões linguísticas.
2) Unitarização: os textos analisados, ou seja, o conteúdo do livro didático referente
ao modelo atômico de Thomson e as respostas dos participantes foram separadas por seus significados. Nessa pesquisa, foi realizada a fragmentação do capítulo referente ao modelo atômico de Thomson (página 81 do livro) (LISBOA et al., 2016), das respostas da entrevista semiestrutura realizada com o docente de Química e dos questionários aplicados aos discentes.
3) Categorização: após a unitarização, os dados foram organizados por unidades
de significado, ou seja, por semelhança de significados. Neste trabalho, foi o momento em que as categorias (pré-estabelecidas) e subcategorias (emergentes) foram organizadas em quatro eixos de análise: Eixo 1: O conteúdo do livro didático; Eixo 2: As respostas do docente; Eixo 3: As respostas dos alunos, e Eixo 4: Confronto do modelo atômico de Thomson (1904) com o encontrado no livro didático e as respostas dos alunos.
4) Metatexto: trata-se de textos descritivos e interpretativos das categorias
relevantes deste estudo. Nessa fase, o pesquisador se esforça em expressar suas intuições e novos entendimentos a partir da sua rigorosa e ostensiva análise dos dados. A validade e confiabilidade dos resultados de uma análise, segundo Moraes (2003), dependem “do rigor com que cada etapa da análise foi construída (p. 206)”, uma vez que “uma unitarização e uma categorização rigorosas encaminham para metatextos válidos e
631 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 representativos dos fenômenos investigados (p. 206)”. A validade e confiabilidade da análise dos resultados deste trabalho foram construídas ao longo do processo da ATD e os metatextos organizados em quatro eixos, conforme o Quadro 1:
Quadro 1. Eixos de análise e categorias presentes no metatexto.
Eixos de Análise Categorias
Eixo 1: O conteúdo do livro didático
a) Caracterização do modelo atômico de Thomson no livro didático.
Eixo 2: As respostas do docente
a) Principais analogias utilizadas para a apresentação do modelo atômico de Thomson.
b) Estratégias utilizadas para fazer a analogia com o modelo atômico de Thomson.
c) As fontes e materiais utilizados pelo docente e alunos sobre o modelo atômico de Thomson.
Eixo 3: As respostas dos alunos
a) Concepção do modelo atômico de Thomson. b) Analogia e Análise do modelo atômico de Thomson.
c) Concepção sobre o comportamento do elétron no modelo de Thomson.
d) Concepções das características do modelo atômico de Thomson.
Eixo 4: Confronto do modelo atômico de Thomson (1904) com o encontrado no livro didático e as respostas dos alunos
a) Confronto de conceitos e concepções.
Fonte: Elaborado pelos autores.
4 Resultados e Discussão
Os resultados, aqui apresentados, são oriundos das análises feitas das categorias e suas subcategorias, dentro de cada eixo do Quadro 1, que tem como propósito alcançar os objetivos apresentados nesta pesquisa.
4.1 Eixo de Análise 1: O conteúdo do livro didático
Para o livro didático, foi analisada a única categoria pré-estabelecida:
Caracterização do modelo atômico de Thomson no livro didático. O livro didático (Figura
2) usa a analogia como uma das ferramentas para apresentar o modelo atômico de Thomson (página 81 do livro) (LISBOA et al., 2016). No entanto, a abordagem utilizada não conduz o discente ao entendimento adequado do conceito análogo ao conceito alvo, deixando que ambos acabem sendo equivocadamente a imagem um do outro. Isto quer dizer que, a forma como o modelo é apresentado faz com que os discentes não consigam compreender as limitações existentes entre o modelo atômico e a analogia utilizada.
632 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 Figura 2: Livro didático e página com o conteúdo sobre o modelo atômico de Thomson.
Fonte: Imagem retirado do Livro Didático (LISBOA et al., 2016, p. 81).
No texto do livro didático: “Esse modelo ficou conhecido por modelo do pudim de
passas (nome que não foi dado por Thomson).” (LISBOA et al., 2016, p. 81), verifica-se a
apresentação do modelo “pudim de passas”, e, apesar das pessoas não terem uma imagem muito definida do que seja um ‘pudim de passas’, muitas fazem uma associação direta dessa expressão com o modelo atômico proposto por Thomson.
Ainda, sobre a utilização da analogia no livro didático, verificou-se que os aspectos culturais e do cotidiano do discente não são respeitados, sendo este um ponto importante quando se faz uso dessa ferramenta. Segundo Munarin e Munarin (2008), a analogia “pudim de passas” não seria adequado para os discentes brasileiros, pois o pudim em nosso país é tradicionalmente uma massa clara, consistente com um furo no meio (tipo da forma) e normalmente não se utiliza passas. Assim, o modelo atômico de Thomson não se enquadraria ao pudim feito no Brasil. O pudim de passas ou pudim de ameixa é uma sobremesa típica da Inglaterra – plum-pudding, não tem muita penetração na cultura gastronômica brasileira, portanto, a maioria dos discentes, não tem familiaridade com o análogo utilizado por seus docentes e apresentado nos livros didáticos, o que torna mais difícil a relação que se deseja construir para facilitar a aprendizagem. É provável que os discentes teriam maior familiaridade com o objeto análogo melancia, pois este está presente na cultura gastronômica brasileira com maior representatividade. Este também apresenta maior quantidade de informações (forma, homogeneidade, sementes etc.) que podem ser trabalhadas e relacionadas ao objeto alvo.
633 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020
4.2 Eixo de Análise 2: As respostas da entrevista semiestruturada com o docente
Na entrevista com o docente de Química, buscou-se analisar as estratégias que foram utilizadas para o ensino do modelo atômico proposto por Thomson. A partir da ATD, as respostas do docente foram organizadas em três categorias pré-estabelecidas:
a) Principais analogias utilizadas para a apresentação do modelo atômico de Thomson: o docente faz uso das analogias “pudim de passas” e “panetone”, sendo a
primeira também citada no livro didático.
Monteiro e Justi (2000) dizem que diante da forma como as analogias são apresentadas nos livros, o professor deve fazer uma avaliação criteriosa delas, no sentido de identificar quais são os seus aspectos positivos e negativos. Só então, a partir dessa avaliação, o docente teria condições de julgar a conveniência das analogias para o ensino e a aprendizagem dos conceitos químicos, uma vez que o pudim de passas não é uma sobremesa tradicional no Brasil. Por sua vez, o modelo “panetone” também não seria uma analogia adequada para apresentar o modelo atômico de Thomson, uma vez que este não apresenta forma esférica. Uma das primeiras características atribuídas por Thomson (1904), ao seu modelo, é que este apresenta a forma de uma esfera. Utilizar o “panetone” como objeto análogo, não sendo esférico, é distanciar consideravelmente de uma característica primária do objeto alvo.
b) Estratégias utilizadas para fazer a analogia com o modelo atômico de Thomson:
a estratégia que o docente relatou para relacionar o análogo (pudim de passas) ao domínio alvo (modelo atômico de Thomson) foi convidar os alunos a fazerem um “pudim de passas” e levá-lo para sala de aula. Juntos discutiram e fizeram as relações necessárias. Infelizmente não houve registro deste momento para que pudesse discutir sobre a “forma do pudim”, elaborado pelo professor e alunos, e analisar as discursões geradas. Monteiro e Justi (2000) dizem que é importante que o professor discuta com seus alunos as analogias apresentadas nos livros, pois só ele tem condições de avaliar em que medida os alunos compreendem os conceitos análogos e se eles estão estabelecendo as relações analógicas corretas. Caso perceba que a analogia não foi compreendida totalmente, o docente pode esclarecê-la através de explicações adicionais.
c) As fontes e materiais utilizados pelo docente e alunos sobre o modelo atômico de Thomson: o livro didático foi o único material utilizado para a elaboração da aula
realizada pelo docente e para o desenvolvimento das atividades realizadas pelos alunos em sala de aula. Como mostrado anteriormente, o livro didático não consegue deixar claro o modelo através da analogia apresentada (Figura 2). Monteiro e Justi (2000) dizem que se o professor não explica as analogias apresentadas no livro didático e/ou se o aluno tem somente o livro didático como material de estudo, a única referência que eles têm é a descrição feita pelo autor. Para Chaves, Santos e Carneiro (2014), é preciso que os docentes entendam que ensinar conceitos de Química exige introduzir, não apenas os trechos históricos fragmentados da história da Química, como apresentados nos livros
634 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 didáticos, mas, sobretudo, as relações de produção do conhecimento científico em contextos mais amplos da sociedade.
4.3 Eixo de Análise 3: As respostas do questionário aplicado aos alunos
No intuito de verificar as concepções dos alunos sobre o modelo atômico de Thomson, a partir das informações do livro didático e das estratégicas de ensino utilizadas pelo docente, foi aplicado um questionário aos discentes e analisada as suas respostas. As categorias (pré-estabelecidas), subcategorias (emergentes) e as frequências absolutas de citação estão caracterizadas nas Tabelas 1, 2, 3 e 4.
Categoria 1 - Concepção do modelo atômico de Thomson: para esta primeira
categoria, buscou-se analisar a concepção de 22 discentes sobre o modelo atômico proposto por Thomson. As subcategorias emergentes da Tabela 1 representam as principais concepções dos discentes sobre este modelo.
Tabela 1: Categorização das respostas dos alunos sobre suas concepções do modelo atômico de Thomson.
CATEGORIA 1 SUBCATEGORIAS FREQUÊNCIA
ABSOLUTA (N)
1) Concepção do modelo atômico de Thomson
1 - Esfera com sinal positivo no meio e sinais
negativos ao redor 19
2 - Esfera com vários sinais positivos 1
3 - Outros (Imagens que não fazem sentido) 1
Fonte: Elaborado pelos autores.
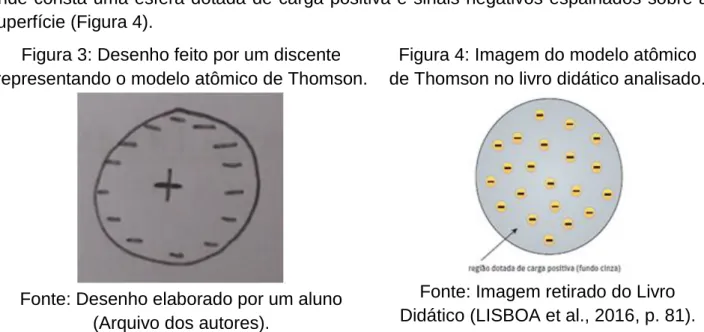
A partir das respostas dos discentes, foram obtidos 19 desenhos representando uma esfera com sinal positivo no meio e sinais negativos ao redor (Figura 3). O desenho desses alunos tem grande semelhança com o exemplo apresentado no livro didático, onde consta uma esfera dotada de carga positiva e sinais negativos espalhados sobre a superfície (Figura 4).
Figura 3: Desenho feito por um discente representando o modelo atômico de Thomson.
Figura 4: Imagem do modelo atômico de Thomson no livro didático analisado.
Fonte: Desenho elaborado por um aluno (Arquivo dos autores).
Fonte: Imagem retirado do Livro Didático (LISBOA et al., 2016, p. 81).
635 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 A partir da comparação entre as figuras 3 e 4, pode-se perceber que o livro didático é a principal referência dos discentes sobre o modelo atômico de Thomson. Frison et al. (2000) dizem que a maioria dos livros didáticos apresentam uma ciência descontextualizada, separada do cotidiano e da sociedade concebendo o método científico como um conjunto de regras fixas para encontrar respostas que nem sempre são apresentadas de forma completa. No entanto, muitas vezes, ele é a única referência para o trabalho do professor, passando a assumir o papel de currículo e de definidor das estratégias de ensino, afetando de modo significativo nos processos de seleção, planejamento e desenvolvimento dos conteúdos em sala de aula. Mota e Cleophas (2015), ao analisarem em seu trabalho a forma como são abordadas as descobertas científicas, identificaram que, de 5 livros didáticos, apenas 1 procura apontar em seus recortes históricos as descobertas científicas de maneira mais ampla, os outros 4 têm uma abordagem linear e superficial, sem muitas explicações para os leitores.
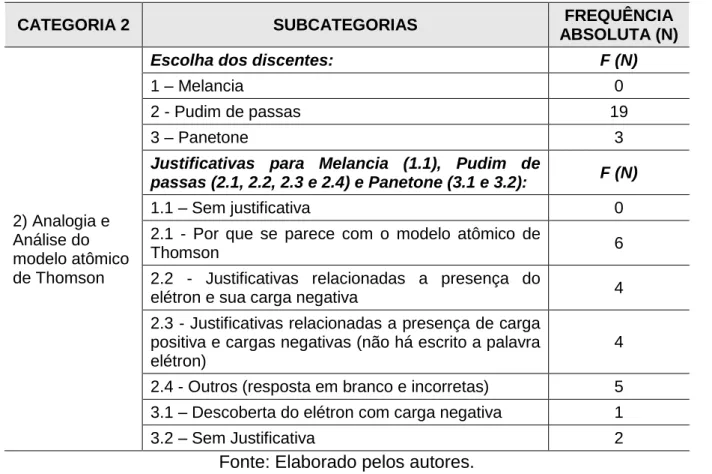
Categoria 2 - Analogia e Análise do modelo atômico de Thomson: nesta categoria,
buscou-se verificar se os alunos conseguiam relacionar o objeto alvo com o objeto análogo. Quando questionado aos discentes qual o análogo se aproximava do modelo atômico proposto por Thomson, verificou-se que dos 22 respondentes, 19 acreditavam que era o “pudim de passas” (Tabela 2), três citaram o “panetone” e nenhum citou, como objeto análogo, a “melancia”.
Tabela 2: Categorização das respostas dos alunos sobre Analogia e Análise do modelo atômico de Thomson.
CATEGORIA 2 SUBCATEGORIAS FREQUÊNCIA
ABSOLUTA (N)
2) Analogia e Análise do modelo atômico de Thomson
Escolha dos discentes: F (N)
1 – Melancia 0
2 - Pudim de passas 19
3 – Panetone 3
Justificativas para Melancia (1.1), Pudim de
passas (2.1, 2.2, 2.3 e 2.4) e Panetone (3.1 e 3.2): F (N)
1.1 – Sem justificativa 0
2.1 - Por que se parece com o modelo atômico de
Thomson 6
2.2 - Justificativas relacionadas a presença do
elétron e sua carga negativa 4
2.3 - Justificativas relacionadas a presença de carga positiva e cargas negativas (não há escrito a palavra elétron)
4
2.4 - Outros (resposta em branco e incorretas) 5
3.1 – Descoberta do elétron com carga negativa 1
3.2 – Sem Justificativa 2
636 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 A Tabela 2 apresenta uma síntese, em forma de subcategorias, dos textos elaborados pelos alunos, de maneira que se pode observar que 32% desses alunos justificaram que “... o pudim de passas se parece com o modelo proposto por Thomson.” (A4) (Figura 5). Como estabelecido por Lopes e Martins (2000), esta analogia transcendeu a relação objeto alvo e objeto análogo e tornou-se praticamente sinônimo do modelo proposto por Thomson, fazendo com que os discentes acabassem ligando um ao outro de forma direta.
Figura 5: Justificativa do aluno A5 ao relacionar o pudim de passas com o modelo de Thomson.
Fonte: Arquivo dos autores.
Observou-se também que 21% do discentes justificaram a sua escolha pela presença do elétron e sua carga negativa. Outros 21% citaram a natureza elétrica no modelo, no entanto não citam a presença do elétron. Ter a consciência da sua existência e identificar os elétrons no modelo atômico de Thomson é um ponto crucial, pois, a partir desta concepção, pode-se introduzir o conceito de cargas (positivas e negativas) dentro dos modelos atômicos. Ademais, a descoberta dos elétrons é um dos pontos mais importantes do modelo atômico de Thomson. Ramos e Mozzer (2018) dizem que dentre as relações de similaridade na analogia do “pudim de passas” somente se observa um único aspecto estrutural entre o análogo e o domínio alvo. Esse aspecto estrutural é o da homogeneidade na distribuição de cargas negativas e da massa positiva.
Categoria 3: Concepção sobre o comportamento do elétron no modelo de Thomson: esta categoria apresenta indicativos sobre a concepção dos discentes em
relação ao comportamento do elétron no modelo atômico de Thomson (Tabela 3).
Tabela 3: Categorização das respostas dos alunos sobre a concepção do comportamento do elétron no modelo atômico de Thomson.
CATEGORIA 3 SUBCATEGORIAS FREQUÊNCIA
ABSOLUTA(N)
3) Concepção sobre o comportamento do elétron no modelo de Thomson
1 – Estão em movimento 6
2 – Explicações incorretas 10
3 – Sem Justificativa 6
637 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 Verifica-se na Tabela 3 que somente 32% dos alunos compreendiam que “O
elétron está em movimento”. Estas respostas estão em consonância com Lopes e Martins
(2000), que diz que as concepções atômicas de Thomson mudaram com o andamento de suas investigações, no entanto, desde suas primeiras explicações, verifica-se a concepção de um átomo dinâmico (anéis vórtices, girostatos e corpúsculos em movimento), ou seja, que tem movimento em seus elementos constituintes. Nesta categoria, também foi observada a maior concentração de respostas erradas com justificativas de diversas naturezas, exemplificadas nas Figuras 6a (“agarrado um no
outro”) e 6b (“Estão juntos”). Como constatado por Lopes e Martins (2000) e Chaves,
Santos e Carneiro (2014), o modelo atômico de Thomson é apresentado nos livros didáticos de forma estática ou não deixam clara a dinâmica do átomo proposta por Thomson.
Figura 6: Resposta dos discentes quanto ao comportamento do elétron no modelo atômico de Thomson
(a) (b)
Fonte: Acervo dos autores.
É provável que conhecer a dinamicidade dos elétrons, dentro do modelo atômico de Thomson, contribui para que o discente entenda o processo de evolução dos modelos atômicos. Dalton apresenta um átomo indivisível, maciço, impenetrável e indestrutível. Na sequência histórica, Thomson apresenta seu modelo onde cargas (positivas e negativas) estão presentes em um sistema estável. Para o modelo atômico proposto por Thomson, onde a carga positiva ocupa o volume total do átomo, a dinamicidade dos elétrons, dentro deste sistema, é um dos pontos que explica sua estabilidade frente às leis da eletrodinâmica clássica.
Categoria 4: Concepções das características do modelo atômico de Thomson:
buscou-se, nesta categoria, identificar quais são as principais características que os discentes identificam no modelo proposto por Thomson (Tabela 4).
Tabela 4: Categorização das respostas dos alunos sobre a concepções das características do modelo atômico de Thomson
CATEGORIA 4 SUBCATEGORIAS FREQUÊNCIA
ABSOLUTA(N)
4) Concepções das características do modelo atômico de Thomson
1 – Características relacionadas ao modelo
atômico de Bohr 5
2 – Características relacionadas ao modelo
atômico de Dalton 1
3 – Características relacionadas a presença de
638 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020
4 – A descoberta do elétron e sua carga negativa 3
5 – A neutralidade do átomo 2
6 – Resposta incompleta 1
7 – Explicação incorreta 2
8 – Sem resposta 5
Fonte: Elaborado pelos autores.
A Tabela 4 apresenta um resumo das unidades de significado provenientes do processo de unitarização da ATD. Pode-se verificar que emergiram diferentes respostas para as concepções das características do modelo atômico de Thomson. Cerca de 27% dos discentes apresentaram caraterísticas de modelos propostos por outros cientistas, como Bohr e Dalton, caracterizando uma confusão destes modelos com o modelo atômico de Thomson. Nesse sentido, Melo e Neto (2013) constataram resultados semelhantes em seu trabalho: discentes atribuíram características de modelos atômicos a outros cientistas, não concebiam o átomo como uma construção científica, pois não estabeleciam limites para o uso de cada modelo e consideravam o átomo como uma unidade sólida e real.
Verifica-se também que, 27% dos alunos relataram características relacionadas às cargas positivas e negativas e à descoberta do elétron e sua carga negativa, ou seja, à natureza elétrica do modelo atômico de Thomson. Também foi verificado que 9% dos discentes levantaram pontos sobre a neutralidade elétrica do modelo atômico de Thomson. Ferry e Marcelos (2013) sugerem em seu trabalho que, embora todos os discentes participantes reconhecessem a natureza elétrica do modelo atômico de Thomson, não significa que a concepção de sua neutralidade seja apontada pelos estudantes, uma vez que essa última ideia pode não estar consolidada, se constituindo como um aspecto irrelevante ou subentendida para eles. Mesmo que os dados evidenciados indiquem uma baixa concepção sobre a neutralidade elétrica do modelo atômico de Thomson, a presença desse conhecimento é importante, uma vez que caracterizaria que o discente tem a consciência da existência de um modelo estável, apesar da presença de cargas positivas e negativas.
4.4 Eixo de Análise 4: Confronto entre o modelo atômico de Thomson (1904) com o encontrado no livro didático e as respostas dos alunos
Neste eixo de análise, emergiu a última categoria, denominada de Confronto de
conceitos e concepções. Nesta categoria, buscou-se entender o fenômeno que surgiu
durante a ATD, a partir do confronto do conteúdo do livro didático e das respostas dos alunos com dois pontos chaves do artigo publicado por Thomson em 1904 (THOMSON, 1904): (i) como Thomson propôs o seu modelo, e (ii) como este modelo era rico, apesar das limitações da época. Segundo Lopes (2009), o artigo de Thomson se tornou referência obrigatória no período de 1904, bem como na história dos modelos atômicos. Esse artigo sintetizava as principais ideias de Thomson sobre o átomo constituído pelos corpúsculos. De acordo com Lopes e Martins (2000), para determinar o arranjo dos
639 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 corpúsculos nos anéis, Thomson, assim como Kelvin, utilizou a analogia com os imãs flutuantes investigados por Mayer. No trecho a seguir, Thomson descreve de forma minuciosa sua proposta de modelo atômico.
Temos assim, em primeiro lugar, uma esfera de eletrificação positiva uniforme, e dentro desta esfera um número de corpúsculos dispostos em uma série de anéis paralelos, o número de corpúsculos em cada anel varia de anel para anel: cada corpúsculo está viajando a uma alta velocidade em volta do anel em que está situado, e os anéis estão dispostos de forma que aqueles que contêm um grande número de corpúsculos estão perto da superfície da esfera, enquanto aqueles que tem um menor número de corpúsculos estão mais no interior. (THOMSON, 1904, p. 254-255, tradução nossa).
A partir deste trecho, observa-se que o modelo atômico de Thomson era rico e detalhado e durante a especificação não é difícil observar uma certa familiaridade com o que hoje se conhece como modelo atômico de Bohr. Segundo Lopes (2009), por motivos de estabilidade eletrodinâmica, Thomson apresentou uma distribuição inversa dos modelos atômicos de Rutherford-Bohr e Nicholson, que propunham, de forma geral, um núcleo positivo e anéis interiores com mais elétrons que o anel exterior. Quando foi analisada a ilustração do livro didático (Figura 4), que representa o modelo atômico de Thomson, não é possível observar características como “rotação” e formação de “anéis”, que são os pontos chaves do artigo de 1904. No livro didático analisado para este trabalho, é indicado a presença de pequenos círculos com um sinal de negativo no meio sem qualquer identificação e distribuídos de forma desorganizada (Figura 4). Verificou-se no Eixo de Análise 3, que a maioria dos alunos também caracterizam esta concepção, por exemplo, na Figura 7, é apresentado a representação do modelo atômico de Thomson de um aluno com grande semelhança ao do livro didático (Figura 4), exemplificando a influência do material no entendimento deste discente: “região dotada de carga positiva” (A3).
Figura 7: Representação do modelo atômico de Thomson por um discente.
Fonte: Arquivo dos autores.
De acordo com Hon e Goldstein (2013), a primeira evidência impressa sobre a expressão “pudim de passas”, com relação ao modelo atômico de Thomson, se deu por um relato de um repórter, que assistia a uma série de palestras ministradas por Thomson. Em seu trabalho, Hon e Goldstein (2013) descrevem que,
640 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020
Entre outras coisas, o professor Thomson sugere [que]... enquanto a eletricidade negativa está concentrada no corpúsculo extremamente pequeno, a eletricidade positiva é distribuída ao longo de um considerável volume. Um átomo consistiria, assim, de pontos minúsculos, onde os corpúsculos negativos estão nadando em uma esfera de eletrificação positiva, como passas em um pudim de ameixa parcimonioso (...). (HON; GOLDSTEIN, 2013, p. 131, tradução nossa.)
O pudim de ameixas (ou passas), ao qual o repórter se referia, é uma sobremesa inglesa muito apreciado no natal (Figura 8a). Apesar da simplicidade do reporte ao fazer uma analogia com o modelo atômico proposto por Thomson, há aspectos da sobremesa que realmente possibilita se fazer uso da analogia. No entanto, quando se observa o pudim de ameixas (ou passas), tradicionalmente feito pelas famílias brasileiras (Figura 8b), não se pode observar nenhuma similaridade que possa ser trabalhada ao se apresentar o modelo atômico de Thomson. Outro análogo presente na cultura brasileira, como a melancia, seria mais adequada para se fazer essa analogia, no entanto, no questionário apresentado aos discentes, nenhum apontou a melancia como a figura que mais se aproxima do modelo atômico de Thomson.
Figura 8: (a) Pudim de passas inglês e (b) Pudim de passas brasileiro.
(a)
Fonte: Google. Disponível em: encurtador.com.br/tL147.
(b)
Fonte: Google. Disponível em: encurtador.com.br/dhlQW.
O modelo atômico proposto por Thomson em 1904 apresentava um raciocínio detalhado de como ele acreditava que fosse uma ligação iônica.
Quando átomos eletronegativos, nos quais os corpúsculos são muito estáveis, são misturados com átomos eletropositivos, nos quais os corpúsculos não são tão firmemente mantidos, as forças às quais os corpúsculos estão sujeitos pela ação dos átomos sobre um ao outro pode resultar na separação de corpúsculos dos átomos eletropositivos e sua transferência para o eletronegativo. Os átomos eletronegativos receberão, assim, uma carga de eletricidade negativa, os átomos eletropositivos, estarão com uma carga positiva, os átomos de carga oposta se atrairão e um composto químico dos átomos eletropositivos e negativos será formado. (THOMSON, 1904, p. 262-263, tradução nossa.)
641 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 De acordo com as informações dos trechos do artigo de Thomson, citados anteriormente (THOMSON, 1904, p. 254-255 e p. 262-263), e com o modelo atômico apresentado na Figura 4 do livro didático, conclui-se que não é possível identificar similaridades que tornam a Figura 4 um modelo correto para exemplificar o modelo atômico proposto por Thomson.
5 Considerações finais
Foi possível verificar que o livro didático e as abordagens do docente são as bases do conhecimento adquirido pelos discentes. Nos dados relatados, o livro didático mostrou ser a principal referência sobre o modelo atômico de Thomson para o docente e os discentes. Este fato reforça a necessidade de os livros didáticos trazerem informações claras, completas e que estejam coerentes com a realidade dos usuários, principalmente dos discentes. O livro didático, utilizado pela escola, apresenta o modelo atômico de Thomson que ao ser comparado com o modelo publicado no artigo de 1904, conclui-se que são distintos, não existindo a coerência necessária para um bom entendimento do modelo proposto.
As principais estratégias de ensino utilizadas pelo docente de Química para trabalhar o modelo atômico de Thomson não proporcionam aos discentes o entendimento apropriado do modelo. Para que este fosse trabalhado de forma adequada, de modo que os discentes compreendessem o seu funcionamento, o docente necessitaria criar estratégias de ensino e abordar pontos que estão além do livro didático, reforçando a necessidade de o mesmo buscar outras fontes.
A concepção da maior parte dos estudantes sobre o modelo atômico de Thomson é a do ’pudim de passas’, e não foi possível identificar se os discentes compreendem as limitações desta analogia. Também foi possível constatar que o modelo atômico de Thomson, na forma de um ‘pudim de passas’, é a analogia predominante no discurso dos autores do livro didático analisado, do professor de Química e dos discentes da pesquisa. Neste sentido, pode-se verificar que esta abordagem faz com que os alunos apresentem uma dificuldade em compreender as características e conceitos essenciais deste modelo. A atuação do PIBID na escola participante possibilitou estas constatações e contribuiu para a formação continuada do docente supervisor. Para uma aprendizagem mais significativa, é importante que os livros didáticos tragam analogias coerentes com o contexto cultural em que os discentes estão inseridos. Infelizmente, ainda não existe um consenso de que a nova Base Nacional Comum Curricular (BNCC) (BRASIL, 2018) possa ser utilizada para contornar possíveis descontextualizações que foram encontradas nesta pesquisa e nos relatos apresentados, porém ela, juntamente com os currículos estaduais e os Projetos Políticos Pedagógicos de cada escola, apresentam possibilidades para que as práticas pedagógicas dos docentes sejam diversificadas: “valorizar a diversidade de saberes e vivências culturais dos discentes” (BRASIL, 2018).
642 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020
6 Referências
BRASIL. Base Nacional Comum Curricular. Brasília: MEC, 2018. Disponível em: http://basenacionalcomum.mec.gov.br/images/BNCC_EI_EF_110518_versaofinal_site.pdf . Acesso em: 19 de dez. de 2019.
CHAVES, L. M. M. P.; SANTOS, W. L. P. D.; CARNEIRO, M. H. D. S. História da Ciência no Estudo de Modelos Atômicos em Livros Didáticos de Química e Concepções de Ciência. Química Nova na Escola, São Paulo, v. 36, n. 4., p. 269-279, 2014. Disponível em: http://qnesc.sbq.org.br/online/qnesc36_4/05-HQ-176-12.pdf.
DUARTE, M. C. Analogia na Educação em Ciências Contributos e Desafios. Investigação
em Ensino de Ciências, v. 10, n. 1., p.7-29, 2005. Disponível em: https://www.if.ufrgs.br/cref/ojs/index.php/ienci/article/view/520/317.
FERRY, A. S.; MARCELOS, M. F. Concepções de estudantes acerca de analogias elaboradas para o ensino de teorias atômicas: o modelo de Thomson e um pudim de ameixas. In: IX Congreso Internacional Sobre Investigación En Didáctica De Las Ciencias, 11., 2013, Girona, ES. Anais… Girona, 2013.
JUNIOR, W. E. F. Analogias em livros didáticos de química: um estudo das obras aprovadas pelo Plano Nacional do Livro Didático Para o Ensino Médio 2007. Ciências &
Cognição, Rio de Janeiro, v. 14, n. 1, p. 121-143, 2009. Disponível em:
http://www.cienciasecognicao.org/pdf/v14_1/m318350.pdf.
FRISON, M. D.; VIANNA, J.; CHAVES, J. M.; BERNARDI, F. N. Livro didático como instrumento de apoio para construção de propostas de ensino de ciências naturais. In: VII - Encontro Nacional de Pesquisa em Educação em Ciências, 7., 2000, Florianópolis, SC.
Anais… Florianópolis, 2000.
HON, G.; GOLDSTEIN, B. R. J. J. Thomson’s plum-pudding atomic model: The making of a scientific myth. Annalen der Physik, Berlin, 525, p. 129-133, 2013. Disponível em: https://onlinelibrary.wiley.com/doi/full/10.1002/andp.201300732.
LISBOA, J. C. F. et al. Ser protagonista: química, 1º ano: Ensino médio. Ediçao SM; ed. 3. v. 1. São Paulo, 2016.
LOPES, C. V. M. Modelos atômicos no início do século XX: da física clássica à introdução da teoria quântica. 173f. 2009. Tese (Doutorado em História da Ciência). Pontifícia Universidade Católica de São Paulo, São Paulo, 2009.
LOPES, C. V. M.; MARTINS, R. D. A. J. J. Thomson e o uso de analogias para explicar os modelos atômicos: O pudim de passas nos livros texto. In: VII - Encontro Nacional de Pesquisa e Educação em Ciências, 7., 2000, Florianópolis, SC. Anais... Florianópolis, 2000.
LÜDKE, M.; ANDRÉ, M. E. D. A. Pesquisa em educação: abordagens qualitativas. São Paulo: EPU, 1986.
643 REnCiMa, São Paulo, v. 11, n. 6, p. 624-643, out./dez. 2020 MELO, M. R.; NETO, E. G. D. L. Dificuldades de Ensino e Aprendizagem dos Modelos; Atômicos em Química. Química Nova na Escola. São Paulo, v. 35, n. 2, p. 112-122, Maio 2013. Disponível em: http://qnesc.sbq.org.br/online/qnesc35_2/08-PE-81-10.pdf.
MELZER, E. E. M.; AIRES, J. A. A. História do desenvolvimento da teoria atômica: um percurso de Dalton a Bohr. Amazônia - Revista de Educação em Ciências e
Matemática. Belém, v. 11, n. 22, p. 62-77, 2015. Disponível em: https://periodicos.ufpa.br/index.php/revistaamazonia/article/download/2137/2635.
MONTEIRO, I. G.; JUSTI, R. S. Analogias em livros didáticos de química brasileiros destinados ao ensino médio. Investigações em Ensino de Ciências. Porto Alegre, v.5,
n. 2, pp. 67-91, 2000. Disponível em:
https://www.if.ufrgs.br/cref/ojs/index.php/ienci/article/download/650/441.
MORAES, R.; GALIAZZI, M. C. Análise Textual Discursiva. Ijuí: UNIJUÍ, 2016.
MOTA, G. C; CLEOPHAS, M. G. História da Ciência: elaborando critérios para analisar a temática dos livros didáticos de química no ensino médio. História da Ciência e Ensino:
Construido Interfaces, v. 11, p. 33-55, 2015. Disponível em: https://revistas.pucsp.br/hcensino/article/viewFile/17476/16768.
MUNARIN, K. D. O.; MUNARIN, E. E. D. O. Uma análise crítica das analogias “bola de bilhar”, “pudim de passas” e “sistema solar” utilizadas para o ensino de química em modelos atômicos. In: XIV Encontro Nacional de Ensino de Química, 14., 2008, Curitiba, PR. Anais... Curitiba.
RAMOS, T. C.; MOZZER, N. B. Análise do Uso da Analogia com o “Pudim de Passas” Guiado pelo TWA no ensino do modelo atômico de Thomson: considerações e recomendações. Ensino de Química na Escola, São Paulo, v. 40, p. 106-115, 2018. Disponível em: http://qnesc.sbq.org.br/online/qnesc40_2/07-EQF-27-17.pdf.
SANTOS, W. D.; DOS SANTOS JÚNIOR, J.; DE SOUZA VELASQUE, L. O Desenvolvimento do Letramento Estatístico pelos Livros Didáticos e a Base Nacional Comum Curricular. Revista de Ensino de Ciências e Matemática, São Paulo, v. 9, n. 2,
p. 210-229, 2018. Disponível em:
http://revistapos.cruzeirodosul.edu.br/index.php/rencima/article/view/1664.
THOMSON, J. J. XXIV. On the structure of the atom: an investigation of the stability and periods of oscillation of a number of corpuscles arranged at equal intervals around the circumference of a circle; with application of the results to the theory of atomic structure.
Philosophical Magazine (1798-1977), v. 39, n. 7, p. 237-265, 1904. Disponível em: