U FOP - CET EC - U EM G
REDEMAT
R
EDET
EMÁTICA EME
NGENHARIA DEM
ATERIAISUFOP – CETEC – UEMG
Tese de Doutorado
"Cerâmicas de mulita obtida do topázio, fabricação
por sinterização, caracterizações microestrutural,
elétrica e mecânica"
Autor: Robson de Miranda Soares
Orientador: Prof. Dr. Antônio Claret Soares Sabioni
Co-orientador: Prof. Dr. Leonardo B. Godefroid
U FOP - CET EC - U EM G
REDEMAT
R
EDET
EMÁTICA EME
NGENHARIA DEM
ATERIAISUFOP – CETEC – UEMG
Robson de Miranda Soares
"
Cerâmicas de mulita obtida do topázio, fabricação por
sinterização, caracterizações microestrutural, elétrica e mecânica
"
Tese de Doutorado apresentada ao Programa de Pós-Graduação em Engenharia de Materiais da REDEMAT, como parte integrante dos requisitos para a obtenção do título de Doutor em Engenharia de Materiais.
Área de concentração: Processos de Fabricação
Orientador: Prof. Dr. Antônio Claret Soares Sabioni
Co-orientador: Prof. Dr. Leonardo Barbosa Godefroid
DEDICATÓRIA
A minha esposa Vera, aos filhos Alessandra e Vinícius, pela paciência, compreensão e força nos momentos difíceis. Aos meus pais (in memorian) Almério e Diolinda, pelo incentivo aos estudos.
“O discípulo não é superior ao mestre; mas o discípulo bem formado será como o seu mestre”.
AGRADECIMENTOS
Agradeço ao Prof. Dr. Antônio Claret S. Sabioni, por conduzir o trabalho de orientação de forma contínua, clara e serena. Sempre presente em todos os momentos, fornecendo os suportes necessários e transmitindo segurança e tranqüilidade.
Ao Diretor do CEFET-ES José Jadir Pella e aos Professores da Coordenadoria de Metalurgia e Materiais, pela política de incentivo ao aprimoramento Profissional dos Docentes, possibilitando com isto um ensino de melhor qualidade.
A REDEMAT- UFOP pelo apoio técnico e financeiro na realização deste trabalho.
Aos Professores e funcionários dos Departamentos de Física, Geologia, Metalurgia, Química e Minas, e ao NUPEB-ICEB, que colaboraram direta ou indiretamente com a realização deste trabalho.
Aos Professores André B. Cota (Laboratório de tratamento térmico - DEFIS-ICEB-UFOP),
Geraldo Magela da Costa (Laboratório de difração de raios X - DEQUI-ICEB-UFOP) e Kátia Monteiro Novack (Laboratório de análise térmica - DEQUI-ICEB-UFOP), Fernando Von Krieger (DEMET-UFOP), Leonardo Barbosa Godefroid (Laboratório de ensaios mecânicos - DEMET-UFOP) e Rosa Malena (Laboratório de sistemas particulados - DEMIN-UFOP), que contribuíram na preparação e caracterização dos materiais cerâmicos e das cerâmicas utilizadas neste trabalho.
À professora Inês Sabioni Resck (UnB-DF) e sua equipe de trabalho, que colaboraram na caracterização da mulita do topázio, por ressonância magnética nuclear.
Ao Prof. Wilmar B. Ferraz (CDTN-BH-MG) que colaborou na preparação de pastilhas de mulita do topázio, nas medidas de suas densidades e das resistências à tração por compressão diametral.
Ao Prof. Demétrio Artur Werner Soares (UNIFEI-Itajubá-MG) que contribuiu na caracterização das medidas elétricas das amostras de cerâmicas de mulita.
À equipe do Laboratório de Difusão em Materiais (DEFIS-ICEB-UFOP) pela amizade, alegria e cooperação na realização dos trabalhos. À Fátima por ter colaborado na elaboração dos slides para a apresentação da tese.
Ao Eng. Sidney Cardoso de Araújo (DEMET-UFOP) pela colaboração e sugestões nos trabalhos de indentação e outros.
Ao técnico Graciliano Dimas Francisco (DEMET-UFOP) pela colaboração nas determinações das densidades, BET e outros.
SUMÁRIO
página
DEDICATÓRIA iii
AGRADECIMENTOS iv
SUMÁRIO vi
LISTA DE FIGURAS x
LISTA DE TABELAS xiv
RESUMO xviii
ABSTRACT xx
CAPÍTULO 1 - INTRODUÇÃO 1
CAPÍTULO 2 – OBJETIVOS 4
CAPÍTULO 3 – REVISÃO BIBLIOGRÁFICA 5
3.1- MULITA 5
3.1.1- Sistema Al2O3-SiO2 5
3.1.2- Estrutura cristalina 6
3.1.3- Composição 8
3.1.4- Massa específica 11
3.1.5- Resistividade elétrica 12
3.1.6- Propriedades físicas e mecânicas 13
3.1.7- Espectroscopia de ressonância magnética nuclear com rotação no ângulo mágico de 29Si e 27Al (29Si e 27Al MAS RMN)
18
3.1.8- Expansão térmica 24
3.2- MINERAL TOPÁZIO 26
3.2.1-Calcinação do topázio 26
3.3- RESISTÊNCIA À TRAÇÃO POR COMPRESSÃO DIAMETRAL 28
3.4-TRATAMENTO ESTATÍSTICO DOS RESULTADOS DA RESISTÊNCIA– DISTRIBUIÇÃO DE WEIBULL
3.5 - TENACIDADE À FRATURA 34
3.5.1- Medida da tenacidade à fratura utilizando a técnica da indentação
Vickers por medida direta dos traços de trincas
34
3.5.1.1- Diagrama universal deformação / fratura 35
3.6 - PROCESSO DE CONFORMAÇÃO POR COLAGEM DE BARBOTINA (SLIP CASTING )
42
3.6.1- Sistema barbotina/gesso 43
3.6.2- Parâmetros do processo de colagem de barbotina 44
3.6.2.1-Mecanismo de formação da parede 44
3.6.2.2-Características de barbotinas. 45
3.6.2.3-Aditivos utilizados 46
3.7 - INTERVALO DE CONFIANÇA 47
CAPÍTULO 4 – MATERIAIS E MÉTODOS 48
4.1- MATERIAIS 48
4.2- METODOLOGIAS 48
4.2.1-Elaboração das amostras 48
4.2.1.1- Preparação do pó de topázio incolor 48
4.2.1.2- Transformação do mineral topázio incolor em mulita 49
4.2.1.3- Processos de fragmentação dos agregados de mulita 51
4.2.1.4- Preparação da sílica obtida por meio da queima da casca de arroz tratada quimicamente.
52
4.3- MULITA M1,63 COM ADIÇÃO DE SÍLICA OU ALUMINA 54
4.4- CONFORMAÇÃO A FRIO 55
4.5- SINTERIZAÇÃO DAS PASTILHAS ″VERDES″ DE MULITA 56
4.6- CARACTERIZAÇÃO POR DIFRAÇÃO DE RAIOS-X 57
4.7-CARACTERIZAÇÃO MICROESTRUTURAL POR MICROSCOPIA
ELETRONICA DE VARREDURA (MEV)
58
4.7.1-Preparação ceramográfica das amostras 58
4.8- RESISTIVIDADE ELÉTRICA 59
4.8.1-Variação da resistividade elétrica com a temperatura 60
4.9- CARACTERIZAÇÃO QUÍMICA 61
4.11- DISTRIBUIÇÃO GRANULOMÉTRICA DAS PARTÍCULAS 62
4.12- RESSONÂNCIA MAGNÉTICA NUCLEAR COM ROTAÇÃO NO ÂNGULO MÁGICO (RMN MAS)
62
4.13- TENACIDADE À FRATURA - KIc 63
4.14-RESISTÊNCIA À TRAÇÃO POR COMPRESSÃO DIAMETRAL -
σtração
65
CAPÍTULO 5 - RESULTADOS E DISCUSSÕES 66
5.1- CARACTERIZAÇÃO QUÍMICA DAS MATÉRIAS PRIMAS 66
5.1.1-Mineral topázio incolor 66
5.1.2-Mulita 66
5.1.3-Sílica da casca de arroz purificada 67
5.1.4-Alumina 68
5.1.5-Mulita M-76h 68
5.2-CARACTERIZAÇÃO MICROESTRUTURAL DOS PÓS DE TOPÁZIO E
DE MULITA - MICROSCOPIA ELETRONICA DE VARREDURA (MEV)
68
5.3-TAMANHO DE PARTÍCULAS E ÁREA SUPERFÍCIAL ESPECÍFICA
DOS PÓS DO MINERAL TOPÁZIO INCOLOR, DA SÍLICA, DA ALUMINA E DA MULITA
73
5.4- CARACTERIZAÇÃO POR DIFRAÇÃO DE RAIOS X DAS MATÉRIAS
PRIMAS EM FORMA DE PÓ
75
5.4.1-Mineral topázio incolor 75
5.4.2-Mulita M1,63 76
5.4.3-Sílica da casca de arroz purificada 77
5.4.4-Mulita M-6h 77
5.4.5- Mulita M1,63 com adição de sílica ou alumina 78
5.5- CONFORMAÇÃO POR PRENSAGEM 79
5.6- SINTERIZAÇÃO DAS PASTILHAS VERDES 79
5.7- CARACTERIZAÇÃO POR DIFRAÇÃO DE RAIOS X DAS PASTILHAS
SINTERIZADAS
83
5.8- PORCENTAGEM MOLAR (m) E RELAÇÃO Al2O3/SiO2 84
5.9- LACUNAS DE OXIGÊNIO POR CÉLULA UNITÁRIA (x) DA MULITA 1,63:1
85
5.10- MICROESTRUTURAS DE MULITAS SINTERIZADAS 86
5.12- CARACTERIZAÇÃO ESTRUTURAL POR RESSONÂNCIA MAGNÉTICA NUCLEAR COM ROTAÇÃO NO ÂNGULO MÁGICO (RMN MAS)
99
5.13 - RESISTÊNCIA À TRAÇÃO POR COMPRESSÃO DIAMETRAL 103
5.13.1 - Mulita M-100-6h 104
5.13.2 -Mulita M-100-76h 108
5.14 - TENACIDADE À FRATURA - KIc PARA A MULITA DO TOPÁZIO
UTILIZANDO A INDENTAÇÃO VICKERS POR MEDIDA DIRETA DE TRAÇOS DE TRINCAS
113
5.14.1- Utilizando o valor de 0,069 ± 0,007 para a relação
H E §R
v ,
conforme a referência [45]
115
5.14.2- Utilizando o valor de R v
§ igual a 0,016 ± 0,004 conforme a
referência [79]
122
5.15- PREPARAÇÃO DE PRODUTOS CERÂMICOS POR COLAGEM
UTILIZANDO BARBOTINA DE TOPÁZIO E DE MULITA
123
CAPÍTULO 6 - CONCLUSÕES 127
CAPÍTULO 7 - REFERÊNCIAS BIBLIOGRÁFICAS 130
LISTA DE FIGURAS
Figura 3.1 - Diagrama de equilíbrio de fases do sistema Al2O3-SiO2. 5
Figura 3.2 - Estrutura cristalina da mulita em uma projeção ao longo do eixo
cristalográfico c e sobre o plano ab. Duas células unitárias são desenhadas ao longo de b
7
Figura 3.3 - Parâmetros de rede a, b e c de mulitas. A linha reta para o parâmetro
a resulta de uma regressão linear, as curvas para b e c foram ajustadas manualmente.
9
Figura 3.4 - Módulo de Young de mulitas em função da porosidade, determinado
com a equação de Spriggs; HP = prensado a quente e S = prensado a frio e sinterizado.
17
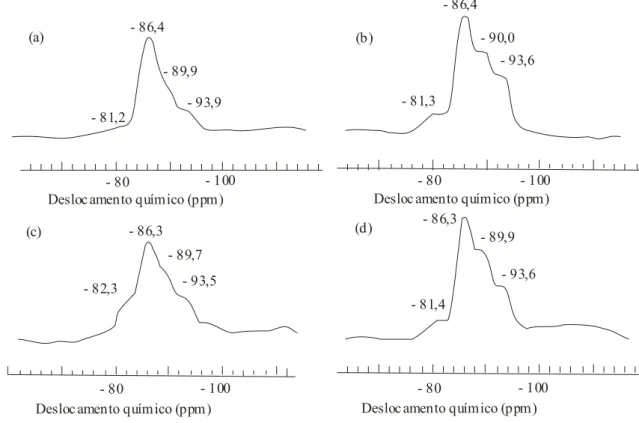
Figura 3.5 - Espectroscopia de ressonância magnética nuclear com rotação no
ângulo mágico do 29Si: (a) Mulita-H com 60% e mols de Al2O3 ; (b)
Mulita-H com 64% e mols de Al2O3 ; (c) Mulita-H com 70% e mols
de Al2O3 e (d) Mulita-L com 64% e mols de Al2O3.
22
Figura 3.6 - (a) Foto da Igreja de São Pedro dos Clérigos – Rio de Janeiro e (b)
Ilustração da simulação do deslocamento sobre rolos.
29
Figura 3.7 - Desenho esquemático do teste de compressão diametral. 29
Figura 3.8 - Diagrama de Weibull 33
Figura 3.9 - Micrografia (MEV) de uma impressão Vickers mostrando os traços
das trincas radiais em uma pastilha de mulita M100-6h, utilizando carga de 10kg (Laboratório de difusão em materiais – REDEMAT-DEFIS – UFOP).
35
Figura 3.10 - Padrão idealizado deformação/fratura para o indentador piramidal
Vickers, mostrando (A) iniciação e (B) estágios de propagação da trinca mediana desenvolvida.
37
Figura 3.11 - Micrografia (MEV) de uma impressão Vickers com lascamento de
uma pastilha de mulita M100-6h, utilizando uma carga de 20kg (Laboratório de difusão em materiais – REDEMAT - DEFIS – UFOP).
40
Figura 3.12 - Formação de trincas por indentação Vickers. 40
Figura 3.13 - Seqüência de produção de peças cerâmicas pelo processo de
colagem. (a) molde de gesso, (b) barbotina de mulita ou topázio natural incolor, (c-e) vazamento e colagem da barbotina, (f) drenagem da barbotina e (g-h) peças “verdes”. Laboratório de cerâmica do CEFET-ES.
Figura 3.14 - Volume de água absorvido em função da consistência do molde. 43
Figura 3.15 - Resistência do molde e da barbotina em função da consistência. 44
Figura 4.1- (a) Fotos: (a) Cristal de mineral topázio incolor e (b) Pó do mineral
topázio incolor.
49
Figura 4.2 - Ciclo térmico, para a calcinação do pó do mineral topázio incolor,
aquecido até 1100ºC e mantido à temperatura de 1340ºC durante 3h e resfriado naturalmente no forno.
50
Figura 4.3 - Aglomerado de mulita resultante do processo de calcinação do
topázio incolor à temperatura de 1340ºC durante 3h.
51
Figura 4.4 - Moinho de Bolas NTK-MARCONI, Laboratório de Cerâmica da
Coordenadoria de Metalurgia e Materiais – CEFET-ES.
52
Figura 4.5 - Foto da panela de pedra sabão contendo a casca de arroz purificada. 53
Figura 4.6 - Pó de sílica resultante do processo de queima da casca de arroz
purificada.
53
Figura 4.7 - Ciclo térmico para a queima à temperatura de 550ºC durante 2h da
casca de arroz purificada.
54
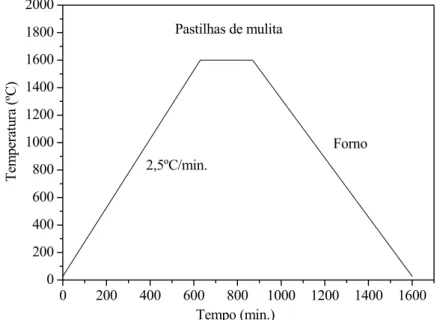
Figura 4.8 - Ciclo térmico para a sinterização de pastilhas de mulita em um forno
mufla EDG 1700ºC à temperatura de 1600ºC durante 4h.
56
Figura 4.9 - Fotografia de uma pastilha de mulita com altura de 10,87mm e
diâmetro de 9,23mm, prensada a 100kN/cm2 e sinterizada a 1600ºC
durante 4h, no CDTN.
57
Figura 4.10 - Politriz automática Phoenix 4000, Laboratório de Difusão em
Materiais do Departamento de Física da UFOP.
59
Figura 4.11 - Pastilha de mulita recobertas com um filme de carbono, com o
auxilio do evaporador a vácuo, modelo JEOL-4C pertencente ao Departamento de Geologia da UFOP.
59
Figura 4.12 - Arranjo experimental para a determinação da resistividade elétrica. 60
Figura 4.13 - Representação esquemática do Gráfico de Arrhenius ln ρ em função
do inverso da temperatura.
61
Figura 4.14 - Micrografias de uma impressão Vickers, realizada em uma pastilha
de mulita, utilizando carga de 15,625kg. Aumento de 120X.
64
Figura 5.1 - Micrografia de partículas do mineral topázio incolor obtidas por
moagem autógena a úmido de cristais de topázio, conforme ilustra a Figura 4.1(a). Aumento de 2000 vezes.
70
Figura 5.2 - Micrografia da superfície de um aglomerado de partículas de mulita
M1,63. Aumento de 500 vezes.
70
Figura 5.3 - Micrografia de partículas de mulita no aglomerado da Figura 5.2.
Aumento de 1500 vezes.
Figura 5.4 - Micrografia de partículas de mulita no aglomerado da Figura 5.2. Aumento de 10000 vezes.
71
Figura 5.5 - Micrografias da mulita M1,63 após desagregação/fragmentação em
gral de cerâmica (M1,63). Aumento de 17000 vezes.
71
Figura 5.6 - Micrografias da mulita M1,63 após fragmentação em moinho de
disco orbital MA 360 durante 15 minutos (M-15m). Aumento de 23000 vezes.
71
Figura 5.7 - Micrografias da mulita M1,63 após fragmentação em moinho de
bolas durante 76h (M-76h). Aumento de 22000 vezes.
72
Figura 5.8 - Distribuição granulométrica do topázio incolor moído a úmido por
73h (moagem autógena), da mulita moída a seco em moinho de disco orbital por 15 minutos e da mulita moída a úmido em moinho de bolas por 6h e 76h, respectivamente.
73
Figura 5.9 - Difratograma de raios-X (Cukα1) do mineral topázio incolor. 75
Figura 5.10 - Difratograma de raios-X (CoKα1) da mulita M 1,63.. 76
Figura 5.11 - Difratograma de raios-X (CoKα1) da sílica obtida pela queima a
550ºC durante 2h da casca de arroz purificada.
77
Figura 5.12 - Difratograma de raios-X (CuKα1) da mulita M-6h. 77
Figura 5.13 - Difratogramas de raios-X (CoKα1) de mulitas: a) 76h, b)
M-Al2O3 (CPTT) e c) M-SiO2 (CPTT).
78
Figura 5.14 - Difratogramas de raios-X (CoKα1) de pastilhas de mulitas obtidas
pela conformação por prensagem a 60 ou 100kN/cm2 e sinterizadas a
1600°C durante 4h: a) M100-76h, b) M60-Al2O3 (CPTT) e c)
M60-SiO2 (CPTT).
83
Figura 5.15 - Micrografia da amostra de mulita M60: a) superfície polida da
amostra e b) o interior de um poro na superfície da amostra. Aumentos de 1000 e 10000 vezes.
88
Figura 5.16 - Micrografia da superfície polida da mulita M60-SiO2 (CPTT).
Aumento de 1000 vezes.
88
Figura 5.17 - Micrografia da superfície polida da mulita M60-Al2O3 (CPTT).
Aumento de 2500 vezes.
89
Figura 5.18 - Micrografia da superfície polida da amostra de mulita M100-15m.
Aumento de 5000 vezes.
89
Figura 5.19 - Micrografia da superfície polida da mulita M100-6h. Aumento de
5000 vezes.
89
Figura 5.20 - Micrografia da superfície polida da mulita M60-76h. Aumento de
10000 vezes.
90
Figura 5.21- Micrografia da superfície polida da mulita M100-76h. Aumento de
10000 vezes
Figura 5.22 - Curvas corrente em função da tensão, a diferentes temperaturas, para mulita M60.
95
Figura 5.23 - Gráfico de ln ρ em função do inverso da temperatura para a amostra
de mulita M60.
95
Figura 5.24 - Curvas corrente em função da tensão da amostra de mulita
M100-15m em função da temperatura. Cada gráfico ilustra as medições nos intervalos: (a) acima de 250°C; (b) entre 160 e 250°C; (c) abaixo de 150°C.
96
Figura 5.25 - Gráfico de lnρ1 em função do inverso da temperatura para a amostra
mulita M100-15m, para baixas tensões (<20V).
97
Figura 5.26 - Gráfico de lnρ em função do inverso da temperatura para a amostra
de solução sólida de mulita M60-SiO2.
97
Figura 5.27 - Gráfico de lnρ em função do inverso da temperatura para a amostra
solução sólida de mulita M60-Al2O3.
97
Figura 5.28 - Resistividade elétrica (ρ) das amostras de mulita M60, M100-15m,
M60-SiO2 e M60-Al2O3 em função da temperatura.
98
Figura 5.29 - Espectros RMN-MAS do 29Si experimentais e deconvoluidos das
amostras de mulita M1,63 e M-TT.
100
Figura 5.30 - Difratogramas XRD (FeKα1) dos pós das amostras: (a) mineral
topázio incolor, (b) mulita M1,63 e (c) mulita M1,63 tratada a 1600ºC durante 4h (M-TT).
101
Figura 5.31 - Espectros RMN-MAS do 27Al experimentais e deconvoluidos das
amostras de mulita M1,63 e M-TT.
102
Figura 5.32 - Diagrama de Weibull – Resistência à tração por compressão
diametral de pastilhas de mulita M100-6h.
105
Figura 5.33 - Diagrama de Weibull – Resistência à tração por compressão
diametral de pastilhas de mulita M100-76h.
109
Figura 5.34 - Micrografia (MEV) de uma pastilha de mulita M100-6h (carga
20kg) mostrando a trinca radial/mediana na região lascada da amostra.
113
Figura 5.35 - Ciclo térmico para a calcinação do topázio incolor a 1300ºC – 2h e
sinterização da mulita obtida a 1600ºC durante 2 ou 4h.
124
Figura 5.36 - Cerâmicas de mulita obtidas por colagem utilizando barbotinas: (a)
topázio TM1, TM2 e TM3 e (b) mulita MM1 e MM2.
125
Figura 5.37 - Micrografia da superfície polida da mulita obtida pelo processo de
colagem, utilizando barbotina de topázio natural incolor. Aumentos de 2500 vezes.
126
Figura 5.38 - Micrografia da superfície polida da mulita obtida pelo processo de
colagem, utilizando barbotina de mulita M-76h. Aumentos de 2500 vezes, respectivamente.
LISTA DE TABELAS
Tabela 3.1 - Posições Wickoff, coordenadas e nomes dos sítios da estrutura
“média” da mulita, grupo espacial Pbam (Nº 55).
7
Tabela 3.2 - Identificação, descrição e história térmica das amostras de mulita em
forma de pó.
9
Tabela 3.3 - Parâmetros refinados das amostras de mulita. 10
Tabela 3.4 - Resistividade elétrica das cerâmicas de alumina, cordierita e
porcelana.
13
Tabela 3.5 - Análise espectrográfica por emissão das impurezas da mulita 3:2 14
Tabela 3.6 - Parâmetros de rede da mulita prensada a quente. 14
Tabela 3.7- Propriedades físicas e mecânicas da mulita 3Al2O3.2SiO2 obtida de
derivados alcóxidos.
14
Tabela 3.8 - Análise química da mulita 1,62:1 comercial - Bakowski 193 CR,
França.
15
Tabela 3.9- Propriedades físicas e mecânica da mulita 1,62:1 sinterizada a 1750ºC
por 5h.
15
Tabela 3.10- Propriedades mecânicas à temperatura ambiente da mulita 1,62:1 sinterizada a 1750ºC por 5h.
15
Tabela 3.11- Efeito da porosidade sobre o módulo de Young de mulita, obtido pela
curva de ajuste dos dados para as equações de Spriggs e Hasselmam.
17
Tabela 3.12- Propriedades de cerâmicas de mulita e de alumina. 18
Tabela 3.13- Valores do coeficiente de expansão térmica linear para a mulita 3:2
monocristalina e policristalina
25
Tabela 3.14 - Resultados da tenacidade à fratura (KIc) por indentação Vickers por
medida direta dos traços de trinca dos materiais utilizados no estudo da tenacidade por indentação.
41
Tabela 4.1- Identificação das amostras de mulita em forma de pó. 55
Tabela 5.1- Composição em peso do topázio incolor. 66
Tabela 5.2- Composição em peso resultante da análise química por fluorescência
de raios X da mulita M1,63.
67
Tabela 5.3- Análise química por fluorescência de raios X da sílica obtida pela
queima da casca de arroz purificada.
Tabela 5.4- Análise química por espectrometria de dispersão de energia (EDS) da amostra de mulita M-76h.
68
Tabela 5.5- Diâmetros (D50) das amostras de topázio incolor e de mulitas M-15m,
M-6h e M-76h.
74
Tabela 5.6- Resultados do BET e das densidades dos pós do mineral topázio
incolor, da sílica da casca de arroz e da mulita.
74
Tabela 5.7- Dimensões das partículas de mulita M1,63 fragmentada em almofariz,
mulita M1,63 fragmentada em disco orbital durante 15 minutos (M-15m) e da mulita M1,63 fragmentada em moinho de bolas durante 76h (M-76h).
75
Tabela 5.8- Parâmetros de rede da mulita M1,63 e M-TT e os volumes de suas
células unitárias.
76
Tabela 5.9- Densidades das amostras de mulita fragmentada em moinho orbital
durante 15 minutos, compactadas à pressão uniaxial em uma prensa
com matriz flutuante a 100kN/cm2 e sinterizadas 1600ºC durante 4 h.
79
Tabela 5.10- Densidades das amostras de mulita fragmentada em moinho de bolas
durante 76h, compactadas à pressão uniaxial em uma prensa com matriz flutuante a 60kN/cm2 e sinterizadas 1600ºC durante 4h.
80
Tabela 5.11- Densidades das amostras de mulita fragmentada em moinho de bolas
durante 76h, compactadas à pressão uniaxial em uma prensa com
matriz flutuante a 100kN/cm2 e sinterizada 1600ºC durante 4h.
80
Tabela 5.12- Densidades das amostras de mulita fragmentada em moinho de bolas
durante 6h, compactadas à pressão uniaxial em uma prensa com matriz flutuante a 100kN/cm2 e sinterizadas 1600ºC durante 4h.
81
Tabela 5.13- Densidades das amostras de mulita fragmentada em moinho de bolas
durante 6h, compactadas à pressão uniaxial em uma prensa com matriz flutuante a 100kN/cm2 e sinterizadas 1600ºC durante 4h.
82
Tabela 5.14- Densidades das amostras verdes e sinterizadas de mulita 1,63:1 e de
suas soluções sólidas, compactadas à pressão uniaxial em uma prensa
com matriz flutuante a 60 ou 100kN/cm2 e sinterizadas 1600ºC
durante 4h.
82
Tabela 5.15- Parâmetros de rede da mulita 1,63:1 e de suas soluções sólidas, compactadas à pressão uniaxial em uma prensa com matriz flutuante a
60 ou 100 kN/cm2 e sinterizadas 1600ºC durante 4h.
84
Tabela 5.16- Relação Al2O3/SiO2 em função da composição química (% molar) e
do parâmetro de rede “a” utilizando a equação (3.3).
86
Tabela 5.17- Resistividade elétrica de mulitas medidas em temperaturas até 42ºC. 94
Tabela 5.18- Resistividades elétricas de mulitas para baixas tensões (<20V)
medidas em temperaturas entre 200º e 324 ºC.
94
Tabela 5.20 - Resultados das medidas dos diâmetros, das alturas, das áreas, dos volumes e das massas de 30 pastilhas de mulita M100-6h.
106
Tabela 5.21- Resultados das tensões de ruptura, obtidas no ensaio de compressão
diametral e os dados necessários a construção do diagrama de Weibull das pastilhas de mulita M100-6h.
107
Tabela 5.22 - Resultados das médias dos diâmetros, das alturas, dos volumes e das massas da amostra M100-6h.
107
Tabela 5.23 - Evolução da função Gama (Γ). 108
Tabela 5.24 - Resultados da análise estatística de Weibull para a mulita M100-76h. 109
Tabela 5.25 - Resultados das medidas dos diâmetros, alturas, áreas, volumes e massas de 30 pastilhas de mulita M100-76h.
110
Tabela 5.26 - Resultados das tensões de ruptura, obtidas no ensaio de compressão diametral e os dados necessários à construção do diagrama de Weibull das pastilhas de mulita M100-76h.
111
Tabela 5.27- Resultados das médias dos diâmetros, das alturas, dos volumes, das
massas e das densidades geométricas.
112
Tabela 5.28 - Resultados dos ensaios de flexão a quatro pontos e de tração por compressão diametral de amostras de mulita e alumina.
112
Tabela 5.29 - Valores médios das durezas e tenacidades à fratura de amostras de mulita M100-6h e M100-76h, utilizando cargas de 10kg, 15,625kg e 20kg, relativos às Tabelas 30 (a-c) e 5.31 (a-c).
114
Tabela 5.30 - (a) - Valores da dureza Vickers (HV) utilizando carga de 10kg e da
tenacidade à fratura(KIc) utilizando a Indentação Vickers por medida
direta de traços de trincas, de amostras de mulita M100-6h em forma de pastilha de diâmetro de 10,20mm e altura de 9,26mm e densidade de 95,25% da densidade teórica e sinterizada a 1600ºC durante 0,5h e re-sinterizadas 1600ºC durante 3,5h, conforme descrição no item 4.13.
116
Tabela 5.30 - (b) - Valores da dureza Vickers (HV) utilizando carga de 15,625kg e
da tenacidade à fratura (KIc) utilizando a Indentação Vickers por
medida direta de traços de trincas, de amostras de mulita M100-6h em forma de pastilha de diâmetro de 10,20mm e altura de 9,26mm e densidade de 95,25% da densidade teórica e sinterizada a 1600ºC durante 0,5h e re-sinterizadas 1600ºC durante 3,5h, conforme descrição no item 4.13.
117
Tabela 5.30 - (c) - Valores da dureza Vickers (HV) utilizando carga de 20kg e da tenacidade à fratura (KIc) utilizando a Indentação Vickers por medida
direta de traços de trincas, de amostras de mulita M100-6h em forma de pastilha de diâmetro de 10,20mm e altura de 9,26mm e densidade de 95,25% da densidade teórica e sinterizada a 1600ºC durante 0,5h e re-sinterizadas 1600ºC durante 3,5h, conforme descrição no item 4.13.
Tabela 5.31 - (a) - Valores da dureza Vickers (HV) utilizando cargas de 10kg e da
tenacidade à fratura (KIc) utilizando a indentação Vickers por
medida direta de traços de trincas. de amostras de mulita M100-76h em forma de pastilhas com diâmetro de 9,70mm e altura de 5,15mm e densidade de 99,68% % da densidade teórica, conforme descrição no item 4.13.
119
Tabela 5.31 - (b)- Valores da dureza Vickers (HV) utilizando cargas de 15,625kg e
da tenacidade à fratura (KIc) utilizando a indentação Vickers por
medida direta de traços de trincas de amostras de mulita M100-76h em forma de pastilhas com diâmetro de 9,70mm e altura de 5,15mm e densidade de 99,68% da densidade teórica, conforme descrição no item 4.13.
120
Tabela 5.31 - (c)- Valores da dureza Vickers (HV) utilizando cargas de 20kg e da
tenacidade à fratura (KIc) utilizando a indentação Vickers por
medida direta de traços de trincas de amostras de mulita M100-76h em forma de pastilhas com diâmetro de 9,70mm e altura de 5,15mm e densidade de 99,68% da densidade teórica, conforme descrição no item 4.13.
121
Tabela 5.32 - Valores estimados do módulo de Young para as amostras de mulita M-100-15m e M-100-6h.
RESUMO
O topázio incolor, transparente e de alta pureza utilizado neste trabalho para produzir mulita com a razão Al2O3/SiO2igual a 1,63 (mulita 1,63:1) e com nível de impureza menor do
que 0,26% em peso é do Estado de Minas Gerais. O número de lacunas de oxigênio por célula
unitária (x) da mulita 1,63:1 foi igual a 0,30. A mulita foi produzida pela decomposição
térmica do mineral topázio incolor à temperatura de 1340ºC durante 3h e resfriado naturalmente no forno, em atmosfera oxidante (ar). Foram preparadas soluções sólidas de mulita com razão Al2O3/SiO2variando de 1,39 a 1,80 por meio da adição de sílica ou alumina
à mulita 1,63:1, com objetivo de verificar o efeito da variação da razão alumina/sílica sobre suas propriedades elétricas. Cerâmicas de mulita do topázio foram preparadas pelos processos de prensagem e de colagem. No processo de prensagem foram utilizados pós de mulitas (1,39:1 ; 1,63:1 e 1,80:1) com diferentes granulometrias e pressões de compactação de
60kN/cm2 e 100kN/cm2, sem a utilização de aglomerantes. No processo de colagem foram
utilizados barbotinas de topázio incolor e de mulita 1,63:1, sem a adição de defloculante. Os
corpos verdes foram sinterizados a 1600oC por 4h, em ar. As densificações variaram de
78,48% a 99,68% da densidade teórica de 3,16g/cm3. RMN-MAS do 27Al e 29Si e difração de
raios X, foram utilizados para caracterizar as estruturas de mulitas obtidas por tratamento térmico do topázio a 1340ºC e a 1600ºC. As duas técnicas revelaram a formação de uma mulita muito pura. Nenhuma dessas técnicas detectou fase amorfa nas diferentes amostras de
mulita. O espectro de RMN-MAS do 29Si mostrou quatro picos de ressonância em 81, 86 e
-90 e -94ppm. O pico em -81ppm corresponde ao silício próximo à lacuna de oxigênio na estrutura da mulita. O pico em -86ppm foi relacionado ao sítio tipo silimanita e é a contribuição principal variando de 42 a 50%. Os outros dois picos, em -90ppm e -94ppm, têm sido interpretados como sendo resultantes do rearranjo do sítio tipo silimanita pela
substituição dos tetraedros AlO4 pelo SiO4. Os dados de RMN-MAS do 27Al exibiram três
diferentes picos para as amostras de mulita: dois são atribuídos aos sítios tetraédricos em 40-45 e 63-67ppm, enquanto o terceiro é atribuído a um sítio octaédrico em cerca de - 6ppm. A razão dos sítios de alumínio tetraédrico para octaédrico depende da temperatura usada no tratamento térmico, sendo mais alta em 1600ºC. Medidas de resistividades elétricas de
resistividades elétricas variaram de 1010ohm.m, 25oC, de 104ohm.m a 324ºC. As energias de ativação variaram entre 0,78eV e 0,88eV. Nas condições experimentais utilizadas, a mulita 1,63:1 e suas soluções sólidas apresentaram comportamento de semicondutor intrínseco. Os valores das resistividades elétricas aumentaram com o aumento do teor de alumina. O ensaio de tração por compressão diametral foi utilizado para caracterizar a resistência de cerâmicas
de mulita, prensadas a 100kN/cm2 e sinterizadas a 1600ºC durante 4h, em ar. Os valores das
resistências à ruptura para uma probabilidade de falha de 50%, variaram de 41 a 52MPa e o
módulo de Weibull (m) variou de 5 a 10. Também foi determinado para estas cerâmicas a
tenacidade à fratura (KIc) utilizando a indentação Vickers por medida direta de traços de
trincas. O valores médios encontrados para KIce para a dureza Vickers foram de 1,5MPam1/2 e
10GPa, respectivamente.
ABSTRACT
The colorless, transparent and high purity topaz used in this work to produce mullite with an Al2O3/SiO2 ratio equals to 1.63 (mullite 1.63:1) and with impurity level lower than
0.26wt.% is from the State of Minas Gerais, Brazil. The number of oxygen vacancies per
average unit cell (x) of the mullite 1.63 was found to be 0.30. The mullite was produced by
thermal decomposition of topaz at 1340ºC for 3hours and slow cooling in the turned off
furnace, in an oxidizing atmosphere (air). Solid solutions of mullite were prepared with an
Al2O3/SiO2 ratio ranging from 1.39 to 1.80 through the addition of silica or alumina to mullite
1.63:1, with the purpose of examining the effect of variation of Al2O3/SiO2 ratio on their
electrical properties. Mullite ceramics from topaz were prepared by pressing and slip casting processes. In the pressing process mullite powders were used (1.39:1, 1.63:1 e 1.80:1) with different particle sizes and pressed under 60kN/cm2 or 100kN/cm2 pressures, without binders. In the slip casting process topaz and mullite 1.63:1 powder suspensions were used, without dispersants. The green bodies were sintered at 1600oC, for 4hours, in the presence of air. The densifications varied from 78.48% to 99.68% of the theoretical density of 3.16g/cm3. 29Si and
27
Al MAS NMR spectroscopy, and X-ray diffraction were used to characterize the structure of mullite obtained by thermal decomposition of topaz at 1340ºC, and after additional thermal
treatment at 1600ºC. No amorphous phase was detected by these techniques. The 29Si MAS
NMR spectra of the mullite samples showed four resonance peaks at 81, 86, 90 and
-94ppm. The peak at -81ppm corresponds to the silicon near oxygen vacancies in the mullite structure. The peak at -86ppm is related to sillimanite-type site and was the major contribution ranging from 42% to 50%. The two other peaks, at -90.0ppm and –94ppm, have been interpreted as being resulting from rearrangements of the sillimanite-type site by replacing
AlO4 by SiO4 tetrahedra. 27Al MAS NMR data of both samples exhibited three different peaks:
two are attributed to tetrahedral sites at 40-45 and 63-67ppm, while the other is assigned to an octahedral site at about -6ppm. The tetrahedral to octahedral aluminum site ratio depends on
the temperature used in the preparation of the mullite being higher at 1600oC. Measurements
of electrical resistivities of mullite ceramics 1.63:1 and its solid solutions were performed
between 25o and 324ºC. The electrical resistivities ranged from 1010ohm.m, at 25oC, to
conditions used in this work, the mullite obtained from topaz (mullite 1.63:1) and its solid solutions showed an intrinsic semiconductor behavior. The values of the electric resistivities increased with the increase of the content of alumina. Brazilian tensile strength (diametral compression test) was used to characterize the tensile strength of topaz mullite ceramics, pressed at 100kN/cm2 and sintered at 1600ºC for 4 hours, in the presence of air. The values of strength to rupture with 50% failure probability, ranged from 41 to 52MPa and the Weibull modulus (m) ranged from 5 to 10. The fracture toughness (KIc) was also determined for these
ceramics using the Vickers indentation through direct measure of crack traces. The average values found for KIc and for Vickers hardness were 1.5MPam 1/2 and 10GPa, respectively.
CAPÍTULO 1
INTRODUÇÃO
Mulita é um mineral raro na natureza. Ocorre em rochas de sanidina e em superfícies de coríndon-silimanita, no contato de intrusões vulcânicas superaquecidas e em formação hidrotermal pós-vulcânica [1].
O nome mulita é derivado da ilha de Mull (Escócia), onde esse mineral foi encontrado pela primeira vez na natureza. Apesar de ocorrer raramente em rochas naturais, não existe nenhuma fase mineral tão importante em cerâmicas como a mulita. A posição proeminente da mulita é documentada por inúmeros artigos científicos e técnicos, publicados nos últimos anos [1]. Particularmente neste contexto, estão os artigos de Davis e Pask [2], Aksay et al [3] e Schneider et al [4,5].
A importância da mulita em cerâmicas tradicionais e avançadas pode ser explicada pelas propriedades do material: baixa densidade, alta estabilidade térmica, estabilidade em ambientes químicos severos, baixa condutividade térmica, boa resistência mecânica e à fluência. A mais importante característica da mulita e cerâmicas de mulita é sua baixa expansão térmica, que explica a sua estabilidade dimensional em altas temperaturas e a excelente resistência ao choque térmico [1]. Recentemente, o campo de aplicação da mulita foi expandido, não somente, para a engenharia aeroespacial, mas também para a indústria eletrônica como substratos de circuitos integrados (IC) [6-8].
A mulita é a única fase cristalina estável no diagrama de equilíbrio de fases do sistema
Al2O3-SiO2. Quando preparada por pares de difusão safira-sílica fundida [9] ou por materiais
granulados [10], funde-se incongruentemente a cerca de 1828º ± 10ºC e preparada pelo
processo sol-gel funde-se incongruentemente a cerca de 1890º ± 10ºC [10,11]. É uma solução
sólida estável na faixa de 70,5 e 74,0% (% em peso de Al2O3) e metaestável entre
aproximadamente 73,0 e 83% em peso de alumina [9]. Embora conhecida pela fórmula
3Al2O3-2SiO2 (mulita 3:2, 71,8% em peso de Al2O3), a mulita pode apresentar outros valores
para a razão Al2O3/SiO2, como ocorre com a mulita 2:1 (2Al2O3.SiO2, 77,27% em peso de
Al2O3) [12]. Mas mulitas de composições não estequiométricas são possíveis devido à
proposta por Cameron [13,14]: AlVI2 [Al2+2x Si2 -2x]IV O10-x, onde x varia de 0,17 a 0,59 e indica o número de lacunas de oxigênio por célula unitária. Os valores extremos desta fórmula geral correspondem aos minerais silimanita (x = 0) e alumina iota (x=1) [4].
A estrutura da mulita consiste de cadeias de octaedros AlO6, compartilhando arestas
alinhadas paralelamente ao eixo cristalográfico c, e ligadas transversalmente por cadeias
duplas de tetraedros de alumínio-oxigênio e silício-oxigênio (AlO4/SiO4), também alinhados
paralelamente ao eixo c [15]. A variação composicional da mulita ocorre devido a
substituição do silício pelo alumínio, com a simultânea formação de lacunas de oxigênio, que pode ser descrita por meio de uma reação de formação de defeitos, usando a notação de
Kröger-Vink [16]:
Al2O3+2SiSix +Oxo ↔2AlSi´ +Vooo +2SiO2 (1.1)
Aumentando o número de lacunas de oxigênio por célula unitária (x), as cadeias
duplas tetraédricas são gradualmente desarranjadas pela remoção das ligações dos átomos de
oxigênio com a formação de novos tetraedros Al*O4. Portanto, quanto mais alto o valor de x,
mais alta a razão de tetraedros de alumínio para silício [16,17].
Levando em conta a importância tecnológica e a grande utilização industrial da mulita, que é rara na natureza como mineral, numerosos processos têm sido utilizados para produzir mulita sintetizada [4].
Neste trabalho foi utilizada mulita com a razão Al2O3/SiO2igual a 1,63 (mulita 1,63:1)
e com 99,74% de pureza. Esta mulita foi obtida pela calcinação do mineral topázio incolor,
que é um flúor silicato de alumínio, com fórmula química Al2SiO4[Fy(OH)1-y]2 [18]. A
preparação de mulita por decomposição térmica do topázio ocorre pela perda de flúor, hidrogênio e silício como gases HF, H2O e SiF4 [18-20]. Esta transformação ocorre somente
quando a temperatura atinge ou excede 1000ºC e pode estar completamente concluída a 1300ºC. A preparação de mulita para aplicações tecnológicas a partir do mineral topázio incolor de alta pureza e baixo custo é uma opção muito atrativa, uma vez que ele tem baixo valor gemológico ou valor comercial e é abundante na natureza [19].
Utilizando como matéria-prima o pó de mulita 1,63:1, foram preparadas soluções sólidas com razão Al2O3/SiO2variando de 1,39 a 1,80 pela adição de sílica e alumina à mulita
Cerâmicas de mulita do topázio foram preparadas pelos processos de prensagem e de colagem. No processo de prensagem foram utilizados pós de mulitas (1,39:1 ; 1,63:1 e 1,80:1)
com diferentes granulometrias e pressõesde compactação de 60kN/cm2 e 100kN/cm2, sem a
utilização de aglomerantes. No processo de colagem foram utilizados barbotinas de topázio e de mulita (1,63:1), sem a adição de defloculante. Os corpos verdes foram sinterizados a
1600oC por 4h, em ar. As densificações variaram de 78,48% a 99,68% da densidade teórica de
3,16g/cm3.
As caracterizações químicas, físicas e mecânicas dos pós de mulita, das cerâmicas de mulita e de suas soluções sólidas foram realizadas utilizando as seguintes técnicas: difração de
raios X; fluorescência de raios X; ressonância magnética nuclear (RMN); adsorção física
(BET); microscopia eletrônica de varredura (MEV); medidas de densidades pelo método do
simples empuxo e com auxílio do multipicnômetro a hélio; resistividades elétricas em função
da temperatura; tenacidade à fratura (KIc) por indentação Vickers, empregando o método de
CAPÍTULO 2
OBJETIVOS
A presente pesquisa teve os seguintes objetivos:
1. Obter mulita de alta pureza e baixo custo.
2. Caracterizar a estrutura cristalina da mulita por ressonância magnética nuclear e raios X.
3. Estudar os efeitos das distribuições granulométricas do pó de mulita obtido por calcinação
do mineral topázio incolor e das pressões de compactação sobre a sinterabilidade das cerâmicas de mulita.
4. Obter corpos cerâmicos de mulita pelo processo de colagem, utilizando barbotina de
topázio incolor e de mulita.
5. Verificar o efeito da razão Al2O3/SiO2 sobre a sinterabilidade e sobre as propriedades
elétricas da mulita.
6. Verificar o comportamento mecânico das cerâmicas de mulita pelos ensaios de compressão
diametral e análise dos resultados pela estatística de Weibull.
7. Realizar ensaios de tenacidade à fratura (KIc) em cerâmicas de mulita utilizando a
CAPÍTULO 3
REVISÃO BIBLIOGRÁFICA
3.1- MULITA
3.1.1- Sistema Al2O3-SiO2
A mulita é a única fase cristalina estável no diagrama de equilíbrio de fases do sistema
Al2O3-SiO2. Quando preparada por pares de difusão safira-sílica fundida [9] ou por materiais
granulados [10], funde-se incongruentemente a cerca de 1828º ± 10ºC e preparada pelo
processo sol-gel funde-se incongruentemente a cerca de 1890º ± 10ºC [10,11]. É uma solução
sólida estável na faixa de 58,43 e 62,60% e metaestável entre aproximadamente 61,39 e 74,17% molar de alumina [9], conforme mostra o diagrama de fases da Figura 3.1.
2000 1900 1800 1700 1600 1500 1400 1300 10 10 20 20 30 30 40 40 50 50 60 60 70 70 80 80 2054º 1828 1587 Líquido
Diagrama de equilíbrio estável Extensão metaestável
Al O 2 3
Al O 2 3
Al O (% em peso) 2 3
Al O (% molar) 2 3
Al O 2 3
SiO 2
T em p er atu ra ( ºC) Líquido Líquido Sílica Mulita (SS) Mulita (SS) Mulita (SS) M ul ita ( S S ) 1726º 1890 10ºC 10ºC 10ºC + + + _ _ _ 90 90 100 + + + +
3.1.2-Estrutura cristalina
A estrutura cristalina da mulita é ortorrômbica e pertence ao grupo espacial Pbam. Ela é formada por cadeias de octaedros AlO6, construídos por íons Al em sítios 2a e átomos de
oxigênio em sítios Oab e Od, compartilhando arestas alinhadas paralelamente ao eixo
cristalográfico c, e ligadas transversalmente por cadeias duplas de tetraedros de
alumínio-oxigênio e silício-alumínio-oxigênio (AlO4/SiO4), com uma distribuição aleatória de átomos de Al e Si
sobre os sítios T, que também estão alinhados paralelamente ao eixo c [15,21].
A variação composicional na mulita resulta da substituição dos cátions Si4+por Al3+e
formação simultânea de lacunas de oxigênio na posição Ocpara manter o balanço de cargas,
que pode ser descrita por meio de uma reação de formação de defeitos, usando a notação de
Kröger-Vink [16]:
Al2O3 +2SiSix + Ox0 ⇔ 2Al'Si + V0oo + 2SiO2 (3.1)
onde V 0oo é uma lacuna de oxigênio ionizada duas vezes positivamente [15].
Aumentando o número de lacunas de oxigênio por célula unitária (x), as cadeias
duplas tetraédricas são gradualmente desarranjadas pela remoção das ligações dos átomos de oxigênio com a formação de novos tetraedros Al*O4, em novas posições T*e o correspondente
vizinho oxigênio será transferido para a posição Oc*. Portanto, quanto mais alto o valor de x,
mais alta a relação tetraédrica de alumínio para silício [15,17]. A Figura 3.2 mostra a estrutura
cristalina da mulita em uma projeção ao longo do eixo cristalográfico c sobre o plano ab.
Duas células unitárias são desenhadas ao longo de b.
O
O
Al(1) Al(2),Si,Al Al
VI IV IV
O-Vacância
O
O
O
C
C
*
*
d
a
a
b
Figura 3.2 – Estrutura cristalina da mulita em uma projeção ao longo do eixo cristalográfico c
sobre o plano ab. Duas células unitárias são desenhadas ao longo de b [17].
No modelo de estrutura “média” da mulita, como determinado por Burnham [21,22] e mais tarde confirmado por Saalfeld e Guse [23] e Angel e Prewitt [24], a distribuição dos átomos nas respectivas posições Wickoff dentro do grupo espacial Pbam (Nº 55) é dada na Tabela 3.1, onde x é o número de lacunas de oxigênio por célula unitária [15,25].
Tabela 3.1- Posições Wickoff, coordenadas e nomes dos sítios da estrutura “média” da mulita,
grupo espacial Pbam (Nº 55) [15].
Átomos Al2 [Al2Si2-2x] Al2x O2 - 3x O2x O4 O4
Posições Wickoff 2 a 4 h 4 h 2 d 4 h 4 h 4 g
Coordenadas 0,0,0 x,y,1/2 x,y,1/2 1/2,0,1/2 x,y,1/2 x,y,1/2 x,y,0
3.1.3-Composição
Mulita é um silicato de alumínio e sua composição pode ser descrita pela fórmula [13,26]:
AlVI2 [Al2+2x Si2 -2x]IV O10-x (3.2)
onde o valor de x varia de 0,17 a 0,59 e indica o número de lacunas de oxigênio por célula
unitária. Os extremos desta fórmula geral são os minerais silimanita (x = 0) e alumina iota (x = 1). Em geral, as composições das mulitas não são estequiométricas. Porém, há composições estequiométricas tais como 3Al2O3.2SiO2 (mulita 3:2), para x = 0,25, ou 2Al2O3.SiO2(mulita
2:1), para x = 0,40, cuja relação Al2O3/SiO2é igual a 1,5 e 2,0, respectivamente [4].
A composição química da mulita a baixa temperatura pode ser obtida por uma relação linear entre seu parâmetro de rede a e a porcentagem molar de Al2O3(m). Usando os dados
obtidos por Fischer et al [27], obtém-se o gráfico mostrado na Figura 3.3. A relação para o cálculo da porcentagem molar m de Al2O3 na mulita é obtida por regressão linear desses dados
[28]:
m = 144,5. a - 1029,5 (3.3)
As incertezas são 0,00008 para A e 0,005 para B conduzindo a erros de cerca de 1,5%
em mol para a determinação de m com esta equação.
O teor molar de Al2O3 (m) pode ser usado para obter o valor de x na fórmula da
composição química da mulita e, conseqüentemente os fatores de ocupação dos respectivos sítios atômicos. A relação entre m e x é dada por [28]:
(
)
(
m 100)
200 m . 6 10 x
+ + −
a a b b c c 7,80 7,70 7,60 2,86 2,88 2,90 2,92 2,94 2,96 2,98 3,00 3,02 7,50 16 50 12 5 0 1175 70 0 80 0 90 0 10 00 11 00 7,40
50 60 70 80 90 100
+ + + + + + + + + + +++ + + + + + + + ++ + +
% molar de Al O
2 3 P ar âm et ro d e r ede a e b ( Â n gs tr o n s) P ar âm et ro d e r ed e c ( Â ng st ro ns )
Figura 3.3- Parâmetros de rede a, b e c de mulitas. A linha reta para o parâmetro a resulta de uma regressão linear, as curvas para b e c foram ajustadas manualmente [27,28].
Johnson et al [15] estudaram as cinéticas, as mudanças estruturais e a estrutura
cristalina desenvolvida na cristalização de um pó de mulita KM 101 (mulita 3:2)
comercialmente obtido pela Kyoritsu Ceramic Materials Co, LTD., Nagoya, Japão, entre as temperaturas de 900 e 1400ºC. O pó foi fundido em um forno e resfriado em água, usando um
laser de CO2para formar pequenas bolas vítreas, como descrito nas referências [29-32]. As
esferas de mulita amorfas foram fragmentadas entre dois pratos de aço inoxidável para formar um pó grosso e posteriormente triturado em gral de ágata. Os fenômenos observados foram
caracterizados usando calorimetria diferencial não-isotérmica (DSC), microscopia eletrônica
de transmissão (TEM), espectroscopia de energia dispersiva (EDS), difração de raios X e
análise de Rietveld.
A Tabela 3.2 mostra a designação das amostras de mulita utilizadas, suas histórias térmicas e a descrição das amostras caracterizadas por várias técnicas.
Tabela 3.2- Identificação, descrição e história térmica das amostras de mulita em forma de pó [15].
Amostras História térmica Análises Detalhes
M 1 40ºC/min até 938ºC, 2,5 h DSC, TEM, XRD Mulita pseudotetragonal
formada em temperatura baixa
M 2 10ºC/min até 900-930ºC,
3 h, várias taxas até 1200ºC.
TEM, XRD, Synchrotron
Mulita pseudotetragonal antes da transição para a fase ortorrômbica
M 3 10ºC/min até 1400ºC TEM, Synchrotron Fase ortorrômbica
A Tabela 3.3 mostra os parâmetros refinados das amostras de mulita M1, M2, M3, M4
[15] e SF [23].
Tabela 3.3- Parâmetros refinados das amostras de mulita [15].
Amostras M1 – LT M2 –LT M3 – HT M4 – HT SF - Mulita 3:2
a (nm) 0,7616 (2) 0,7606 (1) 0,75454 (2) 0,75499 (3) 0,7553 (1) b (nm) 0,7678 (2) 0,7682 (1) 0,76956 (2) 0,76883 (3) 0,7686 (1) c (nm) 0,2889 (4) 0,2871 (4) 0,288398 0,288379(9) 0,28864 (7) V (nm3) 0,16897 0,16870 0,16746 0,16739 0,16756 Densidade (g/cm3) 3,10 3,09 3,15 3,16 3,16
RWP 0,049 0,049 0,051 0,032 -
RBtagg 0,060 0,063 0,049 0,025 0,027
X (Al) 0,0 0,0 0,0 0,0 0,0
Y (Al) 0,0 0,0 0,0 0,0 0,0
Z (Al) 0,0 0,0 0,0 0,0 0,0
B (Al) 0,9 (3) 1,0 (3) 0,5 (1) 0,5 (1) -
Occ. (Al) 1,0 1,0 1,0 1,0 1,0
X (T) 0,148 (2) 0,147 (2) 0,1480 (6) 0,1474 (6) 0,1485 Y (T) 0,339 (2) 0,340 (1) 0,3412 (6) 0,3410 (6) 0,341
Z (T) 0,5 0,5 0,5 0,5 0,5
B (T) 1,7 (4) 0,8 (3) 0,3 (1) 0,3 (1) -
Occ. (T ), Al 0,5 0,5 0,5 0,5 0,5
Occ. (T ), Si 0,25 (2) 0,21 (2) 0,332 (7) 0,334 (7) 0,363 X (T*) 0,275 (2) 0,282 (4) 0,275 (3) 0,268 (3) 0,2621 Y (T*) 0,195 (4) 0,194 (4) 0,209 (2) 0,207 (2) 0,2057
Z (T*) 0,5 0,5 0,5 0,5 0,5
B (T*) 0,1 (4) 3 (1) 1,7 (8) 1,2 (8) - Occ. (T*), Al 0,25 (2) 0,29 (2) 0,168 (7) 0,166 (7) 0,137 X (Oab) 0,354 (2) 0,349 (1) 0,3567(6) 0,3566(6) 0,3579
Y (Oab) 0,423 (2) 0,422 (1) 0,4195 (6) 0,4201 (6) 0,4221
Z (Oab) 0,5 0,5 0,5 0,5 0,5
B (Oab) 0,2 (2) 0,4 (2) 0,8 (1) 0,8 (1) -
Occ. (Oab) 1,0 1,0 1,0 1,0 1,0
X (Od) 0,136 (2) 0,133 (1) 0,1270(9) 0,1263(9) 0,1265
Y (Od) 0,220 (2) 0,222 (1) 0,2219 (8) 0,2216 (8) 0,2201
Z (Od) 0,0 0,0 0,0 0,0 0,0
B (Od) 0,2 (2) 0,4 (2) 0,8 (1) 0,8 (1) -
Occ. (Od) 1,0 1,0 1,0 1,0 1,0
X (Oc) 0,5 0,5 0,5 0,5 0,5
Y (Oc) 0,0 0,0 0,0 0,0 0,0
Z (Oc) 0,5 0,5 0,5 0,5 0,5
B (Oc) 0,2 (2) 0,4 (2) 0,8 (1) 0,8 (1) -
Occ. (Oc) 0,26 (1) 0,58 (3) 0,49 (1) 0,50(1) 0,590
X (Oc*) 0,442 (8) 0,457 (6) 0,453 (5) 0,451 (5) 0,4507
Y (Oc*) 0,039 (9) 0,029 (8) 0,049 (5) 0,048 (5) 0,0518
Z (Oc*) 0,5 0,5 0,5 0,5 0,5
B (Oc*) 0,2 (2) 0,4 (2) 0,8 (1) 0,8 (1) -
Occ. (Oc*) 0,25 (1) 0,29 (2) 0,168 (7) 0,166 (7) 0,137
Mulita x 0,49 (4) 0,58 (3) 0,34 (1) 0,33 (1) 0,274 m (a) - %molar 70,9 69,5 60,7 61,4 61,8 m(mulita x) -
%molar
3.1.4- Massa específica
A massa específica ou densidade teórica de mulitas pode ser calculada mediante a expressão [33]:
(
)
3 -i i i cm g N V M Z unitária célula da Volume unitária célula da Massa d∑
== (3.5)
sendo,
Zi, número de átomos do elemento i por célula unitária;
Mi, massa molecular do elemento i;
V, volume da célula unitária;
N = 6,02 x 1023 (mol)-1, número de átomos por mol (número de Avogadro).
O valor da densidade teórica da mulita 3:2 determinada utilizando os dados das Tabelas 3.1 e 3.3 e a expressão (3.5) é:
Números de átomos por célula unitária:
Al Æ 2a Æ Al Æ 2 x 1 = 2 ; Oab Æ 4h Æ O Æ 4 x 1 = 4 T(Si/Al) Æ 4h Æ Al Æ 4 x 0,5 = 2 ; Od Æ 4g Æ O Æ 4 x 1 = 4
Æ 4h Æ Si Æ 4 x 0,363 = 1,452 ; Oc* Æ 4h Æ O Æ 4 x 0,137 = 0,548
T* (Al*) Æ 4h Æ AlÆ 4 x 0.137 = 0,548 ; Oc Æ 2 Æ O Æ 2 x 0,590 = 1,18
Total de átomos de Al = 4,548 ; Total de átomos de Si = 1,452; Total de átomos de O = 9,728
3 23
22 3,16g/cm
10 02 , 6 x 0 1 x 6756 , 1 99 , 15 728 , 9 08 , 28 x 452 , 1 98 , 26 x 548 , 4 2 : 3 mulita da teórica específica
Massa = + − + =
x
3.1.5- Resistividade elétrica
As cerâmicas são conhecidas como materiais dielétricos por possuírem altos valores de resistividade elétrica associada também as suas versáteis propriedades química e mecânica. [34].
O desenvolvimento tecnológico e cientifico contribuiram para a ampliação do campo de aplicação das cerâmicas, para os quais as propriedades elétricas são importantes. Os materiais cerâmicos com propriedades de isolantes podem ser utilizados para isolação elétrica de baixa e alta voltagem. Como exemplo de materiais, podemos citar: porcelanas, vidros e outros. Por outro lado as cerâmicas com propriedades de semicondutores são usados para muitas aplicações, dentre elas: conversão de energia elétrica em energia térmica (elementos de resistência para aquecimento), controladores de voltagem (resistores fixos) e resistores de temperatura controlada (termistores) ou resistores de voltagem controlada (retificadores e varistores) [35].
Buchnan [36] mediu a resistividade elétrica à temperatura ambiente da mulita 3:2 pura obtida pela sinterização de misturas de SiO2 e Al2O3 e encontrou o valor de aproximadamente
1011Ω.m, que corresponde a resistividade de isolantes [37]. Com o aumento da temperatura a
resistividade da mulita caiu para 104Ω.m a 1000ºC e para 102Ω.m a 1400ºC. O espaçamnto
entre as bandas de energia (Eg) calculada desses dados é de 1,43eV [38].
Chaudhuri et al [39] mediram, em temperaturas elevadas, a resistividade elétrica da mulita3:2 pura, preparada por co-precipitação de solução de reagente analítico Al(NO3)3.9H2O
e Si(OC2H5)4 pelo reagente analítico NH4OH. As densidades das amostras de mulita após
sinterização a 1600°C durante 3h variaram de 50 a 80% da densidade teórica. Os valores das
resistividades elétricas foram de 1,38x106Ω.m a 500°C e 6,46x102Ω.m a 1400°C, e a largura da faixa proibida (Eg) de 1,44eV. As resistividades às altas temperaturas e os valores de Eg
claramente sugerem que a mulita pertence ao grupo dos materiais semicondutores [39]. Saalfield e Guse [40] estudaram a resistividade elétrica de mulita 2:1. Os resultados
mostraram que o valor da banda proibida (Eg) para a mulita 2:1 foi de 7,7eV. A mulita 2:1 é,
portanto, um bom isolante elétrico comparável com a SiO2 e a Al2O3.
Tabela 3.4 – Resistividade elétrica das cerâmicas de alumina, cordierita e porcelana [41-43].
Propriedades Cerâmicas
Porcelana Alumina (42) (44)
(99,9 % Al2O3)
Cordierita (43)
2Al2O3.5SiO2.2MgO
8B 8A
Densidade teórica (g/cm3)
4,00 2,65 --- ---
Densidade (g/cm3) 3,97 1,9 a 2,1 --- ---
Porosidade (%) < 1 20 a 30 --- ---
20ºC > 1012 > 1010 2,75 x 1012 9,77 x 1011
300ºC 1010 1,32 x 106 3,23 x 106 1,09 x 106
Resistividade elétrica
(ohm. m) 1000ºC 105
5,12 x 102 5,37 x 103 1,86 x 103
Eg (eV) --- 1,008 1,27 1,20
3.1.6- Propriedades físicas e mecânicas
Mazdiyasni [44,45] preparou por decomposição hidrolítica de misturas de alcóxidos
metálicos, pó de mulita estequiométrica (3Al2O3.2SiO2) extremamente ativo, com área
superficial de 280m2/g ± 10% e de alta pureza (99,99%).
Amostra do pó de mulita estequiométrica foi observada por difração de raios X, sobre
um substrato de Pt40Rh usando radiação CuKα . De 1200º a 1700ºC todos os picos
correspondem a mulita. Esta fase foi mantida durante resfriamento à temperatura ambiente e a
reciclagem da amostra, indicando completa solução sólida de 3Al2O3.2SiO2, sob as condições
experimentais [44].
Foi realizada análise espectrográfica da mulita 3:2 por emissão das impurezas presentes, conforme resultado apresentado na Tabela 3.5.
Amostras completamente brancas de mulita estequiométrica com densidades de 99 a
99,5% da teórica (3,18 a 3,19g/cm3) foram prensadas a quente no vácuo à pressão de 5kpsi
(34,47MPa) e em temperaturas variando de 1400 a 1600ºC em intervalo de tempo de 15 a 60
minutos. Dados de difração de raios X foram utilizados para computar os parâmetros de rede
e a densidade teórica da mulita, conforme a Tabela 3.6 [44].
Tabela 3.5- Análise espectrográfica por emissão das impurezas da mulita 3:2 (ppm) - [44].
Amostra Cu Pb Fe B Zr Ni Mg Mn V,
Mo
Sn Cr,Ti Cd, Co,Zn
Na
Mulita 3:2 20 < 1 3 1 < 5 < 1 1 < 1 < 3 < 5 < 10 < 30 < 300
Tabela 3.6- Parâmetros de rede da mulita 3:2 prensada a quente [44].
Prensagem a quente a0 (Ǻ) b0 (Ǻ) c0 (Ǻ) V (Ǻ3) Densidade
(g/cm3 )
1400ºC, 34,5 MPa,30min. 7,528 ±0,004 7,685±0,004 2,879±0,001 166,56 3,18
1500ºC, 34,5 MPa,15min 7,525±0,002 7,680±0,002 2,878±0,001 166,32 3,19
1500ºC, 34,5 MPa,30min 7,530 ±0,001 7,681±0,001 2,876±0,001 166,34 3,19
NT. 1psi = 6,8948x103 Pa
Tabela 3.7– Propriedades físicas e mecânicas da mulita 3Al2O3.2SiO2 obtida de derivados
alcóxidos [44].
Ponto de fusão (ºC) Densidade
(g/cm3 )
Módulo de elasticidade (GPa)
Resistência à Flexão (4 pontos a T.A.) (MPa)
1880 ± 5% 3,15–3,16 220 269
Módulo de cisalhamento (GPa)
Módulo de compressibilidade (GPa)
Relação de Poisson Resistência à Compressão
(GPa)
87 157,2 0,266 2,4
Hvizdos [46] estudou o comportamento à tenacidade de mulita sinterizada, utilizando
a fadiga por flexão com indentação (IFF), à temperatura ambiente e a 1300ºC, a partir de pó
de mulita comercial (Bakowski 193 CR, França). O tamanho médio das partículas é de 2,7μm
e a superfície específica de 3,1m2 /g.
A difração de raios X indicou que o pó é predominantemente mulita, com possíveis
traços de cristobalita e coríndon. A relação molar Al2O3/SiO2 determinada por análise química
Tabela 3.8 – Análise química da mulita 1,62:1 comercial - Bakowski 193 CR, França [47].
Mulita Al2O3 SiO2 Fe2O3 CaO MgO NaO K2 O
% em peso 72,6 26,4 0,1 0,09 0,03 0,12 n.d.
n.d. = não detectável
O pó de mulita foi prensado isostaticamente a 200MPa na forma de placas com dimensões de 4x25x45mm e sinterizado a 1750ºC por 5h. Durante o resfriamento da temperatura de sinterização, as amostras foram mantidas por 5h a 1450ºC a fim de reduzir o teor de fase amorfa. A Tabela 3.9 mostra as propriedades físicas e mecânicas da mulita 1,62:1 sinterizada a 1750ºC por 5h [46,47].
A dureza Vickers da mulita foi de 9,0 ± 0,4GPa. O valor da tenacidade à fratura
medida pelo corpo-de-prova SEVNB foi de 2,0 ± 0,2MPam1/2. Este valor está consistente com
o valor de 2,3 ± 0,2MPam1/2 obtido utilizando o corpo-de-prova compacto de tração (CT)
[46]. A Tabela 3.10 mostra as propriedades mecânicas à temperatura ambiente da mulita 1,62:1 sinterizada a 1750ºC por 5h.
Tabela 3.9 – Propriedades físicas e mecânica da mulita 1,62:1 sinterizada a 1750ºC por 5h [46,47].
Amostra Densidade (g/cm3 )
Porosidade
estimada. (% vol.)
Fase vítrea estimada (% vol.)
Resistência à flexão (MPa) Mulita 1,62:1
Bakowski 193 CR
2,95 2,94 2 259
Tabela 3.10 – Propriedades mecânicas à temperatura ambiente da mulita 1,62:1 sinterizada a 1750ºC por 5h [46].
Tenacidade à Fratura – KIc (MPam1/2 )
Dureza Vickers (GPa)
CT † SENVB†† IFF †††
9,0 ± 0,4 2,3 ± 0,2 2,0 ± 0,2 2,1
Penty et al [48] estudaram a variação do Módulo de Young de amostras de duas composições de mulita, dentro da região de estabilidade, contendo 60,1 e 62,8% em mols de Al2O3 de 1 a 10% de porosidade.
O pó de mulita submicrom obtido pela técnica gel, foi submetido a prensagem a quente em vácuo, produzindo corpo-de-prova cilíndricos de 25,4mm de diâmetro.
O módulo de Young foi medido à temperatura ambiente pela técnica do oscilador
compósito (composite oscillator technique), usando amostras usinadas com precisão de
0,00508mm.
A porosidade foi calculada a partir do peso e das dimensões dos corpos de prova e tomando como referência a densidade teórica de 3,16g/cm3 [49].
Os resultados para o módulo de Young são comparados com dados da literatura na Figura 3.4. Os dados foram ajustados pela análise dos mínimos quadrados às equações empíricas propostas por Spriggs [49] e por Hasselman [50], para o efeito da porosidade sobre o módulo de Young de materiais refratários, conforme Tabela 3.11. A equação empírica de Spriggs é dada por [50]:
bp
0e
E
E= − (3.6)
onde E é o módulo de Young, E0e b são constantes e p é a porosidade da amostra.
A equação de Hasselman é dada por [50]:
⎭ ⎬ ⎫ ⎩
⎨ ⎧
⎥ ⎦ ⎤ ⎢
⎣ ⎡
− + − =
p 1) (A 1
p A 1
E
E 0 (3.7)
0 15 20
60,1 (HP)
60,1 (S) 66,7 (S)
60,0 (S) 62,8 (HP) Dados atuais 25 6 30 35 2 4 Porosidade (%) M ódu lo de youn g (1 0 ps i)
6 8 10 12
++ + + + + + + + ++ + + + + + + +
Fenstermacher & Hummel
* * * * * Lang
60,0 (HP)
x
x
x
Al O
2 3(% mol)
Equação de Spriggs (dados combinados)
Figura 3.4- Módulo de Young de mulitas em função da porosidade, determinado com a equação de Spriggs; HP = prensado a quente e S = prensado a frio e sinterizado [48].
Tabela 3.11- Efeito da porosidade sobre o módulo de Young de mulita, obtido pela curva de ajuste dos dados para as equações de Spriggs e Hasselmam [48].
Equação de Spriggs E = E0 e− bP
Equação de Hasselman E = E0 {1 − [ (AP) / ( 1 + (A − 1) P ]}
Composição (% em mols de Al2O3)
Faixa de porosidade (%)
Nº de dados
Eo (106 psi) b Eo (106 psi) A
60,1 2,63 – 7,49 8 32,8 ( ± 1,2)* 3,45 ( ± 0,65) 33,0 ( ± 1,3) 3,74 ( ± 0,92) 62,8 0,81 – 9,48 17 32,5 ( ± 0,9) 2,99 ( ± 0,42) 32,5 ( ± 0,9) 3,14 ( ± 0,48) Dados
combinados
0,81 – 9,48 25 32,4 ( ± 0,8) 3,03 ( ± 0,35) 32,5 ( ± 0,8) 3,18 ( ± 0,40)
NT.: 1psi = 6,8948x103Pa
A respeito das propriedades mecânicas, a disponibilidade de pós de mulita pura, fina e novas rotas de processamento, tem tornado possível a obtenção de mulita policristalina, densa
Tabela 3.12- Propriedades de cerâmicas de mulita e de alumina [34,52,53].
PROPRIEDADES MULITA ALUMINA
Temperatura de fusão - Tf (ºC) 1828 ± 10 2054 ± 10
Estabilidade química e térmica Ótima Ótima
Tenacidade à fratura - KIC (MPa.m1/2) ~ 2 3,5 – 4,0
Resistência à flexão - σf (MPa ) 185 275 – 550
Constante dielétrica (a 25ºC e 1MHz) 6,6 8,6 – 10,6
Resistência à fluência Alta Boa
Resistência ao choque térmico Ótima Boa
Condutividade térmica (W.m-1.K-1) 6,1 35 – 39
Coeficiente de expansão térmica (x10-6C-1) 4,5 a 5,6 7,2 – 8,8
Densidade (g/cm3) 3,15 a 3,22 3,98
Estrutura cristalina Ortorrômbica Hexagonal compacta
Índice de refração 1,64 1,76 (safira)
Vickers (GPa) 15 19 – 26
Durezas
Mohs 6 - 7 9
Módulo de elasticidade (GPa) 145 393
Resistividade elétrica (Ω.m) > 1012 > 1013
3.1.7- Espectroscopia de ressonância magnética nuclear com rotação no ângulo mágico de 29
Si e 27Al (27Al e 29Si MAS NMR) de mulitas.
Experimentos realizados com as técnicas de RMN evidenciam as propriedades
magnéticas dos núcleos, que por apresentarem cargas, geram um dipolo magnético ao girarem em torno do eixo nuclear. A magnitude deste dipolo expressa-se como momento magnético
nuclear (μ). O momento angular da carga em movimento é descrito como número de spin (I)
que pode assumir valores 0, 1/2, 3/2, 5/2, etc e pode ser determinado a partir da massa
atômica e número atômico. Núcleos que possuem I=1/2, como o 29Si; mesmo com baixa
abundância natural, têm distribuição de carga esférica e uniforme, já os que apresentam I≥1,
como 27Al (I=5/2) têm distribuição de carga não esférica. Esta assimetria é descrita por um
Sob condições apropriadas, em um campo magnético, uma substância pode absorver radiação eletromagnética na região de radiofreqüência (rf), e ser submetida a transições entre níveis de energia, representado por [54]:
π
2
γ
h B
ΔE= 0 (3.8)
ondeΒ0é a intensidade do campo magnético estacionário, h é a constante de Plank, γ é a
razão giromagnética do núcleo.
A radiofreqüência aplicada em MHz (ν1) é dada por [54]:
π
2
γ
B
υ 0
1= (3.9)
Substituindo o valor de B0 da expressão (3.9) em (3.8) obtém-se ΔE em função da
radiofreqüência [54]:
ΔE = h ν1 (3.10)
A Ressonância Magnética Nuclear de sólidos ou de espécies fortemente adsorvidas, restringidos de movimentos randômicos e rápidos comuns em líquidos, apresentam os efeitos das interações magnéticas nucleares que causa grande alargamento das linhas dos espectros. Estas interações em sólidos são anisotrópicas, dependentes da orientação dos eixos cristalográficos em relação ao campo externo. Além da largura de linhas do espectro, estas interações determinam a posição dos sítios de específicos núcleos, que contêm valiosas informações sobre a geometria, estrutura e movimentos no sólido [54].
A partir dos anos 70, introduziu-se a técnica experimental de RMN, com rotação no
ângulo mágico (em inglês, MAS) que permite reduzir as interações dipolares entre os núcleos.
A amostra é girada a elevadas velocidades (2 a 20kHz), a um ângulo de 54º47’ em relação ao
eixo Z. A rotação da amostra no ângulo mágico reduz ou elimina a anisotropia do
deslocamento químico, produzindo espectros bem resolvidos [54].
A espectroscopia de ressonância magnética nuclear com rotação no ângulo mágico de
29
![Figura 3.1 - Diagrama de equilíbrio de fases do sistema Al 2 O 3 -SiO 2 [10].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15927300.676409/26.892.198.691.671.1108/figura-diagrama-de-equilíbrio-fases-sistema-al-sio.webp)
![Tabela 3.1- Posições Wickoff, coordenadas e nomes dos sítios da estrutura “média” da mulita, grupo espacial Pbam (Nº 55) [15]](https://thumb-eu.123doks.com/thumbv2/123dok_br/15927300.676409/28.892.117.783.901.1041/tabela-posições-wickoff-coordenadas-sítios-estrutura-média-espacial.webp)
![Tabela 3.7– Propriedades físicas e mecânicas da mulita 3Al 2 O 3 .2SiO 2 obtida de derivados alcóxidos [44]](https://thumb-eu.123doks.com/thumbv2/123dok_br/15927300.676409/35.892.103.793.638.816/tabela-propriedades-físicas-mecânicas-mulita-obtida-derivados-alcóxidos.webp)
![Tabela 3.13 – Valores do coeficiente de expansão térmica linear para a mulita 3;2 monocristalina e policristalina [1,33,67]](https://thumb-eu.123doks.com/thumbv2/123dok_br/15927300.676409/46.892.104.808.406.629/tabela-valores-coeficiente-expansão-térmica-linear-monocristalina-policristalina.webp)

![Figura 3.14 - Volume de água absorvido em função da consistência do molde [89].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15927300.676409/64.892.255.630.477.819/figura-volume-de-água-absorvido-função-consistência-molde.webp)
![Figura 3.15- Resistência do molde e da barbotina em função da consistência [89].](https://thumb-eu.123doks.com/thumbv2/123dok_br/15927300.676409/65.892.275.613.197.477/figura-resistência-do-molde-da-barbotina-função-consistência.webp)