5 – Schéma d'une liaison hydrogène : interaction de type électrostatique via l'atome H. 8 – Effet de l'interaction d'un groupe O–H avec l'environnement : ´ échelle qualitative des déplacements de sa fréquence d'extension.

Principe
Après la collision, les molécules sont « froides », ce qui signifie que leur énergie interne ne dépasse pas quelques Kelvins : seuls le niveau vibrationnel le plus bas (v”=0) et quelques niveaux rotationnels sont peuplés. Premièrement, elle permet de s’affranchir des effets environnementaux, donnant ainsi accès aux caractéristiques intrinsèques des molécules ou des complexes.
Mise en œuvre
Plus on s'éloigne d'une distance z de l'orifice, plus la densité diminue (qui varie en 1/z2 pour un jet percé) jusqu'à former le disque de Mach où la pression du jet est égale à la pression résiduelle du carter. L’analyse des spectres est également plus simple, car seul le plan v”=0 et quelques niveaux rotationnels de l’état fondamental sont peuplés : les spectres sont plus simples et donc plus faciles à exploiter qu’en phase condensée ou en cellule à des températures où la les niveaux de rotation et de vibration de l'état fondamental sont remplis conformément à la loi de distribution de Maxwell-Boltzmann.
Spectroscopie ´ electronique
- La fluorescence induite par laser
- Source lumineuse : le laser ` a colorant
- La d´ etection
Pour les spectres d’excitation de fluorescence et de fluorescence diffusée, nous utilisons un laser à colorant commercial (Sirah) pompé par un laser Nd3+:YAG pulsé. Ainsi, les axes du laser, du faisceau et de la détection sont perpendiculaires deux à deux (Figure 1.4).

Spectroscopie vibrationnelle
- Spectroscopie de double r´ esonance IR–UV
- Source lumineuse : les oscillateurs param´ etriques optiques
- La d´ etection
Un tiers de la puissance du laser Nd3+:YAG (0,5 W) est réfléchi à travers une plaque séparatrice vers la cavité de l'OPO infrarouge. Observer le dépeuplement de l’état fondamental est possible car il persiste suffisamment longtemps pour être sondé par le faisceau UV.

Calculs semi-empiriques
Calculs de la fonctionnelle de la densit´ e
- Fr´ equences harmoniques
- Calcul de l’´ energie de liaison
- Energie de d´ eformation
- Convention
La figure 3.23 (a) montre les spectres d'excitation de fluorescence de mélanges de (S)-NapOH/(R)-1-amino-2-propanol, (R)-NapOH/(R)-1-amino-2-propanol et ( R/S )- NapOH/(R)-1-amino-2-propanol permet ainsi de distinguer les bandes dues aux complexes hétérochiraux (SR) de celles dues aux complexes homochiraux (RR). 4.13 – Spectre d'excitation de fluorescence du mélange (S)-NapOH/(S)-méthyl lactate dans le jet supersonique dans la région 000 de la transition NapOH (31738 cm−1), qui est prise comme source d'énergie (a) à concentration élevée et (b) à faibles concentrations de (S)-méthyl lactate.

Spectroscopie de double r´ esonance IR–UV
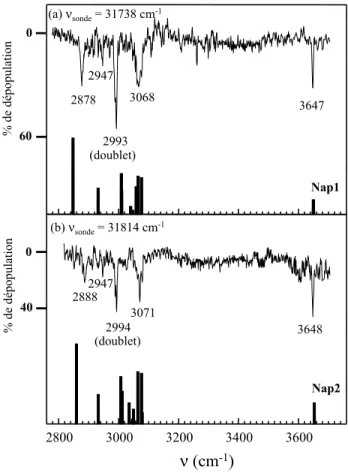
Les spectres de dépeuplement IR-UV (Figure 1.3) ont été enregistrés dans la gamme des fréquences de vibration O-H et CH lorsque la sonde est fixée sur les transitions. Dans la région vibrationnelle C-H, le spectre présente un multiplet non résolu et centré.
Etude th´ eorique
- Spectroscopie ´ electronique
- Spectroscopie de double r´ esonance IR–UV
- Etude th´ eorique
Le passage vers les hautes ou basses énergies de la transition électronique S0 → S1 dépend de l'équilibre entre forces électrostatiques et forces de dispersion à l'état fondamental et à l'état excité au sein du complexe. Dans les complexes où les interactions OH · · ·π sont en jeu, on observe souvent un déplacement de la transition S0 → S1 vers haut. Nous suggérons que, comme pour les complexes 1:1, nous nous basions sur le décalage de la transition électronique 000 du complexe par rapport à celle du chromophore.
L’affaiblissement de la vibration OH est également dû à un effet coopératif qui renforce la force donneuse du groupe OH du méthanol.

Complexe (R/S)-2-naphtyl-1-´ ethanol/(H 2 O) 2
- Spectroscopie ´ electronique
- Spectroscopie de double r´ esonance IR–UV
- Etude th´ eorique
Les vibrations O – H (· · · O) sont couplées et provoquent des modes délocalisés sur les groupes OH de NapOH et la partie WD du dimère d'eau. La fréquence la plus élevée est comparée à l'étirement O – H associé au dimère d'eau isolé et la fréquence la plus basse au chromophore isolé. Les fréquences calculées des modes d'étirement situés sur la partie WA du dimère d'eau sont réduites respectivement de 38 et 30 cm−1 par rapport au dimère ` isolé en raison des interactions de type OH···π.
Expérimentalement, la fréquence du mode antisymétrique ν3(as) du dimère d'eau est décalée de 37 cm−1 via l'interaction OH · · ·π.

Discussion
- Effets de la complexation
- Effets de la taille du cycle et de la chaˆıne lat´ erale du NapOH . 82
Nous avons regroupé dans le tableau 2.5 les fréquences d'étirement O–H observées dans NapOH/(H2O)2 et les avons comparées à celles observées dans PetOH/(H2O)2. La tendance générale observée est un changement moins significatif des fréquences d'étirement OH dans le complexe avec NapOH par rapport aux complexes avec PetOH (Δ (Δν) > 0). On observe que le décalage de la fréquence d'étirement O–H(· · · π) est moins significatif (Δν= -58 cm−1) dans le cas du NapOH que dans le cas de l'anthracite (Δν=-68 cm− 1). e qui possède cependant un anneau plus aromatique.
Dans le complexe NaOH/(CH3OH)2, les fréquences de vibration OH dans l’état S1 sont légèrement inférieures à celles dans S0.

Conclusion
Dans le complexe NapOH/(H2O)2, seuls les modes d´elocalis´es sur le chromophore et l'eau ont pu ˆetre observ´es `a l'´etat S1; par rapport `a l'´etat fondamental, les fr´equences sont diminu´ees de 11 cm−1 et 10 cm−1. 4] "Formation of hydrogen-bonded structures in jet-cooled complexes of a chiral chromophore as studied by IR/UV double resonance spectroscopy: Diastereoisomeric complexes of (±)2-naphthyl-1-ethanol with (±)2-amino-1-propanol" K. 6 ] "Structures of Hydrogen Bonded Clusters of Benzyl Alcohol with Water Studied by Infrared-Ultraviolet Double Resonance Spectroscopy in Supersonic Jet" N.
14] "Density Functional Theory Calculations of the Structures, Binding Energies and Infrared Spectra of Methanol Clusters" F.
G´ en´ eralit´ es sur les α -amino-alcools
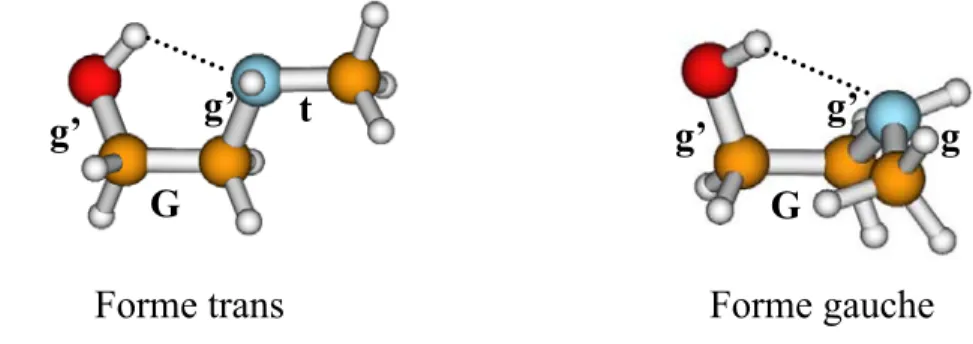
Les alcools aminés sont des molécules flexibles qui peuvent exister sous diverses formes isomères et diffèrent par leur rotation autour des axes C-N, C-C et C-. L'équipe de Simons a également étudié les conformations de la noradrénaline ou de molécules similaires en interaction avec des molécules d'eau ou du 2-amino-1 par spectroscopie IR-UV. L'éthanol en interaction avec des molécules aromatiques telles que le phénol [12]. Dans notre approche, les aminoalcools sont utilisés comme solvant pour observer le rôle de leur conformation dans la complexation avec le chromophore.
De plus, nous souhaitons étudier les interactions entre les molécules chirales utilisant le (R/S)-2-naphtyl-1-éthanol et les α-aminoalcools chiraux comme chromophore chiral.

Syst` eme mod` ele non chiral : le 2-amino-1-´ ethanol
- Structure
- Complexes (R/S)-2-naphtyl-1-´ ethanol/2-amino-1-´ ethanol
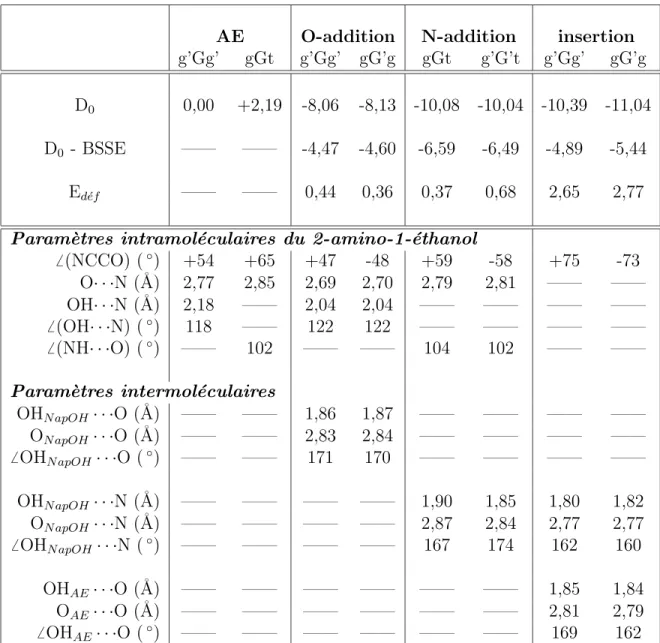
La liaison intramoléculaire OH · · ·N du 2-amino-1-éthanol est préservée et même renforcée. Les paramètres structurels des deux formes de 2-amino-1-éthanol et des complexes avec (S)-Nap1 sont donnés en degrés (◦) pour les angles et en ˚A pour les distances. Les structures d'insertion et d'addition de N diffèrent considérablement dans la fréquence d'étirement O – H du 2-amino-1-éthanol.
Une autre structure observée est une structure de type O-addition (bande C) où le 2-amino-1-éthanol est sous sa forme A1 « fermée ».

Complexes avec des amino-alcools non chiraux substitu´ es sur l’azote . 109
- Spectroscopie de double r´ esonance IR–UV
- Discussion
Ce tronçon a une fréquence inférieure de 60 cm−1 à celle du complexe NapOH/AE. Dans le complexe NapOH/MAE, la bande la plus intense à -99 cm−1 a été attribuée à un complexe de type N sur la base du spectre infrarouge et par analogie avec la position de la bande A du complexe NapOH/AE située à -97 cm−1 1. Tout d’abord, on voit que les fréquences sont légèrement plus faibles en énergie dans le complexe NapOH/DMAE que dans le complexe NapOH/AE.
La fréquence vibrationnelle ν(OH)N apOH est plus décalée dans le complexe NapOH/DMAE que dans NapOH/AE.
Complexes avec des amino-alcools chiraux
- Complexes (R/S)-2-naphtyl-1-´ ethanol/(R)-1-amino-2-propanol 118
- Absence de complexe d’insertion
- Complexes N-addition
- Complexes O-addition : comparaison des paires homo et h´ et´ e-
- Transitions vibrationnelles ` a l’´ etat excit´ e
Les géométries des complexes avec (S)-Nap1 sont ensuite optimisées grâce à la méthode DFT (B3LYP/6-31G**). Les structures des complexes hétérochiraux et homochiraux sont illustrées à la figure 3.26. Les fréquences des modes d'extension O – H calculées dans le complexe de type N-addition SR (3415 cm−1 et 3753 cm−1) excluent également l'attribution des deux complexes hétérochiraux présents dans le jet et possédant ce type de structure.
Une structure de type addition N peut être observée dans le complexe avec le 2-amino-1-éthanol.

Conclusion
- Mol´ ecules chirales
- Mol´ ecules non chirales
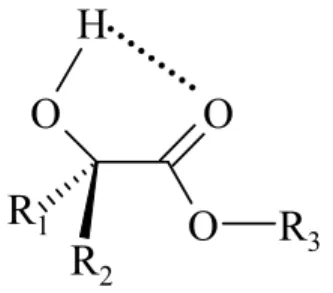
Par exemple, le (R/S)-méthyl lactate est produit en quantités industrielles car il entre dans la composition de nombreux cosmétiques. Comme les alcools α-amino, les esters α-hydroxy sont des composés bifonctionnels qui peuvent fournir une liaison intramoléculaire en raison de la position du groupe –OH en α de la fonction ester. Nous nous sommes également intéressés aux analogues non chiraux des lactates tels que le glycolate de méthyle et l'α-hydroxyisobutyrate de méthyle dont les agrégats ont
L'α-hydroxy-isobutyrate de méthyle (MeHib) possède deux groupes méthyle portés par le carbone α de l'ester.
Complexes (R/S)-2-naphtyl-1-´ ethanol/(S)-lactate de m´ ethyle
- Complexes h´ et´ erochiraux
- Complexes homochiraux
Nous verrons qu'une étude de pression de la bande la plus intense à -58 cm−1 indique qu'il s'agit d'un complexe 1:1. La bande située à -107 cm−1 de la transition 000 NapOH n'appartient pas à cette progression vibrationnelle. Il n'apparaît pas dans le spectre enregistré à faible concentration de solvant (spectre (b) sur la figure 4.9).
Les calculs ont été effectués pour des structures 1:1 en utilisant la géométrie 1a.

Complexes (R/S)-2-naphtyl-1-´ ethanol/(S)-lactate d’´ ethyle
- Complexes h´ et´ erochiraux
- Complexes homochiraux
Enfin, on note la présence d'une bande à -40 cm−1, probablement due à un complexe 1:2 selon le spectre infrarouge et appelée RSS. Le complexe sondé est donc un complexe 1:1, qui diffère du complexe RS1, nous l'appelons donc RS2. Nous avons enregistré le spectre de double résonance IR-UV pour la sonde fixée à -40 cm−1.
Nous montrerons plus tard, grâce au spectre de double résonance IR-UV, que le complexe associé à la bande à -25 cm−1 est un complexe 1:2, c'est pourquoi nous l'appelons SSS.

Complexes avec des α -hydroxy-esters non chiraux
- Spectroscopie ´ electronique
- Spectroscopie de double r´ esonance IR–UV
La similitude avec les spectres des mélanges hétérochiraux NapOH/MeLac et NapOH/EtLac est frappante. Deux bandes apparaissent également à une énergie plus élevée que la transition NapOH originale à +9 et +24 cm−1 et sont notées IB. 4.22 – Spectre d'excitation de la fluorescence du mélange (R)-NapOH/MeHib dans un faisceau supersonique au voisinage de la transition 000 de NapOH (31738 cm−1) qui est prise comme origine des énergies.
Il montre deux transitions vibrationnelles à 3501 cm−1 et 3524 cm−1 qui se situent dans la même région de fréquences vibrationnelles observées pour les complexes hétérochiraux de lactate de méthyle et de lactate d'éthyle.

Discussion
- Complexes 1:1
- Enantios´ electivit´ e
- Complexes 1:2
La taille des complexes des lactates avec le chromophore NapOH montre une préférence énantiomérique marquée : des complexes 1:1 ne sont observés que dans le cas d'associations hétérochirales. Sur la base de la différence observée dans les complexes avec le méthylglycolate et le méthyl-α-hydroxyisobutyrate, des complexes 1:2 ont été observés dans les complexes homo- et hétérochiraux, par opposition aux complexes 1:1.
On peut imaginer que dans le cas des systèmes homochiraux, les complexes 1:2 ne se forment pas à partir de complexes 1:1 ce qui n'a pas été démontré expérimentalement.

Conclusion
Nous avons appliqué cette technique à la détermination de la structure des paires de contacts impliquées dans la reconnaissance chirale. En augmentant le nombre de liaisons hydrogène intermoléculaires, nous espérons augmenter la rigidité des systèmes et améliorer l’efficacité de la reconnaissance chirale. Le rôle joué par les molécules prébiotiques dans l’émergence de la vie reposerait, entre autres, sur la formation de structures moléculaires homochirales.
Le spectre infrarouge obtenu pour observer les vibrations de l'état excité S1 montre une forte diminution de la fréquence du mode d'étirement ν (OH) (au) compd.