Hellyda Katharine Tomaz de Andrade Silva
Estudo da influência do biodiesel de mamona como aditivo antioxidante
para o biodiesel de girassol e soja
________________________________________________________
Dissertação de Mestrado
Natal/RN, março de 2011
INSTITUTO DE QUÍMICA
Hellyda Katharine Tomaz de Andrade Silva
ESTUDO DA INFLUÊNCIA DO BIODIESEL DE MAMONA
COMO ADITIVO ANTIOXIDANTE PARA O BIODIESEL DE
GIRASSOL E SOJA
Dissertação apresentada ao Programa de
Pós-Graduação em Química da Universidade Federal do
Rio Grande do Norte, como parte dos requisitos para
a obtenção do título de Mestre em Química.
Orientador: Prof. Dr. Valter José Fernandes Júnior
UFRN / Biblioteca Central Zila Mamede. Catalogação da Publicação na Fonte
Silva, Hellyda Katharine Tomaz de Andrade.
Estudo da influência do biodiesel de mamona como aditivo antioxidante para o biodiesel de girassol e soja. – Natal, RN, 2014. 180f. : il.
Orientador: Prof. Dr. Valter José Fernandes Júnior.
Dissertação (Mestrado) – Universidade Federal do Rio Grande do Norte. Centro de Ciências Exatas e da Terra. Programa de Pós-Graduação em Química.
1. Biodiesel – Dissertação. 2. Transesterificação – Dissertação. 3. Estabilidade oxidativa – Dissertação. 4. P-DSC – Dissertação. 5. Rancimat – Dissertação. I. Fernandes Júnior, Valter José. II. Universidade Federal do Rio Grande do Norte. III. Título
DEDICATÓRIA
A meu querido e bondoso Deus
AGRADECIMENTOS
“A gratidão é um dos sentimentos, a qual denota a essência do homem. É por intermédio deste, que o aprendizado da nossa não auto-suficiência aflora e a aceitação
de que sempre necessitaremos do próximo, se dá humildemente...” Munida por este
sentimento e de forma singela, almejo externar minha mais terna e sincera gratidão a
todos que contribuíram para a concretização deste trabalho.
A Deus, responsável por esta “fotólise”. A Ti Senhor, pela orientação oriunda da
Tua luz. Bondade, misericórdia, amor e conforto, estiveram presentes como acalanto
nas dificuldades e fustigações da árdua batalha, encorajando-me até o fim.
A toda minha família, em especial a minha mãe, Maria Cleilda, que é e sempre
será exemplo e por ter me conduzido à maior de todas as lições que é dispor de caráter,
dignidade e respeito ao próximo, elementos que são fontes de inspiração e
aprendizagem na minha formação.
Ao professor Dr. Valter José Fernandes Júnior, pela orientação, oportunidade,
compreensão, paciência e valioso aprendizado.
Ao Prof. Dr. Antonio Souza de Araújo pelas contribuições e pelo apoio.
Ao Coordenador do PRH-22, Senhor Prof. Cordeiro que juntamente com os
Senhores Carlos Alberto Poletto e José Marcos Leite Pacheco (PETROBRAS),
gentilmente me ajudaram em algumas indagações para enriquecimento deste trabalho.
Aos queridos colegas da ICR3 Científica, Jeferson Benvindo e Sander Lima
pelas dúvidas elucidadas quanto à metodologia dos equipamentos.
A Fátima Dutra e a todos do Laboratório de Cromatografia (CENPES –
PETROBRAS), pela amizade e pelos riquíssimos ensinamentos nas análises de
biodiesel por cromatografia a gás, bem como pela oportunidade.
As queridas amigas Dra. Amanda Gondim, pela relevante e incomensurável
contribuição, amizade e apoio, MSc. Edjane Buriti pela colaboração na realização das
análises termogravimétricas, Fabíola Correia por todo apoio desde o início e por ter sido
meu braço direito na execução dos experimentos e ao amigo Tarcísio Amaro pelo
auxílio no processo de purificação do biodiesel.
Aos colegas do Laboratório de Combustíveis e Lubrificantes pela amizade e
auxílio: André, Camila, Cedrick, Giovanna, Lívia, Luan, Mariana, Nadjane, Rafaela,
Aos meus queridos amigos, Ana Cláudia, Emerson Faião, José Antônio, Filipe
Alves e Stevie Hallen pelo companheirismo, amizade e auxílio na realização deste
trabalho.
Aos colegas do Laboratório de Catálise e Petroquímica: Aline Araújo, Ana
Adalgisa, Anne Gabriela, Geraldo Eduardo, João Paulo, Késia Kelly, Luzia Patrícia,
Larissa Luz, Maria Costa (Dedéia), Marcela Barbosa, Marcílio Pelicano, Regineide
Lima, Ricardo Miguel, Thiago Chellappa e Vinícius Caldeira.
A todas as minhas amadas irmãs da Residência Universitária Praça Cívica, que
na ausência do meu lar, foram a minha família.
Aos meus queridos “pais adotados” Dr. Ricardo Craciun e MSc. Marciano
Furukava pelas palavras de incentivo e carinho.
A todos os professores da graduação pela valiosa contribuição não apenas na
minha formação acadêmica, mas também pela agregação de valores, em especial ao Dr.
Filipe Martel, Dr. Franklin Nelson da Cruz, MSc. Luiz Seixas das Neves, Dr. Marconi
Floripe Ginani e Dr. Ótom Anselmo.
A minha querida “mammy” Dona Irany, por todo o amor e cuidado desde a
minha iniciação científica e ao Seu Antônio Murilo (secretário do PRH – 30) pelo
incansável esforço quanto às tentativas de fomentar a divulgação deste trabalho.
Ao Programa de Pós-Graduação em Química pela oportunidade, em especial aos
funcionários Ana Alice e Severino Higino.
As bancas examinadoras pela relevante contribuição na revisão e, por
conseguinte aperfeiçoamento deste trabalho.
A Agência Nacional do Petróleo, Gás Natural e Biocombustíveis por fomentar
este estudo.
Não poderia, EM HIPÓTESE ALGUMA, finalizar essa nota de agradecimento
sem mencionar duas pessoas indescritíveis, que se não fosse o incomensurável apoio,
contribuição e amizade que a mim foi dedicado, vencer a “energia de ativação” para
este processo, teria sido muito mais difícil. É muito bom saber que temos seres humanos
tão especiais, que nos estendem a mão quando mais necessitamos. A vocês Profa. Dra.
Tatiana de Campos Bicudo e MSc. Mariana Santana a minha mais terna gratidão e
Alegrei-me sobremaneira no Senhor porque, agora, uma vez mais,
renovastes a meu favor o vosso cuidado; o qual também já tínheis
antes, mas vos faltava oportunidade.
Digo isto, não por causa da pobreza, porque aprendi a viver
contente em toda e qualquer situação.
Tanto sei estar humilhado como também ser honrado; de tudo e
em todas as circunstâncias, já tenho experiência, tanto de fartura como
de fome; assim de abundância como de escassez;
“Tudo posso Naquele
que me fortalece”.
RESUMO
Biodiesel é um combustível constituído por mono-alquil-ésteres de ácidos graxos de
cadeias longas, derivado de óleos vegetais ou gordura animal. Este combustível pode
ser utilizado em motores de ignição por compressão para a propulsão de veículos
automóveis ou geração de energia, como um substituto parcial ou total de diesel fóssil
combustível. O biodiesel pode ser processado a partir de diferentes mecanismos. A
transesterificação é o processo mais comum para obtenção do biodiesel, em que um
éster reage com um álcool para formar outro éster e um novo álcool. Essas reações são
normalmente catalisadas pela adição de um ácido ou uma base. Inicialmente, foram
determinadas as propriedades físico-químicas dos óleos de girassol, mamona e soja de
acordo com as especificações de metodologias de teste padronizadas, com o intuito de
avaliar se os mesmos possuíam condições favoráveis para serem utilizados como
matéria-prima na reação de transesterificação. O biodiesel desses óleos foi obtido
através da reação de transesterificação pela rota metílica, fazendo uso de KOH no
preparo do catalisador (metóxido de potássio). O rendimento das reações de
transesterificação foi acima de 93% m/m. Os biocombustíveis e as blends foram
caracterizados pelos índices de acidez e iodo, ponto de fulgor, pela massa específica,
pelos teores de enxofre, metanol e ésteres. As estabilidades térmica e oxidativa foram
avaliadas através da Termogravimetria (TG), da Calorimetria Exploratória Diferencial
sob Pressão (P-DSC) pelos métodos dinâmico e isotérmico, e do Rancimat. As amostras
de biodiesel de girassol e soja apresentaram conformidade com as especificações
estabelecidas pela Resolução ANP no 7/2008. O biodiesel de mamona, como esperado,
apresentou elevadas massa específica e viscosidade cinemática. A adição do biodiesel
de mamona como antioxidante ao biodiesel de girassol e de soja é promissora, pois
promoveu uma melhora significativa na resistência à auto-oxidação e, por conseguinte,
na estabilidade oxidativa de ambos. Para as blends estudadas, o aumento da
concentração de biodiesel de mamona contribuiu para um aumento da massa específica,
viscosidade cinemática e ponto de fulgor. As blends que apresentaram conformidade às
exigências da ANP foram àquelas compreendidas na faixa de 20-40% de biodiesel de
mamona adicionado, o que as tornam candidatas à substituta do diesel fóssil.
Palavras-Chaves: Biodiesel. Transesterificação. Estabilidade Oxidativa. P-DSC.
ABSTRACT
Biodiesel is a fuel made up by mono-alkyl-esters of long chain fatty acids, derived from
vegetable oils or animal fat. This fuel can be used in compression ignition engines for
automotive propulsion or energy generation, as a partial or total substitute of fossil
diesel fuel. Biodiesel can be processed from different mechanisms. Transesterification is
the most common process for obtaining biodiesel, in which an ester compound reacts
with an alcohol to form a new ester and a new alcohol. These reactions are normally
catalyzed by the addition of an acid or a base. Initially sunflower, castor and soybean oil
physicochemical properties are determined according to standard test methods, to
evaluate if they had favorable conditions for use as raw material in the
transesterification reaction. Sunflower, castor and soybean biodiesel were obtained by
the methylic transesterification route in the presence of KOH and presented a yield
above 93% m/m. The sunflower/castor and soybean/castor blends were studied with the
aim of evaluating the thermal and oxidative stability of the biofuels. The biodiesel and
blends were characterized by acid value, iodine value, density, flash point, sulfur
content, and content of methanol and esters by gas chromatography (GC). Also studies
of thermal and oxidative stability by Thermogravimetry (TG), Differential Scanning
Calorimetry High Pressure (P-DSC) and dynamic method exothermic and Rancimat
were carried out. Biodiesel sunflower and soybean are presented according to the
specifications established by the Resolution ANP no 7/2008. Biodiesel from castor oil,
as expected, showed a high density and kinematic viscosity. For the blends studied, the
concentration of castor biodiesel to increased the density, kinematic viscosity and flash
point. The addition of castor biodiesel as antioxidant in sunflower and soybean
biodiesels is promising, for a significant improvement in resistance to autoxidation and
therefore on its oxidative stability. The blends showed that compliance with the
requirements of the ANP have been included in the range of 20-40%. This form may be
used as a partial substitute of fossil diesel.
LISTA DE FIGURAS
Figura 1 - Evolução dos biocombustíveis no Brasil... 25
Figura 2 - Potencialidade brasileira para produção de oleaginosas... 28
Figura 3 - Representação do arranjo molecular dos triglicerídeos em moléculas de gordura e óleo... 32
Figura 4 - Plantação de girassóis em Fargo, Dakota do Norte nos Estados Unidos e sementes de girassol... 33
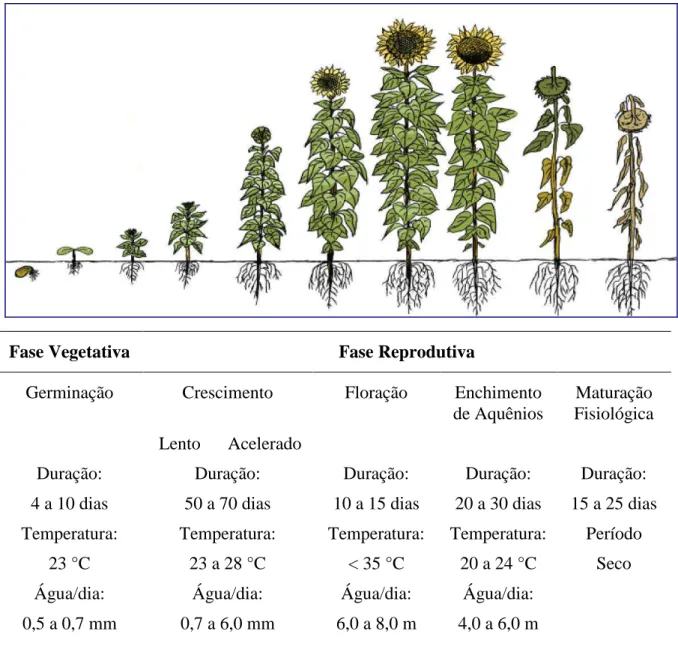
Figura 5 - Fases de desenvolvimento do girassol, com as respectivas exigências
térmicas e hídricas... 35
Figura 6 - Cacho de mamona e endosperma da semente da mamoneira... 38
Figura 7 - Esquema ilustrativo da organografia da mamoneira... 39
Figura 8 - Estrutura molecular do ácido ricinoléico de estrutura linear e com a
formação das pontes de hidrogênio intramoleculares... 41
Figura 9 - Plantação de soja transgênica na cidade de Ronda Alta, Rio Grande do Sul e grãos de soja... 43
Figura 10 - Mecanismo da transesterificação de óleos vegetais catalisada por base. 51
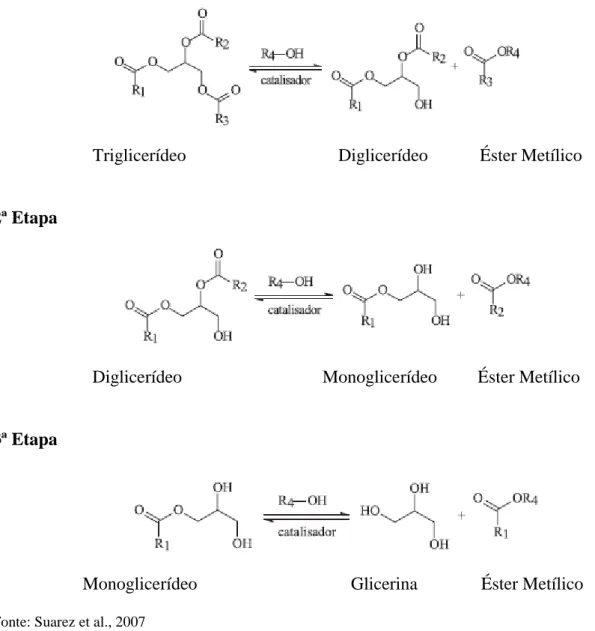
Figura 11 - Reações envolvidas na transesterificação de triglicerídeos... 52
Figura 12 - Perfil cinético da reação de transesterificação... 53
Figura 13 - Esquema da reação iodométrica do ácido oléico, mostrando a
clivagem da ligação e a titulação do iodo em excesso... 60 Figura 14 - Reações químicas representativas para a adição dos reagentes de Wijs (ICl) e de Hanus (IBr) para formação de I2... 60
Figura 15 - Viscosímetro de Ostwald... 64
Figura 16 - Mecanismo simplificado da autoxidação inicial de um lipídeo... 67
Figura 17 - Esquema geral de mecanismo de oxidação lipídica. RH – ácidos
graxos insaturados; R• - radical livre; ROO• - radical peróxido, e ROOH –
hidroperóxido... 69
Figura 18 - Estrutura para o ácido linolênico (C18:3) e seu isômero com arranjo
de insaturações conjugadas... 71
Figura 19 - Esquema representativo da suscetibilidade dos hidrogênios para uma porção do ácido linolênico (C18:3) como substrato e sua probabilidade de
ocorrência... 72
Figura 20 - Mecanismo de atuação dos antioxidantes primários, onde ROO• e R• - radicais livres, AH –antioxidante com um hidrogênio ativo e A• - radical inerte... 73
Figura 21 - Esquema representativo para determinação do período de indução... 77
Figura 22 - Modo de funcionamento do backflush (válvula de fluxo reverso) e do injetor split/splitless... 80
Figura 24 - Ensaio de estabilidade à oxidação ilustrando a determinação do
período de indução... 86
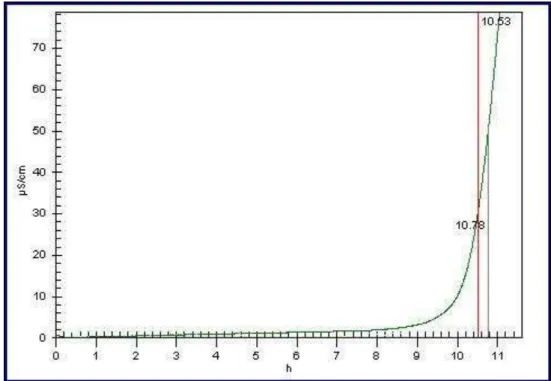
Figura 25 - Curva típica do ensaio de estabilidade oxidativa proposto pela norma EN14112... 87
Figura 26 - Reação de transesterificação do óleo de girassol e reação do metóxido de potássio com o óleo de girassol no reator EUROSTAR... 89
Figura 27 - Processo de separação do biodiesel de girassol no reator e por gravimetria... 90
Figura 28 - Processo de lavagem do biodiesel metílico e biodiesel após o processo de purificação... 91
Figura 29 - Reação de transesterificação do óleo de mamona e processo de separação entre o biodiesel de mamona e a glicerina... 92
Figura 30 - Container de aço-inox utilizado para armazenagem das amostras... 92
Figura 31 - Fluxograma geral da produção de biodiesel... 93
Figura 32 - Titulador potenciométrico automático de bancada modelo AT-500N da marca KEM... 96
Figura 33 - Densímetro digital de bancada DE-40... 100
Figura 34 - Equipamento HFP 380 Pensky Martens utilizado para a determinação do ponto de fulgor... 102
Figura 35 - Tampa do aparelho de ponto de fulgor... 103
Figura 36 - Analisador de enxofre TS 3000 da Thermo Scientific... 105
Figura 37 - Viscosímetro cinemático TVB445... 107
Figura 38 - Equipamento de cromatografia a gás utilizado para determinação do teor de metanol e etanol em biodiesel... 109
Figura 39 - Analisador da estabilidade oxidativa de biodiesel, óleos e gorduras, modelo 843 Biodiesel Rancimat da Metrohm... 114
Figura 40 - Cromatograma da determinação de metanol e etanol do biodiesel de girassol... 123
Figura 41 - Cromatograma da determinação e quantificação dos ésteres no biodiesel de girassol... 126
Figura 42 - Cromatograma da determinação e quantificação dos ésteres no biodiesel de mamona... 126
Figura 43 - Cromatograma da determinação e quantificação dos ésteres no biodiesel de soja... 127
Figura 44 - Efeito da adição do biodiesel de mamona sobre a massa específica do biodiesel de girassol e do biodiesel de soja... 130
Figura 45 - Efeito da adição do biodiesel de mamona sobre a viscosidade cinemática do biodiesel de girassol e do biodiesel de soja... 132
Figura 47 - Curvas TG/DTG do óleo de girassol, óleo de mamona e óleo de soja... 136
Figura 48 - Sobreposição das curvas TG do óleo de girassol e do seu respectivo
biodiesel... 141
Figura 49 - Sobreposição das curvas TG do óleo de mamona e do seu respectivo
biodiesel... 141
Figura 50 - Sobreposição das curvas TG do óleo de soja e do seu respectivo
biodiesel... 142
Figura 51 - Sobreposições das curvas TG do biodiesel de girassol, mamona e soja. 143
Figura 52 - Sobreposições das curvas DTG do biodiesel de girassol, mamona e
soja... 143
Figura 53 - Sobreposições das curvas TG das blends composta por biodiesel de
girassol e mamona (G/M) nas proporções 20, 40, 50, 60 e 80%... 145
Figura 54 - Curvas DTG sobrepostas das blends de biodiesel de girassol e
mamona nas proporções 20, 40, 50, 60 e 80%... 146
Figura 55 - Sobreposições das curvas TG das blends composta por biodiesel de
soja e mamona nas proporções 20, 40, 50, 60 e 80%... 147
Figura 56 - Sobreposições das curvas DTG das blends composta por biodiesel de
soja e mamona nas proporções 20, 40, 50, 60 e 80%... 148
Figura 57 - Curvas de P-DSC dinâmica sobrepostas do biodiesel de girassol,
mamona e soja... 150
Figura 58 - Curvas de P-DSC dinâmica sobrepostas das blends de girassol e
mamona... 151
Figura 59 - Sobreposição das curvas de P-DSC das blends de soja e mamona... 153
Figura 60 - Sobreposições das curvas de P-DSC modo isotérmico para os
biocombustíveis de girassol, mamona e soja... 154
Figura 61 - Sobreposição das curvas de P-DSC do modo isotérmico das blends de girassol e mamona... 156
Figura 62 - Sobreposição das curvas de P-DSC, método isotérmico das blends
soja/mamona 20, 40, 50, 60 e 80%... 157
Figura 63 - Sobreposição das curvas Rancimat (teste de estabilidade oxidativa)
dos óleos de girassol, mamona e soja... 159
Figura 64 - Sobreposição das curvas Rancimat (teste de estabilidade oxidativa)
dos biocombustíveis de girassol, mamona e soja a 110 °C... 160
Figura 65 - Curvas Rancimat (teste de estabilidade oxidativa) sobreposta do
biodiesel de girassol, mamona e soja a 110 °C... 162
Figura 66 - Curvas Rancimat (teste de estabilidade oxidativa) sobreposta do
LISTA DE TABELAS
Tabela 1 - Composição aproximada dos ácidos graxos em alguns óleos e gorduras
comuns... 30
Tabela 2 - Ácidos graxos de ocorrência natural com seus respectivos pontos de fusão... 31
Tabela 3 - Características físico-químicas do óleo de girassol... 37
Tabela 4 - Características físico-químicas do óleo de mamona... 42
Tabela 5 - Características físico-químicas do óleo de soja... 45
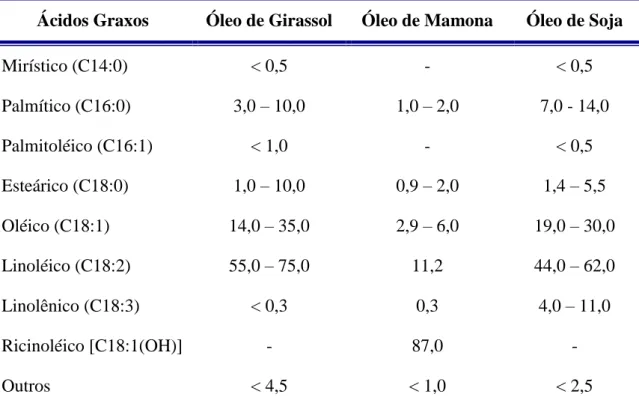
Tabela 6 - Composição média de ácidos graxos (%) dos óleos de girassol, mamona e soja... 45
Tabela 7 - Tamanho da alíquota a ser analisada conforme acidez da amostra de acordo com a NBR 14448... 97
Tabela 8 - Tamanho da alíquota a ser analisada conforme teor de enxofre da amostra, de acordo com a NBR 5353... 106
Tabela 9 - Condições de análise para determinação do teor de enxofre total pela ASTM D6751... 106
Tabela 10 - Condições de análise de acordo com a NBR 15343... 110
Tabela 11 - Condições de programação de temperatura do forno para análise de teor de ésteres... 112
Tabela 12 - Composição e percentuais relativo do padrão F.A.M.E mix (C8:0 - C24:1)... 112
Tabela 13 - Características físico-químicas dos óleos de girassol, mamona e soja... 117
Tabela 14 - Rendimento das reações de transesterificação das amostras de biodiesel... 119
Tabela 15 - Características físico-químicas do biodiesel de girassol, mamona e soja obtidos pela rota metílica... 120
Tabela 16 - Dados obtidos na determinação de metanol e etanol do biodiesel de girassol, mamona e soja por cromatografia a gás... 124
Tabela 17 - Determinação e quantificação do total de ésteres do biodiesel de girassol, mamona e soja por cromatografia a gás... 128
Tabela 18 - Dados termogravimétricos do óleo de girassol, mamona e soja... 139
Tabela 19 - Dados termogravimétricos do biodiesel de girassol, mamona e soja... 144
Tabela 20 - Dados termogravimétricos das blends girassol/mamona na razão de aquecimento 10 ºC.min-1... 147
Tabela 21 - Dados termogravimétricos das blends soja/mamona na razão de aquecimento 10 ºC.min-1... 149
Tabela 23 - Dados da temperatura onset (OT) obtidos por P-DSC através do
método dinâmico para as blends de girassol/mamona... 152
Tabela 24 - Dados das temperaturas onset (OT) obtidos por P-DSC através do
método dinâmico para as blends de soja/mamona... 153
Tabela 25 - Dados dos tempos de indução oxidativa (OIT) obtidos pela análise de P-DSC, método isotérmico do biodiesel de girassol, mamona e soja... 155
Tabela 26 - Dados dos tempos de indução oxidativa (OIT) obtidos pela análise de P-DSC, método isotérmico para as blends girassol/mamona... 156
Tabela 27 - Dados do tempo de indução oxidativo (OIT) obtidos pela análise de
P-DSC, método isotérmico para o biodiesel de girassol, mamona e soja... 158
Tabela 28 - Períodos de indução (IP) obtidos pela análise de Rancimat para os
óleos de girassol, mamona e soja... 159
Tabela 29 - Períodos de indução (IP) obtidos pela análise de Rancimat para o
biodiesel de girassol, mamona e soja... 161
Tabela 30 - Períodos de indução (IP) obtidos pela análise de Rancimat para as
blends girassol/mamona... 162
Tabela 31 - Períodos de indução (IP) obtidos pela análise de Rancimat para as
LISTA DE ABREVIATURAS
ABIOVE - Associação Brasileira das Indústrias de Óleos Vegetais
ABNT - Associação Brasileira de Normas Técnicas
AGL - Ácidos Graxos Livres
AH - Antioxidante
ANVISA - Agência Nacional de Vigilância Sanitária
ANP - Agência Nacional do Petróleo, Gás Natural e Biocombustíveis
AOCS - American Oil Chemist’s Society
AOM - Active Oxygen Method
ASTM - American Society of Testing and Materials
BLEND G/M - Mistura de biodiesel de girassol e mamona
BLEND S/M – Mistura de biodiesel de soja e mamona
B100 – Biodiesel puro
BHA - Buthylated Hydroxy Anisole
BS EM - British Standart
CG - Cromatografia a Gás
CONAB - Companhia Nacional de Abastecimento
DMA - Análise Mecânica Dinâmica
DSC - Calorimetria Exploratória Diferencial
DTA - Análise Térmica Diferencial
DTG - Termogravimetria Derivada
FAME - Fatty Acid Methyl Esters
FID - Flame Ionization Detector
ICOA - International Castor Oil Association
ICTAC - International Confederation for Thermal Analysis and Calorimetry
II - Índice de Iodo
LII - Límpido e Isento de Impurezas
ND - Não Detectado
NI - Não Identificado
IP - Induction Period
OIT - Tempo de Indução Oxidativo
OSI - Oxidative Stability Index
OPEP - Organização dos Países Exportadores de Petróleo
PE - Ponto de Ebulição
PF - Ponto de Fusão
PNDB - Programa Nacional de Produção e Uso de Biodiesel
PDSC - Calorimetria Exploratória Diferencial a Alta Pressão
PTV - Programmed Temperature Vaporization
PV - Value Peroxid
RANP - Resolução da Agência Nacional do Petróleo, Gás Natural e Biocombustíveis
RDC - Resolução da Diretoria Colegiada
SEBRAE - Serviço Brasileiro de Apoio às Micro e Pequenas Empresas
TG - Termogravimetria
TMA - Análise Térmica Mecânica
TMDSC - Calorimetria Exploratória Diferencial com Temperatura Modulada
USDA - United States Department of Agriculture
SUMÁRIO
1 INTRODUÇÃO... 20
2 OBJETIVOS... 23
2.1 OBJETIVO GERAL... 23
2.2 OBJETIVOS ESPECÍFICOS... 23
3 FUNDAMENTAÇÃO TEÓRICA... 24
3.1 ATUAL SITUAÇÃO ENERGÉTICA... 24
3.2 ENERGIAS RENOVÁVEIS... 26
3.2.1 Óleos e gorduras... 29
3.2.1.1 Girassol... 33
3.2.1.1.1 Características do óleo de girassol... 36
3.2.1.2 Mamona... 37
3.2.1.2.1 Características do óleo de mamona... 40
3.2.1.3 Soja... 42
3.2.1.3.1 Características do óleo de soja... 44
3.3 ÓLEOS VEGETAIS COMO ALTERNATIVA DE COMBUSTÍVEIS ... 46
3.4 BIODIESEL... 47
3.4.1 Processo de obtenção de biodiesel... 48
3.4.1.1 Reação de transesterificação..., 50
3.4.2 Biodiesel de girassol... 53
3.4.3 Biodiesel de mamona... 54
3.4.4 Biodiesel de soja... 55
3.5 ESPECIFICAÇÕES DO BIODIESEL... 57
3.5.1 Índice de acidez... 57
3.5.2 Índice de iodo... 59
3.5.3 Massa específica ... 61
3.5.4 Viscosidade cinemática... 62
3.5.5 Ponto de fulgor... 64
3.6 ESTABILIDADE DE ARMAZENAMENTO... 65
3.6.1 Reação de oxidação... 68
3.6.1.1 Antioxidantes... 73
3.7 METODOLOGIAS PARA TESTE DE ESTABILIDADE ... 74
3.7.1 Teste de forno Schaal... 75
3.7.3 Índice de estabilidade oxidativa... 76
3.7.4 Calorimetria exploratória diferencial a alta pressão... 77
3.8 CROMATOGRAFIA EM FASE GASOSA... 78
3.8.1 Técnicas de injeção... 78
3.9 ANÁLISE TÉRMICA... 81
3.9.1 Termogravimetria (TG)... 82
3.9.2 Termogravimetria derivada (DTG)... 83
3.9.3 Calorimetria exploratória diferencial a alta pressão... 83
3.10 RANCIMAT... 85
4 METODOLOGIA... 88
4.1 CARACTERIZAÇÃO DOS ÓLEOS VEGETAIS... 88
4.2 OBTENÇÃO DO BIODIESEL DE GIRASSOL, MAMONA E SOJA... 88
4.2.1 Biodiesel a partir dos óleos de girassol e soja... 89
4.2.2 Biodiesel a partir do óleo de mamona... 91
4.2.3 Fluxograma da produção de biodiesel... 93
4.3 CARACTERIZAÇÃO FÍSICO-QUÍMICA... 94
4.3.1 Ácidos graxos livres... 94
4.3.2 Índice de acidez... 95
4.3.2.1 Óleos vegetais... 95
4.3.2.2 Biocombustíveis e blends... 96
4.3.3 Índice de iodo... 98
4.3.4 Massa específica a 20 °C... 100
4.3.5 Ponto de fulgor... 101
4.3.6 Teor de enxofre total por fluorescência ultravioleta... 104
4.3.7 Viscosidade cinemática a 40 ºC... 107
4.4 CROMATOGRAFIA EM FASE GASOSA... 108
4.4.1 Determinação de metanol e etanol em biodiesel... 108
4.4.2 Teor de ésteres... 111
4.5 ESTUDO DA ESTABILIDADE TÉRMICA E OXIDATIVA DOS ÓLEOS VEGETAIS, BIOCOMBUSTÍVEIS E SUAS RESPECTIVAS BLENDS... 113
4.5.1 Termogravimetria (TG/DTG)... 113
4.5.2 Calorimetria exploratória diferencial a alta pressão (P-DSC)... 113
4.5.3 Estabilidade oxidativa a 110 °C pelo método Rancimat... 114
5.1 CARACTERIZAÇÃO FÍSICO-QUÍMICA DOS ÓLEOS DE GIRASSOL,
MAMONA E SOJA... 116
5.2 OBTENÇÃO E CARACTERIZAÇÃO FÍSICO-QUÍMICA DO BIODIESEL DE GIRASSOL, MAMONA E SOJA... 119
5.3 CARACTERIZAÇÃO DO BIODIESEL DE GIRASSOL, MAMONA E SOJA POR CROMATOGRAFIA À GÁS... 123
5.3.1 Determinação do metanol e etanol no biodiesel de girassol, mamona e soja... 123
5.3.2 Determinação e quantificação dos ésteres no biodiesel de girassol, mamona e soja... 125
5.4 EFEITO DA ADIÇÃO DO BIODIESEL DE MAMONA SOBRE O BIODIESEL DE GIRASSOL E SOJA NAS PROPORÇÕES 20, 40, 50, 60 E 80% ... 129
5.4.1 Massa específica... 130
5.4.1.1 Blends girassol/ mamona e soja/mamona... 130
5.4.2 Viscosidade cinemática... 131
5.4.2.1 Blends girassol/mamona e soja/mamona... 131
5.5 ESTUDO DA ESTABILIDADE TÉRMICA E OXIDATIVA... 134
5.5.1 Análise termogravimétrica (TG/DTG)... 135
5.5.1.1 Óleo de girassol, mamona e soja... 135
5.5.1.2 Biodiesel de girassol, mamona e soja... 140
5.5.1.3 Blends... 145
5.5.1.3.1 Blends girassol/mamona 20, 40, 50, 60 e 80%... 145
5.5.1.3.2 Blends soja/mamona 20, 40, 50, 60 e 80%... 147
5.5.2 Análise por calorimetria exploratória diferencial a alta pressão (P-DSC)... 149
5.5.2.1 Método dinâmico... 149
5.5.2.1.1 Biodiesel de girassol, mamona e soja... 149
5.5.2.1.2 Blends de girassol/ mamona 20, 40, 50, 60 e 80%... 151
5.5.2.1.3 Blends de soja/mamona 20, 40, 50, 60 e 80%... 152
5.5.2.2 Método isotérmico... 154
5.5.2.2.1 Biodiesel de girassol, mamona e soja... 154
5.5.2.2.2 Blends de girassol/mamona 20, 40, 50, 60 e 80%... 155
5.5.2.2.3 Blends de soja/mamona 20, 40, 50,60 e 80%... 157
5.5.3 Rancimat... 158
5.5.3.1 Óleo de girassol, mamona e soja... 158
5.5.3.3 Blends girassol/mamona 20, 40, 50, 60 e 80%... 161
5.5.3.4 Blends soja/mamona 20, 40, 50, 60 e 80%... 163
6 CONSIDERAÇÕES FINAIS... 165
1 INTRODUÇÃO
A preocupação, bem como a discussão e a busca por combustíveis ambientalmente
corretos, tem nos últimos anos aguçado a comunidade científica. Busca esta, bem
antecedente às etapas de escassez que sumarizaram na crise mundial do petróleo. Essa
preocupação reside no fato, de que os combustíveis que suprem a grande demanda
energética serem oriundos principalmente de fontes não-renováveis de energia, acentuando
ao fato de serem nocivos ao meio ambiente e, por conseguinte poluidores em potencial
(KNOTHE et al., 2005, MA et al., 1999, CAMARA, 2006).
Atualmente, as mudanças climáticas associadas à liberação de gases provenientes
da queima de combustíveis fósseis, ao alto preço internacional do petróleo e à preocupação
com o desenvolvimento sustentável tem contribuído para a retomada da intenção original
de Rudolph Diesel de empregar óleos vegetais em motores movidos a diesel mineral
(SCHUCHARDT et al., 2007).
Os óleos vegetais foram inicialmente, estudados como fonte alternativa de
combustíveis pelo engenheiro alemão Rudolph Christian Karl Diesel, logo após a obtenção
da patente para o seu motor de auto-ignição em 23 de fevereiro de 1892. Em 1898, por
ocasião da Feira Mundial de Paris o motor foi oficialmente apresentado, fazendo uso de
óleo de amendoim como combustível. Os primeiros motores tipo diesel eram de injeção
direta, razão pela qual, podiam ser alimentados por petróleo filtrado, óleos vegetais in
natura e até mesmo por óleo de peixe. Nesse âmbito, entre 1911 e 1912 afirmou “o motor a diesel poderá ser alimentado por óleos vegetais, e ajudará no desenvolvimento agrário
dos países que vierem a utilizá-los. O uso de óleos vegetais como combustível pode ser
insignificante hoje em dia, mas com o tempo, irão se tornar tão relevante quanto o
petróleo e o carvão vegetal são atualmente.” (CAMARA, 2006).
Óleos vegetais são misturas compostas essencialmente por triacilglicerídeos de
diferentes ácidos graxos (SUAREZ, 2007), que atribuem ao fluido algumas propriedades
físicas como alta viscosidade, elevado ponto de névoa e baixa volatilidade, além de
características químicas, como alto grau de insaturação, cujos efeitos no motor limitam a
sua possibilidade de uso na forma direta.
Dessa forma, visando à modificação das propriedades indesejáveis dos óleos
vegetais no motor, várias abordagens têm sido consideradas para contornar esses
a inserção dos óleos vegetais na matriz energética, tais como: modificações no motor,
misturas de óleos vegetais com diesel fóssil, microemulsificações, transesterificação e
craqueamento ou pirólise de óleos, gorduras ou ácidos graxos, sendo este último inviável
economicamente por ocorrer a altas temperaturas (acima de 350 °C) na ausência ou
presença de um catalisador. (MIERTUS, 2009, SUAREZ e MENEGHETTI, 2007).
Dentre as possibilidades apresentadas, a transesterificação, de fato, denota ser uma
excelente opção, devido à simplicidade no processo de obtenção e viabilidade tecnológica
e de custos, além de boas conversões e alto rendimento de produtos (SCHUCHARDT et
al., 2007, FONTOURA et. al., 2008).
O biodiesel apresenta-se como um recurso natural renovável e biodegradável, e
devido às vantagens apresentadas nos aspectos econômico, tecnológico, social e ambiental,
verifica-se que a produção do mesmo é sustentável (CONCEIÇÃO et al., 2007). No
entanto, a oferta de matéria-prima parece ser uma das principais dificuldades restritivas
para a implementação de um programa de produção extensiva de biodiesel. A maior parte
do biodiesel produzido no mundo deriva do óleo de soja e canola, porém, segundo Parente
(2003), todos os óleos vegetais podem ser transformados em biodiesel. Dentre eles, o óleo
de girassol destaca-se por suas excelentes características físico-químicas, cuja produção da
oleaginosa está entre as maiores culturas do mundo, apresentando viabilidade
técnico-ambiental na produção de biocombustíveis (SOUZA et al., 2005).
Atualmente, a matéria-prima para produção de óleo no Brasil encontra-se
fortemente concentrada na cultura da soja. A diversificação da matéria-prima é uma saída
para o aumento da oferta de oleaginosas destinada à produção de biodiesel. Nesse
contexto, o óleo de mamona é uma das mais promissoras matérias-primas entre as
disponíveis no Brasil. A mamoneira cresce mesmo sem cultivo e em grandes quantidades
na maioria dos países tropicais e subtropicais. É bastante tolerante a diferentes climas e
tipos de solos, além de ser disponível a baixo custo (OGUNNIYI, 2006). Tem
características incomuns para um óleo vegetal, a exemplo da viscosidade elevada e a maior
solubilidade em álcoois, decorrentes das ligações de hidrogênio dos seus grupos hidroxilas,
além de uma alta estabilidade.
A determinação da qualidade do combustível é, portanto, um aspecto de grande
importância para o sucesso da comercialização do biodiesel. A manutenção da oferta de
um combustível de alta qualidade é um pré-requisito para aceitação do biodiesel no
oleaginosas não atendem às especificações exigidas e, nesses casos, uma alternativa é a
utilização de blends de biodiesel utilizando diferentes oleaginosas.
O biodiesel é susceptível à oxidação quando na presença de fatores como ar,
elevada temperatura, luz e outros parâmetros que podem acelerar os processos oxidativos.
A questão da estabilidade oxidativa afeta a qualidade do biodiesel principalmente em
decorrência de um longo período de armazenagem.
Os testes acelerados, recorrendo a condições padronizadas de oxidação acelerada
(oxigenação intensiva, tratamento térmico e/ou catálise metálica), permitem estimar de
forma rápida a estabilidade oxidativa de uma matéria graxa. Uma vez que os fenômenos
naturais de oxidação são processos lentos, desenrolando-se frequentemente ao longo de
vários meses, os testes de estabilidade em tempo real tornam-se por vezes incompatíveis
com o controle de qualidade em nível industrial. Deste modo, os testes de estabilidade
acelerados assumem particular importância na rotina analítica.
Os procedimentos padrões para a determinação da estabilidade oxidativa (medida
do período de indução) utilizam equipamentos Rancimat e Oxidative Stability Instruments
(OSI). Porém, muitos pesquisadores têm procurado por técnicas mais rápidas e eficientes
para tal análise, e em muitos estudos, tem sido utilizado a Calorimetria Exploratória
Diferencial (DSC), pois a oxidação é um fenômeno exotérmico e o tempo de análise média
é de 4 horas, bem menor do que através dos métodos convencionais (GONDIM, 2009).
É nessa premissa que este trabalho visa avaliar o efeito e a viabilidade da adição do
biodiesel de mamona como agente antioxidante em distintas percentagens, sobre as
estabilidades térmica e oxidativa do biodiesel metílico de girassol e de soja, em frações
2 OBJETIVOS
2.1 OBJETIVO GERAL
O referido trabalho visa avaliar o efeito e a viabilidade da adição do biodiesel
metílico de mamona como agente antioxidante em distintas percentagens, sobre as
estabilidades térmica e oxidativa do biodiesel metílico de girassol e de soja, em frações
mássicas variando de 20 a 80% m/m.
2.2 OBJETIVOS ESPECÍFICOS
Determinar as propriedades físico-químicas dos óleos de girassol, mamona e soja,
visando à qualidade dos mesmos para a produção do biodiesel;
Obter o biodiesel de girassol, mamona e soja pela rota metílica e catálise
homogênea alcalina;
Caracterizar os biocombustíveis pelas suas propriedades físico-químicas, bem
como, determinar os teores de ésteres, metanol e/ou etanol por cromatografia a gás;
Obter as blends girassol/mamona e soja/mamona nas percentagens: 20, 40, 50, 60 e
80%;
Estudar a estabilidade térmica dos óleos, biocombustíveis e suas respectivas blends
utilizando a termogravimetria (TG/DTG);
Avaliar e comparar a estabilidade oxidativa dos óleos, biocombustíveis e das blends, fazendo uso de métodos termoquímicos, tais como: Calorimetria
3 FUNDAMENTAÇÃO TEÓRICA
3.1 ATUAL SITUAÇÃO ENERGÉTICA
Decorreram entre os anos de 1973 e 1980, os dois choques mais íngremes do
petróleo, durante os quais o Brasil sofreu o impacto da elevação dos preços, principalmente
devido a uma forte dependência materializada na importação de 80% do óleo bruto
consumido no país.
A partir do novo patamar de preços e das necessidades de crescimento econômico e
desenvolvimento industrial, o país adotou duas grandes estratégias para contornar a crise
investindo no aumento da produção doméstica de petróleo e na implantação do Proálcool,
considerado como o mais bem-sucedido programa de substituição de combustíveis
derivados de petróleo do mundo. Hoje, a matriz energética brasileira é um exemplo de
sustentabilidade, pois conta com a maior participação de energias renováveis
(MINISTÉRIO DE MINAS E ENERGIA, 2010).
Segundo a Organização dos Países Exportadores de Petróleo (OPEP), os preços do
petróleo podem alcançar, em breve, US$ 200 o barril, e muitos analistas acreditam que
nunca será inferior a US$ 100. As consequências desse novo patamar para o Brasil poderão
acarretar em um grau de dependência infinitamente inferior àquele verificado nas décadas
de 1970 e 1980, o que permite afirmar, com uma política energética adequada, que os
desafios do futuro, no âmbito energético, poderão ser sanados.
Segundo a Revista BiodieselBR, a produção de petróleo segue uma curva em forma
de sino (curva de Hubbert). Na parte ascendente da curva, os custos de produção são
significativamente mais baixos do que na parte descendente, quando é necessário um maior
esforço (despesa) para extrair petróleo de poços que estão tendendo a inativez, ou seja, o
petróleo é abundante e barato na curva ascendente, escasso e caro na curva descendente. O
pico da curva coincide com o ponto em que as reservas mundiais de petróleo estão
consumidas em 50%. Peak Oil é o termo da indústria para o topo da curva e, uma vez
passado esse pico, a produção de petróleo começa a decair enquanto os custos começam a
aumentar (BIODIESELBR, 2010).
As estatísticas mais otimistas indicam que o pico da produção petrolífera será
governamentais como o Observatório Geológico dos Estados Unidos, das companhias de
petróleo, ou de economistas que não consideram a dinâmica do esgotamento de recursos.
Segundo a Agência Nacional do Petróleo, Gás Natural e Biocombustíveis (ANP),
cerca de 45% da energia e 18% dos combustíveis consumidos no Brasil já são renováveis.
No mundo, 86% da energia advêm de fontes energéticas não-renováveis. Pioneiro mundial
no uso de biocombustíveis, o Brasil alcançou uma posição almejada por muitos países que
buscam fontes renováveis de energia, como alternativas estratégicas ao petróleo. A figura 1
sumariza o histórico da evolução dos biocombustíveis no Brasil em virtude das crises do
petróleo, que resultaram em escassez e, por conseguinte, alto custo de aquisição dessas
fontes de energia limpa.
Figura 1 - Evolução dos biocombustíveis no Brasil.
Fonte: ANP, 2010
A permanência dos preços atuais poderá acarretar numa recessão em muitos países
devido ao impacto dos preços dos energéticos na economia, inclusive nos preços dos
necessidade de políticas de conservação de energia, de ampliação da fronteira de
prospecção e aproveitamento das reservas existentes, e, principalmente, da busca por
fontes renováveis de energia. Sendo esta a mais poderosa arma no combate à escalada de
preços das commodities agrícolas.
Diversas razões justificam um programa que tem por intuito substituir o diesel
oriundo do petróleo. Para o Brasil é um fator relevante, pois o mesmo, não possui
auto-suficiência em diesel e sua posição é de importador. É neste âmbito, que o Programa
Nacional de Produção e Uso de Biodiesel (PNPB) surge visando à implantação do
processo de produção e do uso desse biocombustível de forma sustentável, técnica e
econômica, com enfoque na inclusão social e no desenvolvimento regional, com a geração
de emprego e renda.
3.2 ENERGIAS RENOVÁVEIS
Mediante o que foi exposto, tem-se buscado por outras fontes de energia que não
sejam limitadas, finitas e não-renováveis, como no caso do petróleo e seus derivados. Essas
fontes denominadas energias alternativas ou renováveis incluem o carvão vegetal, as
energias solar e eólica e a biomassa.
Segundo Omachi et al. (2004), biomassa é todo material orgânico, não-fóssil, que
possua energia química intrínseca. Podem ser incluídas no grupo das biomassas todas as
vegetações aquáticas ou terrestres, as árvores, o lixo orgânico, resíduo de agricultura,
esterco de animais e outros tipos de restos industriais. As oleaginosas são opções de fontes
de matéria-prima, os óleos vegetais, para a produção de combustíveis renováveis.
O Brasil é um país que por sua extensa área geográfica e climas tropical e
subtropical apresenta uma ampla diversidade de matérias-primas cotejadas para a produção
de biodiesel. Dentre as principais, estão oleaginosas como: algodão, amendoim, dendê,
girassol, mamona, pinhão manso e soja (CARTILHA BIODIESEL SEBRAE, 2009).
Na literatura, podem ser encontrados diversos estudos oriundos de pesquisas
brasileiras sobre o tema fontes renováveis. Nesse âmbito, podem ser citados os trabalhos
desenvolvidos por Sodré et al. (2011) cujo enfoque foi o estudo das propriedades
físico-químicas de blends (misturas) de biodiesel de óleo de fritura ou biodiesel de óleo de
mamona com óleo diesel mineral. Os pesquisadores avaliaram algumas propriedades como
teor de enxofre, os quais foram medidos de acordo com métodos de teste padrão. Foi
observado um aumento da densidade e da viscosidade concomitante ao aumento da
concentração do biodiesel. Enquanto o teor de enxofre e o índice de cetano foram
diminuídos com o elevado teor do biodiesel no óleo diesel mineral.
Soares et al. (2010) estudaram os parâmetros favoráveis à produção do biodiesel
obtido pela síntese etanólica dos óleos de nabo forrageiro, girassol e soja. Os parâmetros
avaliados foram à quantidade de catalisador, o tempo reacional e a temperatura, os
comportamentos térmicos também foram avaliados. Além disso, também foi investigada a
relação entre o rendimento de conversão e a composição química dos ácidos graxos de
cada matéria-prima.
Uma metodologia rápida de degradação térmica e contato com o ar foi a estudo
desenvolvido por Célio et al. (2009), para avaliar a estabilidade oxidativa do biodiesel do
óleo de mamona sob influência de quatro tipos de antioxidantes fenólicos sintéticos e a
concentração de cada um foram observados.
Com a finalidade de ilustrar a relevância dessas matérias-primas no âmbito energias
renováveis e a potencialidade do país na produção de oleaginosas, a figura 2 ilustra um
mapa com a distribuição dos diversos cultivares oleaginosos no território brasileiro, a qual,
permite a visualização das regiões brasileiras e as principais matérias-primas nelas
produzidas, levando em consideração as condições edafoclimáticas do zoneamento
Figura 2 - Potencialidade brasileira para produção de oleaginosas. Mapa construído a
partir dos trabalhos de Meireles (2003) e do Zoneamento Agrícola de Risco Climático –
MAPA
Fonte: Cartilha SEBRAE, 2009
O semiárido brasileiro é uma das maiores, mais populosas e também mais úmidas
ecoregiões do mundo, estendendo-se por uma área que abrange a maior parte dos Estados
da Região Nordeste (86,48%), a Região Setentrional do Estado de Minas Gerais (11,01%)
e o norte do Espírito Santo (2,51%), ocupando uma área total de 974.752 km2
(RODRIGUES, 2009 apud BELTRÃO, 2009). Ainda na Figura 3.2 é perceptível a forte
predominância de pinhão-manso, algodão e mamona no semi-árido nordestino, fontes que
se destacam por apresentarem um alto teor de óleo em suas sementes, resistência à seca e
3.2.1 Óleos e gorduras
Óleos e gorduras são substâncias insolúveis em água (hidrofóbicas), de origem
animal, vegetal ou mesmo microbiana, formadas predominantemente de produtos de
condensação entre glicerol e ácidos graxos chamados de triacilglicerídeos (MORETTO e
FETT, 1998).
Triacilglicerídeos, também chamados de triglicerídeos, são compostos em que os
três grupos OH do glicerol são esterificados com ácidos graxos (BRUICE, 2006). Quando
constituídos em grande parte por ácidos graxos saturados apresentam pontos de fusão e/ou
ebulição altos, caso contrário, se há uma considerável proporção de ácidos graxos
insaturados e poliinsaturados, os pontos de fusão são mais baixos, e isso também
dependerá da natureza da ligação. A tabela 1 mostra a percentagem aproximada de ácidos
graxos em alguns óleos e gorduras comuns, pode-se observar a relação existente entre o
Tabela 1- Composição aproximada dos ácidos graxos em alguns óleos e gorduras comuns
Ácidos Graxos Saturados Ácidos Graxos Insaturados
PF (°C) Láurico (C12:0) Mirístico (C14:0) Palmítico (C16:0) Esteárico (C18:0) Oléico (C18:1) Linoléico (C18:2) Linolênico (C18:3) Gorduras
Manteiga 32 2 11 29 9 27 4 -
Banha de Porco 30 - 1 28 12 48 6 -
Humana 15 1 3 25 8 46 10 -
Baleia 24 - 8 12 3 35 10 -
Óleos
Milho 20 - 1 10 3 50 34 -
Algodão -1 - 1 23 1 23 48 -
Oliva -24 - - 6 3 19 24 47
Linhaça -6 - - 7 2 84 5 -
Amendoim 3 - - 8 3 56 26 -
Cártamo -15 - - 3 3 19 70 3
Gergelim -6 - - 10 4 45 40 -
Soja -16 - - 10 2 29 51 7
Fonte: Bruice, 2006
Dentre todas as espécies relatadas, o óleo de oliva (Tabela 1) é o que apresenta
maior percentual de ácido linolênico (C18:3), e, por conseguinte, o menor ponto de fusão.
Segundo Bruice (2006), as propriedades físicas dos ácidos graxos dependem do
comprimento da cadeia de hidrocarbonetos e do grau de insaturação; como esperado, os
pontos de fusão dos ácidos graxos aumentam com o aumento da massa molecular devido
ao aumento das interações de van der Waals entre as moléculas.
A banha de porco é a que apresenta o maior percentual de ácido esteárico (C18:0) e
o segundo maior ponto de fusão, sendo o maior PF o da manteiga devido à maior
concentração dos ácidos graxos saturados: láurico (C12:0) e mirístico (C14:0), quando
comparado a substância supracitada. As ligações duplas em ácidos graxos insaturados
possuem geralmente a configuração cis. Essa configuração produz uma curvatura nas
moléculas que as impede de empacotarem firmemente como os ácidos graxos saturados.
Como resultado, os ácidos graxos insaturados possuem menos interações moleculares e,
moleculares equivalentes. Os pontos de fusão dos ácidos graxos insaturados diminuem à
medida que o número de duplas ligações aumenta. Um ácido graxo com 18 átomos de
carbono saturado, por exemplo, funde a 69 °C; a 13 °C, se possuir uma ligação dupla; a -5
°C, caso possua duas ligações duplas; e em -11 °C, se possuir três duplas ligações, como
pode ser visto na tabela 2 abaixo (BRUICE, 2006).
Tabela 2 - Ácidos graxos de ocorrência natural com seus respectivos pontos de fusão
Número de carbonos
Nome Comum
Nome Sistemático
Estrutura Ponto de
fusão (°C)
Saturado
12 Láurico Dodecanóico 44
14 Mirístico Tetradenóico 58
16 Palmítico Hexadecanóico 63
18 Esteárico Octadecanóico 69
20 Araquídico Eicosanóico 77
Insaturado
16 Palmitoléico (9Z)- hexadenóico 0
18 Oléico (9Z)- octadecenóico 13
18 Linoléico (9Z,12Z)- octadecadienóico
-5
18 Linolênico (9Z,12Z,15Z)- octadecatrienóico
-11
20 Araquidônico (5Z,8Z,11Z,14Z)- eicosatetraenóico
-50
20 EPA (5Z,8Z,11Z,14Z,17Z)-eicosapentaenóico
Os óleos vegetais diferem das gorduras, quanto ao seu estado de agregação à
temperatura ambiente. Enquanto os óleos são líquidos, em virtude da presença de
insaturações nas cadeias, que dificultam assim as interações moleculares, as gorduras se
caracterizam por misturas sólidas, em geral, por exibirem maior facilidade de
empacotamento intermolecular, em virtude da proporção dos grupos acila saturados e
insaturados presentes nos triglicerídeos. Os ácidos graxos representam mais de 95% da
massa molecular dos seus triglicerídeos (MORETTO e FETT, 1998). Na figura 3 estão
ilustradas as estruturas de uma molécula de gordura (a) e um óleo (b).
Figura 3 - Representação do arranjo molecular dos triglicerídeos em moléculas de gordura
(a) e óleo (b).
(a) (b)
Fonte: Bruice, 2006.
Além dos triacilgliceróis, os óleos contêm vários componentes em menor
proporção, como: mono e diglicerídeos (importantes como emulsionantes); ácidos graxos
livres; tocoferol (importante antioxidante); proteínas, esteróis e vitaminas (REDA e
3.2.1.1 Girassol
O girassol (Helianthus annuus L.) é uma planta oleaginosa, dicotiledônea,
pertencente à família Asteraceae, também conhecida como Compositea ou composta,
originária da América do Norte, provavelmente do Sudoeste dos Estados Unidos (figura 4)
(ANWAR, 2008 apud BELTRÃO, 2009). Esta espécie teve maior desenvolvimento na
antiga União Soviética, estando atualmente concentrada principalmente na Federação
Russa, Ucrânia, Argentina, Índia e França, países considerados os maiores produtores
mundiais na atualidade. No Brasil, presume-se que o cultivo do girassol tenha sido iniciado
na época da colonização, principalmente na região Sul, com a introdução do hábito do
consumo de suas sementes torradas (BELTRÃO, 2009).
Figura 4 - (a) Plantação de girassóis em Fargo, Dakota do Norte nos Estados Unidos e (b)
sementes de girassol.
(a) (b)
Fonte: Wikipédia, 2010
O girassol consiste numa das principais culturas de oleaginosas em todo o mundo,
cuja produção de óleo está entre 45-50% (baseado na massa de sementes sem casca)
(ANWAR, 2008). De acordo com o USDA (United States Department of Agriculture), na
safra de 2003/04, o girassol esteve entre as cinco maiores culturas de oleaginosas
soja (56,3%), canola (11,69%), algodão (10,46%) e amendoim (9,58%). No Brasil,
segundo esse mesmo órgão, pelos dados da CONAB, a produção de girassol do ano de
2003/08, passou de 85,8 para 144,3 toneladas métricas (BARROS, 2008).
Quando comparado à maioria das espécies normalmente cultivadas no Brasil,
apresenta características importantes, quando comparada à maioria das espécies
normalmente cultivadas no Brasil, das quais destacam-se: ciclo curto, elevada qualidade e
bom rendimento de óleo, que fazem dela uma opção atrativa aos produtores brasileiros
(FERRARI, 2005). Devido a essas particularidades agronômicas e à crescente demanda
dos setores industrial e comercial, a cultura do girassol está se constituindo em uma
importante alternativa econômica no sistema de rotação, consórcio e sucessão de culturas
nas regiões produtoras de grãos (OLIVEIRA,VIEIRA, 2004).
Embora possua um sistema radicular pivotante e profundo, caule vigoroso - como
ilustrado na figura 5, e ciclo rápido - entre 65 a 155 dias da emergência das plântulas, esta
é sensível à seca, podendo ser até um pouco tolerante em determinados períodos de seu
ciclo e dependendo do estresse, em condições de deficiência de água, sua produtividade
Figura 5 - Fases de desenvolvimento do girassol, com as respectivas exigências térmicas e
hídricas.
Fonte: Castro, 2007
Segundo Castro et al. (2005), temperaturas elevadas podem prejudicar o
desenvolvimento desta Asteraceae, em especial em condições de estresse hídrico. Esses
pesquisadores atribuem como temperaturas ótimas para o cultivo e desenvolvimento do
girassol, a faixa entre 18 e 24 °C, temperaturas estas, que distam da realidade do semiárido
nordestino.
A partir desta oleaginosa, é produzido o óleo comestível e os subprodutos da
extração, tais como: tortas, expeller e farinhas, que são também aproveitadas. Segundo
Oliveira e Vieira (2004), mais de 90% da produção mundial de girassol são destinados à
Fase Vegetativa Fase Reprodutiva
Germinação Crescimento Floração Enchimento
de Aquênios
Maturação Fisiológica
Lento Acelerado
Duração:
4 a 10 dias
Duração:
50 a 70 dias
Duração:
10 a 15 dias
Duração:
20 a 30 dias
Duração:
15 a 25 dias
Temperatura:
23 °C
Temperatura:
23 a 28 °C
Temperatura:
< 35 °C
Temperatura:
20 a 24 °C
Período
Seco
Água/dia:
0,5 a 0,7 mm
Água/dia:
0,7 a 6,0 mm
Água/dia:
6,0 a 8,0 m
Água/dia:
elaboração de óleo comestível, e a maior parte dos 10% restantes, para alimentação de
pássaros e para o consumo humano direto.
De acordo com Oliveira e Vieira (2004), para cada tonelada de grão, em média, são
produzidos 400 kg de óleo, 250 kg de casca e 350 kg de torta, com 45 a 50% de proteína
bruta, sendo este subproduto, basicamente, aproveitado na produção de ração, em misturas
com outras fontes de proteína.
3.2.1.1.1 Características do Óleo de Girassol
A qualidade de um óleo vegetal está intrinsecamente ligada a sua composição
química, ou seja, é dada pela composição de ácidos graxos, e sua utilidade na indústria
também depende desse fator. Um exemplo são os óleos direcionados ao ramo alimentício,
como os óleos utilizados para frituras, que devem possuir um alto grau de estabilidade
oxidativa a temperaturas elevadas (OLIVEIRA e VIEIRA, 2004); para tal, devem
apresentar na sua composição teores mínimos de ácidos graxos insaturados, altamente
susceptíveis aos processos oxidativos. Portanto, os teores de ácidos oleico (C18:1),
linoleico (C18:2) e linolênico (C18:3) devem ser relativamente baixos nesses compostos
gráxeos. Essa característica também é considerada para os óleos vegetais direcionados ao
ramo energético, pelo mesmo motivo.
O óleo de girassol está entre os óleos vegetais que apresentam um dos maiores
percentuais de ácidos graxos poliinsaturados, principalmente o ácido linoléico (C18:2)
(OLIVEIRA e VIEIRA, 2004). No entanto, contém apenas traços do ácido linolênico,
facilmente oxidável na presença de luz e calor (OLIVEIRA e VIEIRA, 2004).
As percentagens do ácido linoléico e oléico são de aproximadamente 90% do total
de ácidos graxos presentes no óleo de girassol. Há uma relação inversa entre ambos, sendo
esta, fortemente influenciada pelas condições ambientais, em especial a temperatura,
durante o desenvolvimento das sementes. Em temperaturas elevadas, ocorre aumento nos
níveis de ácido oléico e diminuição nos níveis de linoléico (OLIVEIRA e VIEIRA, 2004).
Tabela 3 - Características físico-químicas do óleo de girassol
Propriedades Físico-Químicas Valores de referência
Massa Específica a 20 °C (g.cm-3) 0,915 – 0,920
Índice de Refração a 25 °C 1,467 – 1,469
Índice de Iodo (g I2.100g-1) 110 – 143
Índice de Saponificação (mg KOH.g-1) 188 – 194
Matéria Insaponificável (%) < 1,5
Acidez (g ácido oléico.100g-1) < 0,3
Índice de Peróxido (meq.kg-1) < 10
Valores de Referência: RDC No482, de 23/09/1999, da Agência Nacional da Vigilância Sanitária – ANVISA Fonte: Campestre, 2008
3.2.1.2 Mamona
A mamoneira (figura 6) é uma oleaginosa de destacada importância no Brasil e no
mundo, a partir dela é obtido o óleo de mamona, também conhecido por óleo de rícino,
óleo de tangantangan, óleo de palma Christi, neolóide e óleo de castor, este é extraído da
semente da planta Ricinus Communis L., pertencente à família Euphorbiaceae, a qual é
abundantemente encontrada em regiões de climas topical e subtropical (MURA, 2005).
Figura 6 - (a) Cacho de mamona e (b) endosperma da semente da mamoneira.
(a) (b)
Foto: Walmar Pessoa
Fonte: Beltrão, 2007
Esta Euphorbiaceae apresenta crescimento denominado dicotômico, com vários
pontos de crescimento na mesma planta. Na figura 7 está ilustrada a organografia da
mamoneira, onde são observados os cachos principais e os de segunda e terceira ordens,
tanto em crescimento, como na fase de botão floral, este fato evidencia um período
indefinido de reprodução da mamoneira que depende do ambiente. A continuidade das
chuvas promove a emissão contínua de cachos pela planta, o que acaba se tornando uma
grande vantagem competitiva para condições de ocorrência de estresses ambientais, em
particular o hídrico (por falta ou excesso de água) e o término ocasionado pela ocorrência
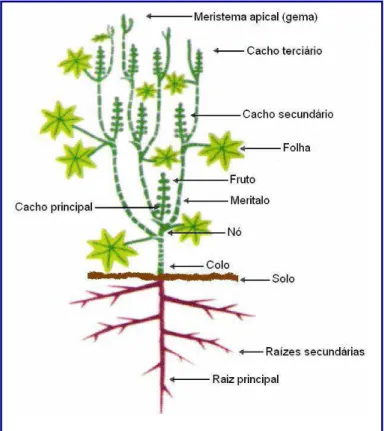
Figura 7 - Esquema ilustrativo da organografia da mamoneira adaptada de Weiss (1983) in
Beltrão et al. (2007).
Fonte: Beltrão et al., 2009
A mamona é de fácil cultivo e resistente à escassez de água, por esse motivo é ideal
para o extenso Semiárido Nordestino. Nessa região existem quase quatro milhões de
hectares apropriados, onde se pode alcançar o rendimento de até 1,5 toneladas de sementes
por hectare, enquanto a média nacional é de 750 kg de baga/ha quilos. Além disso, a
mamona pode se tornar uma alternativa produtiva para cerca de 1,5 milhões de pessoas de
baixa renda na região mais carente do Brasil (SILVA e LINO, 2009 apud BELTRÃO,
2009).
O teor de óleo extraído das sementes da mamona pode variar entre 35 a 55%
(BELTRÃO, 2009) mas a maior parte das cultivares plantadas comercialmente no Brasil
3.2.1.2.1 Características do óleo de mamona
Mura (2005), caracteriza o óleo de mamona como um líquido viscoso, amarelo
claro de odor característico, familiarmente conhecido devido ao seu uso como óleo
purgativo, cuja semente é extremamente tóxica devido à presença da proteína licina, mas
que não se encontra no óleo (ENCYCLOPEDIA OF CHEMICAL TECHNOLOGY, 1980;
THE MERCK INDEX, 2001; VILAR, 1991 apud MURA, 2005).
O óleo de mamona é considerado como um recurso comercial único de aplicações
singulares na indústria química em virtude da sua composição, cerca de 90% do óleo é
composto por um triglicerídeo, principalmente por ricinoleína, que é o componente
majoritário do ácido ricinoléico (ácido 12-hidroxi-9-octadeceno; C18:1,OH). O ácido
ricinoléico possui uma ligação insaturada, o qual lhe confere características peculiares
como o único óleo vegetal naturalmente hidroxilado, portanto, pertencente ao grupo dos
hidroxiácidos, além das propriedades químicas atípicas, é caracterizado pelo seu alto peso
molecular (298) e baixo ponto de fusão (-5 °C) (BELTRÃO, 2008; CVENGROS, 2006).
O grupo hidroxila confere ao óleo de mamona a propriedade exclusiva de
solubilidade em álcool (WEISS, 1983; MOSHKIN, 1986 apud BELTRÃO, 2008) e uma
alta viscosidade, a qual é mantida em uma ampla faixa de temperatura, essa propriedade é
apontada como a grande problemática que circunda o uso do óleo de mamona como
matéria-prima na produção de biodiesel, pois mesmo após o processo de transesterificação
o biodiesel apresenta valores de viscosidade que não se adequam as especificações. A alta
viscosidade pode ser atribuída à formação das pontes de hidrogênio inter ou
intramoleculares, como pode ser observado na figura 8, nas moléculas do ácido ricinoléico,
além de solidificarem a baixas temperaturas, possibilitando assim uma alta estabilidade
Figura 8 - Estrutura molecular do ácido ricinoléico de estrutura “linear” (a) e com a
formação das pontes de hidrogênio intramoleculares (b)
Fonte: Medeiros, 2010
A principal razão para a grande demanda mundial pelo óleo de mamona são suas
formas de utilização, tais como: hidrogenado, desidratado e oxidado, servindo como base
para diversos produtos industriais. Esses produtos, segundo International Castor Oil
Association (ICOA) são oriundos das seguintes reações químicas, listadas em ordem de
relevância: pirólise para produção do nylon, hidrogenação, desidratação, fusão cáustica
para produção dos ácidos sebácico e undecilênico e do heptaldeído (ambos, subprodutos da
pirólise), sulfonação, alcoxilação, oxidação/polimerização, esterificação, dimerização (da
desidratação) e outras (ICOA, 2009).
Dentre as vertentes supracitadas e outras ainda não relatadas, fazem do óleo de
mamona uma interessante matéria-prima de estrutura peculiar, as suas propriedades estão
Tabela 4 - Características físico-químicas do óleo de mamona
Propriedades Físico-Químicas Valores de referência
Massa Específica a 25°C (g.cm-3) 0,945 – 0,965
Índice de Refração 25 °C 1,473 – 1,477
Índice de Iodo (g I2.100g-1) 81 – 91
Índice de Saponificação (mg KOH.g-1) 176 – 187
Matéria Insaponificável (%) -
Acidez (g ácido oléico.100g-1) -
Índice de Peróxido (meq.kg-1) -
Valores de Referência: Physical and Chemical Characteristics of Oils, Fats and Waxes – AOCS. Fonte: Campestre, 2008
3.2.1.3 Soja
A soja [Glycine max (L.) Merrill] (figura 9) é uma espécie de leguminosa nativa,
pertencente à família Fabaceae, também conhecida com Leguminosae, proveniente da
Ásia Oriental, onde se desenvolveu principalmente ao longo do Rio Amarelo, na China.
Portanto, nas três primeiras décadas do século XX, a produção de soja era quase
exclusivamente feita nos países do Oriente, como a China, Indonésia, Japão e Coréia
(BELTRÃO, 2008).
O início da evolução da soja ocorreu com o aparecimento de plantas naturais
oriundas do cruzamento entre duas espécies de soja selvagem na antiga China