CENTRO DE CIÊNCIAS DA SAÚDE
PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS DA SAÚDE
BIODISPONIBILIDADE DE EDTMP-
153SAMÁRIO EM RATOS
TRATADOS COM DOCETAXEL
ARTHUR VILLARIM NETO
ARTHUR VILLARIM NETO
BIODISPONIBILIDADE DE EDTMP-
153SAMÁRIO EM RATOS
TRATADOS COM DOCETAXEL
Tese apresentada ao Programa de
Pós-Graduação em Ciências da Saúde da
Universidade Federal do Rio Grande do Norte
para a obtenção do título de Doutor
Orientador: Prof. Dr. Aldo da Cunha Medeiros
Co-orientador: Prof. Dr. Mário Bernardo Filho
iv
ARTHUR VILLARIM NETO
BIODISPONIBILIDADE DE EDTMP-
153SAMÁRIO EM RATOS
TRATADOS COM DOCETAXEL
Presidente da Banca Examinadora:
Prof. Dr. Aldo da Cunha Medeiros - UFRN
Banca Examinadora:
Prof. Dr. Adenilson de Souza da Fonseca (UERJ)
Prof. Dr. Jael Soares Batista (UFERSA)
Prof. Dr. Artur da Silva Carriço (UFRN)
Prof. Dr. Irami Araújo Filho (UFRN)
CATALOGAÇÃO NA FONTE
V722bVillarim Neto, Arthur.
Biodisponibilidade de EDTMP-153Samário em ratos tratados com docetaxel / Arthur Villarim Neto. – Natal, 2009.
58p.
Orientador: Prof. Dr. Aldo José da Cunha Medeiros. Co-orientador: Prof. Dr. Mário Bernardo Filho.
Tese (Doutorado) – Programa de Pós-Graduação em Ciências da Saúde. Centro de Ciências da Saúde. Universidade Federal do Rio Grande do Norte.
1. Quimioterapia – Tese. 2. Metástase óssea – Tese. 3. Radiofármacos – Tese. 4. EDTMP-153Samário – Tese. I. Bernardo Filho, Mário. II. Bernardo Filho, Mário. III. Título.
iii
CENTRO DE CIÊNCIAS DA SAÚDE
PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS DA SAÚDE
COORDENADORA DO PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS
DA SAÚDE:
v
DEDICATÓRIA
A José Martins, meu querido pai, maior incentivador dos meus estudos,
exemplo de superação pessoal, e a minha mãe, Rejane, pela dedicação à
família, minha eterna gratidão.
A Rachel, esposa e Sol da minha vida.
vi
A Deus,
Ao Professor Dr. Aldo da Cunha Medeiros, meu orientador, pela amizade,
apoio, inteligência e integridade exemplares.
Ao Professor Dr. Artur da Silva Carriço, pelo incentivo e pelas boas idéias.
A Rodrigo e Lídia, irmãos de sangue e companheiros de caminhada nesta vida.
A Gerôncio e Suely, amigos de todas as horas.
Ao Professor Dr. Irami Araújo Filho, pelo apoio prático e decisivo na execução
deste projeto.
A Amália Rego, pela presença constante e atenciosa no laboratório.
A Ítalo Medeiros de Azevedo, pela boa vontade e pela inteligência na análise
estatística.
A Dra. Marla Medeiros, médica nuclear e amiga, por ter trabalhado em dobro
nas horas em que estive ausente.
A Kércia e Kadja, companheiras nesta jornada e colegas de trabalho.
vii
SUMÁRIO
RESUMO...ix
1
INTRODUÇÃO ... 1
2
REVISÃO DE LITERATURA... 4
2.1.
Mecanismo de formação das metástases ósseas ... 4
2.2.
Tratamento da dor causada por metástases ósseas... 6
2.2.1. Medicações antiinflamatórias e opióides ... 6
2.2.2. Bifosfonatos e bloqueadores hormonais... 7
2.2.3. Tratamento cirúrgico... 7
2.2.4. Radioterapia externa ... 8
2.2.5. Radiofámacos utilizados no alívio da dor óssea... 8
2.2.6. Quimioterapia ... 14
3
ANEXAÇÃO DE ARTIGOS PUBLICADOS ... 17
3.1.
Biodistribution of samarium-153-EDTMP in rats treated with docetaxel.18
3.2.
Biodistribution of the Radiopharmaceutical Sodium Pertechnetate after
Biliopancreatic Bypass with a Duodenal Switch. ... 27
3.3.
Biodistribution of the radiophamarceutical sodium pertechnetate
(Na99mTcO4) after massive small bowel resection in rats... 38
3.4.
Influence of Splenectomy on the Biodistribition of Technetium-99m
Dimercaptosuccinic Acid (99mTc-DMSA)... 51
3.5.
Biodistribution of the Radiopharmaceutical Technetium-99m-Sodium
Phytate in Rats After Splenectomy ... 58
4
COMENTÁRIOS, CRÍTICAS E SUGESTÕES ... 65
viii
MBq
megabequerel
MBq/Kg
megabequerel por kilograma
% ATI
percentual de atividade injetada
% ATI/g
percentual de atividade injetada por grama
UFRN
Universidade Federal do Rio Grande do Norte
µCi
micro Curie
153
Sm
153Samário
EDTMP
etilenodiamina-tetrametileno fosfonato
EDTMP-
153Sm
153Samário
complexado
a
etilenodiamina-tetrametileno fosfonato
Emax
energia máxima de emissão
MeV
Mega elétron-volt
keV
quilo electron-volt
Gy
Gray (unidade de dose absorvida)
Bcl-2
B-cell lymphoma 2 (linfoma 2 de célula B)
MDP-Tc
99m99m
Tecnécio complexado a metileno-disfofonato
IPEN
Instituto de Pesquisas Energéticas e Nucleares
USP
Universidade de São Paulo
CNEN
Comissão Nacional de Energia Nuclear
PSA
Prostate-specific antigen (antígeno específico da
ix
RESUMO
A dor óssea decorrente das metástases é um sintoma comum nos tumores
avançados de mama e próstata. Nenhuma opção terapêutica isolada é
completamente eficaz, e uma série de modalidades costuma ser empregada,
entre eles a terapia com radiofármacos, como o samário
153-etilenodiamina-tetrametileno fosfonato (EDTMP-
153Sm). O docetaxel, um taxano com ação
sobre tumores avançados de mama e próstata, tem-se apresentado como uma
nova opção de tratamento quimioterápico. Muitos pacientes fazem uso
simultâneo de EDTMP-
153Sm e docetaxel. Este estudo procurou avaliar a
influência do docetaxel na biodisponibilidade de EDTMP-
153Sm em ratos
Wistar, aleatoriamente alocados em 2 grupos de 6 animais cada. O grupo DS
(docetaxel/samário) recebeu docetaxel (15 mg/kg) intraperitoneal em dois
ciclos com 11 dias de intervalo. Os ratos do grupo S (samário/controle) não
foram tratados com docetaxel. Nove dias após a quimioterapia, todos os
animais receberam 0.1ml de EDTMP-
153Sm via plexo orbital (25 Ci). Após 2
horas, os animais foram mortos, e realizaram-se análises de amostras de
cérebro, tireóide, pulmão, coração, estômago, cólon, fígado, rim e fêmures. O
percentual de radioatividade por grama (%ATI/g) de tecido de cada biópsia foi
determinado em contador gama automático (Wizard-1470, Perkin-Elmer,
Finland). No 9º dia após 2º ciclo de docetaxel, os ratos tiveram perda de peso
significante, passando de 353.66± 22.8g (controle/pré-tratamento) para
314,50±22,09g (p<0.5). Os %ATI/g nos órgãos dos ratos tratados com
EDTMP-153Sm e docetaxel tiveram redução significante nos fêmures direito e esquerdo,
rim, fígado e pulmão, quando comparados aos animais não tratados com
docetaxel. Em conclusão, a combinação de docetaxel com EDTMP-
153Sm foi
associada à menor concentração do radiofármaco em órgãos alvo. Futuras
investigações sobre o impacto do docetaxel na biodisponibilidade do
EDTMP-153Sm poderão complementar estes achados. Deve-se ressaltar o caráter
multidisciplinar deste estudo, que contou com a participação ativa e com a
troca constante de conhecimentos entre profissionais das áreas de Medicina
70 % dos pacientes acometidos por tumores avançados da mama e da próstata(1).
A dor óssea decorrente das metástases é um sintoma comum nestes casos e
freqüentemente determina a qualidade de vida nos últimos estágios da doença(2). O
principal mecanismo de dor óssea nas metástases é a distensão e o aumento da
pressão mecânica sobre as terminações nervosas locais(3). Tal sintoma interfere na
qualidade de vida do paciente e requer tratamento efetivo. Infelizmente, várias
modalidades terapêuticas, como analgésicos, terapia hormonal, orquiectomia,
quimioterápicos, bifosfonatos e tratamento cirúrgico não são eficazes em todos os
casos, especialmente no estágio final da doença(1). Radioterapia pode ser realizada
apenas em lesões ósseas bem definidas. A extensão do campo irradiado pode ser útil,
mas geralmente é acompanhada por graves efeitos colaterais(4).
Desta forma, a terapia sistêmica com radioisótopos, utilizando radiofármacos
com afinidade pelo tecido ósseo, torna-se uma opção valiosa e eficaz no tratamento da
dor óssea em pacientes com metástases difusas, especialmente no câncer de mama e
de próstata.
Os principais radiofármacos com eficácia estabelecida no tratamento da dor
óssea metastática são:
32Fósforo,
89Estrôncio,
186Rênio,
188Rênio e
153Samário. No
Brasil, a produção nacional restringe-se ao
153Samário (
153Sm). O
153Samário possui
meia vida física de 46,3h e decai por emissão de fótons gama e de partícula beta
(Emax
0,81
Mev).
Este
isótopo
forma
um
complexo
estável
com
etilinodiaminotetrametiletilenodifosfonato
(EDTMP)(5).
EDTMP-
153Sm
fixa-se
à
7:1 entre a metástase óssea e o osso normal(6). Após a administração de
EDTMP-153
Sm, 65 a 80% dos pacientes apresentam alívio da dor óssea(7). A resposta é
tipicamente rápida, ocorrendo dentro de uma semana, com duração média de 8
semanas (variação de 4 a 35 semanas)(8).
Estudos randomizados, duplos cegos e controlados demonstraram alta eficácia
clínica e estabeleceram a atividade ótima administrada de 37 MBq/Kg (8-10). A
toxicidade para esta atividade é limitada, com discreta mielossupressão com um nadir
de quatro semanas. O tratamento pode ser repetido com segurança(8). Portanto, com
eficácia já estabelecida e com disponibilidade regular em nosso meio, o EDTMP-
153Sm
torna-se uma ferramenta importante no manejo dos pacientes com dor óssea
metastática.
Novas opções terapêuticas têm surgido no tratamento do carcinoma de próstata
avançado. Entre os novos quimioterápicos disponíveis, destaca-se o docetaxel, um
taxano que inativa a proteína Bcl-2, presente em células metastáticas, causando
inativação e morte das células tumorais(9).
Alguns protocolos têm empregado docetaxel nos pacientes com carcinoma
prostático avançado que se tornam refratários ao bloqueio hormonal, com resultados
superiores àqueles obtidos com os esquemas quimioterápicos tradicionais
(mitoxantrona associada a prednisona ou hidrocortisona)(12-14).
O crescente emprego de docetaxel, neste grupo de pacientes, que normalmente
apresenta dor óssea significativa e é elegível para terapia com EDTMP-
153Sm, conduz
a situações clínicas em que ocorre o emprego simultâneo das duas terapêuticas.
Faz-se necessário avaliar Faz-se a biodisponibilidade do EDTMP-
153Sm, especialmente nos
ser necessária uma correção da atividade radioativa administrada aos pacientes,
visando à otimização terapêutica.
Uma eventual alteração da concentração óssea de EDTMP-
153Sm, em pacientes
em tratamento com docetaxel, poderia levar a uma redução da eficácia terapêutica do
radiofármaco. Adicionalmente, é necessário esclarecer se ocorre alguma modificação
na sua biodistribuição, pois uma eventual redistribuição do EDTMP-
153Sm poderia gerar
um aumento indesejável da sua concentração em outros tecidos além do tecido ósseo,
com aumento indesejável dos níveis dosimétricos. Considerando que o efeito
terapêutico deste radiofármaco baseia-se em sua ação no tecido ósseo, sua fixação
extra-óssea é contraproducente e pode estar associada a um aumento de reações
adversas e da toxicidade do tratamento. A busca de respostas para essas questões
constitui a base de partida deste experimento.
A pesquisa foi realizada no Núcleo de Cirurgia Experimental do Centro de
Ciências da Saúde da Universidade Federal do Rio Grande do Norte. Os experimentos
foram possíveis através de convênio firmado entre a Universidade Federal do Rio
Grande do Norte e a Liga Norteriograndense Contra o Câncer, Serviço de Medicina
Nuclear.
Deve-se ressaltar o seu caráter interdisciplinar, uma vez que contou com a
participação ativa e com a troca constante de conhecimentos entre profissionais das
2 REVISÃO DE LITERATURA
2.1.
Mecanismo de formação das metástases ósseas
Aproximadamente 70% dos pacientes com câncer avançado apresentam dor
decorrente de metástases ósseas especialmente nos tumores de mama, próstata e
pulmão (1;3;3;10;11). As células tumorais podem atingir o tecido ósseo por extensão
direta ou, mais freqüentemente, por via hematogênica, atingindo, em primeira instância,
a medula óssea(3).
Entre os pacientes com doença óssea metastática, 70% apresentam
envolvimento da coluna vertebral e arcos costais, 40% da pelve, 25% dos fêmures e
15% da calota craniana. Fraturas patológicas ocorrem em 10% das lesões
metastáticas, especialmente no câncer de mama(3). Outras complicações da doença
óssea metastática são: hipercalcemia e déficit neurológico ocasionado por compressão
de raízes nervosas(12).
A metástase de células tumorais para o tecido ósseo altera a sua arquitetura e a
homeostase mineral, possibilitando um meio propício para a multiplicação das células
tumorais(13). As lesões ósseas são classificadas através da radiografia, como
osteolíticas ou osteoblásticas. Nas lesões osteolíticas, a destruição ocorre pela ação
dos osteoclastos, como visto em pacientes portadoras de câncer de mama. As lesões
osteoblásticas predominam no câncer de próstata e caracterizam-se pelo aspecto de
esclerose na análise radiográfica(14). Uma complexa interação entre as células
óssea, ou lesões osteoblásticas, onde ocorre formação óssea(12;13). Contudo, um
padrão misto é comum em muitas lesões, com reabsorção e formação óssea ocorrendo
simultaneamente(14).
A matriz óssea é um rico depósito de fatores de crescimento, que são liberados
durante a reabsorção óssea. Análise histológica das metástases ósseas osteolíticas
indica que a destruição óssea é mediada pelos osteoclastos e não diretamente pelas
células tumorais(12;15;16). Essas observações sugerem um ciclo vicioso, levando à
formação de metástases osteolíticas: células tumorais secretam fatores de estímulo
aos osteoclastos dentro da medula óssea, causando reabsorção de osso e liberação de
fatores de crescimento a partir da matriz óssea. Esses fatores de crescimento são
essenciais para a colonização e subseqüente invasão do microambiente ósseo pelas
células tumorais(12;13;15;17).
No câncer de próstata, o comportamento osteolítico é, em parte, determinado
pela ativação dos osteoclastos, com elevação de marcadores séricos associados à sua
formação, entre eles o fator de diferenciação de osteoclastos (18). No câncer de
pulmão, estudo in vitro da colonização tumoral do tecido ósseo identificou moléculas
sinalizadoras e proteínas capazes de modular o fator de crescimento beta a estimular a
formação de novos osteoclastos (19). No câncer de mama, o fator de diferenciação de
osteoclastos foi identificado como um pré-requisito para a formação e manutenção de
2.2.
Tratamento da dor causada por metástases ósseas
O mecanismo exato da dor óssea metastática não é conhecido(14). A distensão
e o aumento da pressão mecânica sobre as terminações nervosas locais estão entre os
principais desencadeadores da dor(3).
As metástases ósseas costumam levar a um quadro de dor progressiva,
exigindo o emprego de diversas modalidades terapêuticas, incluindo medicamentos
(ex:
antiinflamatórios,
opióides,
bloqueadores
hormonais,
bifosfonatos
e
quimioterápicos), intervenções cirúrgicas e uso de radiações ionizantes, através de
radioterapia externa ou do tratamento com radiofármacos(3;21;22). O seu manejo
apresenta, portanto, um caráter interdisciplinar, visando ao controle da dor e à melhora
na qualidade de vida do paciente.
2.2.1. Medicações antiinflamatórias e opióides
Analgesia com medicamentos antiinflamatórios não esteróides é a primeira
opção na maioria dos pacientes, com progressão para opióides mais potentes à
medida que ocorre piora no quadro doloroso(14).
Aproximadamente dois terços dos pacientes com doença óssea metastática
necessitam de medicação analgésica, em geral um opióide, e podem ser afetados
2.2.2. Bifosfonatos e bloqueadores hormonais
Os bifosfonatos são análogos do pirofosfato, um componente normal da matriz
óssea. Estes agentes ligam-se aos cristais de hidroxiapatita, tornando-os menos
suscetíveis à reabsorção pelos osteoclastos. Adicionalmente, os bifosfonatos inibem o
recrutamento de precursores dos osteoclastos, previnem a sua migração para o tecido
ósseo e inibem a produção de prostaglandina-E2, interleucina 1 e enzimas
proteolíticas(25).
Estudos clínicos controlados e randomizados comprovaram sua eficácia no
tratamento de pacientes com metástases ósseas decorrentes do câncer de próstata,
reduzindo as complicações esqueléticas relacionadas a esta patologia(25-27).
Os bloqueadores hormonais são utilizados no câncer de próstata e no câncer de
mama, tumores cujo crescimento é estimulado pela presença dos hormônios sexuais,
respectivamente testosterona e estrógeno. O bloqueio desses hormônios é realizado
com o emprego de análogos do hormônio liberador do hormônio luteinizante(25;28-32).
Entretanto, durante a evolução natural da doença, as células tumorais
freqüentemente desenvolvem mecanismos que permitem a sua sobrevivência e
proliferação em um ambiente com mínima quantidade de estrógeno e, portanto,
tornam-se refratárias ao bloqueio hormonal(28;33-36).
2.2.3. Tratamento cirúrgico
Pouco utilizado, restringe-se à correção de fraturas patológicas e a casos onde
2.2.4. Radioterapia externa
A radioterapia local apresenta resposta em cerca de 80% dos casos, com
resposta completa em 30 a 60% das situações. Seu efeito analgésico tem duração
média de quatro meses, restringindo-se, entretanto, ao sítio irradiado.(21;22;38)
.
A
radioterapia de hemicorpo isolado ou seqüencial, com doses de 6 a 8 Gy, pode ser
empregada em pacientes com metástases disseminadas, apresentando resposta
completa em aproximadamente 20% e parcial em 50-60% dos casos.
A irradiação de grandes áreas é limitada pela toxicidade hematopoética, pulmonar e
gastrointestinal, decorrentes da alta dose de radiação absorvida, com mielossupressão
em 10 a 30% dos pacientes(21;38;39).
2.2.5. Radiofámacos utilizados no alívio da dor óssea
Em pacientes com múltiplas metástases ósseas, onde o emprego da
radioterapia externa torna-se proibitivo, em virtude dos seus efeitos colaterais,
radiofármacos de uso sistêmico podem ser utilizados no alívio da dor óssea com bons
resultados(1;3;10;11;14;22;25;25;40;41). Esses agentes terapêuticos são emissores de
partículas beta negativas e possuem afinidade química por sítios de neoformação
devido ao aumento do fluxo sanguíneo nessas áreas e a maior presença de superfície
de contato com os cristais de hidroxiapatita recém formados(3).
Os principais radiofármacos utilizados são compostos fosfonados marcados com
153
Samário,
188Rênio,
186Rênio,
89Estrôncio e
32Fósforo. Os dois mais empregados
mundialmente são
89Estrôncio e
153Samário(42;43).
Embora apresentem eficácia analgésica similar(44), esses radiofármacos
apresentam diferenças significativas na meia-vida física e na emissão de partículas, o
que resulta em diferentes efeitos colaterais, principalmente na supressão medular(25).
O
89Estrôncio possui longa meia-vida física no osso (quase 60 dias), e pode levar
à queda substancial no número de leucócitos e especialmente de plaquetas. Isto torna
difícil a sua indicação em um grupo de pacientes que, muitas vezes, possui indicação
de realizar quimioterapia simultaneamente(25).
O EDTMP-
153Sm, em contraste, pode ser administrado com baixa toxicidade
medular(45;46). A dose 37 MBq/Kg demonstrou ser mais efetiva que placebo no
controle da dor(47). No Brasil, a disponibilidade e o custo do EDTMP-
153Sm o tornaram
o agente de escolha nesta modalidade de tratamento(22;48-51).
2.2.5.1. EDTMP-
153Sm
O
153Samário é ligado à molécula de etilenodiamina-tetrametileno fosfonato,
adsorção aos cristais de hidroxiapatita(22). O complexo EDTMP-
153Sm demonstra
captação altamente seletiva pelo tecido ósseo, de forma similar aos radiofármacos
utilizados na cintilografia óssea(10). Seu efeito terapêutico deve-se à radiação beta
negativa de curto alcance emitida pelo radionuclídeo. Sua produção nacional é
realizada pelo Instituto de Pesquisas Energéticas e Nucleares (IPEN), autarquia
estadual associada à Universidade de São Paulo (USP) e gerenciada pela Comissão
Nacional de Energia Nuclear (CNEN).
153
Samário é um metal terra rara, produzido em reator. Possui um esquema de
decaimento complexo, incluindo raios-x e raios gama, além do decaimento principal por
partículas beta. Sua meia-vida física é de 46,3h. A energia das emissões beta é
relativamente baixa, resultando em penetração média de 0,83 mm na água e máxima
de 1,7 mm no osso e 3,1 mm em tecido mole. A emissão gama média de 103,2 keV é
satisfatória para aquisição de imagens em gama-câmara(10).
Do ponto de vista prático, essas características físicas significam que o
153
Samário tem seu efeito terapêutico limitado ao tecido alvo, evitando a irradiação
desnecessária das áreas circunjacentes. Além disso, o fato de ser também um emissor
gama possibilita a realização de uma cintilografia óssea após a sua aplicação, servindo
de controle e eventual comparação com tratamentos posteriores. O
153Samário é
facilmente complexado ao EDTMP. A preparação é quimicamente estável e não
apresenta decomposição apreciável por mais de 48h(11). A dose sugerida para
tratamento da dor óssea é de 37 MBq/Kg, administrada lentamente em um acesso
2.2.5.2 EDTMP-
153Sm : biodistribuição e dosimetria
EDTMP-
153Sm liga-se ao tecido ósseo normal e ao patológico, a uma razão
lesão-osso normal de 4,04±2,62 e lesão-tecido mole de 6,87±3,18(5). Esses valores
são bastante similares aos encontrados nos radiofármacos utilizados para realização
da cintilografia óssea, como o metileno-disfofonato marcado com
99mTecnécio
(MDP-Tc
99m)(52). EDTMP-
153Sm compartilha com MDP-Tc
99ma mesma qualidade de
imagem e sensibilidade na identificação de lesões ósseas(52).
Em estudo realizado em ratos normais, sem doença óssea, EDTMP-
153Sm
demonstrou elevada captação óssea (>55% da dose injetada), com baixa concentração
no sangue 2h após a injeção(11).
A porcentagem total que se liga ao osso é
geralmente 50% ou mais da atividade injetada, dependendo da extensão da doença
óssea metastática. O restante da dose é rapidamente excretada por filtração
glomerular. A excreção urinária é virtualmente completada após 6 horas(52), o que é
de interesse prático, pois possibilita o tratamento ambulatorial, com liberação do
paciente para casa após este período.
Após a administração, EDTMP-
153Sm é rapidamente clareado do espaço
intravascular, fixando-se ao tecido ósseo. A excreção urinária e a captação óssea
identificam a bexiga e a medula óssea como os órgãos críticos em relação à radiação.
doença metastática e depende da freqüência miccional do paciente, que deve ser
orientado a ingerir líquidos em abundância e urinar regularmente. A taxa de exposição
da medula óssea à radiação é um ponto crítico, uma vez que a toxicidade da medula
óssea é o fator dose-limitante na prática clínica(10). Para o propósito clínico, é
necessário manter a dose administrada em torno de 37MBq/Kg, com avaliação prévia
da contagem de plaquetas e leucócitos. Admitindo-se uma queda de até 50% nessas
contagens, é contra-indicada a administração de EDTMP-
153Sm em pacientes com
contagens de plaquetas inferiores a 100 x 10
9/litro e número de leucócitos inferiores a
3.5 x 10
9/litro. Quimioterapia e radioterapia externa realizadas recentemente também
devem ser consideradas. Tomadas essas precauções, a supressão medular costuma
ser transitória e de grau leve a moderado e constitui o único efeito adverso da
administração de EDTMP-
153Sm. A queda no número de plaquetas e leucócitos
apresenta nadir (ponto mais baixo, onde ocorre a maior depressão) entre a 3ª e 4ª
semanas após a administração, com recuperação aos níveis anteriores em 8
semanas(25;47;53). A repetição do tratamento pode ser feita após esse período, com
resultados semelhantes(54). Estes dados atestam a segurança do emprego de
EDTMP-
153Sm no tratamento da dor óssea metastática e sugerem que o seu uso pode
2.2.5.3 EDTMP-
153Sm : eficácia clínica
Após administração de EDTMP-
153Sm, 65 a 80% dos pacientes apresentam
alívio da dor óssea(7;8;47;55-63). A resposta é tipicamente rápida, ocorrendo dentro de
5 a 10 dias(14). A duração média da resposta é de 8 semanas (variação de 4 a 35
semanas)(41). Apesar da resposta clínica eficaz no alívio da dor, não há melhora da
sobrevida destes pacientes(14;47).
Homens com câncer de pulmão, lesões nas vértebras ou na pelve e metástases
adicionais nos ossos dos membros inferiores apresentam pior resposta ao
EDTMP-153
Sm(14;64).
Em estudo que comparou a eficácia de duas doses de EDTMP-
153Sm no alívio
da dor óssea metastática, empregando-se uma dose menor (18,5 MBq/Kg) e uma dose
maior (37MBq/kg), verificou-se um redução global no nível de dor em todos os
pacientes, mas aqueles que receberam a dose maior apresentavam melhora mais
significativa na 4ª semana após a avaliação (p=0,04).
A proporção de pacientes que
conseguia dormir à noite aumentou de 33% para 45% naqueles que receberam a dose
mais baixa e para 59% para os que receberam a dose mais alta(14;65). Achados
semelhantes foram encontrados em outro estudo duplo cego controlado, com melhor
eficácia ao se utilizar a dose maior (37MBq/kg): melhora da dor em 67% dos pacientes,
em relação àqueles que utilizaram dose menor (18,5 MBq/Kg), com alívio da dor em
42% dos casos. Neste trabalho, verificou-se aumento progressivo no consumo de
enquanto nos grupos tratados com EDTMP-
153Sm houve redução no uso de
analgésicos(8;14).
Em outro estudo clínico, randomizado e controlado, a eficácia de EDTMP-
153Sm
foi avaliada em 152 homens com câncer de próstata e diversas lesões ósseas
dolorosas(14;47). Os pacientes foram selecionados para receber EDTMP-
153Sm na
dose de 37MBq/kg ou o mesmo produto, na sua forma não radioativa. Os diários dos
pacientes foram utilizados para registrar o uso de analgésicos e o nível de dor, que foi
avaliado através de uma escala visual e de uma escala de palavras. Entre 3 e 4
semanas, o consumo de analgésico decresceu significativamente no grupo tratado em
relação ao grupo placebo (p<0,05). Além disso, tanto a escala visual de dor quanto a
escala de palavras demonstrou significativa melhora no grupo tratado entre 2 e 4
semanas (p=0,0004).Os grupos não apresentaram diferença em relação à
sobrevida(14;47).
2.2.6. Quimioterapia
A quimioterapia apresenta um papel preponderante no tratamento de pacientes
com dor óssea provocada por metástases ósseas. É sabido que, durante a sua
evolução clínica, os tumores de próstata e mama tornam-se refratários ao bloqueio
hormonal. O tratamento, a partir deste momento, inclui o emprego de diversos
quimioterápicos. Além do alívio da dor e melhora da qualidade de vida dos pacientes,
alguns esquemas terapêuticos têm demonstrado melhora na sobrevida no câncer de
radiofármacos com quimioterápicos pode levar a um aumento da eficácia no alívio da
dor em relação ao emprego dos dois agentes separadamente(71-74).
Entre os quimioterápicos que vêm sendo empregados nesta situação,
destaca-se a clasdestaca-se dos taxanos, incluindo viblastina, paclitaxel e docetaxel(25;32;75-81). Entre
estes, o docetaxel demonstrou ser o mais ativo, isoladamente ou associado à
etamustrina(33;82-84). O docetaxel é um taxano semissintético com vários
mecanismos de ação anti-neoplásica. O mais aceito desses mecanismos é a
estabilização de microtúbulos, Na divisão celular normal, os microtúbulos agem como o
citoesqueleto da célula em mitose. O docetaxel liga-se aos microtúbulos, impedindo o
seu processo de polimerização e, desta forma, interrompendo o processo de divisão
celular, levando à apoptose da célula tumoral(25). Um segundo mecanismo proposto
para a ação citotóxica do docetaxel é seu efeito sobre a proteína BCL-2. Foi
demonstrado que a expressão deste oncogene protege a célula tumoral, evitando sua
apoptose. Docetaxel atua na fosforilação da BCL-2, levando à perda de sua função
anti-apoptótica(25;85-87).
Estudos com utilização de docetaxel em pacientes com câncer de próstata
refratário ao tratamento hormonal demonstraram vantagem em relação aos esquemas
quimioterápicos anteriores, com aumento na sobrevida e melhor resposta na
diminuição da dor, redução dos níveis de PSA (prostate-specific antigen – antígeno
específico da próstata) e melhora na qualidade de vida(40;69;70). Após estes achados,
o docetaxel passou a ser considerado o quimioterápico de primeira linha nesta situação
O crescente emprego de docetaxel neste grupo de pacientes já vem sendo
observado na prática médica. Isto conduz a situações em que ocorre o seu emprego
simultâneo com EDTMP-
153Sm. A influência do docetaxel na biodisponibilidade do
EDTMP-
153Sm, especialmente nos ossos, precisa ser avaliada, uma vez que, nesta
situação, pode ser necessária uma correção da atividade radioativa administrada aos
3 ANEXAÇÃO DE ARTIGOS PUBLICADOS
Artigo I: Biodistribution of samarium-153-EDTMP in rats treated with docetaxel.
Publicado no periódico Acta Cirúrgica Brasileira, 2009 Jan-Feb;24(1):62-6, Qualis
Internacional C
Artigo II: Biodistribution of the Radiopharmaceutical Sodium Pertechnetate after
Biliopancreatic Bypass with a Duodenal Switch.
Publicado no periódico Brazilian Archives of Biology and Technology, 2007;
50:189-197,Qualis Internacional B
Artigo III: Biodistribution of the radiophamarceutical sodium pertechnetate
(Na99mTcO4) after massive small bowel resection in rats
Publicado no periódico Acta Cirúrgica Brasileira, 2007 Nov-Dez;22(6):430-435, Qualis
Internacional C
Artigo IV: Influence of Splenectomy on the Biodistribition of Technetium-99m
Dimercaptosuccinic Acid (99mTc-DMSA)
Publicado no periódico Brazilian Archives of Biology and Technology, 2008;
51:197-202,Qualis Internacional B
Artigo V: Biodistribution of the Radiopharmaceutical Technetium-99m-Sodium
Phytate in Rats After Splenectomy
Publicado no periódico Brazilian Archives of Biology and Technology, 2008;
3.1. Biodistribution of samarium-153-EDTMP in rats treated with docetaxel.
Publicado no periódico Acta Cirúrgica Brasileira, 2009 Jan-Feb;24(1):62-6,
ORIGINAL ARTICLE
Effects of Drugs
Biodistribution of samarium-153-EDTMP in rats treated with docetaxel
Biodistribuição de EDTMP-153-samário em ratos tratados com docetaxel
Arthur Villarim Neto
I, Maria Kadja Meneses Torres Açucena
I, Kércia Regina Santos
Gomes Pereira
I, Amália Cínthia Meneses Rêgo
I, Ítalo Medeiros Azevedo
II, Mário
Bernardo-Filho
III, Aldo Cunha Medeiros
IVI
Fellow PhD degree, Postgraduate Program in Health Sciences, UFRN, Brazil.
IIStatistician, Department of Surgery, UFRN, Brazil.
IIIPhD, Full Professor, Department of Biophysics and Biometry, State University of Rio de
Janeiro, Brazil.
IV
PhD, Full Professor, Department of Surgery, UFRN, Brazil.
ABSTRACT
Purpose: Many patients with metastatic bone disease have to use radiopharmaceuticals
associated with chemotherapy to relieve bone pain. The aim of this study was to assess the
influence of docetaxel on the biodistribution of samarium-153-EDTMP in bones and other
organs of rats. Methods: Wistar male rats were randomly allocated into 2 groups of 6 rats each.
The DS (docetaxel/samarium) group received docetaxel (15 mg/kg) intraperitoneally in two
cycles 11 days apart. The S (samarium/control) group rats were not treated with docetaxel. Nine
days after chemotherapy, all the rats were injected with 0.1ml of samarium-153-EDTMP via
orbital plexus (25 Ci). After 2 hours, the animals were killed and samples of the brain, thyroid,
lung, heart, stomach, colon, liver, kidney and both femurs were removed. The percentage
radioactivity of each sample (% ATI/g) was determined in an automatic gamma-counter
(Wizard-1470, Perkin-Elmer, Finland). Results: On the 9
thday after the administration of the 2
ndchemotherapy cycle, the rats had a significant weight loss (314.50±22.09g) compared (p<0.5) to
pre-treatment weight (353.66± 22.8). The % ATI/g in the samples of rats treated with
samarium-153-EDTMP had a significant reduction in the right femur, left femur, kidney, liver and lungs of
animals treated with docetaxel, compared to the control rats. Conclusion:
The combination of
docetaxel and samarium-153-EDTMP was associated with a lower response rate in the
biodistribution of the radiopharmaceutical to targeted tissues. Further investigation into the
impact of docetaxel on biodistribution of samarium-153-EDTMP would complement the
findings of this study.
Key words: Taxoids. Samarium. Biological Availability. Drug Therapy. Rats.
RESUMO
orbital (25 Ci). Após 2 horas, os animais foram mortos e feitas biópsias de cérebro, tireóide,
pulmão, coração, estômago, cólon, fígado, rim e fêmures. O percentual de radioatividade por
grama (%ATI/g) de tecido de cada biópsia foi determinado em contador gama automático
(Wizard-1470, Perkin-Elmer, Finland). Resultados: No 9º após 2º ciclo de docetaxel os ratos
tiveram perda de peso significante, passando de 353.66± 22.8g (controle/pré-tratamento) para
314,50±22,09g (p<0.5). Os % ATI/g nos órgãos dos ratos tratados com EDTMP-153–samário e
docataxel tiveram redução significante nos fêmures direito e esquerdo, rim, fígado e pulmão,
quando comparados com os não tratados com docetaxel. Conclusão: A combinação de docetaxel
com EDTMP-153-samário foi associada com resposta mais baixa na biodistribuição do
radiofármaco em órgãos alvo. Futuras investigações sobre o impacto do docetaxel na
biodistribuição do EDTMP-153-samário poderão complementar os achados teste estudo.
Key words: Taxóides. Samário. Disponibilidade Biológica. Quimioterapia. Ratos.
__________________________________________________________________
1Research performed at the Postgraduate Program in Health Sciences, Federal University of Rio
Grande do Norte (UFRN), Brazil.
Introduction
Bone metastases are a frequent complication of cancer, occurring in up 70% of patients
suffering from advanced breast or prostate cancer
1.
Bone metastases patients often present with
severe bone pain, especially in the advanced stage of disease
1,2.
The major pain mechanism of
small metastases appears to be the stimulation of nerve endings in the endosteum by a variety of
chemical mediators. Larger bone metastases produce stretching of the periosteum, which leads to
pain
2.
The resulting bone pain interferes with the patient’s quality of life and requires effective
treatment. Unfortunately, various non-radiotherapeutic modalities such as analgesics, hormone
therapy, orchidectomy, cytostatic and cytotoxic drugs, bisphosphonates, and surgery are not
effective in all cases, especially in the late stage of the disease
1,2.
Systemic radionuclide therapy
using boneseeking radiopharmaceuticals is considered a valuable and effective method for
treating patients with widespread skeletal metastases and increased bone turnover, especially in
patients with bone metastases from prostate and breast cancer
3,4,5.
In the 1980s the radiopharmaceutical samarium-153 ethylenediamine tetramethylene
phosphonate (Sm-153-EDTMP) with short physical half-life was developed, and has been
considered effective in the treatment of bone pain
4,5.
Docetaxel is one of the taxane class
chemotherapies that is being increasingly used to treat various solid tumors, including those of
prostate and breast cancer. It acts by Bcl-2 protein inactivation in the metastatic cells, causing the
death of tumor cells by apoptosis
6. In patients with prostate cancer, docetaxel has been suggested
in various studies as the first-line choice for treating metastatic hormone-refractory disease. This
treatment increases survival, compared to previously accepted chemotherapy schemes
6.
Methods
We used male rats provided by the Health Science Center vivarium, Federal University of
Rio Grande do Norte, Brazil. The animals were randomly allocated into 2 groups of 6 rats each.
They were weighed and placed in individual cages with water and food (Labina Purina ®) "ad
libitum" and acclimatized in the lab for 7 days. The rats were kept under temperature (21ºC),
humidity (60 - 70%) and lighting (12 / 12 hour cycle light / dark) control and they were handled
in accordance with International Standards of Care and Use of Laboratory Animals, following
the guidelines of the Brazilian College of Animal Experimentation.
The animals of the DS group (docetaxel/samarium) were administered docetaxel
(Trixotene ®, Novartis, São Paulo, Brazil), intraperitoneally, using a 15 mg/kg dose in two
administration cycles 11 days apart. The S group (samarium/control) rats were not treated with
docetaxel. The animals remained under observation for 9 days after the 2
ndcycle and were then
injected with 0.1 mL of Sm-153-EDTMP via the orbital plexus, corresponding to radioactivity of
925 Bq (25 Ci). Two hours after radiopharmaceutical administration, the animals were killed
with an anesthesia overdose (thiopental sodium, via the intracardiac cannula) and underwent
surgery for removal of samples from the brain, thyroid, lung, heart, stomach, colon, liver, kidney
and both femurs
.
The tissue samples were washed in 0.9% saline, weighed on a precision scale
(Mark 160®, Bel equipment, Italy) and their radioactivity was determined in an automatic
gamma counter (Wizard 1470, Perkin-Elmer, Finland). The results are shown in counts per
minute (CPM), corrected by disintegrations per minute (DPM). The efficiency of the gamma
counter was 86%, as specified by the manufacturer. The specific activity of each sample was
calculated by dividing its absolute count DPM by its weight (DPM/g). The percentage of
radioactivity of each sample (% ATI/g) was calculated by dividing its specific activity (DPM/g)
by the total radioactivity injected in each animal. The total activity administered to each animal
was calculated from the average of three patterns with the same volume injected.
The data were expressed as mean ± standard deviation. Statistical analysis for comparison
between groups was performed by the Student and Tukey tests, using a significance level of
0.05.
Results
No animal died during the experiment. On the eleventh day after the 1
stchemotherapy
cycle with docetaxel, the animals showed weight loss (mean 329.16±29.2 g), but not
significantly different from pre-treatment weight (mean 353.66± 22.8). Meanwhile, on the 9
thday after administration of the 2
ndchemotherapy cycle, there was significant weight loss
(314.50±22.09g) compared to pre-treatment weight (Figure 1). We observed no changes in
animal behavior or side effects, such as diarrhea and hair loss. During the laparotomy to remove
organ samples, few peritoneal adhesions were observed in DS group rats. No macroscopic
changes were detected in the abdominal organs.
significant reduction in radioactivity biodistribution in brain, thyroid, heart, stomach and colon
samples (Table 1).
Pre 1st 2nd
Cycle 280
300 320 340 360 380 400
W
e
ig
h
t
(g
)
* *
FIGURE 1 – The evolution of rats weight comparing pretreatment and after the first (1
st) and
second (2
nd) post-docetaxel treatment
TABLE 1 - Comparison of percentage of radioactivity/g (% ATI/g) of samples from each organ
of rats treated with Sm-153-EDTMP (group S) and with docetaxel + Sm-153-EDTMP (group
DS)
% ATI/g
Organs
Group S
Group DS
p
Brain
0.01 ± 0.002
0.01 ± 0.005
0.753022
Thyroid
0.40 ± 0.079
0.30 ± 0.066
0.07301
Lung
0.17 ± 0.033
0.13 ± 0.025
0.043126
Heart
0.12 ± 0.019
0.11 ± 0.019
0.300239
Stomach
0.18 ± 0.042
0.14 ± 0.032
0.091458
Colon
0.13 ± 0.041
0.11 ± 0.038
0.484202
Liver
1.48 ± 0.187
0.96 ± 0.267
0.007438
Kidney
1.21 ± 0.160
0.86 ± 0.144
0.007411
Femur (right)
0.73 ± 0.105
0.46 ± 0.093
0.002484
Femur (left)
0.72 ± 0.004
0.50 ± 0.086
0.003599
Mean ± SD, Student t test. S, samarium; DS, docetaxel+samarium.
Discussion
The advantages of radiopharmaceutical use include the ease of administration, the ability to treat
multiple sites of metastatic disease, the improved potential therapeutic ratio due to bone location
and the potential of combining with chemotherapy agents and external beam radiation for an
enhanced therapeutic effect
4,5. A subset of trials has suggested improved pain palliation by
combining a radiopharmaceutical agent with chemotherapy
4,5,12.
Taxanes (docetaxel and paclitaxel) are currently one of the most extensively studied new
chemotherapeutic agents for metastatic breast cancer. Single-agent docetaxel has demonstrated
significant survival advantages over other recognized regimens in two trials involving patients
with anthracycline-pretreated metastatic breast cancer
10.
Some data suggest that docetaxel is one
of the most active agents available for treating these patients
11.
The primary objective of this study was to evaluate if combined chemotherapy interferes
with the biodistribution of Sm-153-EDTMP to bone and other organs. It was based on the
possibility of using Sm-153-EDTMP combined with docetaxel for the treatment of bone
metastasis pain in patients with prostate or breast cancer. Recently, Ricci et al.
12reported that
Sm-153-EDTMP is effective in bone pain relief, with minimal toxicity. When administered in
combination with chemotherapy (estramustine phosphate or mitoxantrone plus prednisone), it
prolonged survival.
Many factors, such as drug therapy, radiation therapy, surgery, in addition to the
pathological process, could affect the biodistribution of different radiopharmaceuticals
13-15.
In
this work, when Sm-153-EDTMP was administered to rats previously treated with docetaxel, the
biodistribution of the radiopharmaceutical to bone, kidney, liver and lung was significantly lower
than that of controls. Based on these data, we can infer that an additional dose of
Sm-153-EDTMP may be necessary to get the desired pain relief effect when docetaxel is used in
combination with this radiopharmaceutical. It was reported that the average duration of bone
pain palliation in patients treated with Sm-153-EDTMP alone was about 3–4 months, while it
was about 9–10 months in patients who started receiving
estramustine phosphate or
mitoxantrone plus prednisone after treatment with the bone-seeking radionuclide
12.
However,
information about the clinical effect of docetaxel associated to
Sm-153-EDTMP is scarce. The
results obtained in the present work provide a rationale for further studies aimed at assessing
combined chemotherapy and bone-targeted radiotherapy (docetaxel plus Sm-153-EDTMP) as a
therapeutic strategy in patients with advanced hormone resistant prostate cancer.
In conclusion, the combination of docetaxel and Sm-153-EDTMP was associated with a
lower response rate in the biodistribution of the radiopharmaceutical to targeted tissues. Further
investigation into the impact of docetaxel on the biodistribution of Sm-153-EDTMP would
complement the findings of this study.
References
1.
Liepe K, Runge R, Kotzerke J. The benefit of bone-seeking radiopharmaceuticals in the
treatment of metastatic bone pain. J Cancer Res Clin Oncol. 2005;131:60-6.
2.
Nielsen OS, Munro AJ, Tannock IF. Bone metastases: pathophysiology and management
policy. J Clin Oncol. 1991;9:509–24.
3.
Sapienza MT, Ono CR, Guimaraes MI, Watanabe T, Costa PA, Buchpiguel CA.
4.
Ubieto MA, Abos MD, Tardin AL, Razola P, Prats E, Garcia F, Polo E, Yubero A, Banzo
J. Treatment of bone metastatic pain with Sm-153-EDTMP. Evaluation of the analgesic
response and the existence of differences according to the primary tumor and the metastatic
pattern. Rev Esp Med Nucl. 2005;24:297-304.
5.
Serafini AN. Systemic metabolic radiotherapy with samarium-153 EDTMP for the
treatment of painful bone metastasis. Q J Nucl Med. 2001;45:91-9.
6.
Petrilak DP, Pangen CM, Hussain MH, Lara PN Jr, Jones JA, Taplin MA, Burch PA, Berry
D, Moinpour C, Kohli M, Benson MC, Small EJ, Raghavan D, Crawford ED. Docetaxel
and estramustine compared with mitoxantrone and prednisone for advanced refractory
prostate cancer. N Engl J Med. 2004;351:1513-20.
7.
Serafini AN. Current status of systemic intravenous radiopharmaceuticals for the treatment
of painful metastatic bone disease. Int J Radiat Oncol Biol Phys. 1994;30:1187-94.
8.
Laing AH, Ackery DM, Bayly RJ, Buchanan RB, Lewington VJ, McEwan AJ, Macleod
PM, Zivanovic MA. Strontium-89 chloride for pain palliation in prostatic skeletal
malignancy. Br J Radiol. 1991;64:816-22.
9.
Eary JF, Collins C, Stabin M, Vernon C, Petersdorf S, Bakre M, Hartnett S, Ferency S,
Addison SJ, Appelbaum F. Samarium-153-EDTMP biodistribution and dosimetry
estimation. J Nucl Med. 1993;34:1031-6.
10.
Nabholtz JM, Senn HJ, Bezwoda WR, Melnychuk D, Deschenes L, Douma J, Vandenberg
TA, Rapoport B, Rosso R, Trillet-Lenoir V, Drbal J, Molino A, Nortier JW, Richel DJ,
Nagykalnai T, Siedlecki P, Wilking N, Genot JY, Hupperets PS, Pannuti F, Skarlos D,
Tomiak EM, Murawsky M, Alakl M, Aapro M. 304 Study Group: Prospective randomized
trial of docetaxel versus mitomycin plus vinblastine in patients with metastatic breast
cancer progressing despite previous anthracycline-containing chemotherapy. J Clin Oncol.
1999;17:1413-24.
11.
Crown J: A review of the efficacy and safety of docetaxel as monotherapy in metastatic
breast cancer. Semin Oncol. 1999;26(1 Suppl 3):5-9.
12.
Ricci S, Boni G, Pastina I, Genovesi D, Cianci C, Chiacchio S, Orlandini C, Grosso M,
Alsharif A, Chioni A, Di Donato S, Francesca F, Selli C, Rubello D, Mariani G. Clinical
benefit of bone-targeted radiometabolic therapy with 153Sm-EDTMP combined with
chemotherapy in patients with metastatic hormone-refractory prostate cancer. Eur J Nucl
Med Mol Imaging. 2007;34:1023-30.
13
. Brito DMM, Gomes ML, Rodrigues PC, Paula EF, Gutfilen B, Bernardo-Filho M. Effect of
the chemotherapeutic drugs on the biodistribution of
99mTc-DTPA in Balb/c mice. J Exp Clin
Cancer Res. 1998;17:313-6.
15.
Chacon DA, Araújo-Filho I, Villarim-Neto A, Rêgo AC, Azevedo IM, Bernardo-Filho M,
Brandão-Neto J, Medeiros AC. Biodistribution of the radiophamarceutical sodium
pertechnetate (Na99mTcO4) after massive small bowel resection in rats. Acta Cir Bras.
2007;22:430-5.
Conflict of interest: none
Financial source: CNPq
Correspondence:Aldo Cunha Medeiros
Av. Miguel Alcides Araújo, 1889 59078-270 Natal – RN Brazil
aldo@ufrnet.br
Received: August 26, 2008 Review: October 28, 2008 Accepted: November 27, 2008
How to cite this article
3.2. Biodistribution of the Radiopharmaceutical Sodium Pertechnetate after
Biliopancreatic Bypass with a Duodenal Switch.
Publicado no periódico Brazilian Archives of Biology and Technology, 2007;
Biodistribution of Sodium Pertechnetate after
Biliopancreatic Bypass with a Duodenal Switch
.
Irami Araújo-Filho, Amália Cínthia Meneses Rêgo, José Brandão-Neto, Arthur
Villarim-Neto, Eryvaldo Sócrates Tabosa Egito, Ítalo Medeiros Azevedo and Aldo Cunha Medeiros*
Programa de Pós-Graduação em Ciências da Saúde; Universidade Federal do Rio Grande do Norte; aldo@ufrnet.br; Rua Cordeiro de Faria S/N; 59010-180; Natal - RN - Brasil
ABSTRACT
Study with the purpose to examine the effects of duodenal switch (DS), regularly performed in morbidly obese patients, on biodistribution of sodium pertechnetate in several organs of rats. There was no early or late mortality in either rats groups. The values of percent radioactivity per gram of tissue (%ATI/g), showed no significant difference in liver, stomach, small bowel, duodenum, kidney, heart, bladder, bone and brain, when compared the DS rats with sham and controls rats. A postoperative significant increase in mean %ATI/g levels was observed in spleen, pancreas and muscle in group DS rats, as compared to group S and C rats (p<0.05). In the lung there was an increase and in thyroid a decrease in mean %ATI/g of DS rats, when compared to sham rats (p>0.05). In conclusion, the biliopancreatic diversion with duodenal switch in rats modified the biodistribution of sodium pertechnetate in tireóide, lung, pancreas, spleen and muscle.
Key words: Bariatric surgery, duodenal switch, sodium pertechnetate, biodistribution
* Author for correspondence.
INTRODUCTION
Worldwide, it is estimated that more than 300 million people are obese (Haslam & James., 2005). Obesity, particularly abdominal obesity, is associated with increased risks of hypertension, diabetes, hyperlipidemia, sleep apnea, coronary heart disease, and stroke (Li et al., 2005). The accumulating evidence identifying obesity-related mortality and comorbidities is an important factor that has led to increased numbers of patients seeking treatment through bariatric surgery. This is a surgical procedure that reduces caloric intake by modifying the anatomy of the gastrointestinal tract and provides effective treatment for many patients with morbid obesity. Bariatric operations are classified as either restrictive or malabsorptive. Restrictive procedures limit intake by creating a small gastric reservoir with a narrow outlet to delay emptying. Malabsorptive procedures bypass varying portions of the small intestine where nutrient absorption occurs (DeMaria & Jamal.,
may
include
nutrient
deficiencies
or
gastrointestinal pathology. Anastomotic leak
and stricture commonly occurs (Schauer et al.,
2000; DeMaria et al., 2002). The most
frequently reported complication of gastric
band placement is prolapse of stomach
superiorly through the band producing
obstruction at the band (O’Brien et al., 1999).
Radiographs and scintigraphs may show an air
fluid level in the gastric pouch, malposition,
angulation of the band bands, problems with
gastric emptying, and gastric obstruction
(O’Brien et al., 2005).
The radiopharmaceuticals are frequently used in diagnostic procedures. Examinations of gastric emptying, patency of anastomoses, enterogastric reflux, hepatic and thyroid diseases, osteoporosis, metastasis, etc, frequently are carried after bariatric surgery (Kitabaiashi et al., 2002; Fonseca et al., 2000; Badiali et al., 2001; Obradovic et al., 2000). Several works have studied the relationship between chemotherapy, phytotherapy and other drugs with the biodistribution of sodium pertechnetate (Braga et al., 2000; Oliveira et al., 2002; Gomes et al., 1998; Ripoll-Hamer et al, 1995; Simões et al., 1997; Feliciano et al., 2002., Abreu et al., 2006., Santos et al., 1995). With regard to potential consequences of bariatric surgery in the biodistribution of radiopharmaceuticals, little or no study was published until now.
As DS is a restrictive and malabsorptive operation, of raised anatomical and metabolic repercussion, postoperative evaluation of patients through scintigraphy can be necessary. If the biodistribution of sodium pertechnetate to organs and tissues is modified as a result of bariatric surgery, scintigraphic examinations can be false-positive or false-negative, resulting in repetition of examinations with unnecessary exposition of patient to ionizing radiations. The purpose of this study was to examine the effects of DS, similar to that performed in morbidly obese patients, on biodistribution of sodium pertechnetate in several organs and tissues of rats.
MATERIAL AND METHODS
Male Wistar rats who were 12 weeks of age and weighing 328g ± 33g were obtained from Center of Experimental Surgery-UFRN, Brazil. Animals were housed in polypropilene cages for 1 week to acclimatize them to the study laboratory: 12-h light/dark cycle, room temperature of 25°C, and 50% relative humidity. Rats were allowed free access to water and standard rat chow (Labina, Purina®). The study was approved by the Institutional Animal Care Committee of the University Hospital-UFRN, Brazil and the international guidelines for the care and use of laboratory animals were followed throughout the study.
Rats were randomly divided into three groups: duodenal switch group (DS), control group (C), and sham-operated group (S). After 12 h of food deprivation, rats were anesthetized with a ketamine and xylazine mixture (200 mg: 5 mg, 0.1 ml/100 g, IM), the abdomen was shaved and prepared, and the operations were performed with aseptic technique. All the surgical procedures were performed by the same investigator, a well trained and experienced surgeon in animal surgery and
three previous series of experiments were performed in sequence to develop the DS model. A single intramuscular dose of 75 mg/kg of ceftriaxone sodium (Roche, SP,Brazil) was given as antimicrobial prophylaxis 30 minutes before the surgical procedures.
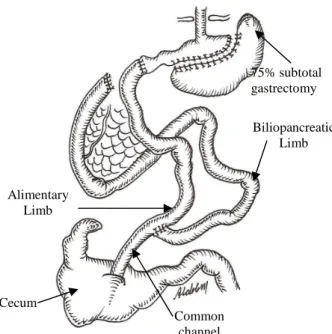
Figure 1 - The biliopancreatic diversion with duodenal switch operation.
Rats were allowed to drink and eat 24 h after surgery. Liquid diet (Nestogeno, Nestlé, SP-Brazil, 1 cal/g) was provided for the first 2 days, followed by ground Purina Labina chow. The sham rats (n=7) were submited to a laparotomy and soft malipulation of stomach, duodenum and small bowel. The control rats (n=7) were not operated.
Body weight, using a digital scale (Filizola®, São Paulo, Brasil), and operative complications were evaluated daily for 10 days.
On the 10th day all the animals were anaesthetized again, and injected with 0.lmL of Na99mTcO4 IV in the orbital plexus, corresponding to radioactive activity of 0.66MBq. After 30 minutes, the animals were killed by lethal dose of anesthetic.
Samples of the liver, spleen, stomach, small intestine, duodenum, pancreas, kidney, heart, lung, thyroid, bladder, muscle, bone (femur) and brain were harvested. The samples were washed in 0.9% saline , weighed on a high-precision digital scale (Bel-Mark 160-II Itália) and subjected to radioactivity detection using a 1470 WizardTM Gamma Counter- Perkin-Elmer, with automatic correction of radiation decline. The percentage of radioactive activity/g (%ATI/g) of each organ was calculated by dividing the activity/g of the tissue by the total activity administered to each animal. Data are expressed as mean ±SD. Statistical analysis was performed using one-way analysis of variance and the Tukey test as appropriate. P values <0.05 were considered to be statistically significant.
RESULTS
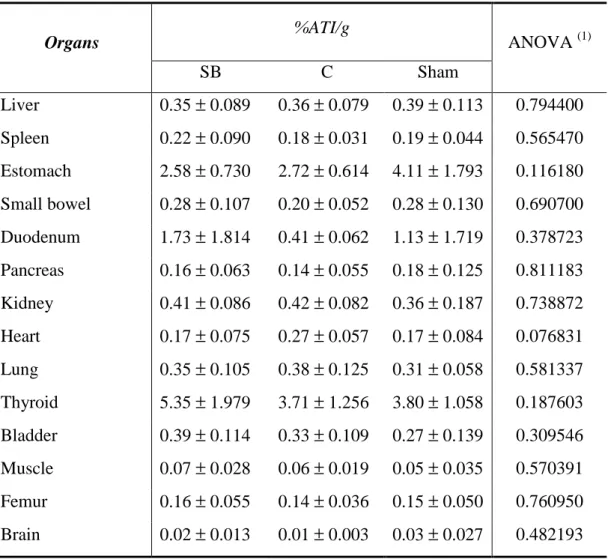
There was no early or late mortality in either rats groups. The values of all sodium pertechnetate biodistribution, expressed as percent radioactivity per gram of tissue (%ATI/g), are shown in Table 1. There was no significant difference in %ATI/g in liver, stomach, small bowel, duodenum, kidney, heart, bladder, bone and brain, when compared the DS rats with S and C rats. A postoperative significant increase in mean %ATI/g levels was observed in spleen, pancreas and muscle in group DS rats, as compared to group S and C rats (p<0.05). Looking at each group separately, in the lung there was an increase and in thyroid a decrease in mean %ATI/g of DS rats, when compared to sham rats (p>0.05).
Table 1 - Results of the percentage of radioactivity/g of organs and tissues(%ATI/g).
Organs %ATI/g
Switch C Sham P(1)
Liver 0.42 ± 0.103 0.35 ± 0.069 0.35 ± 0.097 0.256
Spleen(2) 0.26 ± 0.079ab 0.18 ± 0.028a 0.17 ± 0.045b 0.016
Stomach 3.39 ± 1.321 2.98 ± 1.507 4.23 ± 0.941 0.205
Small bowel 0.19 ± 0.052 0.19 ± 0.052 0.26 ± 0.109 0.209
Duodenum 0.65 ± 0.541 0.44 ± 0.088 0.61 ± 0.484 0.633
Pancreas(2) 0.27 ± 0.089ab 0.14 ± 0.045a 0.15 ± 0.078b 0.006
Kidney 0.53 ± 0.157 0.42 ± 0.075 0.36 ± 0.174 0.115
Heart 0.28 ± 0.131 0.27 ± 0.061 0.16 ± 0.079 0.050
Lung(2) 0.44 ± 0.075a 0.39 ± 0.143 0.28 ± 0.075a 0.030
Thyroid(2) 1.48 ± 2.070a 3.60 ± 1.578 4.44 ± 1.143a 0.010
Bladder 0.30 ± 0.115 0.33 ± 0.094 0.32 ± 0.173 0.929
Muscle(2) 0.09 ± 0.028ab 0.06 ± 0.018a 0.05 ± 0.026b 0.008
Bone 0.14 ± 0.032 0.14 ± 0.032 0.14 ± 0.050 0.958
Brain 0.03 ± 0.033 0.01 ± 0.003 0.01 ± 0.007 0.244
Mean
±
standard deviation
1.
P-value.
2.
Groups identified by the same letter differ significantly. Significance 0.05 using the
Tukey test.
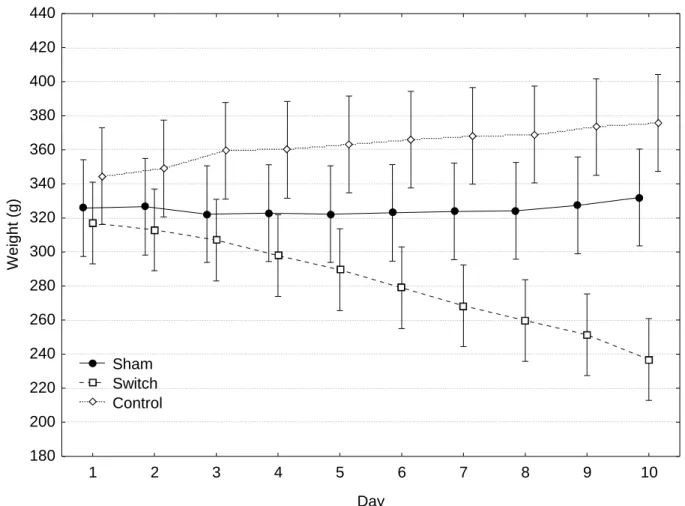
Preoperative and postoperative data of weight loss of DS rats are summarized in Figure 2. Before treatments, there were no significant differences between groups in terms of weight. The operative time for the sham operation was equivalent to that of DS. Postoperatively in group DS there was a significant decrease in body weight during the 10
Figure 2 - Effect of duodenal switch, sham and control on body weight in rats during the observation period.
1 2 3 4 5 6 7 8 9 10
Day 180
200 220 240 260 280 300 320 340 360 380 400 420 440
W
e
ig
h
t
(g
)
Sham Switch Control
Body weight decreased significantly in the duodenal switch group vs the sham and control, P<0.05. No difference was observed between sham and control rats.