Universidade Federal de Ouro Preto
Programa de Pós-Graduação em Engenharia Ambiental Mestrado em Engenharia Ambiental
OTIMIZAÇÃO E VALIDAÇÃO DE EXTRAÇÃO LÍQUIDO-LÍQUIDO
COM PARTIÇÃO EM BAIXA TEMPERATURA DE
MICROCONTAMINANTES ORGÂNICOS EM AMOSTRAS DE
ESGOTO E ANÁLISE POR CG-EM
Bárbara Diniz Lima
Universidade Federal de Ouro Preto
Programa de Pós-Graduação em Engenharia Ambiental Mestrado em Engenharia Ambiental
Bárbara Diniz Lima
OTIMIZAÇÃO E VALIDAÇÃO DE EXTRAÇÃO LÍQUIDO-LÍQUIDO
COM PARTIÇÃO EM BAIXA TEMPERATURA DE
MICROCONTAMINANTES ORGÂNICOS EM AMOSTRAS DE
ESGOTO E ANÁLISE POR CG-EM
Dissertação apresentada ao Programa de Pós-Graduação em Engenharia Ambiental, Universidade Federal de Ouro Preto, como parte dos requisitos necessários para a obtenção do título de Mestre em Engenharia Ambiental.
Área de Concentração: Meio Ambiente
Orientador: Prof. Dr. Robson José de Cássia Franco Afonso
Catalogação: sisbin@sisbin.ufop.br
L732o Lima, Bárbara Diniz.
Otimização e validação de extração líquido-líquido com partição em baixa temperatura de microcontaminantes orgânicos em amostras de esgoto e análise por CG-EM [manuscrito] / Bárbara Diniz Lima. – 2013.
104 f. : il. color.; tabs.
Orientador: Prof. Dr. Robson José de Cássia Franco Afonso.
Dissertação (Mestrado) - Universidade Federal de Ouro Preto. Instituto de Ciências Exatas e Biológicas. Núcleo de Pesquisas e Pós-Graduação em Recursos Hídricos. Programa de Pós-Graduação em Engenharia Ambiental. Área de concentração: Meio Ambiente.
1. Microcontaminantes orgânicos - Teses. 2. Esgotos - Teses. 3. Extração (Química) - Teses. 4. Derivatização - Teses. 5. Cromatografia gasosa - Teses. 6. Espectrometria de massa - Teses. I. Afonso, Robson José de Cássia Franco. II. Universidade Federal de Ouro Preto. III. Título.
AGRADECIMENTOS
Agradeço primeiramente a Deus por estar sempre me guiando e me propiciando graças. Aos meus pais, Vera e José Geraldo e meu irmãos Gustavo e Caio, por terem abraçado esse sonho comigo e me auxiliado em todos os momentos sendo sempre o meu porto seguro. Amo vocês!
Ao meu orientador, Prof. Dr. Robson José de Cássia Franco Afonso, pela oportunidade, profissionalismo e por ser um verdadeiro mestre. Foi uma honra trabalhar com você e poder usufruir dos seus ensinamentos e experiências.
Aos professores da pós-graduação pela transmissão de conhecimentos e ao Prof. Dr. Maurício Xavier Coutrim pela disposição em ajudar sempre que preciso e pela convivência.
Aos amigos do laboratório de Caracterização Molecular e Espectrometria de Massas e dos laboratórios parceiros: Amanda, Keila, Regiane, Júlia, Bruno, Diego, Marina, André, Cíntia, Francine, Luide, Ramon, Tereza, Cláudia, Daniela, Oscar, Rafaela, Débora, Jéssica e Carlúcio, pelo companheirismo, ajuda e por tornarem os dias de trabalho mais agradáveis.
À Ananda Lima Sanson por ter me ajudado em todas as etapas deste trabalho, pela
paciência, por ter sido uma “co-orientadora”. Além de ter se tornado uma amiga querida. Muito obrigada!
À Taynara, Wanda e Jéssica por estarem ao meu lado em todos os momentos de alegria e tristeza. Amigas queridas, meus maiores presentes de Ouro Preto. Amo vocês!
À amada República Joselitas por ter sido meu lar nessa caminhada e a todas as “Sem Noção”. Foram ensinamentos diários, momentos inigualáveis e amizades para a vida toda.
Obrigada por terem sido minha família em Ouro Preto!
Aos amigos de Viçosa e Sete Lagoas por estarem sempre na torcida mesmo de longe. À Fapemig pela concessão da bolsa de estudos.
“Tudo posso Naquele que me fortalece”
RESUMO
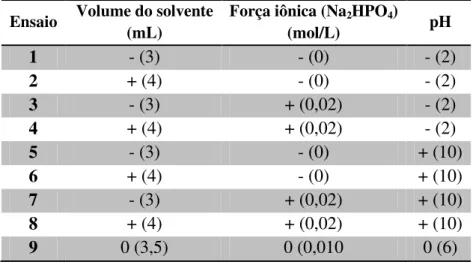
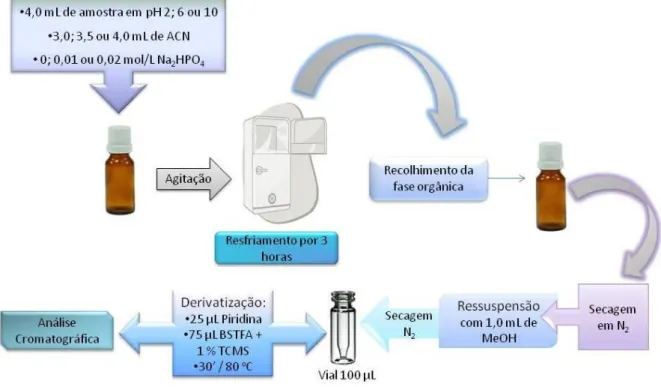
Os microcontaminantes emergentes são uma classe de contaminantes que vêm chamando a atenção da sociedade científica quanto às consequências que estes podem trazer para o meio ambiente mesmo em concentrações muito baixas (na faixa de ng/L e µg/L). São várias as substâncias assim classificadas sendo: fármacos e produtos de higiene pessoal, medicamentos veterinários, perturbadores endócrinos e nanomateriais. A rota de contaminação ambiental passa, na maioria das vezes, pela ingestão, excreção e uso tópico por humanos e animais destas substâncias, que atingem os esgotos e cursos d’água. As estações de tratamento de esgotos (ETEs) podem não ser eficazes no tratamento e remoção destes compostos. O presente trabalho apresenta a otimização do método de extração líquido-líquido com partição em baixa temperatura (ELL-PBT) de microcontaminantes dentre eles fármacos (ácido acetilsalicílico, ibuprofeno, paracetamol, genfibrozila e diclofenaco), hormônios naturais e sintéticos (estrona, estradiol, etinilestradiol e estriol) e fenóis (bisfenol A, 4-nonilfenol e 4-octilfenol) em amostras de esgoto doméstico. Foram avaliadas condições de extração como volume de solvente extrator, força iônica e pH da amostra através de um planejamento fatorial completo com ponto central. Com essa abordagem foi possível determinar como melhores condições para maior recuperação da maioria dos analitos o ajuste do pH da amostra para 2, 4 mL de amostra de esgoto, adicionar a ela 3 porções de 3 mL de acetonitrila como solvente extrator e resfriamento por 3 horas para cada extração. Os extratos foram secos em N2 gasoso e submetidos a reação de derivatização com o reagente
BSTFA+1% TCMS seguido de análise por cromatografia gasosa acoplada a espectrometria de massas (CG/EM). O método foi validado pelos parâmetros: linearidade com faixa de trabalho de 0,1 a 200 µg/L (R2 > 0,98); limites de detecção e quantificação do método (inferiores a 0,21 e 0,96 µg/L, respectivamente); precisão com desvios padrão relativos de 0,578 a 8,00%; exatidão e efeito matriz foram avaliados a partir da amostra e spike de extratos. Amostras
reais de esgoto bruto e efluentes UASB e FBP foram submetidas ao método proposto onde foram encontrados ácido acetil salicílico, paracetamol, bisfenol A, estrona e estriol.
ABSTRACT
Emergent microcontaminants are substances that have been drawing the attention of the scientific society due to the consequences they may bring to the environment, even in very low concentrations (in the range of ng/L to µg/L). There are several substances classified as emerging organic pollutants such as: drugs and personal care products, veterinary products, endocrine disruptors and nanomaterials. The environmental contamination route for these substances are, in most cases, due to the ingestion, excretion, topic use on humans and animals, leading to sewage and waterways. Sewage treatment plants (STPs) may not be effective in the treatment and removal of these compounds. This work presents an analytical optimized method using liquid-liquid extraction with low temperature partition (LLE-LTP) for emerging microcontaminants in domestic sewage samples, among them drugs (aspirin, ibuprofen, acetaminophen, diclofenac and gemfibrozil), natural and synthetic hormones (estrone, estradiol, ethinylestradiol and estriol) and phenols (bisphenol A, 4-octylphenol and 4-nonylphenol). The extraction conditions were assessed varying extractor solvents, the solvent volumes, ionic strength and sample pH, through a center point complete factorial experimental design. With this approach it was possible to determine the conditions for the best extraction recoveries for the majority of analytes. The optimized conditions where: sample pH = 2, 4 ml sewage samples, multistage 3 x 3 mL of acetonitrile as solvent extractor, 3 hours freezing for each extraction. The extracts were dried under nitrogen subjected to derivatization reaction with 70% BSTFA + 1% TCMS plus 30% pyridine, followed by gas chromatography coupled to mass spectrometry (GC/MS) analysis. The method was validated by the parameters: linearity, with working range from 0,1 to 200 µg/L (R2 > 0,98); method detection and quantification limits (0,21 and 0,96 µg/L, respectively); precision relative standard deviations in the range of 0,84 to 18,17%; accuracy and matrix effect was also evaluated through sample and extract spikes. Real samples of raw sewage and effluents from UASB and FBP treatment were analyzed by the proposed method, where acetyl salicylic acid, acetaminophen, bisphenol A, estrone and estriol were found.
ÍNDICE
1
INTRODUÇÃO ... 14
2
REVISÃO BIBLIOGRÁFICA ... 16
2.1 Microcontaminantes Emergentes ... 16
2.1.1 Fármacos ... 17
2.1.1.1 Anti-inflamatórios ... 18
2.1.1.2 Reguladores Lipídicos ... 19
2.1.1.3 Estimulantes ... 20
2.1.2 Desreguladores Endócrinos ... 21
4-Nonilfenol (4NP) ... 26
4-Octilfenol (4OP) ... 26
Bisfenol A (BPA) ... 26
Estrona (E1) ... 27
Estradiol (E2) ... 27
Etinilestradiol (EE2) ... 28
Estriol (E3) ... 30
2.2 Esgoto ... 30
2.3 Métodos Analíticos para Determinação de Microcontaminantes ... 31
2.3.2 Espectrometria de Massas (EM) ... 40
2.3.3 Métodos de preparação de amostras ... 42
2.3.3.1 Extração líquido-líquido com partição em baixa temperatura (ELL-PBT) ... 43
2.3.4 Derivatização ... 45
2.3.4.1 Reação de sililação ... 46
2.4 Validação ... 47
2.5 Planejamento Experimental e Tratamento de Dados ... 51
3
OBJETIVOS ... 53
3.1 Objetivos específicos ... 53
4
MATERIAIS E MÉTODOS ... 54
4.1 Reagentes e vidrarias ... 54
4.2 Filtração e armazenamento das amostras ... 55
4.3 Preparo das soluções padrão ... 55
4.4- Derivatização ... 60
4.5- Condições Cromatográficas e de Detecção ... 61
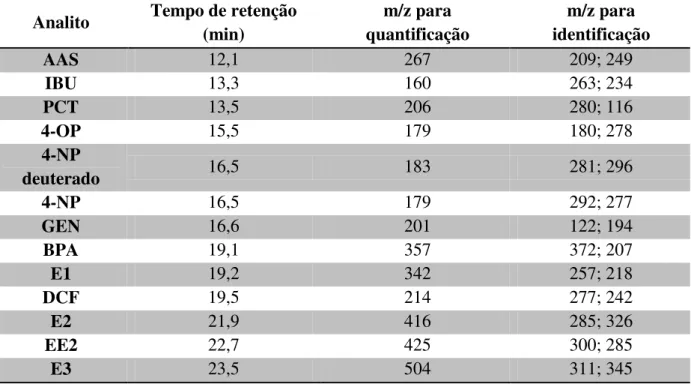
4.5.1 Relação Massa / Carga dos microcontaminantes ... 63
4.6 Validação do método de quantificação dos microcontaminantes ... 65
4.7 Análise de amostras reais ... 67
5
RESULTADOS E DISCUSSÃO ... 69
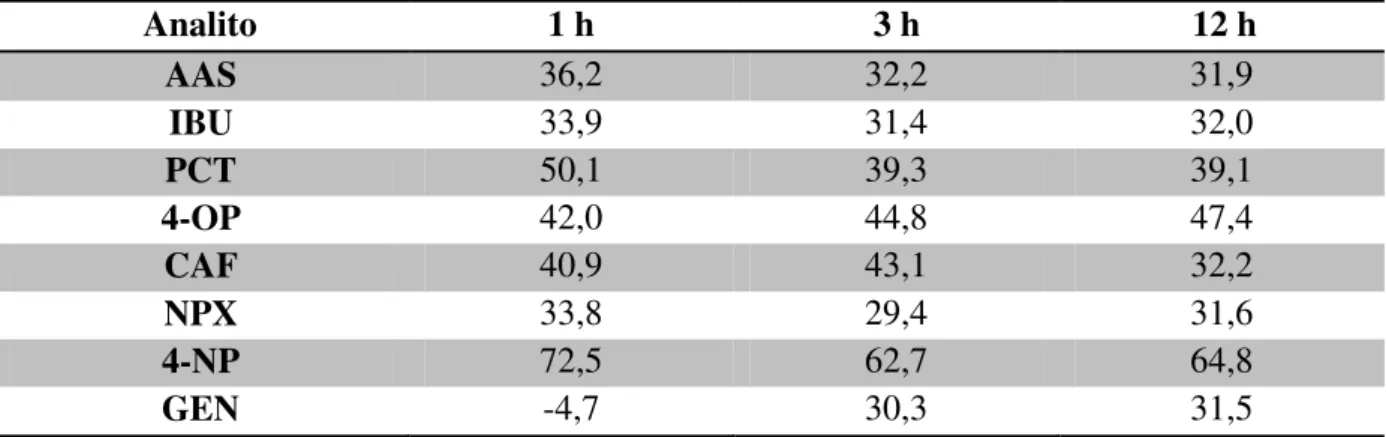
5.1 Otimização do método de extração ... 69
5.2 Validação do método ... 74
5.2.1 Seletividade ... 74
5.2.2 Curva analítica e ajuste ... 77
5.2.3 Limite de detecção e de quantificação ... 82
5.2.4 Precisão ... 83
5.2.5 Exatidão e precisão do método ... 85
5.2.6 Efeito Matriz ... 87
5.3 Análise de amostras reais ... 88
6
CONCLUSÕES ... 91
7
TRABALHOS FUTUROS ... 92
LISTA DE FIGURAS
Figura 2.1- Esquema das possíveis rotas de entrada dos microcontaminantes no meio
ambiente. Fonte: Adaptado de KUMAR et al (2012) ... 17
Figura 2.2- Ácido Acetilsalicílico ... 18
Figura 2.3- Ibuprofeno ... 18
Figura 2.4- Naproxeno ... 18
Figura 2.5- Diclofenaco Sódico ... 18
Figura 2.6- Acetaminofeno ... 19
Figura 2.7- Genfibrozila ... 20
Figura 2.8- Cafeína ... 20
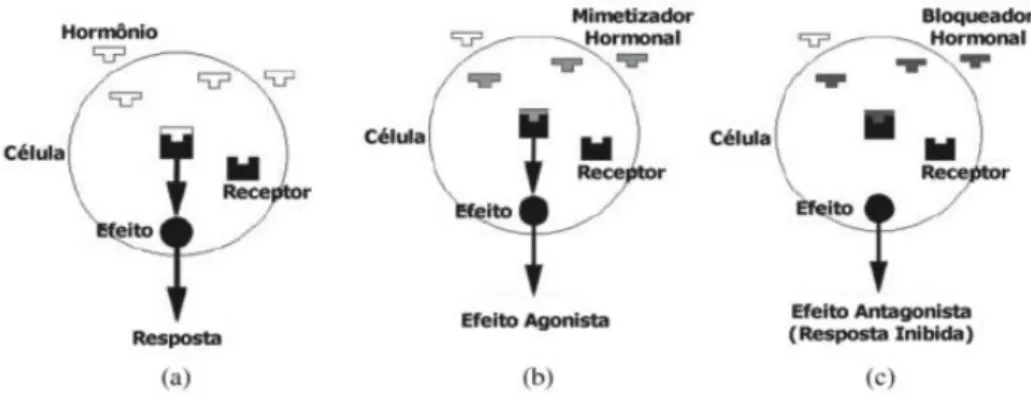
Figura 2.9- Disfunções endócrinas: a) resposta natural, b) efeito agonista, c) efeito antagonista. Fonte: (GHISELLI e JARDIM, 2007). ... 22
Figura 2.10- Representação esquemática da principal via de entrada de disruptores endócrinos hormonais em sistemas aquáticos. Adaptado de Filho et al., 2006 ... 24
Figura 2.11- Estrutura química do 4-nonilfenol ... 26
Figura 2.12- Estrutura química do 4-octilfenol ... 26
Figura 2.13- Estrutura química do bisfenol A ... 27
Figura 2.14- Estrutura química da estrona ... 27
Figura 2.15- Estrutura química do estradiol ... 28
Figura 2.16- Estrutura química do etinilestradiol ... 29
Figura 2.17- Estrutura química do estriol ... 30
Figura 2.18- Diagrama de um espectrômetro de massas ... 41
Figura 2.19- Mecanismo genérico da reação de sililação, onde X varia de acordo com os diferentes derivatizantes. Fonte: (BECKER, 2012) ... 47
Figura 4.1- Esquema da extração líquido-líquido com partição em baixa temperatura ... 60
Figura 4.3- GCMS-QP2010 plus (Shimadzu®) ... 62
Figura 4.4- Esquema dos pontos de coleta ... 68
Figura 5.1- Procedimento de preparação de amostra ... 74
Figura 5.2- Cromatograma e espectro de massa dos íons monitorados do ibuprofeno ... 75
Figura 5.3- Cromatograma e espectro de massa dos íons monitorados do 4-octilfenol ... 76
Figura 5.4- Cromatograma e espectro de massa dos íons monitorados da estrona ... 77
Figura 5.5- Curva analítica para o ácido acetil salicílico (0,1 a 200 µg/L) ... 79
Figura 5.6- Curva analítica para o ibuprofeno (2,5 a 175 µg/L) ... 79
Figura 5.7- Curva analítica para o ácido paracetamol (2,5 a 200 µg/L) ... 79
Figura 5.8- Curva analítica para o 4-octilfenol (2,5 a 200 µg/L) ... 79
Figura 5.9- Curva analítica para o 4-nonilfenol (2,5 a 200 µg/L) ... 80
Figura 5.10- Curva analítica para a genfibrozila (2,5 a 200 µg/L) ... 80
Figura 5.11- Curva analítica para o bisfenol A (0,1 a 200 µg/L) ... 80
Figura 5.12- Curva analítica para o diclofenaco (2,5 a 200 µg/L) ... 80
Figura 5.13- Curva analítica para a estrona (0,1 a 200 µg/L) ... 81
Figura 5.14- Curva analítica para o estradiol (1 a 200 µg/L) ... 81
Figura 5.15- Curva analítica para o etinilestradiol (0,1 a 175 µg/L) ... 81
LISTA DE TABELAS
LISTA DE NOTAÇÕES
4-NP: 4-nonilfenol
4-OP: 4-octilfenol
AAS: Ácido acetilsalicílico
AINH: Anti-inflamatórios não
hormonais
APCI: Atmospheric pressure chemical ionization
BPA: Bisfenol-A
BSTFA: N,O-bis (trimetilsilil)
trifluoroacetamida CAF: Cafeína
CAS: Chemical Abstracts Service CePTS: Centro de Pesquisa e Treinamento em Saneamento
CG: Cromatografia gasosa
CLAE: Cromatografia líquida de alta eficiência
CV: Coeficiente de variação
DCF: Diclofenaco
DE: Desreguladores endócrinos
E1: Estrona
E2: Estradiol
EE2: Etinilestradiol
E3: Estriol
EFS: Extração em fase sólida
ELL: Extração líquido-líquido
EM: Espectrometria de massas
EPA: Environmental Protection Agency
ESI: Electrospray Ionization
ETE: Estação de tratamento de esgoto
FBP: Filtro biológico percolado
GEN: Genfibrozila
IBU: Ibuprofeno
IE: Ionização por impacto de elétrons
IUPAC: International Union of Pure and Applied Chemistry
LD: Limite de detecção
LQ: Limite de quantificação
MEFS: Microextração em fase sólida
MM: Massa molecular
NPX: Naproxeno
PI: Padrão interno
SCAN: Scanning íon
SIM: Selected ion monitoring PCT: Paracetamol
Kow: Coeficiente de partição octanol/água
PE: Ponto de ebulição
POP: Poluentes Orgânicos Persistentes
PPCP: Produtos de Higiene Pessoal e Produtos Farmacêuticos
TCMS: Trimetilclorosilano
UASB: Upflow anaerobic sludge blanket
UE: União Europeia
14
1
Introdução
Atualmente, um dos tópicos mais relevantes na química ambiental é a qualidade das águas. A preocupação com micropoluentes (poluentes que estão presentes no meio ambiente em concentrações da ordem de μg/L e ng/L) tem aumentado expressivamente nos últimos anos. Fármacos, desreguladores endócrinos e poluentes orgânicos persistentes (POPs) são classes de substâncias muito investigadas devido, principalmente, aos seus possíveis efeitos no meio ambiente. Uma grande preocupação relacionada a essas classes de substâncias é que podem produzir efeitos adversos aos organismos expostos em concentrações muito baixas (BILA e DEZOTTI, 2007). Incluem não só as substâncias originais, mas também seus subprodutos ou metabólitos, ou seja, produtos da degradação química e biológica dos compostos originais. Os microcontaminantes representam uma mudança no conceito tradicional sobre contaminação ambiental, pois muitos são produzidos industrialmente e estão dispersos no ambiente pelo uso doméstico, comercial e industrial.
A classe de Produtos de Higiene Pessoal e Produtos Farmacêuticos (PPCPs) é a mais diversa categoria de substâncias emergentes. Nesta classe de microcontaminantes, se encontram as drogas de prescrição terapêutica, medicamentos veterinários, fragrâncias, aditivos de cosméticos, protetores solares, agentes de diagnóstico, nutracêuticos (ex. vitaminas) e drogas ilícitas (anfetaminas, cocaína, etc.). Muitos destes compostos são solúveis em água e são expostos aos compartimentos ambientais através de águas residuárias (industriais e municipais), fossas sépticas, drenagem do lodo de esgotos, estrume de animais, chorume e lixiviado de aterros sanitários. A rota de contaminação passa, na maioria das vezes, pela ingestão e uso tópico por humanos e animais, ou pela exposição involuntária nas águas e nos alimentos. Devido às propriedades recalcitrantes e antibióticas destes compostos, as estações de tratamento de esgotos (ETEs) podem não ser eficazes no seu tratamento e remoção (KÜMMERER, 2010).
Os compostos classificados como desreguladores endócrinos são produtos químicos hormonalmente ativos capazes de interferir no sistema endócrino de animais (KUMAR et al.,
15
diabetes tipo 2, síndrome metabólica, complicações pulmonares e cardiovasculares, além de doenças do fígado), bem como outras questões de saúde, como problemas psicológicos e ou sociais, problemas reprodutivos e algumas formas de câncer (HATCH et al., 2010; SAAL et al., 2012).
Pesquisadores do mundo inteiro vêm se empenhando no desenvolvimento de métodos
analíticos suficientemente sensíveis, com limites de detecção na ordem de μg/L e ng/L para detecção desses compostos em diversas matrizes ambientais. A preparação e concentração de dos analitos das amostras são extremamente importantes quando se trata de análise de traços. Dentre as técnicas mais utilizadas a extração em fase sólida (EFS), microextração em fase sólida (MEFS) têm se destacado (BUENO et al., 2012; SHIN e OH, 2012; GOMES et al.,
2011). Os equipamentos utilizados nestas determinações, em geral, são bastante sofisticados e apresentam elevada detectabilidade, enquanto que os procedimentos de extração e concentração dos produtos farmacêuticos e de higiene pessoal e dos possíveis interferentes endócrinos são bastante minuciosos. Dentre os métodos de análise, a cromatografia gasosa e líquida acoplada a espectrometria de massas têm ganhado destaque.
16
2
Revisão Bibliográfica
2.1 Microcontaminantes Emergentes
Os microcontaminantes emergentes são uma classe de contaminantes que vêm chamando a atenção da sociedade científica quanto às consequências que estes podem trazer para o meio ambiente aquático mesmo em concentrações muito baixas (na faixa de ng/L e µg/L). De acordo com a EPA, 2008 as substâncias classificadas como microcontaminantes são:
Poluentes orgânicos persistentes (POP) tais como éteres difenílicos polibromados utilizados em retardantes de chama, plastificantes, assim como ácidos orgânicos perfluorados;
Fármacos e produtos de higiene pessoal incluindo os fármacos de uso humano com prescrição ou venda livre, bactericidas, protetores solares e fragrâncias;
Medicamentos veterinários, como os antibióticos, antifúngicos e hormônios;
Perturbadores endócrinos que inclui hormônios naturais e sintéticos, pesticidas, alquilfenois, etc; e
Nanomateriais: nanotubos de carbono, dióxido de titânio particulado em nano escala, etc.
17
Figura 2.1- Esquema das possíveis rotas de entrada dos microcontaminantes no meio ambiente. Fonte: Adaptado de KUMAR et al (2012)
Dentre os microcontaminantes citados, uma revisão bibliográfica acerca da ocorrência e procedimentos analíticos para alguns fármacos e perturbadores endócrinos avaliados neste trabalho é apresentada.
2.1.1 Fármacos
A indústria farmacêutica cresce a cada ano e está presente no cotidiano da população mundial. Com isso, estes microcontaminantes vêm sendo cada vez mais detectados no meio ambiente. No entanto, pouco se sabe sobre seu impacto ambiental. A ocorrência de medicamentos humanos e veterinários no meio ambiente tem sido um assunto de preocupação, pois muitos destes contaminantes emergentes têm demonstrado persistência no solo e na água (CELIZ et al., 2009).
Os fármacos chegam ao meio ambiente via excreção, parte em sua forma ativa e parte em forma de metabólitos, além de muitas vezes serem descartados de maneira inadequada no vaso sanitário (KUMMERER, 2010). Efluentes de indústrias farmacêuticas e efluentes rurais também contribuem, e muito, para a descarga desses contaminantes no meio ambiente. A baixa volatilidade dos produtos farmacêuticos indica que a distribuição no ambiente ocorre, principalmente, pelo transporte aquático e pelos alimentos na dispersão de cadeia (FENT, 2006).
Estudos recentes têm demonstrado que, apesar das concentrações relativamente baixas de medicamentos no meio ambiente, há a preocupação quanto aos efeitos adversos causados
18
pesquisadores estão investigando as condições operacionais na eficiência de remoção de produtos farmacêuticos em águas residuais de modo a minimizar a sua liberação para os sistemas terrestres e aquáticos. Além disso, as avaliações de riscos e monitoramento ambiental estão sendo realizados a fim de obter informações suficientes que permitam o monitoramento e regulação de produtos farmacêuticos (CELIZ et al., 2009).
2.1.1.1 Anti-inflamatórios
Os anti-inflamatórios não hormonais (AINH) fazem parte de um grupo de medicamentos dos mais comercializados em todo o mundo e estão entre os fármacos mais encontrados no meio ambiente (SANTOS et al., 2010).
Os AINHs constituem um grupo heterogêneo de compostos de um ou mais anéis aromáticos ligados a um grupamento ácido funcional. São ácidos orgânicos fracos que atuam, principalmente, nos tecidos inflamados e ligam-se, significativamente, à albumina plasmática (CHAHADE et al., 2008). As figuras 2.2 a 2.5 representam as estruturas químicas dos AINHs
estudados neste trabalho.
Figura 2.2- Ácido Acetilsalicílico
O
O O C
H3
OH
Figura 2.3- Ibuprofeno O
C H3
CH3
OH
CH3
Figura 2.4- Naproxeno
O
O H
O CH3
Figura 2.5- Diclofenaco Sódico Na O
NH Cl
19
O acetaminofeno (N-acetil-p-aminofenol, 4-acetamidofenol, paracetamol), apresentado na figura 2.6, é um composto p-aminofenólico que apresenta atividades analgésica e antipirética. Este fármaco não possui atividade anti-inflamatória, mesmo assim é, provavelmente, o antipirético-analgésico de segunda escolha, principalmente aos pacientes alérgicos ao ácido acetilsalicílico ou que sofram de úlceras pépticas (BECKER, 2012).
Figura 2.6- Acetaminofeno
O
OH NH
C H3
Gómez e colaboradores (2007) monitoraram uma estação de tratamento de esgoto (ETE) no sul da Espanha por um ano para análise simultânea de 14 contaminantes orgânicos. Dentre os estudados, encontraram ibuprofeno, acetaminofeno e diclofenaco nas concentrações médias de 84, 134 e 1,5 µ/L respectivamente, antes do tratamento. No efluente encontraram uma média de 7,1, 0,22 e 0,9 µ/L. As análises foram feitas por cromatografia gasosa acoplada a espctrometria de massa (CG-EM).
Também na Espanha, Bueno e colaboradores (2012) monitoraram 100 compostos orgânicos durante dois anos em cinco ETEs municipais. Dentre os compostos que representaram a maior parte da poluição do efluente, não apenas pelas concentrações, mas também pelo número de vezes em que foram detectados, estão os AINHs ibuprofeno, diclofenaco, naproxeno; o regulador lipídico genfibrozila e o estimulante cafeína.
2.1.1.2 Reguladores Lipídicos
Reguladores lipídicos são medicamentos que reduzem o nível de colesterol total e de triglicérides e utilizados para o tratamento de doenças coronarianas e infarto do miocárdio.
20
Figura 2.7- Genfibrozila O CH3
CH3
C H3
CH3
O
OH
Bendz (2005) e colaboradores monitoraram vários compostos farmacêuticos ativos em uma ETE na Suécia. Dentre esse compostos a genfibrozila foi encontrada na concentração de 0,71 µg/L e sendo obtida uma eficiência de remoção de 75% da planta em questão deste composto.
2.1.1.3 Estimulantes
Cafeína
A cafeína é um alcalóide, identificado como 1,3,7-trimetilxantina, cuja estrutura contém um esqueleto de purina (Figura 2.8). Este alcaloide é encontrado em grande quantidade nas sementes de café e nas folhas de chá verde (Camilla sinensis). Também pode ser achado em outros produtos vegetais, particularmente no cacau (Theobroma cocoa), no
guaraná (Paullinia cupana) e na erva-mate (Ilex paraguayensis). Embora uma parcela
pequena da população consuma cafeína na forma de fármacos, como, por exemplo, antigripais, grande parte deste alcalóide é ingerida na forma de bebidas. Uma xícara de café pode conter em média cerca de 80 mg de cafeína, enquanto uma lata de coca-cola em torno de 34-41 mg (MARIA e MOREIRA, 2007).
Figura 2.8- Cafeína CH3
CH3 C
H3
O
O N
N N
N
21
aumenta a capacidade de concentração, aumenta a memória de curto prazo, aumenta a capacidade de resolver problemas que exigem raciocínio, aumenta a capacidade de tomar decisões corretas e aumenta a capacidade de funcionamento cognitivo e de coordenação neuromuscular (GLADE, 2010).
A cafeína é considerada por muitos autores um marcador químico de contaminação antropogênica (DANESHVAR et al., 2012; BUERGE et al., 2003). No entanto, tal função é
limitada a áreas em que não há relevantes fontes naturais e industriais de cafeína (BUERGE et al., 2006).
2.1.2 Desreguladores Endócrinos
Há evidências de que uma ampla gama de produtos químicos presentes no meio ambiente são capazes de interferir no sistema endócrino de animais selvagens, incluindo aves, peixes, mamíferos, répteis e moluscos. Estes produtos químicos hormonalmente ativos, conhecidos como desreguladores endócrinos (DE), podem atingir os sistemas ribeirinhos através de uma variedade de entradas, incluindo fluxos de resíduos urbanos, rurais, industriais e de atividades de agricultura intensiva (KUMAR et al., 2012).
Alguns efeitos citados na literatura, tais como diminuição na eclosão de ovos de pássaros, peixes e tartarugas; feminização de peixes machos; problemas no sistema reprodutivo em peixes, répteis, pássaros e mamíferos e, alterações no sistema imunológico de mamíferos marinhos, têm sido associadas à exposição de espécies de animais aos desreguladores endócrinos. Em alguns casos esses efeitos podem conduzir ao declínio da população. Em seres humanos esses efeitos incluem a redução da quantidade de esperma, o aumento da incidência de câncer de mama, de testículo e de próstata e a endometriose (BILA e DEZOTTI, 2007).
22
Os estrogênios ambientais podem causar respostas antagônicas e agônicas, por mecanismos de ação via receptores hormonais. A atividade agonista é a capacidade de uma substância acoplar-se ao receptor de hormônios esteróides e elucidar uma resposta. Em contrapartida, a atividade antagonista é a habilidade de uma substância acoplar-se ao receptor de estrogênio e bloquear a ação do ligante natural e, assim, sua resposta não será elucidada (BILA e DEZOTTI, 2007).
Figura 2.9- Disfunções endócrinas: a) resposta natural, b) efeito agonista, c) efeito antagonista. Fonte: (GHISELLI e JARDIM, 2007).
A tabela 2.1 mostra alguns efeitos causados por vários compostos classificados como desreguladores endócrinos.
23 Tabela 2.1- Compostos desreguladores endócrinos, suas fontes e efeitos estudados em laboratório.
Classificação Compostos Fontes Efeitos biológicos
Hormônios naturais 17β-estradiol (E2) Estrona (E1)
Estriol (E3) Testosterona
ETA Hermafroditismo e VTG em peixes
Fitoestrogênios β-sitosterol Isoflavonóides Coumesterol
Zearalenona Lignanas Genisteína
EFPC, comida Ligar a receptores estrogênicos, alterar produção de esteróides.
Hormônios sintéticos 17α-etinilestradiol (EE2)
Mestranol Dietilestilbestrol EFPC, tratamento médico Efeito agonista e antagonista, VTG, estimular formação de óvulo em peixes e caracóis machos.
Alquilfenóis Nonilfenol (NP) Octilfenol Butilfenol
Pentafenol EFPC Redução da reprodução, produção de ovos, indução da VTG, hermafroditismo em peixes machos.
Fenóis Bisfenol A (BPA) Bisfenol F EFPC Efeito agonista, hermafroditismo em peixes.
Ftalatos Dietilhexilftalato Diciclohexilftalato
Dihexiftalato Diciclohexilftalato
Lixiviação de plásticos Efeito agonista e antagonista
Pesticidas Antrazina Dieldrin/Aldrin Endosulfan
Lindano Permerina
ETA, região agrícola Hermafroditismo em peixes e sapos, produção de VTG, alteração nos níveis de hormônios de sapos.
Adaptado de KUMAR et al., 2012
24
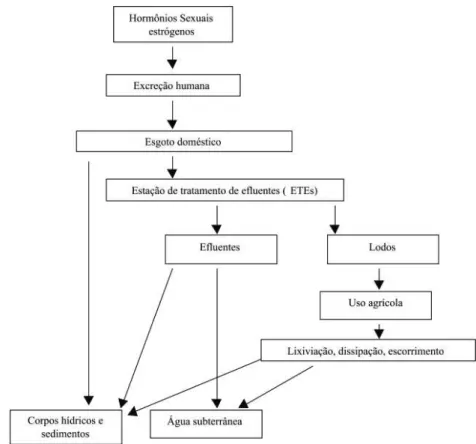
Os hormônios excretados através da urina e fezes seguem para a rede coletora, adentrando depois ao ambiente. O lançamento de efluentes in natura ou mesmo processados são as principais vias de contaminação do ambiente aquático, seja pelo déficit de infraestrutura em saneamento, seja pela ineficiência (tecnológica e/ou operacional) das estações de tratamento. Apesar de possuírem meia-vida relativamente curta quando comparados a outros compostos orgânicos (como alguns pesticidas), os estrógenos naturais são continuamente introduzidos no ambiente o que lhes concede um caráter de persistência. Estudos relatam que até 40% das doses ministradas de estrógenos sintéticos podem ser disponibilizadas para o ambiente. A Figura 2.10 exemplifica o modo de entrada destes contaminantes para os ecossistemas (FILHO et al., 2006).
Figura 2.10- Representação esquemática da principal via de entrada de disruptores endócrinos hormonais em sistemas aquáticos. Adaptado de Filho et al., 2006
25
Tabela 2.2- Substâncias químicas classificadas como DE
Ftalatos Pesticidas
dietil ftalato (DEP) di-iso-butil ftalato (DIBP)
di-n-butil ftalato (DBP) butilbenzil ftalato (BBP) diciclohexilo ftalato (DCHP) di-2-(2-etil-hexil) ftalato (DEHP)
di-n-octil ftalato (DOP) di-isooctil ftalato (DIOP) di-iso-nonil ftalato (DINP)
di-iso-decil ftalato (DIDP
Inseticida
DDT (2,2 bis-p-clorofenil-1,1,1-tricloroetano) DDE (2,2 bis-p-clorofenil-1,1-dicloroetileno)
deltametrina carbofurano Herbicidas atrazina linuron Fungicidas
vinclozolina tridemorfos carbendazina procimidona penconazol epoxiconazol
procloraz
Pesticidas organoclorados Lindano (1,2,3,4,5,6-hexacloroexano) Alquilfenóis
nonilfenol nonilfenol etoxilado octilfenol octilfenol etoxilado
Organoclorados dibenzo-p-dioxina
TCDD (2,3,7,8-tetraclorodibenzeno-p-dioxina)
TCDF (2,3,7,8-tetraclorodibenzofurano) Compostos orgânicos de estanho
Bisfenol Tributilestanho (TBT)
Trifenilestanho (TPT) Bisfenol A
Parabenos Policlorados de bifenilas
benzilparabeno isobutilparabeno butilparabeno n-propilparabeno etilparabeno metilparabeno
2,4,4’-triclorobifenil 2,2’,5,5’-tetraclorobifenol 2,2’,4,5,5’-pentaclorobifenil 2,3,4,4’,5-hexaclorobifenil 2,2’3,4,4’,5- hexaclorobifenil 2,2’,4,4’,5,5’-hexaclorobifenil 2,2’,3,4,4’,5,5’-heptaclorobifenil Hidrocarbonetos aromáticos policíclicos
Naftalina Acenaftileno Fluoreno Fenantreno Antraceno Fluoranteno Pireno Benzo[a]antraceno Criseno Benzo[b]fluoranteno Benzo[k]fluoranteno Benzo[a]pireno Indeno[123-cd] pireno Dibenzo[ah]antraceno Benzo[ghi]perileno
Retardantes de chama bromado Polibromobifenila( PPB) polibromobifenila( PPB)
2,2’,4,4’-tetrabromodifenil éter 2,2’,4,4’,5-pentabromodifenil éter
2,2’,4,4’,6-pentabromodifenil éter 2,2’,4,4’,5,5’-hexabromodifenil éter
2,2’,4,4’,5,6-hexabromodifenil éter 2,2’,3,4,4’,5,6-heptabromodifenil éter
octabromodifenil éter (BDE octa) decabromociclodifenil éter (BDE 209)
hexabromociclododecano (HBCD) tetrabromobisfenol A (TBBA) Metais pesados
Cádmio Mercúrio
Chumbo Zinco
Agentes terapêuticos e farmacêuticos
Dietilestilbestrol (DES) 17α-etinilestradiol (EE2)
Fitoestrogênios Estrogênios naturais
Isoflavona: daidzeína e genisteína Lignanas: metaresinol e enterodiol Estrona (E1)
17β-estradiol (E2) Estriol (E3)
Fonte: (BILA e DEZOTTI, 2007)
26 4-Nonilfenol (4NP)
A liberação do 4-nonilfenol para o meio ambiente pode ser resultante dos resíduos de vários produtos uma vez que são utilizado na preparação de lubrificantes, aditivos de óleo, resinas, plastificantes, agentes tenso ativos, antioxidantes para borrachas e plásticos, e como material de partida para a produção de resinas fenólicas. O 4-nonilfenol foi identificado em água potável, águas subterrâneas, rios e lagos, estação de tratamento de efluentes, e é um contaminante de destaque no lodo de esgoto (“PUBCHEM, 2012”).
Figura 2.11- Estrutura química do 4-nonilfenol O
H
CH3
Liu e colaboradores (2012) confirmaram que desreguladores endócrinos, entre eles o 4-nonilfenol, se acumulam nos músculos de peixes quando estes são expostos a efluentes contendo este microcontaminantes. Esta acumulação pode explicar vários efeitos biológicos nas espécies em estudo.
4-Octilfenol (4OP)
O 4-octilfenol, junto com o 4-nonilfenol, são produtos da degradação do dos alquilfenóis etoxilados, que são surfactantes usados em formulações de detergentes de uso industrial e doméstico. Também são usados na produção de resinas fenólicas, como aditivos plásticos, emulsificantes, agentes umificantes e em formulações de agrotóxicos. A principal fonte desses compostos para o meio aquático é proveniente do uso doméstico de surfactantes (RAIMUNDO, 2007).
Figura 2.12- Estrutura química do 4-octilfenol O
H
CH3
Bisfenol A (BPA)
27
de materiais e produtos (por exemplo, garrafas, tubos, revestimentos, selantes dentários, embalagens de alimentos, esmaltes e materiais retardadores de chama). Devido a sua ampla utilização a população humana pode facilmente entrar em contato com o BPA no dia-a-dia (ASIMAKOPOULOS et al., 2012).
Figura 2.13- Estrutura química do bisfenol A
CH3
CH3
OH O
H
Uma grave consequência da exposição ao BPA foi relatada por Aldad e colaboradores (2011) que expuseram fêmeas de macacos a este composto e comprovaram que o BPA, indiretamente, aumenta a ação de estrogênios. Esse efeito pode explicar doenças como endometriose, hiperplasia do endométrio, câncer, além de poder estar associado a abortos espontâneos.
Estrona (E1)
A estrona é um estrogênio natural mais potente que o estriol e menos que o estradiol. É o principal estrógeno circulante após a menopausa e a maior parte está conjugada sob a forma de sulfato. É muito utilizada para avaliação do hipogonadismo, avaliação da puberdade precoce (completa ou parcial), diagnóstico de tumores feminilizantes e acompanhamento de reposição hormonal na menopausa, em alguns casos (NOBEL, 2012).
Figura 2.14- Estrutura química da estrona O
O H
No trabalho de Salste et al (2007) a estrona foi o único estrogênio encontrado acima
do limite de quantificação indicando que ele é o principal contribuinte para a atividade estrogênica do efluente de uma estação de tratamento da cidade de Turku, na Finlândia.
Estradiol (E2)
28
consideravelmente. Além disso, também é responsável pela manutenção dos tecidos do organismo, garantindo a elasticidade da pele e dos vasos sanguíneos e a reconstituição óssea, entre outras funções (GOODMAN GILMAN, 2005). É metabolizado principalmente no fígado, sendo os principais metabólitos a estrona e o estriol e seus conjugados, os quais são consideravelmente menos potente do que o estradiol. A maior parte dos metabólitos são excretados na urina como glucuronídeos e sulfatos (BALFOUR, J.A. e HEEL, R.C.,1990)
Figura 2.15- Estrutura química do estradiol OH
O H
Estradiol e os seus ésteres semi-sintéticos (valerato de estradiol, especialmente), são os principais estrogênios utilizados no tratamento de perturbações da menopausa. A sua utilização também tem sido proposta para a prevenção de doenças cardiovasculares (IARC, 2012).
Devido ao uso do estradiol para tratamentos, além de ser um estrogênio natural, há a preocupação quanto a sua ocorrência no meio ambiente. No trabalho de Svenson e colaboradores (2003) foi relatado que, em efluentes de estações de tratamento de esgoto doméstico da Suécia, havia compostos estrogênicos correspondentes ao estradiol nas concentrações de 0,1-15 ng / L. Além disso, baixos níveis de atividade estrogênica também foram encontrados em um rio que recebe efluentes municipais, tomada a cerca de 3,5-35 km a jusante de uma estação de tratamento de esgoto. Já em esgoto não tratado, as concentrações de estradiol estava em torno de 1-30 ng de estradiol / L.
Etinilestradiol (EE2)
29
Figura 2.16- Estrutura química do etinilestradiol CH O
H
O H
O uso de medicamentos contendo estrógenos sintéticos possuem muitos pontos negativos e entre os mais graves, o desenvolvimento e evolução de câncer de mama. Tais compostos possuem maior potencial endócrino e são excretados na urina de mulheres que usam os contraceptivos (TOMŠÍKOVÁ et al., 2012).
Vários estudos já comprovaram que a exposição de animais aquáticos ao EE2, e outros estrógenos, causam mudanças no fenótipo como falha nos órgão reprodutivos, feminização (ou demasculinização) de machos, formação de hermafroditas e aumento na produção da proteína vitelogenina (proteína sintetizada pelas fêmeas durante a maturação óocita) (SUMPTER e JOHNSON, 2008).
Kidd e colaboradores (2007) expuseram peixes da espécie Pimephales promelas, em
uma lagoa experimental no Canadá, a baixas concentrações de EE2 (5-6 ng/L) durante sete anos. Eles constaram a feminização de machos da espécie devido a produção da proteína vitelogenina, alterações no desenvolvimento gonadal comprovada pela presença de peixes hermafroditas e mudanças na oogênese de fêmeas. Por fim, houve uma diminuição significativa da população dos peixes no lago.
Tompsett e colaboradores (2012) expuseram girinos da espécie Xenopus laevis a três
níveis de concentração de EE2 (0,09, 0,84, ou 8,81mg/L) e em todos eles foi observado atrasos significativos no tempo de metamorfose. Houve um grande número de anfíbios com genótipo masculino que exibia fenótipo dos dois sexo (hermafroditismo), além do aumento na produção da proteína vitelogenina em ambos os sexos.
30 Estriol (E3)
O estriol é um estrógeno natural, altamente sintetizado durante a gravidez e pode ser originado pelo metabolismo do estradiol e da estrona sendo menos ativo que estes (RAIMUNDO, 2007). É amplamente utilizado na reposição hormonal na menopausa uma vez que o estriol induz a normalização do epitélio vaginal, cervical e uretral, ajudando a restaurar a microflora normal e o pH fisiológico da vagina. Além disso, aumenta a resistência das células para inflamação e infecção (VOOJIS e GEURTS, 1995).
Figura 2.17- Estrutura química do estriol
Em amostras do rio Dourados, no estado do Mato Grosso do Sul, que devido a criação extensiva de gado na região pode receber excrementos destes animais, foram feitas análises de estrógenos naturais. O estriol foi o encontrado em maior quantidade, com concentrações na faixa de 11 e 130 ng/L (ZOCOLO et al., 2010).
2.2 Esgoto
A palavra esgoto costuma ser usada para definir tanto a tubulação condutora das águas servidas de uma comunidade, como também o próprio líquido que flui por estas canalizações. Hoje este termo é usado quase que apenas para caracterizar os despejos provenientes das diversas modalidades do uso e da origem das águas, tais como as de uso doméstico, comercial, industrial, as de utilidades públicas, de áreas agrícolas, de superfície, de infiltração, pluviais, e outros efluentes sanitários.
Os esgotos costumam ser classificados em dois grupos principais: os esgotos sanitários e os industriais. Os primeiros são constituídos essencialmente de despejos domésticos, uma parcela de águas pluviais, águas de infiltração, e eventualmente uma parcela não significativa de despejos industriais, tendo características bem definidas.
31
Compõem-se essencialmente da água de banho, urina, fezes, papel, restos de comida, sabão, detergentes, águas de lavagem.
Os esgotos industriais, extremamente diversos, provêm de qualquer utilização da água para fins industriais, e adquirem característicos próprias em função do processo industrial empregado. Assim sendo, cada indústria deverá ser considerada separadamente, uma vez que seus efluentes diferem até mesmo em processos industriais similares (JORDÃO, 1995).
O esgoto doméstico é uma matriz bastante complexa do ponto de vista analítico. Ele pode conter muitos compostos orgânicos tais como, ácidos húmicos e fúlvicos, proteínas, lipídeos, além de detergentes do tipo alquilbenzeno-sulfonados de cadeia linear (LAS), surfactantes aniônicos que são amplamente utilizados e estão no esgoto em altas concentrações (cerca de 10mg/L). Devido sua abundância e atividade surfactante esses compostos são interferentes importantes encontrados na matriz esgoto, que podem competir com os analitos de interesse no sistema cromatográfico.
2.3 Métodos Analíticos para Determinação de Microcontaminantes
Os microcontaminantes entram no meio ambiente constantemente, porém em concentrações muito baixas na ordem de µg/L e ng/L. As amostras ambientais (água superficial, efluente de ETE, esgoto bruto), são amostras muito complexas fazendo necessário o desenvolvimento de técnicas eficientes de preparação e concentração das mesmas (KOSTOPOULOU e NIKOLAOU, 2008).
Técnicas cromatográficas, líquida e gasosa, são as mais utilizadas para análises desses compostos. O acoplamento da espectrometria de massas a essas técnicas é o mais apropriado devido a sua grande seletividade. A cromatografia gasosa ainda exige um passo a mais que é a derivatização dos analitos para que seja possível a adição de grupamentos que levam a diminuição do ponto ebulição, para que assim sejam passíveis a esse tipo de análise (GABET
et al., 2007). A Tabela 2.3 apresenta alguns dados de monitoramento de microcontaminantes
32 Tabela 2.3- Dados de monitoramento de microcontaminantes em amostras ambientais
Matriz Analitos Preparo de
amostra Derivatização
Análise
Instrumental Recuperação (%) LD e LQ (ng/L)
Concentração encontrada
(µg/L) Referência
Esgoto e efluente de estação de tratamento PCT IBU DCF NPX GEN CAF EFS: HLB (200 mg), MeOH ELL (2x hexano) - CLAE/EM: (coluna Zorbax C18 250 x 3,0 mm x 5 µm; fase
móvel (A) ACN e água MilliQ com
0,1% de ácido fórmico e (B) ACN e
água MilliQ). CG/EM (coluna
HP-5MSi 15m x 0,25 mm x 0,25 µm)
34 (PCT), 98 (NPX), 116
(IBU), 120 (DCF), 114 (GEN), 100
(CAF),
Esgoto: LD: 19,6 (PCT), 14,4 (NPX), 2,2 (IBU),
0,7 (DCF), 0,1 (GEN), 8,8 (CAF)
LQ: 65,4 (PCT), 48,2 (NPX), 7,4 (IBU), 2,4 (DCF),
0,3 (GEN), 29,4 (CAF)
Esgoto: 19,3-180,5 (PCT), 14 (IBU),
>59 (CAF) Efluente: 0,08-13,8
(PCT), 5 (IBU), 3,5 (DCF), 1,2
(NPX) 0,01-0,3 (GEN), <8
(CAF) BUENO, 2012 Esgoto e efluente de estação de tratamento IBU
PCT CAF BPA
EFS: HLB (200 mg), acetato de etila - CLAE/ESI/EM: (coluna Zorbax C8 150 mm x 4,6 mm x
5 µm; fase móvel metanol: água
(15%)) CG/EM (coluna
ZB-5 MS, 30 m × 0,2ZB-5 mm × 0,25 µm; He a
1 ml/min; EI a 70 eV)
83 (IBU), 75 (PCT), 94 (CAF), 85 (BPA)
LD: 23 (IBU), 32 (PCT), 1 (CAF), 7
(BPA) Esgoto: 34-168 (IBU), 29-246 (PCT), 52-192 (CAF), 0,72-3.4 (BPA) Efluente: 0,24-28 (IBU), <LD-4,3 (PCT), 1.4-44 (CAF), 0,14-0,98 (BPA)
33 Tabela 2.3- Dados de monitoramento de microcontaminantes em amostras ambientais (continuação)
Matriz Analitos Preparo de
amostra Derivatização Instrumental Análise Recuperação (%) LD e LQ (ng/L)
Concentração encontrada
(ng/L) Referência
Esgoto e efluente de estação de tratamento DCF CAF GEN IBU
NPX EFS: RP-C18
PFBBr, MTBSTFA ou mistura de MSTFA,
TMSI e DTE CG/EM - -
Esgoto: 3,02 (DCF), 230 (CAF), 0,44 (NPX), ND (GEN
e IBU) Efluente: 2,51
(DCF), 0,18 (CAF), 0,07 (GEN), 0,1 (IBU),
0,08 (NPX) HEBERER, 2002 Água superficial IBU
NPX DCF ELL (2x de 20 mL diclorometano) 200 µL de HCl 1,0 mol/L em metanol
CG/EM (coluna DB-5 30 m x 0,25 mm x 0,25 µm; He
a 1 mL/min; EI a 70 eV)
102 (IBU), 99 (NPX), 98 (DCF)
LD: 20 (IBU), 0,3 (NPX), 3,0
(DCF) LQ: 60 (IBU),
1 (NPX), 10 (DCF)
ND (IBU), 4,5
(NPX), 310 (DCF) SHIN e OH, 2012
Água do mar CAF NPX IBU
DCF GEN
EFS (resina XAD-2 PS–DVB,
metanol) -
CLUE/ESI/EM (coluna Acquityn HSS T3 (2,1 x 100 mm x 1,8 µm; fase
móvel: ácido acético:água 0,01M
e ácido acético:ACN
0,01M)
10,6 (CAF), 37,9 (NPX), 63 (IBU), 37,6 (DCF), 64,5
(GEN)
LD: 8 (CAF), 12 (NPX), 7
(IBU), 4 (DCF), 6 (GEN) LQ: 26 (CAF),
40 (NPX), 23 (IBU), 13 (DCF), 20 (GEN)
51,2 (CAF), ND (NPX, IBU, DCF,
GEN)
34 Tabela 2.3- Dados de monitoramento de microcontaminantes em amostras ambientais (continuação)
Matriz Analitos Preparo de
amostra Derivatização Instrumental Análise Recuperação (%) LD e LQ (ng/L)
Concentração encontrada
(ng/L) Referência
Efluente de estação de tratamento DCF IBU NPX PCT CAF GEN
EFS (HLB, metanol
e acetato de etila) -
CLAE/ESI/EM (coluna Polaris C18 150mm x 2 mm x 3 µm; fase móvel (A) água MilliQ com 0,015% ácido fórmico
+ 5% metanol e (B) metanol)
-
LQ: 39 (CAF), 15 (DCF), 17
(GEN), 19 (IBU), 24 (NPX), 26 (PCT)
1,49 (DCF), ND (IBU, NPX, PCT,
CAF, GEN)
NÖDLER et al., 2010
Água superficial e água potável E1 E2 E3 EE2 BPA 4OP 4NP
EFS (HLB 500 mg,
MeOH) -
CLAE/ESI/EM (coluna (Zorbax SB-C18 2,1 x 3 mm x 3,5
µm; fase móvel (A) água e (B) MeOH, ambos com 0,1% de hidróxido de amônio)
81 (E1), 109 (E2), 140 (E3), 103 (EE2), 82 (BPA), 98 (4OP), 72 (4NP)
LD: 0,1 (E1), 0,2 (E2, E3), 1,0 (EE2), 0,4
(BPA), 0,04 (4OP, 4NP)
LQ: 0,3 (E1), 0,6 (E2, E3), 3,1 (EE2), 1,2
(BPA), 0,1 (4OP, 4NP)
Água superficial: <LQ (E1), 1,48 a 7,7 (E3), 2,76 a 11,4 (BPA), <LQ a
1,96 (4OF), 1,24 (4NF).
Água potável: ND (E1, E2, E3, EE2), <LQ (BPA, 4OF,
4NF)
JARDIM et al., 2012
Esgoto e efluente de
estação de tratamento
IBU
NPX E1 E2
MEFS (fibra PDMS/DVB (polidimetilsiloxan
o/divinilbenzeno)
ECF e solução de EtOH e
piridina
CG/EM (coluna Rtx-5MS 15 m x 0,25 mm
x 0,25 µm; EI a 70 eV)
-
LD: 105 (IBU), 160 (NPX), 160 (E1), 95,2
(E2) LQ: 500 (IBU,
NPX, E1, E2)
Nenhum analito >
35 Tabela 2.3- Dados de monitoramento de microcontaminantes em amostras ambientais (continuação)
Matriz Analitos Preparo de
amostra Derivatização Instrumental Análise Recuperação (%)
LD e LQ (ng/L)
Concentração encontrada
(ng/L) Referência
Água de
rio E1 E2, MeEE2 EE2
EFS: HLB (200 mg), 2 × 4 mL acetato de
etila
Derivatização: 125 µL piridina
+ 25 µL BSTFA: 1 %
TCMS
LVI-PTV-CG-EM (coluna HP5 MS, 30 m
× 0,25 mm × 0,25 µm; He a
1,0 mL/min; EI a 70 eV)
129 (E1), 105 (E2), 102 (EE2)
LD: 0,07 (E1), 0,05 (E2), 0,04 (EE2)
- BIZKARGUENAGA et al., 2012
Esgoto E1 E2 EE2
E3 BPA
4OP
EFS (HLB 200mg,
metanol) -
CLAE/ESI/EM (coluna Pursuit XRs Ultra-C18 50 mm x 2 mm x 2,8 µm; fase
móvel (A) água e (B) MeOH, ambos
com 0,1% ácido acético
glacial e 15 mM de acetato
de amônio.
82 (4NP), 79 (4OP), 82 (BPA), 81 (E1),
91 (E2), 88 (E3), 79 (EE2)
LD: 2,7 (4NP), 5,7 (4OP), 5,7 (BPA), 4,0 (E1), 3,3 (E2), 3,7 (E3), 2,8 (EE2)
9,7 (4NP), 6,1 (4OP), 13,4 (BPA), 16,3 (E2),
15,5 (E1), 22,2 (E3), 9,3 (EE2)
VEGA-MORALES et al., 2010
Esgoto e efluente de
estação
E1
E2 EE2 E3
EFS
(diclorometano/MeOH
(80/20)) -
CLAE/ESI/EM (coluna Alltima 25 mm x 4,6 mm x 5µm); fase móvel (A)
ACN e (B) água
Esgoto: 86 (E3), 88 (E2),
86 (EE2), 91 (E1) LQ: 0,6 (E3), 0,6 (E2), 0,9 (EE2), 0,2 (E3)
Esgoto: 70 (E3), 22 (E2), 2,9 (EE2), 132 (E1)
Efluente: 3,3 (E3), 2,9 (E2),
1,0 (EE2), 13 (E1)
36 Tabela 2.3- Dados de monitoramento de microcontaminantes em amostras ambientais (continuação)
Matriz Analitos Preparo de
amostra Derivatização Instrumental Análise Recuperação (%) LD e LQ (ng/L)
Concentração encontrada
(µg/L) Referência
Lodo ativado E1 E2 E3 EE2 BPA 4NP
EFS (HLB 50º mg, 10 mL
diclorometano/acetone (7:3))
50 µL piridina + 50 µL BSTFA+1%
TCMS (aquecimento 30’ a 60-70 oC
em banho ultrasônico)
CG/EM (coluna HP-5MS 30m x 0,25 mm x 0,25 µm; He a 1,5 mL/min; EI)
87,2 (4NP), 96 (BPA), 90,3 (E1), 96,3 (E2), 110,9 (EE2), 103,3 (E3) LQ: 30,3 (4NP), 0,2 (BPA), 1,2 (E1), 0,8 (E2), 4 (EE2),
2,3 (E3)
199,8 (4NP), 135,3 (BPA), ND (E1, E2), 6,3 (EE2), 17,6
(E3)
NIE et al., 2009 Esgoto e efluente de estação de tratamento 4OP 4NP BPA E1 E2 EE2
EFS (HLB 0,2 g, 10 mL de acetato de
etila)
50 µL piridina + 50 µL BSTFA+1%
TCMS (aquecimento
30’ a 60-70 oC)
CG/EM (coluna HP-5 30 m x 0,25
mm x 0,25 µm; He a 1,0 mL/min)
Efluente: 71,2 (4OP), 85,5 (4NP), 75,3 (BPA), 76,5 (E1), 82,7 (E2), 84,7 (EE2) - Esgoto: 8-65 (4OP), 0,2-0,8 (4NP), 0,1-8 (BPA), 0,3-41 (E1), 10-22 (E2), 0,5-5 (EE2) Efluente: 0,3-30(4OP), <0,2 (4NP), 0,1-12 (BPA), 0,3-17 (E1), 0,7-9 (E2), <0,5 (EE2)
37
Tabela 2.3- Dados de monitoramento de microcontaminantes em amostras ambientais (continuação)
Matriz Analitos Preparo de
amostra Derivatização Instrumental Análise Recuperação (%) LD e LQ (ng/L)
Concentração encontrada
(ng/L) Referência
Esgoto e efluente de estação de tratamento DCF IBU NPX CAF GEN PCT E1 E2 EE2 E3
EFS (HLB, 60 mg
3x 1 mL acetona) -
CLAE/DAD/Fl (coluna Zorbax Eclipse XDB-C18
150 mm x 4,6 mm x 5µm; fase móvel (A) ACN e (B) solução de 25
mM de dihidrogênio fosfato de potássio) - Esgoto: LD: 323 (E1) LQ: 67 (EE2),
145 (E2),
Efluente: LD: 162 (E1) LQ: 72 (E2)
Esgoto: 0,72 (DCF), 50,6 (IBU), 4,09 (NPX), 0,89 (CAF), <LQ (EE2, E1), 0,12 (E3), < LD (E1),
2,64 (GEN) Efluente: 0,53 (DCF), 3,74 (IBU), 2,58 (NPX), 0,24 (CAF), 0,12 (EE2), <LQ (E1),
0,59 (E3), <LD (E1), 3,07 (GEN)
MARTÍN et al., 2012
Efluente de estação de tratamento E1 E2 E3 PCT DCF IBU NPX GEN CAF
EFS (HLB, 10% MeOH/MTBE e
MeOH) -
CLAE/ESI/EM (coluna ZORBAX Eclipse XDB-C18 4,6 x 150 mm x 3,5 µm;
82 (BPA), 98 (OF), 72 (NF) 81 (E1),
109 (E2), 140 (E3), 103
(EE2), LQ: 0,088-5,07 0-27(PCT), 13-49 (DCF), 15-75 (IBU), 37-166 (NPX), 9-26 (GEN), 0-60 (CAF), 0-24 (E1),
ND (E3, E2)
38 Tabela 2.3- Dados de monitoramento de microcontaminantes em amostras ambientais (continuação)
Matriz Analitos Preparo de
amostra Derivatização Instrumental Análise Recuperação (%) LD e LQ (ng/L) encontrada (ng/L) Referência Concentração
Esgoto IBU PCT NPX DCF E1 E2 EE2 E3 EFS (HLB 200mg, Strata,
6 mL MeOH)
50 µL de piridina + 50 µL
BSTFA + 1%
TCMS, 60oC por
30’)
CG/EM (coluna Rtx-5 30 m x 0,25
mm x 0,25 µm; He a 2,0 mL/min
EI a 70 eV.)
102,4(IBU), 89,4 (PCT), 70,8 (NPX), 75,6 (DCF), 80,3 (E1),
68,2 (E2), 83,9 (EE2), 99,8 (E3)
LD: 6,6 (IBU), 7,6 (PCT), 16,9 (NPX), 52,9 (DCF), 8,5 (E1), 10 (E2), 8,1 (EE2), 6,8 (E3). LQ: 19,5 (IBU), 22,4 (PCT), 56,5 (NPX), 158,7 (DCF), 24,9 (E1), 29,3 (E2), 23,8 (EE2), 20 (E3)
280 (IBU), 240 (NPX), 460 (DCF),
120 (EE2), <LD (PCT, E1, E2, E3)
MIGOWSKA et al., 2012
PCT: Paracetamol DCF Diclofenaco IBU: Ibuprofeno NPX: Naproxeno GEN: Genfibrozila CAF: Cafeína BPA: Bisfenol A 4NP: 4-Nonilfenol 4OP: 4-Octilfenol E1: Estrona E2: 17 β Esradiol EE2: 17-α Etinilestradiol MeEE2: Mestranol E3: Estriol
EFS: Extração em fase sólida ELL: Extração líquido-líquido MEFS: Micro extração em fase sólida PFBBr: brometo de pentafluorobenzil MTBSTFA: N-metil-N-(terc- Butildimetiltrifluoroacetamida)
MSTFA: N-Metil-N-(trimetilsilil) trifluoroacetamida TMSI: trimetilsililimidazol
DTE: dithioerytrol ECF: cloroformiato de etila
BSTFA: N,O-bis (trimetilsilil) trifluoroacetamida TCMS: trimetilclorosilano
CLAE/EM: Cromatografia líquida de alta eficiência acoplada a espectrometria de massas
CG/EM: Cromatografia gasosa acoplada a espectrometria de massas
ESI: Ionização por eletrospray
CLUE: Cromatografia líquida de ultra eficiência LVI: large volume injection
PTV: programmed temperature vaporiser
DAD: Detector de arranjo de diodos Fl: Fluorescência
39
2.3.1 Técnicas cromatográficas
Nos últimos anos, muitos métodos para a análise de contaminantes emergentes em amostras de águas foram publicados. Dentre as técnicas instrumentais disponíveis para quantificação de perturbadores endócrinos e fármacos em amostras ambientais a cromatografia é sem dúvida a mais utilizada. A cromatografia é uma técnica físico-química de separação. Ela está fundamentada na migração diferencial dos componentes de uma mistura, que ocorre devido a diferentes interações, entre duas fases imiscíveis, a fase móvel e a fase estacionária. A grande variedade de combinações entre fases móveis e estacionárias a torna uma técnica extremamente versátil e de grande aplicação (DEGANI et al, 1998).
Cromatografia Líquida de Alta Eficiência (CLAE)
A cromatografia líquida de alta eficiência (CLAE) é o tipo mais versátil e mais amplamente empregado de cromatografia por eluição. Essa técnica é utilizada para separar e determinar espécies em uma grande variedade de materiais orgânicos, inorgânicos e biológicos. Na cromatografia líquida, a fase móvel é um solvente líquido, o qual contém a amostra na forma de uma mistura de solutos (SKOOG, 2005). Dentre os detectores para a CLAE podemos destacar absorbância no UV/Vis, fluorescência e, o mais recentemente usado, espectrômetros de massas.
As principais fontes de ionização empregadas em CLAE/EM são: ionização por eletronebulização (electrospray ionization, ESI), ionização química à pressão atmosférica
(atmospheric pressure chemical ionization, APCI). No entanto, tais métodos de ionização são
suscetíveis a efeitos de matriz, principalmente quando se trata de matrizes complexas como as ambientais, levando aos efeitos de supressão ou aumento do sinal analítico. Tem sido relatado que a ionização por APCI é menos sensível a efeitos de matriz que a ionização por eletrospray (WICK et al., 2010; BUCHBERGER, 2011).
Cromatografia Gasosa (CG)
40
interage com as moléculas do analito; sendo sua única função transportar o analito através da coluna (SKOOG, 2005).
Essa técnica é recomendada para amostras voláteis e termicamente estáveis. No entanto, reações de derivatização podem ser feitas para compostos não voláteis. A derivatização consiste em uma reação em que o peso molecular da amostra é aumentado pela substituição de um grupo proveniente do reagente derivatizante e seu ponto de ebulição é então diminuído pela redução na polaridade, tornando-se passível de análise por CG. Dentre
os vários reagentes derivatizantes podemos citar o pentafluorobenzil (PFBr), N,O-bis
(trimetilsilil) trifluoroacetamida (BSTFA) e o N
-(tert-butildimetilsilil)-N-metil-trifluoracetamida (MTBSTFA) que conduzem a formação de derivados contendo grupos
trimetilsilil (TMS) e tributilsilil (TBS).
Todavia, quando se deseja identificar e quantificar compostos, apenas a separação deles pela coluna cromatográfica e comparação dos tempos de retenção não é suficiente, tornando necessário o emprego de um detector. Vários são os detectores para a cromatografia gasosa os quais podemos citar: ionização em chama, condutividade térmica, captura de elétrons, espectrômetro de massas, termiônico, condutividade eletrolítica, fotoionização, infravermelho com transformada de Fourier. Neste trabalho foi adotada a cromatografia gasosa acoplada a espectrometria de massas (CG/EM).
2.3.2 Espectrometria de Massas (EM)
41
Figura 2.18- Diagrama de um espectrômetro de massas
As fontes de ionização em CG/EM produzem fragmentos, os quais podem também ser ionizados. Portanto, os íons das moléculas da amostra, denominados íons moleculares, íons de fragmentos e moléculas ionizadas, saem da fonte de ionização. As moléculas não-carregadas e os fragmentos são normalmente extraídos da fonte de íons através de bombas de vácuo empregadas para produzir o ambiente de baixa pressão. A próxima seção do espectrômetro de massas é o estágio analisador. O analisador serve para selecionar os íons de acordo com seus valores de massa carga (m/z). Os íons separados são então detectados e um gráfico contendo a intensidade do sinal gerado pelo íon versus m/z é produzido pelo sistema de dados (SKOOG, 2005).
A fonte de ionização do espectrômetro de massas utilizado neste trabalho é a ionização por elétrons (IE). Nessa fonte, as moléculas são bombardeadas com um feixe de elétrons de alta energia. Isso produz íons positivos (radicais cátions), íons negativos e espécies neutras. Os íons positivos são dirigidos para o analisador por repulsão eletrostática. Em IE, o feixe de elétrons é tão energético que muitos fragmentos são produzidos. Esses fragmentos, contudo, são muito úteis na identificação das espécies moleculares (SKOOG, 2005).
O modo de varredura do espectrômetro de massas é um requisito instrumental importante para que a análise seja realizada. O mais conveniente é a varredura em uma faixa de massas completa. Nesse modo SCAN, o espectrômetro realiza uma varredura sobre uma
42
Outro modo de varredura muito utilizado é o monitoramento seletivo de íon (SIM).
Nesse método o analisador de massas pode ser programado para amostrar um ou mais valor de m/z no decorrer da separação cromatográfica. No monitoramento de apenas um valor de m/z, a sensibilidade é aumentada em três ordens de magnitude, dependendo da faixa de massas, assim o aparelho não gasta tempo no registro de razões m/z que não correspondem aos compostos de interesse. Essa técnica é útil pata análise quantitativa de compostos alvos onde o pico base do anlito é normalmente escolhido para o monitoramento de m/z. A análise por SIM sintetiza a seletividade e sensibilidade do CG-EM (BECKER, 2012).
A espectrometria de massa acoplada à cromatografia gasosa e líquida são técnicas ideais para a determinação de contaminantes orgânicos em águas residuais devido ao recurso de separação do CG e CLAE atrelado a seletividade e sensibilidade do espectrômetro de massas. Este acoplamento da cromatografia com detecção de massa seletiva permite a determinação de muitos contaminantes em concentrações por partes por trilhão (ppt) ou inferiores (KANDA e GLENDINNING, 2011).
2.3.3 Métodos de preparação de amostras
Embora o uso de EM permita aumentar a sensibilidade, um procedimento de pré-concentração do analito é quase sempre necessário para atingir limites de detecção baixos o suficiente para determinar os níveis residuais em que os contaminantes emergentes estão presentes no ambiente (RODRIGUEZ-MOZAZ et al., 2007).
As técnicas mais utilizadas para extração ou pré-concentração de compostos são: extração líquido-líquido (ELL) ou liquid-liquid extraction (LLE), extração em fase sólida
(EFS) ou solid phase extraction (SPE), microextração em fase sólida (MEFS) ou solid phase microextraction (SPME) e extração com fluido supercrítico (EFS) ou supercritical fluid extraction (SFE).
A EFS baseia-se principalmente na imobilização física ou adsorção de certos compostos orgânicos na superfície de alguns sólidos orgânicos ou inorgânicos modificados ou não que são os suportes que preenchem o cartucho de extração. A seleção dos suportes é geralmente baseada nas propriedades dos analitos de interesse a serem extraídos (DAS et al.,
43
extraçao. Por isso, em alguns casos, é necessária a etapa de clean-up da amostra (BIZKARGUENAGA et al., 2012).
A microextração em fase sólida (MEFS) é uma técnica recentemente usada para análise de multirresíduos em amostras ambientais. O princípio da técnica é a extração de compostos a partir da adsorção destes em uma fibra (polímero ou sólido adsorvente) que recobre um tubo de fibra de vidro capilar. A quantidade do composto captada pela fibra é proporcional à sua concentração na amostra à medida que o equilíbrio é atingido com auxílio de agitação. Após a extração, a fibra de MEFS é transferida para a porta de injeção do CG, onde os compostos são dessorvidos (FATTA-KASSINOS et al., 2011). Para compostos
voláteis é feita a extração indireta (headspace), já que a fibra não entra em contato direto com a solução. A amostra é aquecida e os componentes voláteis são extraídos para a fibra pelo processo de sorção ou partição (OLIVEIRA et al., 2008).
O princípio da extração líquido-líquido (ELL) de dois líquidos imiscíveis (fase aquosa e fase orgânica) para a extração da substância de interesse se dá pelo coeficiente de partição do analito entre as duas fases imiscíveis. A eficiência da extração, portanto, depende da afinidade do soluto pelo solvente extrator e da razão entre as duas fases. No entanto, a ELL tem várias limitações tais como baixa recuperação, necessidade de um grande volume de amostra, baixa seletividade além da limitação para a extração de compostos hidrofílicos (KOLE et al., 2011). Uma variação da ELL convencional foi desenvolvida utilizando baixas
temperaturas para facilitar a partição de fases com polaridades próximas.
2.3.3.1 Extração líquido-líquido com partição em baixa temperatura (ELL-PBT) A partição em baixa temperatura foi primeiramente relatada por Anglin e McKinley (1960) que extraíram cera utilizando acetona a -70 oC durante o clean up de extratos de plantas para determinação de DDT (Dicloro-Difenil-Tricloroetano). Em 1997, Juhler extraiu organofosforados em matizes gordurosas da mesma forma, no entanto, a temperatura utilizada foi de -10 oC.