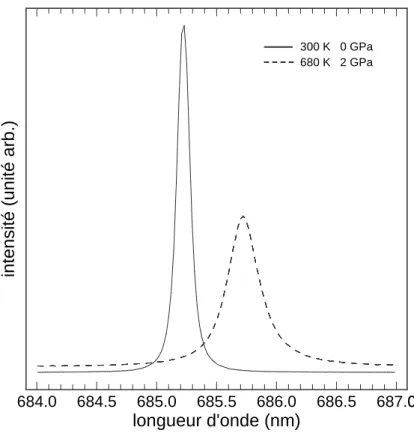
C'est donc un candidat idéal pour étudier l'évolution de la structure du liquide en fonction de la pression et rechercher une éventuelle transition liquide-liquide. L'évolution, en fonction de la pression et de la température, de la structure locale des différentes phases est présentée.
Les formes cristallines du chlorure de zinc
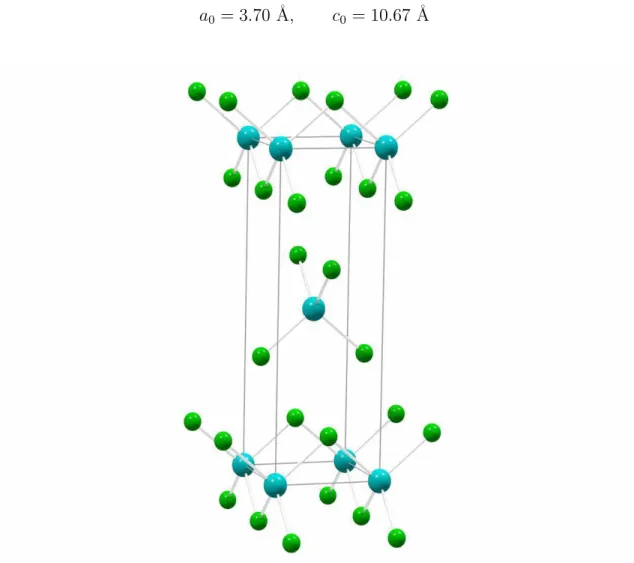
- Le chlorure de zinc t´etragonal : α-ZnCl 2
- Le chlorure de zinc monoclinique : β-ZnCl 2
- Le chlorure de zinc t´etragonal, lamellaire : γ-ZnCl 2
- Le chlorure de zinc orthorhombique : δ-ZnCl 2
- Le chlorure de zinc `a haute pression
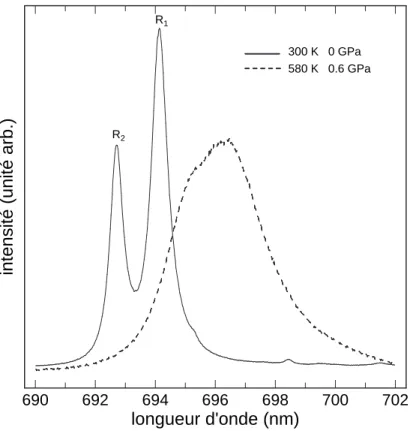
La partie inférieure de la figure 1.5 montre le spectre Raman de ZnCl2-xH2O à température ambiante. De même, le composé « hydraté » dont le spectre est présenté dans le panneau inférieur de la figure 1.5 a la structure γ-ZnCl2.
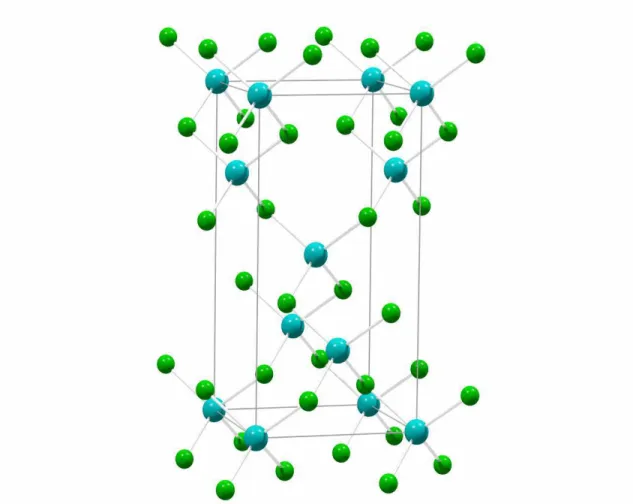
Les formes d´esordonn´ees du chlorure de zinc
Le chlorure de zinc vitreux
Des expériences de diffraction neutronique ont montré que la structure du chlorure de zinc vitreux consiste en un réseau compact et déformé d'ions Cl−, dans lequel les ions Zn2+ sont répartis de manière aléatoire dans des sites tétraédriques [10]. La faible température de transition vitreuse et le point de fusion du chlorure de zinc en font donc un modèle expérimental utile pour étudier et comprendre les propriétés physico-chimiques du système des verriers de type AB2, en fonction de la pression et de la température (Tg = 103) ˚ C et Tm = 293 ˚C).
Le chlorure de zinc liquide
Les auteurs identifient la phase cristalline résultante comme étant la phase cristalline à haute pression décrite par Sakai et al. Selon les mêmes auteurs, lors de la décompression, la phase haute pression persiste jusqu'à 1,1 GPa, après quoi elle se transforme en γ-ZnCl2.
Conclusion
Mais dans un premier temps, nous étudierons l’évolution de la phase vitreuse du chlorure de zinc en fonction de la pression et de la température. Lors de la compression, la cristallisation du chlorure de zinc vitreux se produit autour de 2,5 GPa.
Principe de fonctionnement
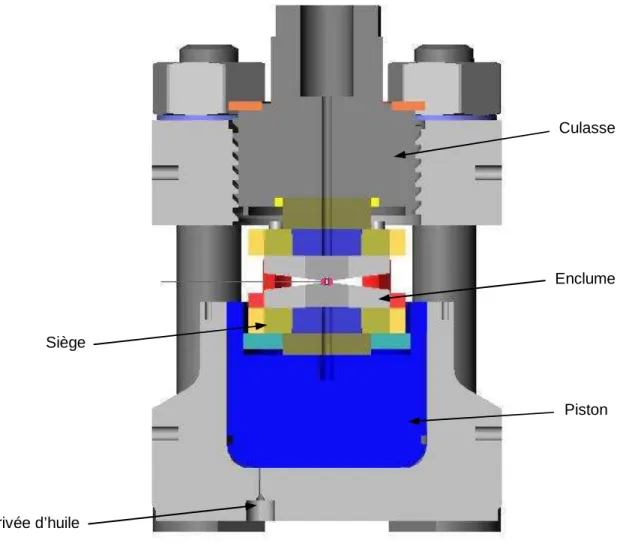
Le principe de base de la cellule à enclume en diamant est illustré dans la figure 2.1. Une enclume est placée sur le corps solide de la cellule, dans laquelle est monté un piston mobile.

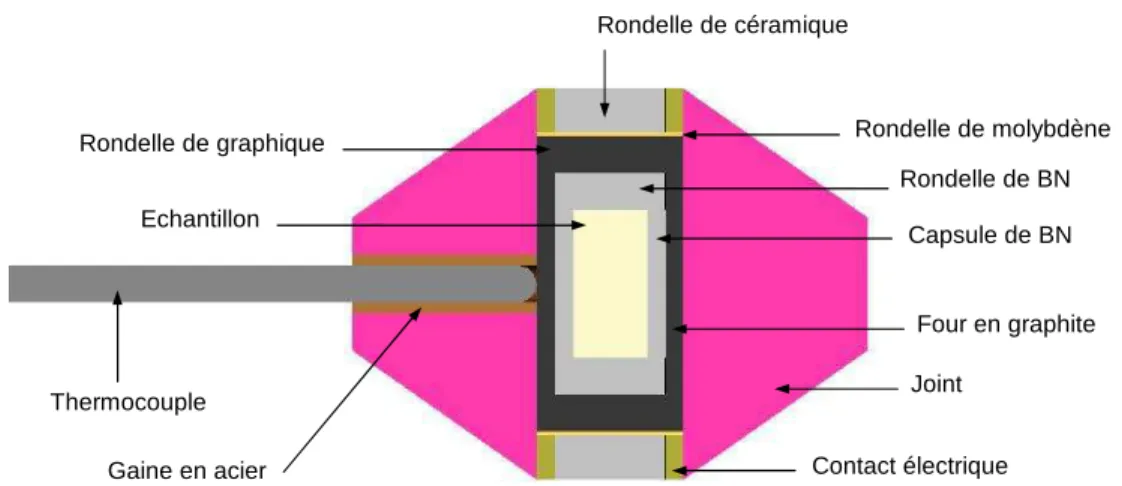
Environnement de l’´echantillon
Cette géométrie permet de réduire les contraintes sur les bords de la culasse, réduisant ainsi les gradients de pression dans la pierre. L'hydrostaticité de la pression sur l'échantillon dépendra largement des propriétés mécaniques du milieu de transfert.
Les dispositifs chauffants
La cellule à enclume de diamant (DAC). du dessus) Manchon chauffant support CED. Cependant, le temps de stabilisation de la température de l'échantillon (au cœur du CED) reste très long (de l'ordre de 2 heures par 100 ˚C en travaillant sous vide).

Chargement de la CED
Après avoir emballé la poudre, la cellule est hermétiquement scellée avec une enclume en diamant puis retirée de la boîte à gants. Il est donc très difficile de trouver un fluide de transfert de pression qui ne réagisse pas avec l’échantillon pouvant être chargé dans la boîte à gants.
L’enceinte `a vide
La pression maximale n'étant pas très élevée, lors de ce travail on peut considérer que l'échantillon a été soumis à une pression relativement hydrostatique. Lorsque le CED est placé dans le boîtier, ses faces supérieure et inférieure font face aux fenêtres en mylar.
La presse Paris-Edimbourg
- Principe de fonctionnement
- Environnement de l’´echantillon
- Chargement du joint
Au cours de ces travaux, toutes les expériences réalisées avec une presse Paris-Edimbourg ont nécessité un chauffage de l'échantillon. Il a donc fallu charger l'échantillon et récupérer les différents éléments dans une boîte à gants puis l'utiliser.
Mesure de la pression
- Les jauges de luminescence
- Les jauges Raman
- Les jauges pour rayons X
L'idéal serait donc un luminescencemètre dont la longueur d'onde caractéristique ne varierait pas ou peu avec la température. Au cours de ces travaux, nous avons mesuré le décalage du mode Raman du diamant en fonction de la température.
Mesure de la temp´erature
- La mesure de temp´erature par thermocouple
- Utilisation du couple (rubis, SrB 4 O 7 : Sm 2+ )
- Diffusion Raman du diamant
Ceci montre donc que l'hydratation du chlorure de zinc conduit à l'acquisition de la phase γ-ZnCl2, à pression et température ambiantes. Chlorure de zinc vitreux à haute pression et haute température. a) : ajustement du signal EXAFS de la phase cristalline basse pression (après décompression) P = 0,5 GPa.

Principe du rayonnement synchrotron
Le rayonnement synchrotron est assuré par un anneau de stockage, dans lequel les électrons circulent à une vitesse proche de celle de la lumière. Les électrons sont soumis à l’action d’un champ magnétique pour infléchir leur trajectoire, et ainsi subir une accélération centripète. Ce rayonnement est émis dans la direction de déplacement de la particule chargée, qui suit la ligne tangente à sa trajectoire.
Capté à différents endroits de l’anneau, le rayonnement synchrotron est dirigé vers les lignes lumineuses.
Int´erˆet du rayonnement synchrotron lors de mesures sous condi-
Diffraction des rayons X
- Principe
- Dispositif exp´erimental en dispersion d’´energie
- Traitement des donn´ees
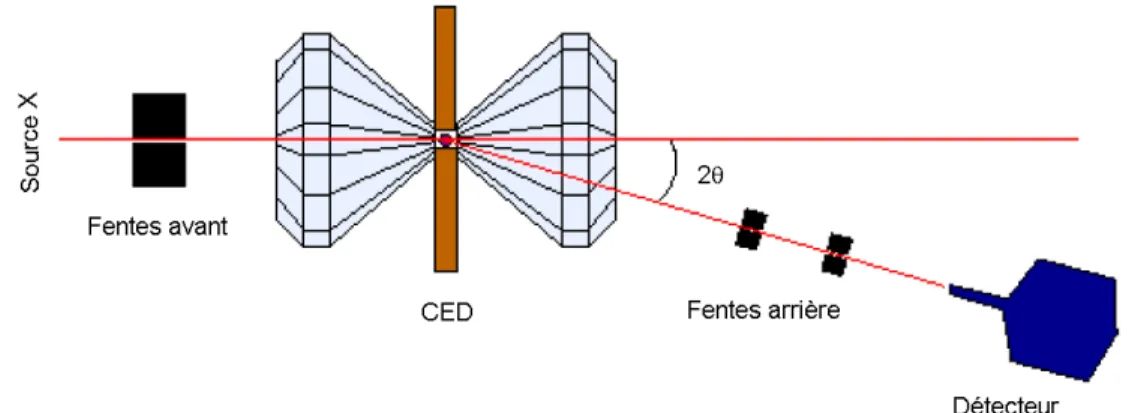
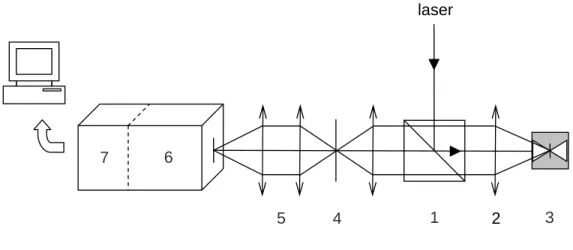
Ce problème peut être résolu en considérant les intensités relatives des pics : pour la réflexion de Bragg, l'amplitude de l'onde diffractée est donnée par l'expression,. D’après l’équation (3.1), deux options s’offrent à l’expérimentateur : travailler à E (ou λ) constant et étudier la diffraction en fonction de l’angle θ (dispersion angulaire) ; ou déterminer θ et effectuer des mesures dépendantes de l'énergie (dispersion d'énergie). La figure 3.2 présente une configuration expérimentale standard pour une expérience de diffraction des rayons X à dispersion d'énergie dans une cellule à enclume en diamant.
Le faisceau collimaté sur l'échantillon est courbé d'un angle fixe 2θ défini par un banc rotatif et un ensemble de fentes situées en aval de l'échantillon. Ce parallélépipède représente le volume examiné par le faisceau de rayons X lors de l'expérience.
Spectroscopie d’absorption des rayons X
- Principe de la SAX
- Formalisme de l’EXAFS
- Dispositifs exp´erimentaux
- Traitement des donn´ees
Le principe de base de la spectroscopie d'absorption des rayons X est l'excitation des électrons profonds (K ou L) d'un atome, grâce à l'absorption d'un photon de même énergie que le seuil K ou L de l'atome. SAX consiste donc à mesurer le spectre d'absorption des photons X à travers la matière, en fonction de l'énergie du rayonnement incident. Dans le cas de l'absorption des rayons X, l'interaction rayonnement-matière peut être traitée comme une faible perturbation de l'hamiltonien du système.
La première étape du traitement des données consiste donc à « calibrer » les spectres, afin d'obtenir l'absorption en fonction de l'énergie des photons incidents. Au contraire, les expériences EXAFS classiques fournissent directement des spectres d'absorption en fonction de l'énergie.
Spectroscopie Raman
- Principe
- Dispositif exp´erimental
- Traitement des donn´ees
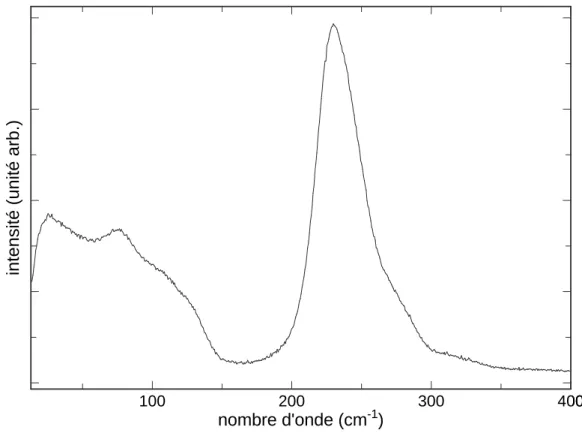
Pour le caractériser de manière univoque, nous avons réalisé un spectre Raman (Figure 4.1) et un spectre de diffraction des rayons X (Figure 4.2) de l'échantillon dans le CED. Une des premières conclusions que l’on peut donc tirer est que le spectre Raman de la figure 4.1 correspond bien à la phase du chlorure de zinc de structure orthorhombique : δ-ZnCl2. La figure 4.3 montre l’évolution de l’échantillon cristallin lorsqu’il est laissé en contact avec l’air puis chauffé juste en dessous de la température de fusion (Tf = 293˚C).
En revanche, lorsque l'échantillon est exposé à l'air, le spectre Raman obtenu est caractéristique de la phase γ-ZnCl2. le spectre central de la figure 4.3). L'intensité des pics dans le spectre supérieur de la figure 4.3 est atténuée en raison de la température élevée de l'échantillon, mais pas du tout.
Le chlorure de zinc vitreux `a haute pression et haute temp´erature
- Caract´erisation par diffusion Raman
- Cristallisation sous pression
- Effet de la temp´erature
- Conclusion
Si le spectre correspond à celui de la figure 4.4, cela signifie que l'échantillon est effectivement déshydraté. On peut donc réaliser des expériences à haute pression et haute température, tout en étant sûr de la nature de l'échantillon étudié. Ces conditions ressemblent fortement à celles de la phase haute pression trouvée par Sakaiet al.
Sur la figure 4.13, nous avons reconstitué le spectre enregistré à P = 2,5 GPa en combinant le spectre de la phase vitreuse et le spectre de la phase cristalline haute pression. Autour de la pression de transition, il existe une bonne coexistence de la phase vitreuse et de la phase cristalline haute pression.
Transition de phase du compos´e cristallin `a haute pression
- Mesures structurales
- Etude vibrationnelle
- Effet de la temp´erature
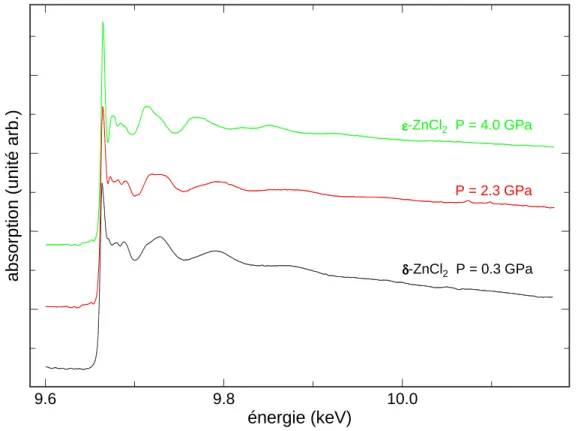
Ils observent une première transition à 2,1 GPa, lors de la compression, de la phase α-ZnCl2 vers une phase cristalline haute pression. Sur la figure 4.15, nous présentons trois spectres d'absorption à différentes pressions, lors d'une compression à température ambiante. De plus, on remarque que, lors de la transition, la distance moyenne du premier voisin (Zn-Cl) montre un saut positif, tandis que le saut est négatif pour la distance moyenne du deuxième voisin (Zn-Zn).
La pression de transition lors de la compression du δ-ZnCl2 est comprise entre 2,6 et 3,1 GPa. La phase haute pression obtenue est la même qu'en compression α, γ ouv-ZnCl2.
Le chlorure de zinc liquide `a haute pression
- Mesures en cellule `a enclumes de diamant
- Mesures en presse Paris-Edimbourg
En effet, cette distance diminue légèrement lorsque la pression et la température augmentent. Ensuite, lorsqu'on augmente la température tout en maintenant P = 2,3 GPa, on obtient un spectre d'absorption qui ressemble beaucoup à celui de la phase vitreuse ou liquide tétracoordonné (voir paragraphes 4.2.2 et 4.3.3). En revanche, si on baisse la température, l'échantillon redevient cristallin et on retrouve le spectre d'absorption de la phase ǫ-ZnCl2, ainsi que son spectre de diffraction.
Dans notre cas, l'évolution de cette énergie en fonction de la température doit témoigner de la transition entre la phase ǫ-ZnCl2. De plus, les courbes α(T) se chevauchent complètement à mesure que la température augmente puis diminue.
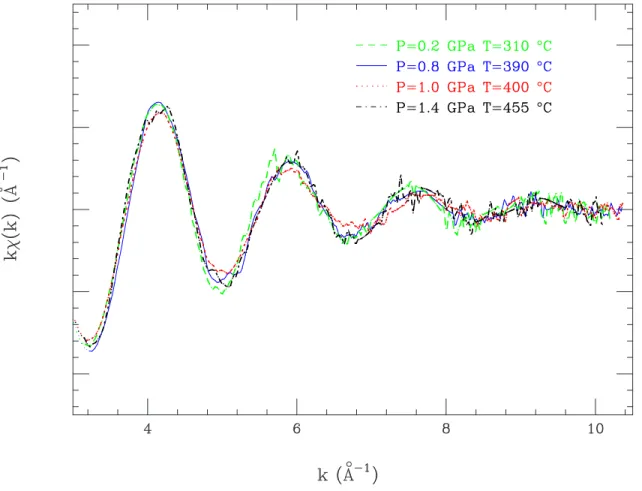
Diagramme de phase de ZnCl 2
- Domaines de stabilit´e des phases solides
- Courbe de fusion
- Conclusion
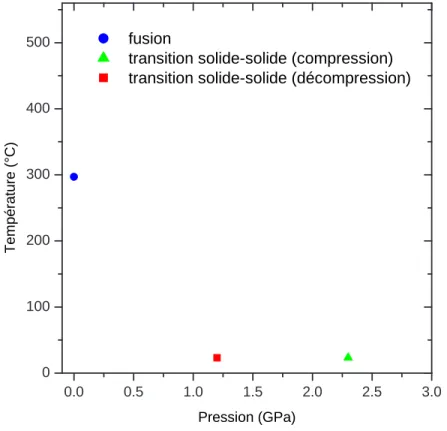
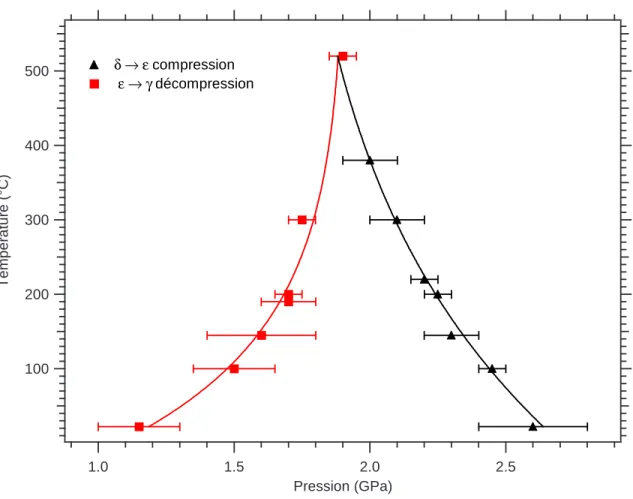
Les résultats obtenus lors de la compression (δ-ZnCl2 → ǫ-ZnCl2) et lors de la décompression (ǫ- ZnCl2 →γ-ZnCl2) sont en accord avec ceux obtenus en CED. Les points de la courbe de fusion deδ-ZnCl2 ont été obtenus selon trois méthodes : 1. Les expériences réalisées avec la presse Paris-Edimbourg visaient à déterminer la courbe de fusion dans le domaine de la phase ǫ-ZnCl2 déterminer
Si l'on étudie le chlorure de zinc déshydraté, cette phase présente une structure orthorhombique lors de la première compression (δ-ZnCl2) ou une structure tétragonale lamellaire lors de la décompression (γ-ZnCl2). Une étude de l'évolution de la phase vitreuse du ZnCl2 en fonction de la pression à température ambiante n'a montré aucune transition de phase vers un verre de haute densité.
Spectres Raman de ZnCl 2 cristallin, contenant diff´erentes quantit´es
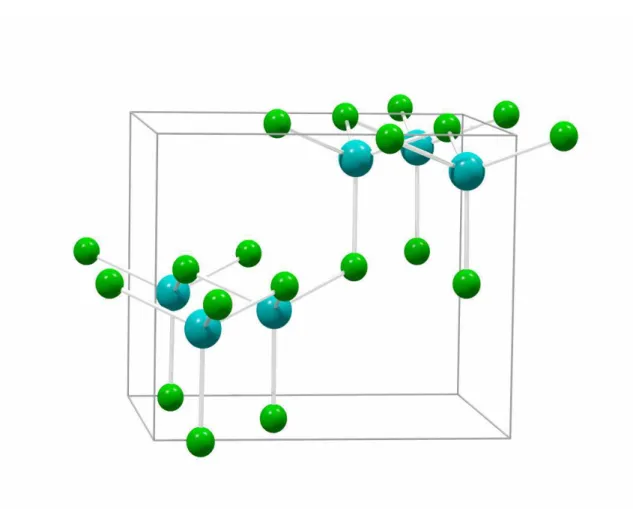
Structures propos´ees pour la phase haute pression de ZnCl 2
Chlorure de zinc vitreux mod´elis´e par la m´ethode Reverse Monte Carlo
Simulation de ZnCl 2 fondu [24]
Diagramme de phase de ZnCl 2 ant´erieur `a ce travail
Sch´ema d’une CED `a membrane
Caract´eristiques des diamants taill´es pour une CED. C : culasse, X
Coeur d’une cellule `a enclumes de diamants
Photo d’une CED envelopp´ee d’un manchon chauffant, branch´e au