1
UNIVERSIDADE FEDERAL DO CEARÁ
CENTRO DE CIÊNCIAS
DEPARTAMENTO DE QUÍMICA ORGÂNICA E INORGÂNICA
PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA
ELAYNE BESSA FERREIRA PINHEIRO
ESTUDO QUÍMICO, BIOLÓGICO E
IN SILICO
de
PLECTRANTHUS GRANDIS (CRAMER) WILLENSE
2
ELAYNE BESSA FERREIRA PINHEIRO
ESTUDO QUÍMICO, BIOLÓGICO E
IN SILICO
de
PLECTRANTHUS GRANDIS (CRAMER) WILLENSE
5
À DEUS
6
AGRADECIMENTOS
Aos meus pais, Everton e Mércia meus eternos incentivadores, sem eles este grande sonho não teria sido realizado. Agradeço aos meus irmãos Emerson e Elana pelo carinho e torcida.
Ao meu marido Bosco Filho e aos meus filhos Rian e Renan, pela paciência e compreensão nos meus momentos de ausência e pelo o amor dedicado e incondicional que me ajuda a continuar trilhando o meu caminho.
A minha sogra Marilene por ter dedicado parte de seu tempo para me ajudar a cuidar de meu filho Renan com carinho e amor nos momentos de minha ausência.
A Profa. Dra. Maria Goretti de Vasconcelos Silva, orientadora deste trabalho, pela oportunidade, incentivo, orientação e confiança. Seus exemplos de dedicação ao trabalho proporcionaram valorosos ensinamentos, os quais foram fundamentais para o desenvolvimento e conclusão deste projeto.
A minha amiga Carol por ter cedido o espaço no Instituto Federal de Educação, Ciência e Tecnologia do Ceará (IFCE) para a elaboração de parte desse trabalho e por sua coorientação para o desenvolvimento do mesmo.
A minha amiga e irmã Juliana pela amizade, estímulo e paciência nestes anos. A minha amiga Irvila pela realização dos ensaios biológicos desse trabalho no DKFZ (German Cancer Research Center).
A minha amiga Jack pela sua ajuda no capitulo de ensaio in silico e aos meus
amigos que já não fazem mais parte do Laborátorio de Produtos Naturais e Biotecnologia, que de uma forma ou outra tiveram sua parcela de contribuição para o desenvolvimento do projeto.
Ao meu amigo, Sales pela disponibilidade da ajuda na coleta do material botânico utilizado em meu projeto.
Aos professores membros da banca pela participação e por contribuírem com a conclusão deste trabalho.
7
RESUMO
A utilização de plantas com fins medicinais é uma das mais antigas formas de práticas da humanidade para tratar as diversas enfermidades. A espécie selecionada cujo estudo é relatado nesse trabalho foi Plectranthus grandis (Cramer) Willense que é um
arbusto popularmente conhecido no Brasil pelo nome de "boldo grande". Esse trabalho compreende a descrição dos procedimentos utilizados no isolamento e determinação estrutural dos compostos isolados de Plectranthus grandis, bem como o estudo da
variação sazonal e circadiana da barbatusina, composto farmacologicamente ativo presente em P. grandis, através da implementação e validação de um método analítico
capaz de detectar e quantificar este metabólito. O método desenvolvido por CLAE foi realizada com uma coluna Phenomenex C18 (250 mm x 4,60 mm - 5 µm), um gradiente binário de água e acetonitrila (8: 2, v / v) a um fluxo de 0,8 mL/ min o mesmo mostrou-se simples, exato, preciso e mostrou-seletivo, podendo mostrou-ser rotineiramente aplicado para a quantificação de barbatusina em amostras de P. grandis em qualquer época do ano,
sendo detectada em maior teor no horário de 0 hr e no mês março. Adicionalmente, foi realizado um estudo in silico para a determinação do potencial anti-malárico,
antitumoral e anti-inflamatório através de ensaios de docagem molecular, descritores moleculares e físico-químicos de uma base de dados implementada com todos os compostos isolados até o presente momento do gênero Plectranthus, onde o diterpeno
plecostonol destaca-se como sendo o mais promissor candidato a fármaco dentre os 270 compostos identificados. Ensaios químicos e biológicos (atividade antioxidante, determinação de polifenóis e de flavonoides, inibição da enzima conversora de angiotensina I e ensaio para inibição da enzima acetilcolinesterase) também foram realizados com o extrato etanólico da espécie em estudo e com a barbatusina onde ambos apresentaram uma baixa atividade ou nenhuma atividade o que não descarta a possibilidade de outros estudos.
Palavras-chave: Plectranthus grandis, barbatusina, ensaio in silico, ensaios químicos e
8
ABSTRACT
The use of plants for medicinal purposes is one of the oldest forms of human practices to treat various diseases. The selected species whose study is reported in this work was
Plectranthus grandis (Cramer) Willense which is popularly known bush in Brazil as the
"boldo-grande". This work includes the description of the procedures used in the isolation and structural determination of isolated Plectranthus grandis compounds and
the study of seasonal and circadian variation of barbatusin composed pharmacologically active present in P. grandis, through the implementation and validation of an analytical
method able to detect and quantify this metabolite. The method developed by HPLC was performed using a Phenomenex C18 column (250 mm x 4.60 mm - 5 µm), a binary gradient of water and acetonitrile (8: 2, v / v) at a flow rate of 0.8 mL / min it proved to be simple, accurate, precise and selective and can be routinely applied for the quantification of barbatusin in P. grandis samples at any time of year and is found in
higher concentration in the 0 hr time and the month March. Additionally, a study was performed in silico to determine the antimalarial potential, antitumor and
anti-inflammatory by molecular docking assays, molecular and physico-chemical descriptors in a database implemented with all compounds isolated to date Plectranthus the genus
where the diterpene plecostonol stands out as the most promising drug candidate among the 270 identified compounds. Chemical and biological assays (antioxidant activity determination of polyphenols and flavonoids, inhibition of angiotensin-converting enzyme I and assay for inhibition of the enzyme acetylcholinesterase) were also performed with the ethanol extract of the species under study and the barbatusin where both showed low activity or any activity which does not rule out the possibility of other studies.
Keywords: Plectranthus grandis, barbatusin, in silico testing, chemical and biological
9
LISTA DE TABELAS
Tabela 1: Compostos químicos isolados de espécies do gênero Plectranthus 9
Tabela 2: Representação estrutural dos compostos químicos isolados das espécies do gênero Plectranthus
28
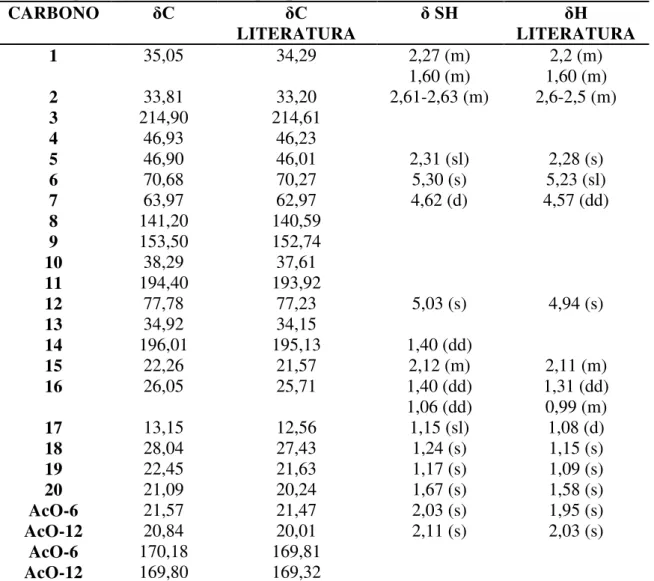
Tabela 3: Valores de deslocamentos dos carbonos e hidrogênios para PG2 45 Tabela 4– Deslocamento químico de RMN 13C de PG3 comparados com os dados da literatura
47
Tabela 5: Teor de Extrativos (g de extrato/100g de folha seca) 53 Tabela 6: Teor de Barbatusina (mg de barbatusina/g de extrato) 53 Tabela 7: Resultados da curva analítica da Barbatusina 55
Tabela 8: Precisão Intradia 55
Tabela 9: Precisão Interdia 56
Tabela 10: Percentuais de recuperação da barbatusina em Plectranthus grandis 57
Tabela 11: Dados do estudo da robustez do método recentemente desenvolvido 58
Tabela 12: Avaliação da atividade antioxidante por três metodologias 59 Tabela 13: Resultados do teor de polifenóis e de flavonoides 61 Tabela 14: Resultado do ensaiode inibição da enzima acetilcolinesterase 63 Tabela 15: Dados oriundos do tratamento cromatográfico de EEPG 67 Tabela 16: Gradiente da fase móvel utilizada na extração em fase sólida das frações de P. grandis utilizando C18
67
Tabela 17: Condições Cromatográficas realizadas 72
Tabela 18: Condições cromatográficas do ensaio da ECA 80
Tabela 19: Descritores fisico-químicos dos compostos candidatos a fármacos isolados do gênero Plectranthus
86
Tabela 20: As pontuações de acoplamento de resíduos específicos de sistemas
de Qi-ligantes e Qo-ligantes 105
Tabela 21: As pontuações de acoplamento de resíduos específicos de sistemas de COX-1-ligantes e COX-2-ligantes
107
Tabela 22: As pontuações de acoplamento de resíduos específicos de sistemas
10
LISTA DE FIGURAS
Figura 1: Representação estrutural da barbatusina 2
Figura 2: Registro fotográfico de Plectranthus grandis (Cramer) Willense 5
Figura 3: Biossíntese de terpenos via mevalonato 7
Figura 4: Estrutura dos núcleos diterpênicos mais comuns encontrados em
Plectranthus spp.
8
Figura 5: Evolução dos relatos científicos do gênero Plectranthus 8
Figura 6: Perfil biofarmacológico de Plectranthus spp. 28
Figura 7: Representação Estrutural da α-amirina e β-amirina 44
Figura 8: Representação estrutural do Lupeol 46
Figura 9: Representação Estrutural da Barbatusina 48
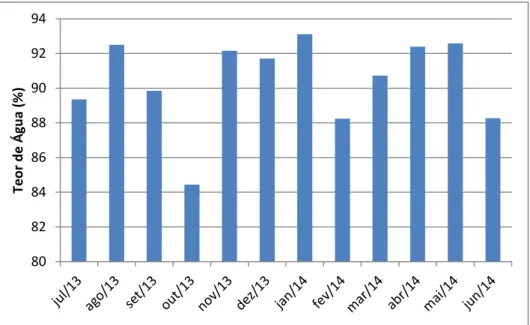
Figura 10: Teor de água nas folhas de P. grandis 49
Figura 11: Umidade do ar no período de 24 hs 49
Figura 12: Temperatura no período de 24 hs 50
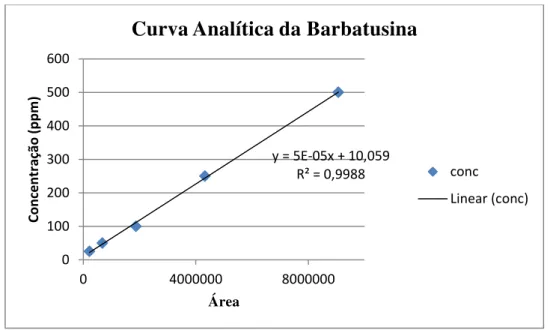
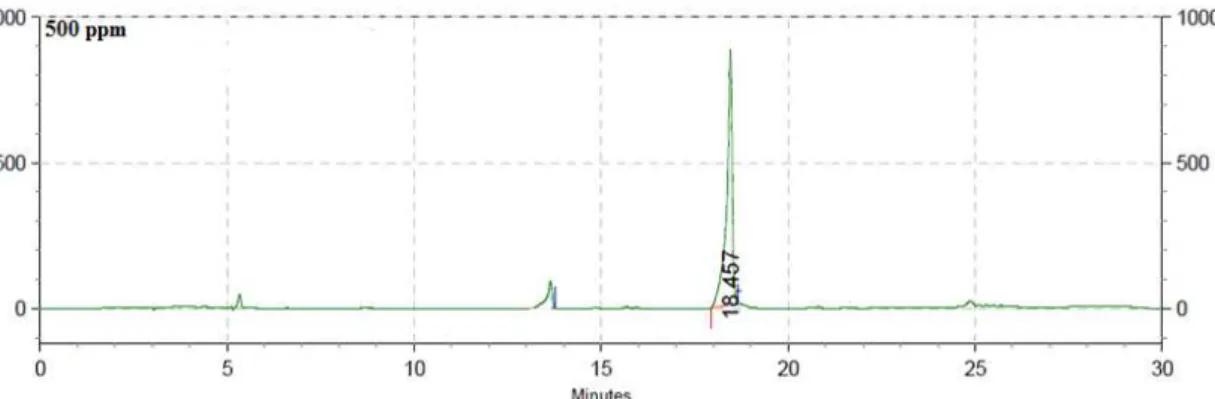
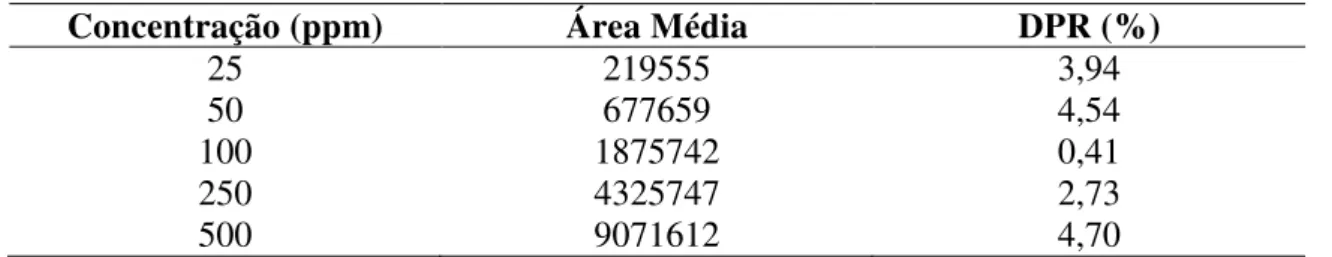
Figura 13: Curva Analítica da Barbatusina obtida por CLAE 51 Figura 14: Cromatogramas CLAE representativos, gerados para a obtenção da curva analítica da barbatusina
52
Figura 15: Variabilidade quantitativa de Barbatusina nos ciclos circadiano e
sazonal 54
Figura 16: Avaliação da Atividade Antioxidante frente ao radical livre DPPH 60 Figura 17: Reação genérica entre o radical livre DPPH e um antioxidante 77 Figura 18: Redução do complexo TPTZ (2,4,6-tri(2-piridil)-1,3,5-triazina) com Fe3+
78
Figura 19: Reações envolvidas no ensaio de inibição da acetilcolinesterase 81 Figura 20: a) Poses de ligação previstas para o composto 258 no sítio ativo Qi do citocromo bc1; b) As interações entre resíduos no local de ligação 258 e Qi
(código PDB 4D6T)
104
Figura 21: a) Poses de ligação previstas para o composto 35 no sítio ativo Qi do citocromo bc1; b) As interações entre resíduos no local de ligação 35 e Qi
(código PDB 4D6T)
104
Figura 22: a) Poses de ligação previstas para o composto 72 no sítio ativo COX-2; b) As interações entre resíduos no local de ligação 72 e COX-2 (código PDB 1CX2)
11 Figura 23: a) Poses de ligação previstas para o composto 268 no sítio ativo Src; b) As interações entre resíduos no local de ligação 268 e Src (código PDB 1CX2)
108
Figura 24: a) Poses de ligação previstas para o composto 72 no sítio ativo GLUT-1; b) As interações entre resíduos no local de ligação 72 e GLUT-1 (código PDB 4PYP)
109
Figura 25: Representação estrutural e respectivas nomenclaturas dos compostos candidatos a fármacos com melhor desempenho na triagem virtual
12
LISTA DE FLUXOGRAMAS
Fluxograma 1 – Obtenção e isolamento de PG1 e de PG2 a partir de PGFH e PGFD
69
13
LISTA DE ABREVIATURAS
CLAE Cromatografia líquida de alta eficiência
ABNT Associação Brasileira de Normas Técnicas
HMG-CoA 3-hidróxi-3-metilglutaril-CoA
IPP isopentenil-pirofosfato
DMAPP dimetilalilpirofosfato
GPP geranil difosfato
FPP farnesil difosfato
GGPP geranilgeranil difosfato
RMN 1H Ressonância Magnética Nuclear de Hidrogênio Deslocamento químico
RMN 13C Ressonância Magnética Nuclear de Carbono 13
ICH International Conference on Harmonisation
ANVISA Agência Nacional de Vigilância Sanitária
AOAC Association of Official Analytical Chemists
LD Limite de Detecção
LQ Limite de Quantificação
DPR Desvio padrão relativo
DPPH 2,2-difenil-1-picril-hidrazila
FRAP Ferric Reducing Antioxidant Power
ORAC Oxygen Radical Absorbance Capacity
EEPG Extrato etanólico das folhas de Plectranthus grandis
FeIII-TPZ Complexo férrico-tripiridiltriazina FeII-TPZ Complexo ferroso-tripiridiltriazina
ECA Enzima conversora de angiotensina I
SRA Renina-angiotensina
IECA Inibidores da ECA
HHL Hipuril-histidil-leucina
AChE Enzima acetilcolinesterase
UFC Universidade Federal do Ceará
CCD Cromatografia de adsorção em camada delgada
14
TPTZ 2,4,6-tri(2-piridil)-1,3,5-triazina
AAPH 3,3‟-azo-bis-(2-amidinopropano)-diidroclorodo
DMSO Dimetilsulfóxido
ATCI iodeto de acetilcolina
DTNB ácido 5,5‟-Ditiobis-2-nitrobenzóico
PSA Área de superfície polar
Log P Partição de uma substância entre as fases aquosa e orgânica no sistema água/octanol
nON Número de grupos aceptores de ligação de hidrogênio
nOHNH Número de grupos doadores de ligação de hidrogênio
log S Solubilidade
ADME Absorção, Distribuição, Metabolização e Excreção
GLUT-1 Proteína transportadora de glucose
MPO Enzima mieloperoxidase
Src proteína tirosina quinase
COX-1 Enzima ciclo-oxigenase-1
15
SUMÁRIO
CAPÍTULO 1
1-INTRODUÇÃO 1
CAPÍTULO 2
2-CONSIDERAÇÕES BOTÂNICAS 4
2.1- A Família Lamiaceae e o Gênero Plectranthus 4
2.2- Plectranthus grandis (Cramer) Willense 5
CAPÍTULO 3
3- QUIMIODIVERSIDADE E PERFIL BIOFARMACOLÓGICO DE
PLECTRANTHUS spp.
6
CAPÍTULO 4
4-RESULTADOS E DISCUSSÃO 43
4.1- Determinação dos constituintes fixos de Plectranthus grandis (Cramer)
Willense
43
4.1.1- Determinação estrutural de PG1 43
4.1.2- Determinação estrutural de PG2 44
4.1.3- Determinação estrutural de PG3 46
4.2- Estudo da Variação Sazonal e Circadiana da Barbatusina nas amostras de
P. grandis por Cromatografia Líquida de Alta Eficiência (CLAE)
48
4.2.1- Análises do teor de água e dos dados de temperatura e umidade relativa 48 4.2.2-Análise da composição química dos extratos obtidos dos ciclos sazonais e
circadianos
50
4.3-Validação do método 54
CAPÍTULO 5
5-ATIVIDADES QUÍMICAS E BIOLÓGICAS 58
5.1-Atividade Antioxidante 58
5.2-Determinação de polifenóis e de flavonoides 61
5.3-Inibição da enzima conversora de angiotensina I (ECA) 62 5.4- Ensaio para inibição da enzima acetilcolinesterase 63 CAPÍTULO 6
16
6.1- Material Botânico 64
6.1.1-Coleta 64
6.1.1.1-Estudo químico e Isolamento de metabólitos secundários 64 6.1.1.2- Estudo da Variação Sazonal e Circadiana da Barbatusina 64
6.2-Técnicas Espectroscópicas 64
6.3- Ponto de fusão 65
6.4- Estudo dos constituintes fixos de Plectranthus grandis 65
6.4.1- Extração em fase sólida 65
6.4.2- Cromatografia em Camada Delgada (CCD) 66
6.4.3- Cromatografia em Coluna por Adsorção 66
6.4.4-Fracionamento preliminar do extrato etanólico das folhas de P. grandis 67
6.4.5-Isolamento de PG1 e PG2 a partir de PGFH e PGFD 67
6.4.6-Isolamento de PG3 a partir de PGFA 69
6.5- Estudo da Variação Sazonal e Circadiana da Barbatusina no extrato
etanólico das folhas de P. grandis por Cromatografia Líquida de Alta Eficiência
(CLAE)
71
6.5.1- Condições cromatográficas utilizadas 71
6.5.2-Preparação das amostras (Clean-up) 71
6.5.3- Quantificação da barbatusina 73
6.5.3.1-Validação do Método 73
6.6-Avaliação do Potencial Biológico do extrato de P. grandis 76
6.6.1-Atividade Antioxidante 76
6.6.1.1-Ensaio Antioxidante frente ao radical livre DPPH 76 6.6.1.2- Ensaio Antioxidante FRAP (Ferric Reducing Antioxidant Power) 77 6.6.1.3- Ensaio Antioxidante ORAC (Oxygen Radical Absorbance Capacity) 78
6.6.2- Determinação dos polifenóis 79
6.6.3-Determinação dos flavonoides 79
6.6.4- Potencial de Inibição da enzima conversora de angiotensina I (ECA) 80 6.6.5- Ensaio para inibição da enzima acetilcolinesterase 80 CAPÍTULO 7
7-ENSAIO IN SILICO DOS CONSTITUINTES ISOLADOS DO GÊNERO PLECTRANTHUS
82
17
7.2-Resultados e Discussão 84
7.2.1-Avaliação dos parâmetros farmacocinéticos 84
7.2.2-Ensaios de docking 103
CAPÍTULO 8
8- CONSIDERAÇÕES FINAIS 112
CAPÍTULO 9
9-REFERÊNCIAS BIBLIOGRÁFICAS 113
18
1-INTRODUÇÃO
A utilização de plantas com fins medicinais é uma das mais antigas formas de práticas da humanidade para tratar as diversas enfermidades (VEIGA Jr. & MACIEL, 2005). Estas práticas contribuem de forma significativa para divulgar as potencialidades terapêuticas dos vegetais, sendo descritas com frequência, mesmo que grande parte das plantas utilizadas popularmente não tenha ainda seus metabólitos secundários conhecidos (MACIEL et al., 2002) e propriedades medicinais comprovadas.
Em plantas, metabólitos secundários consistem em classes de compostos produzidos por diferentes vias biossintéticas cuja variabilidade qualitativa e quantitativa é fortemente suscetível a influências ambientais e potenciais predadores naturais (PAVARINIA et al., 2012). A produção desses compostos pode sofrer modificações de acordo com a interação de processos bioquímicos, fisiológicos, ecológicos e evolutivos que dependem das condições ambientais (GOBBO-NETO & LOPES, 2007). Dentre os diversos fatores que controlam a síntese dos metabólitos secundários, dois efeitos distintos podem ser determinados, o abiótico e o biótico. Efeitos abióticos incluem todos os efeitos físicos do habitat. Já os efeitos bióticos estão relacionados tanto às interações de plantas com micro-organismos ou aspectos fisiológicos da planta (PAVARINIA et al., 2012). Os principais fatores que influenciam a dinâmica dos metabólitos são os ciclos sazonais, circadianos e fenológicos, latitude, altitude, disponibilidade hídrica e de nutrientes, nível de radiação, poluição atmosférica, indução por estímulos mecânicos, herbivoria e ataques por patógenos. Há um grande número de estudos sobre a influência destes fatores na produção de metabólitos secundários, ficando evidente inclusive, que esses fatores não atuam isoladamente (GOBBO-NETO & LOPES, 2007).
O gênero Plectranthus (δ‟Her.) pertence à família δamiaceae, compreende
muitas plantas de interesse medicinal e econômico, embora sua composição química ainda seja pouco conhecida. Das 300 espécies do gênero Plectranthus já identificadas,
62 são mencionadas por possuírem propriedades medicinais, alimentícias, flavorizantes, antissépticas, repelentes e por serem utilizados como pastagens e como plantas ornamentais (LUKHOBA et al., 2006).
A espécie selecionada cujo estudo é relatado nesse trabalho foi Plectranthus grandis (Cramer) Willense que é um arbusto popularmente conhecido no Brasil pelo
19 apenas dez artigos publicados, onde apenas quatro desses relatam sobre a sua constituição química com destaque para a barbatusina identificada em P. grandis e P. barbatus (RODRIGUES et al., 2010).
A barbatusina, C24H30O8 (Figura 1), é um diterpeno tetracíclico abietano que tem duas atividades relatadas na literatura, atividade Gastroprotetora (ALBUQUERQUE et al., 2007) e a atividade Antitumoral (LIMA, 2013), sendo este composto bastante promissor para estudos farmacológicos futuros.
Figura 1: Representação estrutural da barbatusina.
Esse trabalho compreende a descrição dos procedimentos utilizados no isolamento e determinação estrutural dos compostos isolados de Plectranthus grandis,
bem como no estudo da variação sazonal e circadiana da barbatusina, composto farmacologicamente ativo presente em P. grandis, através da implementação e
validação de um método analítico capaz de detectar e quantificar este metabólito. Adicionalmente, foi realizado um estudo in silico para a determinação do
potencial anti-malárico, antitumoral e anti-inflamatório através de ensaios de docking, descritores moleculares e físico-químicos de uma base de dados implementada com todos os compostos isolados até o presente do gênero Plectranthus.
A elaboração dessa tese obedece aos padrões preestabelecidos pelo Programa de Pós-Graduação em Química da Universidade Federal do Ceará, bem como as regras e normas básicas da ABNT.
CH3 H
AcO O
O
H OAc
OH O
1
2
3
4 5
6 7 8 9
10
11 12 13
14 15
18
17 16
19
20
2-CONSIDERAÇÕES BOTÂNICAS
2.1- A Família Lamiaceae e o Gênero Plectranthus
A família Lamiaceae compreende 236 gêneros e 7173 espécies compostas por ervas, arbustos e árvores distribuídas principalmente na região mediterrânea, Ásia Central, sul da África, Madagascar, China, Austrália, América do Norte, México e América do Sul (HARLEY et al., 2004). No Brasil a família está representada por 34 gêneros e 498 espécies (HARLEY et al., 2010).
Essa família contém plantas ricas em óleos essenciais destinados às indústrias na produção de fármacos, perfumes e cosméticos, como lavanda (Lavandula angustifolia),
boldo-brasileiro (Plectranthus barbatus) e algumas espécies também são cultivadas
como plantas ornamentais, por exemplo, sálvia (Salvia splendens) (SOUZA &
LORENZI, 2012). Todas estas diferentes plantas pertencem à mesma família apresentando caules jovens quadrangulares, grande número de tricomas glandulares ricos em terpenos e flores bilabiadas com 5 pétalas (JUDD et al., 2002).
Na medicina popular, a família Lamiaceae ocupa o terceiro lugar em ordem de importância, com muitas espécies apresentando substâncias biologicamente ativas (HARLEY et al., 2004), com destaque para o gênero Plectranthus que compreende
cerca de 300 espécies amplamente distribuídas pela África, Ásia e Austrália (LUKHOBA et al., 2006). O nome Plectranthus vem das palavras gregas plektron
(esporão) e anthos (flor), sendo seu significado devido às flores apresentarem um esporão em sua base (WALDIA et al., 2011). As espécies que compõem este gênero são ricas em diterpenos e possuem uma ampla utilização na medicina popular para tratar distúrbios digestivos, problemas de pele, distúrbios respiratórios, infecções e febre, entre outras.
21 2.2- Plectranthus grandis (Cramer) Willense
Plectranthus grandis (Cramer) Willense é popularmente conhecido no Brasil
pelas denominações de boldo-grande ou boldo-da-folha-grande sendo utilizado largamente pela população no combate a dispepsia (MATOS, 2007). É um arbusto com até 3 m de altura com folhas maiores do que 4,7 cm, caule subquadrangular, espesso com pelos, inflorescência racemosa, racemo simples, erétil, 26 - 56 cm, pedúnculo rígido, flores com corola maior do que 2,0 cm de comprimento de coloração azul. Esta espécie é capaz de florescer no Nordeste nas regiões serranas, litorâneas ou sertão central, no que difere das outras espécies que necessitam de clima mais ameno ou temperado para se desenvolver.
Figura 2: Registro fotográfico de Plectranthus grandis (Cramer) Willense
22
3- QUÍMIODIVERSIDADE E PERFIL BIOFARMACOLÓGICO DE
PLECTRANTHUS
spp.
Desde a década de 60, a composição química das espécies de Plectranthus vem
sendo estudada e até o momento, foram identificados mais de 200 compostos, sendo os diterpenos, a classe mais frequente no gênero.
23 Figura 3: Biossíntese de terpenos via mevalonato (ANDRADE, 2010)
Vários núcleos diterpênicos são encontrados em espécies de Plectranthus, como
24
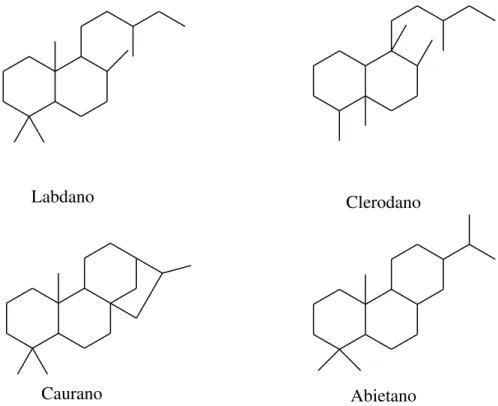
Labdano Clerodano
Abietano Caurano
Figura 4: Estrutura dos núcleos diterpênicos mais comuns encontrados em Plectranthus
spp.
Com o propósito de identificar os compostos isolados das espécies de
Plectranthus foi realizado uma pesquisa bibliográfica utilizando as ferramentas de busca Scopus.com, utilizando como palavra-chave “Plectranthus”. Observou-se uma modesta
evolução no número de publicações (Figura 5), com um incremento nos anos de 2014 e 2015, mostrando resultados expressivos com relação a atividades biológicas do gênero
Plectranthus.
Figura 5: Evolução dos relatos científicos do gênero Plectranthus
0 5 10 15 20 25 30 35 40 45 50 a-1 946 a-1 958 a-1 968 a-1 971 a-1 978 a-1 981 a-1 983 a-1 985 a-1 988 a-1 990 a-1 992 a-1 994 a-1 996 a-1 998 a-2 000 a-2 00 2 a-2 004 a-2 006 a-2 008 a-2 010 a-2 012 a-2 014 a-2 016
Nº de pu
bli
caç
õe
s
25 Foram identificados 270 compostos em apenas 40 espécies do gênero
Plectranthus. Os dos compostos isolados de Plectranthus que a literatura relata,
encontram-se na Tabela 1, dispostas em ordem alfabética pelo nome científico da espécie, seguido pelo nome dos compostos identificados para cada planta, órgão vegetal utilizado no estudo, a atividade farmacológica relatada para o composto e a referência bibliográfica.
Tabela 1: Compostos identificados, órgão vegetal utilizado no estudo, a atividade farmacológica relatada para o composto e a referência bibliográfica de espécies do gênero Plectranthus.
Planta Composto Fonte Atividade Referência
Plectranthus albidus
1-(4′
-hidroxifenil)tetradecan-5- ona (1)
Planta
Inteira Antioxidante Burgi, 1993
1-(4′
- hidroxifenil)hexadecan-5-ona (2)
Planta
Inteira Antioxidante Burgi, 1993
1-(4′
-hidroxifenil)octadecan-5- ona (3)
Planta
Inteira Antioxidante Burgi, 1993
1-(3′,4′ -diidroxifenil)decan-5- ona (4)
Planta
Inteira Antiinflamatória Antioxidante Burgi, 1993 1-(3′,4′-
diidroxifenil)dodecan-5-ona
(5)
Planta
Inteira Antioxidante Burgi, 1993
1-(3′,4′-
diidroxifenil)tetradecan-5-ona
(6)
Planta
Inteira Antioxidante Burgi, 1993
1-(3′,4′
-diidroxifenil)hexadecan-5- ona (7)
Planta
Inteira Antioxidante Burgi, 1993
1-(3′,4′
- diidroxifenil)octadecan-5-ona (8)
Planta
Inteira Antiinflamatória Antioxidante Burgi, 1993
1-(3′,4′
-diidroxifenil)icosan-5-ona
(9)
Planta
Inteira Antioxidante Burgi, 1993
1-(4′ -hidroxifenil)octadec-13-en-5-ona (10)
Planta
Inteira Antioxidante Burgi, 1993 1-(3′,4′
- diidroxifenil)octadec-13-en-5-ona (11)
Planta
Inteira Antioxidante Burgi, 1993
(E,E)-1-(3′,4′
- diidroxifenil)deca-1,3-dien-5- ona (12)
Planta
26 Plectranthus
ambiguus
(2S,3R,16R)-filocladano-2,3,16,17-tetrol 2,3-diacetato (13)
Partes
aéreas - Liu, 2003
5,6-diidroxi-4',7-
dimetoxiflavona (14) Partes aéreas Antitumoral Liu, 1996 (16R)-2α-(3 -metil-2-
butenoiloxi)-3α-
acetoxifilocladano-16,17-diol (15)
Partes aéreas
- Liu, 1996
(16R)-2α-(3-metil-2- butenoiloxi)-3α,17- diacetoxi-16-
hidroxifilocladano (16)
Partes
aéreas - Liu, 1996
(16R)-2α
-(3-metilbutanoiloxi)- 3α - acetoxifilocladano-16,17-diol (17)
Partes
aéreas - Liu, 1996
(16R)-2α
-(3-metilbutanoiloxi)- 3α,17 -diacetoxi-16-
hidroxifilocladano (18)
Partes
aéreas - Liu, 1996
(16R)-3α
- Acetoxifilocladano-16,17-diol (19)
Partes
aéreas - Liu, 1996
(16R)-2α -(3-metil-2- butenoiloxi)-16,17-dihidroxi-
filocladano-3-ona(20)
Partes
aéreas - Liu, 1996
Plectranthus argentatus
6β-hidroxi-7α-
formiloxiroileanona (21) Folhas - Alder, 1984
6β-hidroxi-7α-
acetoxiroileanona (22) Folhas Antibacteriana Antioxidante Antitumoral
Alder, 1984
6β-formiloxi-7α-
hidroxiroileanona (23) Folhas - Alder, 1984
6β,7α-dihidroxiroileanona
(24)
Folhas Antitumoral Alder, 1984
coleona-U-quinona (25) Folhas Antifúngica Antibacteriana
Inseticida
Alder, 1984
coleona V (26) Folhas - Alder, 1984
coleona U (27) Folhas Antifúngica Antibacteriana
Inseticida Antitumoral
Alder, 1984
5,6-diidrocoleona U (28) Folhas - Alder, 1984
Plectranthus barbatus
forscolina (29) Planta
inteira Antihipertensiva Cardioprotetora Anti-HIV Mohammed, 2015 Alasbahi, 2010 Bodiwala,200 9 Saleem, 2006
27
aéreas 2014
5,6-diidro-7-hidroxi-taxodona (31) Partes aéreas Antiprotozoária Mothana, 2014 taxodiona (32) Partes
aéreas Antiprotozoária Antitumoral Mothana, 2014 20-deoxocarnosol (33) Partes
aéreas Antiprotozoária Antitumoral Mothana, 2014
6α,11,12,-triidroxi-7β,20 -epoxi-8,11,13-abietatrieno
(34)
Partes
aéreas Antiprotozoária Antitumoral Mothana, 2014
1,2,3,4,6-penta-O-galoil-β
-D-glucose (35) Folhas Antiparasitária Antioxidante Antitumoral Inibidor de
melanoma
Inibidor de α -glicosidase
Dos Santos, 2012
1-deoxiforscolina (36) Partes
aéreas Anti-HIV Bodiwala,2009 1,9-dideoxiforscolina (37) Partes
aéreas - Bodiwala,2009
isoforscolina (38) Partes
aéreas - Bodiwala,2009
ácido rosmarínico (39) Partes
aéreas Antiacetilcolinesterase Antioxidante Antiinflamátória
Antibacteriana
Inibidor de α -glucosidase
Falé, 2009
escutellareina 4′-metil éter
7-O- glucuronideo (40) Partes aéreas Antiacetilcolinesterásica Falé, 2009 (16S)-coleona E (41) Partes
aéreas Antiacetilcolinesterásica Falé, 2009 Ruedi, 1986 ciclobutatusina (42) Folhas Antimicrobiana Albuquerque,
2007
barbatusina (43) Folhas Gastroprotetora Albuquerque, 2007
7β-acetil-12-
desacetoxiciclobutatusina
(44)
Folhas - Albuquerque,
2007
13-epi-sclareol (45) Raízes Antitumoral Sashidhara, 2007
Plectrinona A (46) Folhas Anti-úlcera Schultz, 2007 Ácido 12-hidroxi-8,13E-
labdadien-15-óico (47) Planta inteira - Xu, 2006 6-acetil-1-deoxiforscolina
(48) Planta inteira - Xu, 2006
6-acetil-1,9-dideoxiforscolina (49) Planta inteira - Xu, 2006 Ácido coleonólico (50) Raízes - Roy, 1990
Plectranthona J (51) Folhas - Ruedi, 1986
28
Inseticida Kubo, 1984
ColeonaF (53) Folhas - Ruedi, 1986
Plectrinona B (54) Folhas - Ruedi, 1986
(16R)-Plectrinona A (55) Folhas - Ruedi, 1986
Plectranthus bishopianus
6β-hidroxi-7α
-metoxiroileanona (56) aéreas Partes - Syamasundar,2012 6,7-diidroroileanona (57) Partes
aéreas Antibacteriana Syamasundar,2012
6β,7α-diidroxiroileanona
(24) aéreas Partes - Syamasundar,2012
ácido oleanólico (58) Partes
aéreas Hepatoprotetora Antioxidante Antiinflamatória Antifúngica Antibiótica Antitumoral Antiacetilcolinester ásica Syamasundar, 2012
β-sistosterol (59) Partes aéreas Antitumoral Antiinflamatória Antinociceptiva Syamasundar, 2012
estigmasterol (60) Partes
aéreas Antiinflamatória Antitumoral Antinociceptiva
Syamasundar, 2012
Plectranthus caninus
coleona T (61) Planta
inteira - Arihara, 1977
coleona S (62) Planta
inteira - Arihara, 1977
coleona R (63) Planta
inteira - Arihara, 1983
coleona M (64) Planta
inteira - Arihara, 1983
7,12-diacetilcoleona J (65) Planta
inteira - Arihara, 1983
coleona N (66) Planta
inteira - Arihara, 1983
coleona Q (67) Planta
inteira - Arihara, 1983
coleona P (68) Planta
inteira - Arihara, 1983
Plectranthus coesta
ácido
ent-7-hidroxikaur-15,16-en-19-oico (69) Folhas Antibacteriana Antitumoral Waldia, 2013 ácido
17-oxokaur-15,16-en-19-oico (70) Folhas Antibacteriana Antitumoral Waldia, 2013 ácido ent-7-hidroxi-15,16-
epoxikauran-19-oico (71)
Folhas Antitumoral Waldia, 2013
plecostonol (72) Planta
inteira - Phadnis, 1986
coestinol (73) - Phadnis, 1987
Plectranthus coetsoides
plecostonol (72) Folhas - Huang, 1989
Coestinol (73) Folhas - Huang, 1989
Coetsidin B (74) Folhas - Huang, 1989
29
Coetsidin D (76) Folhas - Huang, 1989
Coetsidin E (77) Folhas - Huang, 1989
Coetsidin F (78) Folhas - Huang, 1989
Coetsidin G (79) Folhas - Huang, 1989
Plectranthus crassus
Nepetoidina A (80) Folhas Antifúngico Grayer, 2003 Nepetoidina B (81) Folhas Antifúngico
Antioxidante Grayer, 2003
Plectranthus cylindraceus
Plectranthona (82) Partes
aéreas - Orabi, 2000
Desacetilplectranthona (83) Partes
aéreas - Orabi, 2000
Isodeacetilplectranthona
(84) aéreas Partes - Orabi, 2000
Pachipodol (85) Partes
aéreas Antimicrobiana Antitumoral Orabi, 2000 Casticina (86) Parte
aéreas Antitumoral Orabi, 2000 Crisosplenol D (87) Partes
aéreas Antiviral Orabi, 2000
Plectranthus ecklonii
Parviflorona D (88) Planta
inteira Antibacteriana Antioxidante Simões, 2010 Nyila, 2009
β-sitosterol (59) e
estigmasterol (60) Planta inteira Antiinflamatória Antitumoral Antinociceptiva
Simões, 2010
Ácidos ursólico (89) e
oleanólico (58) Planta inteira Antihepatotóxica Antioxidante Antiinflamatória Antifúngica Antibiótica Antitumoral Antiacetilcolinester ase Simões, 2010
Parviflorona F (90) Planta
inteira Antibacteriana Antioxidante Nyila, 2009 Uchida, 1980 Ecklonoquinona A (91) Folhas - Uchida, 1980 Ecklonoquinona B (92) Folhas - Uchida, 1980 2 (S)-5,4′-dihidroxi-6,7-
dimetoxiflavanona (93) Folhas - Uchida, 1980
Cirsimaritin (94) Folhas Antibacteriana Antiinflamatória Antioxidante Anti-ansiedade Anti-espasmódico Anti-proteinúria Uchida, 1980 Plectranthus edulis
Lanugona A (95) - Kunzle, 1987
(4βS,7R,8αR)
-7-Formiloxi-4β,5,6,7,8,8α-hexahidro- 3-hidroxi-4β ,8,8-trimetil-2- (2-propenil)fenantren-1,4-diona (96)
- Kunzle, 1987
6β,7α-Dihidroxiroileanona
(24)
Antitumoral Kunzle, 1987
(4βS,7R,8αR,9S,10S)
30 7,8,8α,9,10
-octahidro-3,9,10-trihidroxi-
4β, 8,8 -trimetil-2-(2- propenil)-fenantren-1,4-diona (97)
(4βS,7R,8αS,9S,10S)-
4β,5,6,7,8,8α,9,10
-
Octahidro-3,9,10-trihidroxi-4β,7 -dimetil-8-metiliden-2- (2-propenil)-fenantren-1,4-diona (98)
- Kunzle, 1987
(2‟ξ,4βS,7R,8αS,9S,10S)-
4β,5,6,7,8,8α,9,
10-Octahidro-3,9,10-trihidroxi-2-(2‟
-hidroxipropil)-4β,7 -dimetil-8-metilidenfenantren- 1,4-diona (99)
- Kunzle, 1987
(2R,2‟S,3‟R,4‟βS,7‟R,8‟αS, 9‟S,10‟S)-3‟,10‟
-diacetoxi-4‟β,5‟,6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-9‟
-hidroxi-2,4‟b,7‟-trimetil-8‟
-
metilidenspiro[ciclopropan-1,2‟(1‟H)
-fenantren]-1‟,4‟(3‟H)-diona (100)
- Kunzle, 1987
(2R,2‟S,3‟R,4‟βS,7‟R,8‟αS, 9‟S,10‟S)-3‟-acetoxi,10‟ -formiloxi-4‟β,5‟,6‟,7‟,8‟, 8‟α,9‟,10‟-octahidro-9‟ -hidroxi-2,4‟b,7‟-trimetil-8‟ -
metilidenspiro[ciclopropan-1,2‟(1‟H)
-fenantren]-1‟,4‟(3‟H)-diona (101)
- Kunzle, 1987
(2R,2‟S,3‟R,4‟βS,7‟R,8‟αS, 9‟S,10‟S)-10‟
-Acetoxi-4‟β,5‟,6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-3‟,9‟
-dihidroxi-2,4‟β,7‟-trimetil-8‟-
metilidenspiro[ciclopropan-1,2‟(1‟H)
-fenantren]-1‟,4‟(3‟H)-diona (102)
- Kunzle, 1987
(2R,2‟S,3‟R,4‟βS,7‟R,8‟αS, 9‟S,10‟S)-3‟-
acetoxi-4‟β,5‟,6‟,7‟,8‟,8‟,9‟,10‟ -octahidro-9‟,10‟
-dihidroxi-2,4‟b,7‟-trimetil-8‟-
metilidenspiro[ciclopropan-1,2‟(1‟H)
-fenantren]-1‟,4‟(3‟H)-diona (103)
- Kunzle, 1987
(2R,2‟S,3‟R,4‟βS,7‟R,8‟αS, 9‟S,10‟S)-10‟
-Formiloxi-4‟β,5‟,6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-3‟,9‟
-dihidroxi-2,4‟b,7‟-trimetil-8‟-
31
metilidenspiro[ciclopropan-1,2‟(1‟H)
-fenantren]-1‟,4‟(3‟H)-diona (104)
(2R,2‟S,3‟R,4‟βS,7‟R,8‟αS, 9‟S,10‟S)-4‟β,5‟,
6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-3‟,9‟,10‟ -trihidroxi-2,4‟β,7‟
-trimetil-8‟
-
metilidenspiro[ciclopropan-1,2‟(1‟H)-fenantren]-
1‟,4‟(3‟H)-diona (105)
- Kunzle, 1987
(2R,2‟S,3‟R,4‟βS,7‟R,8‟αR, 9‟S,10‟S)-9-acetoxi-7‟ -
formiloxi-4‟β,5‟,6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-3‟,10‟
-dihidroxi-2,4‟β,8‟,8‟
-
tetrametilspiro[ciclopropan-1,2‟(1‟H)
-fenantren]-1‟,4‟(3‟H)-diona (106)
- Kunzle, 1987
Lanugona G (107) - Kunzle, 1987
(2R,2‟S,3‟R,4‟βS,7‟R,8‟αR, 9‟S)-7‟-Formiloxi-
4‟β,5‟,6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-3‟,9‟
-dihidroxi-2,4‟b,8‟,8‟-tetrametilspiro- [ciclopropan-1,2‟(1‟H) -fenantren]-1‟,4‟(3‟H)-diona
(108)
- Kunzle, 1987
Lanugona F (109) - Kunzle, 1987
(2R,2‟S,3‟R,4‟βS,7‟R,8‟αR, 9‟S,10‟S)-7‟,10‟
-
Bisformiloxi-4‟β,5‟,6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-3‟,9‟
-dihidroxi-2,4‟β,8‟,8‟-tetrametilspiro[ ciclopropan-1,2‟(1‟H)- fenantren]-1‟,4‟(3‟H)-diona
(110)
- Kunzle, 1987
(2R,2‟S,3‟R,4‟βS,7‟ξ,8‟αR, 9‟S,10‟S)-7‟,10‟
-diacetoxi-4‟β,5‟,6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-3‟,9‟
-dihidroxi-2,4‟β,7‟-trimetil-8‟-
metilidenspiro[ciclopropan-1,2‟(1‟H)
-phenanthren]-1‟,4‟(3‟H)-diona (111)
- Kunzle, 1987
(2S,2‟S,3‟R,4‟βS,7‟R,8‟αR, 9‟S,10‟S)
-7-Formiloxi-4‟β,5‟,6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-3‟,9‟
-diacetoxi-10‟-hidroxi-2,4‟β,8‟, 8‟
32
tetrametilspiro[ciclopropan-1,2‟(1‟H)
-fenantren]-1‟,4‟(3‟H)-diona (112)
(2S,2‟S,3‟R,4‟βS,7‟R,8‟αR, 9‟S,10‟S)-7‟,10‟-
Bisformiloxi-4‟β,5‟,6‟,7‟,8‟,8‟α,9‟,10‟ -octahidro-3‟,9‟
-dihidroxi-2,4‟β,8‟,8‟-tetrametilspiro[ ciclopropan-1,2‟(1‟H)- fenantren]-1‟,4‟(3‟H)-diona
(113)
- Kunzle, 1987
Coleona Z (114) - Kunzle, 1987
(15S)-Lanugona O (115) - Kunzle, 1987
(4βS,8αS)-2-(2-
acetoxipropil)-4β,5,6,7,8,
8a-hexahidro-1,4-dihidroxi-4β,8,8-trimetilfenantren- 3,9-diona (116)
- Kunzle, 1987
(2,4βS,8αS)-4β,5,6,7,8,8α -hexahidro-
1,4-dihidroxi-2-(2‟ -hidroxipropil)-4β,8,8 - trimetilphenanthren-3,9-diona (117)
- Kunzle, 1987
(2,3αR,10βR)-8-(2‟- acetoxi-1‟-metiletil)-3,3α -
dihidro-7,9,10-trihidroxi-3α,10β -dimetil-1H- fenantro[10,1bc]-furan-4(2H),6(10bH)-diona (118)
- Kunzle, 1987
16-O-Acetilcoleona C (119) - Kunzle, 1987
Coleona U (27) Antifúngica
Antibacteriana Inseticida
Kunzle, 1987
Coleona C (120) Antitumoral Kunzle, 1987
16-O-Acetilcoleona D (121) - Kunzle, 1987
(15S)-Coleona D (122) - Kunzle, 1987
(2,4αS,10αS)-
1,2,3,4,4α,10α-hexahidro- 5,6,8-trihidroxi-7-(2‟ - hidroxipropil)-1,1,4a- trimetilphenanthren-9,10-diona (123)
- Kunzle, 1987
(2,4αR)-2,3,4,4α -tetrahidro-5,6,8,10- tetrahidroxi-7-(2‟ -hidroxipropil)-1,1,4α - trimetilphenanthren-9(1H)-ona (124)
- Kunzle, 1987
Edulona A (125) - Kunzle, 1987
Buchbauer, 1978
(1‟S,10βS)-7,9,10-
33
metiletil)-3,10β -dimetil-1H-benzo[g]ciclopenta[de][1]be nzopiran-4(2H),6(10βH) -diona (126)
(3R)-6,9-Dihidroxi-3,4- dimetil-7-(1-metiletil)-3-(2-propenil)nafto[2,3-β] -furan-2-(3H),5,8-triona (127)
- Kunzle, 1987
(2,3R)-7-(2‟-Acetoxi-1‟ - metiletil)-6,9-dihidroxi-3,4-dimetil-3-(2‟‟-propenil)- nafto[2,3-b]furan-2-(3H),5,8-triona (128)
- Kunzle, 1987
Plectranthus elegans 11-Hidroxi-12-oxo-7,9(11),13-abietatrieno (129) Partes
aéreas Antimicrobiana Dellar, 1996
7α,11
-Dihidroxi-12-metoxi-8,11,13-abietatrieno (130) aéreas Partes Antimicrobiana Dellar, 1996
Plectranthus ernstii
rel-15(ζ),16-epoxi-7α- hidroxipimar-8,14-eno
(131)
Planta inteira
Antibacteriana Stavri, 2009
rel-15(ζ),16
-epoxi-7-oxopimar-8,14-eno (132) Planta inteira Antibacteriana Stavri, 2009
1R,11S-dihidroxi-8R,13R-epoxilabd-14-eno (133) Planta inteira Antibacteriana Stavri, 2009
Plectranthus forsteri
Ácido caféico (134) Partes
aéreas Antiinflamátória Antioxidante Anti-HIV Antitumoral
Kubínová, 2013
Ácido rosmarinico (39) Partes
aéreas Antiacetilcolinesterásica Antioxidante Antiinflamátória
Kubínová, 2013
Nepetoidinos A (135) e B
(136) aéreas Partes Antioxidante Antifúngica Kubínová, 2013
7β,6β-dihidroxiroileanona
(137) aéreas Partes Antibacteriana Inibidor de α -glucosidase
Kubínová, 2013
7β-acetoxi-6β
-hidroxiroileanona (138) aéreas Partes - Kubínová, 2013 6,7-dihidroroileanona (57) Partes
aéreas - Kubínová, 2013
Plectranthus fruticosus
Ácido
ent-kaur-15-en-19-óico (139) aéreas Partes Antifúngica Rijo, 2010
Ácido ent-12β
34
Ácido ent-7β
-hidroxi-15β,16β- epoxikauran-19-óico (71)
Partes
aéreas - Rijo, 2010 Gaspar-Marques, 2004
10(14)-Aromadendreno-4β,15- diol (141) aéreas Partes - Gaspar-Marques, 2004 Ent-3β
-acetoxilabda-8(17),12Z,14-trien-2α-ol
(142)
Partes
aéreas - Gaspar-Marques, 2004 Ácido ent-12β-acetoxi-15β-
hidroxikaur-16-en-19-óico
(143)
Partes
aéreas - Gaspar-Marques, 2004 Ácido ent-12β-acetoxi-7β-
hidroxikaur-16-en-19-óico
(144)
Partes
aéreas - Gaspar-Marques, 2004 Ácido ent-7β
-hidroxikaur-15- en-19-óico (145) aéreas Partes - Gaspar-Marques, 2004 Ácido ent-12β-acetoxi-17-
oxokaur-15-en-19-óico
(146)
Partes
aéreas - Gaspar- Marques, 2004
Ent-labda-8(17),12Z,14-trien-2α-ol (147) aéreas Partes
-
Gaspar-Marques, 2003 Ent-2α
-Acetoxilabda-8(17),12Z,14-trien-3β-ol
(148)
Partes
aéreas - Gaspar-Marques, 2003
3β
-acetoxilabda-8(17),12E,14- trien-2α-ol
(149)
Partes
aéreas - Gaspar-Marques, 2003 Ácido ent-15β,16β
-epoxikauran-19-óico (150) aéreas Partes Antimicrobiana Gaspar-Marques, 2003 Ent-15β,16β
-epoxikauran-19- ol (151) aéreas Partes - Gaspar-Marques, 2003
β-sitosterol (59) e
estigmasterol (60) aéreas Partes Antiinflamatória Antitumoral Antinociceptiva Gaspar-Marques, 2003 Plectranthus glaucocalyx
Plectrina (52) Folhas Antimicrobiana
Inseticida Elizarova, 1965
Plectranthus grandidentatus
7α-acetoxi- 6β
35
(24) inteira
Gaspar-Marques, 2006 Cerqueira, 2004 Marques, 2002 Horminona (152) Planta
inteira Antimicrobiana Antibacteriana Rijo, 2010 Gaspar-Marques, 2006
Teixeira, 1997 6,7-dihidroroileanona (57) Planta
inteira Antibacteriana Rijo, 2010 Gaspar- Marques, 2006
Teixeira, 1997 Coleona U (27) Planta
inteira Antibacteriana Antifúngica Inseticida Antitumoral
Inibidor de α -glucosidase Coutinho, 2009 Rijo, 2007 Gaspar-Marques, 2006 Cerqueira, 2004 Marques, 2002 Uchida, 1981 14-O-Acetilcoleona U (153) Partes
aéreas - Rijo, 2007
6β-hidroxiroileanona (154) Planta
inteira - Gaspar- Marques, 2006
Teixeira, 1997 Roileanona (155) Planta
inteira
Citotóxico Gaspar- Marques, 2006 6,12,14-Trihidroxi-9α-(2-
oxopropil)abieta- 5,8(14),12-trieno-7,11-diona (156)
Partes
aéreas - Gaspar-Marques, 2005
7α-aciloxi-6β-
hidroxiroileanona (157) Planta inteira Antitumoral Cerqueira, 2004 Marques, 2002
Teixeira, 1997 Grandidona A (158) Planta
inteira Antitumoral Cerqueira, 2004 Marques, 2002
Uchida, 1981 Grandidona C (159) Planta
36
inteira Uchida, 1981
7-epigrandidona D (161) Planta inteira
- Teixeira, 1997
Uchida, 1981
7α-aciloxi-6β,12-dihidroxi- abieta- 8,12-diene-11,14-diona (162)
Planta
inteira - Teixeira, 1997
14-Hidroxitaxodiona (163) Folhas - Uchida, 1981
Coleona V (26) Folhas - Uchida, 1981
Grandidona B (164) Folhas - Uchida, 1981
7-epigrandidona B (165) Folhas - Uchida, 1981
7-epigrandidona A (166) Folhas - Uchida, 1981 Plectranthus
grandis
Barbatusina (43) Folhas Gastroprotetora Rodrigues, 2010
3β
-hidroxi-3-deoxibarbatusina (167) Folhas Gastroprotetora Rodrigues, 2010
Plectranthus hereroensis
Horminona (152) Raízes Antibacteriana
Antimicrobiana Gaspar- Marques, 2006
Batista, 1996 Batista, 1995 Batista, 1994 7α
,12-dihidroxi-17(15→16)abeo
-abieta-8,12,16-trieno-11,14-diona
(168)
Raízes Antimicrobiana Gaspar- Marques, 2006
Batista, 1994 16-acetoxi-7α
,12-dihidroxi- 8,12-abietadieno-11,14-diona (169)
Raízes Partes aéreas Antimicrobiana Antibacteriana Antiviral Gaspar- Marques, 2006 Batista, 1996 Batista, 1995 3β-acetoxi-6β,7α,12
-
trihidroxi-17(15→16),18(4→3) -bisabeo
-abieta- 4(19),8,12,16-tetraeno-11,14-diona (170)
Partes
aéreas Antibacteriana Gaspar- Marques, 2006
Batista, 1996
1(10)-aristolen-13-al (171) Raízes Antimicrobiana Rodriguez, 1995
16-Acetoxihorminona (172) - Batista, 1996
Plectranthus japonicus
Rabdosin B (173) Planta
inteira Antitumoral Wang, 1990
Plectranthus lanuginosus
Lanugona A (95) Folhas - Schmidt, 1982
6,7-Dihidroroileanona (57) Folhas Antibacteriana Schmidt, 1982
Lanugona B (174) Folhas - Schmidt, 1982
Lanugona C (175) Folhas - Schmidt, 1982
Lanugona D (176) Folhas - Schmidt, 1982
Lanugona E (177) Folhas - Schmidt, 1982
Lanugona G (107) Folhas - Schmidt, 1982
Lanugona F (109) Folhas - Schmidt, 1982
Lanugona H (178) Folhas - Schmidt, 1982
Lanugona I (179) Folhas - Schmidt, 1982
Lanugona J (180) Folhas - Schmidt, 1982
37
δanugona K‟ (182) Folhas - Schmidt, 1982
(15S)-Lanugona O (115) Folhas - Schmidt, 1982
Lanugona P (183) Folhas - Schmidt, 1982
Lanugona Q (184) Folhas - Schmidt, 1982
Lanugona M (185) Folhas - Schmidt, 1982
Lanugona L (186) Folhas - Schmidt, 1982
Lanugona N (187) Folhas - Schmidt, 1982
(15S)-Coleona D (122) Folhas - Schmidt, 1982
(15S)-Coleona C (188) Folhas - Schmidt, 1982
Lanugona R (189) Folhas - Schmidt, 1982
Lanugona S (190) Folhas - Schmidt, 1982
Plectranthus madagascariens is
Ácido rosmarínico (39) Planta inteira
Antibacteriana
Inibidor de α -glucosidase Antiacetilcolinester ásica Antioxidante Antiinflamátória Kubínová, 2014
7β, 6β-dihidroxiroileanona
(137) Inteira Planta Antibacteriana Inibidor de α -glucosidase
Kubínová, 2014
7β-acetoxi-6β
-hidroxiroileanona (138) Inteira Planta Antibacteriana Inibidor de α -glucosidase
Kubínová, 2014
Coleona U (27) Planta
inteira Antibacteriana Antifúngica Inseticida Antitumoral
Inibidor de α -glucosidase
Kubínová, 2014
Plectranthus marrubioides
Crisosplenetina (191) Folhas Antiviral
Antitumoral Hensch, 1972
Plectranthus montanus
Éter 3,7-dimetil quercetina
(192)
Folhas Vasorelaxante
Antioxidante Grayer, 2010
Éter 3,6,7,4′-tetrametil
quercetina (193) Folhas - Grayer, 2010
Crisosplenol D (87) Folhas Antiviral Grayer, 2010 Casticina (86) Folhas Antitumoral Grayer, 2010
Plectranthus myrianthus
Grandidona A (158) Folhas Antitumoral Uchida, 1981
6β, 7α-Dihidroxiroileanona
(24)
Folhas Antitumoral Miyase, 1977
6β-Hidroxi-7α-
formiloxiroileanona (21) Folhas - Miyase, 1977
Coleona U (27) Folhas Antifúngica Antibacteriana
Inseticida Antitumoral
Inibidor de α -glucosidase
38
Coleona V (26) Folhas - Miyase, 1977
Plectranthus nilgherricus
Parviflorona C (194) Folhas - Miyase, T.;
1977 Parviflorona E (195) Folhas Antioxidante Miyase, T.;
1977
Sanguinon A (196) Folhas - Miyase, T.;
1977 (16R)-17,19-diacetoxi-16-
hidroxi-13β-kauran-3-ona
(197)
Folhas - Miyase, T.;
1977
Nilgherron A (198) Folhas - Miyase, T.;
1977
Nilgherron B (199) Folhas - Miyase, T.;
1977 Fuerstiona (200) Folhas Antioxidante
Moluscida Miyase, T.; 1977
3β-Acetoxifuerstiona (201) Folhas - Miyase, T.;
1977
Plectranthus nummularius
Plectrantol A (202) Folhas Antioxidante Narukawa, 2001 Plectrantol B (203) Folhas Antioxidante Narukawa,
2001 Parviflorona E (195) Folhas Antioxidante Narukawa,
2001 Parviflorona F (90) Folhas Antioxidante
Antibacteriana Narukawa, 2001
Plectranthus ornatus
Ácido rinocerotinóico (204) Planta
inteira Antiinflamatório Rijo, 2010 Rijo, 2007 Ácido 11R
*-Acetoxihalima-5,13E-dien-15-óico (205)
Planta
inteira Antimicrobiana Rijo, 2007 6-O-acetilforscolina (206) Planta
inteira - Rijo, 2005
1,6-di-O-acetilforscolina
(207)
Planta
inteira - Rijo, 2005
1,6-di-O-acetil-9-
deoxiforscolina (208) Planta inteira - Rijo, 2005 Plectrornatin A (209) Planta
Inteira - Rijo, 2002
Plectrornatin B (210) Planta
Inteira - Rijo, 2002
Plectrornatin C (211) Planta
inteira - Rijo, 2002
Plectranthus parviflorus
Parviflorona A (212) Folhas - Rüedi, 1978
Parviflorona B (213) Folhas - Rüedi, 1978
Parviflorona C (194) Folhas - Rüedi, 1978
Parviflorona D (88) Folhas Antioxidante Antibacteriana
Antitumoral
Rüedi, 1978
Parviflorona E (195) Folhas Antioxidante Rüedi, 1978 Parviflorona F (90) Folhas Antibacteriana
Antioxidante Rüedi, 1978
Plectranthus porcatus
(13S,15S)-6β,7α,12α,19
39 8-abieteno-11,14-diona (214) Plectranthus punuctatus 3,11,12,14,19-pentahidroxi-5,8,11,13-abietatraen-7- piran[4,6]-16-diona (215)
Planta
inteira Antioxidante Kebede, 2011
Plectranthus purpuratus
19-Isovaleroiloxitaxodiona
(216) Planta inteira
- Katti, 1982
19-Senecioiloxitaxodiona
(217) Planta
inteira
- Katti, 1982
Parviflorona A (212) Planta
inteira - Katti, 1982
11-Hidroxi-19-
isovaleroiloxi-5,7,9(11),13-abietatetraen-12-ona (218)
Planta inteira
- Katti, 1982
6α,11-Dihidroxi-19- isovaleroiloxi-7,9(11), 13-abietatrien-12-ona (219)
Planta
inteira - Katti, 1982
6α,11-Dihidroxi-19- senecioiloxi-7,9(11),13-abietatrien-12-ona (220)
Planta
inteira - Katti, 1982
11,12-Dihidroxi-19- isovaleroiloxi-8,11,13-abietatrien-7-ona (221)
Planta
inteira - Katti, 1982
11,12-Dihidroxi-19- senecioiloxi-8,11,13- abietatrien-7-ona (222)
Planta
inteira - Katti, 1982
(16R)-17,19-Diacetoxi-16-hidroxi-13β-kauran-3-ona
(197)
Planta
inteira - Katti, 1982
Plectranthus rugosus
Ácido plectranthoico A
(223) Folhas - Razdan, 1982
Ácido plectranthoico B
(224) Folhas
- Razdan, 1982
β-Sitosterol (59) Folhas Antitumoral Antiinflamatória
Antinociceptiva
Razdan, T.K., 1982
Misra, 1971 Ácido (19S)-3α
-hidroxi-18α-urs-12- en-29β-óico
(225)
Folhas - Razdan, T.K.,
1982
Ácido acetilplectranthoico
(226)
Folhas - Razdan, T.K.,
1982
Plectranthadiol (227) Folhas - Razdan, T.K.,
1982 Ácido oleanólico (58) Folhas Hepatoprotetora
Antioxidante Antiinflamatória Antifúngica Antibiótica Antitumoral Antiacetilcolinester ase Misra, 1971
Ácido ursólico (89) Hepatoprotetora
40 Antiinflamatória Antifúngica Antibiótica Antitumoral Antiacetilcolinester asica
Betulina (228) Antioxidante
Antiinflamatória Antitumoral Antialérgica Antiviral Hepatoprotetora Misra, 1971
Hexacosanol (229) Neurotrófica Misra, 1971
Plectranthus saccatus
Ácido ent-7α
-acetoxi-15-beieren-18-óico (230) aéreas Partes - Simões, 2010
Plectranthus sanguineus
7-O-Formilhorminona (231) Planta
inteira - Matloubi- Moghadam, 1987
6β-Hidroxi-7α-
formiloxiroileanona (21) Planta inteira
- Matloubi-
Moghadam, 1987
6β-Hidroxi-7α- acetoxiroileanona (22)
Planta
inteira Antibacteriana Antioxidante Antitumoral
Matloubi- Moghadam, 1987
6β-Hidroxiroileanona (154) Planta
inteira - Matloubi- Moghadam, 1987 5,6-Dihidrocoleona U (28) Planta
inteira - Matloubi- Moghadam, 1987 Horminona (152) Planta
inteira Antibacteriana Antimicrobiana Matloubi- Moghadam, 1987 6β,7α- Dihidroxi(alil)roileanona (232) Planta
inteira - Matloubi- Moghadam, 1987
6β,7α-Dihidroxiroileanona
(24) Planta inteira Antitumoral Matloubi- Moghadam,
1987 Coleona-U-quinona (25) Planta
inteira Antibacteriana Antifúngica Inseticida Matloubi- Moghadam, 1987 8α,9α-Epoxi-8,9- dihidrocoleona-U-quinona (233) Planta
inteira - Matloubi- Moghadam, 1987 14-Hidroxitaxodiona (163) Planta
inteira - Matloubi- Moghadam, 1987 16-O-Acetilcoleona D (121) Planta
inteira
- Matloubi-
Moghadam, 1987 Coleona U (27) Planta
inteira Antibacteriana Antifúngica Inseticida
41
Grandidona A (158) Planta
inteira Antitumoral Matloubi- Moghadam, 1987 7-Epigrandidona A (166) Planta
inteira - Matloubi- Moghadam, 1987 Grandidona B (164) Planta
inteira - Matloubi- Moghadam, 1987 7-Epigrandidona B (165) Planta
inteira - Matloubi- Moghadam, 1987 Sanguinon A (196) Planta
inteira
- Matloubi-
Moghadam, 1987
Plectranthus sp.
das fronteiras de Lake Kiwu, Ruanda
Plectranthona F (234) Planta
inteira - Alder, 1986
Plectranthona G (235) Planta
inteira - Alder, 1986
6β,7α-Dihidroxiroileanona
(24) Planta inteira Antitumoral Alder, 1986
Plectranthona H (236) Planta
inteira - Alder, 1986
Plectranthona I (237) Planta
inteira - Alder, 1986
Plectranthona J (51) Planta inteira
- Alder, 1986
Plectranthona K (238) Planta
inteira - Alder, 1986
Plectranthona L (239) Planta
inteira - Alder, 1986
Coleona F (53) Planta
inteira - Alder, 1986
(16S)-Coleona E (41) Planta inteira
Antiacetilcolinester asica
Alder, 1986
(15S)-2α-Acetoxicoleona C
(240)
Planta
inteira - Alder, 1986
(15S)-Coleona H (241) Planta
inteira - Alder, 1986
(15S)-2α-Acetoxicoleona D
(242) Planta inteira Alder, 1986
(15S)-Coleona I (243) Planta
inteira Alder, 1986
Plectrinona B (54) Planta
inteira - Alder, 1986
(16S)-Plectrinona A (244) Planta
inteira Alder, 1986
Plectranthona B (245) Planta
inteira Alder, 1986 Alder, 1984 Plectranthona A (246) Planta
inteira Alder, 1986 Alder, 1984 Plectranthona C (247) Planta
inteira Alder, 1986 Alder, 1984
42
inteira Alder, 1984
Plectranthona E (249) Planta
inteira Alder, 1986
Plectranthus strigosus
Ent-16-Kauren-19-ol (250) Planta
Inteira Anti-herpética Gaspar-Marques, 2008 Ácido
ent-16-kauren-19-oico (251)
Planta Inteira
Anti-herpética Gaspar-Marques, 2008 Ácido xilopico (252) Planta
Inteira Antimicrobiana Gaspar-Marques, 2008 Ácido xilopinico (253) Planta
Inteira - Gaspar-Marques, 2008 Hinokiol (254) Planta
Inteira
Antioxidante Gaspar-Marques, 2008
4β,6β-dihidroxi-1α,5β(H)
-guai-9-eno (255) Inteira Planta - Gaspar-Marques, 2008 4β,6β-dihidroxi-1α,5β(H)
-guai-10(14)-eno (256) Inteira Planta - Gaspar-Marques, 2008 Hexacosan-1,26-diol (257)
e octacosan-1,28-diol (258) Inteira Planta Antioxidante Gaspar-Marques, 2008 Acido ferúlico (259) Planta
Inteira Fotoprotetora Antioxidante Antitumoral
Gaspar-Marques, 2008 2-(4-hidroxifenil)-etanol
(260) Inteira Planta Antioxidante Gaspar-Marques,
2008 Parviflorona D (88) Planta
inteira Antibacteriana Antioxidante Gaspar- Marques, 2008 Alder, 1984
Parviflorona A (212) Folhas - Alder, 1984
Parviflorona H (261) Folhas - Alder, 1984
Parviflorona C (194) Folhas - Alder, 1984
Parviflorona E (195) Folhas Antioxidante Alder, 1984
Parviflorona B (213) Folhas - Alder, 1984
Parviflorona F (90) Folhas Antibacteriana
Antioxidante Alder, 1984
Parviflorona G (262) Folhas - Alder, 1984
Plectranthus sylvestris
1-(3′,4′-
dihidroxifenil)icosan-5-ona
(9)
Partes
aéreas Antioxidante Juch, 1997
4-[(2S,4R,6S
)-4- (acetiloxi)tetrahidro-6-pentil-2H
-piran-2-il]benzeno-1,2-diol (263)
Partes
aéreas Antioxidante Juch, 1997
43
hidroxi-6-pentil-2H
-piran-2-il]benzeno-1,2-diol (264) aéreas
4-[(3S,5S)-5-(acetiloxi)-3-
hidroxidecil]benzeno-1,2-diol (265)
Partes
aéreas Antioxidante Juch, 1997
4-[(3S,5S)3-(acetiloxi)-5-
hidroxidecil]benzeno-1,2-diol (266)
Partes
aéreas Antioxidante Juch, 1997
(3S,13Z)-1-(3,4-
dihidroxifenil)-3-hidroxidocos-13-en-5-ona
(267)
Partes
aéreas Antiinflamatório Antioxidante Analgésica
Juch, 1997
(Z
)-1-(3,4- dihidroxifenil)docos-13-en-5-ona (268)
Partes aéreas
Antioxidante Juch, 1997
Plectranthus venteri
2-hidroxi-3,4,5,6-tetrametoxi-acetofenona
(269)
Partes
aéreas Antibacteriana Maree, 2014
2-hidroxi-4,5,6-trimetoxi-acetofenona (270) aéreas Partes Antibacteriana Maree, 2014
Nesse estudo foram detectados 270 compostos diferentes isolados de 40 espécies do gênero Plectranthus observando-se que algumas destas como P. edulis e P. barbatus
têm vários relatos sobre sua composição química, embora raros são os trabalhos publicados sobre a composição química de outras espécies como P. grandis. Diversas
classes foram encontradas como triterpenos, flavonoides, ácidos graxos, no entanto, a maioria dos compostos identificados são diterpenos do tipo abietano. A representação estrutural dos compostos químicos isolados das espécies do gênero Plectranthus
encontra-se na tabela 2.
O potencial farmacológico das espécies estudadas de Plectranthus apresentou-se
44 Figura 6: Perfil biofarmacológico de Plectranthus spp.
Tabela 2: Representação estrutural dos compostos químicos isolados das espécies do gênero plectranthus.
O
OH
( )n
1. n=1 2. n=3 3. n=5
O
OH OH
( )n
4. n=1 7. n=7 5. n=3 8. n=9 6. n=5 9. n=11
O
OH R 10. R=H 11. R=OH
HO
HO
O
12 0
10 20 30 40 50 60
Nº de compostos
Antioxidante Antiinflamatória Antitumoral Antibacteriana Antifúngica Inseticida Antinoceptiva Antiviral
45 AcO AcO OH OH 13 O OCH3 O OH HO CH3O
14
R1 OH
AcO
OR2
15. R1= OCOCH=C(CH3)2, R2= H
16. R1= OCOCH=C(CH3)2, R2= Ac
17. R1= OCOCH2CH(CH3)2, R2= H
18. R1= OCOCH2CH(CH3)2, R2= Ac
19. R1= R2= H
O OH OAc O O 20 O O OH R2 R1
21. R1= OH, R2= OCHO 22. R1= OH, R2= OAc 23. R1= OCHO, R2= OH 24. R1= R2= OH
46 O OH OAc OH OH O
29 30
OH OH HO O 31 O HO O 32 HO R OH O
33. R= H 34. R= OH
O O O O O O O O O O HO HO OH HO HO OH HO HO OH HO OH OH O HO OH OH 35 O OAc OH O R
36. R= OH 37. R= H
O OAc O OH OH 38 O OH HO
O O OH OH
47 OH OH OH O O 46 COOH OH 47 O OAc OAc R O
48. R= OH 49. R= H
48 OH HO OH O HO OH 62 O O OAc AcO OAc OAc 63 O O OAc OH OAc 64 O O OAc OH OAc
65. α CH3
66. β CH3
O HO O HO 67 O HO O O 68 HOOC R1 R2
69. R1= OH, R2= CH3 70. R1= H, R2= COH
COOH OH O 71 O O OH HO OH 72 O R2 R1 R1 HO
73. R1= β-OH, R2= α-OH 74. R1= α-OH, R2= β-OH
R1 OH HO O O R2 R3
75. R1= H, R2=OCH3, R3= H
76. R1= OH, R2= OCH3, R3= H
77. R1= H, R2= OC2H5, R3= H
78. R1= R3= H, R2= OH 79. R1= R2= H, R3= OH
O O HO R2 OH OH R1
49
R2
O
R1
82. R1= R2= OAc 83. R1= OH, R2= OAc 84. R1= OAc, R2= OH
O CH3O
O OH OCH3 R3 R4 R2 R1
85. R1= R2= H, R3=OH, R4= OCH3
86. R1= R3= OCH3, R2= OH, R4= H
87. R1= OCH3, R2= R3= OH, R4= H
OH O O OH OAc 88 HO H O 89 O HO H O O HO OH 90 O O O O 91 O O O O 92 O OH CH3O
CH3O
OH O
93
O
OH CH3O
CH3O
OH O 94 O O OH R
95. R= H 96. R= OCHO
50 O O OH OH OH OH 99 O O OR2 OH OR1 H
100. R1= R2= Ac 101. R1= CHO, R2= Ac 102. R1= Ac, R2=H 103. R1= H, R2= Ac 104. R1= CHO, R2= H 105. R1= R2= H
O O R2 R1 OH H R3
106. R1= OCHO, R2= OAc, R3= OH
107. R1= H, R2= OH, R3= OCHO
108. R1= OCHO, R2= OH, R3= H
109. R1= H, R2= R3= OH 110. R1= R3= OCHO, R2= OH
O O OH AcO OH H OAc 111 O O R2 R1
R2 H
R3
112. R1= OCHO, R2= OAc, R3= OH
113. R1= R3= OCHO, R2= OH O O OH OAc H OH 114 O O HO OH OH H 115 O O HO
OHOR2
R1
116. R1= H, R2= Ac 117. R1= R2= H
51 OH HO R1 OH O OH R2
119. R1= OAc, R2= H 120. R1= OH, R2= H
OH HO R OH O O H
121. R= OAc 122. R=OH OH HO OH O O OH 123 OH HO OH O OH OH 124 O O O OH OH OH R H 125. R=OAc 126. R=OH O OH O R OH O O
127. R= CH3 128. R= OAc
O HO 129 OCH3 HO OH 130 O OH 131 O O 132 O O HO OH 133 OH HO OH O 134 O O OH OH HO R2 R1
135. R1= H, R2= OH 136. R1= OH, R2= H
O
O OH
OH R
137. R= OH 138. R=OAc
COOH
52 COOH
AcO
140 HO
141 AcO
HO 142 OAc HOOC R1 R2
143. R1= OH, R2= H 144. R1= H, R2= OH
R1
HOOC R3
R2
145. R1= H, R2= CH3, R3= OH
146.R1= OAc, R2= COH, R3= H
R3 R4 R1
R2
147. R1= OH, R2= R3= R4= H 148. R1= OAc, R2= R4= H, R3= OH
149. R1= R3= H, R2= OH, R4= OAc
R
O
150. R=COOH 151. R= CH2OH
O O OH OH 152 OH O OH HO OAc 153 R O O OH
154. R= OH 155. R= H
O
OH
OH
O OH
CH3OC
53 O O OH O O O OH O OH 7 12' 11'
158. β-C(7)-O-C(11‟) 166. β-C(7)-O-(12‟)
OH O O O O OH O O H H 159 O O O OH O O O OH 7 14
160. α-C(7)-O-C(14)
161. β-C(7)-O-C(14)
O
O OH OCH3
OH 162 O HO OH O 163 O OH O O O O OH O O 7 12' 11'
164. β-C(7)-O-C(11‟)
165. β-C(7)-O-C(12‟) OAc O O HO OAc OH 167 OH O O OH 168 OH O O OH OAc 169 OH O O OH OH AcO 170 CHO 171 OH O O OAc OH 172 O O O OH H AcO AcO 173 O O OH R
174. R= OH
O O OH R2 OH R1